Osteotomie versus unicompartimentele knieprothese bij geïsoleerde mediale en laterale artrose van de knie
Uitgangsvraag
Wanneer is een osteotomie versus een unicompartimentele knieprothese geïndiceerd bij knieartrose?
Aanbeveling
Verricht bij voorkeur een correctie osteotomie bij een jonge, actieve patiënt met:
- unicompartimentele knieartrose;
- een malalignment; en
- een operatie indicatie.
Plaats bij voorkeur een unicompartimentele knieprothese bij een oudere patiënt met eindstadium unicompartimentele knieartrose en een operatie indicatie.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Er is literatuuronderzoek verricht naar de verschillen in klinische uitkomsten tussen osteotomie en unicompartimentele knieprothese (UKP) in patiënten met unicompartimentele knieartrose, waarbij 2 gerandomiseerde studies zijn gevonden.
Postoperatieve pijn en kwaliteit van leven zijn gedefinieerd als cruciale uitkomstmaten. Door de zeer lage bewijskracht is het onduidelijk of er een verschil is in pijn tussen de 2 interventies. Kwaliteit van leven werd niet beschreven in de gevonden literatuur.
Om te kiezen tussen de ene en de andere interventie, is vervolgens gekeken naar de uitkomstmaten die als belangrijk gedefinieerd zijn. Voor de belangrijke uitkomstmaten functie, complicaties, revisies, en patiënttevredenheid is het op basis van de geïncludeerde literatuur door de zeer lage bewijskracht onduidelijk welke behandeling beter is. De uitkomstmaat “terugkeer naar werk of sport” werd niet beschreven in de gevonden literatuur.
De totale bewijskracht, de laagste gevonden bewijskracht voor één van de cruciale uitkomstmaten, is zeer laag. Hier ligt een kennislacune.
Op basis van de geïncludeerde literatuur lijkt er geen duidelijke voorkeur voor de ene of de andere interventie. Er zijn echter meerdere overwegingen die meegenomen moeten worden voordat de chirurg samen met de patiënt de keuze maakt voor een osteotomie dan wel unicompartimentele prothese.
Ten eerste moet men zich goed realiseren dat bij de meeste patiënten de indicatie voor een correctie osteotomie anders is dan die voor een prothese. Bij jonge patiënten (< 65 jaar) met milde tot matig ernstige unicompartimentele knieartrose (Kellgren&Lawrence graad 1 tot 3) en een malalignment is er eerder een correctie osteotomie geïndiceerd en bij oudere patiënten met eindstadium (Kellgren&Lawrence graad 4) unicompartimentele artrose eerder een UKP. Dit is ook wel een reden waarom er weinig geschikte literatuur is, want het vergelijken van twee behandelopties met eigenlijk een ander indicatie is natuurlijk tegenstrijdig. Echter er is een grijs gebied en dan moeten er een aantal andere factoren worden meegenomen om een beslissing te kunnen nemen. Het gaat hierbij zowel om patiëntkenmerken als operatiegebonden factoren. Daarbij moeten in overleg met de patiënt goed de voor- en nadelen van beide ingrepen besproken worden, en de wensen van de patiënt en operateur betrokken worden in de uiteindelijke beslissing voor het type operatie (samen beslissen).
Leeftijd en geslacht van de patiënt
Als voorspellende factoren voor een succesvolle osteotomie komen alleen leeftijd en geslacht naar voren, zij het met een beperkte bewijskracht (zie de module Patiëntkenmerken succesvolle osteotomie). De richtlijncommissie meent dat het waarschijnlijk is dat de tijdsperiode tussen een osteotomie en een revisie naar een TKP klinisch relevant korter is bij een oudere leeftijd in vergelijking met een jongere leeftijd, en bij vrouwen korter dan bij mannen. In veel literatuur wordt de jonge patiënt aangeduid als iemand onder de 65 jaar. Echter er is een verschil tussen biologische leeftijd en kalender leeftijd, en het is dan ook van belang om tevens naar comorbiditeiten en activiteitsniveau van de patiënt te kijken.
Functie en terugkeer naar sport
In westerse landen zien we een afname van het aantal osteotomieën en een forse stijging in prothesiologie. In Aziatische landen is er een omgekeerd beeld. Dit heeft er onder andere mee te maken dat knielen en hurken erg belangrijk zijn. Aangezien een osteotomie een gewrichtssparende behandeling is, blijft de natuurlijke functie van de knie over het algemeen intact en kunnen patiënten blijven knielen en hurken (Koh, 2015), in tegenstelling tot de functie na het plaatsen van een prothese (Cao, 2018). Verder is er een hoog percentage patiënten die na een osteotomie terugkeren op sportniveau (8 van de 10 patiënten (Hoorntje, 2017)). Na een UKP is het ook mogelijk om terug te keren naar sportniveau. Dit zijn echter wel vaak laag-impact sporten (Witjes, 2016).
Stabiliteit van de knie
Bij een UKP is een intacte voorste kruisband gewenst, wat niet het geval is bij een osteotomie. Een voorste kruisband ruptuur is een contra-indicatie voor een UKP met mobile bearing, echter dit is voor een osteotomie niet het geval. In tegenstelling, een correctie van de slope is een behandeloptie voor een voor-achterwaarts instabiele knie.
BMI
Patiënten met een hoog BMI hebben over het algemeen meer risico op complicaties na een operatie (Wagner, 2012). Obesitas is mogelijk een risicofactor voor non-union na een open wig osteotomie (Siboni, 2018). Over het algemeen zijn obese patiënten minder actief. De voorkeur kan dan eerder komen te liggen op het plaatsen van een UKP.
Survival van de interventie
Hoewel op basis van de geïncludeerde studies onduidelijk is of er een verschil in survival is tussen de twee interventies, is er uit literatuur wel wat bekend over de survival van osteotomieën en UKPs. De 10-jaars overlevingspercentages van tibiale osteotomiën liggen tussen de 75% en 98% (Song, 2016; Wulfften Palthe, 2018) en 15-jaars overleving 55% (Wulfften Palthe, 2018). De 10-jaars overleving is voor UKPs ongeveer 85% (Crawford, 2020) en 15-jaars overleving 76% (Evans, 2019). Een belangrijk verschil is dat een osteotomie een gewrichtssparende behandeling is en een UKP een gewrichtsvervangende behandeling. Als een osteotomie of UKP faalt dan is de volgende stap een revisie naar een TKP. Er zijn aanwijzingen in de literatuur dat de survival van een TKP lager is na een UKP dan na een osteotomie (El-Galaly, 2020). Een revisie knieprothese is geassocieerd met aanzienlijke kosten, morbiditeit en inferieure klinische uitkomsten in vergelijking met een primaire knieprothese en de belasting voor de patiënt en samenleving is dan ook enorm (Bhandari, 2012). Echter de survival van een UKP is hoger dan dat van een osteotomie. Bij een jonge patiënt kan men dus overwegen, afhankelijk van de mate van artrose en de mate van klachten, om een osteotomie te verrichten, danwel te wachten tot de patiënt wat ouder is en direct over te gaan op een UKP als primaire behandeling voor eindstadium artrose. Tot slot moet vermeld worden dan een tibiakoposteotomie in de voorgeschiedenis een relatieve contra-indicatie is voor een UKP.
Complicaties
Het aantal complicaties lijkt over het algemeen hoger na een osteotomie dan na een UKP (Stukenborg, 2001). Dit komt ook uit andere literatuur (Santoso, 2017). Echter de bewijskracht is laag. Ook de ernst van een complicatie is van belang, dit wordt niet altijd gespecificeerd in de literatuur. Van belang is om patiënten goed voor te lichten betreft de risico’s van een ingreep.
Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)
Er zijn meerdere factoren die van invloed kunnen zijn op de keuze voor een osteotomie of UKP in de behandeling van unicompartimentele knieartrose. De wens van een patiënt is een belangrijk onderdeel in de gedeelde besluitvorming. De behandelend orthopedisch chirurg zou hier dan ook actief naar moeten vragen. Meestal is pijnreductie de belangrijkste reden om een operatie te ondergaan, maar ook andere wensen kunnen van belang zijn om voor een bepaald type operatie te kiezen. Zo kan een jonge, actieve patiënt eerder een voorkeur voor een osteotomie hebben, gezien het behoud van het gewricht, betere functie en hogere kans op terugkeer naar sportniveau. Oudere, minder actieve patiënten met eindstadium artrose kunnen eerder besluiten tot een UKP, vanwege minder kans op complicaties en lagere revisie percentage.
Kosten (middelenbeslag)
Er is niet veel literatuur bekend over verschil in kosteneffectiviteit tussen een osteotomie en een UKP. Eén studie laat zien dat een osteotomie bij patiënten onder de 60 jaar meer kosteneffectief is dan een UKP, en boven de 60 jaar is dit andersom (Smith, 2017). Wat in de overweging ook meegenomen moet worden is het verhoogde risico op revisie van een TKP na een UKP in vergelijking met een osteotomie. Het is bekend dat revisie prothesiologie zeer veel kosten met zich meebrengt. De verwachting is dat de jaarlijkse economische last voor revisie prothesiologie in Amerika boven de 30 miljard dollar uit gaat komen in 2030 (Kurtz, 2007)
Aanvaardbaarheid, haalbaarheid en implementatie
Stepped care is van belang bij de behandeling van unicompartimentele knieartrose. De eerste stap in de behandeling is altijd conservatief. Pas als een conservatieve behandeling onvoldoende effect heeft en patiënt dusdanig klachten heeft, met daarbij voldoende radiologische afwijkingen, dan valt een operatieve behandeling te overwegen. Bij unicompartimentele knieartrose heeft indien mogelijk een gewrichtssparende behandeling de voorkeur boven een gewrichtsvervangende behandeling. De indicatie voor een osteotomie danwel UKP moet strikt blijven. Zo moet een UKP alleen geplaatst worden bij bot-op-bot op de röntgenfoto. Er worden wereldwijd steeds meer knieprotheses geplaatst en steeds minder osteotomieën verricht.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Uit de geanalyseerde literatuur komt er geen duidelijke voorkeur naar voren voor een correctie osteotomie danwel een UKP in de behandeling van unicompartimentele knieartrose. Stepped care is van belang bij de behandeling van unicompartimentele knieartrose, waarbij er altijd gestart wordt met een conservatieve behandeling. Daarna volgt indien nodig een operatieve ingreep. Dit kan gewrichtsparend (een correctie osteotomie) of gewrichtsvervangend (een UKP) zijn. De werkgroep is echter van mening dat de indicaties voor beide ingrepen grotendeels verschillen. Bij een jonge, actieve patiënt met milde tot matige unicompartimentele knieartrose en een malalignment heeft een correctie osteotomie de voorkeur boven een UKP. Dit om het gewricht zo lang mogelijk te behouden. De range of motion na een osteotomie lijkt ook beter dan na een prothese. Bij een oudere patiënt met eindstadium unicompartimentele knieartrose gaat de voorkeur uit naar een UKP. Verder dient er in de overwegingen meegenomen te worden dat er mogelijk een verhoogd risico is op een revisie van een totale knieprothese na een UKP in vergelijking met een correctie osteotomie. Dit brengt veel ziektelast en hoge kosten met zich mee.
Onderbouwing
Achtergrond
Wanneer conservatieve behandeling onvoldoende effectief is, zijn er voor unicompartimentele knieartrose verschillende chirurgische behandelopties, zoals een correctie osteotomie, een unicompartimentele knieprothese (UKP) en een totale knieprothese (TKP). Hoewel over het algemeen de indicatie voor een correctie osteotomie meer past bij de jonge actieve patiënt met matig ernstig unicompartimentele knieartrose en die voor UKP meer bij de oudere patiënt met eindstadium unicompartimentele knieartrose, is er een grijs gebied. Er bestaat nog steeds onduidelijkheid of een correctie osteotomie de voorkeur heeft boven een UKP bij unicompartimenle knieartrose, met name in het gebied waarin indicaties elkaar overlappen. Verschillende factoren spelen een rol bij de keuze voor een correctie osteotomie danwel een UKP, zoals patiëntgebonden factoren (onder andere leeftijd, mate van artrose, mate van malalignment, stabiliteit van de knie, leeftijd van de patiënt, BMI, comorbiditeiten, activiteitenniveau), chirurg gebonden factoren (onder andere voorkeur voor een procedure, kennis en ervaring van een procedure) en operatiegebonden factoren (onder andere complicaties, revalidatie, survivalrate).
Conclusies / Summary of Findings
|
Very low GRADE |
It is unclear whether high tibial osteotomy results in lower pain scores compared to unicompartmental knee arthroplasty in patients with medial knee osteoarthritis.
Sources: (Borjesson, 2005) |
|
- GRADE |
The outcome “quality of life” was not described in RCTs that directly compared high tibial osteotomy with unicompartmental knee arthroplasty in patients with medial knee osteoarthritis. |
|
Very low GRADE |
It is unclear whether high tibial osteotomy results in better knee scores (BOA and KSS scores) or range of motion compared to unicompartmental knee arthroplasty in patients with medial knee osteoarthritis.
Sources: (Borjesson, 2005; Stukenborg, 2001) |
|
Very low GRADE |
It is unclear whether high tibial osteotomy results in higher patient satisfaction compared to unicompartmental knee arthroplasty in patients with medial knee osteoarthritis.
Sources: (Borjesson, 2005) |
|
Very low GRADE |
It is unclear whether high tibial osteotomy results in lower complication rate compared to unicompartmental knee arthroplasty in patients with medial knee osteoarthritis.
Sources: (Stukenborg, 2001) |
|
Very low GRADE |
It is unclear whether high tibial osteotomy results in lower revision rate compared to unicompartmental knee arthroplasty in patients with medial knee osteoarthritis.
Sources: (Stukenborg, 2001) |
|
- GRADE |
The outcome return to work was not described in RCTs that directly compared high tibial osteotomy with unicompartmental knee arthroplasty in patients with medial knee osteoarthritis. |
|
- GRADE |
The outcome return to sport was not described in RCTs that directly compared high tibial osteotomy with unicompartmental knee arthroplasty in patients with medial knee osteoarthritis. |
Samenvatting literatuur
Description of studies
Borjesson (2005) is a RCT and the follow-up study of Weidenhielm (1993). The study describes the 5-year follow-up of 40 patients that received a closing-wedge (CW) HTO (n=18) or a UKA (Bragham, n=22). Patients in both groups were 63±4 years, with patients in the intervention (HTO) group being 56% male, and 50% male in the control (UKA) group.
Stukenborg (2001) describes the 7.5-year follow-up of 60 patients who received a CW-HTO (n=32) or a UKA (Tubingen pattern, n=28). Patients in the intervention (HTO) group were 67 years old (range 60 to 79), on average, and 59% male, whereas patients in the control (UKA) group were 67 years old (range 60 to 80), on average, and 21% male.
The overall risk of bias of the two RCTs was assessed as high, due to potential bias in patient selection, concealment of allocation, blinding of patients, caregivers and assessors, and the selection of reported results.
Results
Pain (critical)
One study reported pain after HTO and UKA (Borjesson, 2005). All patients (HTO, N=18; UKA, N=22) reported no to mild pain on the Borg CR10 scale, ranging from 0 ‘no pain’ to 10 ‘worst imaginable pain’), both at 1-year follow up (median 0, range 0-3) and at 5-year follow up (median 0, range 0-2). There was no difference between pain reported after HTO compared to UKA.
Level of evidence of the literature
The level of evidence for the outcome “pain” started at high, as it was based on a RCT, but was downgraded by 3 levels to very low, because of study limitations (risk of bias, -1), and the very small population size (imprecision, -2).
Quality of life (critical)
Quality of life was not described in the included studies.
Level of evidence of the literature
The level of evidence could not be assessed as no literature comparing quality of life after HTO and UKA was available.
Function (important)
Function was described as knee score including a function and pain component, as well as range of motion (ROM). Two studies described knee scores, but these scores could not be pooled, as the distribution of the data was not reported in the studies. Borjesson (2005) used the British Orthopaedic Association (BOA) score and reported median and range scores. There was no difference between function, as assessed with knee score, after HTO and UKA (HTO: N=18, median 37 [36-39]; UKA: N=22, median 37 [31-39]). Stukenborg (2001) used the Knee Society Score (KSS) and reported mean and range scores. This study found no clinically relevant difference in knee score after HTO compared to UKA (HTO: n=32, mean 76 [29-100]; UKA: n=28, mean 74 [31-94]).
Two studies reported the ROM after HTO and UKA (figure 1). Borjesson (2005) did not find differences in passive ROM between groups (HTO: 119°; UKA: 119°). Stukenborg (2001) did not specify type of ROM and reported ROM in favour of the HTO group (HTO: 117±12.5; UKA: 103±26.3). In order to pool these results, we have imputed the standard deviation of Stukenborg (2001) specific to treatment to the mean results of Borjesson (2005). As ROM measurement was not specified, we used the SMD to pool the results. The overall SMD is 0.36 [95% CI -0.31 to 1.04] in favour of HTO. This difference was not clinically relevant.
Figure 1 Range of motion (degrees) after HTO or UKA
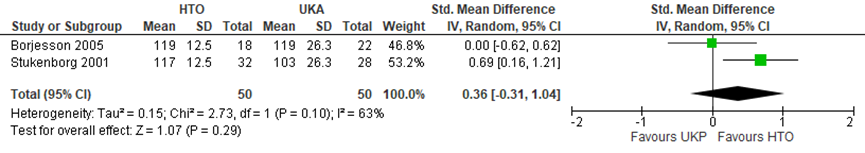
Random effects model; CI: confidence interval; df: degrees of freedom; HTO: high tibial osteotomy; I2: statistical heterogeneity; UKA: unicompartmental knee arthroplasty; Z: p-value van pooled effect
Level of evidence of the literature
The level of evidence for the outcome “function” started at high, as it was based on RCTs, but was downgraded by 3 levels to very low, because of study limitations (risk of bias, -1) the low number of included patients and the fact that the clinical decision threshold was crossed (both imprecision, -2).
Patient satisfaction
Patient-reported improvement at 5-year follow up was reported by 1 study (Borjesson, 2005), as assessed with a 3-grade scale indicating whether patients felt that their knee had improved, deteriorated or remained unchanged compared to before surgery. All patients of the HTO group (18/18, 100%) reported improvement, with all patients but one reporting improvement in the UKA group (21/22, 95%). When expressed as a dichotomous variable (improvement yes/no), patients reported improvement after 5 years more often after HTO compared to UKA (RR 1.04 (95% CI 0.91 to 1.19), but this difference was not clinically relevant.
Level of evidence of the literature
The level of evidence for the outcome “patient satisfaction” started at high, as it was based on an RCT, but was downgraded by 3 levels to very low, because of study limitations (risk of bias, -1) and a very limited number of included patients (imprecision, -2).
Complications (important)
One study reported the number of complications at 7.5-year follow up (Stukenborg, 2001). More complications were registered for participants in the HTO group (9/32, 28%) compared to the UKA group (2/28, 7%; RR 3.94 (95% CI 0.93 to 16.72)). This difference is clinically relevant.
Level of evidence of the literature
The level of evidence for the outcome “complications” started at high, as it was based on a RCT, but was downgraded by 3 levels to very low, because of study limitations (risk of bias, -1), the number of included patients and the fact that the clinical decision threshold was crossed (both imprecision, -2).
Implant survival (revision; important)
One study reported the number of revisions (Stukenborg, 2001). At 7.5-year follow up, the number of revisions in the HTO group (10/32, 31%) was higher compared to the UKA group (6/28, 21%; RR 1.46, 95% CI 0.61 to 3.50). This difference is clinically relevant.
Level of evidence of the literature
The level of evidence for the outcome “complications” started at high, as it was based on a RCT, but was downgraded by 3 levels to very low, because of study limitations (risk of bias, -1), the number of included patients and the fact that the clinical decision threshold was crossed (both imprecision, -2).
Return to work/sport (important)
Return to work or sport was not described in the included literature.
Level of evidence of the literature
The level of evidence could not be assessed as no literature comparing ‘return to work or sport’ after HTO and UKA was available.
Zoeken en selecteren
A systematic review of the literature was performed to answer the following question:
What is the efficacy of high tibial osteotomy compared to unicompartmental knee arthroplasty in patients with medial knee osteoarthritis?
P: patients with medial knee osteoarthritis;
I: high tibial osteotomy;
C: unicompartmental knee arthroplasty;
O: pain, quality of life, function, patient satisfaction, complications, survivorship (revision), return to work/sport.
Relevant outcomes
The guideline development group considered pain and quality of life to be critical outcomes for decision-making; and function, side effects, complications, patient satisfaction, return to work/sport and survivorship/revisions to be important outcomes for decision-making.
The working group did not define the outcomes listed above a priori but used the definitions used in the studies. The working group defined 25% as a minimal clinically (patient) important difference for dichotomous outcomes, 10% for VAS scales and PROM scores (Pijls, 2011), and 0.5 for standardized mean differences (SMD).
Search and select (Methods)
The databases [Medline (via OVID) and Embase (via Embase.com)] were searched with relevant search terms until October 2019. The detailed search strategy is outlined in the Methods section. The systematic literature search resulted in 124 hits. Studies were selected based on the following criteria: 1) directly comparing osteotomy and unicompartimental knee arthroplasty 2) patients with medial knee osteoarthritis and 3) one of the following outcomes: pain, quality of life, function, complications, survivorship (revision), patient satisfaction, return to work/sport. 11 studies were initially selected based on title and abstract screening. After reading the full texts, 1 additional study was identified. Next, 10 studies were excluded (see the table with reasons for exclusion in the Methods section), and 2 studies were included.
Results
Two randomized controlled trials (RCTs) that directly compared high tibial osteotomy (HTO) and UKA (unicompartmental knee arthroplasty) in an adult population with medial unicompartmental knee osteoarthritis were included in the literature analysis (Borjesson, 2005; Stukenborg, 2001). Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
Referenties
- Bhandari M, Smith J, Miller LE, Block JE. (2012) Clinical and economic burden of revision knee arthroplasty. Clin Med Insights Arthritis Musculoskelet Disord. 5:89-94.
- Börjesson, M & Weidenhielm, Lars & Mattsson, E & Olsson, E. (2005). Gait and clinical measurements in patients with knee osteoarthritis after surgery: A prospective 5-year follow-up study. The Knee. 12. 121-7. 10.1016/j.knee.2004.04.002.
- Cao Z, Mai X, Wang J, Feng E, Huang Y. (2018) Unicompartmental Knee Arthroplasty versus High Tibial Osteotomy for Knee Osteoarthritis: A Systematic Review and Meta-Analysis J Arthroplasty. Mar;33(3):952-959.
- Crawford DA, Berend KR, Thienpont E. (2020). Unicompartmental Knee Arthroplasty: US and Global Perspectives. Orthop Clin North Am. 2020 Apr;51(2):147-159.
- El-Galaly A, Nielsen PT, Kappel A, Jensen SL. (2020) Reduced survival of total knee arthroplasty after previous unicompartmental knee arthroplasty compared with previous high tibial osteotomy: a propensity-score weighted mid-term cohort study based on 2,133 observations from the Danish Knee Arthroplasty Registry. Acta Orthop. Apr;91(2):177-183.
- Evans JT, Walker RW, Evans JP, Blom AW, Sayers A, Whitehouse MR. How long does a knee replacement last? A systematic review and meta-analysis of case series and national registry reports with more than 15 years of follow-up (published correction appears in Lancet. 2019 Feb 20;:). Lancet. 2019;393(10172):655-663. doi:10.1016/S0140-6736(18)32531-5.
- Hoorntje A, Witjes S, Kuijer PPFM, Koenraadt KLM, van Geenen RCI, Daams JG, Getgood A, Kerkhoffs GMMJ (2017). High Rates of Return to Sports Activities and Work After Osteotomies Around the Knee: A Systematic Review and Meta-Analysis. Sports Med. Nov;47(11):2219-2244.
- Kleeblad LJ, Jelle P van der List, Hendrik A Zuiderbaa, Andrew D Pearle (2017) Larger Range of Motion and Increased Return to Activity, but Higher Revision Rates Following Unicompartmental Versus Total Knee Arthroplasty in Patients Under 65: A Systematic Review Knee Surg Sports Traumatol Arthrosc Jun;26(6):1811-1822.
- Koh IJ, Kim MW, Kim JH, Han SY, In Y (2015). Trends in High Tibial Osteotomy and Knee Arthroplasty Utilizations and Demographics in Korea From 2009 to 2013. J Arthroplasty. Jun;30(6):939-44.
- Steven Kurtz, Kevin Ong, Edmund Lau, Fionna Mowat, Michael Halpern. (2007). Projections of Primary and Revision Hip and Knee Arthroplasty in the United States From 2005 to 2030 J Bone Joint Surg Am. 2007 Apr;89(4):780-5.
- Liddle AD, Andrew Judge, Hemant Pandit, David W Murray (2014). Adverse Outcomes After Total and Unicompartmental Knee Replacement in 101,330 Matched Patients: A Study of Data From the National Joint Registry for England and Wales Lancet Oct 18;384(9952):1437-45.
- Liddle AD, Hemant Pandit, Andrew Judge, David W Murray (2016). Effect of Surgical Caseload on Revision Rate Following Total and Unicompartmental Knee Replacement J Bone Joint Surg Am Jan 6;98(1):1-8.
- Pijls, B. G., Dekkers, O. M., Middeldorp, S., Valstar, E. R., Van der Heide, H. J., Van der Linden-Van, H. M., & Nelissen, R. G. (2011). AQUILA: assessment of quality in lower limb arthroplasty. An expert Delphi consensus for total knee and total hip arthroplasty. BMC musculoskeletal disorders, 12(1), 173.
- Santoso MB, Wu L. (2017) Unicompartmental knee arthroplasty, is it superior to high tibial osteotomy in treating unicompartmental osteoarthritis? A meta-analysis and systemic review. J Orthop Surg Res Mar;28;12(1):50.
- Siboni R, P Beaufils, P Boisrenoult, C Steltzlen, N Pujol. (2018). Opening-wedge High Tibial Osteotomy Without Bone Grafting in Severe Varus Osteoarthritic Knee. Rate and Risk Factors of Non-Union in 41 Cases Orthop Traumatol Surg Res. 2018 Jun;104(4):473-476.
- Smith William B, Joni Steinberg, Stefan Scholtes, Iain R Mcnamara (2017) Medial Compartment Knee Osteoarthritis: Age-Stratified Cost-Effectiveness of Total Knee Arthroplasty, Unicompartmental Knee Arthroplasty, and High Tibial Osteotomy Knee Surg sports traumatol Arthroscopy Mar;25(3):924-933.
- Song SJ, Bae DK, Kim KI, Lee CH (2016) Conversion Total Knee Arthroplasty after Failed High Tibial Osteotomy. Knee Surg Relat Res. Jun;28(2):89-98.
- Stukenborg-Colsman, C., Wirth, C.J., Lazovic, D., & Weer, A (2001). High tibial osteotomy versus unicompartmental joint replacement in unicompartmental knee joint osteoarthritis: 7–10-year follow-up prospective randomised study. The Knee, Volume 8, Issue 3, 187 – 194.
- Wagner IJ, Szpalski C, Allen RJ Jr, Davidson EH, Canizares O, Saadeh PB, Warren SM (2012) Obesity impairs wound closure through a vasculogenic mechanism. Wound Repair Regen 20(4):512–522.
- Witjes S, Gouttebarge V, Kuijer PP, van Geenen RC, Poolman RW, Kerkhoffs GM. (2016) Return to Sports and Physical Activity After Total and Unicondylar Knee Arthroplasty: A Systematic Review and Meta-Analysis Sports Med. Feb;46(2):269-92.
- van Wulfften Palthe AFY, Clement ND, Temmerman OPP, Burger BJ (2018). Survival and functional outcome of high tibial osteotomy for medial knee osteoarthritis: a 10-20-year cohort study. Eur J Orthop Surg Traumatol. Oct;28(7):1381-1389.
Evidence tabellen
Evidence table for intervention studies (randomized controlled trials and non-randomized observational studies (cohort studies, case-control studies, case series))1
This table is also suitable for diagnostic studies (screening studies) that compare the effectiveness of two or more tests. This only applies if the test is included as part of a test-and-treat strategy - otherwise the evidence table for studies of diagnostic test accuracy should be used
*BOA: includes pain/function/deformity; scale 0-39, worst to best
**KSS: comprises knee score (pain/ROM/deformities etc) + funct. Score (mobility, walking aids); scale 0-100, worst to best, of which 85-100: excellent, 70-84 good, 60-69 fair, <60 poor.
Therefore, total BOA best comparable to KSS total score.
Notes:
- Prognostic balance between treatment groups is usually guaranteed in randomized studies, but non-randomized (observational) studies require matching of patients between treatment groups (case-control studies) or multivariate adjustment for prognostic factors (confounders) (cohort studies); the evidence table should contain sufficient details on these procedures.
- Provide data per treatment group on the most important prognostic factors ((potential) confounders).
- For case-control studies, provide sufficient detail on the procedure used to match cases and controls.
- For cohort studies, provide sufficient detail on the (multivariate) analyses used to adjust for (potential) confounders.
Risk of bias table for intervention studies (randomized controlled trials)
|
Study reference
(first author, publication year) |
Describe method of randomisation1 |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Borjesson, 2001 |
Unclear, Randomly selected by drawing lots |
unclear |
Likely; not possible |
Likely; not possible |
Unclear |
Unclear |
Unclear |
Likely (no intention-to-treat analysis Weidenhielm 1993) |
|
Stukenborg, 2005 |
Unclear, computer-randomized |
unclear |
Likely; not possible |
Likely; not possible |
Unclear |
Unclear |
Unlikely;
“For the 7.5-year follow-up, all patients could be assessed.” |
Unlikely
“For the 7.5-year follow-up, all patients could be assessed.” |
- Randomisation: generation of allocation sequences have to be unpredictable, for example computer generated random-numbers or drawing lots or envelopes. Examples of inadequate procedures are generation of allocation sequences by alternation, according to case record number, date of birth or date of admission.
- Allocation concealment: refers to the protection (blinding) of the randomisation process. Concealment of allocation sequences is adequate if patients and enrolling investigators cannot foresee assignment, for example central randomisation (performed at a site remote from trial location) or sequentially numbered, sealed, opaque envelopes. Inadequate procedures are all procedures based on inadequate randomisation procedures or open allocation schedules.
- Blinding: neither the patient nor the care provider (attending physician) knows which patient is getting the special treatment. Blinding is sometimes impossible, for example when comparing surgical with non-surgical treatments. The outcome assessor records the study results. Blinding of those assessing outcomes prevents that the knowledge of patient assignement influences the proces of outcome assessment (detection or information bias). If a study has hard (objective) outcome measures, like death, blinding of outcome assessment is not necessary. If a study has “soft” (subjective) outcome measures, like the assessment of an X-ray, blinding of outcome assessment is necessary.
- Results of all predefined outcome measures should be reported; if the protocol is available, then outcomes in the protocol and published report can be compared; if not, then outcomes listed in the methods section of an article can be compared with those whose results are reported.
- If the percentage of patients lost to follow-up is large, or differs between treatment groups, or the reasons for loss to follow-up differ between treatment groups, bias is likely. If the number of patients lost to follow-up, or the reasons why, are not reported, the risk of bias is unclear.
- Participants included in the analysis are exactly those who were randomized into the trial. If the numbers randomized into each intervention group are not clearly reported, the risk of bias is unclear; an ITT analysis implies that (a) participants are kept in the intervention groups to which they were randomized, regardless of the intervention they actually received, (b) outcome data are measured on all participants, and (c) all randomized participants are included in the analysis.
Table of excluded studies
|
Author and year |
Reason for exclusion |
|
Brouwer et al. 2014 |
SR, original RCTs included in this analysis |
|
Cao et al. 2018 |
SR, original RCTs included in this analysis |
|
Cho et al. 2018 |
Retrospective trial |
|
Fu et al. 2013 |
SR, original RCTs included in this analysis |
|
Gandhi et al. 2009 |
SR, original RCTs included in this analysis |
|
Griffin et al. 2007 |
SR, original RCTs included in this analysis |
|
Han et al. 2017 |
SR, original RCTs included in this analysis |
|
Kim et al. 2018 |
Prospective, not randomized |
|
Liu et al. 2018 |
Network meta-analysis of non-randomized trials |
|
Song et al 2019 |
Retrospective trial |
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 17-11-2021
Beoordeeld op geldigheid : 30-09-2021
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
De richtlijn is ontwikkeld in samenwerking met:
- Koninklijk Nederlands Genootschap voor Fysiotherapie
- Patiëntenfederatie Nederland
- ReumaNederland
- Nationale Vereniging ReumaZorg Nederland
Doel en doelgroep
Doel
Het doel van de richtlijn is het beschrijven de gewenste diagnostiek en behandeling voor patiënten die lijden aan unicompartimentele artrose van de knie, gebaseerd op de meest actuele literatuur, ervaringen van patiënten en experts uit het veld.
Doelgroep
Deze richtlijn is bestemd voor alle zorgverleners die betrokken zijn bij de behandeling van patiënten met geïsoleerde mediale of laterale knieartrose. De richtlijn informeert ook de patiënt zodat deze samen met de arts een besluit kan nemen over de behandeling.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2019 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met geïsoleerde mediale of laterale artrose van de knie.
Werkgroep
- Dr. R.W. Brouwer, orthopedisch chirurg in Martini ziekenhuis Groningen, NOV (voorzitter)
- Dr. R.C.I. van Geenen, orthopedisch chirurg in Amphia Ziekenhuis, NOV
- Drs. A. Goud, orthopedisch chirurg in Diakonessenhuis, NOV
- Dr. N. van Egmond, orthopedisch chirurg in UMC Utrecht, NOV
- Prof. dr. S.M.A. Bierma-Zeinstra, hoogleraar artrose en gerelateerde aandoeningen in Erasmus MC, NOV
- Drs. T.W.G.M. Meys, radioloog in Martiniziekenhuis, NVvR
- Dr. J.T. Wegener, anesthesioloog-pijnspecialist in Sint Maartenskliniek, NVA
- Dr. M. van der Esch, senior onderzoeker/fysiotherapeut/epidemioloog in Reade en hoofddocent/lector Hogeschool van Amsterdam, KNGF
- N. Lopuhaä, beleidsmedewerker Patiëntbelangen, ReumaNederland
- M. Frediani-Bolwerk, patiëntpartner Nationale Vereniging ReumaZorg Nederland
- Drs. P. Pennings, beleidsmedewerker Communicatie & Participatie, Nationale Vereniging ReumaZorg Nederland
Met ondersteuning van
- Dr. M.S. (Matthijs) Ruiter, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. S.N. (Stefanie) Hofstede, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten.
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Brouwer (voorzitter) |
Orthopedisch chirurg Martiniziekenhuis
|
Medische staf FC Groningen (betaald), ODEP member (onbetaald), bestuurslid DKS (onbetaald) COIC (onbetaald) Bestuurslid WAR (betaald). |
Geen |
Geen actie |
|
Van Geenen |
Orthopedisch chirurg Amphia Ziekenhuis |
Consultant Zimmer Biomet (betaald), Secretaris werkgroep knie/Dutch Knee Society (onbetaald) |
De orthopedische onderzoekstichting FORCE ontvangt gelden van verschillende industriële partners (Mathys, Stryker, Zimmer Biomet) |
Geen auteur van uitgangsvragen met betrekking tot keuze van prothese |
|
Frediani-Bolwerk |
Patiëntvertegenwoordiger |
Geen |
Geen |
Geen actie |
|
Patricia Pennings |
Beleidsmedewerker Communicatie & Participatie bij Nationale Vereniging ReumaZorg Nederland. |
Geen |
Geen |
Geen actie |
|
Van der Esch |
Senior onderzoeker/fysiotherapeut/epidemioloog in Reade, centrum voor revalidatie en reumatologie te Amsterdam; Hoofddocent/lector Hogeschool van Amsterdam, faculteit gezondheid. |
Geen |
Geen |
Geen actie |
|
Meys |
Radioloog Martini Ziekenhuis Groningen met aandachtsgebied musculoskeletaal |
Geen |
Geen |
Geen actie |
|
Lopuhaä |
Beleidsmedewerker Patiëntenbelangen ReumaNederland |
Geen |
Geen |
Geen actie |
|
Van Egmond |
Orthopedisch chirurg, UMC Utrecht |
Geen |
In het UMC Utrecht is kniedistractie ontwikkeld, daar is een spin-off bedrijf uit voortgekomen (arthrosave), welke nu zelfstandig is en geen relatie meer heeft met UMC Utrecht. Persoonlijk ben ik niet betrokken bij de ontwikkeling hiervan, maar UMC Utrecht is wel expertise centrum. |
Geen actie |
|
Bierma-Zeinstra |
Hoogleraar artrose en gerelateerde aandoeningen, Erasmus MC |
Associate editor Osteoarthritis & Cartilage (betaald), Commisielid Swedisch Research Council - clinical studies (onbetaald), Ethical board OARSI (onbetaald), Scientific advisory board Arthritis UK Pain Centre Nottingham University (onbetaald), Commissielid Annafonds (onbetaald), Editorial board member Maturitas (onbetaald), |
Ik heb meerdere subsidies voor epidemiologisch en klinisch artrose onderzoek van ZonMW, CZ, Europesche Unie, Foreum, en ReumaNederland. |
Geen actie |
|
Goud |
Orthopedisch chirurg Diakonessenhuis |
Bestuurslid Dutch knee society, (onbetaald), Bestuurslid Nederlandse vereniging voor Arthroscopy, (onbetaald). |
Geen |
Geen actie |
|
Wegener |
Anesthesioloog-Pijnspecialist |
Instructuur DARA (betaald), Examinator EDRA (onkostenvergoeding), Course Director ESRA Instructor Course (onkostenvergoeding), Lid ledenraad NVA sectie Pijn (geen onkostenvergoeding). |
Geen |
Geen actie |
|
Hofstede |
Senior adviseur Kennisinstituut van de Federatie Medisch Specialisten |
Geen |
Geen |
Geen actie |
|
Ruiter |
Adviseur Kennisinstituut van de Federatie Medisch Specialisten |
Geen |
Geen |
Geen actie |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door het uitnodigen van diverse patiëntorganisaties voor de Invitational conference. Het verslag hiervan (zie bijlagen) is besproken in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. Gedurende de richtlijnontwikkeling zaten vertegenwoordigers van ReumaNederland en Nationale Vereniging ReumaZorg Nederland in de werkgroep. Er is verder specifiek een module gewijd aan patiëntvoorlichting en communicatie. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de patiëntorganisaties die ook waren uitgenodigd voor de Invitational conference en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Methode ontwikkeling
Evidence based
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten met geïsoleerde mediale of laterale artrose van de knie. Tevens zijn er knelpunten aangedragen door ReumaNederland en Nationale Vereniging ReumaZorg Nederland via de Invitational conference. Een verslag hiervan is opgenomen in de bijlagen.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur en de beoordeling van de risk-of-bias van de individuele studies is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello, 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE-methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE-gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende wetenschappelijke verenigingen en patiëntorganisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
October 30, 2019
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID) 1997 – okt 2019
|
1 exp Osteotomy/ or ((tibia* or fem?r* or correction or valgus or varus or knee or proximal) adj4 (osteotomy or osteotomi*)).ti,ab,kw. (37071) 2 ((exp Arthroplasty, Replacement, Knee/ or exp Knee Prosthesis/) and (partial or unicompartmental or unicondylar).ti,ab,kw.) or ((partial or unicompartmental or unicondylar) adj2 knee adj2 (arthroplasty or replacement or prosthes*)).ti,ab,kw. or (uka or pka or pkr).ti,ab,kw. (31548) 3 1 and 2 (274) 4 limit 3 to (english language and yr="1997 -Current") (182) 5 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (417625) 6 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1911949) 7 Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or (cohort adj (study or studies)).tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ (Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies) (3290880) 8 4 and 5 (19) 9 (4 and 6) not 8 (13) 10 (4 and 7) not (8 or 9) (64) 11 8 or 9 or 10 (96)
= 96 (49 unique) |
124 |
|
Embase 1997 – okt 2019 |
'osteotomy'/exp OR 'knee osteotomy'/exp OR 'valgus osteotomy'/exp OR (((tibia* OR fem?r* OR correction OR valgus OR varus OR knee OR proximal) NEAR/4 (osteotomy OR osteotomi*)):ti,ab) AND 'unicompartmental knee prosthesis'/exp OR 'unicompartmental knee replacement'/exp OR 'unicompartmental knee arthroplasty'/exp OR 'unicondylar knee arthroplasty'/exp OR (((partial OR unicompartmental OR unicondylar) NEAR/2 knee NEAR/2 (arthroplast* OR replacement* OR prosthes*)):ti,ab) OR uka:ti,ab OR pka:ti,ab OR pkr:ti,ab AND (english)/lim AND (1997-2019)/py NOT 'conference abstract':it
Gebruikte filters: Sytematische reviews ('meta analysis'/de OR cochrane:ab OR embase:ab OR psycinfo:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp)
RCT’s ('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it
Observationeel onderzoek 'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti)
= 75 (75 unique) |
