Dynamische stabilisatie bij spinaalchirurgie
Uitgangsvraag
Wat is de effectiviteit van dynamische stabilisatie ten opzichte van spondylodese, decompressie of non operatieve interventie bij degeneratieve aandoeningen van de thoracolumbosacrale wervelkolom?
Aanbeveling
Een discusprothese biedt geen duidelijke voordelen boven spondylodese bij chronische lage rugpijn. Gezien het beperktere indicatiegebied en het hogere revisie-percentage wordt het gebruik van discusprotheses voor deze indicatie daarom niet aanbevolen, tenzij in studieverband met informed consent van de patiënt.
Indien chirurgische behandeling van symptomatische lumbale kanaalstenose zonder spondylolisthesis wordt overwogen, heeft decompressie alleen de voorkeur boven een IPD.
Bij symptomatische lumbale kanaalstenose met graad 1 spondylolisthesis kan in plaats van geïnstrumenteerde spondylodese met decompressie, een decompressie met plaatsing van een interspinale implantaat worden overwogen hoewel dit niet de voorkeur heeft gezien het hoge revisie-percentage op korte termijn.
Overwegingen
Discusprothese versus spondylodese bij chronische lage rugpijn
De verschillen tussen beide methodes waren niet klinisch relevant, de resultaten op langere termijn zijn niet bekend en een deel van de studies werd gesponsord door de industrie wat mogelijk tot bias zou kunnen hebben geleid.
Discusprothese versus niet-operatief bij lage rugpijn met aspecifieke degeneratieve kenmerken
De verschillen tussen beide methodes waren statistisch significant doch niet klinisch relevant. Er werd slechts een studie uitgevoerd die vergeleek met niet-operatief. Zowel operatieve als niet-operatieve behandeling leidden tot substantiële klinisch relevante vermindering van klachten. Een niet-operatieve aanpak gaat gepaard met minder complicaties en lagere kosten en daarom zou operatief beleid pas ingezet moeten worden als conservatief beleid gefaald heeft.
Interspinosale implantaten (IPD) versus spondylodese bij lumbale kanaalstenose en spondylolisthesis
De verschillen tussen beide methodes waren niet klinisch relevant. Het is niet zeker of fusie altijd nodig is, er zijn slechts weinig lange termijn resultaten bekend en er worden hoge percentages revisieoperaties gezien. Het is dus belangrijk de patiënt voor te lichten dat een IPD-operatie vaak een tijdelijke stabilisatie en/of decompressie betreft met een hoog risico op revisieoperatie.
Interspinosale implantaten (IPD) versus benige decompressie bij lumbale kanaalstenose
De verschillen tussen beide methodes waren niet klinisch relevant. Het is wel zo dat operaties voor interspinale implantaten minder langdurig zijn en daardoor gepaard gaan met minder bloedverlies. Bij een eventuele reoperatie is decompressie een mogelijkheid. Wel is het zo dat er vaak een heroperatie nodig is na een interspinosaal implantaat: 33% na IPD versus 8% na benige decompressie (Mooijen, 2015).
Interspinosale implantaten (IPD) versus niet-operatieve interventie bij lumbale kanaalstenose
Een interspinosaal implantaat laat een klinisch relevant beter functioneren zien dan een niet-operatief beleid. Een nadeel is wel dat een interspinosaal implantaat vaak duurder is en vaker complicaties laat zien dan niet-operatief beleid.
Dynamische posterieure pedikelschroeffixaties versus rigide pedikelschroeffixaties bij degeneratieve lumbale spondylolisthesis
De verschillen tussen beide methodes waren niet klinisch relevant. Dynamische pedikelschroefficaties zijn mogelijk iets mobieler dan rigide, waarbij mogelijk ook minder adjacent segment disease zou optreden, hoewel dat nooit bewezen is. Een nadeel is dat dynamische pedikelschroeffixaties vaak falen, zeker op de iets langere termijn. Dat maakt ze niet goedkoper.
Kennishiaat
PROMs worden nog onvoldoende onderzocht in de gepubliceerde studies.
Er zijn onvoldoende studies naar minimaal invasieve operatietechnieken.
Onderbouwing
Het doel van dynamische instrumentatie van de lage rug is stabilisatie van wervelsegmenten met behoud van (enige) beweging. De vraag rijst of deze technieken gebaseerd zijn op voldoende bewijs. In deze module wordt de effectiviteit van interventies voor dynamische stabilisatie uitgezocht bij de indicaties chronische lage rugpijn, lumbale kanaalstenose, spondylolisthesis, en degeneratieve deformiteiten.
Voor de definitie van chronische lage rugpijn, zie algemene inleiding.
Discusprothese versus spondylodese bij chronische lage rugpijn
|
Laag |
Discusprothese leidt niet tot klinisch relevante pijnvermindering ten opzichte van spondylodese.
Bronnen (Berg, 2009; Blumenthal, 2005; Gornet, 2011; Moreno, 2008; Zigler, 2007, Jacobs, 2011) |
|
Gemiddeld |
Discusprothese leidt niet tot klinisch relevante functieverbetering ten opzichte van spondylodese.
Bronnen (Berg, 2009; Blumenthal, 2005; Gornet, 2011; Moreno, 2008; Zigler, 2007, Jacobs, 2011) |
|
Zeer Laag |
Discusprothese leidt niet tot klinisch relevante verbetering van kwaliteit van leven ten opzichte van spondylodese.
Bronnen (Berg, 2009; Blumenthal, 2005; Gornet, 2011; Moreno, 2008; Zigler, 2007, Jacobs, 2011) |
Discusprothese versus niet-operatieve behandeling bij lage rugpijn met aspecifieke degeneratieve kenmerken
|
Zeeg Laag |
Discusprothese leidt niet tot klinisch relevante pijnvermindering ten opzichte van een gestructureerd multidisciplinair revalidatieprogramma.
Bronnen (Hellum, 2011) |
|
Zeer Laag |
Discusprothese leidt niet tot klinisch relevante functieverbetering ten opzichte van een gestructureerd multidisciplinair revalidatieprogramma.
Bronnen (Hellum, 2011) |
|
Zeer Laag |
Discusprothese leidt niet tot klinisch relevante verbetering van kwaliteit van leven ten opzichte van een gestructureerd multidisciplinair revalidatieprogramma.
Bronnen (Hellum, 2011) |
Interspinosale implantaten (IPD) versus spondylodese bij lumbale kanaalstenose en graad 1 spondylolisthesis
|
Laag |
IPD (al dan niet met decompressie) leidt niet tot klinisch relevante pijnvermindering ten opzichte van spondylodese.
Bronnen (Azzazi, 2010 (zonder decompr); Davis, 2013 (met decompr.); Yu, 2012) |
|
Laag |
IPD (al dan niet met decompressie) leidt niet tot klinisch relevante functieverbetering ten opzichte van spondylodese.
Bronnen (Azzazi, 2010 (zonder decompr); Davis, 2013 (met decompr.); Yu, 2012) |
|
Zeer Laag |
IPD (al dan niet met decompressie) leidt niet tot klinisch relevante verbetering van kwaliteit van leven ten opzichte van spondylodese.
Bronnen (Azzazi, 2010 (zonder decompr); Davis, 2013 (met decompr.); Yu, 2012) |
Interspinosale implantaten (IPD) versus decompressie bij lumbale kanaalstenose
|
Gemiddeld |
IPD (zonder decompressie) leidt niet tot klinisch relevante pijnvermindering ten opzichte van decompressie alleen.
Bronnen (Stromqvist, 2013; Moojen, 2013) |
|
Gemiddeld |
IPD (zonder decompressie) leidt niet tot klinisch relevante functieverbetering ten opzichte van decompressie alleen.
Bronnen (Stromqvist, 2013; Moojen, 2013) |
|
Gemiddeld |
IPD (zonder decompressie) leidt niet tot klinisch relevante verbetering van kwaliteit van leven ten opzichte van decompressie alleen.
Bronnen (Stromqvist, 2013; Moojen, 2013) |
Interspinosale implantaten (IPD) versus niet-operatieve interventie bij lumbale kanaalstenose
|
Geen |
IPD leidt niet tot klinisch relevante pijnvermindering ten opzichte van niet-operatieve interventies.
Bronnen (Moojen, 2011; Anderson, 2004; Zucherman, 2004) |
|
Laag |
IPD laat een klinisch relevante functieverbetering zien ten opzichte van niet operatieve interventies.
Bronnen (Moojen, 2011; Anderson, 2004; Zucherman, 2004) |
|
Zeer Laag |
IPD laat een verbetering zien in kwaliteit van leven ten opzichte van niet-operatieve interventies.
Bronnen (Moojen, 2011; Anderson, 2004; Zucherman, 2004) |
Dynamische posterieure pedikelschroeffixaties versus rigide pedikelschroeffixaties bij degeneratieve lumbale spondylolisthesis
|
Laag |
Dynamische posterieure pedikelschroeffixaties leiden niet tot klinisch relevante pijnvermindering ten opzichte van rigide pedikelschroeffixaties.
Bronnen (Kaner, 2002; Korovessis, 2004; Yu, 2012) |
|
Zeer Laag |
Dynamische posterieure pedikelschroeffixaties leiden niet tot meer klinisch relevante functieverbetering leidt ten opzichte van rigide pedikelschroeffixaties
Bronnen (Kaner, 2002; Korovessis, 2004; Yu, 2012) |
|
Zeer Laag |
Dynamische posterieure pedikelschroeffixaties leiden niet tot een klinisch relevante verbetering van kwaliteit van leven dan rigide pedikelschroeffixaties.
Bronnen (Kaner, 2002; Korovessis, 2004; Yu, 2012) |
Discusprothese versus spondylodese bij chronische lage rugpijn
Voor de vergelijking van discusprotheses en fusie werden vier systematische reviews gevonden (Van den Eerenbeemt, 2010; Yajun, 2010; Jacobs, 2012; Wang, 2012). De review van Jacobs is de meest recente en tevens een Cochrane review en werd daarom als uitgangspunt genomen. Vijf studies in deze review vergelijken een discusprothese met spondylodese (Berg, 2009; Blumenthal, 2005; Gornet, 2011; Moreno, 2008; Zigler, 2007).
Pijn (VAS-schaal)
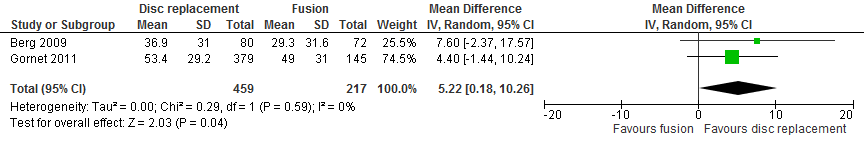
De review van Jacobs liet zien dat rugpijn op verbeterde op basis van twee studies (Berg, 2009; Gornet, 2011). De gepoolde verbetering in de VAS-rugpijn-score na twee jaar bedroeg 5,22 in de discusprothesegroep ten opzichte van de spondylodese-groep (95% BI 0,18 tot 10,26, zie figuur 1). Dit effect wordt niet gezien als klinisch relevant.
Figuur 1 Pijn gemeten met de VAS schaal, forest plot voor de vergelijking discusprothese versus spondylodese na twee jaar follow-up
Functioneren (Disability)
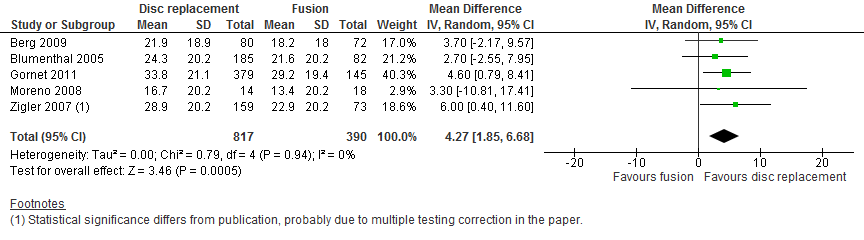
Vijf studies keken naar functioneren middels de ODI (Berg, 2009; Blumenthal, 2005; Gornet, 2011; Moreno, 2008; Zigler, 2007). Na twee jaar werd in de discusprothesegroep 4,27 punten op de ODI (95%BI 1,85 tot 6,68, zie figuur 2) meer verbetering gezien dan in de fusiegroep. Dit wordt niet gezien als een klinisch relevant verschil.
Figuur 2 Functionaliteit gemeten met de ODI, forest plot voor de vergelijking disc replacement versus fusie na twee jaar follow-up
Kwaliteit van leven
Slechts één studie rapporteerde over kwaliteit van leven. De review van Jacobs et al beoordeelde het niveau van bewijs zeer laag.
Discusprothese versus niet-operatieve behandeling bij chronische lage rugpijn
De review van Jacobs (2012) includeerde één RCT (Hellum, 2011) die discusprothese met niet-operatieve behandeling vergeleek.
Pijn (VAS-schaal)
De review van Jacobs vond bewijs gebaseerd op één studie (Hellum, 2011) dat een discus prothese tot meer verbetering van rugpijn leidt na 24 maanden dan revalidatie bestaande uit cognitieve therapie onder begeleiding van een multidisciplinair team en fysiotherapie onder begeleiding. Preoperatief VAS-rugpijn in de discusprothesegroep bedraagt 64,9 (sd 15,3) versus in de revalidatiegroep 73,6 (sd 13,9), en postoperatief discusprothese VAS 35,4 (sd 29,1) versus revalidatie 49,7 (sd 28,4); het gepoolde behandeleffect bedraagt -12,2 (95% BI -21,3; -3.1). Dit effect is weliswaar significant doch overschrijdt niet consistent het minimaal klinisch relevante verschil tussen de 2 behandelingen en gezien de potentiële complicatierisico’s werd dit verschil door de auteurs dan ook als niet klinisch relevant beschouwd.
Functioneren (Oswestry Disability Index ODI)
De review vond bewijs van laag niveau gebaseerd op één studie met laag risico op bias (Hellum, 2011) dat discus prothese tot meer verbetering van functioneren (ODI) leidt dan revalidatie na 24 maanden. Preoperatief discusprothese 41,8 (sd 9,1) en revalidatie 42,8 (sd 9,3), postoperatief discusprothese 19,8 (sd 16,7) revalidatie 26,7 (sd 14,5); verschil discusprothese: 41,8-19,8=22 punten en revalidatie: 42,8-26,7=16,1, het gepoolde verschil bedroeg -6,7 (95% BI -11,7; -2,1). Dit verschil is niet klinisch relevant aangezien het niet het minimaal klinisch relevant verschil overschrijdt waar de auteurs van uitgegaan waren.
Kwaliteit van leven
De studie van Hellum (Hellum, 2011) liet zien dat de discusprothese tot meer verbetering van fysiek functioneren (SF-36 subschaal) leidt dan revalidatie (5,8 punten, 172 patiënten; (95% BI 2,5 tot 9,1).
Interspinosale implantaten (IPD) versus spondylodese bij lumbale kanaalstenose en spondylolisthesis
Bij deze vergelijking moet onderscheid worden gemaakt tussen het gebruik van de IPD-implantaat als stand alone of als toevoeging aan een decompressie. Voor de vergelijking van IPD zonder decompressie ten opzichte van spondylodese werd één gerandomiseerde studie geïncludeerd (Azzazi, 2010). Voor de vergelijking van IPD als toevoeging aan decompressie ten opzichte van spondylodese werd één studie gevonden (Davis, 2013). Davis heeft een laag risico op bias en gebruikte de Coflex als implantaat.
Pijn (VAS-schaal)
Azazi liet een gemiddelde VAS-rugpijn verbeteren van 80,5 preoperatief naar 35,5 voor de transpediculaire schroef fixatie en van 52 naar 29,5 voor dynamische stabilisatie. Preoperatieve beenpijn verbeterde van 80,5 naar 35,5 voor de transpediculaire schroef fixatie en van 82,5 naar 25,5 voor dynamische stabilisatie (Azzazi, 2010).
Davis liet een VAS preoperatief voor rugpijn zien van 79,5 (sd 15) in de Coflexgroep en 79,2 (sd 13,5) in de controlegroep, na twee jaar was deze 23,6 (sd 26,2) in de Coflexgroep en 27,0 (sd 29,3) in de controlegroep. Deze verschillen waren niet klinisch relevant. VAS preoperatief voor beenpijn zien van 76,0 (sd 20,4) in de Coflexgroep en 78,3 (sd 18,4) in de controlegroep, na twee jaar was deze 20,6 (sd 27,4) in de Coflexgroep en 24,1 (sd 30,6) in de controlegroep. Deze verschillen waren niet klinisch relevant (Davis, 2013).
Functioneren (Disability)
Azzazi liet een ODI zien die verbeterde van 55 preoperatief naar 34,5% voor de transpediculaire schroef fixatie en van 53 naar 26,5 voor dynamische stabilisatie (Azzazi, 2010).
Davis liet een ODI preoperatief zien van 60,8 (sd 11,8) in de Coflexgroep en 60,7 (sd 11,5) in de controlegroep, na twee jaar was deze 22,0 (sd 18,6) in de Coflexgroep en 26,7 (sd 21,3) in de controlegroep. Deze verschillen waren niet klinisch relevant (Davis, 2013).
Kwaliteit van leven
De studie van Davis laat een grotere verbetering van kwaliteit van leven (SF-12) zien voor de coflexgroep na 24 maanden (15,5 vs 12,6; P = 0,050) (Davis, 2013).
Interspinale implantaten (IPD) versus decompressie bij lumbale spinale stenose
Bij deze vergelijking moet onderscheid worden gemaakt tussen het gebruik van de IPD-device als stand alone of als toevoeging aan een decompressie. Voor de vergelijking van IPD zonder decompressie ten opzichte van decompressie alleen werden twee gerandomiseerde studies geïncludeerd (Stromqvist, 2013; Moojen, 2013). Stromqvist gebruikte de X-stop en Moojen gebruikte het Coflex IPD-implantaat. Voor de vergelijking van IPD als toevoeging aan decompressie met decompressie alleen werd één observationele studie gevonden (Richter, 2010).
Pijn (VAS-schaal)
Alle drie de studies rapporteerden pijn.
Stromqvist liet een VAS preoperatief voor rugpijn zien van 59 (sd 28) in de X-Stopgroep en 60 (sd 26) in de decompressiegroep, na twee jaar was deze 34 (sd 25) in de Coflexgroep en 23 (sd 27) in de controlegroep.
Mooijen liet een VAS preoperatief voor rugpijn zien van 60 [37 tot 83] in de interspinous process device (IPD) -groep en 49 [44 tot 56] in de decompressiegroep, na één jaar was deze 23 [17 tot 29] in de IP-groep en 31 [24 tot 37] in de decompressiegroep.
Richter liet met een ANOVA zien dat er geen verschil in VAS-pijnscores was tussen de groepen (p=0,66) bij een follow-up duur van 12 maanden.
Geen van de bovengenoemde studies liet gedurende de follow-up een klinisch relevant verschil zien tussen de behandelingen voor pijn.
Functioneren (Disability)
Alle drie de studies rapporteerden minimaal één score met betrekking tot functioneren. Twee studies rapporteerden de Zurich Claudication Questionnaire (Moojen, 2013; Stromqvist, 2013) en beide studies lieten gedurende de follow-up geen verschil zien tussen interspinale implantaten en decompressie. Twee studies rapporteerden de gemodificeerde Roland Disability Questionnaire (mRDQ) (Moojen, 2013; Richter, 2010) en beide studies lieten gedurende de follow-up geen verschil zien tussen interspinale implantaten en decompressie. Eén studie rapporteerde de ODI (Richter, 2010) en liet gedurende de follow-up geen verschil zien tussen interspinale implantaten en decompressie (p=0,22).
Kwaliteit van leven
Twee studies rapporteerden de SF-36 (Moojen, 2013; Stromqvist, 2013). De preoperatieve waardes voor Stromqvist waren 25 voor X-Stop en 28 voor decompressie, postoperatief waren deze 40 en 38, deze verschillen waren niet klinisch relevant. Voor Moojen varieerden de p-waardes van 0,34 tot 0,95 voor de verschillende domeinen. Beide studies lieten dus geen verschil zien voor kwaliteit van leven tussen interspinale implantaten en decompressie.
Interspinale implantaten (IPD) versus niet-operatieve interventie bij lumbale kanaalstenose
Voor de vergelijking van IPD met niet-operatieve interventies werd één review (Moojen 2011) met twee studies (Anderson 2006, Zucherman 2004) geïncludeerd. In beide studies werd de X-stop als het IPD-implantaat gebruikt, en minimaal één steroïde injectie met eventueel aanvullende fysiotherapie in de controlegroep.
Pijn (VAS-schaal)
Pijn werd in de studies niet meegenomen.
Functioneren (Disability)
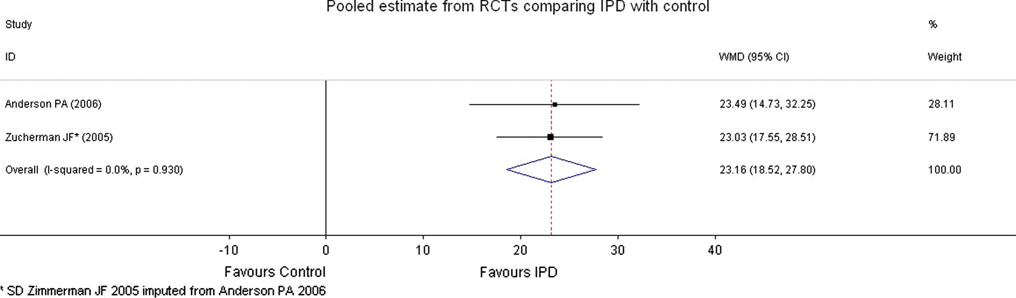
Beide studies (Anderson, 2006; Zucherman, 2004) rapporteerden de ZCQ en in beide studies werd een beter resultaat gezien voor interspinale implantaten vergeleken met conservatieve behandeling. Dit bestond in deze studies uit tenminste één epidurale steroïde injectie, NSAID’s, pijnstillers en fysiotherapie indien nodig. Het gepoolde effect was 23,16 95% BI 18,52 tot 27,80). Dit wordt gezien als een klinisch relevant verschil.
Figuur 3 Functionaliteit gemeten met de ZCQ, forest plot voor de vergelijking IPD versus controlegroep.
Kwaliteit van leven
Kwaliteit van leven met SF-36 werd in één studie gerapporteerd (Anderson, 2006) en liet een betere uitkomst zien voor interspinale implantaten bij analyse van een gecombineerde score. Dit verschil was niet statistisch significant.
Dynamische posterieure pedikelschroeffixaties versus rigide pedikelschroeffixaties bij degeneratieve lumbale spondylolisthesis
Voor de vergelijking van dynamische pedikelschroeffixaties met traditionele rigide fixaties werd één RCT (Yu, 2012) en twee observationele studies (Kaner, 2010; Korovessis, 2004) geïncludeerd. Beide observationele studies gebruikten het Cosmic implantaat.
Pijn (VAS-schaal)
Yu vond geen verschillen tussen Dynesis en spondylodese na drie jaar follow-up qua verbetering in beenpijn (-5,37 ± 1,42 versus -5,08 ± 1,55; p=0,475) of qua verbetering in rugpijn (-4,33 ± 2,37 versus -4,15 ± 2,77; p=0,801). Kaner vond geen verschil in “pijn” (niet gedifferentieerd) tussen de Cosmic dynamische schroeffixatie en rigide schroeffixatie op 3, 12 en 24 maanden (24 maanden: 8,4 ± 6,7 versus 10,0 ± 10,7, p=0,94). Korovessis liet resultaten zien die niet klinisch relevant van elkaar verschilden.
Functioneren (Disability)
Kaner vond geen verschil in Oswestry score tussen Cosmic dynamische schroeffixatie en rigide schroeffixatie op 3, 12 en 24 maanden (24 maanden: 9,23 ± 5,43 versus 10,2± 7,8, p=0,67). Yu vond geen verschil tussen Dynesis en spondylodese na drie jaar qua verbetering in Oswestry score (-32,7 ± 8,6 versus -29,3 ± 12,7; p=0,25).
Kwaliteit van leven
Korovessis liet resultaten zien die niet klinisch relevant van elkaar verschilden.
Bewijskracht van de literatuur
Discusprothese versus fusie bij lage rugpijn met aspecifieke degeneratieve kenmerken
De kwaliteit van de geïncludeerde studies is geëvalueerd in de review van Jacobs (2011) (zie daarvan tabel Characteristics of included studies). De kwaliteit van de studies was laag door gebrek aan blindering, retrospectieve studieplannen en sponsoring.
Rugpijn
Voor verbetering van rugpijn is de bewijskracht van de studies “laag” omdat er mogelijk publicatiebias is en vanwege imprecisie van de data.
Beenpijn
Voor beenpijn is de bewijskracht “zeer laag” vanwege mogelijk publicatiebias, imprecisie en inconsistentie.
Functioneren
Voor functioneren gemeten met de ODI is de bewijskracht “gemiddeld” vanwege inconsistentie van de resultaten.
Kwaliteit van leven
Voor kwaliteit van leven beoordeelde de review het bewijs als zeer laag.
Discusprothese versus niet-operatief bij lage rugpijn met aspecifieke degeneratieve kenmerken
Aangezien er slechts één vergelijkende niet gerandomiseerde studie (Hellum, 2011) kon worden geïncludeerd, is de bewijskracht voor pijn, functioneren en kwaliteit van leven laag. Vanwege imprecisie werd de bewijskracht verlaagd werd naar zeer laag (men kon namelijk niet concluderen of de verbeteringen klinisch relevant waren).
Interspinale implantaten (IPD) versus fusie bij lumbale kanaalstenose
Twee observationele studies (Azzazi, 2010; Davis, 2013) hebben een hoog risico op bias mede door gebrek aan blindering. De bewijskracht van de studies is daarmee “laag” voor pijn en functioneren. Slechts één studie rapporteert over kwaliteit van leven, waarin de bewijskracht “zeer laag” is vanwege mogelijke publicatiebias.
Interspinale implantaten (IPD) versus decompressie bij lumbale kanaalstenose en graad 1 spondylolisthesis
Twee RCTs (Moojen, 2013; Stromqvist, 2013) werden kwalitatief goed uitgevoerd en hebben daardoor een hoge bewijskracht. De bewijskracht werd verlaagd vanwege imprecisie naar gemiddeld.
Interspinale implantaten (IPD) versus niet-operatieve interventie bij lumbale spinale stenose
De kwaliteit van de geïncludeerde studies (Anderson, 2006; Zucherman, 2004) is geëvalueerd in de review van Moojen (2011). Eén studie had een laag risico op bias en één studie had een hoog risico op bias. De bewijskracht is voor functioneren Laag en voor kwaliteit van leven Zeer laag. Over pijn waren geen gegevens beschikbaar.
Dynamische posterieure pedikelschroeffixaties versus rigide pedikelschroeffixaties bij degeneratieve lumbale spondylolisthesis
Hier werd één RCT geïncludeerd met een hoog risico op bias en twee observationele studies; de bewijskracht werd daarom als Laag gewaardeerd. De bewijskracht voor pijn is Laag. Voor functioneren en kwaliteit van leven is de bewijskracht Zeer laag vanwege mogelijke publicatiebias en imprecisie.
In de databases Medline (Pubmed), Embase en Cochrane is met relevante zoektermen gezocht naar studies over chirurgische ingrepen bij degeneratieve aandoeningen van de wervelkolom. Er werd eerst een overkoepelende search verricht gericht op reviews en vervolgens een aanvullende search naar mogelijke nieuwe primaire studies. De selectie heeft zich beperkt tot de vergelijkingen van dynamische stabilisatie met fusie, decompressie of niet-operatieve behandeling.
Voor de indicatie lage rugpijn met aspecifieke degeneratieve kenmerken werden enkel interventies met discusprotheses gevonden.
Voor de indicaties kanaalstenose en spondyolisthesis werden ter dynamische stabilisatie de interventies dynamische posterieure instrumentatie (dynamic rods) en posterieure interspinosale implantaten (IPD, interspinal process devices) gevonden.
Voor de indicatie deformiteiten werden geen studies gevonden.
Relevante uitkomstmaten
De werkgroep achtte pijnbeleving en functioneren voor de besluitvorming kritieke uitkomstmaten. Daarnaast worden kwaliteit van leven en psychosociaal functioneren voor de besluitvorming belangrijke uitkomstmaten geacht.
- Anderson PA, Tribus CB, Kitchel SH. Treatment of neurogenic claudication by interspinous decompression: application of the X STOP device in patients with lumbar degenerative spondylolisthesis. J Neurosurg Spine 2006;4:463-471.
- Azzazi A, Elhawary Y. Dynamic Stabilization Using X-stop Versus Transpedicular Screw Fixation in the Treatment of Lumbar Canal Stenosis; Comparative Study of the Clinical Outcome. Neurosurg Q Volume 2010;20(3):165-169.
- Berg S, Tullberg T, Branth B, et al. Total disc replacement compared to lumbar fusion: a randomised controlled trial with 2-year follow-up. Eur Spine J 2009;18:1512-1519.
- Blumenthal S, McAfee PC, Guyer RD, et al. A prospective, randomized, multicenter Food and Drug Administration investigational device exemptions study of lumbar total disc replacement with the CHARITE artificial disc versus lumbar fusion: part I: evaluation of clinical outcomes. Spine (Phila Pa 1976 ) 2005;30:1565-1575.
- Davis RJ, Errico TJ, Bae H, et al. Decompression and Coflex interlaminar stabilization compared with decompression and instrumented spinal fusion for spinal stenosis and low-grade degenerative spondylolisthesis: two-year results from the prospective, randomized, multicenter, Food and Drug Administration Investigational Device Exemption trial. Spine (Phila Pa 1976). 2013;38(18):1529-39. doi: 10.1097/BRS.0b013e31829a6d0a. PubMed PMID: 23680830.
- Gornet MF, Burkus JK, Dryer RF, et al. Lumbar disc arthroplasty with Maverick disc versus stand-alone interbody fusion: a prospective, randomized, controlled, multicenter investigational device exemption trial. Spine (Phila Pa 1976). 2011;36:E1600-E1611.
- Hellum C, Johnsen LG, Storheim K, et al. Surgery with disc prosthesis versus rehabilitation in patients with low back pain and degenerative disc: two year follow-up of randomised study. BMJ. 2011;342:d2786.
- Jacobs W, Van der Gaag NA, Tuschel A, et al. Total disc replacement for chronic back pain in the presence of disc degeneration. Cochrane Database Syst Rev. 2012;9, PubMed PMID:22972118.
- Jacobs W, Willems PC, Kruyt M, et al. Systematic review of anterior interbody fusion techniques for single- and double-level cervical degenerative disc disease. Spine (Phila Pa 1976). 2011;36(14):E950-60. doi: 10.1097/BRS.0b013e31821cbba5. Review. PubMed PMID: 21522044.
- Kaner T, Dalbayrak S, Oktenoglu T, et al. Comparison of posterior dynamic and posterior rigid transpedicular stabilization with fusion to treat degenerative spondylolisthesis. Orthopedics. 2010;33(5).
- Korovessis P, Baikousis A, Koureas G, et al. Correlative analysis of the results of surgical treatment of thoracolumbar injuries with long Texas Scottish rite hospital construct: is the use of pedicle screws versus hooks advantageous in the lumbar spine? J Spinal Disord Tech 2004;17:195-205.
- Moojen WA, Arts MP, Bartels RH, et al. Effectiveness of interspinous implant surgery in patients with intermittent neurogenic claudication: a systematic review and meta-analysis. Eur Spine J 2011;20:1596-1606.
- Moojen WA, Arts MP, Jacobs WC, et al. Interspinous process device versus standard conventional surgical decompression for lumbar spinal stenosis: randomized controlled trial. BMJ. 2013;347:f6415.
- Moojen WA, Arts MP, Jacobs WC, et al. IPD without bony decompression versus conventional surgical decompression for lumbar spinal stenosis: 2-year results of a double-blind randomized controlled trial. Eur Spine J. 2015;24(10):2295-305. doi: 10.1007/s00586-014-3748-2. Epub 2015 Jan 14. PubMed PMID: 25586759.
- Moreno P, Boulot J. [Comparative study of short-term results between total artificial disc prosthesis and anterior lumbar interbody fusion]. Rev Chir Orthop Reparatrice Appar Mot. 2008;94(3):282-8.
- Richter A, Schutz C, Hauck M, et al. Does an interspinous device (Coflex) improve the outcome of decompressive surgery in lumbar spinal stenosis? One-year follow up of a prospective case control study of 60 patients. Eur Spine J 2010;19:283-289.
- Strömqvist BH, Berg S, Gerdhem P, et al. X-stop versus decompressive surgery for lumbar neurogenic intermittent claudication: randomized controlled trial with 2-year follow-up. Spine (Phila Pa 1976). 2013;38(17):1436-42. PubMed PMID: 23403549.
- Van den Eerenbeemt KD, Ostelo RW, van Royen BJ, et al. Total disc replacement surgery for symptomatic degenerative lumbar disc disease: a systematic review of the literature. Eur Spine J 2010;19:1262-1280.
- Wang JC, Arnold PM, Hermsmeyer JT, et al. Do lumbar motion preserving devices reduce the risk of adjacent segment pathology compared with fusion surgery? A systematic review. Spine (Phila Pa 1976 ) 2012;37:S133-S143.
- Yajun W, Yue Z, Xiuxin H, et al. A meta-analysis of artificial total disc replacement versus fusion for lumbar degenerative disc disease. Eur Spine J 2010;19:1250-1261.
- Yu SW, Yang SC, Ma CH, et al. Comparison of Dynesys posterior stabilization and posterior lumbar interbody fusion for spinal stenosis L4L5. Acta Orthop Belg. 2012;78(2):230-9.
- Zigler J, Delamarter R, Spivak JM, et al. Results of the prospective, randomized, multicenter Food and Drug Administration investigational device exemption study of the ProDisc-L total disc replacement versus circumferential fusion for the treatment of 1-level degenerative disc disease. Spine (Phila Pa 1976). 2007;32:1155-1162.
- Zucherman JF, Hsu KY, Hartjen CA, et al. A prospective randomized multi-center study for the treatment of lumbar spinal stenosis with the X STOP interspinous implant: 1-year results. Eur Spine J 2004;13:22-31.
Table of quality assessment
Research question: Discusprothese versus spinale fusie (of spondylodese)
Indicatie lage rugpijn met aspecifieke degeneratieve kenmerken
Risk of bias table for intervention studies (randomized controlled trials)
|
Study reference
(first author, publication year) |
Bias due to method of randomisation (Describe method) 1
(unlikely/likely/unclear) |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3 (unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Berg 2009 |
Unlikely |
Unlikely |
Likely |
Likely |
Likely |
Unclear |
Unlikely |
Unlikely |
|
Blumenthal 2005 |
Unlikely |
Unlikely |
Likely |
Likely |
Likely |
Unclear |
Unlikely |
Unlikely |
|
Gornet 2011 |
Unlikely |
Unlikely |
Unclear |
Likely |
Unclear |
Unclear |
Unlikely |
Unlikely |
|
Hellum 2011 |
Unlikely |
Unclear |
Likely |
Likely |
Unlikely |
Unclear |
Unlikely |
Unlikely |
|
Moreno 2008 |
Unclear |
Unclear |
Likely |
Likely |
Likely |
Unclear |
Unlikely |
Unlikely |
|
Zigler 2007 |
Unlikely |
Likely |
Likely |
Likely |
Unclear |
Unclear |
Unlikely |
Unlikely |
Research question: Interspinaleprocessdevices (IPD) versus fusie
Indicatie: lumbale spinale stenose
Risk of bias table for intervention studies (randomized controlled trials)
|
Study reference
(first author, publication year) |
Bias due to method of randomisation (Describe method) 1
(unlikely/likely/unclear) |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3 (unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Azzazi 2010 |
Unclear |
Unclear |
Unclear |
Likely |
Unclear |
Unclear |
Unclear |
Unclear |
|
Davis 2013 |
Unlikely |
Unlikely |
Likely |
Likely |
Likely |
Likely |
Unlikely |
Unlikely |
|
Yu 2012 |
Unlikely |
Unclear |
Likely |
Likely |
Likely |
Unclear |
Unlikely |
Likely |
Research question: Interspinaleprocessdevices (IPD) versus decompressie
Indicatie: lumbale spinale stenose
Risk of bias table for intervention studies (randomized controlled trials)
|
Study reference
(first author, publication year) |
Bias due to method of randomisation (Describe method) 1
(unlikely/likely/unclear) |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3 (unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Stromqvist 2013 |
Unclear |
Unlikely |
Likely |
Likely |
Likely |
Unlikely |
Unlikely |
Unlikely |
|
Moojen 2013 |
Unlikely |
Unlikely |
Unlikely |
Likely |
Unlikely |
Unlikely |
Unlikely |
Unlikely |
Risk of bias table for observational studies (prospective controlled trials)
|
Study reference
(first author, publication year) |
Representativeness of the exposed cohort |
Selection of the non exposed cohort |
Ascertainment of exposure |
Demonstration that outcome of interest was not present at start of study |
Comparability of cohorts on the basis of the design or analysis |
Assessment of outcome |
Was follow-up long enough for outcomes to occur |
Adequacy of follow up of cohorts |
|
Richter 2010 |
truly representative of the average degenerative spondylolisthesis patient |
drawn from the same community as the exposed cohort |
secure record (eg surgical records) |
Yes |
No control for confounding |
self report |
yes |
Unclear |
Research question: Interspinaleprocessdevices (IPD) versus niet-operatieve interventie
Indicatie: lumbale spinale stenose
Risk of bias table for intervention studies (randomized controlled trials)
|
Study reference
(first author, publication year) |
Bias due to method of randomisation (Describe method) 1
(unlikely/likely/unclear) |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3 (unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Anderson 2006 |
Likely |
Likely |
Likely |
Likely |
Unclear |
Unclear |
Unlikely |
Unlikely |
|
Zucherman 2004 |
Likely |
Likely |
Likely |
Likely |
Unclear |
Unclear |
Unlikely |
Unclear |
Research question: Dynamische posterieure pedikelschroeffixaties versus rigide pedikelschroeffixaties
Indicatie: degeneratieve lumbale spondylolisthesis
Risk of bias table for observational studies (prospective controlled trials)
|
Study reference
(first author, publication year) |
Representativeness of the exposed cohort |
Selection of the non exposed cohort |
Ascertainment of exposure |
Demonstration that outcome of interest was not present at start of study |
Comparability of cohorts on the basis of the design or analysis |
Assessment of outcome |
Was follow-up long enough for outcomes to occur |
Adequacy of follow up of cohorts |
|
Kaner 2002 |
truly representative of the average degenerative spondylolisthesis patient |
drawn from the same community as the exposed cohort |
secure record (eg surgical records) |
Yes |
No control for confounding |
self report |
yes |
complete follow up - all subjects accounted for |
|
Korovessis 2004 |
truly representative of the average degenerative spondylolisthesis patient |
drawn from the same community as the exposed cohort |
secure record (eg surgical records) |
Yes |
No control for confounding |
self report |
yes |
complete follow up - all subjects accounted for |
Research question: Discusprothese versus spinale fusie (of spondylodese), Discusprothese versus conservatieve behandeling
Indicatie lage rugpijn met aspecifieke degeneratieve kenmerken
Systematic review of RCTs and observational studies (intervention studies)
|
Study reference |
Study characteristics SR meta-analysis type of studies Literature search date Studies Source of funding |
Patient characteristics Selection criteria # studies included Important patient characteristics at baseline (per study:N, mean age) Type of back pain: Groups comparable at baseline? |
Intervention (I)
|
Comparison / control (C)
|
Follow-up End-point of follow-up For how many participants were no complete outcome data available?
|
Outcome measures and effect size Outcome measure-1 Defined as.Oswestry Disability Score (ODI). Outcome measure-2
|
Comments |
|
Jacobs |
SR
|
N=6 |
Discus prothese |
Any other intervention (fusion, conservative intervention) |
|
|
|
Research question: Discusprothese versus spinale fusie (of spondylodese)
Indicatie lage rugpijn met aspecifieke degeneratieve kenmerken
Systematic review of RCTs and observational studies (intervention studies)
|
Study reference |
Study characteristics SR meta-analysis type of studies Literature search date Studies Source of funding |
Patient characteristics Selection criteria # studies included Important patient characteristics at baseline (per study:N, mean age) Type of back pain: Groups comparable at baseline? |
Intervention (I)
|
Comparison / control (C)
|
Follow-up End-point of follow-up For how many participants were no complete outcome data available?
|
Outcome measures and effect size Outcome measure-1 Defined as.Oswestry Disability Score (ODI). Outcome measure-2
|
Comments |
|
Moojen 2011 |
SR
|
|
|
|
|
|
|
Intervention studies (randomized controlled trials and non-randomized observational studies [cohort studies, case-control studies, case series])1
Research question: Discusprothese versus spinale fusie (of spondylodese)
Indicatie lage rugpijn met aspecifieke degeneratieve kenmerken (From Jacobs 2011)
|
Study reference Ref |
Study characteristics Type of study: Setting: Country: Source of funding: |
Patient characteristics 2 Inclusion criteria: Exclusion criteria: N total at baseline: Important prognostic factors2 |
Intervention (I) Describe intervention (treatment/procedure/test):
|
Comparison / control (C) 3 Describe control (treatment/procedure/test):
|
Follow-up Length of follow-up: Loss-to-follow-up: Incomplete outcome data |
Outcome measures and effect size 4 Outcome measures and effect size (include 95%CI and p-value if available): Disability (Oswestry index, mean change, mixed model): Pain (VAS, mm): Functional (SF-36) Functional EQ-5D Quality of life Psychosocial functioning |
Comments |
|
Berg 2009 |
RCT
|
DDD, 1 or 2 level, MRI Degeneration LBP >1 year; LBP >leg pain ODI >30 or back pain VAS >50 20–55 yr >3 mo conservative treatment N=152 Age: 39,4 (21–55, 8,0) |
CHARITÉ, ProDisc, or Maverick |
Fusion with local or iliac crest bone graft, pedicle screws, posterolateral or interbody fusion with Brantigan cage |
Preoperative 1 and 2 year |
VAS Leg pain VAS back pain SF36 Oswestry disability Index EQ5D Work status |
|
|
Blumenthal 2005 |
RCT |
DDD, single level, L4–S1, discography confi rmed Back and or leg pain ODI >30; VAS >40 18–60 yr >6 mo conservative treatment N=304 Age: 39,6 (19–60, 8,5) |
CHARITÉ |
BAK (2 cages) with iliac crest autograft |
Preoperative 6 weeks 3 and 6 months |
VAS back pain Oswestry disability index Score SF-36 neurological status patient satisfaction ROM disc height neuroforaminal height segmental translation |
|
|
Gornet 2011 |
RCT |
DDD, L4–S1, single level Back pain w/wo leg pain Oswestry >30, back pain >20 >6 mo conservative treatment 18–70 yr Age: 40,0 (18–70, ?) |
MAVERICK disc |
Anterior fusion with LT-CAGE lumbar tapered fusion device and INFUSE bone graft (fusion) |
|
SF-36 Back pain status Leg pain status Patient satisfaction Patient global perceived effect return to work doctor’s perception
|
|
|
Moreno 2008 |
RCT |
DDD, single level, L4–S1, no instability, Modic 1 or 2 on MRI Chronic LBP <55 yr >6 mo conservative treatment, previous discectomy, or chemonucleolysis allowed Age: 42 (33–55, ?) |
CHARITÉ III |
ALIF with KLA cage, iliac crest autograft and anterior plate |
|
VAS Oswestry disability index Score Return to work Satisfaction |
Preoperative 6 months Latest (23 or 26 mo) |
|
Zigler 2007 |
RCT |
DDD, single level, L3–S1 CT/MRI /discography/FEX (instability >3 mm translation, >5º angulation disc height decrease >2 mm; scarring/ thickening annulus; HNP; vacuum phenomenon) Back and/or leg (radicular) pain ODI >40 18–60 yr >6 mo conservative therapy Age: 39,2 (?, 7,9) |
Total disc replacement: ProDisc-L |
Control: Circumferential fusion with femoral ring allograft with pedicle screws and iliac crest autograft |
|
Oswestry disability index Score SF-36 Physical examination Neurological examination |
|
|
Hellum 2011 |
RCT |
Chronic low back pain Degenerative disc disease Age: 41,0 (?, 7,1) |
Device: total disc prosthesis |
Behavioral: multidisciplinary rehabilitation program |
|
Cost-effectiveness Side effects Time out of work Fear-avoidance beliefs Self-effi cacy for pain Hopkins symptoms Drug consumption EQ-5D SF-36 |
|
Intervention studies (randomized controlled trials and non-randomized observational studies [cohort studies, case-control studies, case series])1
Research question: Interspinaleprocessdevices (IPD) versus fusie
Indicatie: lumbale spinale stenose
|
Study reference Ref |
Study characteristics Type of study: Setting: Country: Source of funding: |
Patient characteristics 2 Inclusion criteria: Exclusion criteria: N total at baseline: Important prognostic factors2 |
Intervention (I) Describe intervention (treatment/ procedure/test):
|
Comparison / control (C) 3 Describe control (treatment/procedure/test):
|
Follow-up Length of follow-up: Loss-to-follow-up: Incomplete outcome data |
Outcome measures and effect size 4 Outcome measures and effect size (include 95%CI and p-value if available): Disability (Oswestry index, mean change, mixed model): Pain (VAS, mm): Functional (SF-36) Functional EQ-5D Quality of life Psychosocial functioning |
Comments |
|
Azzazi 2010 |
RCT |
|
|
|
|
|
Nu usable data analyses or presentation |
|
Davis 2013 |
RCT Multicenter US Paradigm Spine, LLC (New York, NY) funds were received in support of this work. |
Radiographical confirmed stenosis 1 or 2 contiguous levels L1–L5 more than 25% reduction of the anteroposterior dimension absence of angular or translatory instability VAS back pain at least 50 mm Neurogenic claudication conservative care between 40 and 80 yr. ODI score at least 20/50 (40%). N=322 |
Interlaminar stabilization (Coflex) with decompression
|
posterior spinal fusion with pedicle screw instrumentation |
baseline, 6 weeks, 3 months, 6 months, 12 months, 18 months, and 24 months |
ODI, Cofl ex cohort showed a trend toward better outcomes at 24 months (22,0 vs 26,7, P = 0,075), with significant differences at 6 weeks ( P = 0,001) and 3-month ( P = 0,033). Zurich Claudication Questionnaire (ZCQ) showed a significant difference at 24 months with respect to ZCQ symptom severity (1,98 vs 2,23; P = 0,023), ZCQ physical function (1,56 vs 1,80; P =0,008), and ZCQ satisfaction (1,42 vs 1,65; P =0,006). VAS back showed a trend toward signifi cantly lower VAS back pain in the Coflex cohort at 3 months ( P = 0,062) and 6 months ( P = 0,063), but not at 24 monts (23,6 vs 27,0; p=0,345). VAS leg pain score was signifi cantly better in the Cofl ex cohort at 3 months ( P = 0,019) and a trend at 6 months ( P = 0,058), but not at 24 months (20,6 vs 24,1;p=0,364). Short-Form 12 (SF-12) improvement was significantly better in the coflex cohort At 24 months, (15,5 vs 12,6; P = 0,050) and 6 weeks ( P = 0,048), and 3 months ( P = 0,032). |
|
Research question: Interspinaleprocessdevices (IPD) versus decompressie
Indicatie: lumbale spinale stenose
|
Study reference Ref |
Study characteristics Type of study: Setting: Country: Source of funding: |
Patient characteristics 2 Inclusion criteria: Exclusion criteria: N total at baseline: Important prognostic factors2 |
Intervention (I) Describe intervention (treatment/ procedure/test):
|
Comparison / control (C) 3 Describe control (treatment/procedure/test):
|
Follow-up Length of follow-up: Loss-to-follow-up: Incomplete outcome data |
Outcome measures and effect size 4 Outcome measures and effect size (include 95%CI and p-value if available): Disability (Oswestry index, mean change, mixed model): Pain (VAS, mm): Functional (SF-36) Functional EQ-5D Quality of life Psychosocial functioning |
Comments |
|
Stromqvist 2013 |
RCT Multicenter Sweden No funds were received in support of this work |
MRI verifi ed spinal stenosis 1 or 2 levels L1–L4 neurogenic claudication for minimum 6 months 40 years or more N=100 |
X stop |
Decompression |
Preoperatively 6, 12, and 24 months |
See tables 4 and 5, no differences found at any follow-up moment SF-36 EQ-5D ZCQ VAS leg pain VAS back pain surgical complications and reoperations IPD vs decompression: 6 vs 26%;p=0,04 |
|
|
Moojen 2013 |
RCT Multicenter Netherlands Paradigm Spine funded this trial. |
40 to 85 years at least three months of intermittent neurogenic claudication single or two level degenerative lumbar canal stenosis MRI evidence of lumbar spinal canal stenosis N=161 |
interspinous process device (Coflex) no bony decompression was done |
standard bony decompression |
baseline 2,4, 8, 12, 26, and 52 weeks |
See table 2 and 3 no differences at 8 weeks, at 52 weeks ZCQ: RMDQ SF36 McGill pain questionnaire Perceived recovery Shuttle walking test HADS reoperations IPD vs decompression: 8 vs 29%;p<0,001 |
|
|
Richter 2010 |
Observational Single center Germany |
symptomatic lumbar spinal stenosis conservative treatment[3 month One or two level No segmental instability Age between 45 and 80 N=60 |
Decompression surgery with additional interspinous CoflexTM device |
Decompression surgery alone |
Preoperative 3, 6 and 12 months |
No differences on any of the outcome parameters ODI RMDQ VAS Back pain
|
|
Research question: Interspinaleprocessdevices (IPD) versus niet-operatieve interventie
Indicatie: lumbale spinale stenose
|
Study reference Ref |
Study characteristics Type of study: Setting: Country: Source of funding: |
Patient characteristics 2 Inclusion criteria: Exclusion criteria: N total at baseline: Important prognostic factors2 |
Intervention (I) Describe intervention (treatment/procedure/test):
|
Comparison / control (C) 3 Describe control (treatment/procedure/test):
|
Follow-up Length of follow-up: Loss-to-follow-up: Incomplete outcome data |
Outcome measures and effect size 4 Outcome measures and effect size (include 95%CI and p-value if available): Disability (Oswestry index, mean change, mixed model): Pain (VAS, mm): Functional (SF-36) Functional EQ-5D Quality of life Psychosocial functioning |
Comments |
|
Anderson 2006 |
RCT Multicenter US Not reported, Dr. Anderson is a consultant for and stockholder of the company manufacturing the X STOP device |
one- or two-level lumbar spinal stenosis at least 50 years symptoms relieved by sitting or flexion at least a 6-month nonoperative treatment. N=75 |
X STOP Device |
at least one epidural steroid injection |
Preoperative 6 weeks 6, 12, and 24 months |
ZCQ improvement X-stop: 27,35, control 3,86 SF-36 Satisfaction Reoperation |
No statistical tests provided |
|
Zucherman 2004 |
RCT Multicenter US Corporate/Industry funds were received in support of this work. |
at least 50 years leg, buttock, or groin pain with or without back pain that was relieved during flexion. to be able to walk at least 50 feet. N=191 |
X STOP |
At least one epidural steroid injection |
Baseline 6 weeks 6 months 1 year, and 2 years |
ZCQ-SS: improvement at 2 years: Xstop 45,4%, control 7,4% in (P<0,001) ZCQ-PF: improvement at 2 years: Xstop 44,34%, control -0,4% in (P<0,001) Complications Six patients in the X STOP group and 24 patients in the control group underwent decompressive surgery (laminectomy) for unresolved stenosis symptoms |
|
Research question: Interspinaleprocessdevices (IPD) versus niet-operatieve interventie
Indicatie: lumbale spinale stenose
|
Study reference Ref |
Study characteristics Type of study: Setting: Country: Source of funding: |
Patient characteristics 2 Inclusion criteria: Exclusion criteria: N total at baseline: Important prognostic factors2 |
Intervention (I) Describe intervention (treatment/ procedure/test):
|
Comparison / control (C) 3 Describe control (treatment/ procedure/test):
|
Follow-up Length of follow-up: Loss-to-follow-up: Incomplete outcome data |
Outcome measures and effect size 4 Outcome measures and effect size (include 95%CI and p-value if available): Disability (Oswestry index, mean change, mixed model): Pain (VAS, mm): Functional (SF-36) Functional EQ-5D Quality of life Psychosocial functioning |
Comments |
|
Kaner 2002 |
Observationeel Multicenter Turkey No relevant conflict of interest as stated |
single-level grade I or II degenerative spondylolisthesis causing central and/or lateral recess syndrome. Excluded: isthmic SPL, degenerative SPL at >1 level, previous lumbar fusion surgery, infections of the spine, systemic diseases N=46 |
Cosmic dynamic transpedicular screws (Ulrich GmbH & Co KG) |
rigid screws |
3, 12, 24 months |
VAS pain ODI |
|
|
Korovessis 2004 |
Observationeel Single center Greece No funding and no conflict of interest as stated |
Symptomatic lumbar spinal stenosis For at least 1 year No prior spine surgery, active infection, or congenital deformity N=45 |
Dynamic pedicle screw: Twinflex21 (Eurosurgical)
Semirigid (Claris) pedicle screw |
“Rigid” pedicle screw: Segmental Contouring System20 (SCS, Eurosurgical, Beaurains, France) device |
47 +/- 14 months (range 27–68 months). |
Short-form 36 (SF-36) Visual Analogue Scale (VAS) for low back Visual Analogue Scale (VAS) for leg pain. |
|
|
Yu 2012 |
RCT Single center China Funding not reported |
38 to 71 years spinal stenosis severe instability preoperative ODI >40 conservative treatment L4L5 one level <= grade I spondylolisthesis N=60 |
Dynesys posterior dynamic stabilization Simple decompression (interlaminar decompression or laminotomy) was performed in most cases |
PLIF was performed in a standard manner using Synthes Click’X spinal implants. When required, extensive decompression and facetectomy were performed |
3 months, 1, 2, and 3 years |
VAS Back pain at 3 year: Dynesis vs fusion: -4,33 ± 2,37 -4,15 ± 2,77; p=0,801, VAS Leg pain at 3 year: Dynesis vs fusion: -5,37 ± 1,42 vs -5,08 ± 1,55; p=0,475, ODI at 3 year: Dynesis vs fusion: -32,74 ± 8,63 vs -29,31 ± 12,72; p=0,254, |
|
Beoordelingsdatum en geldigheid
Publicatiedatum : 29-05-2017
Beoordeeld op geldigheid : 22-04-2017
Uiterlijk in 2021 bepaalt het bestuur van de NOV of deze richtlijn nog actueel is. Zo nodig wordt een nieuwe werkgroep geïnstalleerd om de richtlijn te herzien. De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De NOV is als houder van deze richtlijn de eerstverantwoordelijke voor de actualiteit van deze richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijk verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de eerstverantwoordelijke over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel van de richtlijn
Het doel van deze richtlijn is het ontwikkelen van een eenduidige indicatiestelling voor geïnstrumenteerde wervelkolomchirurgie (operaties met gebruik van spinale implantaten) en het beoordelen van de effectiviteit van dergelijke ingrepen bij degeneratieve aandoeningen van de thoracolumbosacrale wervelkolom. Deze ingrepen beogen correctie en/of stabilisatie van de wervelkolom, al dan niet gepaard met neurologische decompressie. In de praktijk betreft het voornamelijk patiënten met degeneratieve scoliose, spondylolysis/spondylolisthesis, of patiënten met chronische lage rug- en/of beenpijn verondersteld te zijn veroorzaakt door discusdegeneratie en/of facetartrose die op beeldvorming werd geconstateerd.
Deze richtlijn beoogt een bijdrage te leveren aan het verhogen van de kwaliteit van zorg met betrekking tot de geïnstrumenteerde operatieve behandeling van degeneratieve wervelkolomaandoeningen. Daarbij is tevens het doel om middels heldere, eenduidige indicatiestelling ongewenste praktijkvariatie terug te dringen.
Afbakening van de richtlijn
De richtlijn richt zich op alle patiënten:
- van 18 jaar en ouder;
- met langer dan drie maanden bestaande rug- en/of beenpijn op basis van degeneratieve aandoeningen van de thoracolumbosacrale wervelkolom;
- bij wie conservatieve behandeling, indien geïndiceerd, met multidisciplinaire gestructureerde oefenprogramma’s inclusief psychologische screening en eventuele pijninterventies, onvoldoende baat heeft gehad;
- die door hun klachten dermate ernstig zijn geïnvalideerd dat ze gemotiveerd zijn om een wervelkomingreep met bijbehorende herstelfase en revalidatie te doorlopen.
Specifiek gaat het in deze richtlijn om de volgende patiëntencategorieën:
- lumbale spondylolysis / laaggradige (graad I of II) spondylolisthesis: patiënten met degeneratieve spondylolisthesis, spondylolysis of spondylolytische spondylolisthesis. Laaggradige lumbale spondylolisthesis kan gepaard gaan met rugpijn en/of radiculaire of niet-radiculaire beenpijn of neurogene claudicatie;
- adulte deformiteiten: het betreft hier patiënten met degeneratieve scoliose op basis van progressie van een reeds bestaande idiopathische scoliose, dan wel patiënten met een nieuw ontstane “De Novo” scoliose van de lumbale wervelkolom; daarnaast patiënten met een alignementsstoornis of deformiteit van de wervelkolom na trauma, tumor, infectie of chirurgie aan de wervelkolom in het verleden;
- chronische lage rug- en/of beenpijn: patiënten met lage rugpijn bij facetarthrosis of discusdegeneratie op röntgenfoto en/of MRI (osteofyten, discusversmalling, black discs, Modic veranderingen, annulus scheuren).
Instrumentatie betekent hier het gebruik van spinale implantaten. Hieronder vallen schroef-/haak- en staafconstructies, intervertebrale cages, discusprotheses en interspinosale spacers.
Deze richtlijn gaat niet over patiënten die geïnstrumenteerde chirurgie van de thoracolumbosacrale wervelkolom ondergaan wegens een tumor, infectie, fractuur of een congenitale afwijking. Zoals reeds vermeld zal voor ongeïnstrumenteerde operatieve behandeling bij HNP en lumbale kanaalstenose een separaat, hieraan gekoppelde richtlijn worden ontwikkeld, welke start in 2015. Ook operatieve behandeling van de cervicale wervelkolom valt buiten de huidige richtlijn.
Beoogde gebruikers van de richtlijn
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen die betrokken zijn bij de zorg voor patiënten met degeneratieve aandoeningen van de wervelkolom, voor patiënten en voor beleidsmedewerkers in de gezondheidszorg: In het bijzonder is de richtlijn opgesteld voor orthopedisch chirurgen en neurochirurgen die zich bezighouden met de operatieve behandeling van degeneratieve aandoeningen van de wervelkolom. Daarnaast biedt de richtlijn houvast voor anesthesiologen en andere (para)medici die betrokken zijn bij de zorg voor patiënten met degeneratieve aandoeningen van de wervelkolom.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2013 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met aspecifieke degeneratieve rugklachten, spondylolisthesis en scoliose te maken hebben (zie hiervoor de samenstelling van de werkgroep).
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep werkte gedurende drie jaar aan de totstandkoming van de richtlijn. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
- Dr. P.C. Willems, orthopedisch chirurg, Maastricht universitair medisch centrum, namens de Nederlandse Orthopaedische Vereniging (NOV), (voorzitter)
- Drs. E.A. Hoebink, othopedisch chirurg, Amphia ziekenhuis Breda, namens de NOV
- Prof. dr. B.J. van Royen, othopedisch chirurg, VUMC Amsterdam, namens de NOV
- Dr. G.J. Bouma, Amsterdam Medisch Centrum UvA, namens de Nederlandse Vereniging voor Neurochirurgie (NVvN)
- Dr. M.P. Arts, MC Haaglanden, namens de NVvN
- Dr. J.M.A. Kuijlen, Universitair Medisch Centrum Groningen, namens de NVvN
- Dhr. L. Voogt, namens de Nederlandse Vereniging voor Rugpatiënten
- Drs. M.A.M.B. Terheggen, Rijnstate ziekenhuis Arnhem, namens de Nederlandse Vereniging voor Anesthesiologie
- Dr. H. van de Meent, Radboud Universitair Medisch Centrum Nijmegen namens de Vereniging van Revalidatieartsen
- Dr. T. Hoogeboom, IQ Healthcare Nijmegen, namens het Koninklijk Nederlands Genootschap voor Fysiotherapie
- Dr. C.G.J. Saris, Radboud Universitair Medisch Centrum Nijmegen, namens de Nederlandse Vereniging voor Neurologie
Met ondersteuning van:
- Dr. M.L. Molag, adviseur, Kennisinstituut van Medisch Specialisten Utrecht
Met dank aan:
- Dr. W.H.G. Jacobs, epidemioloog, Dutch Spine Society
Belangenverklaringen
De werkgroepleden hebben schriftelijk verklaard of ze in de laatste vijf jaar een (financieel ondersteunde) betrekking onderhielden met commerciële bedrijven, organisaties of instellingen die in verband staan met het onderwerp van de richtlijn. Tevens is navraag gedaan naar persoonlijke financiële belangen, belangen door persoonlijke relaties, belangen door middel van reputatiemanagement, belangen vanwege extern gefinancierd onderzoek, en belangen door kennisvalorisatie. Een overzicht van de ingevulde belangenverklaringen vindt u bij de verantwoording.
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door deelname van een vertegenwoordiger van patiëntenvereniging de Wervelkolom aan de werkgroep. Er werd reeds een focusgroep gehouden met rugpatiënten tijdens de ontwikkeling van de richtlijn Wervelkolom gerelateerde pijnklachten, een belangrijk uitgangspunt voor de huidige richtlijn. Afgesproken werd om voor deze richtlijn geen nieuwe focusgroep te houden. De conceptrichtlijn zullen we tijdens de commentaarfase laten lezen door rugpatiënten via de Wervelkolom om op die manier hun input op de aanbevelingen te kunnen gebruiken. De verslagen van de invitational conference en focusgroep zijn besproken in de werkgroep en de belangrijkste knelpunten zijn verwerkt in de richtlijn. Het verslag is te vinden in de bijlage.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen volgens het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwalititeit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II) (www.agreecollaboration.org), dat een internationaal breed geaccepteerd instrument is en op ‘richtlijnen voor richtlijn’ voor de beoordeling van de kwaliteit van richtlijnen.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens zijn er knelpunten aangedragen tijdens een invitational conference met de Vereniging van Scoliosepatiënten, patiëntenvereniging de Wervelkolom, zorgverzekeraars, Inspectie voor de Gezondheidszorg en Zorginstituut Nederland en door een focusgroepbijeenkomst met patiënten. Een verslag hiervan kunt u vinden onder aanverwante items.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang als cruciaal, belangrijk en onbelangrijk.
Als relevante uitkomstmaten waarop studies zullen worden geselecteerd en beoordeeld heeft de werkgroep gekozen:
- pijn middels een Visual Analogue Scale (VAS-beenpijn, VAS-rugpijn);
- functionele beperkingen middels gevalideerde vragenlijsten, zoals Oswestry Disability Index (ODI), Quebec Back Pain Disability Scale (QBPDS) of Roland Morris Disability Questionnaire (RMDQ);
- kwaliteit van Leven middels EuroQoL, EQ5D, SF-36;
- patiënt-tevredenheid.
De werkgroep wil benadrukken dat een deel van de vastgestelde conclusies sterk samenhangt met de door de werkgroep vastgestelde klinisch relevante verschillen tussen groepen patiënten die in studies zijn vergeleken. Klinisch relevante verschillen werden door de werkgroep vastgesteld op basis van een consensus—artikel van Ostelo (Ref Ostelo, Spine 2008). De resultaten kunnen uiteraard anders uitpakken als deze grenzen tussen succes en falen iets hoger of lager worden gelegd.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar bestaande buitenlandse richtlijnen en naar systematische reviews in Medline, Cochrane en Cinahl. Vervolgens werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekactie of gebruikte trefwoorden van de zoekactie en de gehanteerde selectiecriteria zijn te vinden in de module van desbetreffende uitgangsvraag.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld door de adviseur en medisch specialist, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (bias) te kunnen inschatten.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij voldoende overeenkomsten tussen de studies werden de gegevens ook opgenomen in een meta-analyse.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) voor interventievragen:
de kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor Grading Recommendations Assessment, Development and Evaluation (zie http://www.gradeworkinggroup.org/) (Atkins, 2004).
B) voor vragen over waarde diagnostische tests, schade of bijwerkingen, etiologie en prognose:
bij dit type vraagstelling kan GRADE (nog) niet gebruikt worden. De bewijskracht van de conclusie is bepaald volgens de gebruikelijke EBRO-methode (Van Everdingen, 2004).
Formuleren van de conclusies
Voor vragen over waarde diagnostische tests, schade of bijwerkingen, etiologie en prognose is het wetenschappelijke bewijs samengevat in een of meerdere conclusies, waarbij het niveau van het meest relevante bewijs is weergegeven.
Bij interventievragen verwijst de conclusie niet naar één of meer artikelen, maar wordt getrokken op basis van alle studies samen (body of evidence). Hierbij maakten de werkgroepleden de balans op van elke interventie. Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen.
Overwegingen
Voor een aanbeveling zijn naast het wetenschappelijke bewijs ook andere aspecten belangrijk, zoals de expertise van de werkgroepleden, patiëntenvoorkeuren, kosten, beschikbaarheid van voorzieningen of organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven een antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module ‘Organisatie van zorg bij spinaalchirurgie’.
Indicatorontwikkeling
De werkgroep kiest ervoor om aan te sluiten bij de Kwaliteitsindicatoren die door het DICA worden uitgevraagd in het kader van de Dutch Spine Registry.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is, dat is aangegeven waar van toepassing.
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor autorisatie en door hen geautoriseerd.
Literatuur
- Appraisal of Guidelines for Research & Evaluation II, www.agreecollaboration.org.
- Atkins D, Best D, Briss PA, et al. Grading quality of evidence and strength of recommendations. BMJ 2004;328(7454):1490.
- Van Everdingen JJE, Burgers JS, Assendelft WJJ, et al. Evidence-based richtlijnontwikkeling. Bohn Stafleu Van Loghum, 2004.
