MRI bij vasculaire stent
Uitgangsvraag
Wat zou het algemene beleid moeten zijn bij patiënten met een vasculaire stent of graft die een MRI moeten ondergaan?
Aanbeveling
Aanbeveling 1 (MR voorwaardelijk)
Bij patiënten met vasculaire stents kan MRI plaatsvinden rekening houdend met aanbevelingen 2, 3 en 4.
Aanbeveling 2 (geen wachttijd)
Patiënten met vasculaire stents kunnen direct na implantatie MRI ondergaan.
Aanbeveling 3 (1,5 T versus 3 T)
Bij patiënten met vasculaire stents kan MRI plaatsvinden bij zowel 1,5 T als 3 T ‘whole body’ MRI-scanners met een horizontale/gesloten supergeleidende magneet.
Aanbeveling 4 (SAR niveau)
Scan patiënten met vasculaire stents zonder aanvullende restricties op het SAR niveau, zolang gescand wordt met een ‘body’ of hoofd RF zendspoel.
Overwegingen
Samenvatting van het literatuuronderzoek
Er is geen klinisch relevant verschil gevonden tussen het aantal negatieve patiënt-gerelateerde uitkomsten die van invloed zijn op de patiënt met vasculaire implantaten tijdens en/of na het ondergaan van een MRI. In de literatuur is er gezocht naar studies die MRI’s vergelijken. Er zijn zes vergelijkende studies geïncludeerd, die strikt voldoen aan de PICO. Door de lage aantallen die zijn gerapporteerd en sterke heterogeniteit was het niet mogelijk om de resultaten samen te voegen. De bewijskracht voor de evidentie uit deze artikelen die strikt aan de PICO voldoen is mede daardoor zeer laag.
In de niet vergelijkende studies is het voorkomen van negatieve effecten door het ondergaan van een MRI relatief laag.
Andere richtlijnen en consensus statements
Er zijn vijf relevante consensus statements of richtlijnen gevonden uit Noord-Amerika en Duitsland (tabel 5).
Tabel 5. Overzicht van gevonden consensus statements en richtlijnen die melding maken over vasculaire stents.
|
Type document (land) |
Auteur, jaar |
Conclusie |
|
AHA Scientific statement (U.S.A.) |
Levine, 2007 |
Coronair stents: Stent implantatie zorgt voor onmiddellijke verankering van de stent, reeds voldoende om additionele krachten door MRI bij beeldvorming te weerstaan. Additionele verankering ontstaat in 6-8 weken na implantatie door weefsel ingroei. Dit laatste heeft geleid tot aanbevelingen om 6-8 weken te wachten bij niet-ferromagnetische coronair stents, echter hiervoor is geen goede (klinische) onderbouwing. Alle heden ten dage gebruikte coronair stent zijn niet ferromagnetisch en kunnen bij 3 T of minder gescand worden direct na implantatie. Aorta stent grafts en perifere stents: De meerderheid van de aorta stents zijn van niet-ferromagnetische of licht ferromagnetische materialen. Ex vivo onderzoek bij 3 T heeft dit laten zien, uitzondering zijn sommige EndoFit stent grafts en extenders (Endomed Inc.). Studies tot nu toe hebben geen MRI geïnduceerde klinische incidenten laten zien bij deze stents. De Zenith AAA endovascular graft (Cook) heeft veiligheidsclassificatie MR onveilig. De fabrikant geeft aan dat er potentieel risico is, en dat er onvoldoende klinische data beschikbaar zijn. Er moet dus een individuele afweging worden gemaakt. De status vanaf 2019: deze graft incl. hulpstukken is MR voorwaardelijk 1,5 T en 3 T, max ‘whole body’ SAR 2 W/kg 15 min per pulssequentie, 7,2 T/m; waarbij het niet duidelijk is of het stent materiaal is gewijzigd (Cook 2019). MRI bij 3 T binnen 6-8 weken in patiënten met aorta of perifere stents die licht ferromagnetisch zijn, moet op een individuele basis worden beoordeeld. Hierbij is een duidelijk klinisch voordeel van MRI snel na implantatie waarschijnlijk groter dan het risico. |
|
Expert consensus document van ACCF/ACR/ AHA/NASCI/ SCMR (U.S.A.) |
Hundley, 2010 |
Coronair en perifere stents: Meeste van deze stents zijn licht ferromagnetisch of niet ferromagnetisch. Verankering in de wand beschermd tegen beweging en verdere verankering vindt plaats in 6-8 weken. Voor niet-ferromagnetische coronair stents is geen goede rationale of klinische data dat MRI na stentplaatsing uitgesteld moet worden. Data over specifieke stent suggereert dat vele als veilig voor MRI beschouwd kunnen worden, maar niet noodzakelijk bij 3 T. Er zijn geen rapporten voor verhoogd risico van stent subacute of late trombose na MRI. Voor medicijn-afgevende stents gelden dezelfde overwegingen. Lichte opwarming van minder dan 1 °C voor stents en 2 °C voor overlappende stents is gerapporteerd, maar dit effect kan in vivo minder prominent zijn door het zogenaamde ‘heat sink’ effect als gevolg van doorbloeding. Aorta stent graft: De meeste van de aorta stents hebben een veiligheidsclassificatie MR voorwaardelijk met uitzondering van de Zenith AAA endovascular graft (Cook) [zie hiervoor] |
|
Consensus statement Deutsche Gesellschaft für Kardiologie (Duitsland) |
Von Knobelsdorff, 2021 |
De meeste vasculaire stents zijn van niet of zwak ferromagnetisch materiaal. Ze zijn op wisselwerking met MRI getest bij 1,5 T, en in mindere mate bij 3 T. De momenteel op de markt aanwezige vasculaire stents zijn allemaal MR veilig of MR voorwaardelijk gekwalificeerd. De stent worden met druk tijdens implantatie verankerd, wat torsie en migratie tegengaat. Weefsel-ingroei in de eerste weken zorgt voor verdere fixatie. Daarmee zijn torsie en migratie ook van zwak-ferromagnetische stents, die in de ex vivo testomgeving magneetwisselwerking vertonen, bij 1,5 T of lager onwaarschijnlijk. Daarnaast kan er theoretisch opwarming van de stent plaatsvinden. Tot op heden is er geen klinisch geval van overmatige opwarming van een stent bekend. Patiënten met niet-ferromagnetische stents kunnen direct na implantatie MRI ondergaan. Bij patiënten met een perifere of aorta stent van zwak ferromagnetisch materiaal moet bij MRI binnen 6-8 weken na plaatsing een risico afweging worden gemaakt. Vele coronaire stents zijn door de fabrikant als MR voorwaardelijk geclassificeerd voor 1,5 T en 3 T; daarom kan MRI plaatsvinden zonder voorwaarden te controleren voor het specifieke stenttype. Algemene aanbevelingen: - Patiënten met coronaire stents kunnen bij 1,5 T en 3 T MR ondergaan onafhankelijk van de spatiele gradiënt van het hoofdmagneetveld en direct na stentplaatsing. - ≤ 3 T - Maximale ‘whole body’ SAR 2 W/kg voor 15 min per pulssequentie (meerdere sequentie per MR studie). De aanbeveling van ‘whole body’ SAR beperkt dagelijkse bedrijfsvoering en behoeft toelichting. Bij cardiale MRI wordt de 2 W/kg vaak overschreden, echter tot op heden zijn er geen complicaties gerapporteerd. Deels doordat er niet continu wordt gescand, deels door afkoeling door de bloedstroom. Hiermee is bovenstaande aanbeveling niet gelijk aan de gangbare klinische praktijk. De auteurs vinden MRI met SAR tot 4 W/kg redelijk, maar vinden dat je de patiënt hierover zou moeten inlichten, en zo mogelijk toch onder de 2 W/kg proberen te blijven. |
|
Expert Consensus (U.S.A. en Canada) |
Jahebdar Maralani, 2020 |
Coronair en carotide stents: Voornaamste risico is verplaatsing. Geen studies hebben complicaties met opwarming gevonden. De belangrijkste aanbevelingen zijn: - De datum van stentimplantatie en de fabrikant moeten worden vastgesteld. - Patiënten met een onbekend model coronair- of carotide-stent kunnen gescand worden als de ‘whole body’ SAR ≤2 W/kg blijft voor elke sequentie van maximaal 15 minuten. - MRI kan worden uitgevoerd in patiënten met zwak-ferromagnetische stents op 1,5 T en 3 T zes weken na implantatie, uitzondering op dit uitstel moet op individuele basis worden gemaakt. |
|
Expert Statement (U.S.A.) |
Shellock, 2019 |
Voor coronaire stents (onafhankelijk van aantal, type, wel of niet overlappend) kan MRI bij 1,5 T en 3 T met maximale ‘whole body’ SAR van 2 W/kg voor 15 minuten per pulssequentie met meerdere pulssequenties per patiëntstudie. |
Incidentdatabases
Voor deze module zijn de volgende incidentdatabases van implantaten doorzocht:
-
- De FDA recalls database;
- Het archief van Inspectie Gezondheidszorg (IGZ);
- De database van de Inspectie Gezondheidszorg en Jeugd (IGJ) met veiligheidsmeldingen vanaf 15 december 2015;
- De FDA Medsun database, periode febr-2002 tot en met dec-2022;
- De FDA MAUDE database, periode 2011 tot en met 2021;
N.B. databases werden doorzocht zonder een beperking op de periode van eventuele meldingen tenzij anders vermeld. Voor de precieze zoekverantwoording wordt verwezen naar de tabel ‘Zoekverantwoording Databases van Recalls en Events’.
- De FDA recall database bevatte geen relevante meldingen voor deze module.
- Het archief van de IGZ bevatte geen relevante meldingen voor deze module.
- De database van de IGJ bevatte geen relevante meldingen voor deze module.
- De Medsun database van de FDA bevatte geen relevante meldingen voor deze module.
- De FDA MAUDE database bevat in de onderzochte periode een aantal meldingen rondom vasculaire stents en opwarming, aantrekkingskracht of losraken. Deze worden hieronder besproken.
Resultaten uit de FDA MAUDE database:
Opwarming. De MAUDE-database bevat een zevental meldingen van pijnklachten mogelijk te wijten aan opwarming bij patiënten met één of meerdere stents. De anatomische locaties van de stents varieerden. Meldingen betroffen coronairstents, maar ook stents in de superior vena cava, of een onbekend vat, en van een stent bedoeld voor plaatsing in de arterie iliaca. Interpretatie van deze meldingen is veelal complex of zelfs speculatief, waarbij belangrijke informatie ontbrak over de uitgevoerde scan zoals de veldsterkte, het toegepaste SAR niveau, het type implantaat, de gescande anatomie en bij meerdere stents of deze aaneengesloten geplaatst waren.
Voor geen van deze gevallen kon worden opgemaakt dat er een causaal verband bestond tussen de gemelde opwarming, het hebben van een vasculaire stent, en het ondergaan van een MRI-onderzoek. De bewijskracht van deze meldingen is hierdoor en ook door het lage aantal meldingen zeer laag.
Stent dislocatie. Er is een drietal meldingen over het losraken van stents. Het gaat telkens om meldingen waarin men het verplaatsen van een stent beschrijft, maar waaruit niet blijkt dat er een causaliteit bestaat met het ondergaan van een MRI-onderzoek. In één geval spreekt men erover dat het “geloofd” werd dat de stent losraakte als gevolg van de MRI, maar blijkt uit de melding niet waarom dit zo zou kunnen zijn en het valt ook niet te verwachten op grond van het stent type (Endeavor sprint over-the-wire (otw) drug-eluting stent) dat deze tijdens een MRI-onderzoek zou kunnen losraken. In een tweede melding rapporteerde de patiënt tijdens het MRI-onderzoek een scherpe pijn op de borst, en waarbij de laborant patiënt gewaarschuwd zou hebben dat mogelijk een losgeraakte stent hier debet aan was. De melding ontbeert informatie over de verdere follow-up van patiënt: het is dus niet duidelijk of de stent daadwerkelijk was losgeraakt. Een laatste melding bevat een casus ook beschreven in de literatuur (Parthasarathy H, 2013), waarbij een Cypher stent, 3,5x8 mm drug eluting stent, geïmplanteerd in de left main coronary artery, op aorta-ostiale locatie in de hoofdstam van de linker coronairarterie, vervolgens moet zijn los geraakt en (na het uitvoeren van een 1,5 T MRI-onderzoek van het hoofd) nadien werd aangetroffen middels CT in de proximale tak van de linker iliacale arterie. Uit ex vivo testen van dit type stent is eerder gebleken dat deze geen ferromagnetische eigenschappen heeft. De melding in de MAUDE-database stelt dat het niet mogelijk is conclusies te trekken over de oorzaak van het losraken van de stent. In de wetenschappelijke publicatie concludeert men wel dat voorzichtigheid geboden is in geval van: relatief korte stents, op aorta-ostiale locaties, bij een beperkte tijd tussen implantatie en MRI. In de publicatie beschouwt men geen andere mogelijke oorzaken dan het ondergaan van een MRI-onderzoek, zoals bijvoorbeeld onvoldoende stentdiameter.
Voor geen van deze gevallen kon worden opgemaakt dat er een causaal verband bestond tussen het losraken van de stent en het ondergaan van een MRI-onderzoek. In één geval is zelfs onduidelijk of er daadwerkelijk een stent was losgeraakt. De bewijskracht van deze meldingen is mede door het lage aantal meldingen zeer laag.
Aantrekking. Er is één melding over een patiënt met meerdere stents (merendeels van onbekend merk en type) in het hart, een nier, en de arterie iliaca, die tijdens het ondergaan van een 1,5 T MRI-onderzoek van het hoofd ervoer dat er werd getrokken aan haar nieren en haar rug. De MRI werd hierop afgebroken. De melding beschrijft niet of patiënt blijvende schade heeft ondervonden van het voorval.
Het is aannemelijk, ook gezien ex vivo testen van een aantal stents met meetbare aantrekkingskracht, dat het gevoel van aantrekking aan de nieren direct gevolg is van het ondergaan van MRI-onderzoek bij deze patiënt bij wie één (of meerdere) ferromagnetische stents waren geïmplanteerd. Deze casus vormt daarmee een voorbeeld van een bekend risico van het brengen van een ferromagnetisch voorwerp in een MRI-scanner.
Enquête zorginstellingen
Door de richtlijnwerkgroep is een enquête uitgezet betreffende de screening voorafgaand aan een MRI-onderzoek bij ≤3 T, specifiek voor de screening op vasculaire stents. Deze is verstuurd naar alle MRI-leden van de NVMBR in november 2022, en daarna zijn nog gerichte herinneringen gestuurd aan leden van de NVMBR en/of NVKF bij instellingen die niet gereageerd hadden. Het antwoordpercentage was 83% (54/65) voor de algemene ziekenhuizen, en 100% (6/6) voor de UMC’s. Daarnaast hebben nog twee overige NVZ-instellingen gereageerd. In één instelling is er over twee locaties verschillend beantwoord. Deze zijn apart beschouwd. In het totaal betreft dit globaal 690.000 MRI patiëntstudies per jaar en 183 MRI-systemen (66% 1,5 T en 34% 3 T). Het totaal aan MRI studies opgegeven in de enquête beslaat daarmee zo’n 69% van de 1 miljoen MRI-onderzoeken in Nederland volgens de RIVM-inventarisatie over 2020 (RIVM 2021).
In 66% van de instellingen is er een specifieke screeningsvraag over (vasculaire) stents, en in de overige 34% van de instellingen wordt er niet specifiek gevraagd naar vasculaire stents (deze verdeling is globaal gelijk bij UMC’s en algemene ziekenhuizen). Als gekeken wordt naar het percentage van het aantal MRI-onderzoeken zonder specifieke screening op vasculaire stents ligt dat in dezelfde orde van grootte (42%). 37% van de instellingen stelt geen voorwaarden voor een MRI-onderzoek bij een patiënt met een vasculaire stent. In de instellingen zonder specifieke screening op vasculaire stents bestaat dit beleid gemiddeld 7 jaar. Indien een patiënt of aanvrager aangeeft dat er sprake is van de vasculaire stent wordt in 34% van de instellingen het individuele stent type uitgezocht. Tabel 6 geeft het overzicht van de MRI voorwaarden die genoemd worden voor een MRI-onderzoek bij 1,5 T en 3 T MRI bij een patiënt met een vasculaire stent.
Tabel 6. Overzicht van MR voorwaarden die in de enquête genoemd worden voor een MRI-onderzoek bij 1,5 of 3 T bij een patiënt met een vasculaire stent.
* hiervan wordt eenmaal 2 weken, en eenmaal 8 weken genoemd
Tenslotte werd in de enquête gevraagd “Zijn er, voor zover u weet, vasculaire stent gerelateerde complicaties opgetreden die hebben geleid tot patiëntschade als gevolg van MRI (uitgezonderd MRI beeldartefacten)”. De twee positieve antwoorden waren: “mogelijk migratie van een nieuwe stent, discutabel of MRI de reden was, 1 keer gebeurd voor zover bekend”, en “bij aortastent (EVAR) is het niet mogelijk een MRI te maken in dat gebied (prostaat, LWK, buik, hart)”.
Implantatendatabase
Met behulp van de databases van MagResource (MR:comp GmbH, Gelsenkirchen, Duitsland) is een overzicht van MR voorwaarden van vasculaire stents gemaakt. Hiertoe is op 23-8-2022 met de zoekterm “stent” of “endoprothesis” een uitdraai gemaakt. Hiermee werden 1790 resultaten gevonden in deze database, waarvan er 582 zijn uitgesloten omdat het geen vasculaire stents betreffen volgens het beoogd gebruik. Daarna zijn verschillende typenummers bij gelijke typenaam, gelijke fabrikant, en gelijk MR voorwaarden samengevoegd. Hiermee ontstond een lijst van 349 type vasculaire stents, waarvan tabel 7 een overzicht geeft van de MR veiligheidsclassificatie.
Tabel 7. Overzicht MR veiligheidsclassificatie vasculaire stent typen ingedeeld op vat van beoogd gebruik.
|
Locatie beoogd gebruik |
Aantal |
MR onveilig |
MR voorwaardelijk |
MR veilig |
MR veilig of voorwaardelijk oude ASTM definitie* |
Onbekend** |
|
coronairvaten |
166 (48%) |
|
131 |
|
33 |
2 |
|
aorta en iliaca |
79 (23%) |
|
72 |
|
7 |
|
|
veneuze vaten |
9 (3%) |
|
8 |
|
1 |
|
|
carotide |
19 (5%) |
|
18 |
|
1 |
|
|
perifere vaten |
61 (17%) |
|
48 |
|
9 |
4 |
|
intracraniële vaten |
10 (3%) |
|
8 |
|
2 |
|
|
onbekend |
5 (1%) |
|
1 |
|
3 |
1 |
|
totaal |
349 |
0 |
286 (82%) |
0 |
56 (16%) |
7 (2%) |
* jaartal van invoer stent handleiding in Magresource database ≤ 2015.
** jaartal van invoer stent handleiding in Magresource database ≤ 2011.
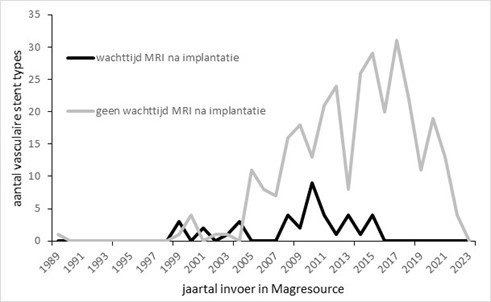
Er worden verschillende voorwaarden gesteld voor MRI-onderzoek. Tabel 8 en 9 geven een overzicht hiervan. Bij stents met een meer recente invoer van de gebruikershandleiding in de Magresource database (vanaf 2016) wordt geen wachttijd na implantatie meer als voorwaarde gesteld, zie figuur 1. De meeste stents waarvoor een wachttijd als voorwaarde is gesteld waren van roestvast staal (82%). Van de stents met de meest recente invoer (vanaf 2016) was slechts 10% van roestvast staal, zie tabel 10. Tenslotte vermelden fabrikanten in de meeste gevallen in de handleiding ex vivo gemeten temperatuurstijging, vooral op basis van het ASTM protocol, zie figuur 2. Dit ASTM protocol wordt verderop in de overwegingen besproken, waar tevens wordt toegelicht welke beperkingen zich voordoen bij de interpretatie van deze gegevens.
Tabel 8. Overzicht MR voorwaarden door stentfabrikant, aantal stenttypen (percentage van totale aantal types).
|
|
1,5 T |
3 T |
1,5 T en 3 T |
|
onbekend |
|
statisch magneetveld (B0) |
19 (5%)# |
5 (1%) |
281 (81%) |
|
44 (13%)* |
|
|
beperkt |
geen beperking |
range |
gemiddeld |
onbekend |
|
spatiële gradiënt statisch magneetveld |
260 (74%) |
89 (26%) |
0,7-225 T/m |
21 T/m |
4 (1%)** |
|
spatiële gradiënt∙B0 |
15 (4%) |
314 (96%) |
22-201 T2/m |
68 T2/m |
4 (1%)** |
|
|
15-20 min |
15 min per sequentie |
30-60 min |
geen beperking |
onbekend |
|
tijdsbeperking RF |
233 (67%) |
7 (2%)## |
5 (1%) |
41 (12%) |
63 (18%)*** |
|
|
beperkt |
geen beperking |
range |
gemiddeld |
onbekend |
|
schakelende gradiënt velden |
11 (3%) |
338 (97%) |
10-60 T/m |
48 T/m |
4 (1%)** |
|
|
geen |
4 weken |
6 weken |
8 weken### |
onbekend |
|
wachttijd geen MRI na implantatie |
160 (46%) |
4 (1%) |
1 (0,3%) |
30 (9%) |
150 (43%) |
* allen met oude ASTM definitie of onbekende MR veiligheidsclassificatie.
** allen met onbekende MR veiligheidsclassificatie.
*** allen (behalve één) stent type met oude ASTM definitie of onbekende MR veiligheidsclassificatie
# jaartal van invoer stent handleiding in Magresource database in range 2009-2020.
## één stent type met 11 minuten wachttijd na elke sequentie.
### 8 weken of na endotheel vorming (n=4).
Figuur 1. Aantal vasculaire stenttypen met en zonder de voorwaarde van wachttijd van geen MRI na stentimplantatie, als functie van het jaar waarin de handleiding van de stent in de Magresource database is ingevoerd. N.B. hierbij was in 46% van de stenttypen expliciet benoemd dat er geen wachttijd is en in 42% van de gevallen werd dit niet expliciet benoemd. Deze typen stents zijn meegeteld als zijnde zonder wachttijd.
Tabel 9. Overzicht aantallen vasculaire stent typen met ‘whole body’ SAR limiet voorwaarden& bij 1,5 T en 3 T voor één stent ingedeeld op vat van beoogd gebruik (bij overlappende stent regelmatig lagere SAR waarden opgegeven).
|
Locatie beoogd gebruik |
0,4-1,5 W/kg |
2 W/kg |
2,5-3,9 W/kg |
4 W/kg |
Niet gespecificeerd* |
|
coronairvaten** |
8 (5%) |
104 (63%) |
8 (5%) |
2 (1%) |
44(27%) |
|
aorta en iliaca |
8 (10%)# |
31 (39%) |
11 (14%) |
23 (29%) |
6 (8%) |
|
veneuze vaten |
3 (33%)## |
3 (33%) |
3 (33%) |
|
|
|
carotiden |
3 (16%) |
9 (47%) |
5 (26%) |
|
2 (11%) |
|
perifere vaten*** |
27 (44%)### |
15 (25%) |
3 (5%) |
3 (5%) |
13 (21%) |
|
intracraniële vaten |
|
5 (50%) |
1 (10%) |
|
4 (40%) |
|
onbekend |
|
|
1 (20%) |
|
4 (80%) |
|
totaal |
49 (14%) |
167 (48%) |
32 (9%) |
28 (8%) |
73 (21%) |
| & | geldend voor de ‘whole body’ RF zendspoel, echter dit is meestal niet gespecificeerd, enkele stent types sluiten expliciet gebruik van lokale RF zendspoelen uit als de stent in het spoelbereik ligt. |
| * | één stent type gespecificeerd met lokale body SAR (i.p.v. ‘whole body’ SAR) van 4,4 W/kg. |
| ** | 6 stent types met verschillende limieten bij 1,5 T en 3 T. |
| *** | één stent type met verschillende limiet voor stent in arm of stent in torso. |
| # | 5 iliaca stent types 1 W/kg bij scan locatie iso-centrum onder de navel, en 2 W/kg boven de navel. |
| ## | één veneuze stent type 1 W/kg bij scan locatie iso-centrum boven de navel, en 2 W/kg onder de navel; en één veneuze stent type 1 W/kg bij scan locatie iso-centrum onder de navel, en 2 W/kg boven de navel. |
| ### | 24 stent types 1 W/kg bij scan locatie iso-centrum onder de navel, en 2 W/kg boven de navel, waarvan 6 stent types met 0,5 W/kg onder de mid bovenbenen. |
Tabel 10. Overzicht van materiaal van alle stents met wachttijd en van alle stents vanaf 2016 (bij geen van deze werd een wachttijd aanbevolen).
|
Materiaal |
Aantal stent types met wachttijd |
Aantal Stent types zonder wachttijd# |
|
roestvast staal |
23 (82%) |
9 (10%) |
|
nitinol |
1 (4%) |
51 (58%) |
|
kobalt-chroom |
3 (11%) |
20 (23%) |
|
anders |
1 (4%) |
5 (6%) |
|
onbekend |
0 |
3 (3%) |
|
totaal |
28 |
28 (100%) |
# Alle stent types waarvan de handleiding vanaf 2016 is verschenen.
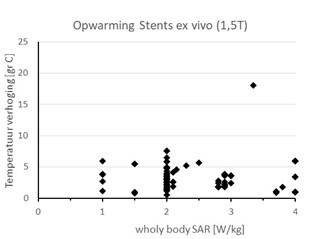
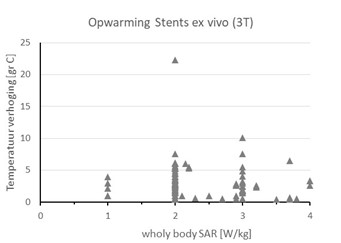
Figuur 2. Maximale temperatuursverhoging bij ‘whole body’ SAR instelling zoals vermeld staat in de handleiding van de stent, of in de MRI-informatie van de stentfabrikant. In de meeste gevallen is dit ex vivo gemeten in een gelfantoom volgens de ASTM standaard. In enkele gevallen, bij recent op de markt gebrachte stents, is dit bepaald d.m.v. simulaties. In de meeste gevallen betreft het de maximale temperatuursverhoging, soms temperatuursverhoging t.o.v. een gemeten referentietemperatuur in het fantoom. De temperatuursverhoging van 18 en 22 °C is gemeten bij de perifere vaatstent type Maris Plus Stent van Medtronic Inc.; gegevens uit 2015.
Hoofdklassen risico’s
In het algemeen kunnen risico’s van metallische implantaten in de MRI in de volgende hoofdklassen ingedeeld worden:
1. Risico op verplaatsing en rotatie van het implantaat door de aanwezigheid van het statische magneetveld en de spatiële gradiënt van dit veld.
2. Risico op opwarming van het implantaat door interactie met het RF-veld.
3. Risico op trilling of inductie van stromen door de oscillerende magnetische veldgradiënten die worden toegepast voor de ruimtelijke codering van het MRI-signaal.
4. Artefact in het MRI-beeld.
5. Risico van krachten door het Lenz-effect bij snelle beweging van geleidende implantaten in het statisch magnetisch veld van de MRI-scanner.
6. Risico op verstoring van de werking van het implantaat.
- Risico’s als gevolg van verplaatsing en rotatie
Ferromagnetische objecten kunnen een aantrekkingskracht ondervinden die onder andere een functie is van de magnetische susceptibiliteit, de sterkte van het statische magneetveld, en de spatiele gradiënt van het statische magneetveld (McRobbie 2020). Deze kracht wordt daarom typisch gemeten nabij de ingang van de tunnel, daar waar het effect het grootst is. Daarnaast werkt op ferromagnetische voorwerpen een rotatiekracht, die ertoe leidt dat objecten zich richten parallel aan de oriëntatie van het statische magneetveld. Dit effect is het sterkst voor lange, smalle objecten of vlakke/dunne objecten. Deze kracht is proportioneel met het kwadraat van de sterkte van het statische magneetveld, en het sterkst in het iso-centrum van de MRI-scanner (Sommer 2004).
De meest voorkomende materialen gebruikt voor het vervaardigen van vasculaire stents zijn roestvast staal (RVS) (voorbeeld: RVS316L), nitinol (nikkel-titanium legering), kobalt-chroom legeringen, en soms ook platina, koolstof, goud, MP35N (een nikkel-kobalt legering), of tantalium (Jabehdar Maralani 2020, Lopic 2013). De meeste van deze materialen zijn non-ferromagnetisch, of wat in de literatuur wordt aangehaald als zwak-ferromagnetisch. Er worden geen stents meer geplaatst die zijn gekwalificeerd als MR onveilig.
Afhankelijk van de sterkte van een eventuele aantrekkings- of rotatiekracht bestaat, in theorie, het risico op het losraken van een zwak-ferromagnetische stent als gevolg van het ondergaan van een MRI-onderzoek. In het verleden heeft deze overweging veel fabrikanten ertoe aangezet om in hun MR voorwaarden op te nemen dat het scannen van patiënten vermeden dient te worden in een periode van 6 tot 8 weken na implantatie (Rutlegde 2001). De hypothese hierbij was dat, doordat gedurende deze wachtperiode de stent vergroeit met de vaatwand (endotheel vorming), na die periode de stent veel beter verankerd zou zitten in het vat. Inmiddels is duidelijk dat de krachten die wordt uitgeoefend op veruit de meeste zwak-ferromagnetische, vasculaire stents als gevolg van het ondergaan van een 1,5 T MRI-onderzoek vele malen kleiner zijn dan de krachten die zonder meer worden uitgeoefend op geïmplanteerde stents, bijvoorbeeld als gevolg van de pulsatiliteit van de bloedflow en/of de contractiliteit van het hart in geval van coronair stents (Rutledge 2001, Levine 2007, Giroletti 2005, Hansmann 2001). De verankering in de vaatwand die ontstaat door het plaatsen van stents middels ballon angioplastiek biedt daarmee onmiddellijke bescherming tegen evt. aantrekkings- en rotatiekrachten uitgeoefend tijdens een 1,5 T MRI-onderzoek. De rationale voor een wachttijd in geval van niet-ferromagnetische stents is onbekend (Shellock 2005) en in algemene zin wordt geen wachttijd meer geadviseerd voor niet-ferromagnetische implantaten (Levine 2007).
Dat een wachttijd inderdaad niet meer nodig is, wordt onderschreven door studies waarin men keek naar de veiligheid van het ondergaan van een MRI-onderzoek kort na stent implantatie (Jabehdar Maralani 2020, Rutlegde 2001, Shellock 2005, Gerber 2003, Jehl 2009, Curtis 2013, Duerinckx 1998, Kaya 2009, Kramer 2000, Syed 2006, Porto 2005). In dergelijke studies wordt geen melding gemaakt van het losraken van stents. In MAUDE database werden in de doorzochte periode (zie de Samenvatting informatie uit incidentdatabases van implantaten) drie voor dit risico relevante meldingen aangetroffen, waarvan één casus ook in de literatuur is gepubliceerd (Parthasarathy 2013). Alleen van de gepubliceerde casus blijkt onomstotelijk dat de stent is losgeraakt. De werkgroep acht het echter onwaarschijnlijk dat dit is gebeurd als gevolg van het ondergaan van een MRI-onderzoek. Het toegepaste type stent (Cypher, 3,5x8 mm drug-eluting stent, Cordis Corp, Markham, Ontario) wordt vervaardigd uit RVS 316L (Wolf 2008) en zou daarom geen noemenswaardige, ferromagnetische eigenschappen mogen hebben. Migratie van de stent als gevolg van een aantrekkings- of rotatiekracht wordt daarmee onwaarschijnlijk. Het Deutsche Gesellschaft für Kardiologie – Herz- und Kreislaufforschung e.V. noemt in een publicatie (Müllerleile 2015) de case studie dan ook controversieel, te meer daar de auteurs van de case studie geen andere oorzaken voor het losraken van de stent overwogen, zoals onvoldoende stent diameter. In de voor deze richtlijn uitgezette enquête wordt ook melding gemaakt van één casus van stent dislocatie, maar ook aldaar is niet vastgesteld dat het MRI-onderzoek de oorzaak was.
Dislocaties van stents komen normaliter vrijwel niet voor. Een dislocatie als gevolg van een te kleine stent diameter is denkbaar, dit betreft een technische fout tijdens het plaatsen en ingeschat wordt dat dit maar zelden voorkomt. Dit betreft dan vooral stents die proximaal in een zij-vat van de aorta worden geplaatst en toch weer in de aorta terecht komen. Wat vaker voorkomt, maar wat in feite geen dislocatie is, is een stent die een of enkele millimeters verwijderd van de beoogde plek geplaatst wordt. Dit wordt veelal verholpen door een tweede stent te plaatsen. Progressieve ziekte van een aneurysma van de abdominale aorta kan ertoe leiden dat de vaatwand deels losraakt van een stent, waardoor deze ook in enige mate zou kunnen verschuiven.
Verder is gehypothetiseerd dat het losraken van bare metal stents de blootstelling van bloedplaatjes zou doen toenemen, met als mogelijke gevolg trombose, wat weer kan leiden tot sterfte en infarcten (Gerber 2003). In deze en andere studies (Levine 2007, Jehl 2009, Patel 2006) wordt echter geen bewijs gevonden voor deze hypothese, zodat auteurs concluderen dat recente stent implantatie geen contra-indicatie zou moeten zijn voor het ondergaan van een 1,5 T MRI-onderzoek. In verschillende internationale richtlijnen is daarom inmiddels opgenomen dat de rationale voor zo’n wachtperiode bij niet- of zwak-ferromagnetische stents ontbreekt (Levine 2007, Müllerleile 20, Hundley 2010, van Knobelsdorff 2021). Sinds 2016 worden er nog altijd RVS stents op de markt gebracht (tabel 10), die mogelijk zwak-ferromagnetisch zijn, maar sinds die periode is er geen sprake meer van een wachttijd in de MR voorwaarden van de fabrikant (figuur 1).
Toen omstreeks 2000 drug-eluting stents (DES) op de markt kwamen (Jabehdar Maralani 2020), bestond er voor dit type stent een zorg dat dit zou kunnen leiden tot vertraagde endotheelvorming (Patel 2006), zodat het ook voor dit type stent relevant zou kunnen zijn om een wachtperiode aan te houden waarin MRI-onderzoek werd afgeraden. In verscheidene studies heeft men daarop gekeken naar de risico’s bij het ondergaan van 1,5 T MRI kort na de implantatie van DES, waarin geen bewijs werd gevonden voor een toegenomen kans op nadelige effecten voor de patiënt (Porto 2005, Shellock 2005). Relevante aanbevelingen en overzichtsartikelen adviseren daarom ook voor DES geen wachtperiode meer (Jabehdar Maralani 2020, Hundley 2010, Schenk 2021). Dit is ook terug te zien in de MR voorwaarden van stentfabrikanten, waarbij bij meer recente stent type geen voorwaarde meer van wachttijd na implantatie wordt genoemd, zie figuur 1. Anderzijds is de wachttijd discussie wel relevant, omdat momenteel verschillende instituten wel rekening houden met deze wachttijd (zie tabel 6).
Hoewel voor het ondergaan van een 1,5 T MRI-onderzoek inmiddels geconcludeerd kan worden dat er een brede consensus bestaat dat dislocatie van zwak-ferromagnetische stents kort na implantatie geen reëel risico is, blijkt de onderbouwing hiervoor voor 3 T MRI-onderzoeken minder sterk. Zo wordt in een Duitse richtlijn (Müllerleile 2020) geadviseerd om bij perifere stents tot 6 weken na implantatie alleen een 3 T MRI-onderzoek uit te voeren na een individuele risico-afweging. Schenk et al. (2021) concluderen dat het ondergaan van een MRI-onderzoek binnen 8 weken na implantatie van coronair stents geen aanleiding lijkt te geven tot een toename van adverse events bij zowel 1,5 T als 3 T, maar dat aanvullend onderzoek naar 3 T gewenst is (in overeenstemming met de conclusies op basis van de systematische literatuursearch voor wat betreft 1,5 T MRI versus 3 T MRI).
Te verwachten torsiekrachten op een zwak-ferromagnetische stent schalen kwadratisch met de veldsterkte en aantrekkingskrachten schalen met het product van veldsterkte en de spatiële gradiënt in het statische magneetveld. Op grond daarvan mag verwacht worden dat torsiekrachten uitgeoefend op ferromagnetische stents maximaal een factor vier hoger zijn bij 3 T dan bij 1,5 T, en dat de aantrekkingskracht op ferromagnetische stents (gegeven typische spatiële gradiënten in het statische magneetveld van klinische scanners) een factor drie hoger zal zijn bij 3 T dan bij 1,5 T. Hoewel de krachten op zwak-ferromagnetische stents toenemen van 1,5 T naar 3 T, schat de werkgroep in dat het aannemelijk is dat deze krachten desondanks onvoldoende groot zullen zijn om te leiden tot dislocatie van stents bij het ondergaan van een onderzoek op 3 T. De werkgroep schat in dat het risico op schade als gevolg van verplaatsing of rotatie voor stents door het sterke magnetische veld van een 1,5 T of 3 T MRI-scanner zeer klein zijn, ongeacht de tijd tussen plaatsing van het implantaat en het MRI-onderzoek.
- Risico op opwarming van het implantaat door interactie met het RF-veld
Algemeen effect
Een RF-veld bestaat uit een elektrisch (E-veld) en een magnetisch veld. De blootstelling van een elektrisch geleidend implantaat aan het E-veld geeft aanleiding tot een geïnduceerde stroom in het implantaat. Bij een supergeleidende, horizontale gesloten bore scanner, waarbij de ‘body’ zendspoel wordt gebruikt is de geïnduceerde stroom maximaal als een implantaat is georiënteerd in de lengterichting van de patiënt (Fujimoto 2018). Deze stroom geeft nauwelijks aanleiding tot opwarming van het implantaat zelf, maar dit is anders in het omliggende weefsel waar de elektrische weerstand typisch hoger is dan in het implantaat, zodat daar relatief gezien meer energie gedissipeerd zal worden. De opwarming wordt verder gemoduleerd door de elektromagnetische eigenschappen van het weefsel rondom het implantaat, een eventueel aanwezige, elektrisch isolerende laag rondom een implantaat, en ook door de positie van het implantaat in de ‘body’ zendspoel van de MRI-scanner (Fujimoto 201, Bassen 2006).
Het opwarmende effect kan versterkt worden wanneer het implantaat zich gaat gedragen als een antenne, waarbij er een opbouw ontstaat van elektrische energie langs het implantaat door staande golven. Dit effect leidt in het bijzonder aan de uiteindes van langgerekte implantaten tot een hogere sterkte van het E-veld, resulterend in pieken in de lokale SAR. Uit antennetheorie blijkt dat dit effect het sterkst is wanneer de lengte van het implantaat ongeveer gelijk is aan een halve golflengte. Een halve golflengte correspondeert in de mens, gegeven een relatieve permitiviteit van het weefsel ε = 80, met ± 13 cm (3 T) en ± 26 cm (1,5 T) (Panych 2018). Hierbij wordt opgemerkt dat deels overlappende stents, of stents die bijna overlappen, zich kunnen gaan gedragen als ware het één stent. In zo’n situatie kan dus niet simpelweg aan de hand van individuele stentlengtes vastgesteld worden of sprake is van een lengte nabij de resonante lengte (Ji 2019, Reiss 2021).
Het is bekend dat temperatuursverhogingen kunnen leiden tot weefselschade. De mate waarin weefselschade optreedt wordt bepaald door de combinatie van temperatuursverhoging, blootstellingsduur en weefselgevoeligheid. Een maat voor deze thermische dosis is CEM43°, het equivalente aantal minuten op 43°C, en te berekenen als , waarbij R=¼ onder de 43°C en erboven ½. In het algemeen is een CEM43 van 10-20 min nodig voor thermische schade (van Rhoon 2013, Sapareto 1984). De acquisitieduur van MRI sequenties met hoge SAR in een klinisch MRI-onderzoek variëren veelal tussen de 5 en 30 minuten. Dus bij stijging naar 43 graden is er schade te verwachten na 10-20 minuten, en bij hogere temperaturen sneller.
Ex vivo metingen
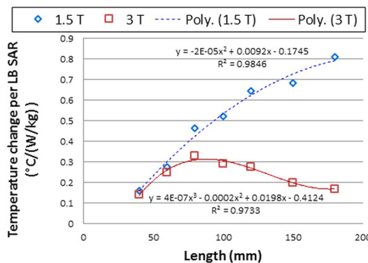
De standaardmethode om vast te stellen of gedurende een MRI-onderzoek de omgeving rondom een implantaat opwarmt staat beschreven in ASTM standaard F2182 (ASTM 2019) . Resultaten van de hierin beschreven test met behulp van een gelfantoom vormen de basis voor veel van de MR voorwaarden gesteld door de stentfabrikanten. In een recent overzicht van dit soort ex vivo testen in het ASTM fantoom van grote aantallen stents door de fabrikanten laat zien dat bij 3 T de opwarming toeneemt tot zo’n 9 cm en daarna weer afneemt (figuur 3). Bij 1,5 T loopt de opwarming nog op tot een stentlengte van 18 á 20 cm (Song 2018), een observatie in overeenstemming met antennetheorie.
Figuur 3. RF geïnduceerde opwarming ex vivo in een gelfantoom van een testlaboratorium als functie van de stentlengte, gemeten volgens de ASTM F2182-11a standaard. Merk op dat langs de verticale as de local background (LB) SAR genoemd staat, en niet de ‘whole body’ (WB) SAR. De figuur is overgenomen uit Song et al. Magn Reson Med 2018.
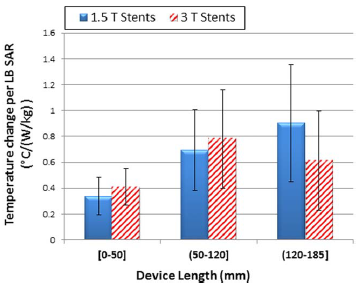
Eenzelfde trend is zichtbaar in figuur 4. In deze figuur zijn de verschillen tussen 1,5 T en 3 T niet statistisch significant. De oorzaak hiervan zijn meetfouten en verschillen in de wijze waarop de ASTM testen bij individuele stents werden uitgevoerd. De testen verschillen met name in de verhouding van local background SAR ter plekke van het implantaat en de ‘whole body’ SAR (LB/WB SAR), variërend van 2 tot 11, als gevolg van het gebruik van verschillende RF spoelen (horend bij de MR systemen) bij de verschillende tests. In de figuren is dit gecorrigeerd door te schalen op lokale background (LB) SAR. Hieruit valt ten eerste te concluderen dat een sterkere opwarming bij 3 T t.o.v. 1,5 T niet waarneembaar is; eerder lijkt het andersom. Verder valt op dat globaal genomen de opwarming van korte stents (5 cm of korter) minder is dan voor langere stents.
Figuur 4. RF geïnduceerde opwarming ex vivo in een gelfantoom bij 59 stents, zoals vermeld in de RF testrapportage voor FDA clearance na 2008 en gemeten volgens de ASTM F2182-11a standaard. Merk op dat langs de verticale as de lokal background (LB) SAR genoemd staat, en niet de ‘whole body’ SAR. De figuur is overgenomen uit Song et al. Magn Reson Med 2018.
Op basis van deze gegevens over RF-geïnduceerde opwarming kan een schatting gemaakt worden in welke mate weefsel opwarmt bij patiënten met stents die een MRI ondergaan. Als we uitgaan van een typische opwarming op basis van figuur 4 van 0,7°C/W/kg voor 1,5 T en stentlengte 50-120 mm (maximaal 1,5 °C/W/kg), dan resulteert dat bij een lokale (LB) SAR van 4 W/kg in een opwarming tot 2,8 °C, uitgaande van een lineaire relatie. In werkelijkheid zal de effectiviteit van koeling toenemen bij hogere mate van opwarming. Echter, de SAR wordt in klinische MRI gereguleerd d.m.v. de ‘whole body’ SAR, welke maximaal 4 W/kg is. Dus voor een schatting is de lokale SAR tot ‘whole body’ (LB/WB) SAR ratio van belang. Deze ratio hangt af van de in vivo locatie en neemt toe met patiëntpostuur. De maximale LB/WB SAR varieert in simulaties, verricht met verschillende posturen, tussen de 5 en 20 (Murbach 2013). Echter de piek lokale SAR waarden komen voor in de armen bij thoracale/abdominale beeldvorming (Murbach 2013), een locatie waar geen stents worden geplaatst en dus geven deze data van Murbach een overschatting. In het algemeen geldt dat piek lokale SAR waardes zich buiten de stentlocatie bevinden (Yao 2021). Realistische LB/WB SAR waarden op locaties waar vasculaire stents geplaatst zijn, is echter een kennislacune. Wel lijkt de LB/WB SAR waarde relatief laag in het hoofd en hoog in benen (Murbach 2013). Nemen we een lage LB/WB SAR waarde aan van 5, dan resulteert dit in bovenstaand scenario op basis van lineaire extrapolatie in een lokale opwarming van 14 °C. Bij een stent op een locatie hogere LB/WB SAR zou dit hoger zijn. Uitgaande van een LB/WB SAR waarde van 5 kan eveneens de in figuur 2 gerapporteerde WB SAR waarde omgerekend worden naar een LB SAR waarde. De dan volgende temperatuurverandering per W/kg (LB SAR) zijn van dezelfde orde-grootte als in figuur 4.
In het bijzonder geldt dat er ook bij lokale RF zendspoelen (behalve een hoofd RF zendspoel) sprake kan zijn van hogere lokale SAR waarden. Zo kunnen deze LB SAR bij extremiteiten oplopen tot 40 W/kg (NEN-IEC 2020), bijvoorbeeld bij een kniespoel. Omdat het gebruik van lokale RF zendspoelen in Nederland beperkt is vallen deze buiten de scope voor deze richtlijn.
Ter afronding van de overwegingen rondom de ASTM standaard worden de volgende, belangrijke beperkingen benoemd.
Beperkingen ex vivo metingen
Bovenstaande bepalingen m.b.v. ex vivo metingen moeten in de juiste context geplaatst worden. Zo blijkt een precieze positionering van de temperatuursensoren cruciaal om een eventuele piekopwarming goed te registreren en wordt gerapporteerd dat de eigenschappen van de toegepaste gel in de praktijk blijkt te variëren tussen verschillende testinstellingen (Bassen 2006). Het onderling vergelijken van ASTM testresultaten is dus niet altijd direct mogelijk, maar belangrijker, algemeen wordt aangenomen dat de gerapporteerde opwarming van stents in het ASTM gelfantoom typisch een forse overschatting geeft van de in vivo te verwachten temperatuurstijging. Dit heeft met name te maken met actieve processen in het lichaam, zoals weefselperfusie en bloedstroming, die warmteafvoer bevorderen.
Zo is bekend uit onder andere hyperthermie en focused ultrasound onderzoek dat er een sterk koelende werking uitgaat van de nabijheid van grotere bloedvaten. Dit effect is bekend als het zogenaamde ‘heat sink’ effect (Shellock 2005, Reiss 2021, Winter 2015). Gevolg is dat een toename van de lokale SAR niet per definitie betekent dat het weefsel ter plekke ook sterk opwarmt. Dit blijkt ook uit dierexperimenteel werk (Gross 2016). In deze studie mat men op 3 T met een door de MR scanner geschatte ‘whole body’ SAR van 5,5 W/kg met in vivo geïmplanteerde temperatuur sensoren de temperatuurstijging rondom coronairarteriën (+0,7 oC), rondom doorbloede coronairarteriën geïmplanteerd met een stent (+0,8 oC), en rondom diezelfde arteriën waarbij met een ballon de bloedflow werd geblokkeerd (+2,4 oC). De precieze grootte van het ‘heat sink’ effect is een kennislacune. Wel is het een aanzienlijk effect, gezien het verschil in warmtecapaciteit van bloed ten opzichte van de stent (Vrtnik 2015). Er zijn enkele publicaties op dit thema. Een korte simulatiestudie gericht op effect van koeling ten gevolge van bloedstroming op de RF geïnduceerde opwarming van hartkleppen laat zien dat een implantaat met een resonante lengte een opwarming van het implantaat zonder doorbloeding laat zien van 1,5 °C en met doorbloeding 0,7 °C; dit bij een RF belasting van 5 W/kg (Stijnman 2019), en de reductiefactor door stroming neemt toe tot 4 bij hogere mate van opwarming. Ook Elder (2013 niet peer reviewed) schat een reductie van opwarming in van meer dan een factor 2 in. Een korte post mortem studie bij varkens, hierboven al genoemd, laat een factor 3 of hoger zien door bloeddoorstroming (Gross 2016). Tenslotte, een simulatiestudie en ex-vivo metingen aan coronair stents bij 4,7 T laten ook een sterk effect van stromingskoeling zien (Vrtnik 2015).
Het is begrijpelijk dat fabrikanten op basis van temperatuurstijgingen in het ASTM fantoom typisch komen tot een voorwaarde om de SAR limieten tijdens een scan met een vasculaire stent te reduceren om weefselschade te voorkomen. De risico’s zijn het grootst voor lange perifere stents en bij gebruik van andere spoelen dan de ‘whole body’ en hoofd RF zendspoelen. Echter, het blijkt uit de beperkingen van de metingen dat dit conservatief opgestelde waardes zijn.
Risico op weefselschade
Omdat de mate van opwarming mede bepaald wordt door de lengte van de stents en mate van doorbloeding is er in tabel 11 een overzicht gemaakt van typische stentlengtes afhankelijk van locatie. Dit laat zien dat typische stentlengte voor vaten in het hoofd, carotis en nieren beperkt zijn, zoals ook voor het merendeel van de coronairstents. Echter een beperkte groep, landelijk zo’n 2-5% van alle coronaire dotterbehandelingen, ondergaat therapie voor chronische totale occlusie (CTO), waarbij grotere stentlengtes worden geplaatst in de coronairvaten (Marechal 2018, Walsh 2020). Langere stents worden verder met name gebruikt in de aorta, femoralis, en de grote veneuze vaten in het bekken/abdomen.
Tabel 11. Vasculaire stentlengte afhankelijk van het toepassingsgebied.
|
Stentlocatie |
Typische lengte (maximale lengte) [cm] |
Bron |
|
Coronairvaten |
2,8 (5)* |
Bona 2016, Kaiser 2010, Vlachojannis 2017 |
|
Coronairvaten, CTO behandeling |
6,5 (12) # / 10±3## |
Werner 2018 / Walsh 2020 |
|
Abdominale aorta |
12-20 |
Shin 2001 |
|
Intracranieel |
1-3,5 (5)# /10±3 |
& 2023 / Ueda 2022 |
|
Carotis |
2- 8 |
Bossiers 2005 |
|
Nier Arterie |
1-2 |
Kadziela 2016 |
|
Arterie Iliaca |
4-8 |
&& 2023 |
|
Arterie Femoralis Superficialis |
8-24* |
Haine 2019 |
|
Vena Iliaca Communis (Vic) |
6-12* |
&&& 2023 |
|
Vena Iliaca Externa (Vie) |
8-12* |
&&& 2023 |
CTO: chronische totale occlusie
* Het betreft hier typische lengtes van geplaatste stents, niet de gecombineerde lengte van overlappende of (bijna) aansluitende stents.
# Het betreft hier maximale stentlengtes inclusief overlappende stents.
## Subgroep met percutane coronair behandeling met dissectie en re-entry techniek (DART).
& persoonlijke communicatie met interventieradioloog UMCU (2023).
&& persoonlijke communicatie interventieradioloog Amsterdam UMC (2023).
&&& persoonlijke communicatie vaatchirurg Hoorn (2023).
Het grootste risico op weefselschade door opwarming is te verwachten bij lange stents met geen of weinig doorbloeding in of rondom de stents. Het merendeel van de patiënten die MRI-onderzoek ondergaan met een stent zonder doorbloeding is er sprake van een onbehandelde obstructie bij de stent, welke niet gerelateerd is aan de vraagstelling van het MRI-onderzoek.
In die gevallen is er naar verwachting geen duidelijk klinisch effect door opwarming rondom de stentuiteinden; de obstructie bestaat dan immers al. Bij een minderheid van de patiënten zal de vraagstelling van het MRI-onderzoek wel gerelateerd zijn aan de stent. Bij de grote vaten zoals aorta, iliaca, femoralis en vena iliaca geeft een stromingsobstructie dusdanige klinische klachten dat dit zal leiden tot interventie. Bij deze vaten wordt in eerste instantie diagnostiek met CT of ultrasound echografie uitgevoerd, maar een MRI-onderzoek tijdens de verdere follow-up is wel mogelijk. In het primaire diagnostische traject van patiënten met klachten na een CTO behandeling met coronairstents wordt wel MRI toegepast. Mocht bij deze MRI-onderzoeken sterke opwarming optreden bij de stent, dan blijft het klinisch gevolg voor het aangedane vat ook beperkt, aangezien er al een obstructie aanwezig is.
Een significante temperatuurstijging zou theoretisch schade kunnen geven aan zenuwbanen die bij veel van de arteriën liggen waar stents worden geplaatst, maar dit zou onmiddellijk zeer pijnlijk moeten zijn (er wordt ook vaak pijn gevoeld bij stentplaatsing), of bij sterkere opwarming leiden tot tintelingen of uitval. Dergelijke complicaties zijn niet bekend in de literatuur en niet gevonden in de incidentdatabases.
Tenslotte zijn er nog een aantal andere redenen waarom klinische effecten minder zijn dan op basis van ex vivo metingen verwacht mag worden. Patiënten met stents gebruiken doorgaans bloedverdunners. Dit beperkt mogelijk het aantal gevallen waarin opwarming van een stent leidt tot een trombotische reactie en restenose van een vat. Ook worden veelal SAR-intensieve metingen afgewisseld met minder SAR-intensieve metingen tijdens het MRI-onderzoek. In veel klinische scanprotocollen zal het ‘whole body’ SAR niveau lager liggen dan 4 W/kg. De lokale SAR-belasting is voor stents onder het hart verwaarloosbaar bij neuro MRI, de meest voorkomende MRI-verwijzing. En bij een deel van de MRI-scanners kan überhaupt een 4 W/kg ‘whole body’ SAR niet gehaald worden, doordat er eerder op andere SAR-limieten wordt beperkt.
Incidentmeldingen
Naast dierexperimentele studies, fantoommetingen en simulaties is er in incidentendatabases en literatuur gezocht naar klinisch bewijs van weefselschade als gevolg van RF opwarming bij patiënten met stents. Mogelijke adverse events die benoemd worden in verschillende publicaties (zie literatuursamenvatting; Kramer 2000, Patel 2006, Schroeder 2000, Syed 2006) zijn veelal te relateren aan het ontstaan van restenose op de stentlocatie door schade aan de vaatwand, met als vaak bestudeerde (secundaire) effecten herhaalde katheterisatie, hernieuwd infarct, hartfalen, trombose, of eventueel het overlijden van de patiënt.
In bovenstaande genoemde studies uit de literatuursamenvatting, met beperkte aantallen geïncludeerde patiënten, werd geen grotere mate van restenose gerapporteerd. In deze studies is veelal geen SAR niveau gerapporteerd, maar er mag aangenomen worden dat juist in deze studies rekening werd gehouden met de RF-voorwaarden gesteld door de stentfabrikanten. Dit vormt daarmee een aanwijzing dat restenose geen klinisch probleem vormt, binnen de door de fabrikanten aanbevolen SAR restricties. Shellock et al. (2000) merkte op dat er destijds geen rapporten lijken te zijn van patiënten die ernstige schade hebben opgelopen als gevolg van opwarming van een metalen implantaat. Ten tijde van deze publicatie werden vooral 1,5 T MRI-scanners klinisch ingezet. Shellock merkte daarom ook op dat aanvullend onderzoek nodig zou zijn voor een veldsterkte als 3 T. Voor deze richtlijn is de MAUDE database doorzocht voor de periode 2011-2021, een periode waarin een veel groter aandeel van de klinische MRI-scanners werkte bij 3 T. Deze database bevat een zevental meldingen van pijnklachten mogelijk te wijten aan opwarming bij patiënten met een of meerdere stents (zie Samenvatting informatie uit incidentdatabases van implantaten), geïmplanteerd op verschillende anatomische locaties. In geen van de gevallen valt eenduidig te concluderen dat dit het gevolg was van het MRI-onderzoek.
In Nederland is het in 37% van de instellingen al voor meerdere jaren gebruikelijk dat patiënten met een vasculaire stent een MRI-onderzoek ondergaan bij 1,5 T en 3 T zonder verdere voorwaarden, zoals gebleken uit de enquête. Tevens blijkt uit de enquête dat de screening voor vasculaire stents zeker niet waterdicht is. En als een patiënt en of aanvragend arts al weet dat er een vasculaire stent is geplaatst, is in de meeste gevallen het precieze stent type en de lengte niet of lastig te achterhalen. Voor zover bekend heeft dit niet geleid tot incidenten door stentopwarming.
In een recente, Duitse richtlijn wordt een vergelijkbare observatie gedaan voor coronairstents (Müllerleile 2015, von Knobelsdorff 2021). Hoewel men daar aanbeveelt om cardiale MRI bij patiënten met coronairstents uit te voeren met maximaal 2 W/kg ‘whole body’ SAR, constateert men ook dat deze patiëntengroep in de praktijk veelal gescand wordt met een ‘whole body’ SAR tot 4 W/kg. In deze richtlijn concludeert men dat gegeven het ‘heat sink’ effect en het uitblijven van gemelde complicaties dit in feite verantwoord is.
Hierbij dient wel opgemerkt te worden dat een in-stent restenose door stentopwarming, die naar verwachting niet acuut ontstaat, niet altijd direct aan het MRI-onderzoek gerelateerd zal worden omdat deze klinische complicaties een hoge incidentie heeft. Na endovasculaire therapie met stents in de benen bij chronische been-bedreigende ischemie treden er ‘major adverse cardiovascular events’ op bij 43% van de patiënten (Farber 2022), en in-stent restenose treedt op in de femoralis of popliteale arterie bij 30-40% van de patiënten (Rymer 2018). In de coronairvaten ligt het percentage van restenose in de orde van 3-20% (Valenti 2013, Dangas 2010).
Conclusie
Hoewel er theoretisch en vanuit ex vivo metingen situaties te bedenken zijn waarin RF opwarming bij ‘whole body’ SAR waarden tot 4 W/kg zou kunnen leiden tot weefselschade is hiervoor geen klinisch bewijs gevonden in de literatuur en incidentendatabases. Ook blijkt dit niet uit de klinische praktijk, waarin regelmatig (per ongeluk of per protocol) patiënten met stents zonder SAR restricties worden gescand. De werkgroep concludeert dat de kans op klinisch relevante schade door RF opwarming bij een vasculaire stent zeer klein is, ook wanneer gescand wordt met een ‘whole body’ SAR in ‘first level’ modus tot 4 W/kg, bij gebruik van een ‘whole body’ of hoofd RF spoel.
- Risico op trilling of stroominductie door de oscillerende magnetische veldgradiënt
Een oscillerende magnetische veldgradiënt induceert zogenaamde wervelstromen (Eddy currents) in elektrisch geleidende materialen en dus ook in geïmplanteerde stents. Lange tijd werd aangenomen dat MRI-geïnduceerde opwarming het gevolg was van de blootstelling aan het RF veld alleen. Recentelijk is echter in de literatuur bewijs verschenen dat oscillerende magnetische veldgradiënten ook aanleiding kunnen geven tot opwarming van relatief grote implantaten, zoals gewrichtsprotheses (Bassen 2022, Graf 2007, Arduino 2022), zij het in veel mindere mate dan RF-geïnduceerde opwarming. De werkgroep schat in dat voor stents deze gradiënt-geïnduceerde stroominducties laag zijn vergeleken met door het RF veld geïnduceerde stromen (zie risico 2). Tevens werden hiervoor in de literatuur geen aanwijzingen gevonden, evenals Reiss et al. schrijven dat er geen studies bekend zijn waarin gradiënt-geïnduceerde opwarming van stents als gevolg van wervelstromen wordt gerapporteerd (Reiss 2021).
De hiervoor beschreven gradiënt-geïnduceerde wervelstromen in een elektrisch geleidend implantaat zullen aanleiding geven tot het ontstaan van een Lorentzkracht, die kan resulteren in een trilling van het implantaat. Ook dit effect is voor stents verwaarloosbaar. Deze conclusie is in lijn met het zeer beperkte aantal stents waarvoor in de MR voorwaarden door de stentfabrikant een beperking is opgelegd aan het gebruik van de oscillerende magnetische veldgradiënt (tabel 8). De werkgroep schat in dat dit effect voor stents vooral een theoretische overweging is, niet relevant voor het veilig kunnen ondergaan van een MRI-onderzoek.
- Artefact in het MRI beeld
In algemene zin geldt dat het soms lastig kan zijn om de anatomie in de (directe) nabijheid van een implantaat goed af te beelden op een MRI-scan. De aanwezigheid van een implantaat kan leiden tot variaties in het statisch magnetisch veld door het verschil in magnetische susceptibiliteit tussen metaal in het implantaat en omliggend weefsel (Hargreaves 2011). Hierdoor kunnen verschillende artefacten ontstaan in de beelden, zoals: signaalverlies door defasering, onvolledige vetonderdrukking, geometrische verstoring en eventueel signaalophoping door lokale verschuiving van de resonantiefrequentie, en verstoring van de plaatsing en dikte van het geëxciteerde vlak (Hargreaves 2011).
Dit fenomeen is ook bekend bij vasculaire stents en fabrikanten merken in het algemeen op om daar rekening mee te houden.
Wanneer een MR angiografie vervaardigd dient te worden voor de beoordeling van het lumen van een stent dan blijkt dit veelal niet goed mogelijk indien sprake is van een stent gefabriceerd uit roestvast staal (Walsh 2008, Wang 2003). Bij stents vervaardigd uit nitinol, platinum of kobalt-legeringen is het eenvoudiger ook het lumen te beoordelen, waarbij wel signaalverlies kan optreden in het lumen als gevolg van afscherming van het B1 veld door de stent (Walsh 2008, Wang 2003, Xia 2018).
- Risico van krachten door het Lenz-effect
Als elektrisch geleidende implantaten bewegen in een extern magnetisch veld, kunnen er stromen opgewekt worden in het implantaat die resulteren in krachten op het implantaat (het Lenz-effect, gerelateerd aan Faraday’s wet van inductie en wervelstromen). De grootte van de kracht is gerelateerd aan de temporele verandering in de magnetische flux. Deze verandering in magnetische flux kan ontstaan als het implantaat roteert terwijl de patiënt in de bore ligt of wanneer de patiënt door tafelbeweging de bore ingebracht wordt (Graf 2006, McRobbie 2020).
Verandering in de magnetische flux als gevolg van rotatie van het implantaat is met name relevant voor hartkleppen en is in silico en ex vivo bestudeerd (Edwards 2015, Golestanirad 2012, Robertson 2000, Condon 2000). Voor grotere implantaten is met name opwekking van stromen door tafelbewegingen van belang (McRobbie 2020). In vergelijking met hartkleppen ondervinden stents relatief weinig beweging en in vergelijking met grotere implantaten (zoals heupimplantaten) zijn de krachten op de stent ook een stuk kleiner, terwijl we verwachten dat de inkapseling van stents relatief groter is. Tevens hebben we geen bewijs gevonden in de literatuur dat het Lenz-effect op stents klinisch relevante effecten geeft bij patiënten. We concluderen daarom dat de risico’s ten gevolge van het Lenz effect voor patiënten met stents die MRI ondergaan op ‘whole body’ systemen met een horizontale/gesloten supergeleidende magneet met een veldsterkte van 1,5 of 3 T verwaarloosbaar zijn.
- Risico op verstoring van de werking van het implantaat
Dit risico is niet van toepassing op passieve implantaten zoals vasculaire stents. Het betreft een risico dat alleen van toepassing is voor actieve implantaten, zoals bijvoorbeeld pacemakers.
Slot-overwegingen
Voor een goede afweging is het belangrijk dat de gevolgen van screeningsbeleid en restricties op het afnemen van MRI-onderzoeken bij patiënten met stents worden afgezet tegen de risico’s. Uit bovenstaande analyse komen drie effecten naar voren die een potentieel risico zouden kunnen vormen: dislocatie, opwarming, en artefacten in de beeldvorming.
Er is geen bewijs dat dislocatie van stents in 1,5 T of 3 T MRI-scanners hebben geleid tot schade bij patiënten. Eerder werd gedacht dat stents gefabriceerd van zwak-ferromagnetische materialen een risico vormden. Dit was een reden om voor dit type stents een wachttijd voor MRI na implantatie aan te houden. Echter voor 1,5 T is er duidelijk bewijs in de literatuur dat dislocatie niet plaats vindt direct na implantatie, ook voor 3 T schat de werkgroep het risico hierop in als zeer klein, ongeacht de tijd tussen plaatsing van het implantaat en het MRI-onderzoek. Hierin is meegewogen dat: een aanmerkelijk deel van de Nederlandse ziekenhuizen niet screent op stents; er geen relevante incidentmeldingen gevonden zijn; bij stents op de markt gebracht na 2016 worden door de stentfabrikanten geen voorwaarden meer gesteld van wachttijd na implantatie, ook niet bij stents van zwak-ferromagnetische materialen; en dat hoewel de aantrekkings- en torsiekrachten op zwak-ferromagnetische stents bij 3 T hoger zullen zijn dan bij 1,5 T, deze in beide gevallen onvoldoende groot zullen zijn om te kunnen leiden tot dislocatie van deugdelijk geplaatste stents.
Er is geen klinisch bewijs dat RF geïnduceerde opwarming van stents heeft geleid tot schade bij patiënten, zowel voor 1,5 T als 3 T. RF opwarming van weefsel door de interactie tussen MRI en stent is een bekend fenomeen ex-vivo maar desondanks is weefselschade als gevolg hiervan voor het merendeel van de stents onwaarschijnlijk. Gegevens waarop de MR voorwaarden van de stentfabrikant zijn gebaseerd zijn conservatief, omdat onder andere afkoeling door weefselperfusie en bloedstroming daarin niet zijn meegenomen. De opwarming zal het grootst zijn bij lange stents met weinig of geen doorbloeding in en rondom het vat. In geval van onbehandelde obstructie bij de stent is een risico op eventuele weefselschade rond het stentuiteinde klinisch aanvaardbaar in de afweging, gezien weefselschade dan hoogstwaarschijnlijk niet tot een klinisch effect zal leiden. Dit risico moet gewogen tegen de toegankelijkheid tot MRI diagnostiek voor patiënten (zie hieronder).
Dat er lokaal artefacten optreden in de MRI beeldvorming bij patiënten met stents is bekend. Dit kan soms leiden tot verminderde diagnostische waarde. De gevolgen hiervan zijn in de meeste gevallen beperkt of niet redelijkerwijs te voorkomen door beleid.
Internationaal wordt als uitgangspunt gehanteerd in het screeningsbeleid dat bekend moet zijn of er scanrestricties bestaan voor implantaten, alvorens een MRI-onderzoek uit te voeren. In geval van een of meerdere vasculaire stents betekent dit strikt genomen dat op individueel niveau de specificaties van die stents uitgezocht moeten worden. Patiënten die een actief implantaat, zoals een pacemaker, geïmplanteerd hebben gekregen, hebben vrijwel altijd specifieke informatie over hun implantaat. Dit is niet het geval voor passieve implantaten zoals vasculaire stents. In de praktijk blijkt dat patiënten met stents, en de arts die het MRI-onderzoek aanvraagt, in veruit de meeste gevallen niet exact kunnen duiden welk type stent zij bij zich dragen. Van recent geïmplanteerde stents is deze registratie wel beter geworden in het patiëntdossier, maar alleen direct beschikbaar in de instelling van implantatie, en voor deze passieve implantaten krijgen patiënten geen implantatiekaart. Goede registratie in hoeverre stents overlappend zijn geplaatst is er ook heden ten dage niet. Evenzo zal de patiënt niet kunnen aangeven wat de lengte van de stent is, en of er meerdere (deels overlappende) stents zijn geplaatst, terwijl dit laatste een veelvoorkomende situatie is. Verder is het niet goed mogelijk de specifieke stents met hoger risico op opwarming efficiënt te kunnen screenen op een manier die goed implementeerbaar is.
Het huidige screeningsbeleid in Nederlandse zorginstellingen verschilt sterk. Een deel van de instellingen screent specifiek op (vasculaire) stents, een ander deel niet, en weer anderen alleen specifiek op stents op bepaalde locaties. Zou er beleid gevoerd worden waarbij voor elke vasculaire stent de MR voorwaarden van de fabrikant in principe leidend zouden zijn, dan heeft dat vergaande consequenties. Er zijn zo’n 350 verschillende types stents (zie tabel 6). In geval van actieve screening zal van elke vasculaire stent de aanvragend arts het stent type moeten achterhalen. Van het type stent zullen de MR-voorwaardelijke voorschriften van de fabrikant moeten worden opgezocht. Als het aangevraagde MRI-onderzoek buiten de MR voorwaarden van het stent type valt, dan moet een arts (radioloog met aanvragend arts) beslissen om het MRI-onderzoek alsnog wel of niet kan worden uit gevoerd, hierbij alle belangen afwegend. Als het protocol dusdanige uitwerking heeft dat in de meeste gevallen de aanvrager of radioloog toch akkoord geeft om buiten de aanbevelingen van een richtlijn te scannen, dan bestaat het risico dat de aandacht voor MR contra-indicaties met bekend grote complicaties afneemt. Dit alles zou een significante tijdsbesteding van vooral aanvragend artsen vragen om te achterhalen welk type stent de patiënt heeft, zeker als de stent in een andere zorginstelling is geïmplanteerd, en ook tijdsbesteding binnen de afdeling Radiologie en Nucleaire Geneeskunde om de MRI voorwaarden per patiënt uit te zoeken, en tijd om in geval het MR onderzoek de MR voorwaarden overtreden te besluiten het MRI-onderzoek wel of niet door te laten gaan. Deze screening leidt mogelijk tot uitstel van het MRI-onderzoek, en er ontstaat een extra belemmering ontstaat om een MRI-onderzoek aan te vragen. Dit zou leiden tot schade door gemiste op MRI gebaseerde diagnoses. Daarnaast leiden de SAR voorwaarden van de fabrikant tot een langere duur van het MR onderzoek, met mogelijk suboptimale beeldkwaliteit.
In de gevonden internationale aanbevelingen of expertgroep statements worden qua SAR alleen voor coronair- en carotisstents aanbevelingen gedaan voor beperking van de ‘whole body’ SAR limiet tot 2 W/kg. Het nadeel van deze beperking is dat een groot deel van deze groep patiënten relatief korte stents heeft, waarbij het opwarmingsrisico klein is, maar de aanbeveling wel de beeldkwaliteit van het MRI-onderzoek negatief beïnvloedt.
Het feit dat er geen enkele melding van klinische complicaties in de wetenschappelijke literatuur beschreven staat terwijl in de Nederlandse situatie bekend is dat de screening op vasculaire stents in de praktijk verre van volledig is, en dat er ook geen eenduidige meldingen in de incidentdatabases gevonden zijn, maakt de kans dat er klinisch relevante patiëntschade optreedt als gevolg van RF opwarming erg klein. Alles afwegend vindt de werkgroep screening op stents, en de daaraan gekoppelde SAR beperkingen, onvoldoende gerechtvaardigd om risico’s, met name de ex vivo gemeten temperatuurstijgingen die zouden kunnen leiden tot weefselschade, verder te verkleinen. Hierbij is meegewogen dat screening mogelijk lijdt tot suboptimale MRI diagnostiek staat door verminderde beeldkwaliteit, langere onderzoeksduur vanwege SAR beperking, en verminderde toegang. Dit leidt tot onderstaande aanbeveling 4.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Het is belangrijk dat een patiënt geen onnodige risico’s loopt bij het ondergaan van een MRI-onderzoek. Anderzijds is het ook onwenselijk dat, als gevolg van beleid om risico’s in te perken, voor een grote groep patiënten de wachttijden langer zijn vanwege screening of dat de scantijd en scankwaliteit negatief beïnvloed worden door beperkingen op de scan parameters.
Als er wel reële risico’s of ernstige mogelijke gevolgen te verwachten zijn dan is het belangrijk dat patiënten en hun naasten hierover geïnformeerd worden en samen met de betrokken zorgverlener een weloverwogen beslissing kunnen maken. Echter, daar hoort ook bij, in lijn met andere modaliteiten en behandelingen in het ziekenhuis, dat zeer weinig voorkomende of in omvang beperkte gevolgen in deze informatieverschaffing niet worden meegenomen omdat dit niet in verhouding staat tot deze risico’s. Naar idee van de werkgroep is het betreffende risico in deze zo klein (Regionaal Tuchtcollege 2021).
Kosten (middelenbeslag)
Met deze richtlijn wordt beoogd het screeningsbeleid te vereenvoudigen, wat zal leiden tot een beperking van de personele inzet tijdens de voorbereiding van MRI-onderzoeken bij patiënten met vasculaire stents. Door vast te stellen dat een wachttijd of SAR beperking niet meer nodig is, vervalt immers de noodzaak om op individueel niveau uit te zoeken welk type stent dat een patiënt geïmplanteerd heeft gekregen, en wat daarvoor de specifieke voorwaarden zijn.
Aanvaardbaarheid, haalbaarheid en implementatie
De richtlijn beoogt een basis te zijn voor vereenvoudiging en een uniformering van het MRI veiligheidsbeleid in Nederlandse ziekenhuizen voor wat betreft het scannen van patiënten met vasculaire stents. Hiermee wordt de toegankelijkheid van een belangrijke, diagnostische modaliteit vergroot. Immers, in de huidige praktijk onthouden sommige ziekenhuizen patiënten een MRI-onderzoek in de eerste weken na implantatie van een stent, terwijl in andere huizen patiënten met eenzelfde stent een MRI-onderzoek aangeboden krijgen met al dan niet een beperking van de gebruikte SAR. Men zou hier als bezwaar tegenin kunnen brengen dat internationaal gezien het algemene uitgangspunt is dat de door de stentfabrikant afgegeven MR veiligheidsclassificatie van de stent met eventuele voorwaarden bekend moet zijn, alvorens het MRI-onderzoek uit te voeren. Strikte toepassing van dit uitgangspunt zou de toegang voor patiënten met een vasculaire stent tot MRI-onderzoeken sterk beperken. Uit de enquête blijkt dat veel ziekenhuizen hier momenteel niet zo strikt mee omgaan en de werkgroep acht dit ook gerechtvaardigd in het licht van de wetenschappelijke literatuur en de beschreven overwegingen.
Aanbeveling 1
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Alle huidige vasculaire stent zijn MR voorwaardelijk, en er zijn geen MR onveilige stents in de markt gevonden, of stents die in het recente verleden zijn geïmplanteerd. Twee procent van alle stent types (welke voor 2011 op de markt zijn gebracht en gepubliceerd in Magresource) hebben geen MR veiligheidsclassificatie. De werkgroep acht het onwaarschijnlijk dat er in de toekomst nog MR onveilige vasculaire stent op de markt worden gebracht.
Aanbeveling 2
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventie
Een groot deel van de vasculaire stents is gefabriceerd van niet-ferromagnetische materialen. Echter een deel van de stents is gemaakt van zwak-ferromagnetische materialen. Voor 2016 is een deel van deze vasculaire stents MR gekwalificeerd met de voorwaarde van een wachttijd van zo’n 6 weken na implantatie voordat MRI kan plaatsvinden. Uit de enquête blijkt dat sommige ziekenhuizen in Nederland wachttijden hanteren voor het ondergaan van een MRI-onderzoek kort na implantatie van een stent.
In de literatuur tekent zich een steeds duidelijker beeld af dat deze wachttijd aanvankelijk uit voorzorg werd geïntroduceerd voor zwak-ferromagnetische stents. Uit steeds meer studies blijkt dat het ondergaan van een MRI-onderzoek kort na implantatie niet leidt tot een toename van het aantal adverse events (met name stent dislocaties) en dit is vertaald naar internationale adviezen in richtlijnen, waarin wordt beschreven dat een wachttijd geen bijdrage levert aan de veiligheid van een MRI-onderzoek. Hoewel de onderbouwing hiervoor sterker is voor 1,5 T dan voor 3 T, en er in sommige richtlijnen geadviseerd wordt een individuele risico-afweging te maken voor een onderzoek bij 3 T, komt de werkgroep tot de afweging dat voor beide veldsterktes een wachttijd niet nodig is. Hierin is meegewogen dat: een aanmerkelijk deel van de Nederlandse ziekenhuizen niet screent op stents; er geen relevante incidentmeldingen gevonden zijn; bij stents op de markt gebracht na 2016 worden door de stentfabrikanten geen voorwaarden meer gesteld voor wachttijd na implantatie, ook niet bij stents van zwak-ferromagnetische materialen; en dat hoewel de aantrekkings- en torsiekrachten op zwak-ferromagnetische stents bij 3 T hoger zullen zijn dan bij 1,5 T, deze in beide gevallen onvoldoende groot zullen zijn om te kunnen leiden tot dislocatie van deugdelijk geplaatste stents.
Aanbeveling 3
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventie
Niet alle stents zijn voor 3 T door de stentfabrikant als MR voorwaardelijk geclassificeerd; een deel is alleen voor 1,5 T geclassificeerd. Dit betreft deels oude MR veiligheidsclassificaties, en deels conservatieve classificaties door stentfabrikanten. De kans op dislocatie bij 3 T wordt verwaarloosbaar geacht, zie aanbeveling 2. De RF-geïnduceerde opwarming zal bij 3 T in z’n algemeenheid niet groter zijn dan bij 1,5 T bij gelijke SAR niveaus, eerder is er kans op minder opwarming. Echter, bij eenzelfde pulssequentie zal het SAR niveau bij 3 T wel hoger liggen dan bij 1,5 T.
Aanbeveling 4
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventie
Het is ex vivo aangetoond dat metalen implantaten met een lengte in de orde van 6-15 cm opwarmen tijdens een MRI-onderzoek als gevolg van de blootstelling aan RF velden. Uit de literatuur blijkt dat stents van 5 cm of korter een beperktere opwarming laten zien. Veel stenttypes zijn MR voorwaardelijk gekwalificeerd door de stentfabrikant met een beperking van het SAR niveau. Deze MR classificatie is echter conservatief en beperkt de SAR meer dan nodig, omdat deze is gebaseerd op ex vivo temperatuurmetingen in een fantoom zonder weefselperfusie, en zonder de bloeddoorstroming door de stent in ogenschouw te nemen.
Bij vasculaire stents acht de werkgroep de aldaar aanwezig bloeddoorstroming zodanig dat SAR beperkingen niet noodzakelijk zijn. Enerzijds voor een optimale onderbouwing van deze minder conservatieve SAR aanbeveling voor alle stents is er sprake van een kennislacune. Anderzijds, incidenten van klinische schade door RF geïnduceerde opwarming van stents zijn niet gevonden in de literatuur en incidentdatabases. In geval van langere stents in vaten waarbij de doorbloeding gestremd is, is het verwachte klinisch effect van een eventuele opwarming klein. Deze kans op schade weegt niet op tegen de extra arbeid om in elke individuele patiënt het vasculaire stent type uit te zoeken om te kunnen scannen binnen de MR voorwaarden gesteld door de stentfabrikant. Veelal is stent type informatie niet beschikbaar, en screening daarop zou leiden tot beperking van toegang tot MRI voor een grote groep patiënten; iets wat zeker tot schade leidt door de beperking in diagnose vorming. Alle patiënten scannen middels de meest conservatieve SAR limieten leidt tot verminderde beeldkwaliteit en langere onderzoeksduren en is daarom onwenselijk. Het gebruik van RF zendspoelen anders dan de ‘body’ of hoofd RF zendspoel is in Nederland beperkt, en valt buiten deze richtlijn.
Onderbouwing
Vasculaire stents en vasculaire grafts (hier stents genoemd) zijn typen implantaten die veelal worden ingezet na reparatie van stenose, om een bloedvat open te houden. Bij screening voor MRI wordt vaak rekening gehouden met stents, omdat deze metaal kunnen bevatten en daarmee potentieel een risico vormen op letsel bij de patiënt.
Er is een groot aanbod aan verschillende typen en modellen stents. In veel gevallen stelt de fabrikant per model condities waaronder een patiënt een MRI-onderzoek mag ondergaan. Deze condities lopen uiteen en zijn vaak conservatief opgesteld. Screening waarbij de specifieke MR voorwaarden van de fabrikant per patiënt per MRI-onderzoek moeten worden uitgezocht leidt tot veel werk en verhoogt de drempel voor een MRI-onderzoek. Daarnaast blijkt het met enige regelmaat onmogelijk te achterhalen welk type stent of graft is geïmplanteerd. Het betreft een grote groep patiënten die een vasculaire stent geïmplanteerd heeft en die op enig moment wordt doorverwezen voor een MRI-onderzoek. Een grove schatting hiervoor is dat dit gaat om zo’n 2% van de patiënten, wat een enorme inspanning zou vragen gegeven de miljoen MRI-onderzoeken die in Nederland jaarlijks vervaardigd worden (RIVM 2021).
Het is de vraag of de daadwerkelijke risico’s een (intensief) screeningsbeleid rechtvaardigen. Er blijkt ook een grote variatie tussen ziekenhuizen welk beleid wordt gevoerd, en is er onduidelijkheid wat de beste aanpak is. Daarom is een richtlijn over het afnemen van MRI-scans bij patiënten met (mogelijk) vasculaire stent gewenst.
Door middel van een literatuurreview en een analyse van verschillende incidentendatabases is een inschatting gemaakt op de risico’s bij het afnemen van een MRI-onderzoek bij patiënten met een stent. Om inzage te krijgen in de huidige stand van zaken is een enquête uitgezet onder Nederlandse ziekenhuizen met een MRI-scanner. Daarnaast is een implantatendatabase geraadpleegd welke scancondities door de fabrikanten worden opgelegd. Op basis van bovenstaande zijn alle risico’s van een MRI-onderzoek bij patiënten met stents in kaart gebracht en in hoofdklassen ingedeeld. Er wordt afgesloten met overwegingen en aanbevelingen.
|
Very low GRADE |
The evidence is very uncertain about the effect of MRI on adverse events when compared with no MRI in patients with vascular stents.
Sources: Kramer 2000, Patel 2006, Schroeder 2000, Syed 2006 |
|
Very low GRADE |
The evidence is very uncertain about the effect of early MRI on adverse events when compared with late MRI in patients with vascular stents.
Sources: Kaya 2009 |
|
Very low GRADE |
The evidence is very uncertain about the effect of 3T MRI on adverse events when compared with 1.5T MRI in patients with vascular stents.
Sources: Nijveldt 2008 |
Description of studies
- 1.5T MRI vs no MRI
Kramer (2000) used a prospective cohort to investigate the safety of performing an MRI after myocardial infarction (MI). Stented patients presenting at the hospital were included and compared with a group of stented patients enrolled at the same institution in the Stent PAM1 (Primary Angioplasty in Acute MI) study. No exclusion criteria were mentioned. In total, 13 patients were included in the intervention (MRI) group (50 ± 13 years, 1 female). Type of stents implanted in included patients were: Multi-link ACS (Guidant, n=8), Crown (Cordis/Johnson & Johnson, n=2), GFX (Arterial Vascular Engineering [AVE], n=2), and Nirvana (Boston Scientific Scimed, n=1). 17 patients were included in the control (no MRI) group (57 ± 9 years, 7 females), all with heparin-coated stents. Stent placement was comparable between groups. Groups were somewhat comparable at baseline. The MRI was performed with a 1.5T MRI at day 3 ± 1 after stent placement , with maximum whole body SAR levels of 0.2 W/kg. Length of follow up was 6 months. Outcome of interest were adverse events.
Patel (2006) performed a retrospective study to investigate safety of cardiac magnetic resonance (CMR) imaging performed early after coronary stent implantation in patients with acute myocardial infarction (AMI), at Duke University Medical Center in the USA. Patients were included in the intervention (1.5T MRI) group if they had an AMI and were referred for cardiac MR imaging, had undergone coronary stent implantation within the previous 14 days, had ST segment-elevation myocardial infarction or had non–ST segment-elevation myocardial infarction. Patients were included in the control group (no MRI) if they had AMI and underwent stent implantation but did not undergo CMR. Matching of intervention and control patients occurred by age, sex, MI type, diabetes, and the extent of de coronary artery disease. In total, 66 patients were included in the intervention (MRI) group (median age 56; 17 female), and 124 patients were included in the control (no MRI) group (median age 58; 29 female). Length of follow up was 30 days (no loss to follow up), and 6 months (n=34 loss to follow up). Included stent types were Cypher (Cordis, n=33), Express (Boston Scientific, n=19), S7 (Medtronic, n=19), S660 (Medtronic, n=7), Driver (Medtronic, n=6), Taxus (Boston Scientific, n=5), other three types (n=8). Outcome measure of interest was adverse events (death, non-fatal MI, revascularization).
Schroeder (2000) performed a prospective study to study whether exposure to cardiac MRI of patients with implanted intracoronary stents is associated with increased risk of stent-thrombosis, stent-restenosis, or other cardiovascular complications, in Aarhus University Hospital in Denmark from 1995 to 1997. Patients were included if they were ≤75 years old and admitted with a first-time diagnosis of AMI. Patients were excluded from the intervention (1.5T MRI) group and submitted to the control (no MRI) group if they were reluctant to participate, had claustrophobia, increased body mass, or for other practical reasons. MRI was performed on average 5.5 months after stent placement; a subgroup of MRI within 1 months was defined (n=13). Implanted stent types were: Palmaz-Schatz (Johnson & Johnson Interventional Systems, n=40), Micro (Medtronic, n=10), Freedom (Boston Scientific Corporation, n=8), NIR (Boston Scientific Corporation, n=8), Crossflex (Cordis, n=5) and Multilink (Guidant, n=2). Length of follow up was 21 ± 5 months. Outcomes of interest were stent-thrombosis and stent-restenosis (in juxtaposition).
Syed (2006) studied the long-term safety of CMR imaging at 1.5T performed shortly after coronary stent implantation, in a hospital in the USA from august 2002 to February 2004. Patients with acute STEMI, undergoing primary coronary intervention with bare-metal stent implantation were included (length 18 ± 7 mm, 86% of 316L stainless steel), if they had chest pain for shorter than 12 hours. Patients were excluded if they were too unstable to undergo CMR, or if they had any of the standard MRI contraindications. In total, 51 patients were included in the intervention (MRI in the first few days after implantation) group (63.1 ± 12.9, 8 female), and 68 patients were included in the control (no MRI) group (68.1 ± 13.6, 23 female). Stent positions, length and diameters were similar between groups. Follow up occurred at 30 days and at 6 months. Outcome of interest were MACE (death, reinfarction, acute coronary syndrome, heart failure, stent thrombosis, in-stent restenosis).
- Early versus late MRI
Kaya (2009) performed a prospective cohort study to study the early and late effects of 1.5T MRI on stent thrombosis and major adverse coronary events after coronary artery stent (CAS) implantation, at the Gazi University Medical Facility in Turkey, from 1998 until 2005. Patients were included if they underwent CAS implantation and MRI scanning. Patients were excluded if they had an impaired left ventricular function on echocardiogram (ejection fraction <0.30), unstable coronary artery disease, and any of the standard MRI contraindications. Early MRI was defined as an MRI within 8 weeks after CAS implantation, and late MRI was defined as an MRI after 8 weeks after CAS implantation. In total, 17 patients were included in the intervention (early MRI) group (61 ± 8 years, 3 females) and 26 were included in the control (late MRI) group (64 ± 11 years, 12 females). Stent lengths were comparable between groups (early MRI 15 ± 4 mm ; late MRI 15 ± 5 mm). Outcome of interest were major adverse cardiac events (MACE).
- 1.5T MRI vs 3T MRI
Nijveldt (2008) performed a prospective study to compare safety of 3T MRI with safety of a 1.5T MRI in patients with coronary vascular stents in the Netherlands. Patients were included if they were admitted with a first ST-elevation acute MI, according to standard electro-cardiographic and enzymatic criteria, and had undergone successful primary PCI with stent implantation. Patients were excluded if they had cardiographic evidence of reinfarction, haemodynamic or other clinical instability or (relative) contra-indications for CMR. In total, 25 patients were included (55 ± 9, 4 female), which accounted for 18 MRIs in the intervention group (3T MRI; 1x Multi-Link Vision n=12, 2x Multi-Link Vision n=1, 1x Driver n=3, 1x Diver/2x TAXUS Liberte n=2; mean number of stents per patient 1.3 ± 0.7 mm), and n=18 MRIs in the control group (1.5T MRI; 1x Prokinetic n=4, 2x Prokinetic n=1, 1x Lekton Motion n=4, 2x Lekton Motion n=1, 1x Lekton motion/ 2x Multi-Link Vision n=1, 1x AVE n=2, 1x Multi-Link Vision n=1, Multi-Link Zeta n=2, 1x CYPHER n=2; mean number of stents per patient: 1.2 ± 0.5 mm). Duration of follow up was 30 days. Outcome of interest were adverse events and image quality.
Results
- 1.5T MRI vs no MRI
Four studies reported on the comparison between 1.5T MRI and no MRI in patients with vascular stents (Kramer 2000, Patel 2006, Schroeder 2000, Syed 2006). Overall, more adverse events were observed when not performing an MRI compared to performing a 1.5T MRI in patients with vascular implants, although percentage wise, the difference was very small (Table 1). Kramer (2000) reported 3 repeat catheterizations in the 1.5T MRI group, one because of in-stent restenosis (AVE stent) and two because of widely patent stents (Both Multi-Link). In the control group (no MRI) 5 repeat catheterizations were reported, due to widely patent stents in 2 patients, and three patients required repeat angioplasty within the stent, two for reinfarction and one for in-stent restenosis (type of stent unknown). Syed (2006) and Patel (2006) did not report results separately for types of stents.
Table 1. Overview of number of patients included and number of events comparing 1.5T MRI and no MRI
|
Adverse events |
MRI |
No MRI |
|||
|
Events |
Total |
Events |
Total |
||
|
Repeat catheterization |
Total: |
3 (23%) |
13 |
5 (29%) |
17 |
|
Kramer (2000) |
3* |
13 |
5 ** |
17 |
|
|
In-stent restenosis |
Total: |
5 (6%) |
87 |
8 (7%) |
109 |
|
Kramer (2000) |
1 ** |
13 |
1 ** |
17 |
|
|
Schroeder (2000) |
3 |
23 |
6 |
24 |
|
|
Syed (2006) |
1 |
51 |
1 |
68 |
|
|
Stent thrombosis |
Total: |
1 (1%) |
74 |
2 (2%) |
92 |
|
Schroeder (2000) |
1 |
23 |
1 |
24 |
|
|
Syed (2006) |
0 |
51 |
1 |
68 |
|
|
Death |
Total: |
1 (1%) |
130 |
6 (3%) |
209 |
|
Kramer (2000) |
0 |
13 |
2 |
17 |
|
|
Patel (2006) |
0 |
66 |
2 |
124 |
|
|
Syed (2006) |
1 |
51 |
2 |
68 |
|
|
Acute coronary syndrome |
Total: |
0 (0%) |
51 |
6 (9%) |
68 |
|
Syed (2006) |
0 |
51 |
6 |
68 |
|
|
Heart failure |
Total: |
0 (0%) |
51 |
1 (2%) |
68 |
|
Syed (2006) |
0 |
51 |
1 |
68 |
|
|
Reinfarction |
Total: |
0 (0%) |
64 |
4 (5%) |
85 |
|
Kramer (2000) |
0 |
13 |
2 ** |
17 |
|
|
Syed (2006) |
0 |
51 |
2 |
68 |
|
|
Stent-restenosis in juxtaposition |
Total: |
4 (17%) |
23 |
2 (8%) |
24 |
|
Schroeder (2000) |
4 |
23 |
2 |
24 |
|
|
Revascularization |
Total: |
1 (2%) |
66 |
5 (4%) |
124 |
|
Patel (2006) |
1 |
66 |
5 |
124 |
|
|
Non-fatal myocardial infarction |
Total: |
0 (0%) |
66 |
2 (2%) |
124 |
|
Patel (2006) |
0 |
66 |
2 |
124 |
|
|
TOTAL COMBINED |
|
17 (11%) |
153 |
36 (15%) |
233 |
* In the study by Kramer et al. three patients in the MRI group underwent repeat catherization, for in-stent restenosis (n=1), for stenting of a stenosis at a different site not previously treated (n=1), and in one case the stent proved widely patent.
** In the study by Kramer et al. five patients in the control group required repeat catherization. Two patients had widely patent stents, three patients required repeat angioplasty (in-stent restenosis: n=1; reinfarction: n=2).
- Early versus late MRI
One study reported on the comparison of adverse events when performing an early MRI (within 8 weeks after implantation) compared with a late MRI (more than 8 weeks after implantation) (Kaya 2009). Overall, relatively more adverse events were observed in the early MRI group (Table 2). Results are not reported separately for types of stents.
Table 2. Overview of number of patients included and number of events comparing early MRI and late MRI (Kaya, 2009).
|
Adverse events |
Early MRI |
Late MRI |
|
|
N=17 |
N=26 |
|
Late stent thrombosis |
1 (6%) |
NR |
|
In-stent restenosis |
2 (12%) |
3 (12%) |
|
De-nova lesion |
4 (24%) |
2 (8%) |
|
Non-cardiac events |
not reported |
2 (8%) |
|
Death |
0 (0%) |
2 (8%) |
- 1.5T MRI vs 3T MRI
One study reported on the comparison between 3T MRI and 1.5T MRI (Nijveldt, 2008). Overall, more artefacts were observed when using 3T MRI compared to use of the 1.5T MRI (Table 3). Results are not reported separately for types of stents.
Table 3. Overview of number of patients included and number of events comparing 3T MRI and 1.5T MRI (Nijveldt, 2008).
|
Adverse events |
3T MRI |
1.5T MRI |
|
|
N=18 |
N=18 |
|
Clinical Events within 30 days |
0 (0%) |
0 (0%) |
|
Visibility of the stent |
9 (50%) |
11 (61%) |
|
Through-plane flow artifacts |
14 (78%) |
0 (0%) |
|
Severe image distortion |
8 (44%) |
0 (0%) |
Seven observational, non-comparative studies were described despite not adhering to our comparison of our PICO. Summary of the evidence found in those studies can be found in table 4.
Table 4. Overview of results of evidence found in non-comparative observational studies.
|
Author, year |
Methods |
N
|
MRI |
Results |
|
Curtis, 2013 |
Patients in a trial with an AMI within 16 days prior to the CMR examination and MRI within 16 days after stent placement |
211 patients
258 coronary stents placed by PCI
Mean stent width: 3.2 ± 0.54 mm Mean stent length: 17.5 ± 5.3 mm
Mean time from implantation to MRI: 6.5 ± 4 days |
1.5T MRI
short and long axis cine steady state free-precession imaging (SSFP) and T1-weighted, delayed enhanced (DE) MRI |
MACE: n=2 (ischemic stroke and heart failure both n=1)
Moderate adverse events: n=2 (pain and elevated cardiac enzymes both n=1) |
|
Duerinckx, 1998 |
Prospective study, including patients undergoing coronary MR angiography |
16 patients 27 coronary stents
4.0-mm-diameter Palmaz-Schatz stent(s) (Johnson & Johnson, Warren, NJ). |
1.5T MRI
82 ± 25 days after implantation |
Angina (requiring coronary angiography) after 15 days, due to stenosis: n=1
No complications
Artifacts: n=26 (96%) (one stent was not found because placement of the stent was unknown) |
|
Engellau, 2000 |
Ex vivo and in vivo experiments |
24 patients (10 for artifacts, 14 for velocity mapping)
bifurcated polyester-covered nitinol stent-graft for the abdominal aorta with platinum markers (Vanguard, Boston Scientific, Oakland, NJ). Whole body SAR up to 1.7 W/kg for 35 min. |
1.5T MR system |
Ex vivo heating to 1.1°C but no measurable temperature difference (≤ 0.2°C) to surrounding saline bath. No ferromagnetism was detected. Artifacts: Minor artifacts, consisting of thin, dark, indistinct ridges apparently indenting the inner lumen corresponding to the stent filaments. Velocity mapping: No differences in mean flow before and after stent placement. Aortic flow did improve. |
|
Gerber, 2003 |
All patients with CAS placement were included |
111 patients
Coronary stents Median stents per patients: 2 (range 1-6) |
128 MRIs 1.5T
MRI <8 weeks after implantation Mean: 21 ± 17 days
|
Adverse events: Stent thrombosis: n=0
Non cardiac death: n=4 Revascularization: n=3 |
|
Hiramoto, 2007 |
All patients (n=550) with stents were retrospectively reviewed, only the ones undergoing (unadvised) MRI were included (n=22). |
17 patients (with consent), of which: n=11
stainless-steel Zenith bifurcated abdominal aorta stent grafts, and n=6 custom-made uni-iliac stent grafts All in which patients were specifically instructed not to undergo MRI |
20 MRIs, 1.5T or less
Mean days after implantation: 669 days (range, 3-2179 days)
|
CT scans showed: no change in the structure, position, or function of the stent graft and no increase in the diameter of the aneurysm in any patient.
No patient experienced any symptoms of abdominal or back pain during or after the MRI.
Editorial: these stents are currently considered MR conditional at 1.5 and 3T |
|
Jehl, 2009 |
Prospective registry, including all patients with AMI (acute myocardial infarction). |
72 patients
Mean number of coronary stents per patient: 1.375 Average stent diameter: 3.2 mm Summed length of stents per patient: 22.4 mm |
3T MRI Number of MRIs not reported <14 days after implantation
|
Death: n=0 MI: n=0 Stable angina: n=4, of which n=2 has in-stent restenosis and n=2 had widely patent stents and lesions
In stent-restenosis found during repeated programmed cardiac catheterization for control of treatment: n=2 (of the n=5 controls) |
|
Porto, 2005 |
Prospective cohort |
49 patients
Mean number of coronary stents per patient: 2.2 ± 1.1 Average stent length per patient: 38 ± 20 mm |
1.5T MRI Number of MRIs not reported
1 – 3 days after complex contemporary percutaneous coronary intervention (PCI), including drug-eluting stent (DES) implantation.
|
No acute stent thrombosis (<48 hours) occurred.
No serious adverse events were reported during MRI examination
Major adverse cardiac event: n=2 (4%) (non-DES group)
No stent thrombosis
Restenosis: n=1 (incl. revascularization and coronary bypass surgery)
Unstable angina: n=1 (incl. repeat revascularization) |
Level of evidence of the literature
- 1.5T MRI vs no MRI
The level of evidence strictly fulfilling the PICO regarding the outcome measure adverse events started at Low because of the observational design and was downgraded by 1 level to Very Low because of number of included patients (imprecision).
- Early MRI vs late MRI
The level of evidence strictly fulfilling the PICO regarding the outcome measure adverse events started at Low because of the observational design and was downgraded by 1 level to Very Low because of number of included patients (imprecision).
- 1.5T MRI vs 3T MRI
The level of evidence strictly fulfilling the PICO regarding the outcome measure adverse events started at Low because of the observational design and was downgraded by 1 level to Very Low because of number of included patients (imprecision).
A systematic review of the literature was performed to answer the following question: What is the chance of negative events in patients with vascular stents undergoing an MRI?
P: Patients with vascular stent/graft.
I: MRI investigation.
C: No MRI investigation, adapted MRI investigation.
O: Negative effects: harmful effects on the patient because of interactions between the vascular stent/graft and the MRI scanner generated magnetic fields and radiofrequent waves.
Relevant outcome measures
The guideline development group considered negative effects as a critical outcome measure for decision making.
The working group defined the GRADE-standard limit of 25% difference for dichotomous outcomes (RR < 0.8 or > 1.25), and 10% for continuous outcomes as a minimal clinically (patient) important difference.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms from 1-1-1980 until 29-6-2022. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 1167 hits. Studies were selected based on the following criteria reporting on vascular stents/grafts, MRI and adverse effects. Furthermore, we included non-comparative studies if they had a size of n=10 or larger and reported on adverse events in patients with vascular stents undergoing MRI scanning. Six non-comparative studies were included. We excluded ex vivo and non-human studies but included those in the considerations of this Guideline. Guidelines were also selected, and an overview is presented in the considerations of this guideline (“overwegingen”). 52 studies were initially selected based on title and abstract screening. After reading the full text, 46 studies were excluded (see the table with reasons for exclusion under the tab Methods), and 6 comparative studies were included.
Results
Six comparative studies were included in the analysis of the literature. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables. Seven non-comparative studies were included.
- Arduino A, et al. (2022). A contribution to MRI safety testing related to gradient-induced heating of medical devices. Magn Reson Med 88: 930-944.
- ASTM international, standard F2182, Standard Test Method for Measurement of Radio Frequency Induced Heating On or Near Passive Implants During Magnetic Resonance Imaging. version 11 2011, version 19 2019).
- Bassen H, et al. (2006). MRI-induced heating of selected thin wire metallic implants-- laboratory and computational studies - findings and new questions raised. Minim Invasive Ther Allied Technol 15: 76-84.
- Bassen H and Zaidi T (2022). Parameters Affecting Worst-Case Gradient-Field Heating of Passive Conductive Implants. J Magn Reson Imaging 56: 1197-1204.
- Bona KH, et al (2016). Drug-Eluting or Bare-Metal Stents for Coronary Artery Disease. N Engl J Med 375: 1242-52. (DOI: 10.1056/NEJMoa1607991).
- Bosiers M, Deloose K, Verbist J and Peeters P (2005). Carotid artery stenting: which stent for which lesion? Vascular 13: 205-210.
- Condon B and Hadley DM (2000). Potential MR Hazard to Patients With Metallic Heart Valves: The Lenz Effect. J Magn Reson Imaging 21: 171-176.
- Cook Medical Gebruiksaanwijzing Zenith Flex AAA Endovascular Graft with the Z-Trak Introductie systeem. T_ZAAF_REV5, 2019. https://www.cookmedical.com/products/ndo_aaamain_webds/
- Curtis JW, Lesniak DC, Wible JH, Woodard PK (2013). Cardiac magnetic resonance imaging safety following percutaneous coronary intervention. Int J Cardiovasc Imaging 29: 1485-90. doi: 10.1007/s10554-013-0231-9.
- Dangas GD, Claessen BE, Caixeta A, Sanidas EA, Mintz GS, Mehran R (2010). In-Stent Restenosis in the Drug-Eluting Stent Era. J Am Coll Cardiol 56: 1897-1907.
- Duerinckx AJ, Atkinson D and Hurwitz R (1998). Assessment of coronary artery patency after stent placement using magnetic resonance angiography. J Magn Reson Imaging 8: 896-902. doi: 10.1002/jmri.1880080420. PMID: 9702892.
- Edwards MB, et al. (2015). In vitro assessment of the lenz effect on heart valve prostheses at 1.5 T. J Magn Reson Imaging 41: 1328-33.
- Elder NI (2013). Effects of Blood Flow on the Heating of Cardiac Stents Due to Radio Frequency Fields. Thesis, Purdue University.
- Engellau L, Olsrud J, Brockstedt S, Albrechtsson U, Norgren L, Ståhlberg F, Larsson EM (2000). MR evaluation ex vivo and in vivo of a covered stent-graft for abdominal aortic aneurysms: ferromagnetism, heating, artifacts, and velocity mapping. J Magn Reson Imaging 12: 112-21. doi: 10.1002/1522-2586(200007)12:1<112::aid-jmri13>3.0.co;2-g. PMID: 10931571.
- Farber A, Menard MT, Conte MS et al. (2022). Surgery or Endovascular Therapy for Chronic Limb-Threatening Ischemia. N Eng J Med 387:2305-2316.
- Fujimoto K, et al. (2018). Radio-Frequency Safety Assessment of Stents in Blood Vessels During Magnetic Resonance Imaging. Front Physiol 9: 1439.
- Gerber TC, Fasseas P, Lennon RJ, Valeti VU, Wood CP, Breen JF, Berger PB (2003). Clinical safety of magnetic resonance imaging early after coronary artery stent placement. J Am Coll Cardiol 42: 1295-8. doi: 10.1016/s0735-1097(03)00993-8. PMID: 14522498.
- Giroletti E and G Corbucci (2005). Cardiac magnetic resonance imaging: patient safety considerations. Phys Med 21: 5-13.
- Golestanirad L, et al. (2012). Comprehensive Analysis of Lenz Effect on the Artificial Heart Valves During Magnetic Resonance Imaging. Progress In Electromagnetics Research 128: 1-17.
- Gosselin MC, et al. (2014). Development of a new generation of high-resolution anatomical models for medical device evaluation: the virtual population 3.0. Physics in Medicine and Biology 59: 5287.
- Graf H, Lauer UA, Schick F (2006). Eddy-current induction in extended metallic parts as a source of considerable torsional moment. J Magn Reson Imaging 23: 585-590.
- Graf H, Steidle G, and Schick F (2007). Heating of metallic implants and instruments induced by gradient switching in a 1.5-Tesla whole-body unit. J Magn Reson Imaging 26: 1328-33.
- Gross DC and Simonetti OP (2016). In vivo and post-mortem measurements of radio frequency induced heating during MRI of pigs implanted with vascular stents. J Cardiovasc Magn Reson 18, Suppl 1:P53.
- Haine A, Schmid MJ, Schindewolfet M, et al. (2019). Comparison Between Interwoven Nitinol and Drug Eluting Stents for Endovascular Treatment of Femoropopliteal Artery Disease. European Journal of Vascular and Endovascular Surgery 58: 865-873.
- Hansmann HJ, et al. (2001). Rational radiologic after-care of endoluminal aortic bypass. Radiologe 41: 674-80.
- Hargreaves B, et al. (2011). Metal Induced Artifacts in MRI. Am J Roentgenol 197: 547-555.
- Hiramoto JS, Reilly LM, Schneider DB, Skorobogaty H, Rapp J, Chuter TA (2007). The effect of magnetic resonance imaging on stainless-steel Z-stent-based abdominal aortic prosthesis. J Vasc Surg 45: 472-4. doi: 10.1016/j.jvs.2006.11.031.
- Hundley WG, Bluemke DA, Finn JP, et al. (2010). ACCF/ACR/AHA/NASCI/SCMR 2010 expert consensus document on cardiovascular magnetic resonance: a report of the American College of Cardiology Foundation Task Force on Expert Consensus Documents. Circulation 121: 2462-508. doi: 10.1161/CIR.0b013e3181d44a8f.
- Hundley WG, et al. (2010). ACCF/ACR/AHA/NASCI/SCMR 2010 Expert Consensus Document on Cardiovascular Magnetic Resonance: A Report of the American College of Cardiology Foundation Task Force on Expert Consensus Documents. Journal of the American College of Cardiology 55: 2614-2662.
- Jabehdar Maralani P, Schieda N, Hecht EM, Litt H, Hindman N, Heyn C, Davenport MS, Zaharchuk G, Hess CP, Weinreb J (2020). MRI safety and devices: An update and expert consensus. J Magn Reson Imaging 51: 657-674. doi: 10.1002/jmri.26909.
- Jehl J, Comte A, Aubry S, Meneveau N, Schiele F, Kastler B (2009). Clinical safety of cardiac magnetic resonance imaging at 3 T early after stent placement for acute myocardial infarction. Eur Radiol 19: 2913-8. doi: 10.1007/s00330-009-1498-z. PMID: 19588151.
- Ji X, et al. (2019). Evaluations of the MRI RF-Induced Heating for Helical Stents Under a 1.5T MRI System. IEEE Transactions on Electromagnetic Compatibility 61: 57-64.
- Kadziela J, Michalowska I, Pregowski J, Janaszek-Sitkowska H, Lech K, Kabat M, Staruch A, Januszewicz A, Witkowski A (2016). Stent sizing strategies in renal artery stenting: the comparison of conventional invasive renal angiography with renal computed tomographic angiography. Adv Interv Cardiol 12, 2: 116-121.
- Kaiser C, et al. (2010). Drug-eluting versus bare-metal stents in large coronary arteries. N Engl J Med 363:2310-9. doi: 10.1056/NEJMoa1009406
- Kaya MG, Okyay K, Yazici H, et al. (2009). Long-term clinical effects of magnetic resonance imaging in patients with coronary artery stent implantation. Coron Artery Dis 20:138-42. doi: 10.1097/MCA.0b013e328322cd48. PMID: 19247183.
- Kramer CM, Rogers WJ Jr, Pakstis DL (2000). Absence of adverse outcomes after magnetic resonance imaging early after stent placement for acute myocardial infarction: a preliminary study. J Cardiovasc Magn Reson 2:257-61. doi: 10.3109/10976640009148689. PMID: 11545124.
- Levine GN, Gomes AS, Arai AE, et al. (2007). Safety of magnetic resonance imaging in patients with cardiovascular devices: an American Heart Association scientific statement from the Committee on Diagnostic and Interventional Cardiac Catheterization, Council on Clinical Cardiology, and the Council on Cardiovascular Radiology and Intervention: endorsed by the American College of Cardiology Foundation, the North American Society for Cardiac Imaging, and the Society for Cardiovascular Magnetic Resonance. Circulation 116:2878-91. doi: 10.1161/CIRCULATIONAHA.107.187256.
- Lopic N, et al. (2013). Quantitative determination of magnetic force on a coronary stent in MRI. J Magn Reson Imaging 37: 391-7.
- McRobbie DW (2020). Essentials of MRI safety. Wiley-Blackwell.
- Müllerleile K, Kolb C, Rittger H, Rybak K, Tillmans C, Wiegand U, Sechtem U, Kelm M, Schulz-Menger J (2015). Passive cardiovascular implants in magnetic resonance imaging: Statement of the German Cardiac Society on the safety of magnetic resonance imaging. Kardiologe 9:4, 303-309.
- Murbach M, Neufeld E, Kainz W, Pruessmann KP, Kuster N (2014). Whole-body and local RF absorption in human models as a function of anatomy and position within 1.5 T MR body coil. Magn Reson Med 71:839-845.
- NEN-IEC 60601-2-33 (2020). Edition 4.0 Medical electrical equipment - Part 2-33: Particular requirements for the basic safety and essential performance of magnetic resonance equipment for medical diagnosis. International Electrotechnical Commission (IEC), Geneva, Switzerland.
- Nijveldt R, Hirsch A, Hofman MB, Beek AM, Spijkerboer AM, Piek JJ, van Rossum AC (2008). 3.0 T cardiovascular magnetic resonance in patients treated with coronary stenting for myocardial infarction: evaluation of short term safety and image quality. Int J Cardiovasc Imaging 24: 283-91. doi: 10.1007/s10554-007-9264-2.
- Panych LP and Madore B (2018). The physics of MRI safety. J Magn Reson Imaging 47:28-43.
- Parthasarathy H, et al. (2013). MRI-Induced Stent Dislodgment Soon After Left Main Coronary Artery Stenting. Circulation: Cardiovascular Interventions 6: e58-e59.
- Patel MR, Albert TS, Kandzari DE, Honeycutt EF, Shaw LK, Sketch MH Jr, Elliott MD, Judd RM, Kim RJ (2006). Acute myocardial infarction: safety of cardiac MR imaging after percutaneous revascularization with stents. Radiology 240: 674-80. doi: 10.1148/radiol.2403050740.
- Porto I, Selvanayagam J, Ashar V, Neubauer S, Banning AP (2005). Safety of magnetic resonance imaging one to three days after bare metal and drug-eluting stent implantation. Am J Cardiol 96: 366-8. doi: 10.1016/j.amjcard.2005.03.077.
- Regionaal Tuchtcollege voor de gezondheidszorg Groningen, Uitspraak in zaak G2020/34, 2021. https://tuchtrecht.overheid.nl/ECLI_NL_TGZRGRO_2021_45.
- Reiss S, et al. (2021). Analysis of the RF Excitation of Endovascular Stents in Small Gap and Overlap Scenarios Using an Electro-Optical E-field Sensor. IEEE Trans Biomed Eng 68: 783-792.
- RIVM. Blootstelling aan straling in de gezondheidszorg. 24-12-2021. https://www.rivm.nl/medische-stralingstoepassingen/trends-en-stand-van-zaken/diagnostiek/echografie-en-mri.
- Robertson NM, Diaz-Gomez M, Condon B (2000). Estimation of torque on mechanical heart valves due to magnetic resonance imaging including an estimation of the significance of the Lenz effect using a computational model. Phys Med Biol 45: 3793.
- Rutledge JM, et al. (2001). Safety of magnetic resonance imaging immediately following Palmaz stent implant: a report of three cases. Catheter Cardiovasc Interv 53:519-23.
- Rymer JA and Jones WS (2018). Femoropopliteal In-Stent Restenosis. What Is the Standard of Care? Circulation: Cardiovascular Interventions 11(12).
- Sapareto SA, Dewey WC (1984). Thermal dose determination in cancer therapy. Int J Radiat Oncol Biol Phys 10:787-800.
- Schenk CD, et al. (2021). Review of safety reports of cardiac MR-imaging in patients with recently implanted coronary artery stents at various field strengths. Expert Review of Medical Devices 18: 83-90.
- Schroeder AP, Houlind K, Pedersen EM, Thuesen L, Nielsen TT, Egeblad H (2000). Magnetic resonance imaging seems safe in patients with intracoronary stents. J Cardiovasc Magn Reson 2: 43-9. doi: 10.3109/10976640009148672.
- Shellock FG (2000). Radiofrequency energy-induced heating during MR procedures: a review. J Magn Reson Imaging 12: 30-6.
- Shellock FG and Forder JR (2005). Drug eluting coronary stent: in vitro evaluation of magnet resonance safety at 3 Tesla. J Cardiovasc Magn Reson 7: 415-9.
- Shellock FG (2021). Guidelines for the Management of Patients with Coronary Artery Stents Referred for MRI Examinations. (https://www.ismrm.org/smrt/safety_page/2021.Shellock.Coronary-Stent.MRI.Guidelines.pdf).
- Shin H, Chavan A, Witthus F, Selle D, Stamm G, Peitgen HO, Galanski M (2001). Precise determination of aortic length in patients with aortic stent grafts: in vivo evaluation of a thinning algorithm applied to CT angiography data Eur Radiol 11: 733-8. doi: 10.1007/s003300000681.
- Sommer T, et al. (2004). High field MR imaging: magnetic field interactions of aneurysm clips, coronary artery stents and iliac artery stents with a 3.0 Tesla MR system. Rofo 176: 731-8.
- Song T, Xu Z, Iacone MI, Angelone LM and Rajan S (2018). Retrospective analysis of RF heating measurements of passive medical implants. Magn Reson Med 80: 2726-2730.
- Stijnman RS, van Nierop BJ, et al. (2019). Assessment of the alleviating impact of perfusion on RF-induced heating due to artificial cardiac valves. Annual Meeting ISMRM, 4154.
- Syed MA, Carlson K, Murphy M, Ingkanisorn WP, Rhoads KL, Arai AE (2006). Long-term safety of cardiac magnetic resonance imaging performed in the first few days after bare-metal stent implantation. J Magn Reson Imaging 24: 1056-61. doi: 10.1002/jmri.20740.
- Ueda T, Takaishi S, Yoshie T, et al. (2022). Long?term outcome and factors associated with restenosis after combination therapy of balloon angioplasty and stenting for symptomatic intracranial stenosis. BMC Neurology 22:477.
- Valenti R, Vergara R, Migliorini A, Parodi G, Carrabba N, Cerisano G , Dovellini EV and Antoniucci D (2013). Predictors of reocclusion after successful drug-eluting stent-supported percutaneous coronary intervention of chronic total occlusion J Am Coll Cardiol 61: 545-550.
- van Rhoon GC, Samaras T, Yarmolenko PS, Dewhirst MW, Neufeld E, and Kuster N (2013). CEM43°C thermal dose thresholds: a potential guide for magnetic resonance radiofrequency exposure levels? Eur Radiol 23: 2215-2227.
- von Knobelsdorff F, Bauer WR, Busch S, Eitel I, Jensen C, Marx N, Neizel-Wittke M, Radunski UK, Schuster A, Rolf A (2021). Safety of non-active cardiovascular implants in MRI examinations: Update 2021: Statement of the German Cardiac Society. Der Kardiologe 15: 262-271.
- Vrtnik S, et al.(2015). Coronary stent as a tubular flow heater in magnetic resonance imaging. Journal of Analytical Science and Technology 6: 1.
- Vlachojannis GJ, Puricel S , Natsuaki M , Morimoto T , Smits PC , Kimura T (2017). Biolimus-eluting versus everolimus-eluting stents in coronary artery disease: a pooled analysis from the NEXT (NOBORI biolimus-eluting versus XIENCE/PROMUS everolimus-eluting stent) and COMPARE II (Abluminal biodegradable polymer biolimus-eluting stent versus durable polymer everolimus-eluting stent) randomised trials. EuroIntervention 12: 1970-1977. (DOI: 10.4244/EIJ-D-16-00773).
- Walsh EG, et al. (2008). Assessment of passive cardiovascular implant devices for MRI compatibility. Technology and Health Care 16: 233-245.
- Walsh SJ, Hanratty CG, McEntegart M, et al. (2020). Intravascular Healing Is Not Affected by Approaches in Contemporary CTO PCI. The CONSISTENT CTO Study. J Am Col Cardiol Intv 13: 1448-47.
- Wang Y, et al. (2003). Quantitative evaluation of susceptibility and shielding effects of nitinol, platinum, cobalt-alloy, and stainless steel stents. Magn Reson Med 49: 972-6.
- Werner GS, Martin-Yuste V, Hildick-Smith D, Boudou N, Sianos G, Gelev V, Rumoroso JR, Erglis A, Christiansen EH, et al. (2018). A randomized multicentre trial to compare revascularization with optimal medical therapy for the treatment of chronic total coronary occlusions. Eur Heart J 39: 484-2493.
- Winter L, et al.(2015). On the RF heating of coronary stents at 7.0 Tesla MRI. Magn Reson Med 74: 999-1010.
- Wolf KV, et al. (2008). An investigation of adhesion in drug-eluting stent layers. J Biomed Mater Res A 87: 272-81.
- Xia Y, et al. (2018). Magnetic resonance imaging of patients with airway stents. J Thorac Dis 10: 5939-5945.
- Yao A, Murbach M, Goren T, et al. (2021). Induced radiofrequency fields in patients undergoing MR examinations: insights for risk assessment. Phys. Med. Biol. 66: 185014.
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Kaya, 2009 |
Type of study: prospective cohort
Setting and country: Gazi University Medical Faculty, Turkey, 1998-2005
Funding and conflicts of interest: no conflicts of interest. Funding not reported. |
Inclusion criteria: - patients undergoing CAS implantation who underwent MRI.
Exclusion criteria: - impaired left ventricular function on echocardiogram (ejection fraction <0.30) - unstable coronary artery disease patients, - and any of the standard MRI contraindications (e.g. pacemaker, defibrillator, intracranial aneurysm clips, or severe claustrophobia)
N total at baseline: Intervention: 17 Control: 26
Important prognostic factors2: age ± SD: I: 61 ± 8 years C: 64 ± 11 years
Sex: F/M I: 3/14 C: 12/14
Stents: Mean stents implanted per patient 1.3 I: size: 3.4 ± 0.5 mm Length: 15 ± 4 mm C: size: 3.3 ± 0.5 mm Length: 15 ± 5 mm
Groups comparable at baseline? Yes |
Describe intervention:
Early MRI: MRI within 8 weeks of the CAS implantation |
Describe control:
Late MRI: MRI after 8 weeks of the CAS implantation
Late: median 7 months (range 2-24) after CAS implantation |
Length of follow-up (months) Total: 36 ± 15 (range: 8-72) Early: 34 ± 17 Late: 37 ± 14
Loss-to-follow-up: Not applicable
Incomplete outcome data: Not applicable
|
Outcome measures and effect size (include 95%CI and p-value if available): MACE (major adverse cardiac events): cardiac death, nonfatal myocardial infarction, and target vessel revascularization by means of coronary artery bypass grafting or percutaneous coronary artery angioplasty
Early: 7/17 (41%) Late: 6/26 (23%) P=0.20
Serious adverse events: 0
Late stent thrombosis Early: n=1 (6%) Late: NR
in-stent restenosis Early: n=2 (12%) Late: n=3 (12%)
De-nova lesion Early: n=4 (24%) Late: n=2 (8%)
Non-cardiac events, pulmonary embolism because of leg fracture and stroke Early: NR Late: n=2 (8%)
Death Early: n=0 Late: n=2 (8%) |
|
|
Kramer, 2000 |
Type of study: prospective cohort
Setting and country: Allgheny General Hospital, Pittsburgh, USA
Funding and conflicts of interest: conflicts of interest not reported. Supported by a grant-in aid from the American Heart Association, PA affiliate, 97PAGS27 |
Inclusion criteria: - stented patients at the Allegheny General Hospital
Exclusion criteria: None mentioned
N total at baseline: Intervention: 13 Control: 17
Important prognostic factors2: age ± SD: I: 50 ± 13 years C: 57 ± 9 years
Sex: F/M I: 1/12 C: 7/10
Type of stents: I: n=6 left anterior descending n=5 right coronary n=1 left circumflex n=1 ramus intermedius
C: n=6 left anterior descending N=10 right coronary N=1 diagonal branch |
Describe intervention:
MRI 1.5T Phased-array body coil placed around patients’ chest breathhold tagged gradient echo cine images at rest and with low-dose dobutamine (5 and 10 pg/kg/min) 3 ± 1 day after stent placement |
Describe control:
No MRI |
Length of follow-up: 6 months
Loss-to-follow-up: none
Incomplete outcome data: none |
Outcome measures and effect size (include 95%CI and p-value if available): Adverse events:
Repeat catheterization for chest pain I: n=3 C: n=5
In-stent restenosis I: n=1 C: n=1 (and n=2 repeat angioplasty)
Widely patent stent I: n=2 C: n=2
Death I: n=0 C: n=2 (n=1 cardiogenic shock, n=1 sudden death due to sub-acute thrombosis)
|
|
|
Nijveldt, 2008 |
Type of study: prospective cohort
Setting and country: Academic medical center, the Netherlands
Funding and conflicts of interest: conflicts of interest: not reported.
Funding: from text: “This study was supported by Netherlands Heart Foundation grant 2003B126 from the Netherlands Heart Foundation. We thank Guerbet Nederland B.V. (Gorinchem, the Netherlands) for providing the contrast agent used in this study.” |
Inclusion criteria: - admitted with a first ST-elevation acute MI, according to standard electro-cardiographic and enzymatic criteria - undergone successful primary PCI with stent implantation
Exclusion criteria: - electro-cardiographic evidence of reinfarction, haemodynamic or other clinical instability or (relative) contra-indications for CMR such as claustrophobia, pacemakers, intracerebral aneurysm clips or very irregular heart rhythm
N total at baseline: Same group, different timepoints: n=25
Important prognostic factors2: age ± SD: 55 ± 9
Sex: F/M: 4/21
Mean no. stents per patient I: 1.3 ± 0.7 Mean length 19 ± 5 mm Diameter 3.2 ± 0.4 mm C: 1.2 ± 0.5 Mean length 19 ± 5 Diameter 3.2 ± 0.4 mm
Groups comparable at baseline? Yes |
Describe intervention:
Before myocardial infarction (MI) Cine imaging and LGE images
MRI: N=18: 3T gradient performance of 30 mT/m slew rate of 150 T/m/s six-element cardiac phased array surface coil
acute phase: n=12 chronic phase: n=6 |
Describe control:
After MI
Cine imaging and LGE images
MRI: N=18: 1.5T gradient performance of 40 mT/m slew rate of 200 T/m/s eight-element cardiac phased array surface coil |
Length of follow-up: 30 days
Loss-to-follow-up: Not reported
Incomplete outcome data: Not reported
|
Outcome measures and effect size (include 95%CI and p-value if available): Adverse events Discomfort or symptoms 3T: n=0 1.5T: n=0
Repeat catheterization 3T: n=9 (50%) (n=9 not visible) 1.5T: n=7 (58%) (n=11 not visible)
Cine imaging Visibility of the stent 3T: n=14 (78%) 1.5T: n=6 (33%)
Through-plane flow artifacts 3T: n=14 (78%) 1.5T: n=0
In-plane flow artifacts 3T: n=4 (not clinically relevant) 1.5T: n=0
Severe image distortion 3T: n=8 (44%) 1.5T: n=0
Total artifacts leading to information distortion 3T: n=12 (67%), of which n=6 by coronary stents 1.5T: n=0
LGE imaging Not sufficient. |
|
|
Patel, 2006 |
Type of study: retrospective study
Setting and country: Duke University Medical Center, USA
Funding and conflicts of interest: from text: “M.R.P. supported in part by an American College of Cardiology/ Merck Research Fellowship Award. T.S.E.A. supported in part by a Sarnoff Fellowship Award. R.M.J. supported in part by National Institutes of Health (NIH) grant R01-HL63268. R.J.K. supported in part by NIH grant R01-HL64726.” |
Inclusion criteria: I: Jan 2002 – May 2004 - patients with AMI who were referred for cardiac MR imaging - had undergone coronary stent implantation within the previous 14 days - patients with ST segment-elevation myocardial infarction or with non–ST segment- elevation myocardial infarction
C: Jan 2001 – Dec 2002 - Patients with AMI who underwent coronary stent implantation but did not undergo cardiac MR imaging
Exclusion criteria: None mentioned.
N total at baseline: Intervention: 66 Control: 124
Important prognostic factors2: Median age (25, 75th perc.): I: 56 (48, 66) C: 58 (49, 65)
Sex: F/M I: 17/49 C: 29/95
No. stents per patient I: 1.5 ± 0.83 C: 1.6 ± 0.86
Groups comparable at baseline? Yes |
Describe intervention:
MRI 1.5T phased-array coil cine imaging
Matching by: age, sex, myocardial infarction type (ST segment-elevation myocardial infarction vs non–ST segment- elevation myocardial infarction), presence of diabetes, and extent of coronary artery disease (single-vessel vs multivessel disease). |
Describe control:
No MRI |
Length of follow-up: 30 days, 6 months
Loss-to-follow-up: 30 days: n=0 6 months: I: n=17 (26%) C: n=17 (14%)
Incomplete outcome data: Not reported, assumed n=0 |
Outcome measures and effect size (include 95%CI and p-value if available): Death I: n=0 C: n=2 (1.6%)
Non-fatal myocardial infarction I: n=0 C: n=2 (1.6%)
Revascularization I: n=1 (1.2%) C: n=5 (4.0%)
Combined: I: n=1 (2% (95%CI: 0.0% - 4.5%) C: n=8 (6.5% (95%CI: 1.6% - 11.3%)
30 day follow up: MR imaging was not associated with death, nonfatal myocardial infarction, or revascularization. OR 0.22 (95%CI: 0.03, 1.82) |
|
|
Schroeder, 2000 |
Type of study: prospective cohort
Setting and country: Aarhus University Hospital, Denmark, 11/9/95 to 10/2/97
Funding and conflicts of interest: not reported |
Inclusion criteria: - ≤75 years old, admitted with a first-time diagnosis of AMI
Exclusion criteria: To be placed in the control group instead of intervention group: - reluctance to participate, claustrophobia, increased body mass, or for other practical reasons
N total at baseline: Intervention: 23 Control: 24
Important prognostic factors2: age ± SD: I: 58 ± 10 C: 59 ± 11
Sex: I: 2/21 C: 3/21
No of stents: I: 33 (1.4 per patient) Mean length: 14.1 ± 4.4 Mean diameter: 3.6 ± 0.5 C: 40 (1.7 per patient) Mean length: 13.6 ± 4.8 Mean diameter: 3.7 ± 0.4
Groups comparable at baseline? Yes |
Describe intervention:
MRI 3-9 days and 3, 6, and 12 months after infarction
1.5-T systems (Philips Gyroscan HP/S15 with 10 mT/m, 10 mT/m/ms gradients, and Philips Gyroscan NT with 15 mT/m, 17 mT/m/ms gradients)
Matching based on age and gender |
Describe control:
No MRI |
Length of follow-up: 21.3 ± 4.5 months
Loss-to-follow-up: Not reported, assumed n=0
Incomplete outcome data: Not reported, assumed n=0
|
Outcome measures and effect size (include 95%CI and p-value if available): stent-thrombosis I: n=1 (4.3%) C: n=1 (4.2%)
stent-restenosis I: n=3 (13.0%) C: n=6 (25%)
Stent-restenosis in juxtaposition I: n=4 (17.4%) C: n=2 (8.3%)
Combined: I: n=8 (34.8%) C: n=5 (20.8%) |
|
|
Syed, 2006 |
Type of study: prospective study
Setting and country: hospital, USA, Aug 2002 – Feb 2004
Funding and conflicts of interest: conflicts of interest: none reported. Grant from National Institutes of Health |
Inclusion criteria: - patients with acute STEMI, undergoing primary coronary intervention (PCI) with bare-metal stent implantation - chest pain less than 12 hour duration
Exclusion criteria: - too unstable to undergo CMR - any of the standard MRI contraindications (e.g., pacemaker, defibrillator, intracranial aneurysm clips, or severe claustrophobia)
N total at baseline: Intervention: 51 Control: 68
Important prognostic factors2: age ± SD: I: 63.1 ± 12.9 C: 68.1 ± 13.6
Sex: F/M I: 8/43 C: 23/48
Stent measurements: I: mean length: 17.6 ± 5.2 Mean diameter: 3.3 ± 0.5 C: mean length: 18.9 ± 7.7 Mean diameter: 3.2 ± 0.5
Stent position: I: n=22 left anterior descending N=6 left circumflex N=20 right coronary N=3 two vessels
C: n=21 left anterior descending N=7 left circumflex N=37 right coronary N=3 two vessels
Groups comparable at baseline? Yes |
Describe intervention:
CMR in the first days after implantation 1.5T Maximum gradient 40 mT/m slew rate 180 mT/m/s four-element cardiac phased-array coil
2.7 ± 3.1 days after stent implantation |
Describe control:
No CMR in the first days after implantation |
Length of follow-up: 30 days and 6 months Mean: 4.4 ± 2.1
Loss-to-follow-up: I: n=4 (7.8%) C: n=8 (11.8%) Reasons not reported.
Incomplete outcome data: Not reported, assumed n=0
|
Outcome measures and effect size (include 95%CI and p-value if available): MACE: major adverse cardiac event
Death from any cause I: n=1 (2.1%) (although not related to the MRI: “it occurred in the patient with a ventricular septal rupture after myocardial infarction which was already present at the time of the examination” C: n=2 (3.3%)
Reinfarction I: n=0 C: n=2 (3.3%)
Acute coronary syndrome I: n=0 C: n=6 (10.0%)
Heart failure I: n=0 C: n=1 (1.7%)
Stent thrombosis I: n=0 C: n=1 (1.7%)
In-stent restenosis I: n=1 (2.1%) C: n=1 (1.7%)
Complications during the scan I: n=0 C: n/a
|
|
Notes:
- Prognostic balance between treatment groups is usually guaranteed in randomized studies, but non-randomized (observational) studies require matching of patients between treatment groups (case-control studies) or multivariate adjustment for prognostic factors (confounders) (cohort studies); the evidence table should contain sufficient details on these procedures
- Provide data per treatment group on the most important prognostic factors [(potential) confounders]
- For case-control studies, provide sufficient detail on the procedure used to match cases and controls
- For cohort studies, provide sufficient detail on the (multivariate) analyses used to adjust for (potential) confounders
Risk of bias table
|
Author, year |
Selection of participants
Was selection of exposed and non-exposed cohorts drawn from the same population?
|
Exposure
Can we be confident in the assessment of exposure?
|
Outcome of interest
Can we be confident that the outcome of interest was not present at start of study?
|
Confounding-assessment
Can we be confident in the assessment of confounding factors?
|
Confounding-analysis
Did the study match exposed and unexposed for all variables that are associated with the outcome of interest or did the statistical analysis adjust for these confounding variables? |
Assessment of outcome
Can we be confident in the assessment of outcome?
|
Follow up
Was the follow up of cohorts adequate? In particular, was outcome data complete or imputed?
|
Co-interventions
Were co-interventions similar between groups?
|
Overall Risk of bias
|
|
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Low, Some concerns, High |
|
|
Kaya, 2009 |
Definitely yes
Reason: same hospital, same inclusion and exclusion; same characteristics |
Definitely yes
Reason: MRI |
Definitely yes
Reason: outcome is death and adverse events
|
Probably yes
Reason: Not specifically reported, but can be assumed. Comorbidties etc are taken into account |
Probably yes
Reason: Not reported, but groups are similar |
Definitely yes
Reason: outcome is death and adverse events
|
Definitely yes
Reason: no loss to follow up |
Definitely yes
Reason: medication is noted and similar between groups |
LOW |
|
Kramer, 2000 |
Definitely yes
Reason: same hospital, same inclusion and exclusion; same characteristics |
Definitely yes
Reason: MRI |
Definitely yes
Reason: outcome is death and adverse events
|
Probably yes
Reason: Not specifically reported, but can be assumed. Comorbidties etc are taken into account |
Probably yes
Reason: Not reported, but groups are similar |
Definitely yes
Reason: outcome is death and adverse events
|
Definitely yes
Reason: no loss to follow up |
Definitely yes
Reason: medication is noted and similar between groups |
LOW |
|
Nijveldt, 2008 |
Definitely yes
Reason: same hospital, same inclusion and exclusion; same characteristics |
Definitely yes
Reason: MRI |
Definitely yes
Reason: outcome artefacts of MRI
|
Probably yes
Reason: Not specifically reported, but can be assumed. Comorbidties etc are taken into account |
Probably yes
Reason: Not reported, but groups are similar |
Defin Definitely yes
Reason: outcome is death and adverse events
|
Definitely yes
Reason: no loss to follow up |
Definitely yes
Reason: medication is noted and similar between groups |
LOW |
|
Patel, 2006 |
Definitely yes
Reason: same hospital, same inclusion and exclusion; same characteristics |
Definitely yes
Reason: MRI |
Definitely yes
Reason: outcome is death and adverse events
|
Probably yes
Reason: Not specifically reported, but can be assumed. Comorbidties etc are taken into account |
Definitely yes / Probably yes / Probably no / Definitely no
Reason:
|
Definitely yes
Reason: outcome is death and adverse events
|
Definitely yes
Reason: loss to follow up is accounted for (in survival analysis) |
Definitely yes
Reason: medication is noted and similar between groups |
LOW |
|
Schroeder, 2000 |
Definitely yes
Reason: same hospital, same inclusion and exclusion; same characteristics |
Definitely yes
Reason: MRI |
Definitely yes
Reason: outcome is adverse events
|
Probably yes
Reason: Not specifically reported, but can be assumed. Comorbidties etc are taken into account |
Definitely yes
Reason: matching |
Definitely yes
Reason: outcome is adverse events
|
Definitely yes
Reason: no loss to follow up |
Definitely yes
Reason: medication is noted and similar between groups |
LOW |
|
Syed, 2006 |
Definitely yes
Reason: same hospital, same inclusion and exclusion; same characteristics |
Definitely yes
Reason: MRI |
Definitely yes
Reason: outcome is adverse events
|
Probably yes
Reason: Not specifically reported, but can be assumed. Comorbidties etc are taken into account |
Definitely yes
Reason: matching |
Definitely yes
Reason: outcome is adverse events
|
Probably yes
Reason: loss to follow up is small |
Definitely yes
Reason: medication is noted and similar between groups |
LOW |
Footnotes
Selection of participants Example of low risk of bias: Exposed and unexposed drawn for same administrative database of patients presenting at same points of care over the same time frame
Exposure Examples of low risk of bias: Secure record (e.g. surgical records, pharmacy records); Repeated interview or other ascertainment asking about current use/exposure
Confounding Examples of low risk of bias regarding assessment: Interview of all participants; Self-completed survey from all participants; Review of charts with reproducibility demonstrated; From database with documentation of accuracy of abstraction of prognostic data.
Example of low risk of bias regarding analysis: Comprehensive matching (e.g. with propensity score) or adjustment for all plausible confounding variables
Assessment of outcome Examples of low risk of bias: Independent blind assessment; Record linkage; For some outcomes (e.g. fractured hip), reference to the medical record is sufficient to satisfy the requirement for confirmation of the fracture
Follow up Examples of low risk of bias: No missing outcome data; Reasons for missing outcome data unlikely to be related to true outcome (for
survival data, censoring is unlikely to introduce bias); Missing outcome data balanced in numbers across intervention groups, with similar reasons for missing data across groups; Missing data have been imputed using appropriated methods
Co-interventions Example of low risk of bias: Most or all relevant co-interventions that might influence the outcome of interest are documented to be similar in the exposed and unexposed
Table of excluded studies
|
Author and year |
Reason for exclusion |
|
American College of Cardiology Foundation Task Force on Expert Consensus Documents, Hundley WG, Bluemke DA, Finn JP, Flamm SD, Fogel MA, Friedrich MG, Ho VB, Jerosch-Herold M, Kramer CM, Manning WJ, Patel M, Pohost GM, Stillman AE, White RD, Woodard PK. ACCF/ACR/AHA/NASCI/SCMR 2010 expert consensus document on cardiovascular magnetic resonance: a report of the American College of Cardiology Foundation Task Force on Expert Consensus Documents. Circulation 2010;121:2462-508. doi: 10.1161/CIR.0b013e3181d44a8f. |
wrong study design (no comparison) |
|
Baikoussis NG, Apostolakis E, Papakonstantinou NA, Sarantitis I, Dougenis D. Safety of magnetic resonance imaging in patients with implanted cardiac prostheses and metallic cardiovascular electronic devices. Ann Thorac Surg. 2011;91:2006-11. doi: 10.1016/j.athoracsur.2011.02.068. |
wrong study design (no comparison) |
|
Dill T. Contraindications to magnetic resonance imaging: non-invasive imaging Heart 2008;94:943-8. doi: 10.1136/hrt.2007.125039. |
wrong publication type (no research article) |
|
Friedrich MG, Strohm O, Kivelitz D, Gross W, Wagner A, Schulz-Menger J, Liu X, Hamm B. Behaviour of implantable coronary stents during magnetic resonance imaging. Int J Cardiovasc Intervent. 1999;2:217-222. doi: 10.1080/acc.2.4.217.222. |
wrong study design (porcine hearts, adverse events in patients not specified) |
|
Fujimoto K, Angelone LM, Lucano E, Rajan SS, Iacono MI. Radio-Frequency Safety Assessment of Stents in Blood Vessels During Magnetic Resonance Imaging. Front Physiol. 2018;9:1439. doi: 10.3389/fphys.2018.01439. |
wrong study design (anatomically realistic virtual patient) |
|
Fujiwara Y, Fujioka H, Watanabe T, Sekiguchi M, Murakami R. A Web-based searchable system to confirm magnetic resonance compatibility of implantable medical devices in Japan: a preliminary study. Radiol Phys Technol. 2017;10:340-348. doi: 10.1007/s12194-017-0409-2. |
wrong study design (development of search strategy for compatibility) |
|
Giroletti E, Corbucci G. Cardiac magnetic resonance imaging: patient safety considerations. Phys Med. 2005;21:5-13. doi: 10.1016/S1120-1797(05)80014-6. |
wrong study design (no comparison) |
|
Grzyska U, Friedrich T, Sieren MM, Stahlberg E, Oechtering TH, Ahlborg M, Buzug TM, Frydrychowicz A, Barkhausen J, Haegele J, Wegner F. Heating of an Aortic Stent for Coarctation Treatment During Magnetic Particle Imaging and Magnetic Resonance Imaging-A Comparative In Vitro Study. Cardiovasc Intervent Radiol. 2021;44:1109-1115. doi: 10.1007/s00270-021-02795-4. |
wrong study design (in vitro experiment) |
|
Gualandro DM, Shiozaki AA, Rochitte CE. Safety of nuclear magnetic resonance after stent coronary angioplasty. REVISTA DA ASSOCIACAO MEDICA BRASILEIRA 2008; 54, 287-288. |
wrong publication (article in Portuguese) |
|
Hansmann HJ, Kampschulte A, Schumacher H, Nöldge G, Richter GM. Rationale radiologische Nachsorge des endoluminalen aortalen Bypasses [Rational radiologic after-care of endoluminal aortic bypass]. Radiologe 2001;41:674-80. German. doi: 10.1007/s001170170117. PMID: 11552382. |
wrong publication (article in German) |
|
Henk CB, Higgins CB, Saeed M. Endovascular interventional MRI. J Magn Reson Imaging 2005;22:451-60. doi: 10.1002/jmri.20411. |
wrong study design (interventional MRIs) |
|
Hilfiker PR, Quick HH, Pfammatter T, Schmidt M, Debatin JF. Three-dimensional MR angiography of a nitinol-based abdominal aortic stent graft: assessment of heating and imaging characteristics. Eur Radiol. 1999;9:1775-80. doi: 10.1007/s003300050921. |
wrong study design (in vitro) |
|
Jabehdar Maralani P, Schieda N, Hecht EM, Litt H, Hindman N, Heyn C, Davenport MS, Zaharchuk G, Hess CP, Weinreb J. MRI safety and devices: An update and expert consensus. J Magn Reson Imaging 2020;51:657-674. doi: 10.1002/jmri.26909. |
wrong study design (no comparison) |
|
Jaimes C, Biaggotti D, Sreedher G, Chaturvedi A, Moore MM, Danehy AR. Magnetic resonance imaging in children with implants. Pediatr Radiol. 2021;51:748-759. doi: 10.1007/s00247-021-04965-5. |
wrong study design (no comparison) |
|
Levine GN, Gomes AS, Arai AE, Bluemke DA, Flamm SD, Kanal E, Manning WJ, Martin ET, Smith JM, Wilke N, Shellock FS; American Heart Association Committee on Diagnostic and Interventional Cardiac Catheterization; American Heart Association Council on Clinical Cardiology; American Heart Association Council on Cardiovascular Radiology and Intervention. Safety of magnetic resonance imaging in patients with cardiovascular devices: an American Heart Association scientific statement from the Committee on Diagnostic and Interventional Cardiac Catheterization, Council on Clinical Cardiology, and the Council on Cardiovascular Radiology and Intervention: endorsed by the American College of Cardiology Foundation, the North American Society for Cardiac Imaging, and the Society for Cardiovascular Magnetic Resonance. Circulation 2007;116:2878-91. doi: 10.1161/CIRCULATIONAHA.107.187256. |
wrong publication type (scientific statement) |
|
Lopič N, Jelen A, Vrtnik S, Jagličić Z, Wencka M, Starc R, Blinc A, Dolinšek J. Quantitative determination of magnetic force on a coronary stent in MRI. J Magn Reson Imaging 2013;37:391-7. doi: 10.1002/jmri.23831. |
wrong study design (in vitro) |
|
Martin ET, Sandler DA. MRI in patients with cardiac devices. Curr Cardiol Rep. 2007;9:63-71. doi: 10.1007/s11886-007-0012-y. |
wrong study design (no comparison) |
|
Ocazionez D, Dicks DL, Favinger JL, Shroff GS, Damani S, Kicska GA, Reddy GP. Magnetic resonance imaging safety in cardiothoracic imaging. J Thorac Imaging 2014;29:262-9. doi: 10.1097/RTI.0000000000000108. |
wrong study design (no comparison) |
|
Prasad SK, Pennell DJ. Safety of cardiovascular magnetic resonance in patients with cardiovascular implants and devices. Heart 2004;90:1241-4. doi: 10.1136/hrt.2003.021154. |
wrong publication (editorial) |
|
Reiss S, Lottner T, Ozen AC, Polei S, Bitzer A, Bock M. Analysis of the RF Excitation of Endovascular Stents in Small Gap and Overlap Scenarios Using an Electro-Optical E-field Sensor. IEEE Trans Biomed Eng. 2021;68:783-792. doi: 10.1109/TBME.2020.3009869. |
wrong study design (in vitro experiment) |
|
Rutledge JM, Vick GW 3rd, Mullins CE, Grifka RG. Safety of magnetic resonance imaging immediately following Palmaz stent implant: a report of three cases. Catheter Cardiovasc Interv. 2001;53:519-23. doi: 10.1002/ccd.1214. |
wrong publication type (case report) |
|
Sardanelli F, Zandrino F, Molinari G, Iozzelli A, Balbi M, Barsotti A. MR evaluation of coronary stents with navigator echo and breath-hold cine gradient-echo techniques. Eur Radiol. 2002;12:193-200. doi: 10.1007/s003300101017. |
wrong study design (placing of the implant) |
|
Schenk CD, Gebker R, Berger A, Pieske B, Stehning C, Kelle S. Review of safety reports of cardiac MR-imaging in patients with recently implanted coronary artery stents at various field strengths. Expert Rev Med Devices 2021;18:83-90. doi: 10.1080/17434440.2021.1860017. |
wrong study design (different focus of the review) |
|
Shellock FG, Curtis JS. MR imaging and biomedical implants, materials, and devices: an updated review. Radiology 1991;180:541-50. doi: 10.1148/radiology.180.2.2068325. |
wrong study design (all kinds of implants) |
|
Shellock FG, Forder JR. Drug eluting coronary stent: in vitro evaluation of magnet resonance safety at 3 Tesla. J Cardiovasc Magn Reson. 2005;7:415-9. doi: 10.1081/jcmr-200053588. PMID: 15881523. |
wrong study design (in vitro experiment) |
|
Shellock FG, Giangarra CJ. In vitro assessment of 3-T MRI issues for a bioabsorbable, coronary artery scaffold with metallic markers. Magn Reson Imaging. 2014;32:163-7. doi: 10.1016/j.mri.2013.10.009. |
wrong study design (in vitro experiment) |
|
Shellock FG, Morisoli S, Kanal E. MR procedures and biomedical implants, materials, and devices: 1993 update. Radiology. 1993;189:587-99. doi: 10.1148/radiology.189.2.8210394. |
wrong study design (all kinds of implants) |
|
Sincleair ST. Is MRI contraindicated after coronary stent placement? Postgrad Med. 2006;119:83-4. doi: 10.1080/00325481.2006.11446057. |
wrong publication type (Q&A) |
|
Sinitsyn VE, Stukalova OV, Kupriianova OM, Ternovoĭ SK. [Safety of magnetic resonance imaging after coronary stenting]. Kardiologiia. 2007;47:94-6. Russian. |
wrong publication (article in Russian) |
|
Sommer T, Maintz D, Schmiedel A, Hackenbroch M, Hofer U, Urbach H, Pavlidis C, Träber F, Schild H, Höher M. Hochfeld-Magnetresonanztomographie: Magnetische Anziehungs- und Rotationskräfte auf metallische Implantate bei 3.0 T [High field MR imaging: magnetic field interactions of aneurysm clips, coronary artery stents and iliac artery stents with a 3.0 Tesla MR system]. Rofo. 2004;176:731-8. German. doi: 10.1055/s-2004-812754. |
wrong publication (article in German) |
|
Symons R, Zimmerman SL, Bluemke DA. CMR and CT of the Patient With Cardiac Devices: Safety, Efficacy, and Optimization Strategies. JACC Cardiovasc Imaging. 2019;12:890-903. doi: 10.1016/j.jcmg.2018.09.030. |
wrong study design (no comparison) |
|
Tejedor-Viñuela P, San Román-Calvar JA, Durán-Hernández JM, Gómez-Salvador I, Sierra-Román J, Fernández-Avilés F. Seguridad de la realización precoz de un estudio de resonancia magnética cardiaca en pacientes con infarto agudo de miocardio y revascularización con stent [Safety of early cardiac magnetic resonance imaging in acute myocardial infarction patients with stents]. Rev Esp Cardiol. 2006 Dec;59(12):1261-7. Spanish. |
wrong publication (article in Spanish) |
|
Titterington B, Puschmann C, Shellock FG. A new vascular coupling device: assessment of MRI issues at 3-tesla. Magn Reson Imaging. 2014;32:585-9. doi: 10.1016/j.mri.2014.01.005. |
wrong study design (phantom study) |
|
Van Speybroeck CDE, O'Reilly T, Teeuwisse W, Arnold PM, Webb AG. Characterization of displacement forces and image artifacts in the presence of passive medical implants in low-field (<100 mT) permanent magnet-based MRI systems, and comparisons with clinical MRI systems. Phys Med. 2021;84:116-124. doi: 10.1016/j.ejmp.2021.04.003. |
wrong study design (no patients) |
|
von Knobelsdorff F, Bauer WR, Busch S, Eitel I, Jensen C, Marx N, Neizel-Wittke M, Radunski UK, Schuster A, Rolf A. Safety of non-active cardiovascular implants in MRI examinations: Update 2021: Statement of the German Cardiac Society ; Implantate - Kardiovaskular; 2021 |
wrong publication (article in German) |
|
Walsh EG, Brott BC, Johnson VY, Venugopalan R, Anayiotos A. Assessment of passive cardiovascular implant devices for MRI compatibility. Technol Health Care. 2008;16:233-45. |
wrong study design (no comparison) |
|
Walsh JJ, Huang Y, Simmons JW, Goodrich JA, McHugh B, Rothman DL, Elefteriades JA, Hyder F, Coman D. Dynamic Thermal Mapping of Localized Therapeutic Hypothermia in the Brain. J Neurotrauma. 2020;37:55-65. doi: 10.1089/neu.2019.6485. |
wrong study design (animal study) |
|
Yoon YE, Hong YJ, Kim HK, Kim JA, Na JO, Yang DH, Kim YJ, Choi EY. 2014 Korean guidelines for appropriate utilization of cardiovascular magnetic resonance imaging: a joint report of the Korean society of cardiology and the Korean society of radiology. Korean Circ J. 2014;44:359-85. doi: 10.4070/kcj.2014.44.6.359. |
wrong population (people without implants) |
Beoordelingsdatum en geldigheid
Publicatiedatum : 01-05-2024
Beoordeeld op geldigheid : 12-02-2026
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2022 een multidisciplinaire werkgroep samengesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij het opstellen van het beleid of het uitvoeren van een MRI bij patiënten met implantaten.
Werkgroep
- Dr. M.B.M. Hofman, klinisch fysicus, Nederlandse Vereniging voor Klinische Fysica (NVKF), voorzitter
- Prof. Dr. ir. C. van Pul, klinisch fysicus, Nederlandse Vereniging voor Klinische Fysica (NVKF)
- Dr. ir. A.L.H.M.W. van Lier, klinisch fysicus, Nederlandse Vereniging voor Klinische Fysica (NVKF)
- Dr. ir. B.J. van Nierop, klinisch fysicus, Nederlandse Vereniging voor Klinische Fysica (NVKF)
- Dr. J.P.A. Kuijer, klinisch fysicus, Nederlandse Vereniging voor Klinische Fysica (NVKF)
- Dr. N. De Jong, klinisch fysicus, Nederlandse Vereniging voor Klinische Fysica (NVKF)
- Dr. R. Keesman, klinisch fysicus in opleiding, Nederlandse Vereniging voor Klinische Fysica (NVKF)
- Prof.dr.ir. J.C.M. Smits, klinisch fysicus audioloog, Nederlandse Vereniging voor Klinische Fysica (NVKF)
- Dr. ir. E.P.A. Vonken, radioloog, Nederlandse Vereniging voor Radiologie (NVvR) (tot juli 2022)
- S.J.A.M. Soomers-Wanders, MBB-C, Nederlandse Vereniging Medische Beeldvorming en Radiotherapie (NVMBR)
- Prof. Dr. M. Meine, cardioloog, Nederlandse Vereniging voor Cardiologie (NVvC)
- Dr. A.M. Wiersema, vaatchirurg, Nederlandse Vereniging voor Vaatchirurgie (NVvV)
- G.M. Burgemeestre, Hartstimulatiespecialist, Vereniging voor Invasief Technische Hartstimulatie Specialisten (VITHaS)
- H. van Rees, Onafhankelijk Platform Cochleaire Implantatie (OPCI)
Klankbordgroep
- I.G.J. Verstraaten, MSc, Harteraad
- Dr. S. Muller, klinisch fysicus, Nederlandse Vereniging van Klinische Fysica (NVKF)
- Dr. T. Ruytenberg, klinisch fysicus, Nederlandse Vereniging voor Klinische Fysica (NVKF)
Met ondersteuning van
- Dr. I. van Dusseldorp, literatuurspecialist, Kennisinstituut van Federatie Medisch Specialisten
- Dr. N. van der Zwaluw, senior adviseur, Kennisinstituut van Federatie Medisch Specialisten
- Drs. A.E. Sussenbach, junior adviseur, Kennisinstituut van Federatie Medisch Specialisten
- Dr. E. Belfroid, adviseur, Kennisinstituut van Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Dr. M.B.M. Hofman |
Klinisch fysicus, Amsterdam UMC |
Geen |
Geen |
Geen actie vereist |
|
Prof. Dr. ir. C. van Pul |
Klinisch fysicus, Maxima Medisch Centrum |
Universitair HoofdDocent TU Eindhoven |
Geen |
Geen actie vereist |
|
Dr. ir. A.L.H.M.W. van Lier |
Klinisch fysicus, UMC Utrecht |
Lid IEC commissie 'Particular requirements for the basic safety and essential performance of MRI based image guided radiotherapy equipment for use with electron accelerators'; ITEA 3 - Signet - Sensing and Image-Guided Neurological therapies, cardiac Electrophysiology and Tumour treatments |
Geen |
Geen actie vereist |
|
Dr. ir. B.J. van Nierop |
Klinisch fysicus, RNG, UMC Utrecht |
Docent Intop zorgsector |
Geen |
Geen actie vereist |
|
Dr. J.P.A. Kuijer |
Klinisch fysicus, Amsterdam UMC |
Geen |
Geen |
Geen actie vereist |
|
Dr. N. De Jong |
Klinisch fysicus, LUMC |
Geen |
Geen |
Geen actie vereist |
|
Dr. R. Keesman |
Klinisch fysicus in opleiding, Radboudumc |
Contractor bij Cablon Medical B.V. voor Design & Development services |
Geen |
Geen actie vereist |
|
Prof.dr.ir. J.C.M. Smits |
Klinisch fysicus audioloog, Hoogleraar klinische en experimentele audiologie, Amsterdam UMC |
Audiological Advisory Council van Advanced Bionics, Advisory Board or Focus Group Participation |
Geen |
Geen actie vereist |
|
Dr. ir. E.P.A. Vonken |
Radioloog |
Geen |
Geen |
Geen actie vereist |
|
S.J.A.M. Soomers-Wanders |
MBB-C, Noordwest Ziekenhuisgroep |
Geen |
Geen |
Geen actie vereist |
|
Prof. Dr. M. Meine |
Cardioloog, UMC Utrecht |
Advise CRT-3 |
Geen |
Geen actie vereist |
|
Dr. A.M. Wiersema |
Chirurg loondienst Dijklander Ziekenhuis, werkzaam U Clinic spataderzorg |
ACTION-1 trial, ZonMw, Medtronic, DLZ, AUMC |
Geen |
Geen actie vereist |
|
G.M. Burgemeestre |
Hartstimulatiespecialist, Noordwest ziekenhuis groep |
Geen |
Geen |
Geen actie vereist |
|
H. van Rees |
Gepensioneerd, actief bij OPCI |
Geen |
Geen |
Geen actie vereist |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door deelname van OPCI aan de werkgroep en deelname van Harteraad aan de klankbordgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan OPCI en Harteraad en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Wkkgz & Kwalitatieve raming van mogelijke substantiële financiële gevolgen
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming blijkt dat er waarschijnlijk geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
|
Module |
Uitkomst kwalitatieve raming |
Toelichting |
|
Module MRI bij vasculaire stent |
geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 3.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II, Brouwers 2010).
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann 2013, Hultcrantz 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello 2016a, Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas 2017, Neumann 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die rand voorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open 2017;7(11):e018593. doi: 10.1136/bmjopen-2017-018593.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 28;353:i2016. doi: 10.1136/bmj.i2016.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016, 353:i2089. doi: 10.1136/bmj.i2089.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ 2010;182(18):E839-42. doi: 10.1503/cmaj.090449.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Tabel Zoekverantwoording Incidentdatabases
|
Database |
Zoektermen1 |
Totaal |
|
FDA Recalls database2
doorzocht op 25-1-2019 |
1 ‘MR’ OR ‘magnetic’ (329) 2 betreft implantaat en MRI (9) 3 betreft relevant implantaat voor deze module (0)
= 0 |
11 |
|
FDA Recalls database2
doorzocht op 9-12-2022 |
1 (‘MR’ OR ‘magnetic’) AND recall date from Jan. 25, 2019 (264) 2 betreft implantaat en MRI (12) 3 betreft relevant implantaat voor deze module (0)
= 0 |
|
|
IGJ database veiligheidsmeldingen3, 6 zonder restrictie op datum
doorzocht op 2-12-2022 |
1a ‘MR’ (93) 8 1b ‘MRI’ (99) 8 1c ‘magnetic’ (42) 2 betreft implantaat en MRI (5) 3 betreft relevant voor deze module (0)
= 0 |
|
|
IGZ archief4, 5
doorzocht op 17- en 29-1-2019 |
1a ‘MR’ (98) 1b ‘MRI’ (92) 1c ‘Magnetic’ (27) 2 betreft implantaat en MRI (0) 3 betreft relevant implantaat voor deze module (0)
= 0 |
|
|
FDA Medsun database7
doorzocht op 12 en 16-12-2022 |
1a1 Devicetype==MRI, date= 20/02/2002 till 12/12/2022 (61) 1a2 Geen van de hits bevat het woord ‘stent’ OF ‘graft’ (0) 1b1 Devicetype==graft, date= 20/02/2002 till 12/12/2022 (233) 1a2 Geen van de hits bevat het woord ‘MRI’ OF ‘magnetic’ (0), een (1) hit bevat de lettercombinatie ‘mr’, maar is niet relevant. 1c1 Devicetype==stent, date= 20/02/2002 till 12/12/2022 (632) 1c2 Geen van de hits bevat het woord ‘magnetic’, twee (2) hits bevatten de lettercombinatie ‘mr’, en een (1) ‘MRI’, maar zijn alle niet relevant.
= 0 |
|
|
FDA MAUDE database9
doorzocht op 12-2022 tot 1-2023 |
1a melding bevat tekst ‘like MRI’ AND (‘like stent’ OR ‘like graft’) (4273) 1b mogelijk relevant (19) Na lezen volledige melding mogelijk relevant (11), waarvan voor opwarming (7), dislocatie (3), en aantrekking (1).
= 1110 |
1 De databases hebben beperkte en onderling verschillende mogelijkheden om deze te doorzoeken. Gekozen is voor de zoek strategieën via MRI. Daarna zijn alle hits hierop na stap 1 gelezen en beoordeeld of ze een implantaat betreffen, en vervolgens of het implantaat relevant is voor deze module. Daarnaast hebben de databases beperkingen, een voorbeeld hiervan is dat een MRI gerelateerde melding van een implantaat uit de database van IGZ niet wordt gevonden in de FDA database omdat aldaar de link naar MRI is weggevallen.
2 https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfres/res.cfm.
3 https://www.igj.nl/onderwerpen/waarschuwingen-medische-hulpmiddelen/documenten.
4 https://igj.archiefweb.eu/?subsite=igz#archive.
5 Deze database is niet opnieuw doorzocht, omdat sinds de vorige query geen nieuwe entries zijn toegevoegd.
6 Het blijkt dat bij een query in de IGJ database uitgevoerd op 2 december 2022 met als datum tot=30 januari 2019 en als zoekterm=MRI méér hits gevonden worden dan met de query zoekterm=MRI uitgevoerd op 29 januari 2019. Kennelijk zijn er sindsdien nog meldingen toegevoegd met een datum eerder dan 30 januari 2019. De eerdere queries zijn daarom herhaald (zonder ‘datum vanaf’).
7 https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/medsun/searchreporttext.cfm
8 Query resultaat van de IGJ database met als zoekterm ‘MR’ vindt niet de entries met daarin ‘MRI’, tenzij ‘MR’ en ‘MRI’ beide voorkomen. Dit gaf aanleiding tot enkele dubbelingen, en in totaal 180 unieke entries.
10 MDR report keys: 3571873, 1963295, 453210, 6959864, 2144543, 2158496, 3230222, 3236593, 682070, 7273667, 12728921.