Nabehandeling flexorpeesletsel zone 1,2 en 3
Uitgangsvraag
Op welke wijze dient een geopereerd flexorpeesletsel in zone 1, 2 of 3 te worden nabehandeld?
Aanbeveling
Volwassenen en kinderen vanaf 10 jaar
- Houd bij de keuze van de nabehandeling rekening met:
- of een patiënt gemotiveerd is;
- of een patiënt in staat is de nabehandeling te volgen;
- de wensen en doelen van de patiënt;
- het werk dat patiënt verricht.
- Start bij voorkeur een ‘early active’ protocol tussen dag 3 en 5 na een operatief herstel van zone 1, 2 of 3 flexorpeesletsel binnen een beperkte range (totale range of motion: eenderde tot een halve vuist).
- Indien voor een ‘early active‘ protocol wordt gekozen, dient deze door een handtherapeut* te worden uitgevoerd.
Kinderen in de leeftijd van 0 tot en met 5 jaar
- Immobiliseer de geopereerde hand gedurende 4-6 weken.
Kinderen in de leeftijd van 6 tot 10 jaar
- Immobiliseer de geopereerde hand gedurende 4-6 weken en combineer dit eventueel met early active nabehandelen van de georpereerde pees tijdens therapiebezoek. Betrek hierbij het kind en de verzorgende(n) in de keuze van de nabehandeling.
* zie de ‘definities en begrippen’ bij de aanverwante producten
Overwegingen
Kwaliteit van bewijs
De kwaliteit van bewijs is matig tot (zeer) laag voor zowel de wenselijke effecten (verbetering range of motion, patiënttevredenheid, terugkeer naar werk) als voor de onwenselijke effecten (rupturen) en kosten.
Waarden en voorkeuren van patiënten
Volgens de werkgroep hebben veel (volwassen) patiënten een voorkeur voor de ‘early active’ nabehandeling vanwege de kortere duur ervan, een beter functioneel resultaat, en eerdere terugkeer naar werk. Ook de grotere patiënttevredenheid wijst in deze richting. Uiteraard kunnen patiënten wel verschillen in hun mogelijkheden tot compliance aan een van beide protocollen.
Professioneel perspectief
Essentieel voor het toepassen van een ‘early active’ nabehandeling is dat 3-5 dagen na de ingreep wordt gestart met actieve flexie (Trumble et al., 2010; Tang, 2015). De flexie dient in de eerste 2-3 weken binnen een derde tot de helft van de totale range of motion te blijven. Deze adviezen zijn voor een belangrijk deel gebaseerd op dierexperimenteel en biomechanisch onderzoek (Cao & Tang, 2006; Zhao et al., 2005; Halikis et al., 1997).
Voor het immobiliseren van jonge kinderen pleiten de resultaten van onderzoek van Sikora, Lai & Arneja (2013) die aannemelijk maakten dat bij kinderen van gemiddeld 8 jaar oud die gedurende 4 weken werden geïmmobiliseerd, functionele uitkomsten niet achteruit gingen. Ander onderzoek (Al-Qattan, 2014) liet zien dat ook een gemodificeerde ‘early active’ nabehandeling onder supervisie van een handtherapeut veilig kan zijn, mits tussen de afspraken de vingers worden geïmmobiliseerd.
Postoperatieve spalk
Bij een flexorpeesletsel in zone 1, 2 of 3 die met early active wordt nabehandeld, wordt om de frictie voor de pees te verminderen de postoperatieve spalk bij voorkeur in een lichte MCP flexie gezet (ongeveer 25-30 graden) en de stand van de pols is in lichte extensie (30 graden).
Verklevingen
De verklevingen die kunnen ontstaan zijn verbonden aan een stugge peeskoker die weinig mee geeft wat ernstige belemmering oplevert voor de excursie van de pees. Als beide pezen zijn betrokken bij het letsel bestaan naast verklevingen aan de huid ook regelmatig verklevingen tussen de FDS en FDP pezen omdat deze dicht op elkaar liggen in deze zones, vooral wanneer de pezen de carpale tunnel ingaan. Dit geeft functioneel soms problemen met het bereiken van een volledige vuist, omdat de FDP niet verder door kan glijden naar proximaal bij de eindfase van deze beweging. Omgekeerd geldt dit ook voor het behalen van volledige extensie hoewel dit minder vaak voorkomt. Vroeg mobiliseren van de pezen middels actief aanspannen is belangrijk voor het voorkomen van verklevingen.
Kosten
Bij de ‘early passive’ nabehandeling worden patiënten vaak tweemaal per week gezien. Dat is bij ‘early active’ niet altijd nodig. De spalken zijn bij ‘early active’ nabehandeling eenvoudiger wat betreft materiaal en grootte. Daarmee zijn ze goedkoper en zijn daarnaast ook nog veel prettiger voor de patiënt. De tijd in therapie is korter bij een ‘early active’ nabehandeling. Kortom, per saldo bespaart een ‘early active’ nabehandeling. Ook het gegeven dat men mogelijk sneller aan het werk kan bij een ‘early active’ nabehandeling, impliceert een kostenbesparing.
Balans van gunstige en ongunstige effecten
De wenselijke effecten (verbetering range of motion, patiënttevredenheid, terugkeer naar werk) afwegend tegen de onwenselijke effecten (rupturen) en kosten lijkt de balans ten gunste van de ‘early active’ nabehandeling uit te vallen.
Aanvaardbaarheid en haalbaarheid
Ervaren therapeuten zijn voorstander van de ‘early active’ nabehandeling omdat je patiëntgericht, kunt werken, d.w.z. de behandeling meer kunt toespitsen op de situatie van de individuele patiënt. Dit in tegenstelling tot passief, dynamisch nabehandelen. Dit laatste is namelijk gebaseerd op een protocol met standaardoefeningen die per week worden beschreven. Een early active benadering vraagt om specifieke kennis en ervaring met nabehandeling van peesletsel in de hand. Deze early active benadering dient dan ook te gebeuren door een handtherapeut. Deze heeft ervaring in de early active nabehandeling, bestaande uit het maken en aanpassen van de spalk, en het geven van oefeningen, gedurende het hele revalidatie traject.
Rationale voor de aanbeveling
Bij het opstellen van de aanbeveling is groot gewicht toegekend aan het feit dat ‘early active’ nabehandeling een vroegere terugkeer naar werk mogelijk lijkt te maken, tot een mogelijk grotere patiënttevredenheid en een grotere range of motion leidt, en recent onderzoek niet wijst op een grotere kans op een ruptuur bij toepassen van ‘early active’ nabehandeling. Er is minder gewicht toegekend aan de kosten.
Onderbouwing
Bij de nabehandeling van een gehechte flexorpees bestaan drie problemen, of gapping, óf een peesruptuur, óf verklevingen waardoor de pees niet kan glijden met als gevolg functieverlies. Met het oog op deze postoperatieve uitdaging zijn verschillende protocollen door de jaren heen verschenen.
‘Early passive’ protocollen; Kleinert/Duran
Uit onderzoek in de jaren zeventig bleek dat vroeg bewegen van een gehechte pees verklevingen kon voorkomen. De twee belangrijkste protocollen die in 1975 werden gepubliceerd waren van Kleinert en Duran & Houser. Veel van de feiten waarop deze twee oorspronkelijke protocollen waren gebaseerd, bleken twijfelachtig wat wetenschappelijke onderbouwing betreft.
Beide protocollen houden bijvoorbeeld de pols in flexie om spanning op de peesnaad te verminderen. Deze gekozen polspositie bleek echter niet te zijn gebaseerd op onderzoek. In 1988 beschreef Savage dat juist pols extensie de meest gunstige stand is.
Dynamische tractie middels elastiekjes wordt gebruikt om de vinger passief te flecteren na actieve strekking van de vinger. Hierdoor worden deze protocollen vaak als ‘actief’ nabehandelen beschreven, dit is echter onjuist. De gehechte flexorpezen worden door vingerextensie passief naar distaal getrokken. De (passieve) vingerflexie middels het elastiek zou de gehechte pees naar proximaal doen glijden, maar dit is nooit bewezen. De resultaten waren wel beter dan met immobilisatie. Omdat de pees passief wordt bewogen, is de belasting op de pees niet te groot en de kans op rupturen klein. Het nadeel is het ontstaan van verklevingen of flexiecontracturen. Deze veroorzaakten op hun beurt een verminderde bewegingsuitslag met secundaire chirurgie als gevolg in de vorm van tenolyses, capsulolyses of littekencorrecties.
‘Early active’ protocollen
In tegenstelling tot passief nabehandelen, wordt de pees bij ‘early-active’ nabehandelen wel actief aangespannen. Actief nabehandelen werd al sinds 1987 gedaan in de USA (Allen et al., 1987) en in de UK vanaf 1989 (Cullen et al, 1989; Small et al., 1989). De resultaten waren veelbelovend omdat minder verklevingen voorkwamen. Helaas kwamen vaker rupturen voor waardoor behandelaars lang terughoudend waren om voor actief nabehandelen te kiezen. Betere hechtmaterialen en hechttechnieken geven nu meer vertrouwen in actief belasten. Daarnaast heeft wetenschappelijk onderzoek gezorgd voor een goede onderbouwing van veilig actief aanspannen (Tang et al., 2007; Amadio et al., 2005). Bij actief aanspannen is het in de eerste 3-4 postoperatieve weken belangrijk dat dit met minimale kracht gebeurt. Er dient voorzichtig en gecontroleerd te worden aangespannen. Sommige auteurs prefereren de “place-hold” techniek en anderen verkiezen de “1/3” of halve vuist waarbij in een beperkte range mag worden bewogen. Ten opzichte van de passieve methode is de uitgangshouding in de postoperatieve spalk veranderd. Deze aanpassingen werden gedaan om de weerstand tegen flexie (work of flexion) bij actief aanspannen te verminderen (Amadio et al., 2006). Zo is vooral de stand van de metacarpale gewrichten verkleind van 60-70 graden naar 25-30 graden om de WOF te verminderen (Kursa et al., 2006; Tang et al., 2003 en 2007).
Definities:
Early active: actief buigen en actief strekken gedurende eerste weken na flexorpeesherstel.
Early passive: passief buigen met actief of passief strekken gedurende eerste weken na flexorpeesherstel (Pettengill, 2005).
|
Laag tot Matig GRADE |
Patiënten die geopereerd zijn aan een flexorpeesletsel van zone 1, 2, 3
Range of motion
Een ‘early active’ mobilisatietechniek lijkt te resulteren in een grotere range of motion dan een ‘early passive’ mobilisatietechniek.
Bronnen Trumble et al. (2010); Frueh et al. (2014) [zone 1/2]; Farzad et al. (2014); Bainbridge et al. (1994) [zone 1/2]; Baktir et al. (1996); Peck et al. (1998); Yen et al. (2008) |
|
Zeer laag tot laag GRADE |
Patiënten die geopereerd zijn aan een flexorpeesletsel van zone 1, 2, 3
Ruptuur
Het is onduidelijk of een ‘early active’ mobilisatietechniek een groter of kleiner risico op rupturen heeft dan een ‘early passive’ mobilisatietechniek.
Bronnen Trumble et al. (2010); Frueh et al. (2014) [zone 1/2]; Farzad et al. (2014); Bainbridge et al. (1994) [zone 1/2]; Baktir et al. (1996); Peck et al. (1998); Yen et al. (2008) |
|
Laag GRADE |
Patiënten die geopereerd zijn aan een flexorpeesletsel van zone 1, 2, 3
Terugkeer naar werk
Patiënten lijken weer sneller aan het werk te zijn met een early active’ mobilisatietechniek als nabehandeling dan met een ‘early passive’ mobilisatietechniek.
Bron Trumble et al. (2010) |
|
Zeer Laag GRADE |
Patiënten die geopereerd zijn aan een flexorpeesletsel van zone 1, 2, 3
Patiënttevredenheid
Patiënten lijken meer tevreden te zijn bij een early active’ mobilisatietechniek als nabehandeling dan bij een ‘early passive’ mobilisatietechniek.
Bron Trumble et al. (2010) |
|
Zeer laag GRADE |
Patiënten die geopereerd zijn aan een flexorpeesletsel van zone 1, 2, 3
Kosten
Een ‘early active’ mobilisatietechniek is mogelijk minder duur dan een ‘early passive’ mobilisatietechniek.
Bron Trumble et al. (2010) |
Meta-analyse van gerandomiseerde, gecontroleerde trials
Trumble et al. (2010) en Farzad et al. (2014) pasten als ‘early active’ mobilisatietechniek de actieve ‘place-and-hold’ techniek toe. Farzad et al. (2014) includeerden 64 vingers (54 patiënten) in zone 2, Trumble et al. (2010) 119 vingers (103 patiënten). Farzad et al. (2014) gebruikten een ‘two strand’ hechttechniek met epitendineuze voortlopende hechting, Trumble et al. (2010) een ‘four strand’ hechttechniek met epitendineuze hechting. De follow-up duur bedroeg 8 weken (Fazad et al., 2014) respectievelijk 52 weken (Trumble et al., 2010). Andere karakteristieken van de gevonden studies zijn opgenomen in de evidence tabellen.
Combineren van de uitkomsten (rupturen en range of motion) van beide RCTs laat zien dat de ‘early active’ nabehandeling een grotere range of motion geeft dan de ‘early passive’ nabehandeling, zonder tot meer rupturen te leiden (figuur 1a en figuur 1b). Het verschil in range of motion bedraagt minimaal 20.3°.
Figuur 1a. Mean difference ‘range of motion’; ‘early active’ versus ‘early passive’ mobilisatietechniek; follow-up duur: 8 – 52 weken (gerandomiseerde studies) voor zone 2 flexorpeesletsel

Opmerking: random effects meta-analyse
Figuur 1b. Odds ratio: ruptuur; ‘early active’ versus ‘early passive’ mobilisatietechniek; follow-up duur: 8 – 52 weken (gerandomiseerde studies) voor zone 2 flexorpeesletsel

Opmerking: random effects meta-analyse.
Trumble et al. (2010) onderzochten ook het effect van de twee mobilisatietechnieken op terugkeer naar werk, patiënttevredenheid en kosten. De aard van het werk werd in het artikel van Trumble et al. (2010) niet benoemd (13 patiënten hadden in de early active groep een workers compensation claim en 10 in de early passive groep).
Patiënten in de ‘early active’ groep namen na gemiddeld 82 dagen hun werkzaamheden weer op. In de ‘early passive’ groep was dit gemiddeld na 103 dagen (p < 0.05). Trumble et al. (2010) vermeldden niet wat de standaardafwijking was.
De patiënttevredenheid (score 1 tot 10; hoger is meer tevreden) was in de ‘early active’ groep 9.4 (sd: 4.3) en in de ‘early passive’ groep 8.2 (sd: 3.9; p < 0.05).
De totale kosten (kosten van chirurgie, therapie en postoperatieve medicatie samen) per patiënt verschilden niet statistisch significant: $14,720 voor de ‘early passive’ benadering en $12,360 voor de ‘early active’ benadering. Dat de kosten voor de ‘early passive’ benadering wat hoger uitvallen heeft daarmee te maken dat de ‘early passive’ nabehandeling 16 weken vergde en de ‘early active’ nabehandeling 12 weken.
Meta-analyse van vergelijkende observationele studies
Van de vijf studies die hieronder kort samengevat worden, hebben twee studies (Frueh et al., 2014; Bainbridge et al., 1994) mede betrekking op zone 1 flexorpeesletsel.
Frueh et al. (2014) omschrijven hun ‘early active’ protocol als ‘controlled active motion’. Frueh et al. includeerden ook vingers uit zone 1 (n=66). Zij includeerden in totaal 159 vingers (132 patiënten). De follow-up duur was 12 weken. Frueh et al. (2014) gebruikten bij 85% van de patiënten een ‘four strand’ hechttechniek en bij 15% een two- of six-strand hechttechniek met epitendineuze circumferentiële hechting. Bainbridge et al. (1994) includeerden 108 patiënten (135 vingers), en omschrijven hun ‘early active’ mobilisatietechniek als ‘controlled active motion’. De follow-up duur was vier maanden. Baktir et al. (1996) includeerden 71 patiënten. De follow-up duur was 12 maanden. Peck et al. includeerden 52 patiënten (52 vingers), en omschreven hun ‘early active’ protocol als ‘controlled active motion’. De follow-up duur was 12 weken. Yen et al. (2008) includeerden 20 patiënten, en maakten gebruik van place-and-hold bij de ‘early active’ mobilisatietechniek. De follow-up duur was 4 maanden.
Combineren van uitkomsten van deze vijf studies laten de volgende effecten zien (figuur 2a en 2b). De ‘early active’ mobilisatietechniek geeft een grotere kans op een excellent/goed functioneel resultaat dan de ‘early passive’ mobilisatietechniek (Odds ratio: 2.44). Anderzijds is de kans op een ruptuur groter bij toepassen van een ‘early active’ mobilisatietechniek (Odds ratio: 2.22). Hierbij moet wel worden opgemerkt dat er onder de vijf studies drie bij zijn die juist een kleiner risico op een ruptuur laten zien.
Figuur 2a. Functioneel resultaat (excellent en goed); ‘early active’ versus ‘early passive’ mobilisatietechniek; follow-up duur: 12-52 weken (observationele studies) voor zone 1 en 2 flexorpeesletsel
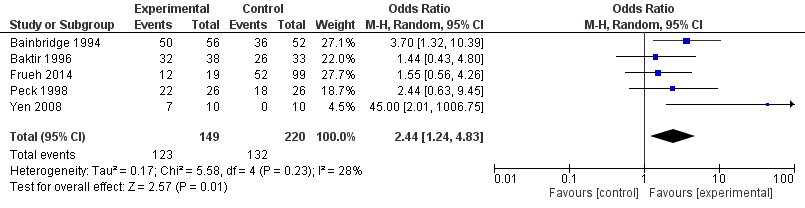
Figuur 2b. Ruptuurrisico ‘early active’ versus ‘early passive’ mobilisatietechniek; follow-up duur 12-52 weken (observationele studies) voor zone 1 en 2 flexorpeesletsel

Frueh et al. (2014) rapporteerden ook over postoperatieve wondinfecties. Op een totaal van 159 vingers zagen zij één postoperatieve infectie. Verder zagen zij geen statistisch significant verschil in de resultaten van het flexorpeesherstel tussen de zones 1 en 2, zonder overigens nadere details (percentage rupturen, ‘total active motion’ etc.) te verstrekken. Bainbridge et al. (1994) zagen geen statistisch significant verschil in functioneel resultaat (goed/excellent volgens Buck-Gramcko classificatie) tussen zone 1 en zone 2.
Kwaliteit van bewijs
Bewijs met betrekking tot gewenste (verbeterde functie; eerdere hervatting van werk en grotere patiënttevredenheid) en ongewenste (rupturen) effecten
=Gerandomiseerde studies=
De kwaliteit van bewijs voor de uitkomstmaat functie is matig vanwege beperkingen in opzet en uitvoering van de studies (waaronder korte follow-up duur en geen blindering van de beoordelaar van de uitkomsten), en zeer laag voor de uitkomstmaat ruptuur om de bijkomende reden van grote onnauwkeurigheid van het geschatte effect.
De kwaliteit van bewijs voor de uitkomstmaten hervatting van werk en patiënttevredenheid is (zeer) laag vanwege de hiervoor genoemde redenen.
=Observationele studies=
Hoewel de studies wijzen op een relatief groot effect (Odds ratio: 2.44) van een ‘early active’ mobilisatietechniek op functionele uitkomsten, is het niet mogelijk om de kwaliteit van bewijs op te waarderen van laag naar matig. De ondergrens van het betrouwbaarheidsinterval laat namelijk zien dat ook sprake kan zijn van een klein effect (Odds ratio: 1.24). Daarbij komt dat een zeer lage kwaliteit van bewijs bestaat voor het risico op een ruptuur vanwege onnauwkeurigheid van het geschatte effect.
In twee observationele studies (Frueh et al., 2014; Bainbridge et al., 1994) werden, naast patiënten met zone 2 flexorpeesletsel, patiënten met zone 1 flexorpeesletsel geïncludeerd. Beide studies rapporteerden de resultaten niet afzonderlijk voor beide zones. Statistische analyse wees volgens de onderzoekers echter uit dat de resultaten niet significant verschilden voor beide zones. De commissie meent daarom dat de resultaten van de studies met betrekking tot nabehandeling van zone 2 flexorpeesletsel toepasbaar zijn voor zone 1. Er werd dan ook niet afgewaardeerd voor ‘indirect bewijs’.
Hoewel geen vergelijkende studies over nabehandeling van patiënten met zone 3 en 4 flexorpeesletsel werden gevonden, meent de commissie in navolging van Boyes (1964) dat de resultaten van de studies met patiënten met zone 2 flexorpeesletsel geëxtrapoleerd kunnen worden naar zone 3 en 4. De argumentatie hiervoor is dat de peesexcursie van een flexorpees welliswaar groter is in zone 3 dan de peesexcursie in zone 2, maar het voorkomen van verklevingen, ondanks dat er geen peeskoker is, dezelfde prioriteit heeft in zone 3 als in zone 2. Er werd dan ook niet afgewaardeerd voor ‘indirect bewijs’”.
Om de uitgangsvraag te kunnen beantwoorden heeft de werkgroep een systematische review gepland met de volgende PICO-vraagstelling:
Wat is het effect van een ‘early active’ mobilisatietechniek versus een ‘early passive’ mobilisatietechniek op de in onderstaande tabel genoemde uitkomstmaten bij kinderen en volwassenen die geopereerd zijn voor een flexorpeesletsel in zone 1, 2 of 3?
Selectiecriteria:
|
Type studies |
|
|
Type patiënten |
|
|
Interventie |
|
|
Type uitkomstmaten |
|
|
Type setting |
|
|
Exclusiecriteria |
|
Uitgangspunt voor de literatuursearch was de systematische review van Starr et al. (2013). Hierin zijn 5 vergelijkende studies opgenomen die werden gepubliceerd vanaf 1980 tot en met 2011 (Trumble et al, 2010; Bainbridge et al, 1994; Baktir et al, 1996, Peck et al, 1998; en Yen et al, 2008). Deze studies vergeleken alle ‘early active’ met ‘early passive’ nabehandeling.
Ter informatie: de review van Starr is niet geïncludeerd, omdat de auteurs in hun analyses geen onderscheid maakten tussen patiëntenseries en vergelijkend onderzoek.
Bij wijze van update van Starr et al. (2013) werd d.d. 2 februari 2016 een search verricht in PubMed en Cochrane Library (CDSR en Central) naar studies over zone 1 of 2 die vanaf 2012 werden gepubliceerd. Voor deze update werd gebruik gemaakt van de zoekstrategie die in deze review werd gehanteerd. Er werden in totaal 43 studies gevonden, waarvan twee aan de inclusiecriteria voldeden (Frueh et al., 2014; Farzad et al., 2014). Frueh et al. (2014) betreft een vergelijkende observationele studie, Farzad et al. (2014) betreft een randomised controlled trial. Zie ook de zoekstrategie.
Farzad et al. (2014) includeerden kinderen vanaf 12 jaar, Frueh et al. (2014) adolescenten vanaf 16 jaar, en Trumble et al. (2010) adolescenten vanaf 15 jaar. Er werden dus geen vergelijkende studies gevonden over kinderen onder de 12 jaar.
Voor de meeste vergelijkende studies in Starr et al, en voor de studies die via de literatuursearch werden gevonden geldt dat ze nabehandeling van zone 2 flexorpeesletsel betreffen, en in enkele gevallen een combinatie van zone 1 en zone 2 flexorpeesletsel.
Op 13 maart 2016 werd een sensitieve search verricht in PubMed naar studies over nabehandeling van zone 3 flexorpeesletsel. Hiervoor werd de zoekstrategie van Starr et al. geadapteerd. Zie ook de zoekstrategie. Geen van de 96 studies die werden gevonden, voldeed aan de inclusiecriteria. Een zoekactie in CSDR en CENTRAL leverde geen relevante studie op.
- Allen BN, Frykman GK, Unsell RS, Wood VE. Ruptured flexor tendon tenorrhaphies in zone II: repair and rehabilitation. J Hand Surg Am. 1987 Jan;12(1):18-21.
- Al-Qattan MM. Flexor tendon injuries in the child. J Hand Surg Eur Vol. 2014 Jan;39(1):46-53.
- Amadio PC. Friction of the gliding surface. Implications for tendon surgery and rehabilitation. J Hand Ther. 2005 Apr-Jun;18(2):112-9.
- Bainbridge LC, Robertson C, Gillies D, et al. A comparison of post-operative mobilization of flexor tendon repairs with passive flexion-active extension and controlled active motion techniques. J Hand Surg Br. 1994;19(4):517521.
- Baktir A, Türk CY, Kabak S, et al. Flexor tendon repair in zone 2 followed by early active mobilization. J Hand Surg Br. 1996;21(5): 624628.
- Boyes, Joseph H. Bunnell's Surgery of the Hand, 1964 4th Edition.
- Cao Y, Tang JB. Resistance to motion of flexor tendons and digital edema: An in vivo study in a chicken model. J Hand Surg Am. 2006 Dec;31(10):1645-51.
- Cullen KW, Tolhurst P, Lang D, Page RE. Flexor tendon repair in zone 2 followed by controlled active mobilisation. J Hand Surg Br. 1989 Nov;14(4):392-5.
- Farzad M, Layeghi F, Asgari A, Ring DC, Karimlou M, Hosseini SA. A prospective randomized controlled trial of controlled passive mobilization vs. place and active hold exercises after zone 2 flexor tendon repair. Hand Surg. 2014;19(1):53-9.
- Frueh FS, Kunz VS, Gravestock IJ, Held L, Haefeli M, Giovanoli P, Calcagni M. Primary flexor tendon repair in zones 1 and 2: early passive mobilization versus controlled active motion. J Hand Surg Am. 2014 Jul;39(7):1344-50.
- Halikis MN, Manske PR, Kubota H, Aoki M. Effect of immobilization, immediate mobilization, and delayed mobilization on the resistance to digital flexion using a tendon injury model. J Hand Surg Am. 1997 May;22(3):464-72.
- Peck FH, Bücher CA, Watson JS, et al. A comparative study of two methods of controlled mobilization of flexor tendon repairs in zone 2. J Hand Surg Br. 1998;23(1):41 45.
- Pettengill KM. The evolution of early mobilization of the repaired flexor tendon. J Hand Ther. 2005 Apr-Jun;18(2):157-68.
- Small JO, Brennen MD, Colville J. Early active mobilisation following flexor tendon repair in zone 2. J Hand Surg Br. 1989 Nov;14(4):383-91.
- Starr HM, Snoddy M, Hammond KE, Seiler JG 3rd. Flexor tendon repair rehabilitation protocols: a systematic review. J Hand Surg Am. 2013 Sep;38(9):1712-7.e1-14.
- Tang JB. Indications, methods, postoperative motion and outcome evaluation of primary flexor tendon repairs in Zone 2. J Hand Surg Eur Vol. 2007 Apr;32(2):118-29.
- Tang JB. Wide-Awake Primary Flexor Tendon Repair, Tenolysis, and Tendon Transfer. Clin Orthop Surg. 2015 Sep;7(3):275-81. doi: 10.4055/cios.2015.7.3.275. Epub 2015 Aug 13. Review.
- Trumble TE, Vedder NB, Seiler JG 3rd, Hanel DP, Diao E, Pettrone S. Zone-II flexor tendon repair: a randomized prospective trial of active place-and-hold therapy compared with passive motion therapy. J Bone Joint Surg Am. 2010 Jun;92(6):1381-9.
- Yen CH, Chan WL, Wong JW, et al. Clinical results of early active mobilisation after flexor tendon repair. Hand Surg. 2008;13(1): 4550.
- Zhao C, Amadio PC, Tanaka T, Yang C, Ettema AM, Zobitz ME, An KN. Short-term assessment of optimal timing for postoperative rehabilitation after flexor digitorum profundus tendon repair in a canine model. J Hand Ther. 2005 Jul-Sep;18(3):322-9.
|
Study id |
Study design |
Number of patients |
Rehabilitation method |
Time From Injury to Surgery Splint Type Total Time Splinted Follow-Up |
Core Suture Repair Method—Suture Size and Material No. Strand Repair |
Functional Results (Classification System) |
Complications Comments on Complications in Multiple-Digit vs Single-Digit Injuries |
Methodological quality |
|
Trumble 2010 |
RCT |
103 patients, 119 digits in zone 2 |
Passive motion—51 patients with 58 digits Active motion with place and-hold—52 patients with 61 digits |
Repaired within 48 h of injury No splint details 6 wk Follow-up at 6, 12, 26, and 52 wk |
FDP: Strickland method—2 core sutures of 3-0 polyester and 6-0 Prolene epitendinous FDS: simple Kessler with 3-0 polyester 4-strand repair |
Strickland: Active motion: IP joint motion was 156° ± 25° with 94% good–excellent Passive motion: IP jointmotion was 128° ± 22°, with 62% good–excellent |
Passive motion: 2 ruptures Active motion: 2 ruptures Six patients with multiple-digit injuries included in each group. Patients with multiple-digit injuries had overall worse outcomes in both groups |
Random sequence generation: adequate Allocation concealment: adequate Blinding of participants & personnel: not blinded Blinding of outcome assessor: not blinded Incomplete outcome data: adequately reported Selective reporting: not suspected Other bias: not suspected |
|
Farzad 2014 |
RCT |
54 patients, 64 digits in zone 2 |
Passive motion - (actively extend the fingers to the dorsal blocking splint, at least 10 repetitions every waking hour for 21 days). |
Less than or greater than 48 hours dorsal static splint 3 wk Follow-up at 8 wk |
FDP: (Time to surgery was categorized as less than or greater than 48 hours). |
Strickland: Active:
Passive: |
No ruptures in either active or passive group |
Random sequence generation: adequate Allocation concealment: unclear Blinding of participants & personnel: not blinded Blinding of outcome assessor: adequate Incomplete outcome data: adequately reported Selective reporting: not suspected Other bias: very short follow-up period |
|
Frueh 2014 |
Retrospective observational study |
191 patients with 231 injured digits |
Passive motion – 138 fingers Early active - 21 fingers
(132 patients)
|
Time From Injury to Surgery unknown Splint type unknown Follow-up at 4, 12 wk |
4-strand core suture with locking loops. Suture material 4-0 or 3-0 polyester braid containing a long chain polyetylene core. Fifteen percent of the tendons were repaired using other suture technique (2-strand or 6-strand). Circumferential epitendinous locking suture was performed with 6-0 polypropylene. |
Passive motion – Excellent: 8% Good: 45%
Active motion – Excellent: 0% Good: 65% |
Passive motion: 1 rupture (5%) Active motion: 10 ruptures (7%). 29 patients with adhesions and unsatisfactory reoperated with tenolysis and inpatient hospitalization for immediate hand therapy. 1 postoperative infection |
Very serious risk of bias: no randomisation, no blinding of personnel and outcome assessors. |
|
Bainbridge 1994 |
Prospec-tive, com-parative cohort study |
Group 1: Group 2: |
Group 1: passive flexion–active extension Group 2: controlled active motion |
Group 1: dorsal splint with wrist in 30° flexion, MCPs in 90° flexion, and IPs in neutral Group 2: dorsal splint with wrist in 30° flexion, MCPs in 90° flexion, and IPs in full extension 6 wk Follow-up at 4 mo |
FDP: modified Kessler suture of 3-0 or 4-0 Prolene with epitendinous 6-0 nylon or Prolene FDS: 4-0 or 5-0 horizontal mattress sutures of either nylon or Prolene 2-strand repair |
Group 1: zone I: 90% good–excellent zone 2: 50% good–excellent Group 2: zone I: 89% good–excellent zone 2: 90% good–excellent |
Group 1: Group 2: |
observational study: low QoE |
|
Baktir 1996 |
Prospec-tive, com-parative cohort study |
71 patients Zone 2 |
Group 1: Kleinert rubber band passive flexion/active extension method Group 2: early active mobilization |
58 tendons repaired within 12 h, 13 tendons repaired within 2 wk (does not state whether hours from injury or from presentation) Group 1: dorsal splintwith wrist in 30° to 40° flexion, MCPs in 70° to 90° flexion, and IPs in full extension Group 2: dorsal splint with wrist in 0° flexion, MCPs in 70° to 90° flexion, and IPs in full extension 6 wk Follow-up at 1 y |
FDP: modified Kessler—4-0 braided polyesterand epitendinous 6-0 Prolene FDS: horizontal mattress sutures—4-0 braidedpolyester 2-strand repair |
Passive flexion group: 78% good–excellent and 84% mean grip strength Active mobilization group: 85% good–excellent and 90% mean grip strength |
2 ruptures in each group Extensor deficit: 10 in Kleinert 5 in early active mobilization No difference in results from multiple tendon injuries in same hand or whether FDP or both FDP and FDS tendons were injured |
observational study: low QoE |
|
Peck 1998 |
Prospec-tive, com-parative cohort study |
52 patients, 52 digits, Zone 2 |
Group 1: controlled active motion—26 patients Group 2: modified Kleinert regime—26 patients |
Repaired within 24 h of injury Group1: thermoplastic dorsalsplint with wrist in 40° flexion, MCPs in 60° flexion, and IPs in neutral Group 2: thermoplastic dorsal splint with wrist in 40°flexion, MCPs in 60° flexion, and IPs in neutral 6 wk Follow-up at 12 wk |
FDP: modified Kessler—3-0 Prolene and 6-0 nylon or Prolene epitendinous FDS: horizontal mattress with 6-0 Prolene. 2-strand repair |
Group 1: 85% good–excellent Group 2: 69% good–excellent |
Group 1: Group 2: |
observational study: low QoE |
|
Yen 2008 |
Prospective, comparative cohort study |
20 patients Zone 2 |
Active extension, active place-and-hold—10 patients Kleinert method—10 patients |
Not described Dorsal splint with wrist in 30° flexion, MCPs in 70° flexion, and IPs in full extension 6 wk Follow-up at 4 mo |
4-0 Prolene core sutures plus 6-0 Prolene circumferential sutures 4-strand repair |
Active motion: 70% good–excellent Kleinert splint: 0% good–excellent |
Active place and hold: 0 complications Kleinert splint: 1 rupture |
observational study: low QoE |
Randomised studies
|
|
Initial quality of eviden-ce |
Study design |
Risk of bias |
Indirectness |
Inconsistency |
Imprecision |
Publication bias |
Quality of evidence |
|
Function |
||||||||
|
Trumble et al.; Farzad et al. |
High |
RCT |
Serious1 |
Not serious7 |
Not serious |
Not serious6 |
Not suspected |
Moderate |
|
Ruptures |
||||||||
|
Trumble et al.; Farzad et al. |
High |
RCT |
Serious1 |
Not serious7 |
Not serious |
Very serious2 |
Not suspected |
Very low |
|
Return to work |
||||||||
|
Trumble et al. |
High |
RCT |
Not serious |
Not serious7 |
N/A |
Very serious3 |
Not suspected |
Low |
|
Patient satisfaction |
||||||||
|
Trumble et al. |
High |
RCT |
Serious1 |
Not serious7 |
N/A |
Very serious4 |
Not suspected |
Very low |
- Personnel and outcome assessors not blinded; Follow-up duration in Farzad et al. short, i.e. 8 wk.
- Very wide confidence interval due to very low event rate.
- Confidence interval not reported in Trumble et al.
- Assuming a difference of 1 could be considered a minimum important difference in patient satisfaction score 504 patients would be needed to demonstrate this difference with α=0.05 and β=0.80. The actual number of patients was substantially less than 504 after 52 weeks.
- Assuming the lower confidence limit of the range of motion difference, i.e. 21 degrees, is clinically relevant.
- Guideline development group considered studies on rehabilitation regarding zone 2 flexor tendon repair to be applicable to zone 1, 3 flexor tendon repair, and decided not to downgrade because of indirectness
Observational studies
|
|
Initial quality of eviden-ce |
Study design |
Risk of bias |
Indirect-ness |
Inconsis-tency |
Imprecision |
Publication bias |
Quality of evidence |
|
Function |
||||||||
|
Frueh et al., |
Low |
observational |
Not Serious |
Not serious2 |
Not serious |
Not serious |
Not suspected |
Low |
|
Ruptures |
||||||||
|
Frueh et al., Bainbridge et al., Baktir et al., Peck et al., Yen et al. |
Low |
Observational |
Not serious |
Not serious2 |
Not serious |
Serious1 |
Not suspected |
Very Low |
- very few events (<<300 events).
- Guideline development group considered studies on rehabilitation regarding zone 2 flexor tendon repair to be applicable to zone 1, 3 flexor tendon repair, and decided not to downgrade because of indirectness.
Beoordelingsdatum en geldigheid
Publicatiedatum : 15-04-2019
Beoordeeld op geldigheid : 07-04-2019
Uiterlijk in 2021 bepaalt het bestuur van de Nederlandse Vereniging voor Plastische Chirurgie of deze richtlijn nog actueel is. Zo nodig wordt een nieuwe werkgroep geïnstalleerd om de richtlijn te herzien. De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De Nederlandse Vereniging voor Plastische Chirurgie is als houder van deze richtlijn de eerstverantwoordelijke voor de actualiteit van deze richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de eerstverantwoordelijke over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door J.J.A. de Beer, zelfstandig richtlijnmethodoloog en B.S. Niël-Weise, zelfstandig richtlijnmethodoloog en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
Het doel van de richtlijn is duidelijkheid en uniformiteit te creëren voor behandelaars over de behandeling van volwassenen en kinderen die zich presenteren met peesletsels van de buigpezen van de hand.
Specifieke doelen zijn:
- de diagnostiek op de spoedeisende hulp;
- operatieve hechttechnieken per betrokken zone en de daaraan gerelateerde nabehandeling;
- de organisatie van zorg en de mogelijke invaliditeit op basis van het letsel;
- bieden van ondersteuning bij de participatie en reïntegratie.
Doelgroep
De richtlijn beoogt een praktisch handvat te bieden aan beroepsgroepen die betrokken zijn bij de diagnostiek, behandeling en nazorg voor patiënten met een flexorpeesletsel: plastisch chirurgen, spoedeisende hulp artsen, traumachirurgen, orthopeden, huisartsen, revalidatieartsen, fysiotherapeuten, ergotherapeuten, bedrijfsartsen, klinisch arbeidsgenees-kundigen en verzekeringsartsen.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2015 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten die zich presenteren met peesletsels van de buigpezen van de hand.
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep werkte gedurende 18 maanden aan de totstandkoming van de richtlijn.
De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
- Dr. C.A. van Nieuwenhoven (voorzitter), plastisch chirurg, Erasmus Medisch Centrum, Rotterdam
- H. ter Linden, plastisch chirurg, Flevoziekenhuis, Almere/EXPERTISEPUNT.com, Utrecht
- D.J.J.C. van der Avoort, plastisch chirurg, Ikazia ziekenhuis, Rotterdam/Xpert Clinic, Rotterdam (tot 7 december 2015 in de werkgroep)
- Dr. T. van Mulken, plastisch chirurg, Universitair Medisch Centrum, Maastricht/ Zuyderland Medisch Centrum
- Dr. M. Obdeijn, plastisch chirurg, Academisch Medisch Centrum, Amsterdam
- B.H.M. Michielsen, revalidatiearts, Zuyderland Medisch Centrum, Heerlen/Adelante, Hoensbroek
- Dr. S. Hovers, spoedeisende hulp arts, Meander MC, Amersfoort
- Dr. M.R. de Vries, traumachirurg, Reinier de Graaf, Delft
- Mw. M. Wind, MSc., ergotherapeut/handtherapeut, CHT-NL, Hand & Pols Centrum Amsterdam, Amsterdam
- G. van Strien, MSc., fysiotherapeut/handtherapeut, CHT-NL, Fysiofit, Den Haag
Meelezers:
- Dr. L. A.M. Elders, bedrijfsarts-klinisch arbeidsgeneeskundige, Rijndam Arbeidsrevalidatie/ Erasmus Medisch Centrum, Rotterdam
- Dr. R. Kok, verzekeringsarts, UWV/NVVG, Rotterdam
- Mevr. R. Brouwers, gipsverbandmeester, Zuiderzeeziekenhuis, Lelystad
Met ondersteuning van:
- Mw. B.S. Niël-Weise, arts-microbioloog (n.p.), zelfstandig richtlijnmethodoloog, Deventer
- Dr. ir. J.J.A. de Beer, zelfstandig richtlijnmethodoloog, Utrecht
- Mw. Drs. H.W.J. Deurenberg, SIROSS, informatiespecialist, Oss
Belangenverklaringen
De werkgroepleden hebben schriftelijk verklaard of ze in de laatste vijf jaar een (financieel ondersteunde) betrekking onderhielden met commerciële bedrijven, organisaties of instellingen die in verband staan met het onderwerp van de richtlijn. Tevens is navraag gedaan naar persoonlijke financiële belangen, belangen door persoonlijke relaties, belangen d.m.v. reputatiemanagement, belangen vanwege extern gefinancierd onderzoek, en belangen door kennisvalorisatie. De belangenverklaringen zijn op te vragen bij de Nederlandse Vereniging voor Plastische Chirurgie, een overzicht vindt u hieronder:
|
Werkgroeplid |
Functie |
Nevenfuncties |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Reputatie-management |
Extern gefinancierd onderzoek |
Kennis Valorisatie |
Overige belangen |
|
Christianne van Nieuwenhoven |
plastisch chirurg |
voorzitter ICHOM CHULD; lid richtlijn commissie NVPC; lid commissie kwaliteit NVPC; voorzitter European Reference Network CHULD (allen onbetaald) |
geen |
geen |
geen |
geen |
geen |
geen |
|
Hein ter Linden
|
Plastisch chirurg |
voorzitter dr Nicolaes Tulp Stichting (onbetaald); secretaris dutch association for facial plastic surgery (onbetaald); voorzitter adviescommissie introductieperiode universiteit Utrecht (onbetaald); expertisepunt (betaald) |
geen |
geen |
Zie nevenwerk-zaamheden |
geen |
geen |
geen |
|
Dirk Jan van der Avoort |
AIOS plastische chirurgie |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
|
Tom van Mulken |
plastisch chirurg |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
|
Miryam Obdeijn |
Plastisch chirurg |
voorzitter Nederlandse Vereniging voor Handchirurgie (onbetaald) |
geen |
geen |
geen |
geen |
geen |
geen |
|
Bernard Michielsen |
revalidatiearts |
opleider revalidatiegeneeskunde voor deelopleiding ziekenhuisrevalidatie (betaald via AMS) |
geen |
geen |
geen |
geen |
geen |
geen |
|
Sarah Hovers |
SEH-arts |
Lid richtlijnencommissie NVSHA |
geen |
geen |
geen |
geen |
geen |
geen |
|
Gwendolyn van Strien
|
handtherapeut docent postacademisch onderwijs zowel in Nederland als internationaal |
Consultant voor handencentra (betaald); coördinator NPI handtherapie opleiding (betaald); board of editors (international) voor journal of Hand Therapy (onbetaald) |
geen |
geen |
geen |
geen |
geen |
geen |
|
Marjolein Wind |
handtherapeut/ ergotherapeut |
Commissielid Hand Across Borders (onbetaald); afstudeerfase masterstudie ‘hand therapy’ aan de University of Derby (onbetaald) |
geen |
Collega’s op de werkvloer zouden baat kunnen hebben bij de uitkomst, echter wordt er al op bepaalde wijze gewerkt in de praktijk. |
nee |
nee |
nee |
nee |
|
Mark de Vries |
traumachirurg; opleider spoedeisende hulp |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
|
Hans de Beer |
|
Honorary fellow International Institute of Social History, Amsterdam. |
geen |
geen |
geen |
geen |
geen |
Lezingen over GRADE bij Nefarma en Roche Nederland. |
|
Barbara Niël-Weise |
|
geen |
geen |
geen |
geen |
geen |
geen |
geen |
Inbreng patiëntenperspectief
Aandacht werd besteed aan het patiëntenperspectief door in de voorbereidende fase de Patiëntenfederatie Nederland te vragen om schriftelijke input omtrent knelpunten en aandachtspunten. De Patiëntenfederatie Nederland gaf aan dat zij niet actief deelnemen aan dit richtlijntraject en daarom geen knelpunten of aandachtspunten zullen aanleveren. De werkgroep heeft tevens geprobeerd een focusgroep te organiseren. Vanwege onvoldoende deelnemers ging de focusgroep bijeenkomst niet door. Tijdens de commentaarfase heeft de Patiëntenfederatie Nederland commentaar geleverd.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren (zie implementatieplan).
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen volgens het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II) (https://www.agreetrust.org/), dat een internationaal breed geaccepteerd instrument is en op ‘richtlijnen voor richtlijn’ voor de beoordeling van de kwaliteit van richtlijnen (http://www.cvz.nl).
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Deze werden met de werkgroep besproken en vervolgens per mail aan de volgende organisaties voorgelegd met de vraag om input: het Zorginstituut Nederland, Inspectie voor de Gezondheidszorg, Nederlandse Zorgautoriteit, Nederlandse Patiënten Consumenten Federatie, Nederlands Huisartsen Genootschap, Zorgverzekeraars Nederland en Medirisk.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken.
Strategie voor zoeken en selecteren van literatuur
Eerst werd oriënterend gezocht naar bestaande buitenlandse richtlijnen [http://www.g-i-n.net/library/international-guidelines-library; https://www.ahrq.gov] en naar systematische reviews [Cochrane Library; Medline]. Vervolgens werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekactie of gebruikte trefwoorden van de zoekactie en de gehanteerde selectiecriteria zijn te vinden in de module van desbetreffende uitgangsvraag.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de methodologische checklijsten.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kwaliteit van bewijs (‘quality of evidence’) werd beoordeeld met behulp van GRADE (Guyatt et al., 2008). GRADE is een methode die per uitkomstmaat van een interventie, of voor een risico- of prognostische factor, een gradering aan de kwaliteit van bewijs toekent op basis van de mate van vertrouwen in de schatting van de effectgrootte (tabel 1 en 2).
Tabel 1 Indeling van de kwaliteit van bewijs volgens GRADE
|
Hoog |
Er is veel vertrouwen dat het werkelijke effect dicht in de buurt ligt van het geschatte effect. |
|
|
|
|
Matig |
Er is matig vertrouwen in het geschatte effect: het werkelijk effect ligt waarschijnlijk dicht bij het geschatte effect, maar er is een mogelijkheid dat het hiervan substantieel afwijkt. |
|
|
|
|
Laag |
Er is beperkt vertrouwen in het geschatte effect: het werkelijke effect kan substantieel verschillen van het geschatte effect. |
|
|
|
|
Zeer laag |
Er is weinig vertrouwen in het geschatte effect: het werkelijke effect wijkt waarschijnlijk substantieel af van het geschatte effect. |
Tabel 2 De kwaliteit van bewijs wordt bepaald op basis van de volgende criteria
|
Type bewijs |
Voor studies over interventies: RCT start in de categorie ‘hoog’. Observationele studie start in de categorie ‘laag’. Alle overige studietypen starten in de categorie ‘zeer laag’.
Voor studies over een risico- of prognostische factor: Prospectieve of retrospectieve cohortstudie start in de categorie ‘hoog’. Voor andere studieontwerpen wordt afgewaardeerd via ‘risk of bias’. |
|
|
|
|
|
|
Afwaarderen |
‘Risk of bias’ |
- 1 Serieus - 2 Zeer serieus |
|
|
|
|
|
|
Inconsistentie |
- 1 Serieus - 2 Zeer serieus |
|
|
|
|
|
|
Indirect bewijs |
- 1 Serieus - 2 Zeer serieus |
|
|
|
|
|
|
Onnauwkeurigheid |
- 1 Serieus - 2 Zeer serieus |
|
|
|
|
|
|
Publicatiebias |
- 1 Waarschijnlijk - 2 Zeer waarschijnlijk |
|
|
|
|
|
|
|
|
|
Opwaarderen |
Groot effect |
+ 1 Groot + 2 Zeer groot |
|
|
|
|
|
|
Dosis-respons relatie |
+ 1 Bewijs voor gradiënt |
|
|
|
|
|
|
Alle plausibele ‘confounding’ |
+ 1 zou een effect kunnen reduceren + 1 zou een tegengesteld effect kunnen suggereren terwijl de resultaten geen effect laten zien. |
Formuleren van de conclusies
Een conclusie verwijst niet naar één of meer artikelen, maar wordt getrokken op basis van alle studies samen (body of evidence).
Overwegingen
Voor het komen tot een aanbeveling zijn naast de kwaliteit van het wetenschappelijk bewijs over de gewenste en ongewenste effecten van een interventie, of over de effectgrootte van een risico- of prognostische factor, vaak ook nog andere aspecten van belang.
Genoemd kunnen worden:
- kosten,
- waarden, voorkeuren en ervaringen van patiënten en behandelaars met betrekking tot interventies en uitkomsten van zorg,
- aanvaardbaarheid van interventies,
- haalbaarheid van een aanbeveling.
Bij voorkeur wordt ook voor deze aspecten naar wetenschappelijk bewijs gezocht. De werkgroep die deze richtlijn heeft opgesteld, heeft hiervan afgezien omdat de hiervoor benodigde tijd in geen enkele verhouding zou staan tot de verwachte opbrengst. De werkgroep heeft, daar waar dit noodzakelijk werd geacht, op basis van eigen ervaring en expertise de hiervoor genoemde aspecten geïnventariseerd.
Deze aspecten worden besproken na de ‘conclusie’ onder het kopje ‘overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven een antwoord op de uitgangsvraag en zijn gebaseerd op het beste beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in desbetreffende module.
Indicatorontwikkeling
Gelijktijdig met het ontwikkelen van de richtlijn werden er interne kwaliteitsindicatoren ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken. Hiervoor werd gebruik gemaakt van de methodiek zoals beschreven in Programm für Nationale VersorgungsLeitlinien von BÄK, KBV und AWMF Qualitätsindikatoren. Manual für Autoren: 6. Qualitätsindikatoren für Nationale VersorgungsLeitlinien (2009).
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is.
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken wetenschappelijke verenigingen voorgelegd voor commentaar. Tevens werd de richtlijn voorgelegd aan de volgende organisaties ter becommentariëring: het Zorginstituut Nederland, Inspectie voor de Gezondheidszorg, Nederlandse Zorgautoriteit, Patiëntenfederatie Nederland, Nederlands Huisartsen Genootschap, Zorgverzekeraars Nederland en de Nederlandse Vereniging van Geneeskundig Adviseurs. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor autorisatie. De Nederlandse Vereniging voor Orthopedie heeft de richtlijn geautoriseerd tot en met de module ‘Indicatie voor revalidatiegeneeskunde’, welke de vakinhoudelijke modules zijn. De overige beroepsverenigingen en organisaties hebben de richtlijn geautoriseerd.
Literatuurlijst
Guyatt et al., 2008Guyatt GH, Oxman AD, Vist GE, Kunz R, Falck-Ytter Y, Alonso-Coello P, Schünemann HJ; GRADE Working Group (2008). GRADE: an emerging consensus on rating quality of evidence and strength of recommendations. BMJ. 336: 924-6.
Programm für Nationale VersorgungsLeitlinien von BÄK, KBV und AWMF Qualitätsindikatoren. Manual für Autoren: 6. Qualitätsindikatoren für Nationale VersorgungsLeitlinien (2009).
Zoekverantwoording
Literatuursearch voor nabehandeling van zone 1, 2 flexorpeesletsel
|
Database |
Zoektermen |
Totaal |
|
PubMed
Limitations: Dutch or English
Year of publication: ≥2012
Human study |
(flexor) AND (tendon) AND (repair OR tenorrhaphy) AND (function OR motion OR outcome OR Strickland OR tam OR Buck-Gramcko)
Based on search strategy Starr et al, 2013 |
2 SRs 2 RCTs/CCTs 6 comparative, observational studies 33 miscellaneous
|
Literatuursearch voor nabehandeling van zone 3 flexorpeesletsel
|
Database |
Zoektermen |
Totaal |
|
PubMed
Limitations: Dutch or English
Year of publication: ≥2012
Human study |
(flexor tendon injury OR flexor tendon repair) AND rehabilitation |
4 SRs 2 RCTs/CCTs 9 comparative observational studies 81 miscellaneous |
