Screening stemming bij dwarslaesie
Uitgangsvraag
Welk beleid is effectief wat betreft screening en behandeling van stemmingsproblematiek bij patiënten met dwarslaesie?
Deelvragen
- Wat is het effect van screenen van patiënten met een dwarslaesie op stemmingsproblematiek in vergelijking met reguliere zorg (niet screenen) op stemmingsproblematiek?
- Welke interventies op het gebied van stemming zijn het meest effectief in het behandelen van patiënten met stemmingsproblematiek na dwarslaesie?
Aanbeveling
Verricht bij alle revalidanten met een recent ontstane dwarslaesie (klinisch en primair poliklinisch) een intake door de op de dwarslaesieafdeling werkzame psycholoog.
Implementatietermijn: één tot drie jaar
Screen alle revalidanten met een recent ontstane dwarslaesie op stemmingsproblemen met behulp van een gestandaardiseerde screeningsvragenlijst (zoals PHQ of HADS) voor stemmingsproblemen (angst, depressie, PTSS). Er bestaat geen duidelijke voorkeur voor een bepaalde vragenlijst.
Verricht bij positieve screeningsresultaten nader psychodiagnostisch onderzoek door een op de dwarslaesieafdeling werkzame GZ-psycholoog.
Implementatietermijn: één tot drie jaar
Vraag bij verdenking op ernstige stemmingsstoornissen een psychiater in consult.
Begeleiding door een GZ-psycholoog dient beschikbaar te zijn in de klinische en poliklinische revalidatie voor mensen met een dwarslaesie in de chronische fase.
Implementatietermijn: één tot drie jaar
Bied peer support door getrainde, geselecteerde ervaringsdeskundigen aan alle klinische en poliklinische revalidanten met een dwarslaesie.
Implementatietermijn: één tot drie jaar
Van aanbevelingen waar geen implementatietermijn bij staat, wordt verwacht dat zij binnen een jaar na publicatie van de richtlijn geïmplementeerd kunnen zijn.
Overwegingen
Screening op psychologische problemen
De literatuursearch leverde geen vergelijkende studies op waaruit het effect van screening zou kunnen blijken.
Een dwarslaesie is een heftige en ingrijpende ervaring. Naast de fysieke revalidatie is ook de mentale revalidatie van belang. Met de term mentale revalidatie wordt bedoeld de professionele begeleiding van het verwerken van de dwarslaesie en de oriëntatie op het toekomstige leven. Schattingen van het voorkomen van depressie, angst en posttraumatische stress lopen sterk uiteen, mede door verschillen in de onderzoeksopzet en het gebruik van verschillende meetinstrumenten en afkappunten. Verreweg de meeste onderzoeken zijn gericht geweest op depressieve symptomen (Williams, 2014; 2015). Naar het vóórkomen van andere psychische problematiek (angst, posttraumatische stress) is relatief weinig onderzoek gedaan en over sociale (eenzaamheid) en existentiële problematiek is maar heel weinig bekend (Le, 2016; Smith, 2015; Littooij, 2015). Het meeste onderzoek is gedaan met zelfrapportage vragenlijsten die wel een indicatie geven van het voorkomen en de ernst van ervaren problemen, maar geen diagnostiek toelaten. Wat in dit stuk kortheidshalve depressie, angst of post-traumatische stress wordt genoemd dient dan ook gelezen te worden als “symptomen van …”, en gaat het hetzij over (verschillen in) een continue score van aantal en ernst van deze symptomen, of over (de mate van vóórkomen van) scores in de klinische range die duiden op de mogelijkheid van een depressiestoornis, angststoornis of post-traumatisch stress syndroom. Verder is vrijwel al het onderzoek gedaan onder mensen met een traumatische dwarslaesie, terwijl ruim de helft van de mensen die vanwege een nieuwe dwarslaesie in Nederland revalideert een niet-traumatische dwarslaesie heeft (Osterthun, 2009).
Ondanks deze beperkingen blijkt het duidelijk uit de literatuur dat een aanzienlijk deel van de mensen met een dwarslaesie ook op langere termijn stemmingsproblemen rapporteert. Craig (2009) verzamelde vijf studies waarin met standaard psychiatrische diagnostiek depressie tijdens de ziekenhuis of revalidatiefase werd gemeten en vond percentages depressie (minor en/of major) van 20 tot 43%. Een recente systematische review van 19 studies naar depressie na een dwarslaesie met in totaal 35.676 patiënten leverde een puntschatting van de prevalentie van depressie op van 22,2% (95% CI 18,7% tot 26,3%) (Williams, 2015). Een systematische review van 17 studies naar angst (2772 patiënten) leverde een percentage op van 27% (95% CI 24% tot 30%) patiënten met zelf-gerapporteerde symptomen van angst in de klinische range (Le, 2016). Voor PTSS is geen meta-analyse beschikbaar en lopen de resultaten van individuele studies uiteen van 7,1% tot 26,6% (Post, 2012). Vaak is sprake van complexe problematiek, een grote Amerikaanse studie wees uit dat twee-derde van de mensen met een dwarslaesie en depressie ook last hadden van PTSD (21%), angst (13%), drugmisbruik (10%), alcoholmisbruik (8%), bipolaire stoornissen (5%), persoonlijkheidsstoornissen (4%) en schizofrenie (3%) (Ullrich, 2014).
Een opvallend gegeven is dat de ernst van de dwarslaesie geen goede indicator is voor de aanwezigheid van psychologische problemen zoals depressie. Wel zijn verbanden gevonden met de aanwezigheid van secundaire gezondheidsproblematiek (met name pijn), pre-existente psychische problemen en gebruik van alcohol en drugs. Verder zijn er aanwijzingen dat depressieve symptomen iets vaker voorkomen bij vrouwen en mensen met een lager opleidingsniveau (Williams, 2014; Bombardier, 2016; Craig, 2015; van Leeuwen, 2012). Deze factoren verklaren echter maar een beperkt deel van de variantie van depressie.
Een internationale richtlijn over opsporen van depressie na een dwarslaesie komt uit Amerika (Consortium for spinal cord medicine, 1998). Daarin wordt primary care physicians aanbevolen om jaarlijks te screenen op het voorkomen van depressie en om standaard een aantal risicofactoren in kaart te brengen. Over de revalidatiefase wordt niets gezegd. In de Nederlandse NHG-standaard Depressie (2012) wordt aangegeven dat een depressie vaak een zelflimiterende en normale reactie is op verlies en wordt een periode van wachten op natuurlijk herstel aanbevolen. Dit watchful waiting is in de revalidatie vanwege de tijdelijkheid niet gewenst, zeker niet wanneer stemmingsproblemen de revalidatie (dreigen te) belemmeren. Ook blijkt uit de literatuur dat gemiddelde scores op depressievragenlijsten niet beter worden in de loop van de klinische revalidatie. Onderzoek in de algemene bevolking (volwassenen) wijst uit dat screening op depressie matig effectief is (Siu, 2016). Echter, deze conclusie is niet zonder meer door te trekken naar specifieke doelgroepen zoals dwarslaesie patiënten. Bij deze patiëntengroep is het belang van een actieve opsporing van manifeste of latente stemmingsproblematiek gewenst vanwege een hogere risico op deze problematiek. Een recente Amerikaanse consensus van de betreffende beroepsgroepen voor de praktijk van psychosociale disciplines adviseert screening bij opname in de revalidatiekliniek door zowel een psycholoog als een maatschappelijk werker (Russell, 2016).
Voor het screenen op depressie en angst na een dwarslaesie worden verschillende vragenlijsten gebruikt. Twee onafhankelijke reviews van screeningsinstrumenten voor depressie of angst vonden dat de psychometrische eigenschappen van deze instrumenten, voor zover bepaald bij mensen met een dwarslaesie, over het algemeen positief waren. Er werd geen aanleiding gezien om dwarslaesie-specifieke instrumenten te ontwikkelen en geen voorkeur voor een bepaald instrument uitgesproken (Sakakibara, 2009; Kalpakjian, 2009). De afkappunten van screeningslijsten zijn vaak zodanig gekozen dat deze instrumenten een redelijke sensitiviteit hebben en een beperkte specificiteit op de koop toegenomen wordt. Het aantal mensen met een dwarslaesie dat een diagnose depressie krijgt is dan ook vaak minder dan de helft van het aantal dat op een depressielijst in de klinische range scoort (Post, 2012).
Psychologen in Nederland gebruiken vaak instrumenten zoals de Beck Depression Inventory, de State-Trait Anxiety Inventory voor het screenen op stemmingsproblemen. In onderzoek wordt vaak voor iets kortere vragenlijsten gekozen. Een veel gebruikte vragenlijst die met in totaal 14 vragen zowel symptomen van angst als depressie meet is de Hospital Anxiety and Depression Scale (HADS). Een vragenlijst met 9 vragen die gebaseerd is op de DSM-criteria voor depressie is de Patient Health Questionnaire (PHQ-9) (Siu, 2016). Deze twee vragenlijsten hebben relatief weinig last van verstoring door fysieke symptomen van een dwarslaesie (Diemen, 2014). Twee vragen van de PHQ-9 (somberheid en interesseverlies) worden samen wel gebruikt voor een eerste oriëntatie op depressieve gevoelens. De in onderzoek meest gebruikte screeningsvragenlijst voor PTSS is de Schokverwerkingslijst.
In de NHG-standaard Depressie (2012) wordt aangegeven dat na een eerste oriëntatie, bij een bevestigend antwoord op twee vragen (de twee PHQ-9 vragen over somberheid en interesseverlies), de huisarts de situatie verder kan exploreren en dat het gebruik van een vragenlijst daarbij behulpzaam kan zijn.
Samenvattend kan gesteld worden dat stemmingsproblematiek frequent voorkomt na een dwarslaesie en dat de begeleiding hiervan een belangrijk onderdeel van de revalidatie is. Het vaststellen van bij wie hiervan sprake is, is dan een noodzakelijke eerste stap. Er is geen evidentie voor het nut van screenen op stemmingsproblemen in de algemene bevolking. Echter, gezien het hogere risico op stemmingsproblemen bij dwarslaesie patiënten, is het voor deze groep wel gewenst. Verschillende risicofactoren voor stemmingsproblematiek zijn geïdentificeerd, maar maken geen goede voorspelling mogelijk. Verschillende korte en weinig belastende vragenlijsten zijn hiervoor beschikbaar en kunnen als onderdeel van een standaard intake worden gebruikt.
Nadere overwegingen
- Patiëntenperspectief: patiënten zitten niet altijd op de psycholoog te wachten, ook al kan de emotionele lijdensdruk groot zijn. Een standaard intake kan drempelverlagend werken doordat er daarmee al persoonlijk contact wordt gelegd.
- Werkbaarheid: de aanbeveling is op meerdere klinische afdelingen al de huidige praktijk, op andere afdelingen is dit wel de beoogde situatie maar is de capaciteit daarvoor soms onvoldoende. Uitbreiding van de standaard intake naar de primaire poliklinische revalidatie (mensen met een primaire laesie) zal in de meeste situaties leiden tot enige uitbreiding van de formatie psycholoog.
- Voorkomen moet worden dat screening leidt tot overbehandeling, met andere woorden dat een hoge score op een screeningslijst automatisch zou leiden tot psychotherapeutische interventie. In plaats daarvan dient eerst nadere psychologische diagnostiek en multidisciplinair overleg plaats te vinden.
- Kosteneffectiviteit: hierover is geen onderzoek beschikbaar.
Psychologische interventies
Uit de systematische review blijkt dat er geen aanwijzingen zijn voor de effectiviteit van psychologische interventies op stemmingsproblemen. Het aantal studies is echter zo klein dat op basis hiervan geen conclusies kunnen worden getrokken.
Een groter aantal gecontroleerde, maar niet gerandomiseerde, studies laat veelal wel positieve effecten van psychologische interventies zien. De belangrijkste beperking van deze studies is dat de controlegroepen nogal eens bestonden uit mensen die geen indicatie voor psychologische behandeling hadden (want op baseline veel beter scoorden op de uitkomstmaten) of die het aanbod van psychologische behandeling weigerden (en daarmee niet goed vergelijkbaar zijn met de groep die wel instemt met behandeling).
Perkes (2014) voerde een systematische review uit waarbij niet-gerandomiseerde studies naar psychologische behandelingen van depressie na een dwarslaesie wel werden geïncludeerd. Zij includeerden negen studies, waarvan er twee ook in de review voor deze richtlijn zijn opgenomen (Duchnik, 2009; Schulz, 2009). Acht daarvan onderzochten de effectiviteit van verschillende vormen van cognitieve gedragstherapie (waaronder coping-effectiviteit, cognitieve therapie en probleemoplossende therapie) en een studie onderzocht psycho-educatie. Zeven studies vonden plaats in een revalidatiesetting (klinisch of poliklinisch). Perkes (2014) vond een matig groot effect van CGT (SMD =−0.52; 95% CI = −0.85, −0.19). Zij keken ook naar specifieke therapievormen en bevonden vooral activity scheduling effectief. Door het (laten) plannen en uitvoeren van plezierige activiteiten beoogt activity scheduling iemands gevoel van eigen waarde en controle (self-efficacy) te vergroten. In deze studies werden overigens geen positieve lange-termijn effecten gevonden, wat erop wijst dat een langere behandeling of follow-up gewenst is.
Al deze studies waren gericht op (behandeling van) depressie. Er zijn geen studies gevonden naar psychologische interventies bij angst of PTSS. Er bestaat al met al nog een grote kloof tussen de schaarse beschikbare evidence en de klinische praktijk, waar de psycholoog vanzelfsprekend onderdeel is van het multidisciplinaire revalidatieteam en de psycholoog begeleiding geeft op een groot aantal gebieden zoals angst, PTSS, hoop, lichaamsbeeld en –beleving, onzekerheid door secundaire problemen, en eventuele cognitieve stoornissen (Diemen, 2014).
De literatuursearch leverde verder een aantal RCTs op waarin stemming als uitkomstmaat is gemeten maar waarbij de interventies niet primair op stemming waren gericht. Gault (2009) reviewde drie studies waarin een psychologische interventie gericht op neuropathische pijn na een dwarslaesie resulteerden in vermindering van angst en depressie. Een vermindering van angst werd ook gevonden in de latere RCT van CGT bij neuropatische pijn door Heutink (2012).
Peer support en peer counseling betreffen begeleiding van nieuwe patiënten door getrainde, ervaringsdeskundigen en zijn in meerdere studies onderzocht. Haas (2013) noemde de volgende functies van peer support: psychologische en emotionele steun, advies over leven met een dwarslaesie, praktische tips en informatie, en voortdurende steun en vriendschap. Verschillende studies vonden een verband tussen het hebben ontvangen van peer mentoring en welbevinden (Sherman, 2004; Sweet, 2016). In een niet-gecontroleerde studie leidde peer mentoring tot een hogere zelfeffectiviteit en minder medische complicaties (Ljungberg, 2011). In de RCT van Duchnick (2009) was deelname aan begeleide peer supportgroepen de controleconditie van een psychologische interventie en bleken beide interventies even effectief.
Houlihan (2013) evalueerde in een RCT een telehealth interventie waarin verpleegkundigen gedurende zes maanden wekelijks telefonisch contact hadden met rolstoelgebonden mensen met een dwarslaesie of MS. De interventie was gericht op het voorkomen van decubitus, depressie en zorggebruik en bleek effectief in het verminderen van depressie, met name bij de deelnemers met hogere depressiescores op de baseline (Mercier, 2015).
Tenslotte zijn in de review meerdere studies aangetroffen waarbij de interventie geen psychologische interventie was, maar wel psychologische uitkomsten werden gemeten. Daaruit blijkt dat pijnvermindering, sociale steun (Muller, 2012), het hebben van een hulphond (Allen, 1996), massage (in vergelijking met oefenen) (Diego, 2002), zangtherapie (Tamplin, 2013), revalidatie in het algemeen (Ruff, 2007) en beweeginterventies (Adamson, 2015; Devillard, 2007) positieve effecten op stemming van mensen met een dwarslaesie kunnen hebben.
Samenvattend kan gesteld worden dat er slechts enkele gerandomiseerde studies naar psychologische interventies voor depressie bij mensen met een dwarslaesie zijn gedaan, en dat deze studies geen positieve effecten laten zien. Niet-gerandomiseerde studies zijn ook nog beperkt aanwezig, maar suggereren wel positieve effecten van cognitieve gedragstherapie, e-health counseling en peer support.
Nadere overwegingen
- Bijwerkingen: Er zijn in de literatuur geen bijwerkingen van psychologische begeleiding of behandeling gerapporteerd (Siu, 2016). Wel kan psychologische begeleiding confronterend zijn en is er in studies soms sprake van aanzienlijke drop-out.
- Patiëntenperspectief: Een grote meerderheid staat niet afkerend ten opzichte van psychologische begeleiding. Fann (2013) deed onderzoek naar preferenties van dwarslaesiepatiënten voor behandeling in geval van depressie. Van de gegeven opties was fysieke training het populairst (78% zou dit wel willen), gevolgd door een of andere vorm van individuele begeleiding (77%), medicatie (72%) en groepsbegeleiding (48%).
- Werkbaarheid: de aanbeveling is op meerdere klinische afdelingen al de huidige praktijk, al beperken de opnameduur en capaciteit de mogelijkheid voor meer langdurige of intensieve begeleidingstrajecten.
- Kosteneffectiviteit: hierover is geen onderzoek beschikbaar.
Onderbouwing
Een dwarslaesie is een ernstige aandoening met consequenties voor zowel fysiek als psychisch functioneren. Stemmingsproblemen worden dan ook veel gerapporteerd door mensen met een dwarslaesie. Dit geldt niet voor iedereen en bij een deel van hen verminderen deze problemen na verloop van tijd. Echter, angst, depressie en posttraumatische stress komen na een dwarslaesie veel vaker voor dan in de algemene bevolking (Le, 2016; Williams 2015). Het is dan ook van belang om stemmingsproblematiek tijdig te signaleren en te behandelen. Op dit moment wordt het systematisch screenen op stemmingsproblematiek bij deze diagnosegroep wisselend toegepast in Nederlandse revalidatiecentra en is het onduidelijk hoe deze problematiek het beste kan worden behandeld.
|
Zeer laag GRADE |
Er is onvoldoende bewijs dat behandeling met psychosociale interventies leidt tot verminderde (symptomen van) depressieve symptomen bij patiënten met dwarslaesie in de revalidatiefase.
Bronnen (Dorstyn, 2012; Duchnick, 2009; Schultz, 2009) |
Beschrijving studies
In de RCT van Duchnick (2009) zijn patiënten gediagnosticeerd als parapleeg of tetrapleeg, zonder ernstige psychiatrische aandoeningen en met voldoende cognitieve capaciteit, geïncludeerd vanuit een revalidatiekliniek. In totaal zijn 41 patiënten geïncludeerd, waarvan er 21 coping effectiveness training ontvingen en 20 alleen ondersteunende groepstherapie. Na ontslag uit de revalidatiekliniek en drie maanden na ontslag is de CESD-vragenlijst ingevuld.
In de RCT van Schulz (2009) zijn patiënten met een dwarslaesie en een mobiliteitsbeperking die een mantelzorger hadden geïncludeerd vanaf 35 jaar oud vanuit de thuissituatie. Geëxcludeerd werden patiënten met doofheid, blindheid of een cognitieve aandoening. Tevens patiënten die een terminale aandoening hadden of waarvan de mantelzorger dit had, met een actieve behandeling van kanker. De onderzoekers vergeleken een interventie voor patiënt en mantelzorger samen met een interventie gericht op alleen de mantelzorgers en een controle-interventie. De interventie gericht op alleen de mantelzorger wordt hier buiten beschouwing gelaten. In totaal zijn 117 patiënten geïncludeerd, waarvan er 57 een educatieve interventie kregen waarin onder andere aandacht werd besteed aan cognitieve en gedragsmatige vaardigheden om hun eigen zorg te verbeteren. De andere 60 patiënten ontvingen een informatiepakket. In aanvulling hierop konden zij deelnemen aan vijf telefonische ondersteunende groepstherapie sessies. De mantelzorgers ontvingen dezelfde interventie, waarbij de groepssessies met andere mantelzorgers plaatsvond. Na zes en twaalf maanden is de CESD-vragenlijst ingevuld, waarbij alleen de resultaten na twaalf maanden zijn gerapporteerd.
In de RCT van Dorstyn (2012) zijn patiënten met een dwarslaesie geïncludeerd ouder dan 18 jaar oud die tijdens opname gebruik had gemaakt van de psychologische dienstverlening. Patiënten met een congenitale wervelkolomaandoening, een cognitieve handicap, of die deelnamen aan andere psychotherapeutische interventies werden geëxcludeerd. In totaal zijn 40 patiënten geïncludeerd, waarvan er 20 telefonische consulten met een klinisch psycholoog kregen en 20 alleen standaard zorg, bestaande uit individuele medische nazorg, fysiotherapie en één consult met een psycholoog, ontvingen. Na 12 weken en drie maanden is de DASS-21 vragenlijst ingevuld.
Ondanks dat de randomisatieprocedures zoals beschreven in de artikelen correct zijn, blijkt er in de studies van Dorstyn (2012) en Duchnick (2009) opvallende verschillen zijn in de mate van compleetheid van de dwarslaesie en de baseline metingen van de CESD en DASS-21-scores tussen de interventie en controlegroepen.
Resultaten
Alle RCTs hadden een uitkomstmaat voor depressie, waardoor een meta-analyse mogelijk was. Echter, omdat verschillende instrumenten of verschillende versies van instrumenten werden gebruikt om depressie te kwantificeren, is een meta-analyse uitgevoerd waarin de resultaten van deze drie studies werden gecombineerd door middel van standardized mean differences. Dit is een maat voor de verhouding tussen het verschil tussen de interventie- en controlegroep en de standaarddeviatie binnen een groep. Door middel van deze uitkomstmaat kunnen effecten van studies waarin verschillende uitkomstmaten gebruikt zijn gecombineerd worden. De resultaten zijn te interpreteren als het aantal standaarddeviaties verschil door de interventie. Een kanttekening hierbij is dat de interventies op verschillende momenten in het proces zijn ingezet en dat vragenlijsten/interviews op verschillende momenten in het proces zijn afgenomen.
Tabel 1 Overzicht geïncludeerde studies
|
Studie ID |
Uitkomstmaat |
Werving patiënten |
Interventie |
Metingen |
|
Duchnick, 2009 |
CESD* (20 items) |
Tijdens revalidatie in het ziekenhuis |
Tijdens revalidatie in het ziekenhuis |
Bij opname Bij ontslag drie maanden follow-up |
|
Schulz, 2009 |
CESD (10 items) |
Thuissituatie |
Thuissituatie |
Baseline Na zes maanden (niet gerapporteerd) Na 12 maanden |
|
Dorstyn, 2012 |
DASS-21** Depression Anxiety Stress |
Tijdens revalidatie in het ziekenhuis |
Thuissituatie |
Bij ontslag 12 weken na ontslag drie maanden na einde interventie |
*CESD: Center for Epidemiological Studies Depression; **DASS: Depression Anxiety Stress Scales
Kortetermijneffecten
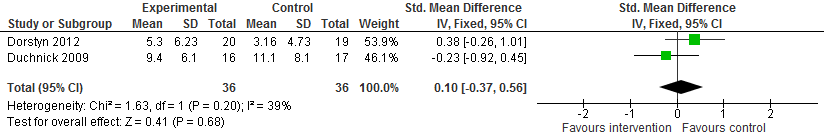
In geen van de drie RCTs werden significante positieve effecten op korte termijn gevonden op de uitkomstmaat depressieve symptomen. Hierbij dient opgemerkt te worden dat er op baseline vaak al verschillen bestonden in de scores op de depressiematen tussen de interventie- en controlegroep. De korte termijn resultaten zijn in de studie van Schulz (2009) niet gerapporteerd, waardoor deze niet meegenomen konden worden in de meta-analyse. Wanneer de resultaten van de twee studies (n=72) gecombineerd werden, was er geen verschil tussen psychologische interventie en controle (standardized mean difference van 0,10 (95% betrouwbaarheidsinterval van -0,37 tot 0,56, P=0,68).
Langetermijneffecten
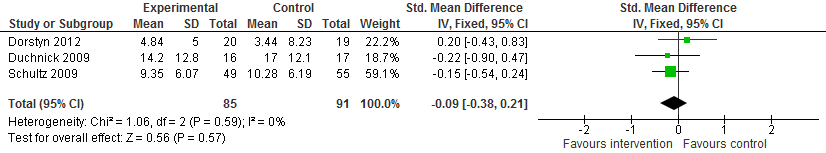
In geen van de drie RCTs werden significante positieve effecten op lange termijn gevonden. Hierbij dient opgemerkt te worden dat er op baseline vaak al verschillen bestonden in de scores op de depressiematen tussen de interventie- en controlegroep.
Wanneer de resultaten op de uitkomst depressieve symptomen van de drie studies (n=176) gecombineerd werden, was er geen verschil tussen psychologische interventie en controle (standardized mean difference van -0,09 (95% betrouwbaarheidsinterval van -0,38 tot 0,21, P=0,57).
Bijwerkingen van de psychosociale interventies zijn in geen van de studies gerapporteerd.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat depressieve symptomen is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (twee niveaus vanwege zeer grote verschillen in depressiescores op baseline) en imprecisie (één niveau vanwege het geringe aantal patiënten).
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag (vragen):
1. screening
P patiënten met een dwarslaesie;
I screenen middels een gevalideerd instrument op stemmingsproblematiek;
C niet screenen op stemmingsproblematiek;
O stemmingsproblematiek.
Het is onwaarschijnlijk dat screenen alleen een effect heeft op stemming. Daarom is gezocht naar literatuur waarin gerichte begeleiding/behandeling (verder: begeleiding) gericht op stemmingsproblematiek wordt aangeboden op basis van een gevalideerd screeningsinstrument versus reguliere revalidatie (geen screening).
2. interventies
P patiënten met een dwarslaesie en stemmingsproblematiek;
I 1) ervaringsdeskundige; 2) psychologische begeleiding (educatie, therapie);
C andere interventies;
O stemmingsproblematiek waaronder depressie.
Relevante uitkomstmaten
De werkgroep definieerde niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
Zoeken en selecteren (Methode)
In de databases Medline (OVID) en PsycINFO (Ovid) is met relevante zoektermen gezocht naar dwarslaesie en stemmingsproblematiek in combinatie met a) screening en b) interventies. De zoekverantwoording is weergegeven in de bijlage. De literatuurzoekactie voor zoekvraag a (screening) leverde 328 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria: inclusie van patiënten met dwarslaesie in de revalidatiefase; onderzoek naar de effectiviteit van het inzetten van screeningsinstrumenten voor stemmingsproblematiek; en vergelijkend onderzoek. Op basis van titel en abstract werden geen studies relevant geacht voor deze uitgangsvraag.
De literatuurzoekactie voor zoekvraag b (interventies) leverde 462 potentieel relevante treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria: inclusie van patiënten met dwarslaesie in de revalidatiefase; onderzoek naar de effectiviteit van interventies primair gericht op de behandeling van stemmingsproblematiek; RCTs of systematische reviews van RCTs; toepassing van een maat voor stemmingsproblematiek tijdens zowel baseline als follow-up. Op basis van titel en abstract werden in eerste instantie 47 studies voorgeselecteerd. Na raadpleging van de volledige tekst werden vervolgens 41 studies geëxcludeerd (zie exclusietabel) en zes studies definitief geselecteerd.
Resultaten
Drie van deze studies waren systematische reviews (Dorstyn, 2011; Mehta, 2011; Perkins, 2014) waarin ook niet-gerandomiseerd onderzoek was geïncludeerd. De andere drie studies waren RCTs (Dorstyn, 2012; Duchnick, 2009; Schulz, 2009). Omdat de in- en exclusiecriteria van de systematische reviews niet volledig overeenkomen met de criteria bij deze uitgangsvraag, zijn de volledige teksten van de geïncludeerde RCTs uit deze reviews geraadpleegd. De ene aanvullende RCT die geïncludeerd was in de studie van Perkes (2014) betrof een interventie niet primair gericht op begeleiding van stemmingsproblematiek en is daarom geëxcludeerd (Phillips, 2001). De belangrijkste studiekarakteristieken en resultaten van de drie RCTs zijn opgenomen in de evidence-tabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk of bias tabellen.
- Adamson BC, Ensari I, Motl RW. Effect of exercise on depressive symptoms in adults with neurologic disorders: a systematic review and meta-analysis. Archives of physical medicine and rehabilitation. 2015;96(7):1329-38.
- Allen K, Blascovich J. The value of service dogs for people with severe ambulatory disabilities. A randomized controlled trial. Jama 1996;275(13):1001-6.
- Bombardier CH, Adams LM, Fann JR, et al. Depression Trajectories During the First Year After Spinal Cord Injury. Archives of physical medicine and rehabilitation. 2016;97(2):196-203.
- Consortium for spinal cord medicine. Depression Following Spinal Cord Injury: A Clinical Practice Guideline for Primary Care Physicians. 1998.
- Craig A, Nicholson Perry K, Guest R, et al. Prospective study of the occurrence of psychological disorders and comorbidities after spinal cord injury. Archives of physical medicine and rehabilitation. 2015;96(8):1426-34.
- Craig A, Tran Y, Middleton J. Psychological morbidity and spinal cord injury: a systematic review. Spinal cord 2009;47(2):108-14.
- Devillard X, Rimaud D, Roche F, et al. Effects of training programs for spinal cord injury. Annales de readaptation et de medecine physique : revue scientifique de la Societe francaise de reeducation fonctionnelle de readaptation et de medecine physique. 2007;50(6):490-8, 80-9.
- Diego MA, Field T, Hernandez-Reif M, et al. Spinal cord patients benefit from massage therapy. The International journal of neuroscience. 2002;112(2):133-42.
- Diemen Tv. Dwarslaesie, Van Heugten C, Post M, et al. Handboek Revalidatiepsychologie. Amsterdam: Boom. 2014.
- Dorstyn D, Mathias J, Denson L. Psychosocial outcomes of telephone-based counseling for adults with an acquired physical disability: A meta-analysis. Rehabil Psychol. 2011;56(1):1-14.
- Duchnick JJ, Letsch EA, Curtiss G. Coping effectiveness training during acute rehabilitation of spinal cord injury/dysfunction: a randomized clinical trial. Rehabil Psychol. 2009;54(2):123-32.
- Fann JR, Crane DA, Graves DE, et al. Depression treatment preferences after acute traumatic spinal cord injury. Archives of physical medicine and rehabilitation. 2013;94(12):2389-95.
- Gault D, Morel-Fatio M, Albert T, et al. Chronic neuropathic pain of spinal cord injury: what is the effectiveness of psychocomportemental management? Annals of physical and rehabilitation medicine. 2009;52(2):167-72.
- Haas BM, Price L, Freeman JA. Qualitative evaluation of a community peer support service for people with spinal cord injury. Spinal cord. 2013;51(4):295-9.
- Heutink M, Post MW, Bongers-Janssen HM, et al. The CONECSI trial: results of a randomized controlled trial of a multidisciplinary cognitive behavioral program for coping with chronic neuropathic pain after spinal cord injury. Pain. 2012;153(1):120-8.
- Houlihan BV, Jette A, Friedman RH, et al. A pilot study of a telehealth intervention for persons with spinal cord dysfunction. Spinal cord. 2013;51(9):715-20.
- Kalpakjian CZ, Bombardier CH, Schomer K, et al. Measuring depression in persons with spinal cord injury: a systematic review. The journal of spinal cord medicine. 2009;32(1):6-24.
- Le J, Dorstyn D. Anxiety prevalence following spinal cord injury: a meta-analysis. Spinal Cord. 2016 Aug;54(8):570-8
- Littooij E, Widdershoven GA, Stolwijk-Swuste JM, et al. Global meaning in people with spinal cord injury: content and changes. The journal of spinal cord medicine. 2015.
- Ljungberg I, Kroll T, Libin A, et al. Using peer mentoring for people with spinal cord injury to enhance self-efficacy beliefs and prevent medical complications. Journal of clinical nursing. 2011;20(3-4):351-8.
- Mercier HW, Ni P, Houlihan BV, et al. Differential Impact and Use of a Telehealth Intervention by Persons with MS or SCI. American journal of physical medicine & rehabilitation / Association of Academic Physiatrists. 2015;94(11):987-99.
- Muller R, Peter C, Cieza A, et al. The role of social support and social skills in people with spinal cord injury--a systematic review of the literature. Spinal cord. 2012;50(2):94-106.
- Nederlands Huisartsen Genootschap (NHG). NHG standaard Depressie. 2012.
- Osterthun R, Post MW, van Asbeck FW. Characteristics, length of stay and functional outcome of patients with spinal cord injury in Dutch and Flemish rehabilitation centres. Spinal cord. 2009;47(4):339-44.
- Perkes SJ, Bowman J, Penkala S. Psychological therapies for the management of co-morbid depression following a spinal cord injury: a systematic review. Journal of health psychology. 2014;19(12):1597-612.
- Post MW, van Leeuwen CM. Psychosocial issues in spinal cord injury: a review. Spinal cord. 2012;50(5):382-9.
- Ruff RL, Adamson VW, Ruff SS, et al. Directed rehabilitation reduces pain and depression while increasing independence and satisfaction with life for patients with paraplegia due to epidural metastatic spinal cord compression. Journal of rehabilitation research and development. 2007;44(1):1-10.
- Russell HF, Richardson EJ, Bombardier CH, et al. Professional standards of practice for psychologists, social workers, and counselors in SCI rehabilitation. The journal of spinal cord medicine. 2016;39(2):127-45.
- Sakakibara BM, Miller WC, Orenczuk SG, et al. A systematic review of depression and anxiety measures used with individuals with spinal cord injury. Spinal cord. 2009;47(12):841-51.
- Schulz R, Czaja SJ, Lustig A, et al. Improving the quality of life of caregivers of persons with spinal cord injury: a randomized controlled trial. Rehabil Psychol. 2009;54(1):1-15.
- Sherman JE, DeVinney DJ, Sperling KB. Social Support and Adjustment After Spinal Cord Injury: Influence of Past Peer-Mentoring Experiences and Current Live-In Partner. Rehabilitation Psychology. 2004;49(2):140-49.
- Siu AL, Bibbins-Domingo K, Grossman DC, et al. Screening for Depression in Adults: US Preventive Services Task Force Recommendation Statement. Jama. 2016;315(4):380-7.
- Smith B, Caddick N. The impact of living in a care home on the health and wellbeing of spinal cord injured people. International journal of environmental research and public health. 2015;12(4):4185-202.
- Sweet SN, Noreau L, Leblond J, et al. Peer support need fulfillment among adults with spinal cord injury: relationships with participation, life satisfaction and individual characteristics. Disability and rehabilitation. 2016;38(6):558-65.
- Tamplin J, Baker FA, Grocke D, et al. Effect of singing on respiratory function, voice, and mood after quadriplegia: a randomized controlled trial. Archives of physical medicine and rehabilitation. 2013;94(3):426-34.
- Ullrich PM, Smith BM, Blow FC, et al. Depression, healthcare utilization, and comorbid psychiatric disorders after spinal cord injury. The journal of spinal cord medicine. 2014;37(1):40-5.
- Van Leeuwen CM, Hoekstra T, van Koppenhagen CF, et al. Trajectories and predictors of the course of mental health after spinal cord injury. Archives of physical medicine and rehabilitation. 2012;93(12):2170-6.
- Williams RT, Wilson CS, Heinemann AW, et al. Identifying depression severity risk factors in persons with traumatic spinal cord injury. Rehabil Psychol. 2014;59(1):50-6.
- Williams R, Murray A. Prevalence of depression after spinal cord injury: a meta-analysis. Arch Phys Med Rehabil. 2015 Jan;96(1):133-40.
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3 |
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Dorstyn, 2012 |
Type of study: Randomized controlled trial.
Setting: Spinal cord injury unit of a rehabilitation center.
Country: US
Source of funding: Not reported. |
Inclusion criteria: Adults ( ≥18y) who had good English comprehension (i.e., at least primary school level); had recently acquired a spinal cord injury (≤1y); had sufficient cognitive capacity to enable them to provide informed consent and participate in the therapy process; had completed their primary rehabilitation in the participating rehabilitation center; and had accessed psychological services during their inpatient rehabilitation in order to assist with their adjustment to disability.
Exclusion criteria: Patients who had a congenital spinal condition; had significant cognitive impairments that would impact on their ability to participate in therapy (ie, severe traumatic brain injury, as determined by medical report); or were currently engaged in another psychotherapeutic intervention (eg, psychology, psychiatry, social work) from another agency.
N total at baseline: I: 20 C: 20
Important prognostic factors2: Age mean (SD): I: 53.8 (16.3) C: 53.1 (20.0)
Sex, n (%): I: 13 (65%) male C: 14 (74%) male
Tetraplegia, n (%): I: 5 (25%) C: 10 (53%)
Complete lesion, n (%): I: 11 (55%) C: 3 (15%)
Length of stay, mean days (SD): I: 205 (131.2%) C: 111 (86.5%)
Functional independence measure, mean (SD): I: 98.8 (21.9) C: 111.4 (15.5)
DASS-21 depression I: 7.10 (9.12) C: 2.74 (6.15)
DASS-21 anxiety I: 5.70 (6.37) C: 2.84 (3.54)
DASS-21 stress I: 8.30 (8.76) C: 4.84 (8.20)
There were large differences between the intervention and control groups, where the intervention group had more complete lesions, a longer length of stay, a worse functional independence, higher depression, anxiety and stress measures. |
Standard care plus a 12-week program with biweekly phone consults with a clinical psychologist at prescheduled times based on motivational interviewing. |
Standard care: routine individual medical follow-up and physical therapy; One face-to-face consultation with a clinical psychologist at 3 months post discharge. |
Length of follow-up: Discharge, 12 weeks post-discharge and three months after the treatment ended.
Loss-to-follow-up: I: 0 (0%) C: 1 (5%) Reason: study withdrawal. |
Outcome measures at three months after the treatment ended:
DASS-21 Depression, mean (SD): I: 4.84 (5.00) C: 3.44 (8.23) Mean difference = 1.40 (95% CI: -2.90, 5.70) P=0.52
DASS-21 Anxiety, mean (SD): I: 4.74 (4.82) C: 1.78 (3.29) P=0.58
DASS-21 Stress, mean (SD): I: 6.63 (7.27) C: 6.22 (9.65) P=0.53
Mini International Neuropsychiatric Interview (version 6.0.0) diagnosis of depression, n (%): I: 1 (5.0%) C: 2 (10.5%) OR: 0.45 (95% CI: 0.04-5.39) P=0.53
|
The intervention group had higher measures of depression, anxiety and stress at baseline, biasing the results towards no effect of the intervention. |
|
Duchnick, 2009 |
Type of study: Randomized controlled trial
Setting: An inpatient SCI rehabilitation program of a large Veterans Affairs hospital between October 2004 and June 2006.
Country: US
Source of funding: James A. Haley Veterans’ Hospital |
Inclusion criteria: Diagnosis of paraplegia or tetraplegia within the preceding 6 months; fluent in the English language; no severe psychiatric condition precluding group therapy; possessed cognitive capacity to provide informed consent and participate in the group process.
Exclusion criteria: Not reported.
N total at baseline: I: 21 C: 20
Important prognostic factors2: Age, mean (SD): I: 50.8 (16.9) C: 54.6 (9.8)
Sex: I: 100% male C: 100% male
Tetraplegia: I: 40% C: 70%
CESD, mean (SD) I: 13.8 (9.0) C: 19.6 (11.7)
SAI, mean (SD) I: 42.2 (14.1) C: 47.5 (15.0)
There were some, but no major differences in baseline characteristics. Employment status could not be interpreted from the reported percentages (e.g. 53% of 21 patients) |
Coping effectiveness training: weekly 60-mintue psychoeducational group intervention sessions including education, group discussion and modelling of coping behaviours, including peer-educators.
|
Supportive group therapy: weekly 60-minute minimally structured, emotion-focused sessions
|
Timing of measurements: Baseline, discharge, 3 months follow-up
Loss-to-follow-up: I: 5 (23.8%) Reasons: withdrew (1), discharged early (1), relocated (3)
C: 3 (15%) Reasons: relocation/declined assessment (3)
Incomplete outcome data: Intervention: N (%) Reasons (describe)
Control: N (%) Reasons (describe)
|
CESD: I: 14.2 (12.8) C: 17.0 (12.1) Mean difference = -2.80 (95% CI: -11.31, 5.71) P=0.52
SAI: I: 36.3 (15.0) C: 41.7 (17.3) Mean difference = -5.40 (95% CI: -16.43, 5.63) P=0.34
|
Not all patients had a spinal cord injury; some patients with stroke were also included. |
|
Schultz, 2009 |
Type of study: Randomized controlled trial
Setting: Patients were recruited from multiple community sites and health and social service agencies.
Country: US
Source of funding: Grans from NINR, NIA, NIMH, MCMHD, NHLBI and the NSF |
Inclusion criteria: Having an SCI (quadriplegia or paraplegia) due to an acquired injury or disease; complete or incomplete lesion; being 35 years or older; having a mobility impairment as a result of the SCI; living in the community in a nongroup setting for a minimum of 1 year after injury; having a telephone; planning to remain in the geographic area for at least 6 months; competency in English.
Exclusion criteria: Caregiver or care recipient had a terminal illness with life expectancy < 6 months; was in active treatment for cancer other than maintenance use of tamoxifen or lupron; was blind or deaf; or had a cognitive impairment.
N total at baseline: I: 57 C: 60
Important prognostic factors2: Age, mean (SD): I: 53.4 (12.7) C: 54.4 (13.2)
Sex, n (%): I: 41 (71.9%) male C: 33 (55%) male
Complete injury (missing, n=26): I: 32.1% C: 38.3%
Level of SCI (missing, n=25) I: 6.5% L, 30.4% T, 63.0% C C: 7.4% L, 38.9% T, 53.7% C
There were some, but no major differences in baseline characteristics, although completeness of injury and level of SCI were missing in 26 and 25 cases respectively. |
Intervention targeted at both the care giver and the care receiver. The intervention aimed at the care receiver was designed to provide the individual with SCI knowledge and cognitive and behavioural skills to improve management of environmental and emotional stress, improve their health and self-care, enhance their access to formal and informal support, and improve their emotional well-being. The intervention was delivered in seven individual intervention sessions, delivered at home (5 sessions) and by telephone (2 sessions). In addition, 5 telephone support group sessions were provided.
The intervention aimed at the care giver was designed to provide the individual with SCI knowledge and cognitive and behavioural skills to reduce environmental and personal stress, improve health and self-care, enhance access to formal and informal support, and improve emotional well-being. The intervention was delivered in seven individual intervention sessions, delivered at home (5 sessions) and by telephone (2 sessions). In addition, 5 telephone support group sessions were provided.
|
Information-only in which the caregiver received standard printed information about caregiving, SCI, and again typically available from social service and health agencies.
|
Length of follow-up: 6 (not reported in the paper) and 12 months
Loss-to-follow-up: I: 7 (12.3%) C: 4 (6.7%) Reasons: refusal, unable to contact, moving of out the area, too ill, death (included reasons provided by care providers). No differences were found between those who completed the study and those who did not.
Incomplete outcome data: Percentages not reported. Multiple imputation and pooling of results were used to handle missing data.
|
CESD at 12 months: I: 9.35 (6.07) C: 10.28 (6.19) Mean difference = -0.93 (95% CI: -3.29, 1.43) P=0.44
The results were reported on 49 patients in the intervention group and 55 in the control group, which are the patients whom care giver was not lost to follow-up.
|
In the study, one intervention was also aimed at the caregiver only. Only the intervention aimed at both the patient and the caregiver was included in this evidence table. |
|
SCI = spinal cord injury; CESD = center for epidemiologic studies-sepression scale; SAI = state-trait anxiety inventory, stage form; FIM = Functional independence measure; DASS-21 = depression, anxiety and stress scale-21; CI = confidence interval. |
|||||||
Risk of bias tabel
|
Study reference
(first author, publication year) |
Describe method of randomisation1 |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Dorstyn, 2012 |
Computer generated and blocked randomization sequence. |
Likely Although a computer generated randomization sequence prior to allocation was reported, there were large differences between the intervention and control group (e.g. 55% vs 15% complete lesion, baseline DASS-21 depression scores of 7.10 (SD 9.12) and 2.74 (6.15) respectively) |
Likely Although blinding of patients is not possible, no sham intervention or other measures were taken to limit the potential placebo effect. |
Likely Standard care was provided by the same clinical psychologist as the intervention. |
Unlikely All assessments were telephone-administered by an independent psychologist who was not informed of group allocation. |
Unlikely All measures described in the methods are reported in the results.
|
Unlikely Only one patient was lost to follow-up. |
Unlikely Only one patient was lost to follow-up and no patients switched between groups. |
|
Duchnick, 2009 |
Randomization table generated by means of a computer random-number generator. |
Likely Although a computer random-number generator prior to allocation was reported, there were large differences between the intervention and control group (e.g. CES-D score on admission of 13.8 (9.0) and 19.6 (11.7) respectively). |
Unlikely Although blinding of patients is not possible, another intervention was provided to the patients in the control group. |
Likely Staff were not blinded for allocation status. |
Likely Outcome assessors were not blinded for allocation status. |
Unlikely All measures described in the methods are reported in the results.
|
Unlikely Although a high percentages was lost to follow-up, no differences were seen in attrition between intervention and control groups. |
Likely No intention to treat analysis was used. |
|
Schulz, 2009 |
Randomization was performed at the Miami site using a computer-generated algorithm and transmitted to the Pittsburgh site using a standard protocol. |
Unlikely Computer-generated algorithm. |
Likely Although blinding of patients is not possible, no sham intervention or other measures were taken to limit the potential placebo effect. |
Unlikely Patients were included when living at home and therefore had minimal contact with formal care providers. |
Unlikely Outcome assessors were blinded for allocation status. |
Unlikely All measures described in the methods are reported in the results except for the 6 months results, which were indicated as not different from the baseline measurement. |
Unclear 14% of the participants dropped out, but no specific numbers were reported for patients, or the distribution between intervention and control groups. |
Unlikely Multiple imputation was used to handle missing data. |
- Randomisation: generation of allocation sequences have to be unpredictable, for example computer generated random-numbers or drawing lots or envelopes. Examples of inadequate procedures are generation of allocation sequences by alternation, according to case record number, date of birth or date of admission.
- Allocation concealment: refers to the protection (blinding) of the randomisation process. Concealment of allocation sequences is adequate if patients and enrolling investigators cannot foresee assignment, for example central randomisation (performed at a site remote from trial location) or sequentially numbered, sealed, opaque envelopes. Inadequate procedures are all procedures based on inadequate randomisation procedures or open allocation schedules..
- Blinding: neither the patient nor the care provider (attending physician) knows which patient is getting the special treatment. Blinding is sometimes impossible, for example when comparing surgical with non-surgical treatments. The outcome assessor records the study results. Blinding of those assessing outcomes prevents that the knowledge of patient assignement influences the proces of outcome assessment (detection or information bias). If a study has hard (objective) outcome measures, like death, blinding of outcome assessment is not necessary. If a study has “soft” (subjective) outcome measures, like the assessment of an X-ray, blinding of outcome assessment is necessary.
- Results of all predefined outcome measures should be reported; if the protocol is available, then outcomes in the protocol and published report can be compared; if not, then outcomes listed in the methods section of an article can be compared with those whose results are reported.
- If the percentage of patients lost to follow-up is large, or differs between treatment groups, or the reasons for loss to follow-up differ between treatment groups, bias is likely. If the number of patients lost to follow-up, or the reasons why, are not reported, the risk of bias is unclear
- Participants included in the analysis are exactly those who were randomized into the trial. If the numbers randomized into each intervention group are not clearly reported, the risk of bias is unclear; an ITT analysis implies that (a) participants are kept in the intervention groups to which they were randomized, regardless of the intervention they actually received, (b) outcome data are measured on all participants, and (c) all randomized participants are included in the analysis.
Beoordelingsdatum en geldigheid
Publicatiedatum : 03-05-2017
Beoordeeld op geldigheid : 01-05-2017
Voor het beoordelen van de actualiteit van deze richtlijn wordt de werkgroep niet in stand gehouden. Uiterlijk in 2020 bepaalt het bestuur van de Nederlandse Vereniging van Revalidatieartsen of de modules van deze richtlijn nog actueel zijn. De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De Nederlandse Vereniging van Revalidatieartsen is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
Initiatief
Nederlandse Vereniging van Revalidatieartsen
In samenwerking met
Nederlandse Vereniging voor Neurochirurgie
Nederlandse Vereniging voor Neurologie
Nederlandse Vereniging voor Plastische Chirurgie
Nederlandse Vereniging voor Urologie
Nederlandse Wetenschappelijke Vereniging voor Seksuologie
Dwarslaesie Organisatie Nederland
Met ondersteuning van
Kennisinstituut van Medisch Specialisten
Financiering
De richtlijnontwikkeling werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS)
Doel en doelgroep
Doel van de richtlijn
Doel van de richtlijn is om aanbevelingen te geven voor in de praktijk ervaren knelpunten en zo te komen tot meer uniforme en beter afgestemde zorgverlening. De aanbevelingen zijn gebaseerd op een zorgvuldige weging van de laatste wetenschappelijke inzichten, expert opinion en patiëntenvoorkeuren. De richtlijn ondersteunt zorgprofessionals in hun klinische besluitvorming en biedt transparantie naar patiënten en derden. De richtlijn heeft niet tot doel om het hele zorgproces omvattend te beschrijven. Hiervoor wordt verwezen naar onder andere het handboek Dwarslaesierevalidatie en de Zorgstandaard Dwarslaesie.
Beoogde gebruikers van de richtlijn
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen die betrokken zijn bij of verwijzen naar revalidatiezorg voor patiënten met een traumatische dwarslaesie.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2015 een multidisciplinaire werkgroep ingesteld (zie hiervoor de samenstelling van de werkgroep). De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
- Dr. C. van Koppenhagen, revalidatiearts (VRA), werkzaam in Universitair Medisch Centrum te Utrecht (voorzitter)
- Dr. I. van Nes, revalidatiearts (VRA), werkzaam in Sint Maartenskliniek te Nijmegen (vicevoorzitter)
- Drs. W.J. Achterberg, revalidatiearts (VRA), werkzaam in Reade te Amsterdam
- Drs. H.M.H. Bongers-Janssen, revalidatiearts (VRA), werkzaam in Adelante te Hoensbroek (tot 1 maart 2016) en Sint Maartenskliniek te Nijmegen (vanaf 1 maart 2016)
- Drs. D. Gobets, revalidatiearts (VRA), werkzaam in Heliomare te Wijk aan Zee
- Drs. E.M. Maas, revalidatiearts (VRA), werkzaam in Roessingh te Enschede
- Dr. E.H. Roels, revalidatiearts (VRA), werkzaam in Universitair Medisch Centrum te Groningen
- Drs. D.C.M. Spijkerman, revalidatiearts (VRA), werkzaam in Rijndam Revalidatie te Rotterdam
- Prof. dr. M.W.M. Post, bijzonder hoogleraar dwarslaesierevalidatie en senior onderzoeker, werkzaam in Universitair Medisch Centrum te Groningen en De Hoogstraat te Utrecht
- Drs. R.E. Feller, neurochirurg (NVVN), werkzaam in VU Medisch Centrum te Amsterdam
- Drs. A.W. Oldenbeuving, neuroloog-intensivist (NVN), werkzaam in Sint Elisabeth Ziekenhuis te Tilburg
- Dr. O. Lapid, plastisch chirurg (NVPC), werkzaam in Academisch Medisch Centrum te Amsterdam
- Dr. B.F.M. Blok, uroloog (NVU), werkzaam in Erasmus MC te Rotterdam
- E. Kruijver, seksuoloog (NVVS), werkzaam in Sophia Revalidatie te Den Haag en De Hoogstraat te Utrecht
- J. Dekkers, voorzitter, Dwarslaesie Organisatie Nederland (DON)
- F. Penninx, penningmeester, Dwarslaesie Organisatie Nederland (DON)
Met ondersteuning van:
- J. Tra MSc, adviseur, Kennisinstituut van Medisch Specialisten
- Dr. N.H.J. van Veen, adviseur, Kennisinstituut van Medisch Specialisten
Belangenverklaringen
De KNMG-Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of ze in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van Medisch Specialisten.
|
Werkgroeplid |
Mogelijke conflicterende belangen met betrekking tot deelname werkgroep |
Toelichting |
|
Achterberg |
Nee |
|
|
Blok |
Nee |
|
|
Bongers-Janssen |
Nee |
|
|
Dekkers |
Nee |
|
|
Feller |
Nee |
|
|
Gobets |
Nee |
|
|
Kruijver |
Nee |
|
|
Lapid |
Nee |
|
|
Maas |
Nee |
|
|
Oldenbeuving |
Nee |
|
|
Penninx |
Nee |
|
|
Post |
Nee |
|
|
Roels |
Nee |
|
|
Spijkerman |
Nee |
|
|
Van Koppenhagen |
Nee |
|
|
Van Nes |
Nee |
|
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door twee afgevaardigden van de patiëntenvereniging (Dwarslaesie Organisatie Nederland) in de werkgroep. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de patiëntenvereniging.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Er is een onderscheid gemaakt tussen aanbevelingen waarvan verwacht wordt dat zij binnen een jaar na publicatie van de richtlijn geïmplementeerd kunnen zijn en tussen aanbevelingen waarvan te verwachten is dat ze niet binnen één jaar na publicatie van de richtlijn overal geïmplementeerd kunnen zijn. De implementatie van deze aanbevelingen heeft meer tijd nodig vanwege een gebrek aan middelen, expertise en/of juiste organisatie van zorg. Of deze aanbevelingen daadwerkelijk in de praktijk gerealiseerd kunnen worden, hangt van de medewerking van meerdere (stakeholder)partijen af.
Er zal na autorisatie van de richtlijn een implementatieplan opgesteld worden voor de aanbevelingen met een implementatietermijn > 1 jaar door het Nederlands-Vlaams Dwarslaesie Genootschap (NVDG).
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is.
Knelpuntenanalyse
Tijdens de voorbereidende fase is er een knelpuntenanalyse gehouden om te inventariseren welke knelpunten er in de praktijk bestaan rondom de zorg voor patiënten met een dwarslaesie. De knelpuntenanalyse vond tijdens een invitational conference plaats. Hiervoor werden alle belanghebbende partijen (stakeholders) uitgenodigd. Knelpunten konden zowel medisch inhoudelijk zijn, als betrekking hebben op andere aspecten zoals organisatie van zorg, informatieoverdracht of implementatie. Voor een overzicht van partijen die uitgenodigd waren, zie bijlage Knelpuntenanalyse (onder aanverwante producten).
De volgende partijen waren aanwezig en hebben knelpunten aangedragen: de Inspectie voor de Gezondheidszorg, Nederlandse Federatie van Universitair Medische Centra, Nederlandse Vereniging voor Ziekenhuizen, Revalidatie Nederland, Zorginstituut Nederland, Zorgverzekeraars Nederland, Dwarslaesie Organisatie Nederland, Ergotherapie Nederland, Koninklijk Nederlands Genootschap voor Fysiotherapie, Nederlands Instituut van Psychologen, Nederlandse Vereniging voor Intensive Care, Nederlandse Vereniging voor Neurochirurgie, Nederlandse Vereniging voor Plastische Chirurgie, Nederlands Vereniging voor Urologie en de Nederlandse Wetenschappelijke Vereniging voor Seksuologie. Een verslag van de invitational conference is opgenomen in de bijlage (Knelpuntenanalyse).
Uitgangsvragen en uitkomstmaten
De knelpunten benoemd tijdens de invitational conference zijn door de werkgroep besproken en geprioriteerd. De geprioriteerde knelpunten zijn omgezet naar uitgangsvragen. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar bestaande buitenlandse richtlijnen (op de websites van de American Spinal Injury Association (ASIA), de European Association of Urology, the Consortium for Spinal Cord Medicine, het Nederlands Vlaams Dwarslaesie Genootschap, National Clinical Guideline Centre, het National Institute for Clinical Excellence (NICE) en de European Federation of Neurological Societies) en systematische reviews (PubMed en het Spinal Cord Injury Research Evidence (SCIRE) project). Vervolgens werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie voor de oriënterende zoekactie en patiëntenperspectief zijn opgenomen onder aanverwante producten.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR – voor systematische reviews; Cochrane – voor gerandomiseerd gecontroleerd onderzoek; ACROBAT-NRS – voor observationeel onderzoek; QUADAS II – voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidence-tabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor Grading Recommendations Assessment, Development and Evaluation (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, matig, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
Er is hoge zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt zoals vermeld in de literatuurconclusie; het is zeer onwaarschijnlijk dat de literatuurconclusie verandert wanneer er resultaten van nieuw grootschalig onderzoek aan de literatuuranalyse worden toegevoegd. |
|
Matig |
Er is matige zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt zoals vermeld in de literatuurconclusie; het is mogelijk dat de conclusie verandert wanneer er resultaten van nieuw grootschalig onderzoek aan de literatuuranalyse worden toegevoegd. |
|
Laag |
Er is lage zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt zoals vermeld in de literatuurconclusie; er is een reële kans dat de conclusie verandert wanneer er resultaten van nieuw grootschalig onderzoek aan de literatuuranalyse worden toegevoegd. |
|
Zeer laag |
Er is zeer lage zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt zoals vermeld in de literatuurconclusie; de literatuurconclusie is zeer onzeker. |
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008), en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in één of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje Overwegingen.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en deze zijn meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt, kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje Overwegingen.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs, de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag.
Indicatorontwikkeling
Gelijktijdig met het ontwikkelen van de conceptrichtlijn werden er interne kwaliteitsindicatoren ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken. De indicatoren zijn terug te vinden in de bijlage Indicatoren (onder aanverwante producten).
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de bijlage Kennislacunes beschreven (onder aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn is aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
- Brouwers MC, Kho ME, Browman GP, et al. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
- Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwaliteit. Link: http://richtlijnendatabase.nl/instructies/richtlijnontwikkeling.html.
- Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013.
- Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008 May 24;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Zoekverantwoording
Screening
|
Database |
Zoektermen |
Totaal |
|
MEDLINE (via Ovid) |
exp spinal cord injuries/ OR exp spinal cord ischemia/ OR (SCI AND spinal cord).ab,ti OR ((spine or spinal or vertebra*) adj6 (injur* or lesion* or traum* or damag*)).ab,ti OR (spinal cord adj6 (contusion OR laceration OR traum* OR ischem*)).ab,ti OR (cauda* adj6 (injur* OR traum* OR lesion* OR syndrom*)).ab,ti OR exp paraplegia/ OR exp quadriplegia/ OR (paraplegi* or quadriplegi* or tetraplegi*).ab,ti
AND
exp mental disorders/di OR ((exp emotions/ OR exp depression/ OR exp depressive disorder/ OR exp anxiety disorder/ OR exp psychological, stress/ OR exp anxiety/) AND (exp mass screening/ OR exp psychological tests/)) OR ((depress* OR anxiety OR distress OR stress*) adj4 (screen* OR ident* OR diagn* OR detect* OR predict* OR measur*)).ti,ab
AND
((meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/))) OR ((exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or clinic$ trial$1.tw. or (clinic$ adj trial$1).tw. or ((singl$ or doubl$ or treb$ or tripl$) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo$.tw. or randomly allocated.tw. or (allocated adj2 random$).tw.) not (animals/ not humans/)) OR (Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or (cohort adj (study or studies)).tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective.tw. or prospective.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/) |
253 |
|
PsycINFO (via Ovid) |
exp spinal cord injuries/ OR (SCI AND spinal cord).ab,ti OR ((spine or spinal or vertebra*) adj6 (injur* or lesion* or traum* or damag*)).ab,ti OR (spinal cord adj6 (contusion OR laceration OR traum* OR ischem*)).ab,ti OR (cauda* adj6 (injur* OR traum* OR lesion* OR syndrom*)).ab,ti OR paraplegia.mp OR quadriplegia.mp OR (paraplegi* or quadriplegi* or tetraplegi*).ab,ti
AND
((exp emotions/ OR exp major depression/ OR exp distress/ OR exp anxiety/ OR exp anxiety disorders/) AND (exp screening/ OR exp screening tests/)) OR ((depress* OR anxiety OR distress OR stress*) adj4 (screen* OR ident* OR diagn* OR detect* OR predict*)).ti,ab |
100 |
|
Tezamen |
Deduplicatie (25) |
328 |
Interventies
|
Database |
Zoektermen |
Totaal |
|
MEDLINE (via Ovid) |
exp spinal cord injuries/ OR exp spinal cord ischemia/ OR (SCI AND spinal cord).ab,ti OR ((spine or spinal or vertebra*) adj6 (injur* or lesion* or traum* or damag*)).ab,ti OR (spinal cord adj6 (contusion OR laceration OR traum* OR ischem*)).ab,ti OR (cauda* adj6 (injur* OR traum* OR lesion* OR syndrom*)).ab,ti OR exp paraplegia/ OR exp quadriplegia/ OR (paraplegi* or quadriplegi* or tetraplegi*).ab,ti
AND
exp psychotherapy/ OR exp counseling/ OR exp self-help groups/ OR (patient education as Topic/ AND (psycho* OR cogniti* OR behaviour* OR behavior* OR depress* OR mood).ab,ti) OR exp cognitive therapy/ OR exp adaptation, psychological/ OR psychotherap*.ab,ti OR ((psycho* OR cogniti* OR behaviour* OR behavior* OR depress* OR mood) adj4 (intervention* OR therap* OR program* OR education* OR treatment* OR counsel* OR training OR support* OR group*)).ab,ti OR ((support OR peer) adj4 group*).ab,ti OR empowerment.ab,ti
AND
((meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/))) OR ((exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or clinic$ trial$1.tw. or (clinic$ adj trial$1).tw. or ((singl$ or doubl$ or treb$ or tripl$) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo$.tw. or randomly allocated.tw. or (allocated adj2 random$).tw.) not (animals/ not humans/)) OR (Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or (cohort adj (study or studies)).tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective.tw. or prospective.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/) |
462 |
|
PsycINFO (via Ovid) |
exp spinal cord injuries/ OR (SCI AND spinal cord).ab,ti OR ((spine or spinal or vertebra*) adj6 (injur* or lesion* or traum* or damag*)).ab,ti OR (spinal cord adj6 (contusion OR laceration OR traum* OR ischem*)).ab,ti OR (cauda* adj6 (injur* OR traum* OR lesion* OR syndrom*)).ab,ti OR paraplegia.mp OR quadriplegia.mp OR (paraplegi* or quadriplegi* or tetraplegi*).ab,ti
AND
exp psychotherapy/ OR exp counseling/ OR exp cognitive therapy/ OR exp self help techniques/ OR exp coping behavior/ OR exp peer counseling/ OR exp peers/ OR exp empowerment/ OR psychotherap*.ab,ti OR ((psycholog* OR psychosoc* OR cogniti* OR behaviour* OR behavior* OR depress* OR mood OR peer* OR coping) adj3 (intervention* OR therap* OR program* OR treatment* OR counsel* or training OR support* OR group*)).ab,ti OR (support adj6 group*).ab,ti OR empowerment.ab,ti
LIMIT TO
("0400 emperical study" or "0430 followup study" or "0450 longitudinal study" or "0451 prospective study" or "0453 retrospective study" or "0830 systematic review" or "1200 meta analysis" or "1800 quantitative study" or "2000 treatment outcome/clinical trial") |
215 |
|
Tezamen |
Deduplicatie (50) Irrelevante artikelen (165) |
462 |
Exclusietabel
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur, jaartal |
Reden van exclusie |
|
Adamson, 2015 |
SR over het effect van bewegen op depressieve symptomen bij patiënten met neurologische aandoeningen. Echter, maar één studie met SCI die ook in deze resultaten staat (Hicks 2003) en geen psychosociale interventie |
|
Zsoldos, 2014 |
Geen controlegroep |
|
Heutink, 2014 |
Geen controlegroep |
|
Bomardier, 2014 |
Alleen preliminary results van een trial met medicatie; definieve resultaten studie in Fann 2015, maar geen psychosociale interventie |
|
Tamplin, 2013 |
Trial over zangtherapapie, primair gericht op longfunctie |
|
Houlihan, 2013 |
Telehealth interventie primair gericht op preventive van decubitus |
|
Hough, 2013 |
Geen controlegroep |
|
Fann, 2013 |
Cross-sectionele survey |
|
Post, 2012 |
Narrative review, niet systematisch (search strategie, in/exclusietabellen ontbreken, kwaliteitsbeoordeling ontbreekt) |
|
Peter, 2012 |
Geen info over interventies |
|
Muller, 2012 |
Geen info over interventies |
|
Heutink, 2012 |
Interventie primair gericht op pijn |
|
Gordan, 2012 |
Observationeel onderzoek |
|
Migliorini, 2011 |
Geen controlegroep |
|
Fann, 2011 |
Cross-sectionele survey |
|
Dorstyn, 2011 |
Relevante studies geïncludeerd, maar resultaten niet dwarslaesie specifiek gerapporteerd |
|
Stuifbergen, 2010 |
Review, maar geen SCI specifieke uitkomsten vermeld. |
|
Perry, 2010 |
Interventie primair gericht op pijn |
|
Beh-Pjooh, 2010 |
Artikel in het Iranees |
|
Gault, 2009, |
Review primair gericht op pijn; geen relevante studies geïncludeerd |
|
Stuntzner, 2008 |
Alleen een abstract |
|
Ruff, 2007 |
Primair gericht op fysieke revalidatie |
|
Devillard, 2007 |
Literature review, maar geen uitkomsten specifiek voor psychosociaal welzijn gerapporteerd in evidence tabellen |
|
Wardell, 2006 |
Allocatie procedure niet gerapporteerd; zeer laag aantal patiënten (n=12) waardoor vergelijkbaarheid interventie- en controlegroep niet gewaarborgd is |
|
Norrbrinkg Budh, 2006 |
Allocatie procedure onduidelijk; primair gericht op pijn |
|
Kennedy, 2006 |
Geen controlegroep |
|
Hughes, 2006 |
4 patiënten met “spinal impairments” geïncludeerd; geen resultaten vermeld. |
|
Kennedy, 2005 |
Secundaire studie |
|
Gorski, 2005 |
Case series (n=3) |
|
Hicks, 2003 |
Trail over effect van fysieke oefentherapie, primair gericht op fysieke revalidatie |
|
Diego, 2002 |
RCT over het effect van massagetherapie primair gericht op fysieke revalidatie |
|
Craig, 1999 |
Adjustment als uitkomstmaat, geen psychosociale maten vermeld |
|
Craig, 1998 |
Geen psychosociale maat op baseline en follow-up als uitkomstmaat |
|
Craig, 1997 |
Zelfde studie als Craig 1998 |
|
Allen, 1996 |
Geen psychosociale maat op baseline en follow-up als uitkomstmaat |
|
Uit review van Perkes 2014 |
|
|
Phillips, 2001 |
Interventie niet primair gericht op psychosociale revalidatie |
