Beeldvormend onderzoek bij distale radiusfracturen
Uitgangsvraag
Wat is het optimale beeldvormende onderzoek bij patiënten met een distale radiusfractuur?
Aanbeveling
Röntgenfoto’s
Maak bij patiënten met verdenking op een distale radiusfractuur ten minste een PA en zuiver laterale röntgenopname.
Overweeg laagdrempelig een laterale radio-carpale röntgenopname voor de beoordeling van het radio-carpale gewrichtsoppervlak.
CT scan
Verricht een CT-scan bij intra-articulaire distale radiusfracturen of als er twijfel is over het wel of niet intra-articulair verlopen van de fractuur, waarbij een operatie-indicatie wordt overwogen of reeds gesteld is.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Voor de diagnostiek en beoordeling van distale radiusfracturen worden standaard röntgenfoto’s gemaakt. Voor aanvullende en betere beoordeling van de distale radius (fractuur), of bij (complexe) intra-articulaire fracturen kan een CT-scan worden gemaakt om aanvullende informatie te leveren. In de literatuur is gekeken naar de toegevoegde diagnostische waarde van een aanvullende CT-scan en welke invloed deze scan heeft op (mogelijke) veranderingen in het behandelplan.
In de literatuur zijn vijf studies gevonden waarin diagnostiek door middel van röntgenfoto’s wordt vergeleken met die van röntgenfoto’s aangevuld met een CT-scan. Uit deze studies blijkt dat een aanvullende CT-scan kan leiden tot een verandering in het behandelplan (23% tot 46% van de cases). Een aantal studies in dit cohort keek ook naar de meerwaarde van de CT-scan bij extra-articulaire fracturen. Daarnaast kan de CT-scan eventuele bijkomende letsels van de overige gewrichten en naastgelegen ossale structuren in kaart brengen. Ook dit kan het behandelplan beïnvloeden.
De patiëntenpopulaties in de gevonden studies zijn echter relatief klein en hebben enkele methodologische beperkingen (risk of bias). De bewijskracht van de literatuur is daardoor laag voor de cruciale uitkomstmaat ‘change in treatment’. Derhalve kunnen er op basis van de literatuur geen sterke conclusies worden getrokken over de toegevoegde waarde van een aanvullende CT-scan en spelen aanvullende overwegingen een belangrijke rol bij de keuze voor een aanvullende CT-scan.
Standaard röntgenfoto’s
Om de definitieve diagnose distale radiusfractuur te stellen is beeldvormend onderzoek geïndiceerd. In de regel geldt dat tenminste een PA (postero-anterior) en een zuiver laterale opname worden gemaakt. Bij voorkeur aangevuld met een laterale radio-carpale opname op aanvraag indien geïndiceerd.
Standaard wordt de PA-opname gemaakt met 900 abductie van de schouder en 900 flexie in de elleboog en de pols in neutrale stand. De laterale röntgenopnamen van de pols worden met de schouder in neutrale stand (in 00 abductie van de schouder met de bovenarm langs het lichaam) en de elleboog 900 geflecteerd en een neutrale rotatie van de onderarm gemaakt (Beeres, 2007; Stoffelen, 1999).
Röntgenfoto van de pols PA
De radius en ulna zijn naast elkaar geprojecteerd. De processus styloideus radii toont een enkele contour. De processus styloideus ulnae projecteert aan de uiterst ulnaire zijde. De 2e tot en met 5e CMC gewrichten moeten parallel verlopende gewrichtsoppervlakken tonen. De breedte van de gewrichtsspleten tussen de carpalia is overal gelijk. De derde straal ligt in het verlengde van de radius. Het proximale deel van de metacarpalia is afgebeeld. (figuur 1a)
Röntgenfoto van de pols lateraal
De radius en ulna zijn op elkaar geprojecteerd. Het os lunatum wordt bedekt door het os scaphoideum en het os pisiforme bedekt de distale pool van het scaphoideum (figuur 1b) (Bernau, 1983; Dol, 1997; Hafner, 1976; Long, 2018).
Figuur 1a, 1b, 1c
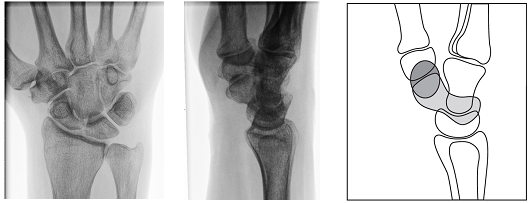
Figuur 1a Een normale PA afbeelding van een normale distale radius. Figuur 1b. Een zuiver laterale polsfoto, waarbij het os pisiforme de distale pool van het os scaphoideum bedekt. Figuur 1c. Schematische weergave van een zuiver laterale polsfoto.
De laterale radio-carpale opname
Hierbij zijn de radius en ulna op elkaar geprojecteerd. Het os lunatum wordt bedekt door het os scaphoideum. De radio carpale gewrichtsspleet wordt open geprojecteerd en de processus styloideus van de radius verschuift naar proximaal (figuur 2).
Figuur 2 Projectierichting derde foto van de pols
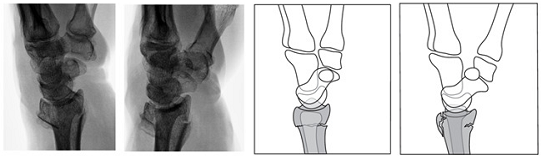
De laterale radio-carpale opname toont het fossa lunatum van de distale radius zonder de overprojectie van het styloid van de radius.
Deze projectie wordt bereikt door plaatsing van een wig met een hoek tussen de 20 en 250 onder de onderarm (figuur 3), de tafel te heffen/kantelen of tijdens de operatie de onderarm bij de hand op te tillen.
Figuur 3
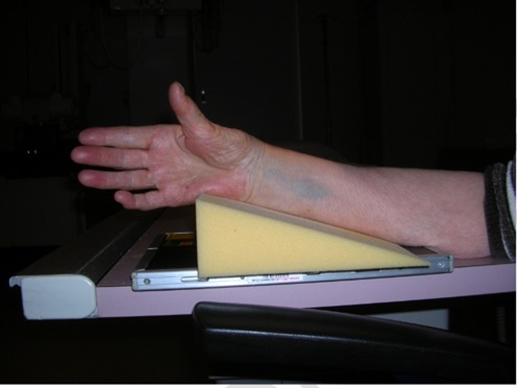
Door het plaatsen van een wig van 20-250 onder de arm, die in neutrale positie blijft, wordt de radio-carpale opname gemaakt.
Normale Anatomie
In de normale anatomie van de distale radius (Medoff, 2005) is er een volaire tilt van 11,20 ± 4,60 en een radiale inclinatie van 24,70 ± 2.50 bij vrouwen en 22,50 ± 2,10 bij mannen (figuur
4).
Figuur 4
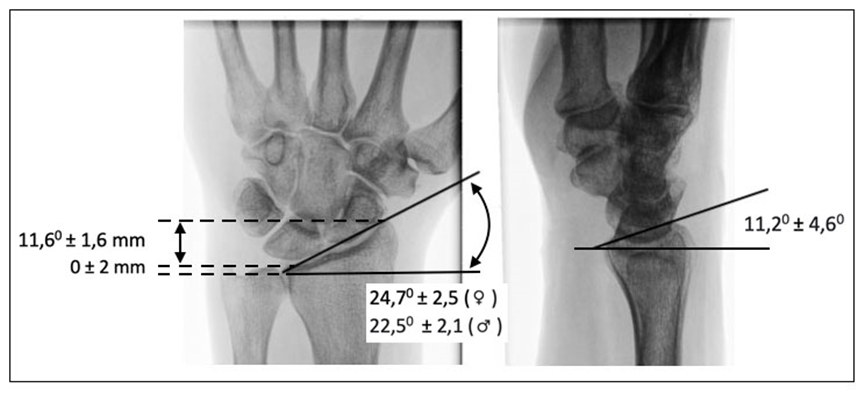
Hoeken van het distale radius oppervlak. VLNR: radiale lengte, radiale inclinatie, volaire tilt.
De radiale lengte (11,6 ± 1,6 mm) is gerelateerd aan de inclinatie en de ulnaire variantie (0 ± 2 mm) geeft de onderlinge relatie weer tussen de radius en de ulna in het distaal radio-ulnair gewricht.
Om een beter beeld van de “normale” anatomie van de pols te krijgen kan laagdrempelig een röntgenopname van de contralaterale pols gemaakt worden, ter vergelijking met de aangedane zijde.
CT-scan
De CT-scan wordt gebruikt voor additionele beeldvorming bij meer complexere DRF, voor het beoordelen van het gewrichtsoppervlak bij intra-articulaire/comminutieve fracturen en voor preoperatieve planning van een operatie.
De CT-scan geeft in de meeste gevallen een duidelijker beeld van het fractuurtype (four-corner concept (Brink, 2016)) en het intra-articulaire verloop door het radio-carpale en distale radio-ulnaire gewricht. Ook de mate van comminutie, de mate van dislocatie/translatie en de grootte van intra-articulaire dislocatie kan op de CT-scan goed in drie richtingen worden bepaald.
Advies met betrekking tot techniek:
Multi-detector CT (MDCT) met submillimeter coupes (≤ 1mm). Reconstructie beelden (MPR) in axiale, coronale en sagittale richting.
Voor preoperatieve planning kan afhankelijk van de wens van de chirurg en lokale afspraken aanvullende 3D reconstructies of reconstructie in andere vlakken vervaardigd worden.
Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)
Het belangrijkste doel van de Röntgendiagnostiek is de fractuur aantonen of uitsluiten.
Een aanvullende CT-scan is in een aantal gevallen nodig om een juiste (of gerichtere) diagnose te krijgen voor een optimale behandeling.
De CT-scan geeft een kleine hoeveelheid extra stralingsbelasting (0,01 en 0,02 mSv) voor de patiënt boven op de straling van de reeds verrichte conventionele foto’s (< 0,005 mSv). De extra stralingsbelasting van een CT-pols is vergelijkbaar met 2 dagen natuurlijke achtergrondstraling (Brink, 2019) en valt onder de categorie minimale stralingsbelasting: < 0,1 mSv (Torabi, 2019).
Een CT-scan brengt extra onderzoek- en wachttijd voor de patiënt op de SEH of in het ziekenhuis met zich mee. Dit is afhankelijk van de lokale logistieke afspraken en wachttijden.
Kosten (middelenbeslag)
Uitvoeren van een CT-scan leidt tot extra kosten; de arbeidstijd voor het maken van de scan en het beoordelen van de beelden (laborant en radioloog) en kosten voor dataopslag. In het artikel van Kleinlugtenbelt (2017) wordt gesproken van additionele kosten van €250,- per scan. Daarentegen kan de verkregen informatie over de fractuur het behandelplan beïnvloeden en mogelijk complicaties of problemen (resulterend in extra bezoeken aan poli en/of extra operaties) beperken of voorkomen. Een sneller of beter herstel van functie levert winst voor de patiënt op en een afname van de totale kosten. De totale kostenbesparing is moeilijk vast te stellen.
Aanvaardbaarheid, haalbaarheid en implementatie
De standaarddiagnostiek bij verdenking op een distale radiusfractuur bestaat uit het maken van conventionele röntgenopnames. Naast deze standaard is een aanvullende CT-scan breed geaccepteerd voor nadere analyse van een complexe of intra-articulaire distale radius fractuur. In vrijwel alle ziekenhuizen bestaat de mogelijk om een aanvullende CT-scan te verrichten. Dit vindt plaats zowel aansluitend op het conventionele onderzoek, al dan niet via de SEH, of op korte termijn via de poliklinische controle.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Röntgenfoto’s
Om een DRF te diagnosticeren wordt standaard conventioneel röntgenonderzoek gebruikt, tenminste in twee richtingen (PA en lateraal) en vaak met een standaard derde opname (radio-carpale opname). Deze beeldvorming is gebruikelijk in Nederland en blijft noodzakelijk als eerste vorm van diagnostiek.
CT scan
Bij complexe en/of intra-articulaire distale radius fracturen geeft de CT-scan een duidelijker beeld van het fractuurtype en het intra-articulaire verloop en daarnaast de mate van dislocatie en comminutie van de fractuur. De CT-scan heeft hier een toegevoegde waarde voor het behandelplan.
Dit wordt onderbouwd door beschikbare literatuur, waarin blijkt dat het behandelplan door een preoperatieve CT-scan regelmatig verandert; bijvoorbeeld van niet-operatief naar operatief of van minimaal invasief naar ORIF (open repositie met interne fixatie).
Onderbouwing
Voor de diagnostiek en beoordeling van distale radiusfracturen is beeldvorming noodzakelijk. Standaard worden in Nederland conventionele röntgenfoto’s gemaakt voor het stellen van de diagnose. Bij twijfel of er sprake is van een intra-articulaire fractuur of om extra informatie te krijgen over een reeds aangetoonde (intra-articulaire) distale radiusfractuur (DRF) kan een CT-scan worden gemaakt. Momenteel is nog onduidelijk wat de toegevoegde diagnostische waarde is van een aanvullende CT-scan en welke invloed deze scan heeft op (mogelijke) veranderingen in het behandelplan (bijvoorbeeld niet-operatief versus operatief, type osteosynthese, duur van de immobilisatie, et cetera).
|
Low GRADE |
Performing a CT-scan in addition to conventional radiographs possibly results in treatment changes in patients with an intra-articular distal radius fracture.
Sources: (Arora, 2010; Brink, 2019; Das Gracas, 2015; Katz, 2001; Kleinlugtenbelt, 2017) |
Description of studies
Arora (2010) performed a cohort study and determined whether the addition of a multidetector CT-scan results in changes in the evaluation of intra-articular DRF and thus changes in the plans for further management. Two authors assessed the eligibility of 319 patients who presented displaced DRFs and selected 117 patients with 120 intra-articular DRF. Characteristics of the patients were not provided in the article. All patients received a radiograph and multidetector CT-scan within three days of injury. This study consisted of 3 cycles. In cycle 1, three orthopaedic surgeons reviewed radiographs in blinded fashion and commented on the desired method of treatment. In cycle 2 (one to three months later), they were given both radiographs and the multidetector CT-scans. In cycle 3 (12 to 36 months later), cycle 2 was repeated. Observers were asked to determine choice of treatment.
Brink (2019) performed a single-institution, prospective cohort study in 98 patients suspected to have a wrist injury, i.e. suspected carpal, distal radius or distal ulnar fractures (median age: 53, range: 18 to 87, 63%F/37%M). All patients underwent conventional radiography, followed by a low dose single-shot wrist CT-scan, after which they were followed for one year. Three surgeons proposed a treatment regimen (functional, cast, reduction, or operative) based on clinical and radiological data; first, based on conventional radiographs and second, based on the CT-scan performed two months later. Authors assessed any treatment changes after CT imaging took place.
Das Graças Nascimento (2015) conducted a cross-sectional study by observing images from 61 patients admitted to the hospital for a DRF. Seventeen observers participated in the study (i.e. 4 hand surgery residents, 4 orthopaedics residents, 6 hand surgeons, 3 orthopaedists), thus a total of 1037 evaluations were assessed. Initially, radiographs alone were evaluated, followed by the same initial radiographs and the associated CT-scans four weeks later. Outcome was assessed regarding the change of surgical treatment (decrease/less invasive, unchanged, increase/more invasive).
Katz (2001) performed a cohort study and determined whether the addition of CT-scanning results in changes in the evaluation of intra-articular DRF. Four hand surgeons independently evaluated 15 intra-articular DRFs. Characteristics of the patients were not provided in the article. Observers evaluated the plain radiographs and 2 to 4 weeks later they reviewed in a random order the plain radiographs with their corresponding CT-scans. Both times observers were asked to determine choice of treatment.
Kleinlugtenbelt (2017) performed a cohort study of 51 patients with displaced intra-articular DRFs (mean age: 50 years ± 14, 75%F/25%M). Four surgeons were asked to predict the usefulness of CT-scans to facilitate choice of treatment plan and/or pre-operative planning. They evaluated scans at 4 time points, resulting in 816 observations (4 surgeons, 51 patients, 4 time points). Instead of patients, number of observations were evaluated.
Surgeons scored the images at four time points (T1-T4) using an interval of at least 4 weeks. At T1 and T2, surgeons evaluated radiographs and assessed: type of fracture (intra- or extra-articular), choice of treatment (operative or nonoperative), whether they would request a CT-scan for pre-operative planning. At T3 and T4, surgeons evaluated X-rays plus their corresponding CT-scan and were asked about: choice of treatment (operative or nonoperative) and the usefulness of the CT-scan for pre-operative planning. The percentage of cases for which a change of treatment plan was indicated has been assessed.
Results
Change in treatment
Arora (2010) concluded that the addition of multidetector CT to plain radiographs frequently changes the therapeutic recommendations. Treatment strategies made by three orthopaedic surgeons (n=360) based on radiographs alone were compared with radiographs and multidetector CT-scans together. Overall, treatment plans changed in 82 of 360 (23%) treatment strategies with the addition of a multidetector CT-scan.
More specifically, closed reduction and plaster-of-Paris cast immobilization was recommended in 223 of 360 (62%) strategies based on radiographs alone. This number decreased to 160 of 360 (44%) when radiographs were supplemented with multidetector CT-scans.
Percutaneous pinning with or without external fixator was recommended in 111 of 360 (31%) strategies based on radiographs alone. This number increased to 140 of 360 (39%) when radiographs were supplemented with multidetector CT-scans.
Open reduction and internal fixation were recommended in 26 of 360 (7%) strategies based on radiographs alone. This number increased to 60 of 360 (17%) when radiographs were supplemented with multidetector CT-scans.
Brink (2019) concluded that a low dose single-shot CT-scan in patients with clinical suspicion of wrist injury increases accuracy of fracture detection and impacts the therapy in this population.
Of all 100 radiographs, there were 39 fractures of the distal radius. CT-scan identified 41 distal radius fractures, of which, 32 had a radio-carpal intra-articular component resulting in an area under the curve for intra-articular fracture detection of 0.87 (95%CI 0.77 to 0.96) for radiographs and 0.96 (95%CI 0.91 to 1.00) for CT-scan. Thus, a CT-scan increases the accuracy of fracture detection.
Authors found therapeutic changes (upgrading or downgrading) in a substantial proportion of all wrist injuries; however, the authors do not specify how often this was the case in distal radius fractures.
Das Graças Nascimento (2015) affirms that the CT can be considered as an adjuvant method, rather than a substitute, for radiographs. A total of 61 patients were evaluated by 17 surgeons (1037 evaluations). Based on the evaluation of radiographs plus the associated CT-scans, 53 (5%) procedures changed to a less invasive treatment, 140 (14%) procedures changed to a more invasive treatment, and 844 (81%) procedures remained unchanged.
Katz (2001) considered CT-scanning as a useful radiographic adjunct in the assessment of intra-articular DRF. The additional information afforded by CT (for example DRUJ involvement, degree of comminution, and articular gapping) influenced management of intra-articular DRF. Four observers assessed 15 cases. Cases classified as nonsurgical based on plain radiographs alone were infrequently changed to surgical after review of an additional CT-scan (2 observers did not make changes, 2 observers made changes in 24% to 46% of cases). Most changes occurred in cases initially treated closed surgically and subsequently converted to an open surgical technique, as 62% to 92% of cases changed. Changes from open to closed surgical procedures ranged from 0% to 17%. For all observers, CT-scanning resulted in no changes between surgical to nonsurgical treatment.
Kleinlugtenbelt (2017) 688 observations of radiographs of intra-articular DRF were included (i.e. radiographs). Surgeons were reasonably able to predict the usefulness of an additional CT-scan for choice of treatment (operative or nonoperative). However, the usefulness of a CT-scan for pre-operative planning was much harder to predict.
Of the 688 radiographs observations, the surgeon requested an additional CT-scan for choice of treatment in 198 cases (29%). With the additional CT-scan, surgeons changed their treatment plan in 41% (82/198) of the cases. When a CT-scan was not requested initially, surgeons changed their treatment plan in 17% (85/490) of cases, after the additional CT-scan. In total, the additional CT-scan changed treatment in 24% (167/688) of the DRFs.
In 474 observations (474/688, 69%), the surgeon decided to treat the patient operatively based on radiographs. The surgeon requested a CT-scan for pre-operative planning in 348 cases (348/474, 73%), and the additional CT-scan was assessed as useful (i.e. good outcome) in 80% (277/348) of the time. When a CT-scan was not requested (126/474, 27%), the additional CT-scan was assessed as useful (i.e. good outcome) in 45% (57/126) cases. Results are summarized in Table 1.
Table 1 Summary of treatment changes. Source: Kleinlugtenbelt (2017)
|
DRFs (n=688): all patients received conventional radiographs + CT-scan |
||
|
Choice of treatment (n=688) |
Changed treatment |
|
|
Surgeon requested an additional CT-scan for choice of treatment |
198 (29%) |
82 (41%) |
|
Surgeon did not request an additional CT-scan for choice of treatment |
490 (71%) |
85 (17%) |
|
Operative treatment based on radiographs (n=474) |
CT useful |
|
|
Surgeon requested an additional CT-scan for pre-op planning |
348 (73%) |
277 (80%) |
|
Surgeon did not request an additional CT-scan for pre-op planning |
126 (27%) |
57 (45%) |
Table 2 provides a brief overview of the selected studies regarding the reported treatment change based on conventional radiographs plus an additional CT-scan.
Table 2 Overview of treatment changes in percentages
|
Study reference |
No. of patients |
Treatment change |
|
Arora, 2010 |
N=117 patients with 120 intra-articular DRFs |
23% |
|
Das Gracas, 2015 |
N=61 patients with intra-articular DRFs |
19% |
|
Katz, 2001 |
N=15 patients with intra-articular DRFs. |
- 2 of 4 observers: 0% - 2 of 4 observers: 24% to 46% |
|
Kleinlugtenbelt, 2017 |
N=51 patients with intra-articular DRFs |
24% |
Level of evidence of the literature
The level of evidence regarding the outcome measure ‘change in treatment’ started as high and was downgraded by two levels to low because of study limitations (risk of bias, -1) and the relatively small number of included patients (imprecision, -1).
A systematic review of the literature was performed to answer the following question:
What is the effect of a CT-scan in addition to conventional radiographs in the decision for a treatment of patients with a (suspected) distal radius fracture?
P: patients with a (suspected) distal radius fracture;
I: conventional radiographs + CT-scan;
C: conventional radiographs:
Ref: Clinical course.
O: change of treatment plan.
Relevant outcome measures
The guideline development group considered ‘change of treatment plan’ as a critical outcome measure for decision making; ‘number needed to treat’ as an important outcome measure for decision making.
A priori, the working group did not define the outcome measures listed above but used the definitions used in the studies.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms from 1995 until 30 January 2020. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 274 hits.
Studies were selected based on the following criteria: RCTs or observational studies comparing conventional radiographs + CT-scan with conventional radiographs alone in patients with a (suspected) distal radius fracture. There were no other restrictions stated for the search.
Studies were initially selected based on title and abstract screening. Full texts of 22 studies were evaluated for inclusion. After reading the full text, 17 studies were excluded (see the table with reasons for exclusion) and 5 studies were included.
Results
Five studies were included in the analysis of the literature. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
- Arora S, Grover SB, Batra S, Sharma VK. Comparative evaluation of postreduction intra-articular distal radial fractures by radiographs and multidetector computed tomography. J Bone Joint Surg Am. 2010;92:2523–2532. doi: 10.2106/JBJS.I.01617.
- Beeres F J P, Rhemrev SJ, Hogervorst M, den Hollander P, Jukema GN. Scafoïdfracturen: diagnostiek en therapie. Ned Tijdschr Geneeskd, 2007; 151, 742-747.
- Bernau A, Berquist TH. Orthopaedic positioning in diagnostic radiology. Baltimore: Urban & Schwarzenberg (1983).
- Brink M, Steenbakkers A, Holla M, de Rooy J, Cornelisse S, Edwards MJ, Prokop M. Single-shot CT after wrist trauma: impact on detection accuracy and treatment of fractures. Skeletal Radiol. 2019 Jun;48(6):949-957. doi: 10.1007/s00256-018-3097-z.
- Brink P, Rikli D. Four-Corner Concept: CT-Based Assessment of Fracture Patterns in Distal Radius. J Wrist Surg. 2016 May;5(2):147-51. doi: 10.1055/s-0035-1570462. Epub 2016 Jan 25.
- das Graças Nascimento V, da Costa AC, Falcochio DF, Lanzarin LD, Checchia SL, Chakkour I. Computed tomography's influence on the classifications and treatment of the distal radius fractures. Hand (N Y). 2015 Dec;10(4):663-9. doi: 10.1007/s11552-015-9773-8.
- Dol J, Geers S. Radiodiagnostisch onderzoek. Utrecht: Elsevier/De Tijdstroom (1997).
- Hafner E, Meuli HCh. Röntgenuntersuchung in der orthopädie. Methode und Technik (1976). Bern: H.Huber. ISBN 10: 3456800258 / ISBN 13: 9783456800257.
- Katz MA, Beredjiklian PK, Bozentka DJ, et al. Computed tomography scanning of intra-articular distal radius fractures: does it influence treatment? J Hand Surg Am. 2001;26(3):415–421. doi: 10.1053/jhsu.2001.22930a.
- Kleinlugtenbelt YV, Madden K, Groen SR, Ham SJ, Kloen P, Haverlag R, Simons MP, Bhandari M, Goslings JC, Scholtes VAB, Poolman RW. Can experienced surgeons predict the additional value of a CT scan in patients with displaced intra-articular distal radius fractures? Strategies Trauma Limb Reconstr. 2017;12(2):91–97. doi: 10.1007/s11751-017-0283-9.
- Long B, Rollins J, Smith B. Merrill's Atlas of Radiographic Positioning and Procedures - 3-Volume Set. 14th Edition 2018. Hardcover ISBN: 9780323566674
- Medoff RJ. Essential radiographic evaluation for distal radius fractures. Hand Clin. 2005 Aug;21(3):279-88. doi: 10.1016/j.hcl.2005.02.008.
- Stoffelen, D. (1999). Fracturen van de pols. In L.de Smet (Ed.) Handchirurgie (pp. 29). Antwerpen: Garant.
- Torabi M, Lenchik L, Beaman FD, et al. ACR Expert Panel on Musculoskeletal Imaging: Appropriateness Criteria® Acute Hand and Wrist Trauma. J Am Coll Radiol. 2019 May;16(5S):S7-S17. doi: 10.1016/j.jacr.2019.02.029.
|
Study reference |
Study characteristics |
Patient characteristics |
Index test (test of interest) |
Reference test |
Follow-up |
Outcome measures and effect size |
Comments |
|
Kleinlugtenbelt, 2017 |
Type of study[1]: Cohort
Setting and country: Emergency Department (ED), The Netherlands
Funding and conflicts of interest: Authors declared no conflicts of Interest. Authors received no financial support. |
Inclusion criteria: - Consecutive patients with displaced distal radius fractures were selected from the ED database. - Presented with a displaced DRF in the ED between 01-01-2007 and 02-03-2011. - Aged ≥18y. - No prior fracture or pathology of distal radius. - Both pre- and postreduction plain posterior–anterior and lateral radiographs of the wrist. - Additional post-reduction CT taken within 5d after the reduction.
Exclusion criteria: N.R.
N=51 (816 observations: 4 time-points, 4 assessors)
Mean age ± SD: 50 years ± 14 Sex: 75%F, 25%M |
Describe index test: X-ray + CT scan Cut-off point(s): N.A.
Comparator test[2]: X-ray Cut-off point(s): N.A.
Methods: 4 surgeons reviewed the images at 4 different time points (interval 4wk): T1 and T2 - Pre- and post-reduction plain radiographs T3 and T4 - Pre- and post-reduction plain radiographs and axial, sagittal and coronal planes CT.
|
Describe reference test[3]: None Cut-off point(s): N.A.
|
Time between the index test + reference test: The CT scan was performed a mean of 2.53 days post-reduction (SD 2.21).
For how many participants were no complete outcome data available? N.R.
Reasons for incomplete outcome data? N.R.
|
Treatment change CT for all N=688 intra-articular fractures, in 167 observations (24%) the additional CT changed treatment.
CT scan for OR indication CT requested n=198 surgeon requested a CT scan: 82/198 (41%) surgeon changed their treatment plan due to the additional CT scan. NNS: 2.6 / NNH: 3.1
CT not requested (CT for all) n=490 CT scan not requested: 85/490 (17%) surgeon changed their treatment plan due to the additional CT scan. NNS: 4.3 / NNH: 1.3
CT scan for OR preparation CT requested n=348 surgeon requested a CT scan: 277/348 (80%) surgeon changed their treatment plan due to the additional CT scan. NNS: 1.3 / NNH: 3.7
CT not requested (CT for all) n=126 CT scan not requested: 57/126 (45%) surgeon changed their treatment plan due to the additional CT scan. NNS: 1.4 / NNH: 3.4 |
Authors’ conclusions: - Surgeons can predict the usefulness of an additional CT scan for intra-articular displaced DRF regarding operatively or nonoperatively approach. - Authors recommend letting surgeons decide which patients require an additional CT scan for treatment planning. - However, for pre-operative planning the usefulness of CT-scans is harder to predict, thus authors could not strongly recommend CT scanning of all patients with a displaced intra-articular DRF.
Considerations: + surgeons were blinded + images were randomized - potential risk of clustering - protocol in hospital was to always order a CT scan for operatively treated cases |
|
Katz, 2001 |
Type of study: Cohort
Setting and country: Hospital of the University of Pennsylvania, USA
Funding and conflicts of interest: No benefits in any form have been received or will be received from a commercial party related directly or indirectly to the subject of this article. |
Inclusion criteria: - Radiocarpal joint involvement. - Adequate orthogonal plain X-rays of the distal radius including posteroanterior, lateral, and oblique views. - Pre- and post-reduction plain X-rays. - Fine-cut (1-2mm intervals) CT scans with multiplanar or reconstruction images incl. axial, coronal, and sagittal planes.
Exclusion criteria: Cases lacking any of the criteria were eliminated from the study. Type or severity of fractures was not a factor.
N=15 Mean age: N.R. Sex: N.R. Other: N.R. |
Describe index test: X-ray + CT scan Cut-off point(s): N.A.
Comparator test[4]: X-ray Cut-off point(s): N.A.
Methods: 15 cases were blindly presented independently to 4 orthopaedic hand surgeons. 1) Observations based on plain X-rays. 2) 4wks later they reviewed in a random order the plain X-rays + corresponding CT images and again were asked to determine the measurements and treatment for each fracture. |
Describe reference test[5]: None Cut-off point(s): N.A.
|
Time between the index test + reference test: 4 weeks
For how many participants were no complete outcome data available? N.R.
Reasons for incomplete outcome data? N.R.
|
Treatment change Changes in treatment from nonsurgical to surgical after review of CT scans: - 2 observers did not make changes. - 2 observers made changes in 24% to 46% of cases.
Changes in treatment from closed to open surgical management after review of CT scans: 62% to 92% of cases changed.
Changes in treatment from open to closed surgical management after review of CT scans: 0% to 17% of cases changed.
For all 4 observers, CT scanning resulted in no changes between surgical to nonsurgical treatment. |
Authors’ conclusion: CT scanning influenced observers to change treatment plans and resulted in increased interobserver reliability in the proposed management of these injuries.
Limitations: - retrospective design. - relatively small sample size. - inability to standardize plain x-rays or CT scanning techniques. - 2001 versus. 2020: nowadays newer techniques.
|
|
Arora, 2010 |
Type of study: Cohort
Setting and country: Medical College & Safdarjung Hospital, New Delhi, India.
Funding and conflicts of interest: No external funding source for the present study. |
Inclusion criteria: - closed fractures. - intra-articular extension. - aged >18 years. - A less than 2wk old injury. - Adequate orthogonal pre-reduction and post-reduction radiographs.
Exclusion criteria: Pathological fractures and fractures associated with other serious life-threatening injuries.
N=117 patients with 120 intraarticular distal radial fractures.
Mean age: N.R. Sex: N.R. Other characteristics: N.R.
|
Describe index test: X-ray + Multidetector CT scan Cut-off point(s): N.A.
Comparator test[6]: X-ray Cut-off point(s): N.A.
Methods: X-rays of 319 patients were assessed by 2 authors for eligibility for the study. This left 117 patients (120 wrists) with acute intra-articular DRFs, who all received an multidetector CT scan (within 3d after injury). Cycle 1: 3 authors received blinded X-rays. Cycle 2: 3mo later, they received both X-rays and the multidetector CT scans. Cycle 3: 12-30mo later, cycle 2 was repeated. |
Describe reference test[7]: None Cut-off point(s): N.A.
|
Time between the index test + reference test: Multidetector CT-scan was performed within 3 days after injury.
For how many participants were no complete outcome data available? N.R.
Reasons for incomplete outcome data? N.R.
|
Treatment change The recommended treatment plan changed in 23% of the cases when the evaluation included multidetector CT scan in addition to conventional X-rays.
Closed reduction and plaster-of-Paris cast immobilization X-ray: 223/360 X-ray + CT scans: 160/360 P<0.001
Percutaneous pinning with or without external fixator X-ray: 111/360 X-ray + CT scans: 140/360 P<0.001
Open reduction and internal fixation X-ray: 26/360 X-ray + CT scans: 60/360 P<0.001
|
Authors’ conclusion: Multidetector CT scan provides more accurate information regarding the anatomy of intra-articular distal radial fractures than X-ray does. X-rays often underestimate the fracture characteristics, and the addition of multidetector CT frequently changed the treatment recommendations in such cases.
Limitations: - 3 observers to recommend treatment strategies. Interobserver agreement can vary with knowledge and experience. - Cost factors and the evaluation of treatment outcome were not considered. |
|
Das Gracas, 2015 |
Type of study: Cross-sectional study
Setting and country: Orthopedic Service, Hospital, São Paulo, Brazil
Funding and conflicts of interest: Authors declared no competing interests. |
Inclusion criteria: - ≥ 18 years of age with distal radius fractures, irrespective of gender, race, or laterality. - At the time of hospital admission, their radiographic images were taken in the 4 projections. - Their sagittal, axial, and coronal CT scans obtained.
Exclusion criteria: - Patients who were skeletally immature. - Inappropriate or insufficient images. - Soft tissue injuries, associated fractures, and bone quality were not considered.
N=61
Mean age: N.R. Sex: N.R. Other characteristics: N.R. |
Describe index test: X-ray + CT scan Cut-off point(s): N.A.
Comparator test[8]: X-ray Cut-off point(s): N.A.
Methods: 17 observers participated who assessed 61 patients. 1) X-rays 2) 4wks later: X-rays + CT scans
|
Describe reference test[9]: None Cut-off point(s): N.A.
|
Time between the index test en reference test: 4 weeks.
For how many participants were no complete outcome data available? N.R.
Reasons for incomplete outcome data? N.R.
|
Surgical treatment change Total Decrease: 53 (5.1%) Unchanged: 844 (81.4%) Increase: 140 (13.5%) p=0.020
Orthopaedic residents Decrease: 13 (5.3%) Unchanged: 191 (78.3%) Increase: 40 (16.4%) p>0.05
Hand surgery residents Decrease: 16 (6.6%) Unchanged: 200 (82%) Increase: 28 (11.5%) p>0.05
Decrease: 22 (6%) Unchanged: 305 (83.3%) Increase: 39 (10.7%) Significant p<0.05
Orthopaedic surgeons Decrease: 2 (1.1%) Unchanged: 148 (80.9%) Increase: 33 (18%) Significant p<0.05 |
Authors’ conclusion: CT scans brought little change to the final treatment as recommended by surgeons. The less experienced in hand surgery the observer was, the more important CT was for determining the fracture pattern. |
|
Brink, 2019 |
Type of study: single-institution, prospective cohort study
Setting and country: Dept. Radiology, Nijmegen, The Netherlands
Funding and conflicts of interest: - Study did not receive any specific grant from funding agencies in the public, commercial, or not-for-profit sectors. - Authors 1+7: received research grants and a speaker honorarium from Canon Medical Systems. - Author 7: received a speaker honorarium from Bracco and Bayer. |
Inclusion criteria: - Aged ≥18 years. - Scheduled for conventional X-ray because of clinical suspicion of wrist trauma not older than 3 days. à patients with clinical suspicion of wrist injury.
Exclusion criteria: - no physical evaluation by a physician before imaging. - open fractures. - patients could not be positioned in upright position because of immobilization on a spine board or transfer to the ICU. - no informed consent or no prospective data collection could be obtained.
N=98 patients with 100 wrists. X-rays detected true-positive fractures in 45, and CT in 61 wrists.
Median age (range): 53(18-87) Sex: 63%F/37%M
|
Describe index test: X-ray + CT scan Cut-off point(s): N.A.
Comparator test[10]: X-ray Cut-off point(s): N.A.
|
Describe reference test[11]: None Cut-off point(s): N.A.
|
Time between the index test en reference test: Taken om the same day. 1) 3 trauma surgeons observed X-ray and proposed a treatment plan. 2) at least 2 months later: observers proposed a treatment plan after reviewing the same X-ray, with addition of the CT findings.
For how many participants were no complete outcome data available? Scans: 100% complete.
Patient questionnaires: 45p baseline, 43p 6 wk, 37p 1y complete
Reasons for incomplete outcome data? N.R. |
Area under the curve X-ray: 0.85 (95%CI 0.77-0.93) à sens=75%, spec=85% CT: 0.97 (95% 0.93–1.00) à sens=100%, spec=97%
Change in treatment: Observer 2, 3: 24 wrists (24%, 95%CI 16-33%) Observer 1: 31 wrists (31%, 95%CI 23-41%).
Additional findings: upgrade - Of all 26 wrists with additional findings on CT: 11 wrists (11% of the total population, 95%CI 6-18%) were upgraded (i.e. more aggressive). - No downgrades occurred in patients with additional findings on CT.
No additional findings: upgrade In wrists without additional findings, 11 wrists were upgraded.
No additional findings: downgrade 21 patients (21% of the total population, 95%CI 14-30%) were downgraded in treatment.
Overall, observers downgraded treatment from cast to functional treatments in 14-16% of all patients. |
Authors’ conclusion: A single-shot CT is highly accurate in fracture detection. Compared to X-ray, CT has a higher detection rate, rules out fractures with greater confidence and changes treatment of patients with suspicion of wrist fractures, possibly avoiding unnecessary cast treatment.
Limitations: - Missing data was considered as absent features. Missing data due to LTFU were not included in analysis. - single-site study with a heterogeneous patient group; a large group of patients were excluded à risk of systematic selection bias. - Low response rate on the questionnaires and no standard patient visit during follow-up. à risk on incorporation bias with an overestimation of CT accuracy - Not all patients underwent an oblique view in addition to an anteroposterior and a lateral CR view of the wrist. |
Risk of bias table (QUADAS II, 2011)
|
Study reference |
Patient selection
|
Index test |
Reference standard |
Flow and timing |
Comments with respect to applicability |
|
Kleinlugtenbelt, 2017 |
Was a consecutive or random sample of patients enrolled? Yes. Selected from Emergency Department database (January 2007-March 2011). - 4 time points were assessed (4 comparisons: T1+T2=X-ray only, T3+T4= X-ray+CT. - 204 observations (4 surgeons; 51 cases) per comparison and 816 observations (204 observations; 4 comparisons).
Was a case-control design avoided? Yes
Did the study avoid inappropriate exclusions? No |
Were the index test results interpreted without knowledge of the results of the reference standard? No. But valid interval (≥4 weeks), digitized, and anonymized.
If a threshold was used, was it pre-specified? N.A.
|
Is the reference standard likely to correctly classify the target condition? Unclear (no clear reference)
Were the reference standard results interpreted without knowledge of the results of the index test? Unclear
|
Was there an appropriate interval between index test(s) and reference standard? Yes. Interval: ≥4 weeks (ref=xray, index=xray + ct)
Did all patients receive a reference standard? Yes. Although not clearly stated, no statements regarding missing or incomplete data.
Did patients receive the same reference standard? Yes. Although not clearly stated, no statements regarding missing or incomplete data.
Were all patients included in the analysis? Yes. No statements regarding missing or incomplete data. |
Are there concerns that the included patients do not match the review question? No.
Are there concerns that the index test, its conduct, or interpretation differ from the review question? Unclear.
Are there concerns that the target condition as defined by the reference standard does not match the review question? Unclear. |
|
CONCLUSION: Could the selection of patients have introduced bias? Unlikely
RISK: LOW |
CONCLUSION: Could the conduct or interpretation of the index test have introduced bias? Unclear
RISK: UNCLEAR |
CONCLUSION: Could the reference standard, its conduct, or its interpretation have introduced bias? Unclear
RISK: UNCLEAR |
CONCLUSION: Could the patient flow have introduced bias? Unlikely
RISK: LOW |
||
|
Katz, 2001 |
Was a consecutive or random sample of patients enrolled? Yes. Radiology records of all patients treated for DRF between June 1998-January 1999 were reviewed retrospectively. Adequate plain x-rays and CT images were available for 15 patients. Relatively small sample size.
Was a case-control design avoided? Yes
Did the study avoid inappropriate exclusions? No |
Were the index test results interpreted without knowledge of the results of the reference standard? Yes. Observers were blinded, valid interval (2-4 weeks) between x-ray and x-ray+CTscan.
If a threshold was used, was it pre-specified? N.A.
|
Is the reference standard likely to correctly classify the target condition? Unclear (no clear reference)
Were the reference standard results interpreted without knowledge of the results of the index test? Unclear
|
Was there an appropriate interval between index test(s) and reference standard? Yes. Interval: 2-4 weeks.
Did all patients receive a reference standard? Yes
Did patients receive the same reference standard? Yes
Were all patients included in the analysis? Unclear
|
Are there concerns that the included patients do not match the review question? Unclear. Very small study population (n=15).
Are there concerns that the index test, its conduct, or interpretation differ from the review question? Unclear.
Are there concerns that the target condition as defined by the reference standard does not match the review question? Unclear.
|
|
CONCLUSION: Could the selection of patients have introduced bias? Unlikely
RISK: LOW |
CONCLUSION: Could the conduct or interpretation of the index test have introduced bias? Unlikely
RISK: LOW |
CONCLUSION: Could the reference standard, its conduct, or its interpretation have introduced bias? Unclear
RISK: UNCLEAR |
CONCLUSION Could the patient flow have introduced bias? Unlikely
RISK: LOW |
||
|
Arora, 2010 |
Was a consecutive or random sample of patients enrolled? Yes. 319 patients presented DRFs between 1 July 2006 14 June 2009. Based on selection criteria, 2 observers selected 117 patients with 120 intra-articular DRFs for this study.
Was a case-control design avoided? Yes
Did the study avoid inappropriate exclusions? Unclear
|
Were the index test results interpreted without knowledge of the results of the reference standard? Yes (study was blinded)
If a threshold was used, was it pre-specified? N.A.
|
Is the reference standard likely to correctly classify the target condition? Unclear (no clear reference)
Were the reference standard results interpreted without knowledge of the results of the index test? Unclear
|
Was there an appropriate interval between index test(s) and reference standard? Yes 1 cycle: X-ray 2 cycle: X-ray+CT-scan (1-3 months) 3 cycle: X-ray+CT-scan (12-36 months)
Did all patients receive a reference standard? Yes
Did patients receive the same reference standard? Unclear
Were all patients included in the analysis? Unclear
|
Are there concerns that the included patients do not match the review question? Unclear (in- / exclusion criteria; bias?)
Are there concerns that the index test, its conduct, or interpretation differ from the review question? Unclear (the authors did not consider articular incongruities - step and gap - they evaluated the coronal fracture line, comminution, and central articular depression)
Are there concerns that the target condition as defined by the reference standard does not match the review question? Unclear |
|
|
CONCLUSION: Could the selection of patients have introduced bias? Unclear
RISK: UNCLEAR |
CONCLUSION: Could the conduct or interpretation of the index test have introduced bias? Unlikely
RISK: LOW |
CONCLUSION: Could the reference standard, its conduct, or its interpretation have introduced bias? Unclear
RISK: UNCLEAR |
CONCLUSION Could the patient flow have introduced bias? Unclear
RISK: UNCLEAR |
|
|
Das Gracas, 2015 |
Was a consecutive or random sample of patients enrolled? Yes. 83 patients presented DRFs between June and November 2012. Based on selection criteria, 4 observers selected 61 patients with DRFs for this study.
Was a case-control design avoided? Yes
Did the study avoid inappropriate exclusions? Unclear (inappropriate or insufficient images were excluded) |
Were the index test results interpreted without knowledge of the results of the reference standard? No (study was not blinded, interval of 4 weeks)
If a threshold was used, was it pre-specified? N.A.
|
Is the reference standard likely to correctly classify the target condition? Unclear (no clear reference)
Were the reference standard results interpreted without knowledge of the results of the index test? Unclear
|
Was there an appropriate interval between index test(s) and reference standard? Yes (4 weeks)
Did all patients receive a reference standard? Yes
Did patients receive the same reference standard? Yes
Were all patients included in the analysis? Unclear
|
Are there concerns that the included patients do not match the review question? Unclear
Are there concerns that the index test, its conduct, or interpretation differ from the review question? Unclear
Are there concerns that the target condition as defined by the reference standard does not match the review question? Unclear
|
|
CONCLUSION: Could the selection of patients have introduced bias? Unclear
RISK: UNCLEAR |
CONCLUSION: Could the conduct or interpretation of the index test have introduced bias? Unclear
RISK: UNCLEAR |
CONCLUSION: Could the reference standard, its conduct, or its interpretation have introduced bias? Unclear
RISK: UNCLEAR |
CONCLUSION Could the patient flow have introduced bias? Unlikely
RISK: LOW |
||
|
Brink, 2019 |
Was a consecutive or random sample of patients enrolled? N=98 patients with 100 wrists (single-institution, prospective cohort study)
Was a case-control design avoided? Yes
Did the study avoid inappropriate exclusions? No
|
Were the index test results interpreted without knowledge of the results of the reference standard? No (interval 2mo, blinded)
If a threshold was used, was it pre-specified? N.A.
|
Is the reference standard likely to correctly classify the target condition? Unclear (no clear reference)
Were the reference standard results interpreted without knowledge of the results of the index test? No
|
Was there an appropriate interval between index test(s) and reference standard? Yes (2mo)
Did all patients receive a reference standard? Yes
Did patients receive the same reference standard? Yes
Were all patients included in the analysis? Unclear
|
Are there concerns that the included patients do not match the review question? Unclear (relatively large group was excluded)
Are there concerns that the index test, its conduct, or interpretation differ from the review question? No
Are there concerns that the target condition as defined by the reference standard does not match the review question? Yes (41 fractures in the distal radius detected) |
|
CONCLUSION: Could the selection of patients have introduced bias? Unlikely
RISK: LOW |
CONCLUSION: Could the conduct or interpretation of the index test have introduced bias? Unclear
RISK: UNCLEAR |
CONCLUSION: Could the reference standard, its conduct, or its interpretation have introduced bias? Unclear
RISK: UNCLEAR |
CONCLUSION Could the patient flow have introduced bias? Unclear
RISK: UNCLEAR |
Table of excluded studies
|
Author and year |
Reason for exclusion |
|
Cole, 1997 |
Voldoet niet aan PICO (geen vergelijking CT+röntgen versus röntgen) |
|
Basha, 2018 |
Voldoet niet aan PICO (geen vergelijking CT+röntgen versus röntgen) |
|
Wijffels, 2012 |
Voldoet niet aan PICO (niet de uitkomstmaat ‘change of treatment’) |
|
Arealis, 2014 |
Voldoet niet aan PICO (niet de uitkomstmaat ‘change of treatment’) |
|
Harness, 2006 |
Voldoet niet aan PICO (geen vergelijking CT+röntgen versus röntgen) |
|
Kleinlugtenbelt, 2015 |
Voldoet niet aan PICO (niet de uitkomstmaat ‘change of treatment’) |
|
Ottenin, 2012 |
Voldoet niet aan PICO (geen vergelijking CT+röntgen versus röntgen) |
|
Hunt, 2013 |
Voldoet niet aan PICO (geen vergelijking CT+röntgen versus röntgen) |
|
Balci, 2015 |
Voldoet niet aan PICO (geen vergelijking CT+röntgen versus röntgen) |
|
Heo, 201 |
Voldoet niet aan PICO (geen vergelijking CT+röntgen versus röntgen) |
|
Alagic, 2019 |
Voldoet niet aan PICO (geen vergelijking CT+röntgen versus röntgen, geen DRFs) |
|
Avery, 2014 |
Voldoet niet aan PICO (geen vergelijking CT+röntgen versus röntgen) |
|
Ma, 2017 |
Voldoet niet aan PICO (geen vergelijking CT+röntgen versus röntgen) |
|
Catalano, 2014 |
Narrative review |
|
Kleinlugtenbelt, 2017 |
Voldoet niet aan PICO (niet de uitkomstmaat ‘change of treatment’) |
|
Ricci, 2019 |
Voldoet niet aan PICO (geen vergelijking CT+röntgen versus röntgen, geen DRFs) |
|
Suojarvi, 2015 |
Voldoet niet aan PICO (geen vergelijking CT+röntgen versus röntgen) |
Beoordelingsdatum en geldigheid
Publicatiedatum : 18-08-2021
Beoordeeld op geldigheid : 02-08-2021
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
De richtlijn is ontwikkeld in samenwerking met:
- Nederlandse Orthopaedische Vereniging
- Nederlandse Vereniging voor Plastische Chirurgie
- Nederlandse Vereniging voor Radiologie
- Nederlandse Vereniging van Spoedeisende Hulp Artsen
- Nederlandse Vereniging van Revalidatieartsen
- Koninklijk Nederlands Genootschap voor Fysiotherapie
- Nederlandse Vereniging voor Handtherapie
- Osteoporose Vereniging
Doel en doelgroep
Doel
Deze multidisciplinaire richtlijn bevat aanbevelingen ter ondersteuning van de dagelijkse praktijk voor hulpverleners die zich bezighouden met diagnostiek en behandeling van patiënten met een distale radius fractuur. De aanbevelingen zijn opgesteld op basis van de huidige wetenschappelijke inzichten. De knelpunten die behandelaars ervaren in de dagelijkse zorgpraktijk bij patiënten met een distale radius fractuur dienen als uitgangspunt bij de ontwikkeling van deze richtlijn.
Ter bevordering van de implementatie wordt geadviseerd om deze richtlijn aanknopingspunt te laten zijn voor lokale behandelprotocollen voor patiënten met een distale radius fractuur. Daarnaast kan de richtlijn gebruikt worden bij het geven van voorlichting aan patiënten met een distale radius fractuur.
Doelgroep
Deze richtlijn is bedoeld voor alle zorgverleners die betrokken zijn bij de zorg voor volwassen patiënten met een intra- of extra-articulaire distale radiusfractuur.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2019 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met een distale radius fractuur.
Werkgroep
- Dr. P.F.W. Hannemann, chirurg, werkzaam in het Maastricht UMC te Maastricht, (voorzitter), NVvH
- Dr. N.W.L. Schep, chirurg, werkzaam in het Maasstad Ziekenhuis te Rotterdam, NVvH
- Dr. D.I. Vos, chirurg, werkzaam in het Amphia ziekenhuis te Breda, NVvH
- Dr. R.L.M. Deijkers, orthopaedisch chirurg, werkzaam in het HagaZiekenhuis te Den Haag, NOV
- Dr. J.W. Colaris, orthopaedisch chirurg, werkzaam in het Erasmus UMC te Rotterdam, NOV
- Drs. J. van Loon, plastisch chirurg, werkzaam bij Blooming plastisch chirurgie te Haarlem, NVPC
- Drs. S. Bollen, radioloog, werkzaam in Het Groene Hart Ziekenhuis te Gouda,NVvR
- Drs. G.J.P. Smits, SEH-arts, werkzaam in het Catharina Ziekenhuis te Eindhoven, NVSHA
- Drs. K.S. van Wonderen, AIOS SEH, werkzaam in het St. Antonius ziekenhuis te Nieuwegein, NVSHA
- Dr. G. Zemack, revalidatiearts, werkzaam bij Libra revalidatie audiologie te Eindhoven, NVR
- Dr. F.J.B. Lötters, fysiotherapeut en docent fysiotherapie, werkzaam bij het Hand & Pols Centrum te Dordrecht en Hogeschool Leiden, KNGF, NVvHandtherapie
- H.J.G. van den Broek, voorzitter Osteoporose Vereniging te Haarlem.
Met ondersteuning van
- Drs. T. Geltink, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. S.N. Hofstede, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Hannemann |
Traumachirurg/hand- en polschirurg (FESSH) Maastricht Universitair Medisch Centrum Maastricht |
Plaatsvervangend opleider heelkunde regio VIII (onbetaald); Course director CASH 3 cursus hand- en polschirurgie (onbetaald); Faculty lid AO (betaald); Faculty lid IBRA (betaald); Course director IBRA hand and wrist courses (betaald); Fellowship director IBRA upper limb training center MUMC Maastricht (betaald); Ontwikkeling course modules upper extremity IBRA (betaald); Faculty lid Esser Master class (onbetaald); ATLS instructor (betaald) Opleider HAIO’s (onbetaald) |
Begunstigde ZonMW subsidie aangaande onderzoek naar correctie osteotomie van de distale radius
Begunstigde Inscite subsidie (extern gefinancierd) voor onderzoek naar artrose van het polsgewricht |
Geen actie. De onderwerpen van de gesubsidieerde studies vallen buiten de afbakening van de richtlijn. |
|
Bollen |
Radioloog Groene Hart Ziekenhuis Gouda |
Geen |
Geen |
Geen actie. |
|
Deijkers |
Orthopedisch Chirurg HagaZiekenhuis Den Haag. |
Voorzitter Hand en Pols Werkgroep van de NOV (onbetaald); Organisator A&A Hand and Wrist Course Utrecht (onbetaald); Instructeur Dutch Wrist Arthroscopy Course (DWAC) (onbetaald); Voorzitter Commissie Certificering Subspecialisatie Handchirurgie van de Nederlandse Vereniging voor Handchirurgie (onbetaald) |
Geen |
Geen actie. |
|
van de Broek |
Voorzitter Osteoporose Vereniging (onbezoldigd)
|
Bestuurslid Energiek Heusden (energie coöperatie,(onbetaald); DGA eigen holding BV (pensioenrechten, betaald) |
Geen |
Geen actie. |
|
Van Loon |
Plastisch chirurg RKZ Beverwijk |
CFO Beverwijk Skin and Scar Company, Haarlem (betaald) |
Geen |
Geen actie. |
|
Colaris |
Orthopedisch chirurg - traumatoloog /hand- en polschirurg (FESSH) |
NOV bestuurslid (onkostenvergoeding); Bestuurslid Orthopedische Traumatologie Portefeuillehouder CCOC (onbetaald); Bestuurslid werkgroep hand-pols NOV (onbetaald); Bestuurslid werkgroep AI NOV (onbetaald); Bestuurslid Zuid West Overleg Traumatologie (onbetaald); Bestuurslid en co-founder BIG hand event (onbetaald); Faculty AO (betaald); Faculty OTC (betaald); Faculty Dutch wrist course (onbetaald); Faculty Esser Master Class (onbetaald) |
ZonMw subsidie voor uitwerking CAST-studie waarbij gereponeerde distale radiusfracturen ofwel in circulair gips ofwel in een gipsspalk worden geïmmobiliseerd. |
Geen actie. |
|
Zemack |
Revalidatiearts, Libra Revalidatie & Audiologie, Eindhoven, Tilburg en Weert. |
Voorzitter van de geaccrediteerde Werkgroep Trauma Revalidatie (WTR) van de VRA (Nederlandse Vereniging van Revalidatieartsen) (onbetaald) |
Geen |
Geen actie. |
|
Smits |
SEH-arts KNMG, Catharinaziekenhuis Eindhoven. |
PhD candidate, TU/e (onbetaald); Docent spoedzorg, Schola Medica Utrecht (betaald) |
Geen |
Geen actie. |
|
Lötters |
Hand-/fysiotherapeut, Bewegingswetenschapper bij Hand en Pols Revalidatie Nederland, locaties Den Haag en Dordrecht |
Docent bij de opleiding fysiotherapie bij de Hogeschool Leiden. |
Geen |
Geen actie. |
|
Schep |
Traumachirurg/hand- en polschirurg (FESSH), Maasstad Ziekenhuis Rotterdam, tevens werkzaam in het Spijkenisse Medisch Centrum |
Bestuurslid Ned. Ver. Handchirurgie (onbetaald); Bestuurslid Big Hand Event (onbetaald); Instructeur Dutch Wrist Ascopie course (onbetaald); Consultant Synthes, Arthrex: betrokken bij cursussen (betaald); Chairman diverse AO cursussen (onkosten vergoeding); Instructeur IBRA course (onkosten vergoeding); Instructeur CASH cursus handfracturen (onkosten vergoeding); Editor boek Leidraad chirurgie co- assistent revenuen; Consultant KLS Martin (betaald) |
Echtgenote heeft een medisch congres bureau. Geen relatie met deze richtlijn; Begunstigde diverse Zonmw subsidies voor onderzoek naar handfracturen, geen relatie met deze richtlijn; Meerdere publicaties aangaande de distale radius die ook in deze richtlijn aan bod komen.
|
Geen actie. |
|
Vos |
Traumachirurg Amphia Ziekenhuis Breda |
Lid klachten-commissie, Jeroen Bosch ziekenhuis den Bosch, (betaald); Lid kwaliteitsvisitatie commissie NVvH (onkostenvergoeding); ATLS instructor (betaald); AO faculty (betaald); consultant Operace Johnson & Johnson (betaald) |
Geen |
Geen trekker of meelezer bij uitgangsvragen over platen. |
|
Van Wonderen |
AIOS SEH bij st. Antoniusziekenhuis te Nieuwegein/Utrecht |
geen |
Geen |
Geen actie. |
Inbreng patiëntenperspectief
Voor de totstandkoming van deze richtlijn is aandacht besteed aan het patiëntenperspectief door uitnodigen van Patiëntenfederatie Nederland en patiëntenvereniging Osteoporose Vereniging voor de invitational conference en door middel van het aanstellen van een afgevaardigde van patiëntenvereniging Osteoporose Vereniging als lid van de werkgroep. Aanvullend zijn er door de Patiëntenfederatie Nederland patiëntervaringen verzameld door een vragenlijst uit te sturen onder het Zorgpanel van de Patiëntenfederatie. Het verslag hiervan (zie de bijlagen) is besproken in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de Osteoporose Vereniging en de Patiëntenfederatie en de daarbij aangeleverde commentaren zijn bekeken en verwerkt.
Methode ontwikkeling
Evidence based
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten met een distale radius fractuur. De werkgroep beoordeelde de aanbeveling(en) uit de eerdere richtlijnmodules (Nederlandse Vereniging voor Heelkunde, 2010) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door de Beroepsvereniging Verzorgenden Verpleegkundigen (V&VN), de Nederlandse Vereniging van Revalidatieartsen (VRA), het Koninklijk Nederlands Genootschap voor Fysiotherapie (KNGF), de Nederlandse Vereniging voor Handtherapie (NVHT) en de Nederlandse Vereniging voor Heelkunde (NVvH) via een schriftelijke invitational conference. Daarnaast is er een enquête uitgezet onder het Zorgpanel van de Patiëntenfederatie. Het rapport hiervan is opgenomen in de bijlagen.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvragen behorende bij de uitgangsvragen inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt gerelateerd) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur en de beoordeling van de risk-of-bias van de individuele studies is te vinden onder ‘Zoeken en selecteren’ onder ‘Onderbouwing’. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello, 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE-methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE-gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module 'Organisatie van zorg'.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID) 1995-jan. 2020 Engels |
1 Radius Fractures/ (8987) 2 (((distal adj3 (radius or radial)) or wrist or colles or smith*) adj3 fracture*).ti,ab,kf. (7033) 3 1 or 2 (12037) 9 exp Tomography, X-Ray Computed/ or ((compute* adj3 tomograph*) or ct-scan or (cat adj scan*)).ti,ab,kf. (578513) 10 3 and 9 (651) 11 limit 10 to (english language and yr="1995 -Current") (530) 12 (meta-analysis/ or meta-analysis as topic/ or (metaanaly* or metanaly* or meta-analy*).ti,ab,kf. or ((systematic* or scoping or evidence based) adj3 (review* or overview*)).ti,kf. or ((evidence or research) adj3 synthesis).ti,kf. or systematic review.pt. or (prisma or (("structured literature" or comprehensive or "quantitative literature" or evidence-based) adj2 (search or review)) or "systematic search" or ((systemic or systematized) adj3 review) or "systematic research synthesis" or (review* adj3 independent*)).ti,ab,kf. or (((quantitative or rapid or short or critical* or structured or comparative or comparitive or evidence or comprehensive) adj3 (review* or overview*)).ti. and search.ab.) or "Review Literature as Topic"/ or cochrane.jw. or (cochrane or embase or medline or cinahl or cinhal or cancerlit).ab. or (("selection criteria" or "data extraction").ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (352041) 13 11 and 12 (7) 14 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1943566) 15 11 and 14 (61) 16 exp "Sensitivity and Specificity"/ or (Sensitiv* or Specific*).ti,ab. or (predict* or ROC-curve or receiver-operator*).ti,ab. or (likelihood or LR*).ti,ab. or exp Diagnostic Errors/ or (inter-observer or intra-observer or interobserver or intraobserver or validity or kappa or reliability).ti,ab. or reproducibility.ti,ab. or (test adj2 (re-test or retest)).ti,ab. or "Reproducibility of Results"/ or accuracy.ti,ab. or Diagnosis, Differential/ or Validation Studies.pt. (6376329) 17 11 and 16 (227) 18 13 or 15 (65) 19 17 not 18 (186) |
274 |
|
Embase (Elsevier) |
(((('distal radius fracture'/exp/mj OR ((distal NEAR/3 (radius OR radial) NEAR/3 fracture*):ti,ab) OR (((wrist OR colles OR smith*) NEAR/3 fracture*):ti,ab)) NOT 'conference abstract':it AND (english)/lim AND ((embase)/lim OR (pubmed-not-medline)/lim) AND (1995-2020)/py) AND ('computer assisted tomography'/exp/mj OR (((compute* NEAR/3 tomograph*):ti,ab) OR 'ct scan':ti,ab OR ((cat NEAR/1 scan*):ti,ab)))) AND (('meta analysis'/exp OR 'meta analysis (topic)'/exp OR 'systematic review (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review):ti) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab) NOT (('animal'/de OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) NOT ('conference abstract':it OR 'conference review'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it))) OR (('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it)) (35) > 6 uniek ('sensitivity and specificity'/de OR sensitiv*:ab,ti OR specific*:ab,ti OR predict*:ab,ti OR 'roc curve':ab,ti OR 'receiver operator':ab,ti OR 'receiver operators':ab,ti OR likelihood:ab,ti OR 'diagnostic error'/exp OR 'diagnostic accuracy'/exp OR 'diagnostic test accuracy study'/exp OR 'inter observer':ab,ti OR 'intra observer':ab,ti OR interobserver:ab,ti OR intraobserver:ab,ti OR validity:ab,ti OR kappa:ab,ti OR reliability:ab,ti OR reproducibility:ab,ti OR ((test NEAR/2 're-test'):ab,ti) OR ((test NEAR/2 'retest'):ab,ti) OR 'reproducibility'/exp OR accuracy:ab,ti OR 'differential diagnosis'/exp OR 'validation study'/de OR 'measurement precision'/exp OR 'diagnostic value'/exp OR 'reliability'/exp) (119) > 17 uniek |
|
