Kortwerkende insulineanalogen en insuline
Uitgangsvraag
Hebben kortwerkende insulineanalogen (lispro, aspart, glulisine) de voorkeur boven humaan kortwerkend insuline (RHI)?
Aanbeveling
Stem de insuline behandeling af op de individuele eet- en leefpatronen van de patiënt.
Houd hierbij rekening met de farmacokinetische eigenschappen van de verschillende insulines.
Gebruik gezien de grote intraindividuele variatie in absorptie bij voorkeur langwerkende insuline-analogen in plaats van NPH insuline.
Overwegingen
Bovenstaande meta-analyse (Rys et al., 2011) laat een geringe extra reductie zien in Hb1Ac in de insuline aspart-groep dan in de controlegroep. Dit verschil is statistisch significant, maar de klinische relevantie is onduidelijk, en zal ondermeer afhangen van de uitgangswaarde van HbA1c in de individuele patiënt, en of de extra reductie in HbA1c gepaard gaat met een toename van hypoglycemie. Hoewel theoretisch insulineanalogen beter de glucosestijging na de maaltijd opvangen, betekent dit ook dat het nemen van extra koolhydraten tussen de maaltijden niet/onvoldoende gedekt is bij het gebruik van analogen. In de studies zijn de patiënten niet geselecteerd op eetgewoonten/eetpatroon hetgeen wel relevant is.
Uit de meta-analyse blijkt tevens dat de kans op een hypoglycemische episode marginaal verhoogd is in de insuline-aspart groep terwijl de kans op nachtelijke hypoglycemie kleiner is dan ten opzichte van het gebruik van humaan kortwerkende insuline.
In conclusie, dit literatuuronderzoek laat geen duidelijk voordeel zien voor insuline aspart ten opzichte van humaan kortwerkend insuline. Waarschijnlijk omdat geen rekening is gehouden met het eet-/leefpatroon van de patiënt. Bij de keuze voor het type kortwerkend insuline zal hiermee rekening gehouden moeten worden. Hierdoor kan één patiënt de twee verschillende kortwerkende insulines gebruiken afhankelijk van zijn/haar koolhydraatintake. Op deze manier wordt een maximale flexibiliteit bewerkstelligd. Maatwerk voor de individuele patiënt staat dus op de voorgrond.
Onderbouwing
Achtergrond
De buitenlandse richtlijn ADA 2012 adviseert insulineanalogen te gebruiken indien hypoglycemieën optreden. De NICE richtlijn adviseert kortwerkende insulineanalogen voor te schrijven indien er nachtelijke of late interprandiale hypoglycemieen optreden en langwerkende insulineanalogen in plaats van NPH insuline indien er nachtelijke hypoglycemieen optreden bij NPH insuline of indien er in de ochtend hyperglycemieën optreden waardoor de glucose regulatie overdag moeizaam verloopt.
Conclusies / Summary of Findings
|
MATIG
|
Toepassing van ultrakortwerkende insulineanalogen bij patiënten met type 1 diabetes leidt tot een beperkte, wel statistisch significante, verlaging van het HbA1c in vergelijking met kortwerkende humaan insuline. De klinische relevantie van deze verlaging is voor het optreden van complicaties op de lange termijn is nooit onderzocht.
Rys et al., 2011; Brock Jacobsen et al., 2011; Garg et al., 2010; Singh et al., 2009 |
|
LAAG
|
Toepassing van ultrakortwerkende insulineanalogen ten opzichte van kortwerkende humaan insuline bij patiënten met type 1 diabetes leidt tot beperkte maar statistisch significante daling van de post-prandiale glucose.
Rys et al., 2011 |
|
LAAG
|
Toepassing van kortwerkende insulineanalogen bij patiënten met type 1 diabetes leidt tot minder nachtelijke hypoglycemische episodes ten opzichte van humaan kortwerkende insuline. De kans op ernstige nachtelijke hypoglycemieën is niet verschillend.
Rys et al., 2011; Brock Jacobsen et al., 2011; Garg et al., 2010; Singh et al., 2009 |
Samenvatting literatuur
De zoekactie leverde drie systematische reviews op (Rys et al., 2011; Garg et al., 2010; Singh et al., 2009). Het meest recente systematische review (Rys et al., 2011) is van goede kwaliteit en includeert 18 RCT’s bij patiënten met DM1, gepubliceerd voor juli 2009. De studies bij patiënten met DM2 zijn buiten beschouwing gelaten. De zoekactie leverde één relevante recentere RCT op (Brock Jacobsen et al., 2011).
De inclusiecriteria van Rys et al. (2011) en de belangrijkste karakteristieken van de geselecteerde studies, inclusief een beoordeling van de studiekwaliteit (Jadad-score), zijn te vinden in de evidence-tabel (zie desbetreffende sectie). Vijf van de achttien geïncludeerde RCT’s zijn cross-over studies, de overige dertien studies hebben een parallel design. De studiegrootte varieert tussen 26 en 1065 deelnemers en de studieduur van zeven weken tot negen maanden. Waardes voor HbA1c, post-prandiaal glucose en nuchter glucose werden als maten voor de glycemische controle vergeleken tussen de groep behandeld met insuline aspart, en de controlegroep behandeld met kortwerkend humaan insuline. Onder de dertien studies met voldoende gedetailleerde HbA1c gegevens, was er in vier studies sprake van een statistisch significant grotere reductie in HbA1c in de insuline aspart groep (0,12-0,35%, p<0,05; follow-up 3-6 maanden). In de overige negen studies was het verschil tussen interventie- en controlegroep statistisch niet significant. Een meta-analyse laat een grotere reductie zien in Hb1Ac in de insuline aspart-groep ten opzichte van de controlegroep (Figuur 1; gewogen gemiddelde verschil, WMD; WMD= -0,11; 95% BI= [-0,16;-0,06]). In tien studies worden de effecten op post-prandiaal glucose voldoende nauwkeurig beschreven, en zijn statistisch significante reducties te zien in de glucosewaardes na ontbijt (-1.43 [-1.75; -1.11] mmol/l; meta-analyse van vijf studies), lunch (-1.11 [-1.61; -0.61] mmol/l; vijf studies), en avondeten (-0.97 [-1.25; -0.69] mmol/l; zes studies). In zeven RCT’s wordt de frequentie van hypoglycemische episodes vergeleken tussen de insuline aspart- en controlegroep. De kans op een hypoglycemische episode lijkt marginaal verhoogd in de insuline-aspart groep (RR=1.06 [1.01; 1.10]; meta-analyse van zes studies), terwijl de kans op nachtelijke hypoglycemie lijkt af te nemen (0.67 [0.54; 0.83]; meta-analyse van drie studies) en die op ernstige hypoglycemie niet significant verandert (0.92 [0.75; 1.12]; zeven studies). Aanvulling van de SR van Rys et al. (2010) met de recente RCT van Brock Jacobsen et al. (2011), leidt niet tot nieuwe inzichten. Het betreft een kleine cross-over studie (zestien patiënten) waarin geen statistisch significant verschil wordt waargenomen in HbA1c waardes of de frequentie hypoglycemie tussen de insuline aspart behandeling en behandeling met humaan kortwerkend insuline (zie evidence-tabel).
Figuur 1 Vergelijking in effectiviteit tussen insuline aspart en humaan kortwerkend insuline. Effectiviteit is gebaseerd op een vergelijking van HbA1c waardes (weighted mean difference, WMD).
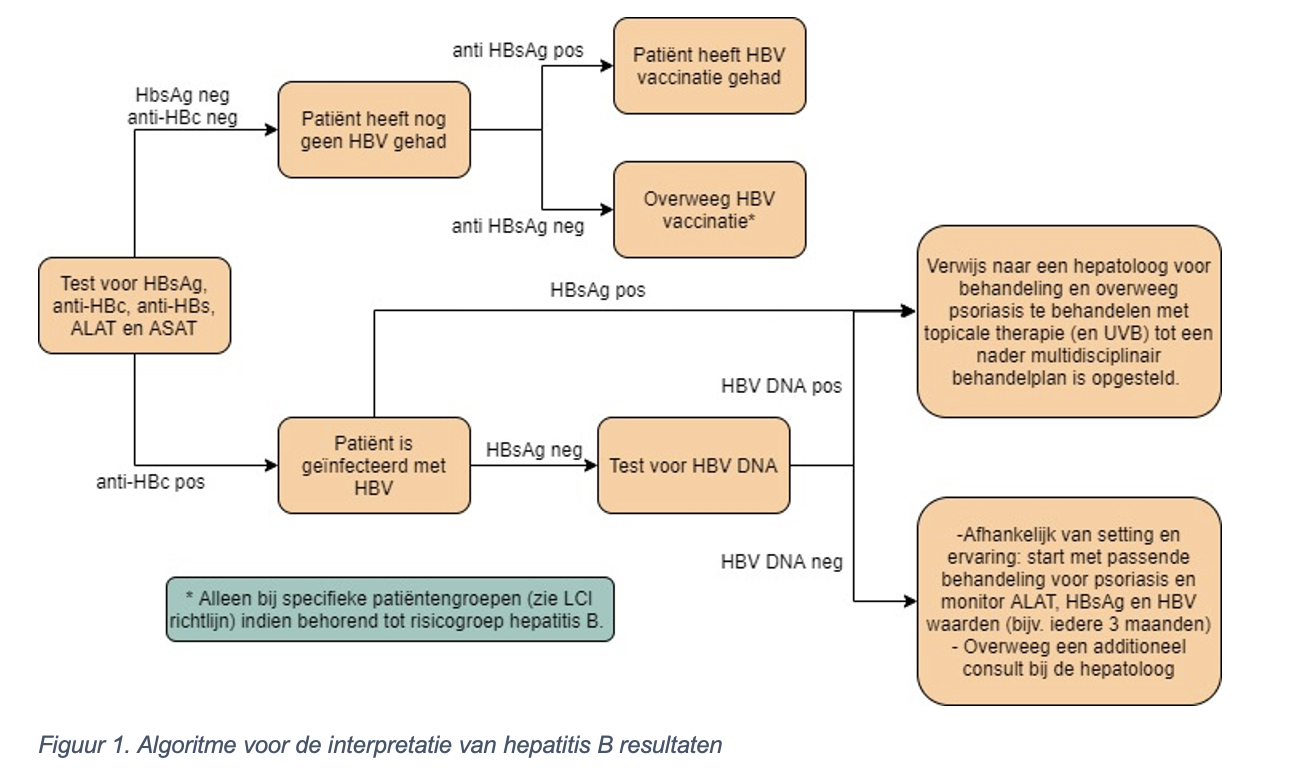
De twee eerdere systematische reviews (Garg et al., 2010; Singh et al., 2009) beperken zich niet tot insuline aspart, maar includeren ook RCTs die de effecten van insuline glulisine en insuline lispro vergelijken met kortwerkend humaan insuline. De conclusies in beide studies komen overeen met die van Rys et al. (2011).
Bij beoordelen van de studies volgens GRADE is de bewijskracht matig voor effecten van behandeling met ultrakortwerkende insulineanalogen op HbA1c, er is één punt afgetrokken vanwege ernstige beperkingen in studieopzet (geen verborgen groepstoewijzing en geen blindering van de behandeling in de meerderheid van de studies). Bij het bepalen van de bewijskracht voor de effecten op post-prandiaal glucose is een tweede punt afgetrokken vanwege indirectheid (inclusie van studies aan kinderen en adolescenten) en is de bewijskracht laag. Tenslotte is de bewijskracht voor de effecten op het optreden van hypoglycemie laag vanwege de beperkingen in studieopzet en vanwege inconsistentie (grote onverklaarde variatie tussen studies, en verschil in geschatte effectiviteit afhankelijk van de gebruikte uitkomstmaat, totaal versus nachtelijk versus ernstige hypoglycemie).
Referenties
- Brock Jacobson, I., Vind, B. F., Korsholm, L., Flyvbjerg, A., Frystyk, J., Holst, J. J., Beck-Nielsen, H., & Henriksen, J.E. (2011). Counter-regulatory hormone responses to spontaneous hypoglycaemia during treatment with insulin Aspart or human soluble insulin: a double-blinded randomized cross-over study. Acta Physiologica, 202, 337-347.
- Colhoun, H. M., SDRN Epidemiology Group (2009). Use of insulin glargine and cancer incidence in Scotland: a study from the Scottish Diabetes Research Network Epidemiology Group. Diabetologia 52:17661777.
- Currie CJ, Poole CD, Gale EA (2009). The influence of glucose-lowering therapies on cancer risk in type 2 diabetes. Diabetologia 52:17661777.
- Dejgaard, A., Lynggaard, H., Rastam, J., & Krogsgaard, T. M. (2009). No evidence of increased risk of malignancies in patients with diabetes treated with insulin detemir: a meta-analysis. Diabetologia, 52, 2507-2512
- Garg, S., Ampudia-Blasco, F. J., & Pfohl, M. (2010). Rapid-acting insulin analogues in Basal-bolus regimens in type 1 diabetes mellitus. Endocr Pract., 16, 486-505.
- Garg, S., Moser, E., Dain, M. P., & Rodionova, A. (2010). Clinical experience with insulin glargine in type 1 diabetes. Diabetes Technology & Therapeutics, 12, 835-846.
- Home, P.D., & Lagarenne, P. (2009). Combined randomised controlled trial experience of malignancies in studies using insulin glargine. Diabetologia, 52, 24992506.
- Jonasson JM, Ljung R, Talback M, Haglund B, Gudbjornsdottir S, Steineck G. Insulin glargine use and short-term incidence of malignancies-a population-based follow-up study in Sweden. Diabetologia. 2009;52:17451754.
- Kølendorf, K., Aaby, P., Westergaard, S., & Deckert, T. (1978). Absorption, effectiveness and side effects of highly purified porcine NPH-insulin preparations (Leo). Eur J Clin Pharmacol., 14, 117-124.
- Lepore, M., Pampanelli, S., Fanelli, C., Porcellati, F., Bartocci, L., Di Vincenzo, A., Cordoni, C., Costa, E., Brunetti, P., & Bolli, G.B. (2000). Pharmacokinetics and pharmacodynamics of subcutaneous injection of long-acting human insulin analog glargine, NPH insulin, and ultralente human insulin and continuous subcutaneous infusion of insulin lispro. Diabetes, 49, 2142-2148.
- Mannucci E, Monami M, Balzi D, et al. (2010). Doses of insulin and its analogues and cancer occurrence in insulin-treated type 2 diabetic patients. Diabetes Care 33:19972003.
- Monami, M., Marchionni, N., & Mannucci, E. (2009). Long-acting insulin analogues vs. NPH human insulin in type 1 diabetes. A meta-analysis. Diabetes, Obesity & Metabolism, 11, 372-378.
- Morden, N., Liu, S., Smith, J., Mackenzie, T., Skinner, J., & Korc, M. (2011). Further exploration of the relationship between insulin glargine and incident cancera retrospective cohort study of older Medicare patients. Diabetes Care, 34, 19651971.
- Roach, P. (2008). New insulin analogues and routes of delivery: pharmacodynamic and clinical considerations. Clin Pharmacokinet., 47, 595-610.
- Rosenstock, J., Fonseca, V., McGill, J.B., et al. (2009). Similar risk of malignancy with insulin glargine and neutral protamine Hagedorn (NPH) insulin in patients with type 2 diabetes: findings from a 5 year randomised, open-label study. Diabetologia, 52, 19711973.
- Roy, B., Chou, M.C., & Field, J.B. (1980). Time-action characteristics of regular and NPH insulin in insulin-treated diabetics. J Clin Endocrinol Metab., 50, 475-479.
- Ruiter, R., Visser, L.E., van Herk-Sukel, M.P.P., Coebergh, J.W.W., Haak, H.R., Geelhoed-Duijvestijn, P.H., Straus, S.M.J.M., Herings, R.M.C., & Ch. Stricker, B.H. (2012). Risk of cancer in patients on insulin glargine and other insulin analogues in comparison with those on human insulin: results from a large population-based follow-up study. Diabetologia, 55, 5162.
- Rys, P., Pankiewicz, O., Lach, K., Kwaskowski, A., Skrzekowska-Baran. I. & Malecki, M. T. (2011). Efficacy and safety comparison of rapid-acting insulin aspart and regular human insulin in the treatment of type 1 and type 2 diabetes mellitus: a systematic review. Diabetes & Metabolism, 37, 190-200.
- Sanches, A. C. C., Correr, C. J., Venson, R., & Pontarolo, R. (2011). Revisiting the efficacy of long-acting insulin analogues on adults with type 1 diabetes using mixed-treatment comparisons. Diabetes research and clinical practice, 94, 333-339.
- Singh, S. R., Ahmad, F., Lal, A., Yu, C., Bai, Z., & Bpharm, H.B. (2009). Efficacy and safety of insulin analogues for the management of diabetes mellitus: A meta-analysis. CMAJ, 180, 385-397.
- Suissa, S., Azoulay, L., Dell'aniello, S., Evans, M., Vora, J., & Pollak, M. (2011). Long-term effects of insulin glargine on the risk of breast cancer. Diabetologia, 54, 22542262.
- Szypowska, A., Golicki, D., Groele, L., & Pankowska, E. (2011). Long-acting insulin analogue detemir compared with NPH insulin in type 1 diabetes: a systematic review and meta-analysis. Pol Arch Med Wewn, 121, 237-246.
Evidence tabellen
Research question: Does the addition of rapid-acting insulin analogs to the basal insulin regime improve treatment of patients with type 1 diabetes?
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C)
|
Follow-up |
Outcome measures and effect size |
Comments |
|
Rys et al, 2011
(individual study characteristics deduced from Rys et al, 2011) |
SR and meta-analysis of 18 RCTs
Literature search up to July 2009
A Ampudia-Blasco, 2005 B Arslanian, 2005 C Bode, 2001 D Bode, 2002 E Boehm, 2002 F Bott, 2003 G Chen, 2006 H Cherubini, 2006 I Danne, 2007 J De Vries, 2003 K Heller, 2004 L Home, 1998 M Home, 2000 N Iwamoto, 2001 O Mathiesen, 2007 P Mortensen, 2006 Q Raskin, 2001 R Tamas, 2001
Parallel design (A-F, H, J, M-P, R) or cross-over design (G, I, K, L, Q)
14 RCTs adults, 4 children/ adolescents (B, H, I, P)
3 adequate allocation concealment (J, K, R)
2 CSII (C, D) |
Inclusion criteria SR: DM1 (DM2 not presented in this table), RCTs insulin aspart vs regular human insulin, no restriction on age, studies ≥ 4 wks, subgroup analysis ≥ 12 wks for HbA1c.
Exclusion criteria SR: N < 10, < 4 wks, gestational or secondary DM.
N/N, mean age (yrs) A 28/26; 32.3 B 187/96; 11.7 C 19/10; 36.6 D 59/59; 42.7 E 88/102; >18 F 283/141; 36.9 G 27; 44.8 H 30; 8.1 I 26/26; 5 J 186/181; 36.9 K 155; 35.7 L 104; 34.3 M 707/358; 38 N 143/62; 33.4 O 157/165; 29.0 P 86/81; 14.4 Q 596/286; 39.2 R 213/213; 36
HbA1c at baseline (%) A 8.5 B 8.3 C 7.2 D 7.4 E ≤ 11.0 F 7.5 G not reported H 7.5 I 7.8 J 8.38 K 8.6 L 7.1 M 7.97 N 7.5 O 6.9 P 9.6 Q 7.9 R 8.325
|
Rapid-acting analogs (RAA)
Insulin aspart (IAsp)
Insulin regimen (basal insulin)
A MDI B MDI C CSII D CSII E Biphas F MDI G Biphas H MDI I MDI J MDI K MDI L MDI M MDI N MDI O MDI P Biphas Q MDI R MDI
MDI with NPH, except A (glargine), and N (not reported) |
Regular human insulin (RHI)
Same insulin regimen as in intervention group |
Duration of follow-up (months): A 6 B 6 C 7 wks D 4 E 3 F 6 G 2 x 3 H 4.5 I 2 x 3 J 16 K 2 x 4 L 2 x 1 M 6 N 6 O 9 P 4 Q 6 R 3
For how many participants were no complete outcome data available? Not stated |
Effect on glycemic control (HbA1c , post-prandial glucose [PPG]), fasting glucose, quality of life/ treatment flexibility, adverse effects; weighted mean difference (WMD), standardized mean difference (SMD), relative risk (RR) [meta-analysis]; [95%CI]
Effect on HbA1c I minus C (WMD; %)); 13 studies pooled <0 favours I (IAsp) >0 favours C (RHI) 16 studies measured HbA1c Excluded: 3 studies lacking sufficient numerical data (G,H,I)
A 0.14 [-0.38; 0.66] B 0.00 [-0.35; 0.35] C -0.20 [-0.66; 0.26] D -0.35 [-0.62; -0.08] E 0.19 [-0.05; 0.43] J -0.14 [-0.35; 0.07] K 0.00 [-0.20; 0.20] M -0.12 [-0.22; -0.02] N -0.24 [-0.57; 0.09] O -0.08 [-0.22; 0.06] P 0.14 [-0.33; 0.61] Q -0.15 [-0.26; -0.04] R -0.16 [-0.30; -0.02] Overall: -0.11 [-0.16; -0.06] Heterogeneity: I2=17.5%; p=0.27
Subgroup-analyses based on basal insulin treatment: Subgroup-CSII (C,D; 2 studies pooled) Overall: -0.31 [-0.55; -0.08] Subgroup-basal bolus (A,B,J,K,M,N,O,Q,R; 9 studies pooled) Overall: -0.12 [-0.17; -0.06]
Effect on post-prandial glucose (PPG; self-measured) I minus C (mmol/l) Reported in 10 studies; studies w/o suff numerical data were excluded Post-breakfast glucose (5 studies) -1.43 [-1.75; -1.11] Post-lunch glucose (5 studies) -1.11 [-1.61; -0.61] Post-dinner glucose (6 studies) -0.97 [-1.25; -0.69]
Effect on fasting glucose (FG) I minus C (mmol/l); 5 studies pooled Reported in 12 studies; in 3 studies RHI was superior over insuline aspart, in 9 studies differences were not significant; 5 studies provided numerical data Fasting glucose 0.15 [-0.55; 0.86) Heterogeneity: I2=72.8%; p=0.005
Adverse effects (hypoglycemic episodes) I minus C (RR) Reported in 7 studies, in 6 studies episodes were self-reported All hypoglycaemic episodes (6 studies) 1.06 [1.01; 1.10]
Reported in 3 studies Nocturnal hypoglyc episodes (3 studies) 0.67 [0.54; 0.83]
Reported in 8 studies, 7 with sufficient numerical data Severe hypoglyc episodes (7 studies) 0.92 [0.75; 1.12]
Quality of life / treatment flexibility I minus C (SMD; DTSQ questionnaire score) Reported in 3 studies, the flexibility part in only 2 Total score (3 studies) 0.30 [0.20;0.40] Flexibility score (2 studies) 0.31 [0.15; 0.47]
|
Authors conclude that IAsp compared with RHI resulted in moderately better metabolic control, as demonstrated by reductions in HbA1c and PPG, and no change in FG; IAsp also resulted in greater treatment satisfaction and a significant reduction of risk for nocturnal hypoglycaemic episodes, but not severe hypoglycaemias or hypoglycaemia in general
Note that it is unclear whether the extra reduction in HbA1c by 0.11 % is clinically relevant
Note that the 2 studies with CSII regimen had the most favourable HbA1c reduction (-0.31 [-0.55; -0.08]) as compared to 9 studies with basal-bolus (MDI) regimen ( -0.12 [-0.17; -0.06])
Note that in most studies, no blinding or allocation concealment was applied (high risk of bias), and that the data reported in some studies were incomplete (HbA1c was measured in most studies, but PPG or hypoglycaemic episodes only in some studies); SR provides no data on risk of publication bias
Quality of RCTs (Jadad score): R1 Random allocation R2 with appropriate rand. method B0 Not double-blind B1 Double-blind W0 No info on reasons withdrawal W1 information provided
A R1 B0 W0 B R1 B0 not reported C R1 B0 W1 D R2 B0 W1 E R2 B0 W1 F R1 B0 W0 G R1 B0 W1 H R1 B0 W0 I R1 B0 W0 J R2 B0 W1 K R2 B1 W1 L R1 B1 W1 M R1 B0 W1 N R1 B0 W0 O R2 B0 W0 P R1 B0 W0 Q R1 B0 W1 R R2 B0 W0
Level of evidence: GRADE
MODERATE* IAsp vs RHI Effect on HbA1c
LOW** IAsp vs RHI Effect on PPG
MODERATE*** IAsp vs RHI Effect on FG
LOW**** IAsp vs RHI Adverse effects (hypoglycemic episodes)
*Downgraded 1 point because of serious study limitations: lack of blinding (12 out of 13 studies) and allocation concealment (10 out of 13 studies)
**Downgraded 2 points because of serious study limitations (lack of blinding and allocation concealment), and indirectness (3 out of 5 [PBG], 1 out of 5 [PLG], and 2 out of 6 [PDG] studies included children/adolescents)
*** Downgraded 1 point because of serious study limitations (lack of blinding and allocation concealment)
****Downgraded 2 points because of serious study limitations (lack of blinding and allocation concealment), and inconsistency (inconsistent results across studies; difference in estimate of treatment effect depending on outcome measure [overall vs nocturnal vs severe hypoglycemic episodes])
A significant reduction of postprandial glucose levels was found in the groups receiving insulin aspart compared to regular human insulin (pooled results of 5-6 studies)
The risk of nocturnal hypoglycaemia measured in 3 studies, was significantly lower in insulin aspart group than in the regular human insulin group (RR= 0.67 [0.54; 0.83])
In contrast, the insulin aspart group showed a slight, but statistically significant, risk increase of all hypoglycaemic episodes compared to the regular human insulin group (RR=1.06 [1.01; 1.10]; pooled result of 6 studies)
Pooled analysis of 2 studies showed that using insulin aspart instead of regular human insulin resulted in greater treatment satisfaction
|
|
Brock Jacobsen et al, 2011 |
Cross-over study; double-blind, randomized, 2 periods
Funding: supported by Novo Nordisk |
Inclusion criteria: type 1 DM for > 1 year; age 18–60 years; BMI of 18–27.5; required to use soluble human insulin before breakfast, lunch and dinner and NPH at bedtime for at least 3 months before entering study
Exclusion criteria: pregnancy, impaired vision, impaired renal or hepatic function, cardiac diseases, uncontrolled hypertension, hypoglycaemic unawareness
13 men, 3 women Age 44.4 ± 8.2 years BMI 24.6 ± 1.3 HbA1c 7.8 ± 1.1% Diab duration 19± 10 years
At baseline, mean daily insulin dose was: soluble insulin 29.4 IU and NPH 22.3 IU |
Insulin aspart (IAsp)
Novo-Rapid; 3X/d
N=16
Insulin regimen (basal insulin): NPH 2X/d |
Regular human insulin (RHI)
Actrapid; 3X/d
N=16
Same insulin regimen as in intervention group |
Duration of follow-up: 2X8 weeks
After 8 weeks of treatment, patients were hospitalized for 22 h
For how many participants were no complete outcome data available? 2/16 (13%); patients left ‘for personal reasons’ |
Effect on glycemic control (HbA1c , post-prandial glucose [PPG]), patient satisfaction, adverse effects; absolute amount, counts, frequency [SD]
Effect on HbA1c (%) I: 7.0 ± 0.2 C: 7.0 ± 0.2 P=NS
Adverse effects (hypoglycemic episodes) I: 214 events (3 nocturnal; 2 extreme [≤ 3.5 mmol/l] C: 297 events (5 nocturnal; 3 extreme)
Hypoglycaemic frequency (events/week) I: 0.9 ± 0.1 C: 1.1 ± 0.2 P=NS
Patient satisfaction (VAS; 0-6) P=NS
During hospitalization:
Effect on post-prandial glucose (PPG) I versus C (mmol/l; p-value) Post-breakfast: 8.2 ± 1.0 vs 12.6 ± 1.1 (P = 0.005) Post-lunch: 3.6 ± 0.4 vs 4.5 ± 0.6 (P = 0.02) Post-dinner: 7.9 ± 1.2 vs 9.9 ± 1.3 (P = 0.01) statistically significant lower PPG during IAsp treatment
|
Authors conclude that IAsp did not improve glycaemic control, and no difference in hypoglycaemic frequency was observed
IAsp elicited a slightly different physiological response to spontaneous hypoglycaemia compared with human insulin; however, the physiological and clinical relevance of these effects remain speculative
Note: during hospitalization, a statistically significant lower PPG was observed during IAsp treatment
Level of evidence: GRADE see above, this study does not alter the conclusion based on Rys et al (2011; note the small study size (N=16) as compared to the studies included in the meta-analysis)
|
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 18-02-2013
Beoordeeld op geldigheid : 20-02-2014
De werkgroep streeft ernaar jaarlijks de aanbevelingen te updaten.
De Nederlandse Internisten Vereniging is als houder van deze richtlijn de eerstverantwoordelijke voor de actualiteit van deze richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijk verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de eerstverantwoordelijke over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
IN SAMENWERKING MET
Nederlandse Vereniging voor Neurologie
Nederlandse Vereniging voor Anesthesiologie
MET ONDERSTEUNING VAN
Kennisinstituut van Medisch Specialisten
FINANCIERING
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van Medisch Specialisten en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Het doel is één integrale, modulair opgebouwde NIV richtlijn diabetes te ontwikkelen volgens het concept netwerkrichtlijnen. De richtlijn moet een praktisch handvat bieden aan de internist en zijn/haar team. De richtlijn richt zich op alle DM patiënten die verwezen worden naar de internist, i.e. alle patiënten DM type 1 en de patiënten DM type 2 in de tweede lijn (volwassen patiënten).
De primaire doelgroep van deze richtlijn is de internist en degenen in zijn/haar team, die onder eindverantwoordelijkheid van de internist zorg leveren. Daarnaast is het belangrijk dat alle beroepsgroepen die betrokken zijn bij de diabeteszorg in de tweede lijn kennis nemen van deze richtlijn en deze ondersteunen.
Samenstelling werkgroep
Totstandkoming werkgroep
Voor het ontwikkelen van de richtlijn is in 2011 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten die met DM te maken hebben (zie hiervoor de samenstelling van de werkgroep).
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep werkte gedurende twee jaar aan de totstandkoming van de richtlijn. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
Samenstelling werkgroep
· Dr. B.J. Potter van Loon, internist, Nederlandse Internisten Vereniging (voorzitter);
· Dr. B.E. de Galan, internist, Nederlandse Internisten Vereniging;
· Mw. dr. C.B. Brouwer, internist, Nederlandse Internisten Vereniging;
· Mw. dr. P.H.L.M. Geelhoed, internist, Nederlandse Internisten Vereniging;
· Prof. dr. N.C. Schaper, internist, Nederlandse Internisten Vereniging;
· Dr. R.P.L.M. Hoogma, internist, Nederlandse Internisten Vereniging;
· Mw. dr. P.J.M. van Gurp, internist, Nederlandse Internisten Vereniging;
· Mw. dr. L.D. Elving, internist, Nederlandse Internisten Vereniging;
· Dr. T.F. Veneman, internist, Nederlandse Internisten Vereniging;
· Mw. dr. H.L. Lutgers, internist, Nederlandse Internisten Vereniging;
· Prof. dr. A.J.M. Loonen, arts/klinisch farmacoloog; Nederlandse Vereniging van Psychiatrie
· Dr. D. Cohen, psychiater; Nederlandse Vereniging van Psychiatrie;
· Dr. G.E.M.G. Storms, internist, Nederlandse Internisten Vereniging;
· Mw. drs. I. Hommel, internist, Nederlandse Internisten Vereniging;
· Dr. T.W. van Haeften, internist, Nederlandse Internisten Vereniging;
· Dr. A.D.M. Stork, internist, Nederlandse Internisten Vereniging;
· Dr. J.L.M. Jongen, neuroloog, Nederlandse Vereniging voor Neurologie;
· Mw. J.M. Ronday, anesthesioloog, Nederlandse Vereniging voor Anesthesiologie;
· Mw. drs. L.J.N. Wind, AIOS, Nederlandse Internisten Vereniging;
· Mw. drs. M.C.J. Knippels, AIOS, Nederlandse Internisten Vereniging;
· Mw. dr. M.M.L. Stikkelbroeck, AIOS, Nederlandse Internisten Vereniging;
· Mw. drs. S.M. van der Leij, AIOS, Nederlandse Internisten Vereniging;
· Mw. dr. L.C.G. de Graaff, AIOS, Nederlandse Internisten Vereniging;
· Mw. dr. C. van Noord, AIOS, Nederlandse Internisten Vereniging;
· Mw. dr. I.J.A. de Bruin, AIOS, Nederlandse Internisten Vereniging;
· Dr. C.K.A. van den Berge, AIOS, Nederlandse Internisten Vereniging;
· Mw. drs. M.P.A. Hoeks, AIOS, Nederlandse Internisten Vereniging;
· Mw. drs. Y.W. van den Berg, AIOS, Nederlandse Internisten Vereniging;
· Dr. E.J.G. Peters, internist, Nederlandse Internisten Vereniging;
Met ondersteuning van:
· Ir. T.A. van Barneveld, hoofd Kennisinstituut van Medisch Specialisten;
· Dr. K.N.J. Burger, epidemioloog, adviseur Kennisinstituut van Medisch Specialisten;
· Mw. Ir. I.W. Loman, junior adviseur Kennisinstituut van Medisch Specialisten;
· Mw. drs. S.B. Muller-Ploeger, junior adviseur Kennisinstituut van Medisch Specialisten;
· Mw. drs. M. Wessels, informatiespecialist Kennisinstituut van Medisch Specialisten;
· Mw. V. Beaujean, secretariaat, Kennisinstituut van Medisch Specialisten;
· Mw. S. Jaber, MSc, beleidsadviseur Kwaliteit, Nederlandse Internisten Vereniging
Belangenverklaringen
De werkgroepleden hebben schriftelijk verklaard of ze in de laatste vijf jaar een (financieel ondersteunde) betrekking onderhielden met commerciële bedrijven, organisaties of instellingen die in verband staan met het onderwerp van de richtlijn. Tevens is navraag gedaan naar persoonlijke financiële belangen, belangen door persoonlijke relaties, belangen d.m.v. reputatiemanagement, belangen vanwege extern gefinancierd onderzoek, en belangen door kennisvalorisatie. De belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van Medisch Specialisten (KIMS).
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door een enquête via internet. Een verslag van de enquête is besproken in de werkgroep en de belangrijkste knelpunten zijn verwerkt in de richtlijn. Het verslag is op te vragen bij het secretariaat van het Kennisinstituut van Medisch Specialisten (KIMS).
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren.
De richtlijn is digitaal verspreid onder alle relevante beroepsgroepen. De richtlijn is te downloaden vanaf de website van de NIV en via de Richtlijnendatabase.
Indicatorontwikkeling
Gelijktijdig met het ontwikkelen van de conceptrichtlijn werden er interne kwaliteitsindicatoren ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken. Meer informatie over de methode van indicatorontwikkeling is op te vragen bij het Kennisinstituut van Medisch Specialisten.
Werkwijze
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens zijn er knelpunten aangedragen door vertegenwoordigers van het Nederlands Huisartsen Genootschap (NHG), de beroepsorganisatie voor Diabeteszorgverleners (EADV), DiabetesVereniging Nederland (DVN), Zorgverzekeraars (ACHMEA en UVIT), farmacie/industrie (Nefarma), Nederlandse Diëtisten Vereniging (NVD) en arts-assistenten in opleiding (JNIV) van de NIV via een Invitational conference. Een verslag hiervan kunt u vinden in de bijlagen.
Methode richtlijnontwikkeling
Deze (concept)richtlijn is opgesteld aan de hand van het Procedureboek NIV richtlijnen die aansluit bij het “Appraisal of Guidelines for Research & Evaluation II” (AGREE II) instrument (www.agreecollaboration.org). Dit instrument is een breed (internationaal) geaccepteerd instrument voor de beoordeling van de kwaliteit van richtlijnen.
Adaptatie
De a/b/c/e-level ADA aanbevelingen (2011, USA) worden in principe overgenomen, mits deze:
-
niet in tegenspraak zijn met deze uit de Duitse richtlijn (2010), de NICE richtlijn (update 2010, Engeland), de Sign richtlijn (2010, Schotland) en de Canadese richtlijn (2008);
-
niet in tegenspraak zijn met de resultaten van een literatuur update van de laatste drie jaar; 3) geldig zijn voor de Nederlandse situatie.
Vaststellen van de belangrijkste uitkomstmaten
De richtlijnwerkgroep heeft per uitgangsvraag de wetenschappelijke uitkomstmaten vastgesteld die zij van belang achtte en hebben deze naar mate van belang voor de patiënt geordend. Hierbij was het streven om vooral harde klinische eindpunten te gebruiken. Tevens heeft de werkgroep aangegeven welk verschil zij klinisch relevant vinden.
Strategie voor zoeken naar en selectie van literatuur
Er werd voor alle afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in de elektronische databases van Medline, Cochrane en, zo nodig, Embase. Daar waar stukken uit de ADA-richtlijn* werden overgenomen werden aanvullende searches gedaan van de afgelopen drie jaar, i.e. van 2008 tot 2011. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar (systematische reviews of meta-analyses van) gerandomiseerde gecontroleerde onderzoeken (RCT’s). In afwezigheid van RCT’s werd verder gezocht naar prospectieve vergelijkende onderzoeken en prospectieve niet-vergelijkende onderzoeken (uitzondering: onderwerpen van a/b level-ADA aanbevelingen: uitsluitend RCT’s; zie later). De werkgroepleden selecteerden artikelen op basis van op voorhand opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. Voor de gebruikte zoekstrategieën zie de bijlagen.
* De ADA-richtlijn wordt elk jaar geüpdate. Onduidelijk is of de richtlijn elk jaar volledig of partieel geüpdate wordt.
Beoordeling van de kwaliteit van studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de tabel ‘Beoordeling kwaliteit studie’ in de bijlagen.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE methodiek. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/) (Atkins et al., 2004).
B) Voor vragen over waarde diagnostische tests, schade of bijwerkingen, etiologie en prognose
Bij dit type vraagstelling kan GRADE (nog) niet gebruikt worden. De bewijskracht van de conclusie is bepaald volgens de gebruikelijke EBRO-methode (van Everdingen et al., 2004). Waarbij de bewoording van de GRADE methode is gebruik zoals hieronder weergegeven.
|
EBRO |
bewoording |
|
Niveau 1 |
Hoog |
|
Niveau 2 |
Matig |
|
Niveau 3 |
Laag |
|
Niveau 4 |
Zeer laag |
Formuleren van de conclusies
Bij interventievragen verwijst de conclusie niet naar een of meer artikelen, maar wordt getrokken op basis van alle studies samen (body of evidence). Hierbij maakten de werkgroepleden de balans op van elke interventie. Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen.
Voor vragen over waarde diagnostische tests, schade of bijwerkingen, etiologie en prognose is het wetenschappelijke bewijs samengevat in een of meerdere conclusie(s), waarbij het niveau van het meest relevante bewijs is weergegeven.
Overwegingen
Voor een aanbeveling zijn naast het wetenschappelijke bewijs ook andere aspecten belangrijk, zoals de expertise van de werkgroepleden, patiëntenvoorkeuren, kosten, beschikbaarheid van voorzieningen of organisatorische zaken. Deze aspecten worden, voor zover niet wetenschappelijk onderzocht, vermeld onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven een antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen.
Procedure voor commentaar en autorisatie
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor commentaar. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de Diabetesvereniging Nederland (DVN), de Beroepsorganisatie voor Diabeteszorgverleners (EADV), het Nederlands Huisartsen genootschap (NHG), Nefarma, de Nederlandse Diabetes Federatie (NDF), de Nederlandse Vereniging van Diëtisten (NVD), en de Nederlandse Vereniging van Klinisch Chemici (NVKC). De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor autorisatie en door hen geautoriseerd.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is. Een overzicht van aanbevelingen voor nader/vervolg onderzoek per module staat in aanverwant 'Kennislacunes'.
Zoekverantwoording
|
Onderwerp:
|
Database |
Zoekstrategie |
Aantal ref. |
|
Met welk insulineschema start je bij een volwassene met een nieuw ontdekte type 1 diabetes zonder acidose?
|
Medline (OVID), 2008-mei 2012 Engels
Cochrane Library (Wiley)
Embase (Elsevier)
|
1 exp *Diabetes Mellitus, Type 1/dt [Drug Therapy] (5415) 2 (diabetes adj1 type adj1 "1").ti. (88) 3 (type adj1 "1" adj1 diabetes).ti. (10062) 4 1 or 2 or 3 (14294) 9 exp Insulins/ad [Administration & Dosage] (14404) 10 regimen*.ti,ab. (155957) 11 basal-bolus.ti,ab. (325) 12 (daily or MDI).ti,ab. (308181) 13 (intensive adj2 therapy).ti,ab. (7771) 14 exp Insulins/ (150523) 15 insulin*.ti,ab. (244792) 16 10 or 11 or 12 or 13 (450940) 17 14 or 15 (276995) 18 16 and 17 (16022) 19 9 or 18 (27710) 20 4 and 19 (3633) 21 ((new or newly or novo or recent* or time) adj3 (diagnose* or onset)).ti,ab. (53257) 22 21 and 20 (177) 23 ((initial adj3 treatment) or (initial adj3 therap*)).ti,ab. (30765) 24 4 and 23 (32) 25 22 or 24 (202) 26 limit 25 to (english language and yr="2008 -Current") (54) 28 SR zoekfilter (1) 57 limit 26 to randomized controlled trial (13) 65 RCT (zoekfilter) (23) 87 56 or 86 (23)
#1 MeSH descriptor Diabetes Mellitus, Type 1 explode all trees #2 (diabetes and "type 1"):ti #3 (#1 OR #2) #4 MeSH descriptor Insulin explode all trees with qualifier: AD #5 (regimen* or basal-bolus or daily or MDI or(intensive and therapy)):ti #6 MeSH descriptor Insulin explode all trees #7 (insulin):ti #8 (( #6 OR #7 ) AND #5) #9 (#4 OR #8) #10 (#9 AND #3) #11 (#10), from 2008 to 2012 #12 (new or newly or novo or recent* or time ) and ( diagnose* or onset ):ti,ab,kw #13 ("initial treatment") or ("initial therapy"):ti,ab,kw #14 (#12 OR #13) #15 (#11 AND #14) 13 trials, 5 uniek
(regimen*:ab,ti OR 'basal bolus':ab,ti OR daily:ab,ti OR mdi:ab,ti OR (intensive NEAR/2 therapy):ab,ti OR scheme:ab,ti) AND ('insulin'/exp/mj OR insulin*:ab,ti) AND (((new OR newly OR novo OR recent* OR time) NEAR/3 (diagnose* OR onset)):ab,ti OR (initial NEAR/3 treatment):ab,ti OR (initial NEAR/3 therap*):ab,ti) AND [english]/lim AND [embase]/lim AND [2008-2012]/py OR ('insulin dependent diabetes mellitus'/exp/mj OR (diabetes NEAR/1 'type 1'):ti OR iddm:ab,ti [embase]/lim AND [2008-2012]/py SR of RCT > 17 , 7 uniek |
34 |
|
Welk soort insuline bij T1DM: humaan of analoog?
|
Medline (OVID), 2008-mei 2012 Engels
Cochrane Library (Wiley)
Embase Elsevier)
|
1 exp *Diabetes Mellitus, Type 1/dt [Drug Therapy] (5415) 2 (diabetes adj1 type adj1 "1").ti. (88) 3 (type adj1 "1" adj1 diabetes).ti. (10062) 4 1 or 2 or 3 (14294) 9 exp Insulins/ad [Administration & Dosage] (14404) 10 ("rapid acting insuline analogues" or lispro or aspart or glulisine or "regular human insulin*" or "insuline analogues" or detemir or glargin or "neutral protamine Hagedorn" or NPH).ti,ab. (3401) 11 Insulin/aa (3270) 12 9 or 10 or 11 (18245) 13 4 and 12 (3145) 14 limit 13 to (english language and yr="2008 -Current") (725) 15 zoekfilter SR (38) 44 limit 14 to randomized controlled trial (157) 45 limit 14 to (guideline or practice guideline) (1) 46 "Practice Guidelines as Topic"/ (67640) 47 14 and 46 (7) 48 43 or 47 (44)- RL of SR
#1 MeSH descriptor Diabetes Mellitus, Type 1 explode all trees #2 (diabetes and "type 1"):ti #3 (#1 OR #2) #4 MeSH descriptor Insulin explode all trees with qualifier: AD #16 ("rapid acting insuline analogues" or lispro or aspart or glulisine or "regular human insulin*" or "insuline analogues" or detemir or glargin or "neutral protamine Hagedorn" or NPH):ti,ab,kw #17 MeSH descriptor Insulin explode all trees with qualifier: AA #18 (#4 OR #16 OR #17) #19 (#18 AND #3) #20 (#19), from 2008 to 2012 195 referenties, 36 uniek
insulin dependent diabetes mellitus'/exp/mj OR (diabetes NEAR/1 'type 1'):ti OR iddm.ti,ab AND ('insulin'/exp/mj/dd_ad OR 'rapid acting insuline analogues':ab,ti OR lispro:ab,ti OR aspart:ab,ti OR glulisine:ab,ti OR 'regular human insulin':ab,ti OR 'insuline analogues':ab,ti OR detemir:ab,ti OR glargin:ab,ti OR 'neutral protamine hagedorn':ab,ti OR nph:ab,ti OR 'insulin derivative'/exp/mj OR 'isophane insulin'/exp OR 'insulin lispro'/exp) AND [english]/lim AND [embase]/lim AND [2008-2012]/py
173 referenties > 63 uniek |
287 |
|
Zijn fluctuaties in glucosewaarden onafhankelijk van het HbA1c geassocieerd met een hoger risico op microvasculaire of macrovasculaire complicaties bij patiënten met type 1 diabetes (T1DM)? |
Medline (OVID), 2008-mei 2012 Engels SR vanaf 2000
|
1 exp *Diabetes Mellitus, Type 1/ (44989) 2 (diabetes adj1 type adj1 "1").ti. (88) 3 (type adj1 "1" adj1 diabetes).ti. (10040) 4 "Diabetes Complications"/ (31948) 5 1 or 2 or 3 or 4 (77127) 12 (Glycaemic adj3 varia*).ti,ab. (99) 13 5 and 12 (35) 26 (glucose adj3 fluctuat*).ti,ab. (486) 27 Hyperglycemia/bl, me [Blood, Metabolism] (5554) 28 (postprandial adj3 hyperglycemia).ti,ab. (850) 29 (Glycaemic adj3 varia*).ti,ab. (99) 30 (Glycaemic adj3 fluctua*).ti,ab. (13) 31 26 or 27 or 28 or 29 or 30 (6822) 32 5 and 31 (823) 33 limit 32 to (english language and yr="2000 -Current") (493) 35 *"Diabetes Complications"/ (15334) 36 *"Diabetes Mellitus, Type 1"/ (44742) 37 risk factors/ (481580) 38 prognosis/ (318249) 39 exp cardiovascular diseases/ or coronary artery disease/ (1710868) 40 exp blood vessels/ or coronary vessels/ (576025) 41 (micro* adj4 macrovascular adj3 complications).ti,ab. (945) 42 ((macrovascular or micro* or vascular) adj3 complications).ti,ab. (11418) 43 35 or 36 or 37 or 38 or 39 or 40 or 41 or 42 (2642015) 45 33 and 43 (455) 46 exp epidemiological study/ (1405698) 47 45 and 46 (63) 48 limit 45 to (clinical conference or clinical trial, all or clinical trial or comparative study or consensus development conference or consensus development conference, nih or controlled clinical trial or government publications or guideline or meta analysis or multicenter study or practice guideline or randomized controlled trial or "research support, american recovery and reinvestment act" or research support, nih, extramural or research support, nih, intramural or research support, non us gov't or research support, us gov't, non phs or research support, us gov't, phs or "review" or validation studies) (349) 49 47 or 48 (373) 50 limit 49 to animals (98) 51 limit 50 to humans (50) 52 49 not (50 not 51) (325) 53 "Diabetes Mellitus, Type 2"/ not (1 or 2 or 3) (64449) 54 52 not 53 (308) 55 limit 54 to "all child (0 to 18 years)" (82) 56 limit 55 to "all adult (19 plus years)" (37) 57 54 not (55 not 56) (263) 58 SR (zoekfilter) (15) 13 uniek 87 limit 57 to yr="2008 -Current" (121) 88 87 not 86 (112) 107 uniek |
120 |
|
Wanneer starten met een statine bij T1DM: bij welke risicofactoren, en op welke leeftijd?
|
Medline (OVID), 2008-mei 2012 Engels
Embase (Elsevier)
Cochrane Library (Wiley)
|
1 exp *Diabetes Mellitus, Type 1/ (44989) 2 (diabetes adj1 type adj1 "1").ti. (88) 3 (type adj1 "1" adj1 diabetes).ti. (10049) 4 1 or 2 or 3 (45708) 9 exp anticholesteremic agents/ (43922) 10 (statin* or Pravastatin or Simvastatin or Lovastatin).af. (29333) 11 ((drug* adj1 anticholesteremic) or (hypocholesteremic adj1 agent*) or (cholesterol adj1 inhibitor*) or (anticholesteremic adj1 agent*)).ti,ab. (113) 12 (Fluvastatin or Atorvastatin or pitavastatin or rosuvastatin).af. (7765) 13 9 or 10 or 11 or 12 (54650) 14 8 and 13 (2) 15 4 and 13 (131) 16 zoekfilter SR (2) (2) 45 limit 15 to (yr="2004 -Current" and english) (76) 46 limit 45 to animals (14) 47 limit 46 to humans (2) 48 45 not (46 not 47) (64) 49 44 or 48 (64) 50 49 not 44 (62)
'insulin dependent diabetes mellitus'/exp/mj OR (diabetes NEAR/1 'type 1'):ti AND ('hydroxymethylglutaryl coenzyme a reductase inhibitor'/exp/mj OR (drug* NEAR/1 anticholesteremic):ab,ti OR (hypocholesteremic NEAR/1 agent*):ab,ti OR (cholesterol NEAR/1 inhibitor*):ab,ti OR (anticholesteremic NEAR/1 agent*):ab,ti OR statin*:ab,ti OR pravastatin:ab,ti OR simvastatin:ab,ti OR lovastatin:ab,ti OR fluvastatin:ab,ti OR atorvastatin:ab,ti OR pitavastatin:ab,ti OR rosuvastatin:ab,ti) AND [english]/lim AND [embase]/lim NOT ('conference abstract':it AND [2004-2012]/py) AND [2004-2012]/py NOT 'animal experiment'/exp NOT ('insulin dependent diabetes mellitus'/exp/mj OR (diabetes NEAR/1 'type 1'):ti Embase: 33 uniek
#1 MeSH descriptor Diabetes Mellitus, Type 1 explode all trees #2 (diabetes and type 1):ti #3 (#1 OR #2) #4 MeSH descriptor Hydroxymethylglutaryl-CoA Reductase Inhibitors explode all trees #5 (statin* or Pravastatin or Simvastatin or Lovastatin or Fluvastatin or Atorvastatin or pitavastatin or rosuvastatin):ti,ab,kw #6 (#4 OR #5) #7 (#3 AND #6) 2 SR (dubbel), 22 divers, 5 uniek |
102 |
|
Is toevoeging van metformine aan insulinetherapie van meerwaarde bij patiënten met diabetes type 1?
|
Medline (OVID), 2008-mei 2012 Engels
Cochrane (Wiley)
Embase (Elsevier)
|
1 exp *Diabetes Mellitus, Type 1/ (44989) 2 (diabetes adj1 type adj1 "1").ti. (88) 3 (type adj1 "1" adj1 diabetes).ti. (10049) 4 1 or 2 or 3 (45708) 5 "The use of metformin in type 1 diabetes: a systematic review of efficacy".m_titl. (1) 6 Adjunct therapy for type 1 diabetes mellitus.m_titl. (1) 7 Metformin added to insulin therapy for type 1 diabetes mellitus in adolescents.m_titl. (1) 8 5 or 6 or 7 (3) 9 4 and 8 (3) 10 ("insulin dependent diabetes" or IDDM).ti. (9188) 11 4 or 10 (48990) 12 11 not 4 (3282) 13 Metformin/ (5566) 14 metformin.af. (8006) 15 13 or 14 (8006) 16 4 and 15 (125) 17 limit 16 to (english language and yr="2008 -Current") (32) 18 Zoekfilter SR (5) 47 Zoekfilter RCT (10) 69 46 or 68 (10) – SR en RCTs
#1 MeSH descriptor Diabetes Mellitus, Type 1 explode all trees #2 (diabetes and type 1):ti #3 (#1 OR #2) #4 MeSH descriptor: [Metformin] explode all trees #5 metformin:ti,ab,kw #6 (#4 OR #5) #7 (#3 AND #6) 21 referenties,15 uniek
('insulin dependent diabetes mellitus'/exp/mj OR (diabetes NEAR/1 'type 1'):ti) AND ('metformin'/exp/mj OR metformin:ab,ti) AND [english]/lim AND [embase]/lim AND [2008-2012]/py |
36 |
|
Heeft het gebruik van e-Health meerwaarde op de uitkomst van de behandeling van T1D?
|
Medline (OVID), 2008-juli 2012 Engels, Nederlands
Embase (Elsevier)
|
1 exp *Diabetes Mellitus, Type 1/ (45639) 2 ((diabetes adj1 type adj1 "1") or (type adj1 "1" adj1 diabetes)).ti. (10355) 3 ("insulin dependent diabetes" or IDDM).ti. (9198) 4 1 or 2 or 3 (49668) 9 Telemedicine/ (9281) 10 "Internet"/ (41760) 11 "Remote Consultation"/ (3285) 12 "Cellular Phone"/ (3073) 13 (telemedic* or e-health or internet or "social media" or telecare or webbased or web-based or telehealth or "mobile phone*" or telemonitoring or real-time or app?).ti,ab. (164771) 14 9 or 10 or 11 or 12 or 13 (195188) 15 4 and 14 (468) 16 limit 15 to (yr="2000 -Current" and (dutch or english or french or german)) (423) 17 zoekfilter SR (13) 46 zoekfilter RCTs (100) 68 exp epidemiological studies/ (1437723) 69 16 and 68 (54) – niet bijgevoegd. 70 67 or 69 (144) 71 70 not 45 (136)
'insulin dependent diabetes mellitus'/exp/mj OR (diabetes NEAR/3 'type 1'):ti OR 'insulin dependent diabetes mellitus':ti OR iddm:ti AND ('telemedicine'/exp/mj OR 'internet'/exp/mj OR 'mobile phone'/exp OR 'teleconsultation'/exp/mj OR telemedic*:ab,ti OR 'e health':ab,ti OR internet:ab,ti OR 'social media':ab,ti OR telecare:ab,ti OR webbased:ab,ti OR 'web based':ab,ti OR telehealth:ab,ti OR (mobile NEAR/2 phone*):ab,ti OR telemonitoring:ab,ti OR 'real time':ab,ti OR app?:ab,ti) AND [embase]/lim AND [2000-2013]/py SR (14) en RCTs (73) (filters) – 36 uniek |
149 |
|
Wat is de optimale organisatie van zorg voor DM1 patiënten in de tweedelijn?
|
Medline (OVID), 2000-aug. 2012 Engels |
1 exp *Diabetes Mellitus, Type 1/ (45639) 2 ((diabetes adj1 type adj1 "1") or (type adj1 "1" adj1 diabetes)).ti. (10361) 3 ("insulin dependent diabetes" or IDDM).ti. (9198) 4 1 or 2 or 3 (49674) 9 "Specialization"/ (20678) 10 4 and 9 (30) 11 (endocrinologist* or "diabetes specialist" or diabetologist*).ti,ab. (2784) 12 "specialist care".ti,ab. (916) 13 (endocrinologist* or "diabetes specialist*" or diabetologist*).ti,ab. (2836) 14 endocrinology/ (4000) 15 or/11-14 (7409) 16 4 and 15 (282) 17 limit 16 to (english language and yr="2000 -Current") (145)
|
|
|
Zoekfilters voor systematische reviews en gerandomiseerd klinisch onderzoek zijn gebaseerd op de zoekfilters van het Scottish Intercollegiate Guidelines Network (SIGN) - http://www.sign.ac.uk/ |
|||

