Farmacotherapie van eerste keuze bij kinderen en adolescenten
Uitgangsvraag
Welk(e) antidepressivum/antidepressiva wordt/worden aanbevolen om als farmacotherapie van eerste keuze bij depressie bij kinderen en adolescenten in te zetten?
Aanbeveling
- We bevelen aan om behandeling met antidepressiva te combineren met psychoeducatie voor kinderen en ouders (zo nodig school), en psychologische begeleiding van de kinderen
- We bevelen aan om ouders/verzorgers en het kind of de adolescent actief te betrekken bij het besluitvormingsproces over de behandelstrategie.
- We bevelen aan om bij het voorschrijven van medicatie bij kinderen en jongeren met een depressie zorgvuldige informatie te geven over de reden voor de medicatie, over de tijd die het duurt voordat therapeutische effecten zichtbaar worden, de mogelijke bijwerkingen inclusief mogelijke toename van suïcidale gedachten en handelingen, het risico op terugval bij afbouwen van medicatie en over het belang van een goede therapietrouw.
- We bevelen aan om in de behandeling van depressies bij kinderen en adolescenten voortdurend de gevaren van de stoornis (risico op geslaagde suïcide, langdurige uitval van functioneren op sociaal, emotioneel en cognitief gebied) af te wegen tegen de risico's van de behandeling (met name risico op toename van suïcidale gedachten bij behandeling met SSRI's) en de beschikbaarheid van psychotherapie.
- Overweeg bij een matig ernstige of ernstige depressie waarbij gestart is met cognitieve gedragstherapie of IPT, bij onvoldoende resultaat na 6 weken met medicatie (fluoxetine) te starten. Hierbij dient vastgesteld te worden dat er nog steeds sprake is van een matig ernstige tot ernstige depressie die medicamenteuze behandeling behoeft.
- Overweeg fluoxetine of citalopram als eerste stap in de behandeling van een ernstige depressies bij kinderen ouder dan 8 jaar. Deze farmacotherapie moet gecombineerd plaatsvinden met CGT om een sneller resultaat te verkrijgen (zie module ‘Combinatiebehandeling’).
- We bevelen niet aan om kinderen en jongeren (<16 jaar) met een depressie met TCA’s te behandelen. Overweeg deze stap bij kinderen >16 jaar bij onvoldoende respons op een SSRI (fluoxetine, citalopram of sertraline) (volwassen richtlijn).
- We bevelen aan om jeugdigen met ernstige depressies wekelijks te zien. Frequente monitoring is noodzakelijk. Vooral in het begin van de behandeling moet controle plaats vinden van mogelijke suïcidale gedachten, intenties en handelingen. De patiënt en zijn ouders/verzorgers dienen te worden geïnstrueerd om contact op te nemen met de behandelaar bij het (later) optreden of onvoldoende verminderen van dit soort symptomen.
- Bij het optreden van een klinische respons op antidepressiva beveelt de Werkgroep aan om gedurende tenminste 6-9 maanden de medicatie te continueren. Nader onderzoek is nodig naar de duur van de voortgezette behandeling bij respons op medicatie of CGT en IPT, en naar effectieve strategieën ter voorkoming van terugval. De medicatie dient over een periode van tenminste 4-6 weken afgebouwd te worden. Hierbij dient altijd psychologische ondersteuning aangeboden te worden gezien het risico op terugval.
- Wij bevelen aan om bij een non-respons op behandeling met fluoxetine (of citalopram) gedurende 6 weken over te gegaan op een ander middel (sertraline of citalopram (of fluoxetine)), wederom in combinatie met cognitieve gedragstherapie. Hierbij dient vastgesteld te worden dat er nog steeds sprake is van een matig ernstige tot ernstige depressie die medicamenteuze behandeling behoeft.
- Wij bevelen onderzoek aan naar de verschillende behandelstrategieën waarbij psychologische interventies en medicatie (apart en in combinatie) met elkaar vergeleken worden. Onderzoek is ook nodig naar de meest effectieve behandeling van depressies die optreden als eerste manifestatie van een bipolaire stoornis bij kinderen en adolescenten.
Overwegingen
Kwaliteit van het bewijs
Er is een groot gebrek aan goede studies naar farmacotherapie bij kinderen en adolescenten. De kwaliteit van de studies is vaak slecht (studies met vele deelnemende centra (en dus één a twee patiënten geïncludeerd per centrum) en nauwelijks geschoold personeel). De reden voor deze kwalitatief slechte studies was het in de inleiding al genoemde feit dat het doen van studies bij kinderen en adolescenten een mogelijkheid was om patenten te verlengen. De verwachting is dat er de komende jaren weinig tot geen nieuwe studies zullen komen, al dan niet gesponsord door de industrie.
In de geselecteerde studies bestaat er een hoge placeborespons en een gering verschil in respons tussen placebo en medicatie. Dit geeft aan dat aspecifieke factoren (zoals het geven van goede uitleg, psychoeducatie, geven van hoop op herstel, een goede therapeutische relatie, uitgebreide monitoring van symptomen) een grote rol spelen bij de respons op SSRI's. Dit wordt mede ondersteund doordat er een groot verschil in effectiviteit bestaat tussen het effect van placebobehandeling en een wachtlijstcontrolegroep. Placebo is effectiever dan een wachtlijstgroep. Het verschil tussen placebo en wachtlijst zijn juist de aspecifieke factoren.
Alle resultaten van RCT's zijn afkomstig uit strak opgezette algoritmisch uitgevoerde behandelingen met frequente afspraken en zelfmonitoring, waarbij aspecifieke factoren belangrijk zijn. Dit kan betekenen dat de effecten van antidepressiva in de RCT's een overschatting kunnen aangeven ten opzichte van de resultaten in de doorsnee klinische praktijk. Het kan ook dat hierdoor de respons in de placebogroepen groter werd, in dat geval wordt het verschil tussen een antidepressivum en het placebo relatief kleiner.
Een gebeurtenis die het vertrouwen in studies bij kinderen en adolescenten heeft verminderd is de heranalyse van de SmithKline Beecham studie 329 (Le Noury et al., 2015). In 2001 hebben Keller et al. een studie gepubliceerd met als conclusie dat paroxetine zowel effectief is als goed getolereerd wordt bij de behandeling van een depressie bij adolescenten. Bij de heranalyse in 2015 van de oorspronkelijke data bleek echter dat ze het eindpunt, een score onder de 8 op de Hamilton depressieschaal, achteraf hadden veranderd en dit dus niet in hun analyseplan vooraf zat. De nieuwe conclusie was nu dat zowel paroxetine als imipramine (ook meegenomen in deze studie) niet effectief waren in de behandeling van depressie bij adolescenten en dat het risico op bijwerkingen, inclusief suïcidaliteit, voor beide middelen was verhoogd, beide ten opzichte van placebo.
Een ander belangrijk punt is dat in bijna alle studies depressie tijdens follow-up zijn gemeten op basis van (afkapwaarden met) vragenlijsten en niet vastgesteld via een klinisch interview. Hierdoor is niet vast te stellen of er wel of niet sprake is van een depressie na behandeling.
Er is weinig bekend over de kans op remissie en functioneel herstel bij behandeling van kinderen en adolescenten met een depressie met een SSRI. In de TADS studie hadden de meeste klinische responders nog functionele beperkingen en waren ze niet in remissie bij 12 weken behandeling (Vitiello et al., 2016; Kennard et al., 2006). De uitkomstmaat kwaliteit van leven is breed en zegt met name iets als er een groot verschil is. Bij gelijke effecten blijft onduidelijk waardoor er geen verschil wordt ervaren en kan er een vertekening optreden doordat verschillende aspecten onder kwaliteit van leven vallen, maar wisselend uitpakken voor de verschillende condities (een betere stemming, maar meer bijwerkingen, kan netto een minder goede kwaliteit van leven betekenen).
Ook is er weinig bekend over de beoogde duur van een behandeling met SSRI’s. Er zijn twee zeer kleine continueringsstudies met fluoxetine gedaan (Emslie et al., 2004 & 2009). In de eerste studie (40 kinderen) werd een groep kinderen en adolescenten die goed reageerden op fluoxetine gerandomiseerd en de helft kreeg na 34 weken placebo. In de placebogroep was het recidiefpercentage 60 procent tegen 34 procent in de continueringsgroep. In de tweede studie (112 kinderen) was dit recidiefpercentage respectievelijk 69 en 42 procent. De resultaten van de twee continueringsstudies sluiten aan bij de resultaten die gevonden zijn bij volwassenen. Dit suggereert dat, in overeenstemming met de Multi Disciplinaire Richtlijn Depressie voor volwassenen, bij het bereiken van een klinische respons tenminste 6 tot 9 maanden dient te worden doorbehandeld met medicatie
Balans gewenste en ongewenste effecten
Een belangrijk medisch-ethisch principe is 'geen schade doen'. Dat betekent dat behandelingen niet alleen geëvalueerd moeten worden in termen van hun therapeutische werkzaamheid, maar ook in termen van het potentieel schade toebrengen aan de patiënt. Vaak is de veiligheid van het gebruik van antidepressiva bij kinderen en adolescenten niet aangetoond. De gevolgen/risico’s op lange termijn (o.a. ten aanzien van ontwikkeling van de hersenen) zijn niet goed onderzocht.
Suïcidaliteit omvat een toename van suïcidale gedachten, intenties en handelingen. Deze dienen -ook zonder gerapporteerde geslaagde suïcides in de studies- als klinisch relevant te worden beschouwd, gezien de impact ervan op de persoon zelf en zijn of haar omgeving. Anderzijds vallen onder het begrip suïcidale ideaties allerlei gedachten en ideeën over de dood en een einde aan je leven maken, maar ook gedachten aan zelfbeschadiging en jezelf pijn doen. Het begrip suïcidale ideatie is daarmee opgerekt. Deze gedachten zijn in potentie ernstige signalen maar ze zijn niet per definitie ernstig.
De kwaliteit van de studies is beperkt ten aanzien van suïcidaliteit. Enerzijds is suïcidaliteit met name bij de oudere studies een exclusiecriterium. Daarmee is het feitelijk onbekend hoe kinderen en jongeren met een depressie en verhoogd suïciderisico (of bijvoorbeeld met comorbide psychische aandoeningen) reageren op SSRI's. Anderzijds wordt suïcidaliteit bij nieuwere studies beter uitgevraagd dan bij oudere studies (tot 2003). Deze informatie-bias kan in het nadeel werken van meer moderne middelen.
De TADS studie (March, 2004) is een van de eerste studies die prospectief naar suïcidaliteit heeft gekeken. In deze 4-armige studie (CGT, fluoxetine, CGT plus fluoxetine en placebo) bleek er niet zo zeer een significante toename van suïcidale ideaties in de fluoxetine arm, maar minder afname dan in de CGT arm en de fluoxetine plus CGT arm.
Wat van belang is, is dat er een significant verhoogde odds-ratio wordt gevonden t.a.v. het optreden van suïcidaliteit bij het gebruik van antidepressiva bij kinderen en adolescenten (2.39 (CI 95% 1.31 - 4.33)) (Sharma et al., 2016), maar dat absolute risico’s van 11 per 1024 (1,07%) bij placebo versus 35 per 1160 (3,02%) bij antidepressiva overeenkomen met een Number Needed to Harm van 51,5. Dat wil zeggen dat er ongeveer 52 kinderen/adolescenten met antidepressiva moeten worden behandeld om 1 keer vaker een situatie met suïcidaliteit tegen te komen. Dit vraagt om alertheid bij de behandelaar.
Aanvullend bewijs
De meta-analyse van Hetrick et al. (2021) is geëxcludeerd, zie ‘zoekstrategie en selectie’ paragraaf. Het is mogelijk wel een belangrijke review die veel geraadpleegd zal worden en daarom is deze meegenomen als aanvullend bewijs.
Hetrick (2021)
Door middel van een systematische review met netwerkmeta-analyse (NMA) hebben Hetrick en collega’s (2021) onderzoek gedaan naar de relatieve effectiviteit en veiligheid van nieuwe generatie antidepressiva voor verschillende uitkomsten bij kinderen en adolescenten met een klinische depressie.
In totaal zijn 26 studies (n ≥ 6.400 op basis van 23 van de 26 studies; range n = 23-784 [mediaan = 275]) geïncludeerd, waarvan acht RCT’s alleen gericht waren op adolescenten tussen 12-18 jaar. Zestien RCT’s gericht op zowel kinderen als adolescenten hadden een lagere leeftijdsgrens van tussen 6-8 jaar. In de meeste RCT’s deden meer meisjes mee dan jongens, maar het ratio verschilde enorm zowel binnen trials (tussen de verschillende armen) als tussen RCT’s: van zeer kleine verschillen tot een verschil waarbij er twee keer zoveel meisjes als jongens meededen. Eén RCT had ongeveer gelijke verdeling van jongens en meisjes en bij vijf RCT’s deden meer jongens dan meisjes mee. Van drie RCT’s is niets bekend over sekse.
De twee primaire uitkomsten waren depressieve stoornis vastgesteld via klinische diagnostiek en suïcide, maar voor deze uitkomsten werden geen data gevonden, waardoor alleen secundaire uitkomsten zijn onderzocht. Secundaire uitkomsten die zijn onderzocht zijn depressiesymptomen (clinician-rated depression symptoms [CDRS-R schaal]) en suïcidaliteit en suïcidale gedachten volgens het Columbia Classification systeem. In de meeste studies die zijn meegenomen, was risico op zelfbeschadiging en suïcide een exclusiecriterium voor de studie.
De meeste antidepressiva kunnen geassocieerd worden met een relatief “kleine en onbelangrijke” afname van depressiesymptomen volgens de CDRS-R schaal (range 17 tot 113: minimaal klinisch relevant verschil [MCID] = 9 ± 2.24) ten opzichte van placebo In tabel 14.1 staat een overzicht van de effectiviteit van de verschillende antidepressiva (versus placebo) op depressiesymptomen.
Tabel 14.1 Effectiviteit antidepressiva versus placebo op depressiesymptomen (CDRS-R)
|
Antidepressivum |
MD (95% BI) |
|
Paroxetine |
-1.43 (-3.90, 1.04) |
|
Vilazodone |
-0.84 (-3.03, 1.35) |
|
Desvenlafaxine |
-0.07 (-3.51, 3.36) |
|
Sertraline |
-3.51 (-6.99, -0.04)* |
|
Fluoxetine |
-2.84 (-4.12, -1.56)* |
|
Escitalopram |
-2.62 (-5.29, 0.04) |
|
Duloxetine |
-2.70 (-5.03, -0.37)* |
|
Vortioxetine |
0.60 (-2.52, 3.72) |
|
Mirtazepine |
-2.72 (-6.72, 1.14) |
|
Citalopram |
-2.90 (-8.23, 2.43) |
|
Venlafaxine |
-1.90 (-5.17, 1.37) |
* significant op basis van betrouwbaarheidsinterval.
De proporties voor suïcidaal gedrag waren laag voor de meeste geïncludeerde studies en de 95% betrouwbaarheidsintervallen waren breed voor alle vergelijkingen. In de tabel 14.2 staat een overzicht van de kans van de verschillende antidepressiva (versus placebo) op suïcidaliteit en suïcidale gedachten.
Tabel 14.2 Effectiviteit van antidepressiva versus placebo op suïcidaliteit en suïcidale gedachten.
|
Antidepressivum |
OR (95% BI) |
|
Escitalopram |
0.89 (0.43, 1.84) |
|
Fluoxetine |
1.27 (0.87, 1.86) |
|
Paroxetine |
1.81 (0.85, 3.86) |
|
Sertraline |
3.03 (0.60, 15.22) |
|
Venlafaxine |
13.84 (1.79, 106.90)* |
|
Mirtazapine |
0.50 (0.03, 8.04) |
|
Duloxetine |
1.15 (0.72, 1.82) |
|
Vilazodone |
1.01 (0.68, 1.48) |
|
Desvenlafaxine |
0.94 (0.59, 1.52) |
|
Citalopram |
1.72 (0.76, 3.87) |
|
Vortioxetine |
1.58 (0.29, 8.60) |
* significant op basis van betrouwbaarheidsinterval.
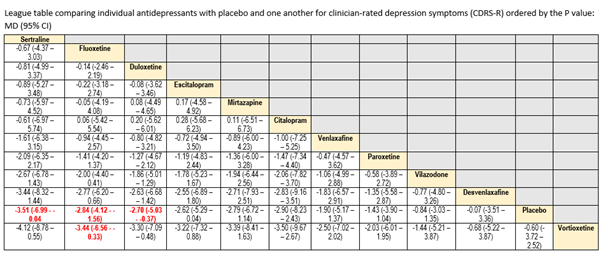
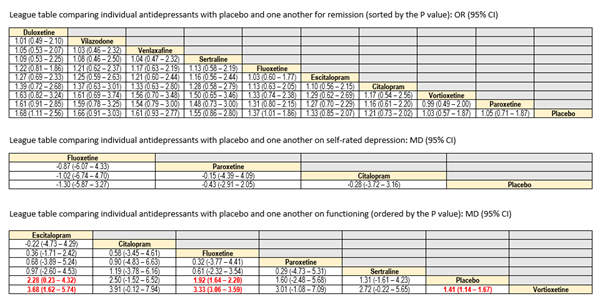
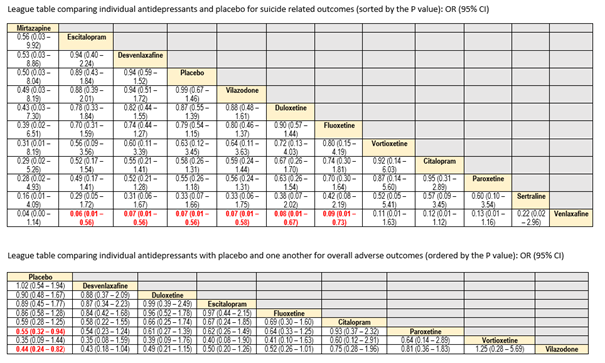
Er is onzekere evidentie dat venlafaxine resulteert in een kleine kans op suïcidaliteit en suïcidale gedachten vergeleken met desvenlafaxine (OR = 0.07, 95% CI: 0.01, 0.56) en escitalopram (OR = 0.06, 95% CI: 0.01, 0.56). Vergelijkingen tussen andere antidepressiva leidde tot een zeer lage mate van bewijs. In bijlage 10.5.4 zijn de league tables opgenomen, met daarin de effectiviteit van de verschillende antidepressiva (versus placebo of andere antidepressiva) op depressiesymptomen, remissie, zelf gerapporteerde depressie, functioneren, suïcidaliteit en suïcidale gedachten, en algemene nadelige uitkomsten.
Professioneel perspectief
Een depressie bij een kind of adolescent is voor de patiënt zelf en diens naasten een onverdraaglijke situatie, zodat in vele gevallen het niet behandelen geen optie is. Gezien de lijdenslast, het verlies van sociale rollen en scholingsachterstand die dreigt, zal in samenspraak een keuze over het starten van een behandeling moeten worden gemaakt. Bespreek daarbij de lage kwaliteit van het bewijs en bespreek expliciet het risico op toename van suïcidaliteit in het begin van de behandeling met patiënten en ouders. Blijf tegelijkertijd bewaken dat de therapietrouw optimaal is/blijft.
Hoewel in dit hoofdstuk expliciet naar effectiviteit t.o.v. placebo wordt gekeken is het op merkelijk dat in de netwerk meta-analyse van Zhou combinatiebehandelingen (psychotherapie met farmacotherapie) beter presteerden qua effectiviteit en dat psychotherapie beter was qua risico op toename van suïcidaliteit (Zhou et al., 2020). De Werkgroep is van mening dat aan kinderen en adolescenten er geen farmacotherapie zonder psychotherapie zou moeten worden aangeboden. Biedt tenminste een adjuvante behandeling in de vorm van psychoeducatie voor ouders (zo nodig school) en psychotherapie voor de jongere.
Fluoxetine is als enige SSRI in Nederland geregistreerd voor de behandeling van depressies vanaf de leeftijd van 8 jaar. Uit een onderzoek naar prescripties door Kinder- en Jeugdpsychiaters is er een clinician based voorkeur voor citalopram (de Vries et al., 2016). Reden daarvoor is dat Fluoxetine een lange halfwaardetijd heeft (men breekt fluoxetine minder snel af) en Citalopram minder bijwerkingen heeft. Echter bij non-compliance (wat vaker voorkomt bij kinderen en adolescenten), is de langere halfwaardetijd van fluoxetine juist weer een voordeel.
De NICE richtlijn (National Institute for Health and Care Excellence, 2019) beveelt sertraline of citalopram - in combinatie met cognitieve gedragstherapie of interpersoonlijke Therapie - aan als tweedelijns SSRI's bij kinderen en adolescenten met depressies (National Institute for Health and Care Excellence, 2019).
TCA’s worden tot nu toe alleen als eventuele 2e of 3e stap gebruikt en in de praktijk worden TCA’s hoogst zelden onder de 16 jaar voorgeschreven. TCA’s blijken in meta-analyses niet effectief bij kinderen t.o.v. placebo (Hazell et al., 1995; Tsapakis et al., 2008). TCA's kunnen aanzienlijke bijwerkingen hebben: van anticholinerge aard (tachycardie, droge mond, obstipatie, mictieproblemen) en van antihistaminerge aard (sedatie, gewichtstoename). Bij overdosering zijn TCA's cardiotoxisch door beïnvloeding van de hartgeleiding.
Voor de stappenvolgorde bij onvoldoende respons vanaf 16 jaar wordt meestal gebruik gemaakt van het stappenplan zoals in deze richtlijn opgesteld voor de volwassenen met een depressie. Uiteraard zijn daar vraagtekens bij te zetten o.b.v. het ontbreken van specifieke studies
Voor het starten met een SSRI dient de familieanamnese op bipolariteit goed te worden uitgevraagd. Een vroeg begin van een depressie kan prognostisch zijn voor het ontwikkelen van een bipolaire stoornis (Curry et al., 2011; Mesman et al., 2013).
Indien er gestart wordt met een SSRI, wordt aangeraden dit met een halve dosering te doen (10 mg fluoxetine, 10 mg citalopram) en op geleide van de klachten en bijwerkingen te verhogen. Hoger doseren dan 20 mg is zelden nodig.
Twee dagen na starten met de medicatie dient een telefonisch contact plaats te vinden over eventuele bijwerkingen, met name eventuele ontremming, toename van wanhoop of suïcidaliteit en slecht slapen. Het is aan te raden met kinderen en adolescenten en ouders te bespreken bij eventuele tekenen van ontremming direct te bellen met de arts.
De eerste maand van de behandeling wordt aangeraden het kind of de adolescent (en ouders) wekelijks te controleren, de tweede maand om de andere week en daarna na 3 maanden (Cheung et al., 2005). Naast het effect op de stemming dienen eventuele ontremming en toename van wanhoop of suïcidaliteit te worden besproken (zie ook module Klinisch management behandeling met antidepressiva).
In ongeveer 30% van de gevallen is sprake van terugval van depressie binnen een periode van 5 jaar. Er zijn eerste aanwijzingen dat terugval na 6 tot 12 maanden onder adolescenten minder was bij gebruik van antidepressiva in vergelijking met placebo (Robberegt et al., 2023). Bij het afbouwen van medicatie wordt het risico op terugval hoger (ongeveer 60% terugval) (Emslie et al., 2009)
Middelenbeslag
Voor farmacotherapie of psychotherapie is qua beschikbaarheid bij instellingen geen verschil qua mogelijkheid. Psychotherapie is wel duurder gezien de tijdsduur van een sessie op korte termijn. Mogelijk duren de effecten op lange termijn langer, en zijn de kosten op e termijn dus lager. Hier is echter geen onderzoek over gevonden.
Organisatie van zorg
De Werkgroep is van mening dat het voorschrijven van medicatie aan kinderen en adolescenten met een depressie alleen dient te gebeuren na diagnostiek door iemand met specialistische kennis op dit terrein, doorgaans een kinder- en jeugdpsychiater. Hierbij bestaat er in de huidige organisatie van zorg een groot probleem qua wachttijd om deze diagnostiek en behandeling te krijgen van de Jeugd GGZ. Gezien de dreigende stagnatie van de ontwikkeling bij kinderen en adolescenten met een depressie dient behandeling echter snel te worden ingezet De Werkgroep pleit daarom voor een voorrang voor kinderen en adolescenten met een depressie en om voor die groep een acute verwijsmogelijkheid te creëren. Het is niet de taak van de huisarts om deze medicatie voor te schrijven.
Maatschappelijk perspectief
Er bestaat een taboe op het gebruik van antidepressiva en bij kinderen en adolescenten in het bijzonder. Deels is de terughoudendheid te begrijpen vanwege de gebrekkige studies, de onbekendheid rond eventuele lange-termijneffecten en het toegenomen risico op suïcidaliteit. Echter als er in samenspraak met de patiënt en diens ouders/naastbetrokkenen een keuze voor antidepressiva is gemaakt, zal die keuze gesteund moeten worden. Adequate voorlichting hierover is wenselijk. Belangrijk is te realiseren dat de lange termijneffecten van depressie bij kinderen en adolescenten een achterstand in sociale ontwikkeling en schoolprestaties zijn. Dit zijn belangrijke secundaire aspecten om beter te voorkomen dan nadien te repareren.
Onderbouwing
Depressie in de kindertijd en adolescentie is recidiverende of zelfs chronische ziektebeeld met een aanzienlijke morbiditeit en mortaliteit, die een zorgvuldige diagnostiek, een snelle behandeling en preventieve maatregelen vereisen, zowel ter voorkoming van een eerste episode als van recidieven (Rao & Chen, 2009; Curry, 2011). Er is beperkt Nederlands epidemiologisch onderzoek. Een substantieel deel van de jongeren (21,4%) heeft last van subklinische depressie (Smit et al., 2003).Uit Amerikaans epidemiologisch onderzoek (The Great Smokey Mountains Study) komt naar voren dat, gemeten over een periode van drie maanden, 2,8% van de meisjes en 1,6% van de jongens tussen de 9 en 16 jaar uit de algemene bevolking een stemmingsstoornis doormaakt. Onder 13- en 14-jarigen heeft 8,4% van de jongeren te maken gehad met een depressieve stoornis; de kans dat een achttienjarige een stemmingsstoornis heeft doorgemaakt is gestegen tot 18,1% (Merikangas et al., 2010). In een recente meta analyse was de wereldwijde prevalentie van een depressieve stoornis onder jongeren 8% (Shorey et al., 2022).
Het klinisch beeld van de depressie bij kinderen en adolescenten verschilt in principe niet van dat bij volwassenen. Ook bij hen worden de kernsymptomen gevormd door een sombere stemming en een verlies van plezier in activiteiten. Maar de manier waarop de kernsymptomen tot uiting komen verschilt per leeftijd en in verschillende ontwikkelingsfasen worden andere begeleidende verschijnselen gezien. Dit bemoeilijkt de diagnostiek (zie hiervoor Kenniscentrum Kinder- en Jeugdpsychiatrie).
Gezien de ontwikkelingstaken van kinderen en adolescenten is op tijd starten met een behandeling (psychologische en farmacologisch) zeer van belang. Betrouwbaar onderzoek naar de behandeling bij kinderen en jeugdigen met antidepressiva (SSRI’s) is, ondanks vele oproepen hiervoor, nog steeds nauwelijks gebeurd. Vanaf 1997 zijn er weliswaar 191 studies bij kinderen en jeugdigen ingediend bij de FDA, maar er zijn slechts 58 studies uitgevoerd. Aanleiding hiervoor was de aankondiging dat bepaalde middelen na januari 2002 uit patent zouden gaan en lopend onderzoek dit patent kon verlengen. De kwaliteit van deze studies is echter zeer discutabel (zo werden er bijvoorbeeld tot 60 sites per studie geïncludeerd).
In de praktijk worden antidepressiva wel voorgeschreven aan kinderen en jeugdigen. Het is daarbij belangrijk om de beperkte evidentie hiervoor samen te vatten en o.b.v. deze samenvattingen aanbevelingen te doen.
|
Het gebruik van antidepressiva bij kinderen en adolescenten met een depressieve stoornis |
|
|
⊕◯◯◯ |
Fluoxetine lijkt depressieve klachten bij kinderen en adolescenten te verminderen, maar het bewijs is zeer onzeker. Zhou et al. ( 2020) |
|
⊕◯◯◯ |
Het bewijs is zeer onzeker over het effect van fluoxetine op verdraagzaamheid. Zhou et al. (2020) |
|
⊕⊕⊕◯ |
Ten opzichte van venlafaxine vermindert fluoxetine waarschijnlijk de kans op suïcidaliteit en suïcidale gedachtes. Zhou et al. (2020 ) |
|
⊕◯◯◯ |
Het bewijs is zeer onzeker over het effect van 2de generatie antidepressiva op het welbevinden. Spielmans & Gerwig (2014) |
|
⊕◯◯◯ |
Antidepressiva lijken de kans op suïcidaliteit bij kinderen en adolescenten te vergroten maar de evidence is zeer onzeker. Sharma (2016) Zhou et.al. (2020 ) |
Zhou (2020)
In een goed uitgevoerde systematische review en netwerk meta-analyse (NMA) uitgevoerd door Zhou et al. (Zhou et al., 2020) (een gedeelte van de auteurs heeft betalingen ontvangen van de farmaceutische industrie voor werkzaamheden) is de effectiviteit en verdraagzaamheid van een zestiental antidepressiva en een zevental psychotherapieën in de behandeling van een depressieve stoornis (depressieve stoornis, dysthymie, andere gestandaardiseerde depressie diagnoses) bij kinderen en adolescenten (< 18 jaar) onderzocht. Hierbij werden ook studies meegenomen waarin deelnemers naast een depressieve stoornis een angststoornis of ADHD hadden. De studies met inclusie van comorbiditeit met andere psychische aandoeningen werden uitgesloten alsmede studies met een kortere looptijd dan 4 weken. Effectiviteit werd geoperationaliseerd als zijnde de gemiddelde reductie/toename in depressiesymptomen gemeten tussen baseline en op het moment van afronding van de behandeling. Verdraagzaamheid werd gedefinieerd als de proportie deelnemers die zich vroegtijdige terugtrokken uit de studie. Als secundaire uitkomstmaat werd het effect van het gebruik van antidepressiva op suïcidaal gedrag of suïcidale ideaties onderzocht.
In totaal zijn er 71 gepubliceerde en ongepubliceerde RCT’s (n=9510, gemiddelde leeftijd = 14 jaar, sd = 2.6) in deze netwerk MA meegenomen waarin het effect van antidepressiva, psychotherapie of en combinatie van deze twee werden onderzocht. De mediaan van de behandelingsduur was 8 weken. De auteurs maakten wel de notitie dat bij twee van de geïncludeerde studies de maximale leeftijd 20 jaar was, maar dat deze studies toch zijn meegenomen omdat het grootste deel van de participanten jonger dan 18 jaar was. Voor het beantwoorden van de huidige uitgangsvraag zal er alleen gekeken worden naar het effect van het gebruik van een antidepressivum als monotherapie en worden de vergelijkingen van een antidepressivum met placebo gebruikt om de uitgangsvraag te beantwoorden. Voor de head-to-head (directe vergelijking tussen antidepressiva) vergelijkingen van individuele antidepressiva en het effect van psychotherapie wordt verwezen naar figuur 3 in het artikel van Zhou en collegae (Zhou et al., 2020).
De auteurs voerden ook een CINeMA assessment uit om het vertrouwen in het bewijs te boordelen. Deze methode heeft gelijkenissen met de GRADE methode maar is toegespitst op het gebruik bij netwerk meta-analyses. Hieruit kwam naar voren dat erover het algemeen gesteld kan worden dat er verhoogde heterogeniteit in de baseline karakteristieken van de verschillende studies waren. Zo waren de ernst van de depressiesymptomen niet gelijk en waren er verschillen in de gemiddelde leeftijd, duur van de behandeling en de genderverdeling. Verder waren er verschillen tussen de studies in de toegepaste doseringen van antidepressiva en werden er voor de uitkomstmaat van effectiviteit verschillende meetinstrumenten gebruikt, hetgeen zorgt voor een verhoogde onnauwkeurigheid van het bewijs. Ook noteerden de auteurs in veel gevallen een verhoogde “risk of bias” bij de geïncludeerde studies en inconsistentie in de resultaten. De uitgevoerde CINeMA assessment zoals beschreven in Zhou et al. (Zhou et al., 2020) is overgenomen.
Effectiviteit
Wanneer er gekeken wordt naar de effectiviteit van het gebruik van een antidepressivum als monotherapie op depressiesymptomen in vergelijking met een placeboconditie, dan laat alleen fluoxetine een significante verbetering zien, terwijl nortriptyline een significante toename in symptomen laat zien t.o.v. placebo. Een overzicht van de effectiviteit van alle antidepressiva en het vertrouwen in het bewijs wordt in tabel 14.3 weergegeven.
Tabel 14.3 Effectiviteit antidepressiva versus placebo*
|
Antidepressivum |
SMD (95% BI**) |
Vertrouwen in het bewijs*** |
|
Fluoxetine |
–0.51 (–0.84; –0.18)# |
Zeer laag |
|
Desipramine |
–0.43 (–1.26; 0.39) |
Zeer laag |
|
Venlafaxine |
–0.25 (–0.87; 0.36) |
Zeer laag |
|
Mirtazapine |
–0.23 (–0.97; 0.50) |
Zeer laag |
|
Duloxetine |
–0.22 (–0.85; 0.42) |
Laag |
|
Citalopram |
–0.18 (–0.89; 0.55) |
Zeer laag |
|
Escitalopram |
–0.17 (–0.88; 0.54) |
Zeer laag |
|
Paroxetine |
–0.16 (–0.67; 0.35) |
Zeer laag |
|
Nefazodone |
–0.14 (–0.85; 0.57) |
Zeer laag |
|
Desvenlafaxine |
–0.12 (–0.79; 0.54) |
Laag |
|
Sertraline |
–0.11 (–0.71; 0.49) |
Zeer laag |
|
Vilazodone |
–0.09 (–1.09; 0.90) |
Laag |
|
Imipramine |
–0.03 (–0.75; 0.68) |
Laag |
|
Amitriptyline |
0.08 (–1.11; 1.27) |
Zeer laag |
|
Clomipramine |
0.33 (–0.83; 1.48) |
Laag |
|
Nortriptyline |
1.14 (0.46; 1.81)# |
Zeer laag |
* Alleen behandelingen met alleen een antidepressivum meegenomen. In de gehele NMA stond op 1 Imipramine in combinatie met CGT, op 2 fluoxetine in combinatie met CGT en op 3 CGT in combinatie met placebo.
** Betrouwbaarheidsinterval.
*** CINeMA assessment beoordeling overgenomen uit Zhou et al. (2020).
# Significant effect (p < 0.05).
Verdraagzaamheid
Ten opzichte van placebo lijken de meeste antidepressiva niet significant te verschillen van een placebo conditie in termen van verdraagzaamheid. Een uitzondering hierop lijkt het gebruik van imipramine te zijn waarbij een toename in studie uitval lijkt te zijn t.o.v. placebo. Een overzicht van de verdraagzaamheid bij alle antidepressiva en het vertrouwen in het bewijs wordt in tabel 14.4 weergegeven.
Tabel 14.4 Verdraagzaamheid antidepressiva versus placebo*
|
Antidepressivum |
OR (95% Crl*) |
Vertrouwen in het bewijs*** |
|
Nefazodone |
0.49 (0.21; 1.39) |
Zeer laag |
|
Vilazodone |
0.59 (0.27; 1.54) |
Laag |
|
Fluoxetine |
0.78 (0.56; 1.15) |
Zeer laag |
|
Desvenlafaxine |
0.85 (0.47; 1.74) |
Laag |
|
Mirtazapine |
0.83 (0.40; 2.08) |
Zeer laag |
|
Nortriptyline |
0.76 (0.28; 3.41) |
Zeer laag |
|
Citalopram |
0.96 (0.52; 1.97) |
Zeer laag |
|
Duloxetine |
1.04 (0.62; 1.96) |
Laag |
|
Venlafaxine |
1.12 (0.53; 2·69) |
Zeer laag |
|
Paroxetine |
1.30 (0.81; 2.27) |
Zeer laag |
|
Escitalopram |
1.40 (0.77; 2.86) |
Zeer laag |
|
Amitriptyline |
1.16 (0.29; 12.13) |
Zeer laag |
|
Sertraline |
1.61 (0.89; 3.27) |
Zeer laag |
|
Clomipramine |
1.75 (0.66; 6.57) |
Laag |
|
Desipramine |
2.21 (0.88; 7.67) |
Zeer laag |
|
Imipramine |
2.51 (1.26; 6.24)# |
Redelijk |
* Alleen behandelingen met alleen een antidepressivum meegenomen.
** Kritisch interval.
*** CINeMA assessment beoordeling overgenomen uit Zhou et al. (2020).
# Significant effect (p < 0.05).
Effect op suïcidaliteit en suïcidale gedachten.
Als er gekeken wordt naar het effect van het gebruik een antidepressivum op suïcidaliteit en het krijgen van suïcidale gedachten lijkt venlafaxine t.o.v. van placebo een significante verhoogde kans op suïcidaliteit te geven. Vervolgens hebben Zhou en collega’s de kans op het optreden suïcidaliteit of het optreden van suïcidale gedachten van de andere antidepressiva vergeleken t.o.v. venlafaxine. Uit deze vergelijking komt naar voren dat venlafaxine een verhoogde kans geeft op het optreden van suïcidaliteit of suïcidale gedachten in vergelijking met desvenlafaxine, imipramine, duloxetine, escitalopram, fluoxetine en citalopram. Een overzicht van alle antidepressiva en het vertrouwen in het bewijs wordt in tabel 14.5 weergegeven. Het is niet duidelijk wat het risico op suïcidaliteit en suïcidale gedachten per antidepressivum is.
Tabel 14.5 Suïcidaliteit en suïcidale ideatie bij antidepressiva versus Venlafaxine*
|
Antidepressivum |
OR (95% Crl*) |
Vertrouwen in het bewijs*** |
|
Nefazodone |
0.17 (0.00;1.03) |
Zeer lag |
|
Desvenlafaxine |
0.10 (0.00; 0.45)# |
Redelijk |
|
Imipramine |
0.12 (0.00; 0.64) # |
Redelijk |
|
Duloxetine |
0.12 (0.00; 0.54) # |
Redelijk |
|
Escitalopram |
0.14 (0.00; 0.68) # |
Laag |
|
Mirtazapine |
0.78 (0.00; 4.15) |
Zeer laag |
|
Fluoxetine |
0.14 (0.00; 0.60) # |
Redelijk |
|
Citalopram |
0.20 (0.00; 0.99) # |
Zeer laag |
|
Clomipramine |
0.25 (0.00; 1.30) |
Zeer laag |
|
Paroxetine |
0.25 (0.01; 1.22) |
Zeer laag |
|
Vilazodone |
0.03 (0.01; 10.13) |
Zeer laag |
|
Sertraline |
0.43 (0.01; 2.41) |
Zeer laag |
|
Venlafaxine† |
8.31 (1.92; 343.17) # |
Laag |
* Alleen behandelingen met alleen een antidepressivum meegenomen. In de gehele NMA stonden op plek 1 t/m 5 (als minst risicovol) CGT en andere vormen van psychotherapie.
** Kritisch interval.
*** CINeMA assessment beoordeling overgenomen uit Zhou et al. (2020).
# Significant effect (p < 0.05).
† Vergeleken met placebo conditie.
Sharma (2016)
In een systematic review met meta-analyse van Sharma en collegae (Sharma et al., 2016) onderzochten zij ernstige bijwerkingen van SSRIs en SNRIs: duloxetine (k=23), fluoxetine (k=3), paroxetine (k=8), sertraline (k=28), en venlafaxine (k=8). De 70 dubbelblinde placebogecontroleerde RCT’s (waarvan 34 voor een depressie, N= 7882) komen van Europese en Britse regelgevende instanties voor geneesmiddelen, en van samenvattingen van onderzoeksrapporten van Eli Lilly's website. Er werden in totaal 18.526 patiënten (12% kinderen/adolescenten;) geïncludeerd. In 63% van de studies was risico op suïcide een exclusie criterium.
Spielmans (2014)
De meta-analyse van Spielsmans (Spielmans & Gerwig, 2014) is een van de weinige meta-analyses die kijkt naar het effect van het gebruik van een antidepressivum op het welbevinden bij kinderen en adolescenten. In deze meta-analyse werden alleen RCT’s met een placebo controleconditie meegenomen waarbij geen “add-on” therapie of medicatie gegeven werd. De geïncludeerde 3 RCT’s gebruikten de volgende antidepressiva als interventie: citalopram, fluoxetine, paroxetine en sertraline. De uitkomstmaat van welbevinden omvat de kwaliteit van leven, functioneren en algemene mentale gezondheid/welbevinden. Wanneer er gekeken wordt naar het welbevinden (op basis van zelfrapportages en door ouders gerapporteerde scores) bleek er geen significant verschil te zijn in het welbevinden wanneer een antidepressivum wordt gebruikt ten opzichte van een placebo, zie tabel 4 voor effecten en GRADE beoordeling. Op basis van de beschrijving van de meta-analyse is het onduidelijk welke studies precies gebruikt zijn om de effect-sizes te berekenen. Om deze reden is er gekozen om de risk of bias als verhoogd in te schalen. Om dezelfde reden is het ook lastig om de sample grootte van de specifieke RCT’s te bepalen die gebruikt zijn voor de schatting van het effect. De auteurs geven echter aan dat de meta-analyse gebaseerd is op een kleine sample, daarom is er gedowngrade voor onnauwkeurigheid.
Tabel 14.6 PICO
|
Patiënts |
Kinderen en adolescenten (<18jr) met een depressieve stoornis |
|
Intervention |
Farmacotherapie met antidepressiva |
|
Control |
Actieve controle met een antidepressivum. Ander soort therapie zoals: Psychotherapie (al dan niet in combinatie met farmacotherapie) Ander soort therapie Placebo |
|
Outcome |
Symptomatisch herstel Functioneel herstel Kwaliteit van leven Werkhervatting Suïcidaliteit |
|
Time |
Vanaf 2010 tot heden |
Selectie van studies
Op 11 mei 2021 is er een search uitgevoerd in de PsychInfo databank en op 17 mei 2021 is er een search uitgevoerd in de Medline, Embase, en Cochrane databanken. De search leverde 372 referenties op. Na ontdubbelen en verouderde Cochrane reviews verwijderd te hebben bleven er 284 referenties over. Er is specifiek gekeken naar systematische reviews en meta-analyses en na beoordeling op titel en abstract bleven 21 referenties over voor de selectie op basis van de volledige teksten (Boaden et al., 2020; C et al., 2017; Cipriani et al., 2016; Cox et al., 2012, 2014; Gibbons et al., 2012; Hazell & Mirzaie, 2013; Hetrick et al., 2010, 2012; Ignaszewski & Waslick, 2018; Ma et al., 2014; Qin et al., 2014; Singh & Reece, 2014; Spielmans & Gerwig, 2014; Stevanovic et al., 2014; Varigonda et al., 2015; Viswanathan et al., 2020; Vitiello & Ordóñez, 2016; Xu et al., 2016; Zhou et al., 2014, 2020). Tijdens de selectie op basis van volledige teksten is er gekeken of er geen overlap tussen de verschillende systematische reviews is in termen van geïncludeerde studies, overlap in onderzochte uitkomstmaten en relevantie van de PICO. In het geval van overlap tussen reviews is er gekozen om, indien van toepassing, de publicatie mee te nemen waarin een meta-analyse is uitgevoerd en die het meest recent is uitgevoerd. Op basis van de volledige teksten zijn er uiteindelijk 2 systematische reviews geselecteerd (Spielmans & Gerwig, 2014; Zhou et al., 2020) voor verdere beoordeling. De netwerk meta-analyse van Zhou et al. (2020) is gekozen als meest recente en meest omvattende publicatie. De meta-analyse van Spielmans et al. (2014) is gekozen i.v.m. de uitkomstmaat kwaliteit van leven waarover wordt gerapporteerd. Verder is er gebruik gemaakt van de resultaten van de zoekstrategie van het NHG voor de module ´Risico op suïcidaliteit door antidepressiva´, De zoekactie leverde één relevante systematische review op (Sharma et al., 2016). Tijdens het richtlijn proces is de search in 2022 geüpdatet en is er een aanvullende meta-analyse gevonden (Hetrick et al., 2021), deze is geëxcludeerd omdat alleen de RCT’s die depressie met de CDRS-R meten werden geïncludeerd. Hierdoor zijn er minstens 12 relevante RCT’s niet opgenomen in de NMA van Hetrick (2021). Het is mogelijk wel een belangrijke review die veel geraadpleegd zal worden en daarom is deze meegenomen als aanvullend bewijs in de paragraaf ‘van bewijs naar aanbeveling’.
- Boaden, K., Tomlinson, A., Cortese, S., & Cipriani, A. (2020). Antidepressants in Children and Adolescents: Meta-Review of Efficacy, Tolerability and Suicidality in Acute Treatment. Frontiers in Psychiatry, 11(717). https://doi.org/10.3389/fpsyt.2020.00717
- Cheung, A. H., Emslie, G. J., & Mayes, T. L. (2005). Review of the efficacy and safety of antidepressants in youth depression. Journal of child psychology and psychiatry, and allied disciplines, 46(7), 735-754. https://doi.org/10.1111/j.1469-7610.2005.01467.x
- Cipriani, A., Zhou, X., Del Giovane, C., Hetrick, S. E., Qin, B., Whittington, C., Coghill, D., Zhang, Y., Hazell, P., Leucht, S., Cuijpers, P., Pu, J., Cohen, D., Ravindran, A. V, Liu, Y., Michael, K. D., Yang, L., Liu, L., & Xie, P. (2016). Comparative efficacy and tolerability of antidepressants for major depressive disorder in children and adolescents: a network meta-analysis. The Lancet, 388(10047), 881-890. https://doi.org/10.1016/S0140-6736(16)30385-3
- Cox, G. R., Callahan, P., Churchill, R., Hunot, V., Merry, S. N., Parker, A. G., & Hetrick, S. E. (2014). Psychological therapies versus antidepressant medication, alone and in combination for depression in children and adolescents. Cochrane Database of Systematic Reviews, 11. https://doi.org/10.1002/14651858.CD008324.pub3
- Cox, G. R., Fisher, C. A., De Silva, S., Phelan, M., Akinwale, O. P., Simmons, M. B., & Hetrick, S. E. (2012). Interventions for preventing relapse and recurrence of a depressive disorder in children and adolescents. Cochrane Database of Systematic Reviews, 11. https://doi.org/10.1002/14651858.CD007504.pub2
- Curry, J., Silva, S., Rohde, P., Ginsburg, G., Kratochvil, C., Simons, A., Kirchner, J., May, D., Kennard, B., Mayes, T., Feeny, N., Albano, A. M., Lavanier, S., Reinecke, M., Jacobs, R., Becker-Weidman, E., Weller, E., Emslie, G., Walkup, J., Kastelic, E., March, J. (2011). Recovery and recurrence following treatment for adolescent major depression. Archives of general psychiatry, 68(3), 263-269. https://doi.org/10.1001/archgenpsychiatry.2010.150
- De Vries, Y. A., de Jonge, P., Kalverdijk, L., Bos, J. H. J., Schuiling-Veninga, C. C. M., & Hak, E. (2016). Poor guideline adherence in the initiation of antidepressant treatment in children and adolescents in the Netherlands: choice of antidepressant and dose. European Child & Adolescent Psychiatry, 25(11), 1161-1170. https://doi.org/10.1007/s00787-016-0836-3
- Emslie, G. J., Heiligenstein, J. H., Hoog, S. L., Wagner, K. D., Findling, R. L., McCracken, J. T., Nilsson, M. E., & Jacobson, J. G. (2004). Fluoxetine treatment for prevention of relapse of depression in children and adolescents: a double-blind, placebo-controlled study. Journal of the American Academy of Child and Adolescent Psychiatry, 43(11), 1397-1405. https://doi.org/10.1097/01.chi.0000140453.89323.57
- Emslie, G. J., Ventura, D., Korotzer, A., & Tourkodimitris, S. (2009). Escitalopram in the treatment of adolescent depression: a randomized placebo-controlled multisite trial. Journal of the American Academy of Child and Adolescent Psychiatry, 48(7), 721-729. https://doi.org/10.1097/CHI.0b013e3181a2b304
- Gibbons, R. D., Brown, C. H., Hur, K., Davis, J. M., & Mann, J. J. (2012). Suicidal Thoughts and Behavior With Antidepressant Treatment. Archives of General Psychiatry, 69(6), 580. https://doi.org/10.1001/archgenpsychiatry.2011.2048
- Hazell, P., & Mirzaie, M. (2013). Tricyclic drugs for depression in children and adolescents. Cochrane Database of Systematic Reviews, 6. https://doi.org/10.1002/14651858.CD002317.pub2
- Hazell, P., OConnell, D., Heathcote, D., Robertson, J., & Henry, D. (1995). Efficacy of tricyclic drugs in treating child and adolescent depression: a meta-analysis. BMJ (Clinical Research Ed.), 310(6984), 897-901. https://doi.org/10.1136/bmj.310.6984.897
- Hetrick, S. E., McKenzie, J. E., Cox, G. R., Simmons, M. B., & Merry, S. N. (2012). Newer generation antidepressants for depressive disorders in children and adolescents. Cochrane Database of Systematic Reviews, 11. https://doi.org/10.1002/14651858.CD004851.pub3
- Hetrick, S. E., McKenzie, J. E., & Merry, S. N. (2010). The use of SSRIs in children and adolescents. Current Opinion in Psychiatry, 23(1), 53-57. http://search.ebscohost.com/login.aspx?direct=true&db=psyh&AN=2010-07009-010&site=ehost-live
- Hetrick S.E., McKenzie J.E., Bailey, A.P., Sharma, V., Moller, C.I., Badcock, P.B., Cox, G.R., Merry, S.N., Meader N.. New generation antidepressants for depression in children and adolescents: a network meta-analysis. Version published: 24 May 2021 https://doi.org/10.1002/14651858.CD013674.pub2
- Ignaszewski, M. J., & Waslick, B. (2018). Update on randomized placebo-controlled trials in the past decade for treatment of major depressive disorder in child and adolescent patients: A systematic review. Journal of Child and Adolescent Psychopharmacology, 28(10), 668-675. https://doi.org/10.1089/cap.2017.0174
- Keller, M. B., Ryan, N. D., Strober, M., Klein, R. G., Kutcher, S. P., Birmaher, B., Hagino, O. R., Koplewicz, H., Carlson, G. A., Clarke, G. N., Emslie, G. J., Feinberg, D., Geller, B., Kusumakar, V., Papatheodorou, G., Sack, W. H., Sweeney, M., Wagner, K. D., Weller, E. B., Winters, N. C., McCafferty, J. P. (2001). Efficacy of paroxetine in the treatment of adolescent major depression: a randomized, controlled trial. Journal of the American Academy of Child and Adolescent Psychiatry, 40(7), 762-772. https://doi.org/10.1097/00004583-200107000-00010
- Kennard, B., Silva, S., Vitiello, B., Curry, J., Kratochvil, C., Simons, A., Hughes, J., Feeny, N., Weller, E., Sweeney, M., Reinecke, M., Pathak, S., Ginsburg, G., Emslie, G., March, J., & TADS Team (2006). Remission and residual symptoms after short-term treatment in the Treatment of Adolescents with Depression Study (TADS). Journal of the American Academy of Child and Adolescent Psychiatry, 45(12), 1404-1411. https://doi.org/10.1097/01.chi.0000242228.75516.21
- Le Noury, J., Nardo, J. M., Healy, D., Jureidini, J., Raven, M., Tufanaru, C., & Abi-Jaoude, E. (2015). Restoring Study 329: efficacy and harms of paroxetine and imipramine in treatment of major depression in adolescence. BMJ (Clinical research ed.), 351, h4320. https://doi.org/10.1136/bmj.h4320
- Ma, D., Zhang, Z., Zhang, X., & Li, L. (2014). Comparative efficacy, acceptability, and safety of medicinal, cognitive-behavioral therapy, and placebo treatments for acute major depressive disorder in children and adolescents: a multiple-treatments meta-analysis. Current Medical Research and Opinion, 30(6), 971-995. https://doi.org/10.1185/03007995.2013.860020
- March, J., Silva, S., Petrycki, S., Curry, J., Wells, K., Fairbank, J., Burns, B., Domino, M., McNulty, S., Vitiello, B., Severe, J., & Treatment for Adolescents With Depression Study (TADS) Team (2004). Fluoxetine, cognitive-behavioral therapy, and their combination for adolescents with depression: Treatment for Adolescents With Depression Study (TADS) randomized controlled trial. JAMA, 292(7), 807-820. https://doi.org/10.1001/jama.292.7.807
- Merikangas, K. R., He, J.-P., Burstein, M., Swanson, S. A., Avenevoli, S., Cui, L., Benjet, C., Georgiades, K., & Swendsen, J. (2010). Lifetime prevalence of mental disorders in U.S. adolescents: results from the National Comorbidity Survey Replication--Adolescent Supplement (NCS-A). Journal of the American Academy of Child and Adolescent Psychiatry, 49(10), 980-989. https://doi.org/10.1016/j.jaac.2010.05.017
- Mesman, E., Nolen, W. A., Reichart, C. G., Wals, M., & Hillegers, M. H. (2013). The Dutch bipolar offspring study: 12-year follow-up. The American journal of psychiatry, 170(5), 542-549. https://doi.org/10.1176/appi.ajp.2012.12030401
- National Institute for Health and Care Excellence (NICE). (2019). Depression in children and young people: identification and management - NICE guideline [NG134]. https://www.nice.org.uk/guidance/ng134
- Qin, B., Zhang, Y., Zhou, X., Cheng, P., Liu, Y., Chen, J., Fu, Y., Luo, Q., & Xie, P. (2014). Selective Serotonin Reuptake Inhibitors Versus Tricyclic Antidepressants in Young Patients: A Meta-analysis of Efficacy and Acceptability. Clinical Therapeutics, 36(7), 1087-1095.e4. https://doi.org/10.1016/j.clinthera.2014.06.001
- Rao, U., & Chen, L. (2009). Characteristics, correlates, and outcomes of childhood and adolescent depressive disorders. Dialogues in Clini- cal Neuroscience, 11, 45-62.
- Robberegt, S. J., Brouwer, M. E., Kooiman, B. E. A. M., Stikkelbroek, Y. A. J., Nauta, M. H., & Bockting, C. L. H. (2023). Meta-Analysis: Relapse Prevention Strategies for Depression and Anxiety in Remitted Adolescents and Young Adults. Journal of the American Academy of Child and Adolescent Psychiatry, 62(3), 306-317. https://doi.org/10.1016/j.jaac.2022.04.014
- Sharma, T., Guski, L. S., Freund, N., & Gotzsche, P. C. (2016). Suicidality and aggression during antidepressant treatment: systematic review and meta-analyses based on clinical study reports. BMJ, 352(1756-1833 (Electronic)), i65.
- Shorey, S., Ng, E. D., & Wong, C. H. J. (2022). Global prevalence of depression and elevated depressive symptoms among adolescents: A systematic review and meta-analysis. The British Journal of Clinical Psychology, 61(2), 287-305. https://doi.org/10.1111/bjc.12333
- Singh, N., & Reece, J. (2014). Psychotherapy, pharmacotherapy, and their combination for adolescents with major depressive disorder: A meta-analysis. The Australian Educational and Developmental Psychologist, 31(1), 47-65. http://search.ebscohost.com/login.aspx?direct=true&db=psyh&AN=2014-29011-005&site=ehost-live
- Spielmans, G. I., & Gerwig, K. (2014). The Efficacy of Antidepressants on Overall Well-Being and Self-Reported Depression Symptom Severity in Youth: A Meta-Analysis. Psychotherapy and Psychosomatics, 83(3), 158-164. https://doi.org/10.1159/000356191
- Stevanovic, D., Tadic, I., & Knez, R. (2014). Are antidepressants effective in quality of life improvement among children and adolescents? A systematic review. CNS Spectrums, 19(2), 134-141. https://doi.org/10.1017/S1092852913000576
- Tsapakis, E. M., Soldani, F., Tondo, L., & Baldessarini, R. J. (2008). Efficacy of antidepressants in juvenile depression: meta-analysis. The British Journal of Psychiatry?: The Journal of Mental Science, 193(1), 10-17. https://doi.org/10.1192/bjp.bp.106.031088
- Varigonda, A. L., Jakubovski, E., Taylor, M. J., Freemantle, N., Coughlin, C., & Bloch, M. H. (2015). Systematic review and meta-analysis: Early treatment responses of selective serotonin reuptake inhibitors in pediatric major depressive disorder. Journal of the American Academy of Child & Adolescent Psychiatry, 54(7), 557-564. http://search.ebscohost.com/login.aspx?direct=true&db=psyh&AN=2015-27624-011&site=ehost-live
- Viswanathan, M., Kennedy, S. M., McKeeman, J., Christian, R., Coker-Schwimmer, M., Cook Middleton, J., Bann, C., Lux, L., Randolph, C., & Forman-Hoffman, V. (2020). No Title. Agency for Healthcare Research and Quality, 4.
- Vitiello, B., & Ordóñez, A. E. (2016). Pharmacological treatment of children and adolescents with depression. Expert Opinion on Pharmacotherapy, 17(17), 2273-2279. https://doi.org/10.1080/14656566.2016.1244530
- Xu, Y., Bai, S. J., Lan, X. H., Qin, B., Huang, T., & Xie, P. (2016). Randomized controlled trials of serotonin-norepinephrine reuptake inhibitor in treating major depressive disorder in children and adolescents: A meta-analysis of efficacy and acceptability. Brazilian Journal of Medical and Biological Research, 49(6), 1-8. http://search.ebscohost.com/login.aspx?direct=true&db=psyh&AN=2016-26345-008&site=ehost-live
- Zhou, X., Michael, K. D., Liu, Y., Del, G. C., Qin, B., Cohen, D., Gentile, S., & Xie, P. (2014). Systematic review of management for treatment-resistant depression in adolescents. BMC Psychiatry, 14(1471-244X (Electronic)), 340.
- Zhou, X., Teng, T., Zhang, Y., Del Giovane, C., Furukawa, T., Weisz, J. R., Li, X., Cuijpers, P., Coghill, D., Xiang, Y., Hetrick, S. E., Leucht, S., Qin, M., Barth, J., Ravindran, A. V, Yang, L., Curry, J., Fan, L., Silva, S. G., Xie, P. (2020). Comparative efficacy and acceptability of antidepressants, psychotherapies, and their combination for acute treatment of children and adolescents with depressive disorder: a systematic review and network meta-analysis. The Lancet Psychiatry, 7(7), 581-601. https://doi.org/10.1016/S2215-0366(20)30137-1
League tables Hetrick (2011)
Spielmans (2014)
Tabel 14.7 Effect van antidepressivum op suicidaliteit vergeleken met placebo bij kinderen/adolescenten met een depressieve stoornis.
|
Uitkomsten |
Absolute effecten* |
Relatief effect |
Aantal deelnemers |
Vertrouwen in het bewijs |
Opmerkingen |
|
|
Risico met placebo |
Risico met antidepressivum |
|||||
|
Suicidaliteit |
11 per 1024 |
35 per 1160 |
Odds ratio: 2.39 (1.31 - 4.33) |
Gebaseerd op data van 2184 patiënten. |
⊕◯◯◯ |
Het bewijs is zeer onzeker over het effect van een antidepressivum op het welbevinden. |
a. Risico op bias: Ernstig. Inconsistentie: Zeer ernstig. Indirect bewijs: Ernstig. Publicatie bias: Ernstig.
Tabel 14.8 Effect van antidepressivum op welbevinden vergeleken met placebo bij kinderen/adolescenten met een depressieve stoornis.
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Vertrouwen in het bewijs |
Opmerkingen |
|
|
Risico met placebo |
Risico met antidepressivum |
|||||
|
Welbevinden (gemeten op het einde van interventie) |
- |
Hedges’ g 0.11 |
- |
(3 RCTs) |
⊕◯◯◯ |
Het bewijs is zeer onzeker over het effect van een antidepressivum op het welbevinden. |
a. Op basis van gegevens uit MA niet vast te stellen wat de RoB was.
b. Verschillende uitkomsten maten en constructen gebruikt om wellbevinden te meten.
c. klein aantal observaties, en 95%BI doorkruist het gebied van geen verschil.
Beoordelingsdatum en geldigheid
Publicatiedatum : 23-05-2024
Beoordeeld op geldigheid : 01-03-2024
Algemene gegevens
Voor de Multidisciplinaire richtlijn Depressie (2013) zijn in het kader van de onderhavige richtlijnherziening nieuwe modules ontwikkeld. In deze modules wordt ingegaan op de beantwoording van uitgangsvragen bij actuele knelpunten in de praktijk van de zorg voor depressie. Uitzondering hierop vormen de modules Diagnostiek, Basisinterventies en eerste-stap interventies en Ondersteunende interventies, voor deze module heeft alleen een tekstrevisie plaatsgevonden.
Samenstelling werkgroep
De Multidisciplinaire richtlijn Depressie is ontwikkeld door de Werkgroep Depressie, in opdracht van de Nederlandse Vereniging voor Psychiatrie (NVvP) en Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
De Werkgroep bestond uit: psychiaters, psychologen, verpleegkundig specialisten, een huisarts en ervaringsdeskundigen, welke door de respectievelijke beroepsverenigingen en patiëntenverenigingen werden afgevaardigd. Voorafgaande aan het ontwikkeltraject werden kennismakingsgesprekken gevoerd met verscheidene kandidaat-leden voor werkgroep deelname. Naast de Werkgroep waren enkele adviseurs betrokken, welke delen hebben meegeschreven en die werden gevraagd voorafgaand aan de commentaarfase schriftelijk te reageren op onderdelen van de concepttekst. Deze adviseurs konden tevens worden gevraagd om tijdens een werkgroep bijeenkomst mee te denken over een specifieke uitgangsvraag. De Werkgroep werd methodologisch, inhoudelijk en organisatorisch ondersteund door het technisch team van het Trimbos-instituut. Dit technisch team bestond uit een projectleider, redacteur/richtlijnontwikkelaar, informatiespecialist, literatuur reviewers, een notulist en projectassistenten. Onderstaande schema's geven een overzicht van de samenstelling van de Werkgroep, de adviseurs en het ondersteunend technisch team.
Leden Werkgroep
|
|
Naam |
Organisatie |
Beroepsvereniging |
|
1. |
Jan Spijker (voorzitter) |
Pro Persona |
Psychiater, NVvP |
|
2. |
Eric Ruhé (vicevoorzitter) |
Radboud UMC |
Psychiater, NVvP |
|
3. |
Claudi Bockting |
Amsterdam UMC |
Psycholoog, NIP |
|
3. |
Philip van Eijndhoven |
Radboud UMC |
Psychiater, NVvP |
|
4. |
Bart Groeneweg |
Depressievereniging |
Ervaringsdeskundige, MIND |
|
5. |
Rob Kok |
Parnassia |
Psychiater, NVvP |
|
6. |
Miranda Kurver |
NHG |
Huisarts, NHG |
|
7. |
Josephine van der Lande |
GGZ InGeest |
Verpleegkundig specialist, V&VN |
|
8. |
Nicoline Lous |
Depressievereniging |
Ervaringsdeskundige, MIND |
|
9. |
Catrien Reichart |
Curium-LUMC |
Psychiater, NVvP |
|
10. |
Marie-Louise Seelen |
PsyQ |
Verpleegkundig specialist, V&VN |
|
11. |
Marc Verbraak |
Pro Persona |
Psycholoog, NIP |
|
12. |
Christiaan Vinkers |
Amsterdam UMC en GGZ InGeest |
Psychiater, NVvP |
|
13. |
Yvonne Suijkerbuijk |
Amsterdam UMC/NVVG/UWV |
Verzekeringsarts, NVVG |
Adviseurs
|
Hoofdstuk |
Naam |
Organisatie |
Beroep |
|
Psychotherapie / stadiëring en profilering |
Ellen Driessen |
Pro Persona/ Radboud Universiteit |
GZ-psycholoog |
|
Psychotherapie / Jeugd |
Yvonne Stikkelbroek |
GGZ Oost-Brabant / Universiteit Utrecht |
Klinisch psycholoog |
|
Psychotherapie / Ouderen |
Arjan Videler |
GGZ Breburg |
Psychotherapeut, GZ-psycholoog |
|
Neuromodulatie
|
Ysbrand van der Werf |
A’dam UMC |
Neurowetenschapper |
|
Jeugd
|
Daan Creemers |
GGZ Oost-Brabant |
Klinisch psycholoog |
|
Jeugd
|
Fleur Velders |
UMC Utrecht |
Psychiater |
|
Ouderen
|
Gert-Jan Hendriks |
Pro Persona |
Psychiater |
|
Ouderen
|
Mardien Oudega |
GGZ InGeest |
Psychiater |
|
Ouderen
|
Angela Carlier |
Pro Persona |
Psychiater |
|
Ouderen |
Hans Jeuring |
UMCG |
Psychiater
|
|
Vaktherapie
|
Sonja Aalbers |
NHL Stenden |
Muziektherapeut |
|
Vaktherapie
|
Cees Boerhout |
Windesheim / Lentis |
Psychomotorisch therapeut |
|
Arbeidsgerichte zorg
|
Jeroen Roggekamp |
Zelfstandige |
Maatschappelijk werker / systeemtherapeut |
|
Arbeidsgerichte zorg |
Marjolein Bastiaansen |
Radboud UMC |
Bedrijfsarts |
|
Organisatie van de zorg voor depressie |
Bea Tiemens |
ProPersona |
|
Methodologische, inhoudelijke en organisatorische ondersteuning
|
Naam |
Ondersteuning |
|
Nicole van Erp / Piet Post |
Projectleider, Trimbos-instituut |
|
Jolanda Meeuwissen |
Redacteur en richtlijnontwikkelaar, Trimbos-instituut |
|
Egbert Hartstra |
Reviewer, Trimbos-instituut |
|
Matthijs Oud |
Reviewer, Trimbos-instituut |
|
Elena Vos |
Reviewer, Trimbos-instituut |
|
Erika Papazoglou |
Reviewer, Trimbos-instituut |
|
Bram Zwanenburg |
Reviewer, Trimbos-instituut |
|
Lex Hulsbosch |
Reviewer, Trimbos-instituut |
|
Beatrix Vogelaar |
Reviewer, Trimbos-instituut |
|
Rikie Deurenberg |
Informatiespecialist, namens Trimbos-instituut |
|
Chris van der Grinten / Jannita Paters |
Notulist, namens Trimbos-instituut |
|
Joyce Huls / Nelleke van Zon / Isa Reijgersberg |
Projectassistent, Trimbos-instituut |
In totaal kwam de Werkgroep Depressie voorafgaand aan de commentaarfase 10 keer bijeen in de periode november 2020 - april 2023. In deze periode werden de stappen van de methodiek voor evidence-based richtlijnontwikkeling (EBRO) doorlopen. De informatiespecialist verrichtte in overleg met de werkgroepleden op systematische wijze literatuuronderzoek en de reviewers maakten per uitgangsvraag een selectie in de gevonden onderzoeken (zie voor informatie over de zoekstrategie en de selectiecriteria: het reviewprotocol). De reviewers beoordeelden de kwaliteit en inhoud van de aldus verkregen literatuur en verwerkten deze per uitgangsvraag in evidence-tabellen, GRADE-profielen, beschrijvingen van de wetenschappelijke onderbouwing en wetenschappelijke (gewogen) conclusies (per module beschreven onder “Onderbouwing”). Leden van de Werkgroep gingen op basis van de gevonden literatuur met elkaar in discussie over praktijkoverwegingen (per module beschreven onder “Overwegingen”) en aanbevelingen (per module beschreven onder “Aanbevelingen”). De werkgroepleden schreven samen met het technisch team van het Trimbos-instituut de concepttekst, welke ter becommentariëring openbaar is gemaakt. De ontvangen commentaren worden verwerkt in een commentaartabel, die tijdens een werkgroep bijeenkomst wordt besproken. Na het doorvoeren van op deze bijeenkomst voorgestelde wijzigingen wordt de definitieve richtlijn aan de opdrachtgever aangeboden.
Methode ontwikkeling
Evidence based
Werkwijze
EBRO-methode voor wetenschappelijke onderbouwing
Deze multidisciplinaire richtlijn is ontwikkeld volgens de methodiek van evidence-based richtlijnontwikkeling (EBRO). Hierbij werd de GRADE-methodiek toegepast. Er zijn ook hoofdstukken overgenomen vanuit de vorige versie van de MDR Depressie (2013). Hierin zijn conclusies gebaseerd op de ‘levels of evidence’.
Levels of evidence
Bij ‘levels of evidence’ krijgt een individuele publicatie een mate van bewijskracht toegekend. Vervolgens wordt er naar alle bewijskracht over een onderwerp gekeken en kort samengevat in een conclusie, met daarbij een niveau van bewijs. Zie hieronder voor de indeling van bewijskracht en de verschillende conclusieniveaus.
Indeling van de literatuur naar de mate van bewijskracht
|
Voor artikelen betreffende preventie of therapie |
|
|
A1 |
systematische reviews die tenminste enkele onderzoeken van A2-niveau betreffen, waarbij de resultaten van afzonderlijke onderzoeken consistent zijn |
|
A2 |
gerandomiseerd vergelijkend klinisch onderzoek van goede kwaliteit (gerandomiseerde, dubbelblind gecontroleerde trials) van voldoende omvang en consistentie |
|
B |
gerandomiseerde klinische trials van matige kwaliteit of onvoldoende omvang of ander vergelijkend onderzoek (niet-gerandomiseerd, vergelijkend cohortonderzoek, patiënt-controle-onderzoek) |
|
C |
niet-vergelijkend onderzoek |
|
D |
mening van deskundigen, bijvoorbeeld de werkgroepleden |
|
Voor artikelen betreffende diagnostiek |
|
|
A1 |
onderzoek naar de effecten van diagnostiek op klinische uitkomsten bij een prospectief gevolgde goed gedefinieerde patiëntengroep met een tevoren gedefinieerd beleid op grond van de te onderzoeken testuitslagen, of besliskundig onderzoek naar de effecten van diagnostiek op klinische uitkomsten, waarbij resultaten van onderzoek van A2-niveau als basis worden gebruikt en voldoende rekening wordt gehouden met onderlinge afhankelijkheid van diagnostische tests |
|
A2 |
onderzoek ten opzichte van een referentietest, waarbij van tevoren criteria zijn gedefinieerd voor de te onderzoeken test en voor een referentietest, met een goede beschrijving van de test en de onderzochte klinische populatie; het moet een voldoende grote serie van opeenvolgende patiënten betreffen, er moet gebruikgemaakt zijn van tevoren gedefinieerde afkapwaarden en de resultaten van de test en de 'gouden standaard' moeten onafhankelijk zijn beoordeeld. Bij situaties waarbij multipele, diagnostische tests een rol spelen, is er in principe een onderlinge afhankelijkheid en dient de analyse hierop te zijn aangepast, bijvoorbeeld met logistische regressie |
|
B |
vergelijking met een referentietest, beschrijving van de onderzochte test en populatie, maar niet de kenmerken die verder onder niveau A staan genoemd |
|
C |
niet-vergelijkend onderzoek |
|
D |
mening van deskundigen, bijvoorbeeld de werkgroepleden |
|
Niveau van de conclusies |
|
|
1 |
gebaseerd op minimaal 1 systematische review (A1) of tenminste 2 onafhankelijk van elkaar uitgevoerde onderzoeken van niveau A1 of A2 |
|
2 |
gebaseerd op tenminste 2 onafhankelijk van elkaar uitgevoerde onderzoeken van niveau B |
|
3 |
gebaseerd op 1 onderzoek van niveau A2 of B of onderzoek(en) van niveau C |
|
4 |
gepubliceerde mening van deskundigen of mening van de werkgroepleden |
GRADE-methodiek
Sinds de introductie van de GRADE-methodiek in 2004 werd dit wereldwijd al snel de methode van voorkeur om wetenschappelijk bewijs te graderen ten behoeve van richtlijnontwikkeling (Guyatt et al., 2008), inclusief deze richtlijn. De GRADE-methodiek gaat er van uit dat de zekerheid van het wetenschappelijk bewijs uit randomized controlled trials (RCT’s) in beginsel hoog is vanwege de, mits goed uitgevoerd, kleine kans op vertekening (bias). In geval van observationele (niet gerandomiseerde) studies is de uitgangspositie van de zekerheid van bewijs laag. De zekerheid van het bewijs per uitkomstmaat wordt, behalve door de methodologische kwaliteit van de individuele onderzoeken, ook bepaald door andere factoren, zoals de mate van consistentie van de gevonden resultaten uit de verschillende onderzoeken en de precisie van de gevonden uitkomst (zie tabel 1.1). Bij observationeel onderzoek kan het bewijs in bepaalde gevallen omhoog worden gegradeerd.
Tabel 1.1 GRADE: Factoren voor downgraden en upgraden 1
|
|
We downgraden de zekerheid van bewijs van studies met een hoge uitgangspositie (RCT’s), bij: |
|
We upgraden de zekerheid van bewijs van observationele studies bij: |
|
|
||
|
|
||
|
|
||
|
|
||
|
|
||
1. De zekerheid van het bewijs (zeer laag, laag, matig en hoog) verwijst naar de mate van vertrouwen dat men heeft in de schatting van het effect van een behandeling.
Bij de beoordeling van het wetenschappelijke bewijs ten aanzien van bovenstaande factoren werd uitgegaan van ‘Grade guidelines’, zoals ook te raadplegen in het ‘Grade handbook’ (Guyatt et al., 2013; Handbook for grading the quality of evidence and the strength of recommendations using the GRADE approach).
Legenda GRADE
Na vaststelling van het niveau van bewijs wordt dit in de bijbehorende conclusies als volgt verwoord:
|
Zekerheid |
Symbolen |
|
Signaalwoorden |
|
Hoog |
⊕⊕⊕⊕ |
“Het is aangetoond dat…” |
geeft, heeft (een effect), resulteert in |
|
Redelijk |
⊕⊕⊕◯ |
“Het is aannemelijk...” |
waarschijnlijk |
|
Laag |
⊕⊕◯◯ |
“Er zijn aanwijzingen…” |
zou kunnen, lijkt, suggereert |
|
Zeer laag |
⊕◯◯◯ |
“Het is onzeker, maar er zijn aanwijzingen dat…” |
onzeker |
Van bewijs naar aanbevelingen: Overwegingen
Naast het wetenschappelijk bewijs bepalen enkele andere factoren mede of een instrument of behandeling wordt aanbevolen. In de teksten van de vorige richtlijn-versies werd dit onder “Overige Overwegingen” beschreven.
Mee te wegen factoren om te bepalen of een instrument of behandeling wordt aanbevolen:
|
1. Kwaliteit van bewijs Hoe hoger de algehele kwaliteit van het bewijs, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. |
|
2. Balans tussen gewenste en ongewenste effecten Hoe groter het verschil is tussen de gewenste en ongewenste effecten, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. Hoe kleiner dit verschil of hoe meer onzekerheid over de grootte van het verschil, des te waarschijnlijker wordt het formuleren van een conditionele aanbeveling. Toelichting:
|
|
3. Patiëntenperspectief Hoe groter de uniformiteit in waarden en voorkeuren van patiënten bij het afwegen van de voor- en nadelen van een interventie, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. |
|
4. Professioneel perspectief Hoe groter de uniformiteit in waarden en voorkeuren van professionals ten aanzien van de toepasbaarheid van een interventie, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. Toelichting:
|
|
5. Middelenbeslag Hoe minder middelen er worden gebruikt (m.a.w. hoe lager de kosten van een interventie zijn vergeleken met de beschouwde alternatieven en andere kosten gerelateerd aan de interventie), des te waarschijnlijker wordt het formuleren van een sterke aanbeveling. Hoe meer onzekerheid over het middelenbeslag, des te waarschijnlijker wordt een conditionele aanbeveling. |
|
6. Organisatie van zorg Hoe meer onzekerheid of de geëvalueerde interventie daadwerkelijk op landelijke schaal toepasbaar is, des te waarschijnlijker wordt het formuleren van een conditionele aanbeveling. Toelichting:
|
Formulering van aanbevelingen
Afhankelijk van deze factoren kun je een instrument of behandeling wel of niet aanbevelen. We maken daarbij onderscheid tussen zwakke en sterke aanbevelingen. In het geval van een sterke aanbeveling zou je behandeling X voor alle patiënten met Y willen aanbevelen. Bij een zwakke aanbeveling is dit bijvoorbeeld afhankelijk van de voorkeuren van de patiënt in kwestie. Het is belangrijk in deze sectie expliciet te vermelden op grond waarvan een behandeling wel of niet wordt aanbevolen en ook waarom die aanbeveling zwak of sterk zou moeten zijn.
Voor de formulering van ‘sterke’ (onvoorwaardelijke) en ‘zwakke’ (voorwaardelijke) aanbevelingen is de volgende indeling aangehouden (zie tabel 1.2):
Tabel 1.2 GRADE Voorkeursformulering sterke / zwakke aanbevelingen
|
Gradering aanbeveling |
Betekenis |
Voorkeursformulering* |
|
STERK VOOR |
De voordelen zijn groter dan de nadelen voor bijna alle patiënten. Alle of nagenoeg alle geïnformeerde patiënten zullen waarschijnlijk deze optie kiezen. |
We bevelen [interventie] aan. |
|
ZWAK VOOR |
De voordelen zijn groter dan de nadelen voor een meerderheid van de patiënten, maar niet voor iedereen. De meerderheid van geïnformeerde patiënten zal waarschijnlijk deze optie kiezen. |
Overweeg [interventie], bespreek de voor- en nadelen). |
|
ZWAK TEGEN |
De nadelen zijn groter dan de voordelen voor een meerderheid van de patiënten, maar niet voor iedereen. De meerderheid van geïnformeerde patiënten zal waarschijnlijk deze optie kiezen. |
Wees terughoudend met [interventie], bespreek de voor- en nadelen). |
|
STERK TEGEN |
De nadelen zijn groter dan de voordelen voor bijna alle patiënten. Alle of nagenoeg alle geïnformeerde patiënten zullen waarschijnlijk deze optie kiezen. |
We bevelen [interventie] niet aan. |
* Het gaat hier om voorkeursaanbevelingen, deze kunnen in een enkele geval afwijken. Voor bepaalde hoofdstukken is GRADE niet toegepast (bijv. Organisatie van zorg) daar zijn uit praktisch oogpunt ook de aanbevelingen niet volgens GRADE.
Leeswijzer
Klachten of symptomen die horen bij een depressieve stoornis (depressie) noemen we ‘depressieklachten’ of ‘depressiesymptomen’. Met ‘depressieve klachten’ bedoelen we stemmingsklachten waar iemand hinder van ondervindt, waarbij niet wordt voldaan aan de DSM-criteria voor een depressieve stoornis (depressie).
Als we spreken van een depressieve stoornis of depressie wordt een unipolaire depressieve stoornis bedoeld, al dan niet chronisch, en inclusief de persisterende depressieve stoornis. Behalve van ‘(psychische/depressieve) stoornis’ spreken we in deze richtlijn, rechtdoende aan het patiëntenperspectief, bij voorkeur van ‘aandoening’.
Met kinderen en adolescenten bedoelen we kinderen van 8 tot 12 jaar en adolescenten van 12 tot 18 jaar. Met jongvolwassenen bedoelen we volwassenen van 18 tot 25 jaar. Met volwassenen bedoelen we mensen van 25 tot 60 jaar. Met ouderen bedoelen we oudere volwassenen van 60 jaar en ouder.
Metapsy
Tijdens de ontwikkeling van deze richtlijn is gebruik gemaakt van metapsy.org. Metapsy is een onderzoeksinitiatief van de Vrije Universiteit Amsterdam, onder leiding van professor Pim Cuijpers. Het hoofddoel van Metapsy is het verschaffen van toegang tot een meta-analytische database van klinische studies die de effecten van psychologische interventies, zoals psychotherapie, preventieve interventies en psychoeducatie, op diverse psychische aandoeningen en geestelijke gezondheidsproblemen onderzoeken.
Metapsy bevat twee R-pakketten waarmee met behulp van klinische variabelen van interesse (PICO) een meta-analyse kan worden uitgevoerd en waarbij alle relevante informatie om tot een GRADE conclusie te komen over de effecten van psychotherapie op depressieve symptomen wordt gepresenteerd in een (pdf) rapport of online zijn te bekijken.