Organisatie van zorg bij HAZ
Uitgangsvraag
Wat is de beste zorg voor vrouwen met een hypertensieve aandoening tijdens de zwangerschap (HAZ) om hart- en vaatziekten op latere leeftijd te voorkomen?
Deze uitgangsvraag bevat de volgende deelvragen:
- Hoe dient het follow-up schema er uit te zien (leeftijd, frequentie)?
- Op welke wijze kan de zorg efficiënt worden ingericht?
- Wat is de plaats van cardiovasculair risicomanagement binnen de keten/netwerkzorg?
- Wat kunnen patiënten zelf doen om zo gezond mogelijk ouder te worden?
Aanbeveling
Informeer een vrouw die een hypertensieve aandoening in de zwangerschap heeft doorgemaakt dat:
- Er een verhoogd risico is op het ontwikkelen van chronische hypertensie;
- er een verhoogd risico is op het ontwikkelen van andere cardiovasculaire risicofactoren zoals diabetes en hypercholesterolemie;
- er een verhoogd risico is op het ontwikkelen van hart- en vaatziekten; en
- er een gezonde leefstijl nagestreefd moet worden om het risico op cardiovasculaire ziekten te verlagen (zie module leefstijladviezen).
Controleer de bloeddruk bij de nacontrole na elke bevalling.
Voer de eerste 5 jaar na een bevalling jaarlijks en daarna eens per 3 jaar een cardiovasculaire risicofactor screening uit naar de bloeddruk en overweeg laboratoriumonderzoek (cholesterol, HDLC, LDLC en triglyceriden, glucose, nierfunctie, microalbuminurie) te bepalen. Maak hierover lokale afspraken.
Als een vrouw die een hypertensieve ziekte in de zwangerschap heeft doorgemaakt nog antihypertensiva gebruikt bij de nacontrole na een bevalling, verwijs haar dan naar de huisarts voor behandeling van de bloeddruk.
Verwijs een vrouw die een hypertensieve aandoening in de zwangerschap heeft doorgemaakt naar een internist met kennis van vasculaire geneeskunde als er verdenking is op secundaire hypertensie of bij comorbiditeit.
Behandeling en preventie verloopt volgens regulier CVRM-traject, hiervoor wordt verwezen naar de CVRM-richtlijn.
Overwegingen
Vrouwen die een HAZ hebben doorgemaakt hebben de eerste jaren na hun zwangerschap een relatief verhoogd risico op HVZ maar een laag 10-jaars risico op HVZ. Echter, het lifetime risico op HVZ en daarmee het potentieel behandelvoordeel is hoog. Vrouwen na een HAZ hebben een hoger cardiovasculair risico dan de algemene bevolking. Andere patiënten met een dergelijk risicoprofiel zijn jonge mensen met diabetes mellitus of familiare hypercholesterolemie. Voor deze groepen geldt dat vanwege het hogere risico de SCORE niet kan worden gebruikt.
Er zijn geen aanwijzingen dat de voor- en nadelen van interventies anders zouden uitvallen voor bepaalde subgroepen van HAZ. Wel blijkt dit risico afhankelijk te zijn van de ernst van de aandoening. Zo is het risico voor vrouwen na ernstige/vroege pre-eclampsie het hoogst. Voorts hebben deze vrouwen ook vaker vermoeidheids- en cognitieve klachten zoals concentratieproblemen en geheugenstoornissen die vaak langdurig aanhouden. Derhalve is de verwachting dat de meeste winst van nazorg in deze groep te verwachten is.
Er zijn verschillende onderzoeken gedaan naar de voorkeuren van patiënten ten aanzien van nazorg na HAZ. Een Nederlands Focusgroep onderzoek met als doel om na te gaan wat de wensen en de meningen waren van vrouwen en behandelaars over nazorg na pre-eclampsie/HELLP toonde aan dat vrouwen een duidelijke wens hadden op nazorg na de 6 weken controle bij de gynaecoloog. (Dijkhuis, 2020) Deze nazorg zou aandacht moeten geven aan de emotionele en fysieke korte-en lange termijn consequenties van pre-eclampsie. Vrouwen gaven aan dat zij graag regelmatig bloeddrukcontrole en bloedtesten zouden willen krijgen vanwege het verhoogde cardiovasculaire risico. Veel vrouwen gaven aan dat leefstijl coaches meerwaarde zouden hebben voor het starten of continueren van een gezonde leefstijl. De meeste vrouwen gaven aan dat 3 tot 12 maanden postpartum een goed moment voor follow-up te vinden. Er was geen duidelijke voorkeur voor het interval tussen vervolgafspraken voor follow-up. Vrouwen gaven geen duidelijke voorkeur aan wie de follow-up zou moeten uitvoeren.
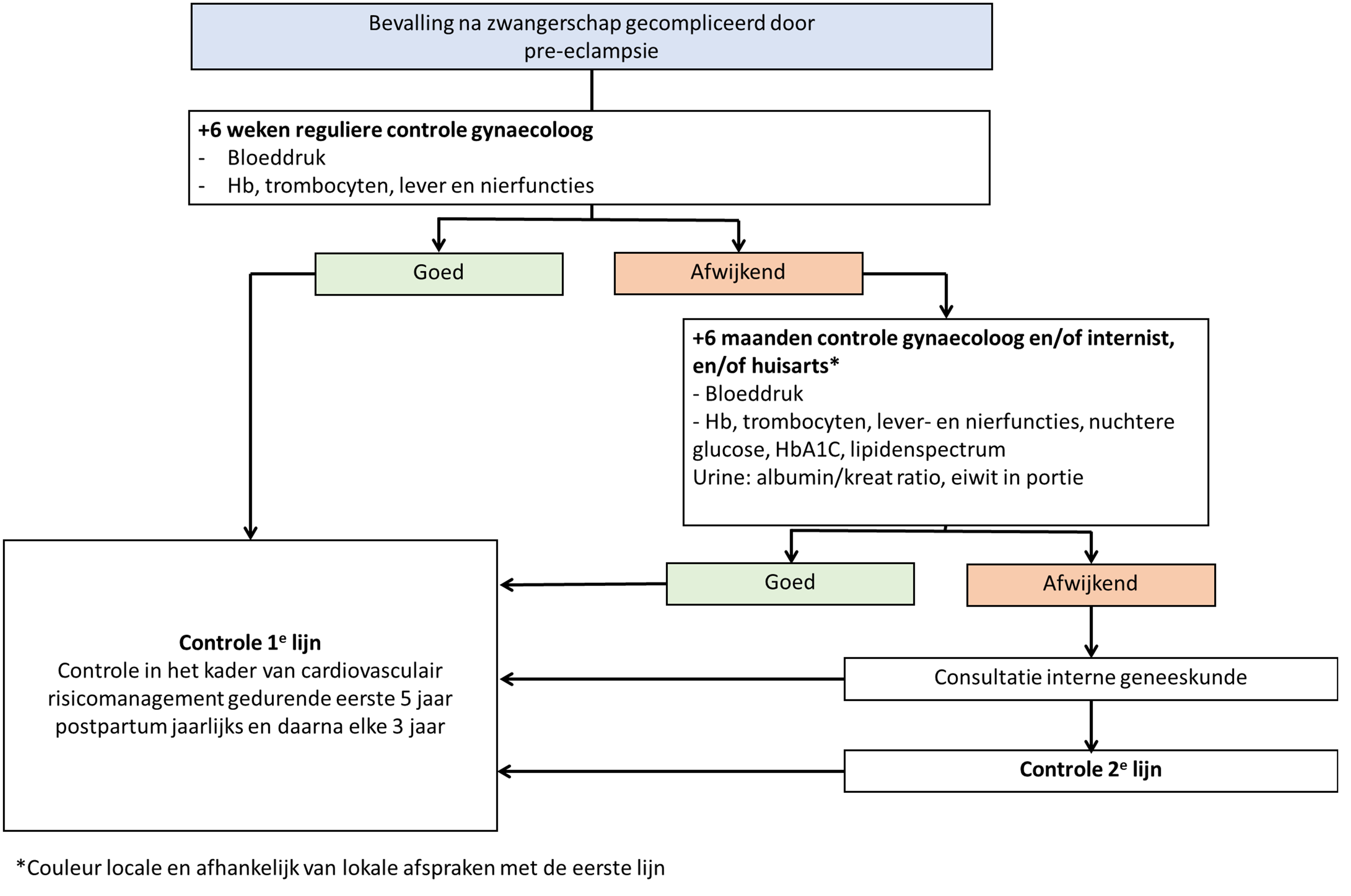
Binnen 6 weken na de bevalling worden patiënten over het algemeen teruggezien op de polikliniek gynaecologie voor hun nacontrole. Tijdens dit bezoek zal standaard anamnese, bloeddruk en aanvullend onderzoek verricht worden. Afhankelijk van de bevindingen tijdens dit consult zal besloten worden om patiënten over te dragen aan de 1e lijn voor behandeling in het kader van CVRM. Indien nodig worden bevindingen besproken met een internist-vasculair geneeskundige (bijvoorbeeld in een multidisciplinair overleg of een eenmalig poliklinisch consult). Twee mogelijkheden dienen zich dan voor: 1) overdragen aan 1e lijn met adviezen ten aanzien van cardiovasculair risicomanagement, of 2) behandeling in de 2e lijn.
Uitgangspunten voor de behandeling in de tweede lijn
- Aanvullende onderzoeken om cardiovasculair risico in kaart te brengen. Zo nodig aanvullende diagnostiek.
- Optimalisatie van de behandeling. Onder andere door aanpassing van de medicamenteuze en niet medicamenteuze therapie.
Uitgangspunten voor terugverwijzen naar en follow-up in de eerste lijn:
- De gynaecoloog of internist-vasculair geneeskundige verwijst terug naar de huisarts als:
- Risicofactoren adequaat behandeld zijn (of geen beter resultaat bereikt kan worden).
- Een stabiele situatie is bereikt.
Informatieoverdracht bij verwijzing van de tweede naar de eerste lijn
- De huisarts ontvangt binnen 4 weken na het laatste polibezoek een brief met de diagnose, alle diagnostische bevindingen en therapeutische interventies.
Controle in de eerste lijn:
- In het kader van CVRM gedurende vijf jaar postpartum ieder jaar en daarna één keer per drie jaar, tenzij er risicofactoren voor HVZ aanwezig zijn. In dat geval wordt de frequentie hoger, afhankelijk van de problematiek en het beloop.
- Consultatie of terugverwijzing naar de internist vasculaire geneeskunde of cardioloog indien dit volgens de Multidisciplinaire richtlijn CVRM aan de orde is.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
We weten dat na ernstige/vroege pre-eclampsie/HELLP er een verhoogd risico is op HVZ en een minimaal viermaal verhoogd risico op premature hypertensie. (Behrens, 2017; Bellamy, 2007; en Brouwers, 2018) Ook zijn er fysiologische gevolgen na ernstigste/ vroege pre-eclampsie gevonden zoals vasculaire schade en geometrische aanpassingen van het hart. (Andrietti, 2008; Krabbedam, 2009; Spaanderman, 2006).
De impact van een dergelijk life-event is geheel vergelijkbaar met een hartinfarct op jonge leeftijd. Uiteraard kan men zich zorgen maken over nodeloos medicaliseren van deze groep patiënten. Echter, zoals hierboven besproken, stellen patiënten zelf de nazorg enorm op prijs.
Dat betekent praktisch:
- Bij obstetrisch ontslaggesprek duidelijke communicatie naar patiënt en de huisarts over expliciete doorverwijzing met verzoek bloeddrukcontroles.
- Secundaire preventie CVRM: controle jaarlijks bij huisarts/praktijkondersteuner.
- Leefstijlbegeleiding via praktijkondersteuner of via Gecombineerde Leefstijl Interventie (GLI) indien geïndiceerd.
- Enkele centra hebben een gestructureerd nazorgprogramma, geef daarover duidelijke informatie bij ontslag als patiënten daarvoor in aanmerking komen.
- Adviseer de patiënt om met een eigen bloeddrukmeter eens per kwartaal de bloeddruk te meten en dit te bespreken tijdens het jaarlijkse bezoek bij huisarts/praktijkondersteuner.
Patiënten met persisterende klachten zoals vermoeidheid, cognitieve en/of psychologische klachten en/of atypische lichamelijke klachten: extra consult bij huisarts, die beoordeelt evt. doorverwijzing naar 2e lijn of psycholoog.
Kosten (middelenbeslag)
Er zijn verschillende kosteneffectiviteitsanalyses gedaan naar het effect van actieve screening op hypertensie en metabool syndroom bij vrouwen na HAZ. Onderzoek liet zien dat jaarlijks screenen op bloeddruk en vroegtijdige behandeling op hypertensie kosten kan besparen met gelijkblijvende kwaliteit van leven. (Drost, 2015) Een ander onderzoek toonde aan dat screening op hypertensie en metabool syndroom een verbetering in levensverwachting liet zien bij gelijkblijvende QALY. (van Baaren, 2014)
Aanvaardbaarheid, haalbaarheid en implementatie
Nazorg zou aan alle vrouwen moeten worden aangeboden. Juist vrouwen met veel gezondheidsachterstand hebben de meeste baat bij follow-up gericht op cardiovasculaire preventie inclusief leefstijl. Daarom is een proactieve benadering vanuit de praktijk gewenst. Een belemmerende factor is dat zorgverleners geschoold moeten worden in het geven van nazorg aan vrouwen na HAZ. Hierover is nog te weinig kennis bij een groot deel van de zorgverleners. Deze zorg is in principe standaard verzekerde zorg en niet kostbaar. Echter, deze vrouwen vallen in de meeste gevallen niet in de doelgroep die al wordt opgeroepen voor CVRM-controles in de huisartspraktijk en het kader van de programmatische ketenzorg. Deze zorg is in principe standaard verzekerde zorg en niet kostbaar, maar de selectie van de vrouwen en het pro-actief benaderen wordt momenteel niet vergoed buiten de ketenzorg om. De wens tot nazorg is afkomstig van de patiënt zelf dus op basis hiervan zou de acceptatie van de patiënt hoog worden ingeschat. Hooguit zal een groep vrouwen vanwege financiële problemen de onderdelen die onder het verplichte eigen risico vallen afwijzen, zoals het eventuele laboratoriumonderzoek.
Voor het succesvol implementeren van nazorg na HAZ is een implementatie plan opgesteld.
Onderbouwing
Achtergrond
De laatste decennia is steeds duidelijker geworden dat HAZ complicaties geven op langere termijn. Na een HAZ hebben vrouwen een verhoogd risico om op jongere leeftijd klassieke cardiovasculaire risicofactoren te ontwikkelen in vergelijking met vrouwen met een normotensieve zwangerschap (zie module follow-up na HAZ).
Atherosclerose is een chronische aandoening die zich ontwikkeld door langdurige blootstelling aan risicofactoren voordat het zich manifesteert als HVZ. Vrouwen die een HAZ hebben doorgemaakt hebben meer subklinische atherosclerose in vergelijking met vrouwen die een normotensieve zwangerschap hadden. (Nilsson, 2020; Zoet, 2018)
Ondanks de uitgebreide literatuur die aantoont dat vrouwen na een HAZ een verhoogd risico hebben op het vroegtijdig ontwikkelen van cardiovasculaire risicofactoren en HVZ, wordt structurele cardiovasculaire risicomanagement niet aangeboden. In veel keten-informatiesystemen van de huisarts kunnen deze vrouwen niet in het oproepsysteem worden meegenomen als zij niet opgenomen zijn in de keten CVRM. En opnemen in de keten CVRM kan pas nadat er een medicamenteuze behandeling plaats vindt, de bloeddruk of het cholesterol sterk verhoogd is of na een hart- en vaatziekte.
De huidige Nederlandse multidisciplinaire richtlijn ‘Cardiovasculaire risicomanagement’ is gebaseerd op de ESC-richtlijn. De hoeksteen van deze richtlijn is dat het 10-jaars risico op cardiovasculaire sterfte (of ziekte en sterfte), volgens de SCORE tabel, leidend is voor interventies. Dit risico is per definitie laag bij vrouwen jonger dan 50 jaar, en kan pas worden gebruikt vanaf 40 jaar, waarbij tevens geadviseerd wordt een schatting van het risico op hart- en vaatziekten pas te overwegen bij postmenopausale vrouwen of vrouwen ≥ 50 jaar. (richtlijn Cardiovasculair risicomanagement (CVRM), 2019) In de huidige richtlijn wordt aanbevolen om “periodieke screening op hypertensie en diabetes te overwegen bij vrouwen met in de voorgeschiedenis (pre)-eclampsie en/of zwangerschapshypertensie”. Dit is een niet erg concrete en vrijblijvende aanbeveling. Bovendien zal dit zelden leiden tot meer intensievere behandeling van risicofactoren dan leefstijl omdat de drempel voor medicamenteuze behandeling gebaseerd is op het hiervoor genoemde SCORE risico. De aanbeveling voor medicamenteuze behandeling van hypertensie voor patiënten met een laag tot gematigd hoog risico op HVZ luidt dat “behandeling worden overwogen indien de bloeddruk boven de streefwaarde is.” De overwegingen luiden: Beginnen met bloeddrukverlagende medicatie kan ook worden overwogen voor patiënten met hypertensie en een laag tot gematigd risico (ESH/ESC, 2013). De NNT voor deze patiëntcategorie is echter heel hoog; patiënten moeten worden geïnformeerd en hun voorkeur moet worden meegewogen.
In de nieuwste ESC/ESH hypertensie richtlijn (ESC richtlijn, 2021) wordt aanbevolen om personen met een laag 10-jaars risico op HVZ met graad 1 hypertensie en een laag en gemiddeld SCORE risico naast leefstijl advies wel medicamenteus te behandelen. (Williams, 2018) Dit advies is gebaseerd op verschillende meta-analyses en een subgroep analyse van de HOPE-3 studie die allen een reductie lieten zien in cardiovasculaire uitkomsten bij personen met een laag/gemiddeld risico op hart- en vaatziekten en graad 1 hypertensie.
Conclusies / Summary of Findings
|
- GRADE |
Not applicable.
|
Zoeken en selecteren
Questions regarding the organization of health issues could not be answered by using systematic literature search as international standards do not reflect the Dutch health standards. Therefore, this question is answered by information following national consensus meetings.
Evidence tabellen
Not applicable.
Verantwoording
Beoordelingsdatum en geldigheid
Laatst beoordeeld : 02-03-2023
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2019 een werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor vrouwen na HAZ.
Werkgroep
- Dr. J.J. (Hans) Duvekot, gynaecoloog-perinatoloog, werkzaam in het Erasmus MC, Nederlandse Vereniging voor Obstetrie en Gynaecologie (voorzitter)
- Prof dr. A.H.E.M. (Angela) Maas, cardioloog, werkzaam in het Radboudumc, Nederlandse Vereniging voor Cardiologie
- Dr. J.E. (Jeanine) Roeters van Lennep, internist vasculaire geneeskunde, werkzaam in het Erasmus MC, Nederlandse Internisten Vereniging
- Prof. dr. M.E.A. (Marc) Spaanderman, gynaecoloog-perinatoloog, werkzaam in het Maastricht UMC, Nederlandse Vereniging voor Obstetrie en Gynaecologie
- Dr. H.M.M. (Hedwig) Vos, huisarts, werkzaam in het LUMC en werkzaam bij V&V Huisartsen, Nederlands Huisartsengenootschap
- Prof. dr. B.K. (Birgitta) Velthuis, radioloog, werkzaam in het UMC Utrecht, Nederlandse Vereniging voor Radiologie
- Mw. K.L.H.E. (Kim) Vanden Auweele, beleidsmedewerker, werkzaam voor de Hellp Stichting
Ondersteuning
• Dr. W.J. (Wouter) Harmsen, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
• Dr. J.H. (Hanneke) van der Lee, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenwerkzaamheden |
Gemelde belangen |
Actie |
|
Duvekot |
Gynaecoloog, Erasmus MC |
Directeur 'Medisch Advies en Expertise Bureau Duvekot', Ridderkerk, ZZP'er |
ZonMw-studie 'Personalised lifestyle na pre eclampsie' |
Geen |
|
Roeters van Lennep |
Internist Vasculaire geneeskunde, Erasmus MC |
* Voorzitter NVIVG (Nederlandse Vereniging Internisten Vasculaire geneeskunde - onbetaald) * Bestuurslid NVGG (Nederlandse Vereniging voor Gender en Geneeskunde - onbetaald) * Raad van Toezicht Healthlife Klinieken - onbetaald * Redactie Focus Vasculair - onbetaald |
ZonMw-studie 'Personalised lifestyle na pre eclampsie' |
Geen |
|
Auweele, Vanden |
Hellp Stichting - Beleidsmedewerker
|
Geen |
Geen |
Geen |
|
Maas |
Hoogleraar cardiologie voor vrouwen, Radboudumc, Nijmegen |
Thema CVRM bij reproductieve aandoeningen behoort tot mijn expertisegebied. |
Twee promovendi mede betaald vanuit Radboudumc onderzoeks-fonds Hartvoorvrouwen |
Geen |
|
Spaanderman |
Hoogleraar verloskunde MUMC+ (100%) Opleider |
* Voorzitter Verloskundig Consortium Limburg: onbetaald * Voorzitter Acute verloskunde NAZL: onbetaald |
Geen. Vanzelfsprekend wel onderzoekers/ promovendi op dit interesse-gebied |
Geen |
|
Velthuis |
Geen |
Bestuurslid NVF (Nederlands Vasculair Forum) en ESCR (European Society of Cardiovascular Radiology) |
Geen |
|
|
Vos |
Huisarts, hoofd huisartsopleiding LUMC |
Lid Verenigingsraad Nederlands Huisartsengenootschap |
ZonMW-studie ‘Hart voor vrouwen in Den Haag’ |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door uitnodigen van patiëntvertegenwoordigers van verschillende patiëntverenigingen voor de schriftelijke Invitational conference en afvaardiging van Stichting Hellp in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen (zie per module ook ‘Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)’. De conceptrichtlijn wordt tevens ter commentaar voorgelegd aan de betrokken patiëntenverenigingen.
Methode ontwikkeling
Evidence based
Implementatie
Implementatieplan
|
Aanbeveling |
Tijdspad voor implementatie: 1-3 jaar of >3 jaar |
Verwacht effect op kosten |
Randvoorwaarden voor implementatie (binnen aangegeven tijdspad) |
Mogelijke barrières voor implementatie1 |
Te ondernemen acties voor implementatie2 |
Verantwoordelijken voor acties3 |
Overige opmerkingen |
|
Module 1 |
<3 jaar |
onbekend |
Uitbreiding pragmatische ketenzorgprogramma’s |
Organisatie niet ondersteund in huidige ketenzorgprogamma’s |
Afspraken maken over uitbreding ketenzorgpgrogramma’s |
Autoriserende partijen |
- |
|
Module 2 |
< 3 jaar |
onbekend |
Uitbreiding pragmatische ketenzorgprogramma’s
|
Mensen zonder behandelde of ernstige hypertensie of hypercholesterolemie niet in de programmatische ketenzorgprogramma’s kunnen worden opgenomen en daarmee dus niet via de standaard manier regelmatig worden opgeroepen door de praktijkondersteuner |
Afspraken maken over mogelijkheid om dit in huisartsenpraktijk bij te houden |
Autoriserende partijen |
- |
|
Module 2 |
< 3 jaar |
onbekend |
Verspreiden van kennis op het gebied van CVRM en HZZ
|
Vrouwen met lage gezondheidsvaardigheden, lage sociaaleconomische status en vaak een ongezonde leefstijl, komen op eigen initiatief mogelijk minder vaak naar de praktijk voor CVRM |
Verspreiden van kennis inzake CVRM na HZZ |
Autoriserende partijen |
- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 Barriëres kunnen zich bevinden op het niveau van de professional, op het niveau van de organisatie (het ziekenhuis) of op het niveau van het systeem (buiten het ziekenhuis). Denk bijvoorbeeld aan onenigheid in het land met betrekking tot de aanbeveling, onvoldoende motivatie of kennis bij de specialist, onvoldoende faciliteiten of personeel, nodige concentratie van zorg, kosten, slechte samenwerking tussen disciplines, nodige taakherschikking, etc.
2 Denk aan acties die noodzakelijk zijn voor implementatie, maar ook acties die mogelijk zijn om de implementatie te bevorderen. Denk bijvoorbeeld aan controleren aanbeveling tijdens kwaliteitsvisitatie, publicatie van de richtlijn, ontwikkelen van implementatietools, informeren van ziekenhuisbestuurders, regelen van goede vergoeding voor een bepaald type behandeling, maken van samenwerkingsafspraken.
- 3 Wie de verantwoordelijkheden draagt voor implementatie van de aanbevelingen, zal tevens afhankelijk zijn van het niveau waarop zich barrières bevinden. Barrières op het niveau van de professional zullen vaak opgelost moeten worden door de beroepsvereniging. Barrières op het niveau van de organisatie zullen vaak onder verantwoordelijkheid van de ziekenhuisbestuurders vallen. Bij het oplossen van barrières op het niveau van het systeem zijn ook andere partijen, zoals de NZA en zorgverzekeraars, van belang.
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerden de werkgroep de knelpunten rondom de zorg voor vrouwen met een hypertensieve aandoening tijdens de zwangerschap. Tevens zijn er knelpunten aangedragen door patiëntenverenigingen tijdens de Invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur en de beoordeling van de risk-of-bias van de individuele studies is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
Definitie |
|
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE-methodiek.
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule wordt aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit.
http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, Glasziou P, Jaeschke R, Vist GE, Williams JW Jr, Kunz R, Craig J, Montori VM, Bossuyt P, Guyatt GH; GRADE Working Group. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008 May 17;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008 May 24;336(7654). doi: 10.1136/bmj.a139.
Schünemann, A Holger J (corrected to Schünemann, Holger J). PubMed PMID: 18483053; PubMed Central PMCID: PMC2386626.
Wessels M, Hielkema L, van der Weijden T. How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. J Med Libr Assoc. 2016 Oct;104(4):320-324. PubMed PMID: 27822157; PubMed Central PMCID: PMC5079497.
Zoekverantwoording
Zoekacties zijn opvraagbaar. Neem hiervoor contact op met de Richtlijnendatabase.
