Fysiotherapie in de eerste lijn
Uitgangsvraag
Is fysiotherapie in de 1e lijn van meerwaarde (m.b.t. klachten, kwaliteit van leven, inspanningsvermogen) bij patiënten met COPD (chronic obstructive pulmonary disease)?
Is het mogelijk om aan te geven welke patientkarakteristieken voorspellend zijn voor een positief effect van deze behandeling?
Aanbeveling
Overweeg bij patiënten met mild tot ernstig COPD een oefenprogramma binnen de 1e-lijns fysiotherapie bij:
een verhoogde symptoomlast (CCQ >1,8)
óf:
wanneer zij een mild/matige symptoomlast (CCQ 1-1,8) hebben en daarbij beperkingen in hun fysieke capaciteit ervaren.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
In het algemeen is het bewijs ten aanzien van de effecten van fysiotherapie op de fysieke capaciteit, de kwaliteit van leven en sterfte bij patiënten met COPD van zeer lage tot lage kwaliteit, waarbij de richting van het effect bij enkele uitkomsten meer in de richting wijst van een voordelig effect van fysiotherapie dan in de richting van een nadelig effect, bijvoorbeeld bij de 6-MWD.
Bij patiënten met COPD met ernstige luchtwegobstructie (waarbij de FEV1 lager is dan 35%) lijkt de literatuur een gunstig effect te laten zien op de 6-MWD. Een verbetering van de loopafstand bij de 6-MWD kan leiden tot een hogere inspanningscapaciteit en een vermindering van de ziektelast, zelfs als de mate van verbetering net onder de MCID ligt.
Dit geldt zowel voor de milde (gedefinieerd op basis van de dyspnoescore) als ernstige (gebaseerd op de mate van ernst van de luchtwegobstructie) COPD-patiëntengroep.
De lage bewijskracht van de literatuur is mede te wijten aan het feit dat de interventie niet dubbelblind uitgevoerd kan worden. Er is daarnaast een enorme diversiteit in de samenstelling van de interventie, de groepssamenstelling (heterogeniteit van de patientengroep), de follow-up duur en uitkomstmaten.
Interventies gericht op het adembewegingsapparaat, zoals bijvoorbeeld ademspierkrachttraining, ademhalingstechnieken, mucusklaring en ontspanningstechnieken vielen buiten de PICO van deze module. Deze interventies kunnen klachtenvermindering geven bij COPD patiënten bij mensen met een hoge symptoomlast bijvoorbeeld bij een dysfunctionele ademhaling, inadequate mucusklaring of dynamische hyperinflatie.
In 2014 werd een systematic review uitgevoerd ten aanzien van determinanten en effecten van fysieke activiteit bij patiënten met COPD (Gimeno-Santos, 2014). Deze SR viel eveneens buiten de onderzoeksvraag van deze module maar toonde aan dat patiënten met COPD die fysiek actiever zijn een verlaagde kans op longaanvallen en een verlaagd risico op overlijden hebben. Er kon geen uitspraak gedaan worden over het effect van interventies gericht op het verhogen van de fysieke activiteit.
In 2015 hebben Mc Carthy e.a. een Cochrane review gedaan. Deze Cochrane kwam niet uit de literatuursearch vanwege de diversiteit van de toegepaste behandelingen. De gehanteerde definitie in deze studie voor pulmonary rehabilitation was: een beweegprogramma van minimaal 4 weken met of zonder educatie en/of een psychologische interventie gedurende het programma. De conclusie van de studie toont een verbetering van kwaliteit van leven (CRQ, SGRQ) en verbetering bij de 6 minuut looptest. Er bestond geen duidelijk verschil in uitkomsten tussen klinische (complex) en poliklinische (minder complexe) programma’s. De auteurs concluderen dat pulmonary rehabilitation kortademigheid en vermoeidheid vermindert, emotioneel verbetering geeft, de gezondheidsgerelateerde kwaliteit van leven en de inspanningscapaciteit verbetert. Tevens is er een afname van het risico op heropname na recente opname in verband met COPD-longaanvallen en een sterke reductie in angst- en depressiesymptomen.
In de geselecteerde studies zijn weinig tot geen nadelige effecten van de interventie gerapporteerd. Dit kan erop wijzen dat fysiotherapie een (relatief) veilige interventie is, waarbij geringe voordelen al op kunnen wegen tegen mogelijke nadelige gevolgen.
In de internationale GOLD richtlijn (2023) wordt ook aandacht besteed aan de effecten van oefentherapie en longrevalidatie bij patiënten met COPD. Zoals in de inleiding vermeld maken zij geen onderscheid tussen 1e, 2e en 3e lijns fysiotherapie en longrevalidatie zoals in de Nederlandse situatie.
Longrevalidatie in het algemeen heeft een positief effect op dyspnoe, gezondheidsgerelateerde kwaliteit van leven, inspanningstolerantie en heropnames na longaanvallen. Ook verminderen gevoelens van angst en depressie.
Een belangrijk aandachtspunt is een assessment voor aanvang van het programma zodat een programma met specifieke persoonlijke- en behandeldoelen kan worden samengesteld.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Een verlaagde loopafstand bij de 6-minuten wandeltest is een teken van verminderd functioneel inspanningsvermogen Niet alleen deconditioneringsproblemen kunnen hieraan ten grondslag liggen; ook adaptatie- of copingproblematiek en daarmee samenhangende participatieproblematiek kunnen hierin meespelen. Verbetering van de fysieke capaciteit kan op diverse domeinen positieve effecten voor patiënt en de omgeving geven. Het is niet altijd duidelijk wat passend bewegen op kan leveren bij COPD-patiënten. Hierom is het bijzonder belangrijk om te werken met vooraf gezamenlijk vastgestelde persoonlijke behandeldoelen.
Combineren met bijvoorbeeld telerevalidatie zou een nieuwe ontwikkeling kunnen zijn. Best practice wat betreft telerevalidatie zijn tot op heden nog niet bekend. Patiënten zien een intensieve behandeling echter niet altijd zitten. Vooralsnog is het zo dat uit de literatuur blijkt (GOLD 2023) dat een optimale behandeling met effect optreedt bij 6-8 weken trainen (opgemerkt dat men hier doelt op verschillende vormen van longrevalidatie).
Indien er complexe onderliggende problematiek is of een hoge ziektelast , is 1e lijns fysiotherapie niet aangewezen maar multidisciplinaire aanpak nodig in 2e- of 3e-lijn. Bij enkelvoudige problematiek kan een fysiotherapeutische interventie gedaan worden in de 1e lijn met als doel verbetering van de inspanningstolerantie, toename van de fysieke activiteit en verlagen van de symptoomlast. Dit komt overeen met het stroomschema zoals dat in de KNGF-richtlijn COPD (2020) staat vermeld. Patiënten ervaren een beweegprogramma bij de fysio-of oefentherapeut als heel waardevol. Aandacht voor zelfmanagement binnen dit programma kan helpen om de positieve resultaten langer te behouden. Evenals actief stimuleren om na het programma te blijven bewegen.
Kosten (middelenbeslag)
Het is aannemelijk dat tijdig ingrijpen en toepassen van fysiotherapie bij patiënten met COPD kostenverlagend zal werken. Door het verbeteren van de inspanningstolerantie en verlagen van de symptoomlast voorkom je dat de patiënten participatieproblemen gaan ondervinden.
Hierdoor nemen zowel kosten door zorgconsumptie als economische kosten door uitval van werk af.
Aanvaardbaarheid, haalbaarheid en implementatie
De richtlijn van de KNGF (2020) geeft een duidelijk advies welke groepen in aanmerking komen voor fysiotherapie in de 1e lijn en welke onderzoeken vooraf gedaan dienen te worden. Via lokale netwerken en transmurale samenwerkingsafspraken probeert men de implementatie vorm te geven.
Het is niet bekend hoeveel patienten voor fysiotherapie in aanmerking zullen komen. Op dit moment volgt slechts 5% van de COPD patienten een beweeg- of longrevalidatieprogramma. Wel is het logisch om je te beperken tot de groep met een onvoldoende fysieke capaciteit en/of fysieke activiteit en/of problemen met het adembewegingsapparaat. Deze aangrijpingspunten gelden wanneer iemand milde tot veel klachten als gevolg van zijn COPD ervaart.
In de KNGF richtlijn wordt een stroomdiagram gevolgd op basis van ziektestabiliteit, ziektelast, fysieke capaciteit en fysieke activiteit waaruit al dan niet een indicatie voor fysiotherapie volgt, die verschillend kan zijn in duur en intensiteit (profiel 1 t/m 6). De mate van luchtstroombeperking (FEV1) wordt buiten beschouwing gelaten omdat deze onvoldoende correleert met de mate van fysieke beperking. Deze indeling zorgt ervoor dat de juiste zorg bij de juiste patiënt terecht komt, maar is anders dan de aanspraken in de basisverzekering.
Sinds 2019 wordt fysiotherapie voor patiënten met COPD Gold 2, 3 en 4 vergoed vanuit de basisverzekering. Een belemmering is echter de eventueel eigen bijdrage die sommige patiënten moeten betalen en het feit dat sommige COPD-patiënten (Gold 1, weinig obstructie maar mogelijk wel significant emfyseem en hoge ziektelast) geen vergoeding krijgen vanuit de basisverzekering maar wel een indicatie hebben voor fysiotherapie o.b.v. de profielindeling van de KNGF.
Aangezien een aanzienlijk deel van de patiënten met COPD uit lagere sociaaleconomische klassen afkomstig is en veelal beperkt of niet aanvullend verzekerd is, belemmert dit de toegang van de zorg.
Daarnaast ontbreekt het vaak aan gezondheidsvaardigheden en ziekte-inzicht juist bij deze groep waardoor motivatie kan ontbreken. Ook de duur en intensiteit van fysiotherapie kunnen een struikelblok vormen, evenals de afstand naar een praktijk die gespecialiseerd is in behandeling van patiënten met COPD of problemen met vervoer er naartoe. Daarom is het belangrijk om de drempel voor deze vorm van zorg laag te houden.
Het hybride toepassen van telerevalidatie kan gebruikt worden om de capaciteit van de beschikbare fysio- en oefentherapie therapie te vergroten, de kosten te verlagen en de drempel van het transport naar een praktijk voor patiënten te verlagen. Onderzoek naar de effectiviteit en veiligheid van telerevalidatie is nodig alvorens hier een aanbeveling over te doen.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Zowel in de internationale als nationale richtlijnen wordt zonder twijfel de aanbeveling gedaan om fysiotherapie voor te schrijven voor patiënten met mild tot ernstig COPD.
Ook volgens het recent herziene GOLD-document (revisie 2023) is er een sterk bewijs (level A) voor de voordelen van fysiotherapie en longrevalidatie bij gemiddeld en ernstig COPD. De voordelen komen tot uiting in verbetering van dyspnoescore, gezondheidsstatus en inspanningstolerantie.
De NHG- standaard (2021) adviseert om COPD-patiënten in de 1e lijn te verwijzen naar een fysiotherapie programma indien er sprake is van een hoge ziektelast (m.n. CCQ ≥ 2) of indien er sprake is van een milde/matige ziektelast (CCQ 1-2) met verminderde inspanningscapaciteit. De KNGF richtlijn (2020) hanteert een CCQ >1,8 als criterium om voor fysiotherapie in aanmerking te komen.
De werkgroep heeft besloten het afkappunt van 1,8 i.p.v. 2 voor de CCQ aan te houden om zoveel mogelijk uniformiteit te creeren.
Daarbij deelt de werkgroep de mening dat er naast een CCQ > 1 ook een beperking van de fysieke activiteit en/of capaciteit aanwezig dienen te zijn voor een overweging tot verwijzing voor 1e lijns beweegprogramma.
Het is lastig de literatuur te interpreteren en vergelijken. De interventies verschillen per studie evenals de duur van de follow-up. Ook zijn de patiëntengroepen erg heterogeen en verschillen de uitkomstmaten van de studies. Hanteren van de grade systematiek maakt hierdoor het level of evidence laag. Dit maakt vertalen naar aanbevelingen lastig. De expert opinion van de werkgroep, het recent vernieuwde GOLD-report (2023) en de KNGF Richtlijn (2020) onderbouwen mede de aanbeveling.
Onderbouwing
- Slechts 5 % van alle COPD-patiënten in Nederland volgt enige vorm van fysio- en oefentherapie of longrevalidatie. Momenteel worden zowel in de 1e lijn, als in de 2e en 3e lijn verschillende beweegprogramma’s en longrevalidatie aangeboden waarbij er een overlap lijkt te zijn in het aanbod. Er zijn verschillen in de bestaande richtlijnen rondom de criteria om deel te nemen en er ontbreekt voldoende onderbouwing. Zo hanteert de NHG een CCQ score ³ 2 en KNGF een CCQ score >1,8 als criterium om door te verwijzen naar fysio- of oefentherapie in de 1e lijn.
- In de 1e lijn wordt het aanbod vooral bepaald door beweeg – en oefenprogramma’s met het accent op het verbeteren van het fysieke functioneren, vaak aangevuld met educatie, over onder andere ziektespecifieke informatie, energieverdeling, en gebruik van hulpmiddelen in de nabije omgeving, voor de minder complexe COPD-patiënten.
- In de richtlijn wordt de Grade systematiek gehanteerd om het level of evidence bij een studie te beoordelen. Hierdoor worden de studies die fysio- of oefentherapie betreffen, altijd lager gewaardeerd omdat blindering niet mogelijk is en vanwege de heterogeniteit van de onderzoekspopulatie.
- Er bestaat een behoefte om meer patiënten van fysiotherapie in de 1e lijn gebruik te laten maken. Dit moet dan wel passend en effectief zijn gericht op het behalen van de persoonlijke behandeldoelen van een patiënt.
- In deze module (Module 2.1) richten we ons op de 1e lijns fysiotherapie voor COPD patiënten en in de volgende module (Module 2.2) zullen wij ditzelfde doen voor 2e en 3e lijns longrevalidatie voor de meer complexe COPD patienten.
- De GOLD richtlijn maakt geen onderscheid in 1e, 2e en 3e lijns therapie.
|
Low GRADE |
Physiotherapy may result in little to no difference in six-minute walking distance compared to usual care in patients with mild COPD.
Sources: Rugbjerg, 2015 |
|
Low GRADE |
Physiotherapy may increase six-minute walking distance compared to usual care in patients with very severe (FEV1 < 35%) COPD.
Sources: Paneroni, 2017 |
|
Very low GRADE |
The evidence is very uncertain about the effect of physiotherapy on improving muscle strength compared to usual care. Sources: Rugbjerg, 2015 |
|
Very low GRADE |
The evidence is very uncertain about the effect of physiotherapy on mortality compared to usual care. Sources: Rugbjerg, 2015 |
|
Very low GRADE |
The evidence is very uncertain about the effect of physiotherapy on improving health-related quality of life compared to usual care. Sources: Rugbjerg, 2015 |
Description of studies
The study of Paneroni (2017) was a systematic review that assessed the question whether exercise training was effective in changing functional capacity and health-related quality of life in patients with very severe but stable COPD.
A systematic search in MEDLINE, EMBASE, Cochrane Central Register of Controlled Trials, and the Cumulative Index to Nursing and Allied Health Literature until October 2015 to find randomised clinical trials (RCTs) that included patients with a clinical diagnosis of COPD and a FEV1 of 35% or less. It excluded studies with patients who had an acute exacerbation in the four weeks prior to the start of the study, or who had major comorbidities. Ten trials that investigated in-patient or outpatient or home- or community-based training programs were found. For this guideline, the literature summary was restricted to the 3 RCTs that focused on outpatient training programs (Singh, 2003; Borghi-Silva, 2009; Pleguezuelos, 2013), including a total of 199 patients with very severe COPD. The physiotherapy interventions were specified, and are summarised in the evidence table. Follow-up duration ranged from four to twelve weeks. All studies had a high risk of bias, as it is impossible to blind patients and caregivers to the allocation of the intervention, and the loss to follow-up was sizeable. The results were meta-analysed, and forest plots and pooled effects from random-effects analyses were reported.
The study of Rugbjerg (2015) was a systematic review that aimed to investigate the effects of physical rehabilitation in patients with mild COPD defined as a modified Medical Research Council dyspnea scale (mMRC) ≥1. In this study, a systematic search was performed in Medline, Embase, CINAHL, PsycINFO, G-I-N International, NICE, National Guideline Clearinghouse, Scottish Intercollegiate Guidelines, HTA (The Health Technology Assessment) Database, The Cochrane Library, SBU (Sweden), Socialstyrelsen (Sweden), Helsedirektoratet (Norway), Kunnskapssenteret (Norway), PEDro and OTseeker until November 20, 2013 to find randomised controlled trials that investigated adults with chronic obstructive pulmonary disease and mild symptoms according to dyspnoea scores, mMRC ≤1, were considered for inclusion. This review used HRQoL, adverse effects, and mortality as crucial outcomes, and 6-MWD, maximal exercise capacity, muscle strength, and dropout rates as important outcomes. The review excluded studies that were not RCTs, did not address the PICO, or were in another language than English, Danish, Swedish, and Norwegian. Four studies were included in this review, which included 498 patients with mild COPD (van Wetering, 2010; Gottlieb, 2011; Liu, 2012; Román, 2013). The physiotherapy interventions were specified, and are summarised in the evidence table. The minimal follow-up duration was 12 months, up to a maximum of 24 months. All studies had a high risk of bias, because due to the nature of the intervention blinding of patients and healthcare providers was impossible. Also, the number of dropouts was relatively large and imbalanced between intervention and control groups. The results were meta-analysed, and forest plots and pooled effects from random-effects analyses were reported.
Results
6-MWD
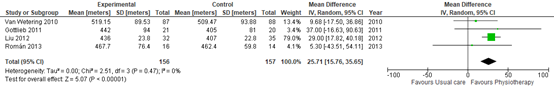
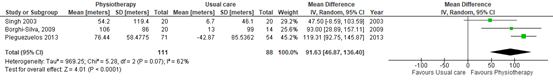
Both studies (Paneroni 2017 and Rugbjerg 2015) reported 6-MWD (Figure 1 and Figure 2). We repeated the meta-analysis of the study of Paneroni restricted to the studies that investigated community-based physiotherapy. For physiotherapy in patients with mild COPD, the effect on 6MWD was estimated to be 25.71 m (95% CI: 15.76 to 35.65) in favour of physiotherapy. In patients with severe COPD, the effect of physiotherapy was estimated to be 91.63 m (95% CI 46.87 to 136.40) in the advantage of physiotherapy.
Figure 1 – Forest plot of the meta-analysis of the effect of physiotherapy on 6-MWD in patients with mild COPD. (Rugbjerg 2015)
6MWD, six-minute walking distance; CI, confidence interval; COPD, chronic obstructive pulmonary disease; df, degrees of freedom; I2, heterogeneity; IV, inverse variance; SD, standard deviation
Figure 2 – Forest plot of the meta-analysis of the effect of physiotherapy on 6-MWD in patients with very severe COPD. (Paneroni 2017)
6MWD, six-minute walking distance; CI, confidence interval; COPD, chronic obstructive pulmonary disease; df, degrees of freedom; I2, heterogeneity; IV, inverse variance; SD, standard deviation
Muscle strength
Rugbjerg (2015) reported that only one study assessed quadriceps strength and hand grip strength. Therefore no meta-analysis was performed. The adjusted mean difference in quadriceps strength was 2.1 Nm (standard error 3.1) lower in the intervention group compared to the control group, p=0.51. The adjusted mean difference in hand grip force was 4.3 lbs (standard error 1.5, p<0.01) favouring the intervention. It was not possible to determine a relative effect, because the baseline muscle strength was not reported.
Quality of life
Rugbjerg (2015) reported the outcome health related quality of life, measured by the St. George's Respiratory Questionnaire. Two studies reported this outcome: Gottlieb 2011 and van Wetering 2010. Gottlieb reported an effect of 2.29 points (95% CI -5.61 to 10.19) increase in SGRQ in the physiotherapy group compared to the control group, while Van Wetering reported a decrease of -2.60 (95% CI -5.13 to -0.08).
Paneroni (2017) reported the outcome quality of life, but no studies included this outcome that investigated a relevant intervention.
Mortality
Rugbjerg (2015) reported the outcome mortality, and pooled the results of the four included RCTs. In the physical rehabilitation group, nine deaths occurred, while seven events were reported in the control group. The resulting odds ratio was 1.35 (95% CI: 0.27 to 6.84). Due to the very low number of incident deaths, a forest plot with pooled data would not be insightful and is not provided.
Level of evidence of the literature
The level of evidence regarding the effect of a community-based physiotherapy intervention in patients with mild COPD on the outcome measure six minute walking distance was downgraded by two levels because of risk of bias (no blinding, missing outcome data), imprecision (confidence interval wide and included the minimal clinical important difference): Low GRADE.
The level of evidence regarding the effect of a community-based physiotherapy intervention in patients with very severe COPD on the outcome measure six minute walking distance was downgraded by two levels because of risk of bias (no blinding, missing outcome data), inconsistency : Low GRADE.
The level of evidence regarding the outcome measure muscle strength was downgraded by three levels because of risk of bias (no blinding and missing outcome data), and imprecision (confidence interval wide and included null): Very Low GRADE.
The level of evidence regarding the outcome measure health-related quality of life was downgraded by three levels because of imprecision (confidence interval wide and included null), lack of blinding, inconsistency, and missing outcome data: Very Low GRADE.
The level of evidence regarding the outcome measure mortality was downgraded by three levels because of imprecision (confidence interval wide and included null), no blinding, and missing outcome data: Very low GRADE.
Search and select
A systematic review of the literature was performed to answer the following question: what is the value of physical therapy in patients with COPD?
P: patients COPD-patiënten zonder actieve COPD-longaanval
I: intervention: usual care + exercise therapy, physical therapy, physiotherapy, home
based rehabilitation.
C: control usual care
O: outcome 6-minute walking distance (6-MWD), mortality, quality of life, and
muscle strength,
Relevant outcome measures
The working group considered 6-MWD, mortality, and muscle strength crucial outcome parameters for decision-making. Quality of life was considered an important outcome parameter for decision making.
The working group defined a set of minimal clinically (patient) important differences (see introduction for further details). For this intervention, the following set was chosen:
• Mortality: ≥10% difference in relative risk
• CCQ-score: >0.4 units
• SGRQ-score: ≥4 units
• Muscle strength: ³25% difference
• 6-MWD: ³30 meters difference
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms until 8 September 2021. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 837 hits. Studies were selected based on the following criteria: systematic reviews that included studies performed in patients with COPD, and investigating the effects of exercise training on the relevant outcomes compared to the effect of no intervention or usual care. Six studies were initially selected based on title and abstract screening. After reading the full text, 4 studies were excluded (see the table with reasons for exclusion under the tab Methods), and 2 studies were included.
Results
Two systematic reviews were included in the analysis of the literature. Important study characteristics and results are summarized in the evidence table. The assessment of the risk of bias is summarized in the risk of bias tables.
- Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease (2022 Report)
- Paneroni M, Simonelli C, Vitacca M, Ambrosino N. Aerobic Exercise Training in Very Severe Chronic Obstructive Pulmonary Disease: A Systematic Review and Meta-Analysis. Am J Phys Med Rehabil. 2017 Aug;96(8):541-548. doi: 10.1097/PHM.0000000000000667. PMID: 28099192.
- Rugbjerg M, Iepsen UW, Jørgensen KJ, Lange P. Effectiveness of pulmonary rehabilitation in COPD with mild symptoms: a systematic review with meta-analyses. Int J Chron Obstruct Pulmon Dis. 2015 Apr 17;10:791-801. doi: 10.2147/COPD.S78607. PMID: 25945044; PMCID: PMC4407740.
- Wuytack F, Devane D, Stovold E, McDonnell M, Casey M, McDonnell TJ, Gillespie P, Raymakers A, Lacasse Y, McCarthy B. Comparison of outpatient and home-based exercise training programmes for COPD: A systematic review and meta-analysis. Respirology. 2018 Mar;23(3):272-283. doi: 10.1111/resp.13224. Epub 2017 Nov 30. PMID: 29194864.
- KNGF-richtlijn COPD. (https://www.kngf.nl/binaries/content/assets/kennisplatform/onbeveiligd/richtlijnen/copd-2020/product-remake/copd-2020-praktijkrichtlijn.pdf)
- Gimeno-Santos E, Frei A, Steurer-Stey C, de Batlle J, Rabinovich RA, Raste Y, Hopkinson NS, Polkey MI, van Remoortel H, Troosters T, Kulich K, Karlsson N, Puhan MA, Garcia-Aymerich J; PROactive consortium. Determinants and outcomes of physical activity in patients with COPD: a systematic review. Thorax. 2014 Aug;69(8):731-9. doi: 10.1136/thoraxjnl-2013-204763. Epub 2014 Feb 20. Erratum in: Thorax. 2014 Sep;69(9):810. multiple investigator names added. PMID: 24558112; PMCID: PMC4112490.
Evidence tables
Fysiotherapie in de eerste lijn
Fysiotherapie in de eerste lijn
Tabel 1 – Risk of biasbeoordeling voor systematische reviews
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/not applicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Rugbjerg, 2015 |
Yes |
Yes |
Yes |
Yes |
Na |
Yes |
Yes |
No |
|
|
Paneroni, 2017 |
Yes |
Yes |
No |
Yes |
na |
Yes Jadad |
No |
Unclear Funnel plots were used but not reported |
No |
Tabel 2 – Risk of biasbeoordeling voor gerandomiseerde studies
|
Study reference
(first author, publication year) |
Was the allocation sequence adequately generated? a
Definitely yes Probably yes Probably no Definitely no |
Was the allocation adequately concealed?b
Definitely yes Probably yes Probably no Definitely no |
Blinding: Was knowledge of the allocated interventions adequately prevented?c
Were patients blinded?
Were healthcare providers blinded?
Were data collectors blinded?
Were outcome assessors blinded?
Were data analysts blinded?
Definitely yes Probably yes Probably no Definitely no |
Was loss to follow-up (missing outcome data) infrequent?d
Definitely yes Probably yes Probably no Definitely no |
Are reports of the study free of selective outcome reporting?e
Definitely yes Probably yes Probably no Definitely no |
Was the study apparently free of other problems that could put it at a risk of bias?f
Definitely yes Probably yes Probably no Definitely no |
Overall risk of bias If applicable/necessary, per outcome measureg
LOW Some concerns HIGH
|
|
Singh, 2003 |
Probably yes |
Probably yes |
Definitely no |
Probably no |
Probably yes |
Probably yes |
Some concerns |
|
Borghi-Silva, 2009 |
Probably yes |
Probably yes |
Definitely no |
Probably no |
Probably yes |
Probably yes |
Some concerns |
|
Pleguezuelos, 2013 |
Definitely yes |
Probably yes |
Definitely no |
Probably yes |
Definitely yes |
Probably yes |
Some concerns |
|
Gottlieb, 2011 |
Probably yes |
Definitely yes |
Definitely no |
Probably no |
Probably yes |
Probably yes |
Some concerns |
|
Liu, 2012 |
Definitely yes |
Probably no |
Definitely no |
Probably yes |
Probably yes |
Probably yes |
Some concerns |
|
Román, 2013 |
Definitely yes |
Definitely yes |
Definitely no |
Definitely no |
Probably yes |
Probably yes |
Some concerns |
|
Van Wetering, 2010 |
Definitely yes |
Probably yes |
Definitely no |
Probably yes |
Probably yes |
Probably yes |
Some concerns |
Beoordelingsdatum en geldigheid
Publicatiedatum : 15-09-2023
Beoordeeld op geldigheid : 31-08-2023
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2020 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met COPD.
Samenstelling van de werkgroep
Werkgroep
- Dr. F. (Folkert) Brijker, longarts, werkzaam in het Spaarne Gasthuis te Haarlem, NVALT (voorzitter, vanaf oktober 2022)
- Dr. J.S. (Jaring) van der Zee, longarts, NVALT (voorzitter, tot oktober 2022)
- Dr. W.H. (Wouter) van Geffen, longarts, werkzaam in het Medisch Centrum Leeuwarden te Leeuwarden, NVALT
- Drs. R. (Renée) van Snippenburg, werkzaam bij Ksyos en waarnemend longarts, NVALT
- Dr. J.C.C.M. (Hans) in ’t Veen, longarts, werkzaam in het Franciscus Gasthuis & Vlietland te Rotterdam, NVALT
- M. (Moniek) Wouters, longarts, werkzaam in het Ziekenhuis Gelderse Vallei te Arnhem, NVALT
- Prof. H.A.M. (Huib) Kerstjens, hoogleraar longziekten, longarts, werkzaam in het UMCG te Groningen, NVALT (vanaf oktober 2022)
- J. (Jeanine) Antons, longarts, werkzaam in het RadboudUMC te Nijmegen, NVALT (vanaf oktober 2022)
- Drs C.L.Y. (Chantal) Knoops, AIOS longgeneeskunde, werkzaam in het Catharina Ziekenhuis te Eindhoven (vanaf oktober 2022)
- Prof. J.W.M. (Jean) Muris, huisarts, werkzaam bij de Universiteit Maastricht, lid van de NHG-Expertgroep CAHAG, NHG
- Drs. E.R. (Erik) van der Meijs, apotheker, KNMP
- W.J.M. (Walter) van Litsenburg, verpleegkundig specialist longgeneeskunde, Catharina Ziekenhuis te Eindhoven, V&VN
- Dr. M.J.H. (Maurice) Sillen, fysiotherapeut, werkzaam bij CIRO, KNGF
- R.A. (Renée) Kool, projectleider, Longfonds
- R. (Ramona) Leysner, diëtiste, Nederlandse Vereniging van Diëtisten (NVD)
- Drs. M. (Menno) Wagenaar, patiëntvertegenwoordiger, Longfonds
- J. (Johan) Smit, patiëntvertegenwoordiger, Longfonds
Met ondersteuning van
- Dr. M. (Margriet) Moret, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Drs. N. (Nicole) Verheijen, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten en longarts
- Dr. T. (Tim) Christen, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Inbreng patiëntenperspectief
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Brijker (voorzitter, vanaf oktober 2022) |
Longarts Spaarne Gasthuis |
Voorzitter sectie COPD NVALT. Dit is een onbetaalde functie binnen de longartsenvereniging NVALT. Lid regionale kwaliteitscommissie COPD/astma. Deze Commissie heeft 2x per jaar vergadering a 2 uur per keer in de avonduren en hiervoor ontvang ik onkostenvergoeding. Docent CASPIR cursussen. dit betreft scholing voor spirometrie voor huisartsen en POH-ers in de regio. Dit vindt een aantal keer per jaar plaats (<5 keer) in de avonduren en hiervoor ontvang ik een onkostenvergoeding |
Geen |
Geen |
|
*Van der Zee (voorzitter, tot oktober 2022) |
Longarts OLVG Amsterdam 0,2FTE tot 1-1-2020 Longarts Amsterdam UMC, locatie AMC, 0,2 FTE |
Lid MEC-U Locatie Nieuwegein, onkosten vergoeding Lid Gezondheidsraad Commissie Gespoten PUR, onkosten vergoeding Incidenteel medische expertises (o.a. DAS, ARAG, Triage, de Rechtspraak), betaald 2019 Speakers fee, Astra-Zeneca, Novartis, Chiesi 2019 1x Ad hoc Advies m.b.t. biologicals bij astma, GSK, betaald |
Geen |
Geen advieswerk tijdens het richtlijnontwikkeltraject |
|
Van Geffen |
Longarts Medisch Centrum Leeuwarden, maatschap Friese Longartsen |
Editorial board Cochrane Airways: Onbetaald Commisie Bronkhorst Nvalt: Onbetaald Richtlijn Commissie NVALT NSCLC: Onbetaald |
Deelname aan een investigator initiated onderzoek firma Novartis. financiering is overgemaakt aan UMCG (2017 beëindigd). Voor de bedrijven Chiesi, Roche, Boehringer en AstraZeneca deelname aan adviesraden betreffende oncologie. Deze gingen niet over COPD of biologicals. De hiervoor gebruikelijke CGR vergoeding werd geweigerd. Chiesi en Boehringer waren wel COPD, maar niet in de laatste 1.5 jaar. |
Geen advieswerk op gebied van COPD of biologicals tijdens het richtlijnontwikkeltraject |
|
In 't Veen |
Longarts bij In 't Veen Longarts BV. Verbonden aan de vakgroep longziekten en STZ expertisecentrum Astma, COPD & Respiratoire Allergie van het Franciscus Gasthuis en Vlietland, Rotterdam. |
Onbetaald: Opleider longziekten Franciscus Gasthuis en Vlietland Lid Concilium Opleiding NVALT Lid Vrij Ademen Akkoord namens NVALT Betrokken longarts bij Schone Lucht Akkoord Lid Move2Improve Lid werkgroep Ziektelastmeter; Generiek en COPD (afgerond) Voorzitter StichtingRoLeX (Rotterdam Leeuwarden eXpertise voor obstructieve longzieken), een stichting die nascholing voor longartsen (i.o.) verzorgd. Bestuurslid LAN Betaald: Longfunctiebeoordelaar Huisartsenlaboratorium STAR-SHL NHG richtlijn COPD namens NVALT Adviseurschap m.b.t. astma: Sanofi, GSK, Boehringer Ingelheim, Chiesi. (laatste 2 jaar (datum invullen 30-6-19) geen persoonlijke betrokkenhied als adviseur bij COPD gerelateerde issues, mede vanwege mijn betrokkenheid bij de NHG richtlijn). Speakers Bureau: Chiesie, Novartis, Boehringer Ingelheim, Inhalatie Technologie Werkgroep Health Agency Stichting RoLeX Sanofi |
Ik beoordeel longfuncties voor een huisarts laboratorium, en heb adviseurschap verricht voor diverse farmaceutische firma's. Er is nooit advies gegeven door mij over medicamenteuze COPD-behandeling, ook niet over biologicals. het genoemde adviseurschap is inmiddels meer dan 3-4 jaar geleden beëindigd. Zie eerder. Research faculty grants, (subsidiegevers Boehringer, Chiesi, Teva, Franciscus wetenschapsbureau) m.b.t. onderzoek bij astma en COPD, via ons expertisecentrum. Van belang hierbij is dat al het onderzoek niet medicatie-gerelateerd is. Zie boven bij onbetaald: Ik ben betrokken bij de bevordering van luchtkwaliteit en als zodanig word ik af en toe geconsulteerd met betrekking tot het schone Lucht Akkoord, een nationaal (door de overheid in gang gezet) platform dat maatregelen hierover in kaart brengt. Voorts ben ik betrokken bij het Vrij Ademen Akkoord, dat oa vanuit LAN, Longfonds, NRS en NVALT aandacht vraagt voor de (toekomstige) patient met een longziekte. |
Geen advieswerk over COPD of biologicals tijdens ontwikkeltraject van de richtlijn. Geen uitwerking van uitgangsvragen over longmedicatie of biologicals. |
|
Van Snippenburg |
Waarnemend Longarts; |
Secretaris Sectie COPD NVALT, onbetaald Werkgroep longen Huisartsen Utrecht Stad, betaald
|
Geen |
Geen |
|
Antons (vanaf oktober 2022) |
Longarts Radboudumc, Nijmegen |
Geen |
Geen |
Geen |
|
Kerstjens (vanaf oktober 2022) |
Hoogleraar longziekten UMCG, 1,0 FTE |
"Voorzitter Noordelijke CARA Stichting. Subsidiegevend orgaan. Onbetaald - Lid RvT bureau bijwerkingen geneesmiddelen LAREB. Betaald aan UMCG - Vz Stichting BEBO. Onafhankelijke METc. Betaald aan UMCG (per 1-1-2023 vz) - Vice-vz Netherlands Respiratory Society. Stichting ter bevordering van wetenschap en wetenschapsklimaat Longziekten NL. Onbetaald. (per 1-1-2023 vz).
Op afroep (geen vaste contracten of afspraken) deelname aan adviesraden van farmaceutische industrieën, en betaling voor lezingen: AstraZeneca, Boehringer Ingelheim, Chiesi, GSK, Novartis. Alles betaald aan UMCG." |
"Geen persoonlijk financieel belang; alles wat er door mij binnenkomt wordt betaald aan UMCG. En krijg ik ook in tweede instantie nooit wat van. 2. Geen dienstverband 3. Betaald adviseurschappen zie bij overige item over nevenwerkzaamheden voor AstraZeneca, Boehringer Ingelheim, Chiesi, GSK, Novartis. 4. Geen directe fianicee belangen of via aandelen of opties. 5. Geen patenten"
"Veel gesponsord onderzoek, o.a. ZonMW VWS Innovatiefonds verzekeraars Industrie: AstraZeneca, Boehringer Ingelheim, Chiesi, GSK, Novartis." |
restricties ten aanzien van besluitvorming met betrekking tot modules over medicatie |
|
Knoops (vanaf oktober 2022) |
AIOS longziekten, Catharina Ziekenhuis Eindhoven |
Geen |
Geen |
Geen |
|
Tazmi (tot oktober 2020) |
Verpleegkundig specialist - werkzaam bij Laurens locatie Intermezzo |
Geen |
Geen |
Geen |
|
Van Jaarsveld |
Adviseur Zorg bij Longfonds |
Geen |
Geen |
Geen |
|
Muris |
Hoogleraar huisartsgeneeskunde, Universiteit Maastricht |
Vervangende werkzaamheden huisartspraktijk Geulle (betaald) |
Geen |
Geen |
|
Van der Meijs |
Apotheker, sinds 1 februari niet meer praktiserend lid namens de KNMP |
SIG-long (SIG = specialist interest group) van KNMP – vacatiegeld |
Geen |
Geen |
|
Van Litsenburg (vanaf oktober 2020) |
Verpleegkundig specialist astma en COPD 36 uur per week 24-uurs thuiszorgverpleegkundige 24 uur per week |
Bestuurslid IMIS (inhalatiemedicatie instructie school) 2u per week Coördinator IMIS Zuid Nederland IMIS trainer Docent Hogeschool Arnhem en Nijmegen Kernteam Picasso voor COPD (momenteel niet actief) Werkgroeplid palliatieve richtlijn COPD |
Kernteamlid Picasso (niet actief) |
Geen |
|
Leysner |
dietist Merem medische revalidatie in Hilversum" |
Incidenteel scholing geven aan studenten hogeschool Holland; betaald |
Geen |
Geen |
|
Wouters |
Bij aanvang AIOS longziekten, Rijnstate Ziekenhuis en thans longarts Ziekenhuis Gelderse Vallei Ede |
Geen |
Geen |
Geen |
|
Wagenaar |
Longervaringsdeskundige bij het Longfonds Geen betaalde functies |
Geen |
Geen |
Geen |
|
Kool |
Projectleider Zorgveld, Longfonds |
Geen |
Geen |
Geen |
|
Sillen |
Resultaatverantwoordelijk fysiotherapeut CIRO+, expertisecentrum voor chronisch orgaanfalen Horn |
Bestuurslid Vereniging voor Hart-, Vaat- en Longfysiotherapie (vacatievergoeding) Extern adviseur Fontys Hogeschool Eindhoven (betaald) Gastdocent Saxion Hogeschool, Enschede en Hogeschool van Amsterdam (betaald) |
Geen |
Geen |
|
Smit |
Longervaringsdeskundige Longfonds (vrijwilligerswerk) |
Geen |
Geen |
Geen |
Implementatie
Er werd aandacht besteed aan het patiëntenperspectief doordat een afgevaardigde patiëntenvereniging zitting nam in de werkgroep. De inbreng van de afgevaardigden is tevens verwerkt in de verslagen hiervan. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan het Longfonds en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerden de werkgroep de knelpunten in de zorg voor patiënten met COPD. De werkgroep beoordeelde de aanbevelingen uit de eerdere richtlijn (NVALT, 2010) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door de NVALT, V&VN Longverpleegkundigen, het Longfonds, NHG, NAPA en KNMP via een invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
De werkgroep heeft uitgebreid over de belangrijkste uitkomstmaten voor de te bespreken interventies gediscussieerd. Het werd wenselijk geacht de set uitkomsten over de verschillende modules waar mogelijk hetzelfde te houden, en zeker met de zelfde minimale klinisch relevante verschillen. Bij specifieke interventies werden soms specifieke relevante uitkomsten toegevoegd. Voor sommige parameters kon geen referentie gevonden worden en werd als onderstaand beschreven een consensus standpunt ingenomen. De werkgroep onderkent dat de absolute risico reductie klinisch beter interpretabel is dan de relatieve, maar kon voor onvoldoende studies die getallen er bij vinden en hield dus vast aan de relatieve risico’s, met toelichting waar mogelijk.
• Exacerbation reduction: ≥20% (Jones, 2014; Chapman 2013)
• Pneumonia: ≥20% difference in relative risk
• Hospital admissions: ≥20% difference in relative risk
• Mortality: ≥10% difference in relative risk
• SGRQ-score: ≥4 units (Jones, 2014)
• CAT-score: >2 units (Kon 2014)
• CCQ-score: >0.4 units
• FEV1: >100 ml (Donohue 2005; Jones, 2014)
• Adverse events: ≥25% difference in relative risk
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur en de beoordeling van de risk-of-bias van de individuele studies is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/) De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
Definitie |
|
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE-methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming blijkt dat er waarschijnlijk geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
|
Module |
Uitkomst kwalitatieve raming |
Toelichting |
|
Module 1.1 Gebruik van inhalatiecorticosteroïden (ICS) bij COPD |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar is (>40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 1.2 Triple therapie in 1 vs in meerdere devices bij COPD |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar is (>40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 1.3 Onderhoudsantibiotica bij COPD
|
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 1.4 Poliklinische behandeling van een COPD-longaanval |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar is (>40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 1.5 Biologicals bij COPD |
Geen substantiële financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten) en zal daarom naar verwachting geen substantiële financiële gevolgen hebben voor de collectieve uitgaven
|
|
Module 2.1 Fysiotherapie in de eerste lijn
|
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 2.2 tweede en derdelijnsrevalidatie bij COPD
|
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 2.3 Voeding bij COPD
|
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar is (>40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 3.1 Zuurstoftherapie bij COPD
|
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar is (>40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 3.2 Longvolumereductie |
geen substantiële financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten) en zal daarom naar verwachting geen substantiële financiële gevolgen hebben voor de collectieve uitgaven.
|
|
Module 3.3 Chronische beademing bij COPD
|
n.v.t. |
Verwijzing naar andere richtlijn |
|
Module 4 COPD zelfmanagement
|
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt ook uit de toetsing het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 5 E-health
|
Geen substantiële financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten) en dat het een nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Het inzetten van digitale zorgtoepassingen zal zijn georganiseerd op lokaal/regionaal niveau en daarom worden op landelijk niveau geen substantiële financiële gevolgen verwacht.
|
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Chapman KR, Bergeron C, Bhutani M, et al. Do we know the minimal clinically important
difference (MCID) for COPD exacerbations? COPD 2013;10(2):243-9.
DOI:10.3109/15412555.2012.733463.
Donohue JF. Minimal clinically important differences in COPD lung function. COPD
2005;2(1):111-124. (http://www.ncbi.nlm.nih.gov/pubmed/17136971).
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Jones PW, Beeh KM, Chapman KR, Decramer M, Mahler DA, Wedzicha JA. Minimal clinically
important differences in pharmacological trials. Am J Respir Crit Care Med
2014;189(3):250-5. DOI: 10.1164/rccm.201310-1863PP.
Kon SS, Canavan JL, Jones SE, et al. Minimum clinically important difference for the COPD
Assessment Test: a prospective analysis. Lancet Respir Med 2014;2(3):195-203. DOI:
10.1016/S2213-2600(14)70001-3.
Kocks JW, Tuinenga MG, Uil SM, van den Berg JW, Stahl E, van der Molen T. Health status
measurement in COPD: the minimal clinically important difference of the Clinical
COPD Questionnaire. Respir Res 2006;7(1):62.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, Glasziou P, Jaeschke R, Vist GE, Williams JW Jr, Kunz R, Craig J, Montori VM, Bossuyt P, Guyatt GH; GRADE Working Group. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008 May 17;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008 May 24;336(7654). doi: 10.1136/bmj.a139.
Schünemann, A Holger J (corrected to Schünemann, Holger J). PubMed PMID: 18483053; PubMed Central PMCID: PMC2386626.
Wessels M, Hielkema L, van der Weijden T. How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. J Med Libr Assoc. 2016 Oct;104(4):320-324. PubMed PMID: 27822157; PubMed Central PMCID: PMC5079497.
Zoekverantwoording
|
Author and year |
Reason for exclusion |
|
Cindy, 2012 |
Wrong study design |
|
Desveaux, 2014 |
No control groups |
|
Gimeno-Santos, 2014 |
Wrong study design |
|
Wuytack, 2018 |
not relevant for PICO |
|
Richtlijn: Update COPD |
|
|
Uitgangsvraag: UV06 fysiotherapie |
|
|
Database(s): Ovid/Medline, Embase |
Datum: 10-8-2021, 8-9-2021 |
|
Periode: |
Talen: nvt |
|
Literatuurspecialist: Ingeborg van Dusseldorp |
|
|
BMI zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Bij gebruikmaking van een volledig zoekblok zal naar de betreffende link op de website worden verwezen. |
|
|
8-9-2021 Voor deze vraag wordt ter oriëntatie gezocht op twee manieren: COPD en fysiotherapie en SR COPD en fysiotherapie en Nederland(s) Vanwege de grote aantallen wordt ervoor gekozen om de SRs vanaf 2010 uit Embase aan te bieden om te bepalen of de strategie kan worden ingeperkt en sleutelartikelen kunnen worden gevonden. Artikelen uit Nederland of Nederlandstalig worden geëxcludeerd omdat deze apart worden aangeboden. Voor deze set wordt geen tijdslimiet toegepast en worden alle studiedesigns en overige referenties getoond.
10-8-2021 Het aantal referenties dat wordt gevonden is erg groot: 406 SR 1628 RCT 1268 OBS
Het sleutelartikel wordt niet gevonden omdat het een richtlijn betreft: 1. Profiling of Patients with COPD for Adequate Referral to Exercise-Based Care: The Dutch Model Spruit M.A., Van't Hul A., Vreeken H.L., Beekman E., Post M.H.T., Meerhoff G.A., Van der Valk A.-L., Zagers C., Sillen M.J.H., Vooijs M., Custers J., Muris J., Langer D., Donkers J., Bregman M., Tissink L., Bergkamp E., Wempe J., Houben-Wilke S., Augustin I.M.L., Bij de Vaate E., Franssen F.F.M., Van Ranst D., Van der Vaart H., Antons J., Van Doormaal M., Koolen E.H., Van der Wees P., Van Snippenburg R., Janssen D.J.A., Simons S. Sports medicine (Auckland, N.Z.) (2020) 50:8 (1421-1429). Date of Publication: 1 Aug 2020
Te gebruiken voor richtlijnen tekst: In de databases Embase en Ovid/Medline is op 2021 met relevante zoektermen gezocht naar systematische reviews, RCTs en observationele studies over (uitgangsvraag). De literatuurzoekactie leverde … unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SRs vanaf 2010 |
291 |
|
283 |
|
SRs Nederland |
47 |
12 |
52 |
|
RCTs Nederland |
116 |
68 |
162 |
|
Observationele studies Nederland |
97 |
49 |
133 |
|
Overig Nederland |
121 |
106 |
207 |
|
Totaal |
|
|
|
Zoekstrategie
Embase
|
No. |
Query |
Results |
|
#25 |
#10 NOT #18 SR NOT Nederland |
291 |
|
#24 |
#18 NOT #21 NOT #20 NOT #19 Overige Nederland |
121 |
|
#23 |
#21 NOT #20 NOT #19 OBS Nederland |
97 |
|
#22 |
#20 NOT #19 RCT Nederland |
116 |
|
#21 |
#9 AND #18 |
162 |
|
#20 |
#8 AND #18 |
141 |
|
#19 |
#7 AND #18 SR Nederland |
47 |
|
#18 |
#15 AND #17 |
380 |
|
#17 |
#3 NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
5900 |
|
#16 |
#4 AND #15 |
263 |
|
#15 |
'netherlands'/exp OR netherlands:ad,ca,ti,ab,kw OR holland:ad,ca,ti,ab,kw OR dutch:ls,la,ti,ab,kw OR nederland:ca,ad,ti,ab,kw |
982144 |
|
#14 |
#12 NOT #11 NOT #10 |
797 |
|
#13 |
#11 NOT #10 |
989 |
|
#12 |
#4 AND #9 |
1406 |
|
#11 |
#4 AND #8 |
1168 |
|
#10 |
#4 AND #7 SR |
330 |
|
#9 |
'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'comparative study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) |
6630255 |
|
#8 |
'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti |
3302394 |
|
#7 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
733409 |
|
#6 |
#4 AND #5 |
1 |
|
#5 |
profiling AND of AND patients AND with AND copd AND for AND adequate AND referral AND to AND 'exercise based' AND care |
1 |
|
#4 |
#3 AND (1-1-2010)/sd NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
3194 |
|
#3 |
#1 AND #2 |
11272 |
|
#2 |
'physiotherapy'/exp/mj OR 'exercise'/exp/mj OR 'physical therap*':ti,ab,kw OR 'physio therap*':ti,kw OR 'physiotherap*':ti,kw OR exercis*:ti,kw OR 'endurance':ti,kw OR 'physical activit*':ti,kw |
373640 |
|
#1 |
'chronic obstructive lung disease'/exp/mj OR ('chronic obstructive' NEAR/2 (lung OR pulmonary OR airway)) OR 'copd':ab,ti,kw OR 'chronic bronchitis':ab,ti,kw OR emphysema:ab,ti,kw OR aecopd:ti,ab,kw |
210767 |
Ovid/Medline
|
# |
Searches |
Results |
|
14 |
5 not 11 not 10 not 9 Overige Nederland |
106 |
|
13 |
11 not 10 not 9 OBS Nederland |
49 |
|
12 |
10 not 9 RCT Nederland |
68 |
|
11 |
5 and 8 |
75 |
|
10 |
5 and 7 |
76 |
|
9 |
5 and 6 SR Nederland |
12 |
|
8 |
Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or cohort.tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ (Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies) |
3933718 |
|
7 |
(exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) |
2162639 |
|
6 |
(meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf.) not (comment/ or editorial/ or letter/ or ((exp animals/ or exp models, animal/) not humans/)) |
517648 |
|
5 |
3 and 4 |
235 |
|
4 |
Netherlands/ or netherlands.cp. or holland.cp,lg. or dutch.ti,ab,kf. or holland.ti,ab,kf. or netherlands.ti,ab,kf. |
1901984 |
|
3 |
1 and 2 |
6081 |
|
2 |
exp Physical Therapy Modalities/ or exp Exercise/ or exp Exercise Therapy/ or physio therap*.ti,kf. or physiotherap*.ti,kf. or exercis*.ti,kf. or endurance.ti,kf. or physical activit*.ti,kf. |
447100 |
|
1 |
exp Pulmonary Disease, Chronic Obstructive/ or ('chronic obstructive' adj2 (lung or pulmonary or airway)).ab,ti,kf. or copd.ab,ti,kf. |
94436 |