Bronchoscopische longvolumereductie
Uitgangsvraag
Welke COPD-patiënten komen in aanmerking voor een bronchoscopische longvolumereductie behandeling?
Aanbeveling
Screen patiënten met een ernstig tot zeer ernstig COPD die gestopt zijn met roken en die een maximale conservatieve behandeling hebben op de aanwezigheid van hyperinflatie.
Verwijs patiënten met hyperinflatie die potentieel geschikt en gemotiveerd zijn voor longvolume reductie naar een behandelcentrum
Bespreek patiënten voorafgaand aan een longvolume reductie behandeling in een MDO
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
In COPD-patiënten met tekenen van ernstige hyperinflatie lijkt er, op basis van de literatuur, sprake van een klinisch relevante verbetering van de longfunctie en loopafstand door endobronchiale longvolume-reductietechnieken met kleppen, wanneer deze vergeleken worden met de standaardbehandeling van COPD. De overall bewijskracht voor klinische verbetering (longfunctie, loopafstand en kwaliteit van leven) door endobronchiale ventielen is redelijk. Voor endobronchiale ‘coils’ is de bewijskracht laag. Plaatsing van zowel endobronchiale kleppen als ‘coils’ gepaard met meer adverse events, vooral pneumothorax en longaanvallen en hogere mortaliteit. De overall bewijskracht is voor zowel kleppen als coils laag voor de vergelijking tussen endobronchiale longvolumereductie en standaard COPD-behandeling.
Op basis van de beschikbare data kan worden gesteld dat longvolume reductie in een zeer kleine en uitermate geselecteerde groep patiënten een significante en klinische relevante verbetering kan opleveren. Op mortaliteit kunnen er geen conclusies worden verbonden aan de beschikbare data, echter op kwaliteit van leven kan dat wel, en ook zijn er cohort onderzoeken waarbij een overleving bij de succesvol behandelde groep is aangetoond op langere termijn (Garner, 2016, 2020). Gezien de voordelen nu, zal het ethisch gezien lastig zijn om geschikte patiënten niet te behandelen en het is daarom zeer de vraag of er betrouwbare zeer lange termijn gerandomiseerde data beschikbaar zal komen met onbehandelde patiënten.
Patiënten worden geselecteerd op basis van diverse criteria. Hierin speelt o.a. de mate van hyperinflatie, klachten, de rookstatus, de comorbiditeiten, de beschikbaarheid van alternatieve behandelingen en de anatomie van de COPD een belangrijke rol. De richtlijn kan op basis van de huidige search geen uitspraak doen over de exacte selectiecriteria van de patiënt voor de specifieke behandelingen. Het verdient daarom aanbeveling potentieel geschikte patiënten te overleggen met experts binnen het veld.
De bewijskracht op het gebied van ventielen heeft deze reeds doen opnemen in het verzekerde pakket in Nederland (zie standpunt zorginstituut Nederland). De beschikbaarheid van coils is er echter op het moment van schrijven niet in de klinische routine. Wel lopen er met zekere regelmaat studies naar de behandeling.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
De voorkeuren van patiënten zijn meegenomen in de beschikbare onderzoeken d.m.v. PROM’s. Vaak betrof het hier de SGRQ. Er is een duidelijk voordeel zichtbaar ten faveure van de behandeling met longvolume reductie (van Geffen, 2019; Klooster, 2015). Dit wordt onderschreven door ervaringsdeskundigen van het Longfonds.
Kosten (middelenbeslag)
De behandeling met endoscopische behandelingen is erg duur. De behandeling met coils is nog vele malen duurder dan die van een ventielbehandeling. Een belangrijke factor hierin zijn de materiaalkosten. Op dit moment zijn behandelingen met ventielen opgenomen in het basispakket. De behandeling dient slechts te worden overwogen bij patiënten die duurzaam gestopt zijn met roken en reeds maximaal conservatief worden behandeld.
Aanvaardbaarheid, haalbaarheid en implementatie
Op dit moment is de behandeling beschikbaar in enkele geselecteerde centra verspreid door het land. Het verdient aanbeveling om patiënten die gemotiveerd en geschikt voorafgaande aan een longvolume reductie behandeling in een lokaal of regionaal MDO te bespreken. De productie van de coils zoals eerder onderzocht en gepubliceerd is gestaakt en zal mogelijk vervangen worden door nieuwe ontwerpen.
Rationale van de aanbeveling
Op basis van de evidence kan longvolume reductie in een zeer kleine en uitermate geselecteerde groep COPD-patiënten een significante en klinische relevante verbetering geven. De richtlijn kan op basis van de huidige search geen uitspraak doen over de exacte selectiecriteria en type behandeling. Het verdient daarom aanbeveling potentieel geschikte en gemotiveerde patiënten met hyperinflatie te overleggen met experts binnen het veld.
Onderbouwing
Voor patiënten met ernstig COPD komen steeds nieuwe behandelingen beschikbaar. Voor een kleine subgroep patiënten met klachten op basis met ernstig emfyseem en hyperinflatie bestaat er naast de standaardbehandelingen, zoals stoppen met roken, inhalatie medicatie, fysiotherapie en revalidatie ook de mogelijkheid om de hyperinflatie te reduceren met een longvolume reductie behandeling. Hiervoor zijn diverse technieken beschikbaar. In Nederland zijn met name chirurgie en bronchoscopische behandeling met ventielen beschikbaar en vinden er studies naar coils plaats. De actuele toevoegde kennis berust op bronchoscopische longvolumereductie. De werkgroep heeft de oude techniek van longvolumereductie chirurgie in het literatuuronderzoek buiten beschouwing van deze module gelaten. Op basis van de beschikbare middelen binnen het budget van de richtlijn update is er door de commissie voor gekozen geen nieuw literatuur onderzoek te verrichten maar uit te gaan van een recente beschikbare meta-analyse met zo homogeen mogelijke inclusie criteria. Daarmee zijn niet alle bestaande studies volledig geëvalueerd. De commissie acht het onwaarschijnlijk dat deze selectiebias zou leiden tot een andere uitkomst of aanbevelingen.
Lung function (FEV1; RV) (crucial outcome measure)
|
Moderate GRADE |
Placement of endobronchial valves probably increases lung function compared to standard care, in a selected group of COPD patients.
Sources: Criner, 2019; van Geffen, 2019; Li, 2019 |
|
Moderate GRADE |
Placement of endobronchial coils probably increases lung function compared to standard care, in a selected group of COPD patients
Sources: van Geffen, 2019 |
6-minute walk test (6MWT) (crucial outcome measure)
|
Moderate GRADE |
Placement of endobronchial valves probably increases 6-minute walk test distance compared to standard care, in a selected group of COPD patients.
Sources: Criner, 2019; van Geffen, 2019; Li, 2019 |
|
Low GRADE |
Placement of endobronchial coils may increase 6-minute walk distance compared to standard care, in a selected group of COPD patients.
Sources: van Geffen, 2019 |
Quality of life (SGRQ) (important outcome measure)
|
Moderate GRADE |
Placement of endobronchial valves probably improves SGRQ-score compared to standard care, in a selected group of COPD patients.
Sources: Criner, 2019; van Geffen, 2019; Li, 2019 |
|
Moderate GRADE |
Placement of endobronchial coils probably improves SGRQ-score compared to standard care, in a selected group of COPD patients.
Sources: van Geffen, 2019 |
Adverse events (AEs) (important outcome measure)
|
Moderate GRADE |
Placement of endobronchial valves probably increases adverse events compared to standard care.
Sources: Criner, 2019; van Geffen, 2019; Li, 2019 |
|
Low GRADE |
Placement of endobronchial coils may increase adverse events compared to standard care.
Sources: van Geffen, 2019 |
Mortality (important outcome measure)
|
Low GRADE |
Placement of endobronchial valves may increase mortality slightly compared to standard care.
Sources: Criner, 2019; van Geffen, 2019; Li, 2019 |
|
Low GRADE |
Placement of endobronchial coils may increase mortality slightly compared to standard care.
Sources: van Geffen, 2019 |
Description of studies
Van Geffen (2019) performed a systematic review and meta-analysis on surgical and endoscopic interventions that reduce lung volume in emphysema patients, based on a literature search up to June 2018. The literature review in this module will only focus on endoscopic techniques. Studies included in this systematic review (Criner 2018, Davey 2015, Kemp 2017, Klooster 2015, Valipour 2016, VENT-trail 2010 and 2012) were RCTs comparing lung volume reduction to standard or sham care in patients with emphysema/COPD, having a post- FEV1 <60% of predicted and a RV >150% of predicted. Inclusion of trials was limited to trials of techniques in which there was sustainable volume reduction. Patients treated for a different indication than emphysema/COPD were excluded. The number of studies included was 6 on endobronchial valves (Pulmonyx Zephyr® Valves) (620 patients) and 3 on endobronchial coils (461 patients). For both, endobronchial valves and coils, trial criteria differed with respect to emphysema distribution (homogeneous and heterogeneous). Follow-up for all studies was between 3 and 12 months.
The EMPROVE study (Criner, 2019) was a prospective, multicentre RCT. In this RCT 113 cases who underwent lung volume reduction by bronchoscopic placement of a Spiration® Valve System were compared to 59 controls treated with standard care. Patients were included between 2013-2017 when having stable COPD with a FEV1 <45%, a TLC >100% and a RV >150% of predicted after bronchodilatation. Patients had to be able to perform a 6MWT >140 m and had to have >40% emphysema destruction in the target lobe. The target and ipsilateral lobes were required to be separated by an intact fissure. Follow-up was 6 months, patients and caregivers were not blinded.
The REACH trial, a multicentre, prospective, unblinded, RCT was performed by (Li, 2019). Patients with stable COPD and severe airflow obstruction (post- FEV1 ≤ 45%) and hyperinflation (TLC ≥100% and RV ≥150%) were included and randomly assigned to either treatment with the Spiration® valve system (72 cases) or standard care (35 controls). Patients were included if they had a highly diseased target lobe (≥40% emphysema involvement), high heterogeneity compared to the ipsilateral lobe (≥15% difference), and an intact interlobar fissure (≥90% complete). Follow-up was 12 months, patients and caregivers were not blinded.
Results
Lung function (FEV1; RV) (crucial outcome measure)
Endobronchial valves
For mean difference in RV after lung volume reduction by endobronchial valves, 8 studies (Criner, 2018; Criner, 2019; Davey, 2015; Kemp, 2017; Klooster, 2015; Li, 2019; Valipour, 2016; VENT-trail, 2010 and 2012) (340 cases; 260 controls) are pooled (figure 1 2). Six studies ((Criner, 2018; Criner, 2019; Davey, 2015; Kemp, 2017; Klooster, 2015; Li, 2019; Valipour, 2016; VENT-trail, 2010 and 2012)) reported on percentage increase in FEV1 (356 cases; 264 controls) (Criner, 2018; Davey, 2015; Kemp, 2017; Klooster, 2015; Valipour, 2016; VENT-trail, 2010 and 2012), whereas 2 studies (Criner, 2019; Li, 2019) reported on volume increase in FEV1 after lung volume reduction by endobronchial valves. As direction of the effect were comparable for all studies, we chose to pool only mean differences of studies presenting percentage FEV1. The latter 2 studies (Criner, 2019; Li, 2019) are described below. Follow-up of studies was 3-12 months.
Criner (2019) reported on FEV1 in 86 patients with COPD undergoing lung volume reduction by valves compared to 39 patients treated with standard care. Mean increase in FEV1 after 6 months was 0.067L (SD 0.167) in cases and -0.032L (SD 0.114) in controls.
Regarding FEV1, the RCT performed by Li (2019), included 63 cases (100% male) and 33 controls (97% male). At the end of 12 months follow-up, mean increase in FEV1 in the lung volume reduction group was 0.091L (SD0.156), whereas the difference for controls was
–0.024L (0.142).
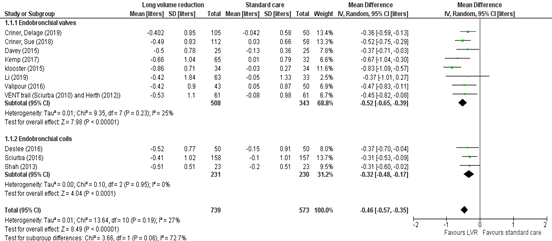
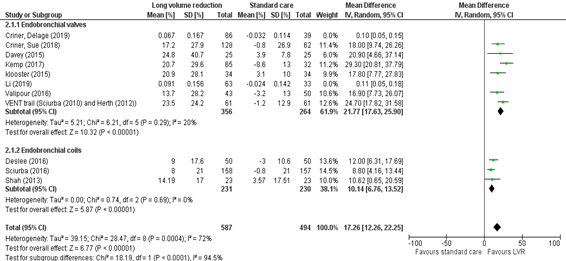
Forest plots for pooled RV and FEV1 are depicted in figure 1 and figure 2. Pooled mean difference for RV(508 cases, 343 controls) was -0.52 (95% CI -0.65 to -0.39) in favour of lung volume reduction. For post-BD FEV1 (356 cases, 264 controls), mean FEV1 was increased by 21.77% (95% CI 17.63 to 25.90) favoring LVR. These results mean that COPD patients undergoing endoscopic lung volume reduction by endobronchial valves experience a clinically relevant improvement in residual volume.
Endobronchial coils
Three studies (Deslee 2016, Sciurba 2016, Shah 2013) in the meta-analysis by Van Geffen (2019) reported on FEV1 (231 cases; 230 controls) and RV (231 cases; 230 controls), see figures 1 and 2. After follow-up of 3-12 months, lung volume with endobronchial coils resulted in a mean increase of FEV1 of 10.14% (95% CI 6.76 to 13.52) and a mean reduction of RV of -0.32L (95% CI -0.48 to -0.17) compared to controls.
Figure 1: mean difference of residual volumes (litres) for lung volume reduction compared to standard care
Figure 2: mean difference of post-bronchodilated FEV1 for lung volume reduction compared to standard care
6-minute walk test (6-MWT) (crucial outcome measure)
Endobronchial valves
Six studies (356 cases, 264 controls) ((Criner, 2018; Davey, 2015; Kemp, 2017; Klooster, 2015; Valipour, 2016; VENT-trail, 2010 and 2012)) were included in a pooled analysis of 6MWT by van Geffen (2019). After 3-12 months follow-up, 6MWT was improved by 49.00 m (95% CI 31.89 to 66.10) in favor of the lung volume reduction group.
In the RCT by Criner (2019) (102 cases, 48 controls) decline in walking distance 6 months from baseline, was less among cases than controls (mean difference 6.90 meters (95% CI -13.91 to 27.71). The RCT conducted by Li (2019) reported an improvement from baseline to 12 months in favor of treatment by endobronchial coils (mean difference 36.40 meters (95% CI 3.85 to 68.95)
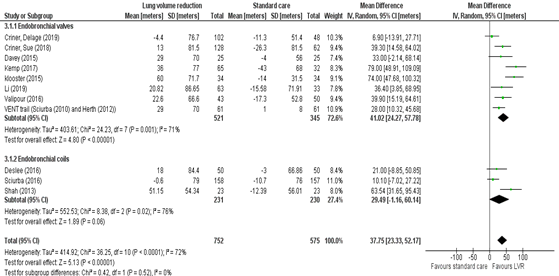
A forest plot is depicted in Figure 3. Pooled mean difference for 6-minute walking distance in COPD patient who underwent lung volume reduction by endobronchial valves compared to standard care is 41.02 m (95% CI 24.27 to 57.78). This is a clinically relevant difference and these results indicate that COPD patients undergoing endoscopic lung volume reduction by endobronchial valves experience an improvement in 6MWT.
Endobronchial coils
Van Geffen (2019) pooled results of 3 studies (Deslee, 2016; Sciurba, 2016; Shah, 2013) (231 cases, 230 controls) to investigate the effect of endobronchial coils on 6MWT. Mean difference was 29.49 m (95% CI -1.16 to 60.14) favoring LVR. The mean value is within the boundaries of clinical important difference (figure 3). This effect is not clinically relevant. Additionally, the confidence interval is wide and includes both, positive and negative effect. The result of treating COPD patient with endobronchial coils on exercise capacity is therefore unsure.
Figure 3: mean difference of 6-minute walk test for lung volume reduction compared to standard care
Quality of life (SGRQ) (important outcome measure)
Endobronchial valves
Van Geffen (2019) included 6 studies (Criner, 2018; Davey, 2015; Kemp, 2017; Klooster, 2015; Valipour, 2016; VENT-trail, 2010 and 2012) in a systematic review and meta-analysis comparing the effect on SGRQ of endobronchial valves (504 cases) to standard care (336 controls). After 3-12 months follow-up mean in quality of life improved by 9.13 points on the SGRQ favoring intervention (mean difference -9.13 points (95% CI -12.37 to -5.89).
RCTs by Criner (2019) (95 cases, 41 controls) and Li (2019) (63 cases, 33 controls) also showed an improvement in SGRQ for case, mean differences between intervention and control groups were -9.5 points (95% CI -14.4 to -4.7) and -10.50 points (95% CI-17.86 to -3.14), respectively.
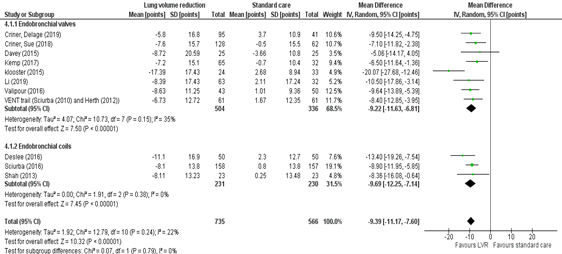
Figure 4 shows a pooled SGRQ of -9.22 points (95% CI -11.63 to -6.81). These results are clinically relevant and indicate that COPD patients undergoing endoscopic lung volume reduction by endobronchial valves experience a clinically relevant improvement in quality of life compared to standard care.
Endobronchial coils
Results of a systematic review and meta-analysis by Van Geffen (2019), included 3 studies (Deslee 2016, Sciurba 2016, Shah 2013) comparing endobronchial coils to standard care, showed a clinically relevant improvement with a mean difference of -9.69 points (-11.17 to -7.60) in favor of endobronchial coils (see also figure 4).
Figure 4: mean difference of St. George Respiratory Questionnaire for lung volume reduction compared to standard care
Adverse events (AEs) including mortality (important outcome measures)
Endobronchial valves
In the systematic review and meta-analysis by (van Geffen, 2019). This review included 6 studies (Criner, 2018; Davey, 2015; Kemp, 2017; Klooster, 2015; Valipour, 2016; VENT-trail 2010 and 2012). Pooled OR for an adverse event, which included mortality, increased following an intervention in comparison to standard care (OR 9.58 (95% CI 5.56 to 16.50) (356 cases; 264 controls 356/264)) favoring standard care. Follow-up was between 3-12 months The most frequent adverse events with bronchial valve treatment were pneumothorax and COPD exacerbations, incidences across studies were 1.4-25% and 4-20%, respectively. Overall mortality did not differ between the intervention and control group (OR 1.84 (95% CI 0.62 to 5.42)).
(Criner, 2019) assessed thoracic adverse events, including mortality, for a period of 0-6 months after valve placing (113 cases; 59 controls). At 6 months, the incidence of thoracic adverse events was 31.0% in the treatment group and 11.9% (between-group difference: 19.1% (95% CI 5.9 to 29.7). This higher treatment group incidence was primarily due to a 12.4% (95% CI 4.6 to 18.6) increased incidence of pneumothorax. Death from any cause was 5.3% in the treatment group, 1.7% in the control group. Between group difference was 3.6% (95% CI 3.9 to 8.9).
(Li, 2019) documented, during a 6-month follow-up period, 22 cases (N=66) and 8 controls (N=33) having adverse events. The majority of these events being acute exacerbations of COPD (13 cases (19.7%), 4 controls (12.1%)). Pneumothorax was the second most frequent event in the treatment group, occurring in 5 patients (7.6%). No deaths occurred in the treatment group; 1 patient died in the control group.
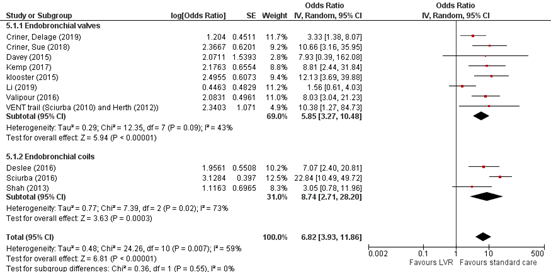
The pooled odds ratio for adverse events, including mortality is 5.85 (95% CI 3.27 to 10.48) in favor of standard care (see figure 5). This means that the odds of experiencing an adverse event in patients undergoing lung volume reduction by endobronchial valves is 5.8 times higher than the odds of adverse events in patients receiving standard care. This difference is clinically relevant.
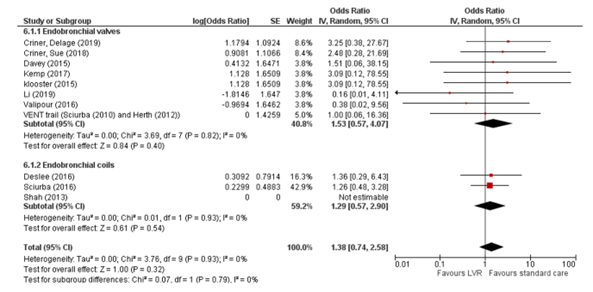
The pooled odds ratio for mortality is 1.53 (95% CI 0.57 to 4.07), in favor of standard care (see figure 6). This difference is clinically relevant. However, as the confidence interval includes both an effect and no effect, this effect is imprecise.
Endobronchial coils
Results of 3 studies (Deslee, 2016, Sciurba; 2016; Shah, 2013) presented by (van Geffen, 2019) showed more adverse events in patients (201 events in 228 patients) treated with coils than in the group receiving standard care (102 events in 230 controls). Pooled OR was 8.74 (95% CI 2.71 to 28.20) (see figure 5), which is a clinically relevant effect. The most common adverse events were pneumonia (incidence across studies 5-20%), COPD exacerbations (incidence across studies 7-28%) and pneumothorax (incidence across studies 5-10%). Although the difference in mortality was clinically relevant, the pooled odds ratio being 1.29 (95% CI 0.57 to 2.00), this effect is imprecise as the confidence interval includes ‘1’.
Figure 5: Odds ratio for adverse events, including mortality for lung volume reduction compared to standard care
Figure 6: Odds ratio for mortality for lung volume reduction compared to standard care
Level of evidence of the literature
Lung function (FEV1; RV) (crucial outcome measure)
Endobronchial valves
The level of evidence regarding the outcome measure lung function started high as we included a meta-analysis and randomized controlled trials. The level of evidence was downgraded by 1 level because the confidence interval crosses the boundaries of clinical relevance (imprecision, -1). The level of evidence is moderate.
Endobronchial coils
The level of evidence regarding the outcome measure lung function started high as we included a meta-analysis and randomized controlled trials. The level of evidence was downgraded by 1 level because the confidence interval crosses the boundaries of clinical relevance (imprecision, -1). The level of evidence is moderate.
6-minute walk test (6MWT) (crucial outcome measure)
The level of evidence regarding the outcome measure 6-minute walk test started high as we included a meta-analysis and randomized controlled trials. The level of evidence was downgraded by 1 level because the confidence interval crosses the boundaries of clinical relevance (imprecision, -1). The level of evidence is moderate.
Endobronchial coils
The level of evidence regarding the outcome measure 6-minute walk test started high as we included a meta-analysis and randomized controlled trials. The level of evidence was downgraded by 2 levels because the confidence interval crosses the boundaries of clinical relevance and no effect (imprecision, -2). The level of evidence is low.
Quality of life (SGRQ) (important outcome measure)
The level of evidence regarding the outcome measure SGRQ test started high as we included a meta-analysis and randomized controlled trials. The level of evidence was downgraded by 1 level because of study limitations (risk of bias, -1, because of lack of blinding). The level of evidence is moderate.
Endobronchial coils
The level of evidence regarding the outcome measure SGRQ started high as we included a meta-analysis and randomized controlled trials. The level of evidence was downgraded by 1 level because of study limitations (risk of bias, -1, because of lack of blinding). The level of evidence is moderate.
Adverse events (AEs) (important outcome measure)
Endobronchial valves
The level of evidence regarding the outcome measure adverse events started at high as we included a meta-analysis and randomized controlled trials. The level of evidence was downgraded by 1 level because of study limitations (risk of bias, -1, because of lack of blinding). The level of evidence is moderate.
Endobronchial coils
The level of evidence regarding the outcome measure adverse events started at high as we included a meta-analysis and randomized controlled trials. The level of evidence was downgraded by 2 level because of study limitations (risk of bias, -1, because of lack of blinding) and inconsistency (-1). The level of evidence is low.
Mortality (important outcome measure)
Endobronchial valves
The level of evidence regarding the outcome measure mortality test started high as we included a meta-analysis and randomized controlled trials. The level of evidence was downgraded by 2 levels because of imprecision (95% CI included a positive effect, no effect and a negative effect of the intervention on mortality, -2). The level of evidence is low.
Endobronchial coils
The level of evidence regarding the outcome measure mortality started high as we included a meta-analysis and randomized controlled trials. The level of evidence was downgraded by 2 levels because of imprecision (95% CI included a positive effect, no effect and a negative effect of the intervention on mortality, -2). The level of evidence is low.
A systematic review of the literature was performed to answer the following question:
1. Does bronchoscopic lung volume reduction improve outcomes in patients with emphysema compared with standard of care?
2. Are these interventions associated with major adverse events compared with standard of care?
P: patients patients with COPD, emphysema
I: intervention bronchoscopic lung volume reduction (LVR):
a. by endobronchial valves
b. by endobronchial coils
C: control standard care or sham care
O: outcome lung function (FEV1; RV), 6-minute walk test (6MWT), quality of life
(SGRQ), adverse events (AEs), mortality
Relevant outcome measures
The guideline development group considered lung function and 6MWT as crucial outcome measures for decision making; and quality of life, AEs and mortality as important outcome measures for decision making.
A priori, the working group did not define the outcome measures listed above but used the definitions used in the studies.
The working group defined a set of minimal clinically (patient) important differences (see introduction for further details). For this intervention, the following set was chosen:
- Exacerbation reduction: ≥20%
- Mortality: ≥10% difference in relative risk
- Pneumonia: ≥20% difference in relative risk
- CAT-score: >2 units
- CCQ-score: >0.4 units
- SGRQ-score: ≥4 units
- Hospital admissions: ≥20% difference in relative risk
- Adverse events: ≥25% difference in relative risk
- FEV1: >100 ml
Search and select (Methods)
The working group used the systematic review by Van Geffen (2019). This systematic review included literature until June 2018. Therefore, an additional a literature search was performed from 1-1-2018 until 5-5-2021. The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms. This search strategy is depicted under the tab Methods. This additional systematic literature search resulted in 169 hits. Studies were selected based on the following criteria: systematic reviews and randomized controlled trials comparing lung volume reduction by endobronchial valves or by endobronchial coils versus standard or sham care in patients with COPD. Apart from the systematic review by van Geffen (2019), 6 additional studies were initially selected based on title and abstract screening. After reading the full text, 4 studies were excluded (see the table with reasons for exclusion under the tab Methods), and 2 studies were included.
Results
One systematic review and 2 RCTs were included in the analysis of the literature. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
- Criner, Gerard J., Antoine Delage, Kirk Voelker, D. Kyle Hogarth, Adnan Majid, Michael Zgoda, Donald R. Lazarus, Roberto Casal, Sadia B. Benzaquen, Robert C. Holladay, Adam Wellikoff, Karel Calero, Mark J. Rumbak, Paul R. Branca, Muhanned Abu-Hijleh, Jorge M. Mallea, Ravi Kalhan, Ashutosh Sachdeva, C. Matthew Kinsey, Carla R. Lamb, Michael F. Reed, Wissam B. Abouzgheib, Phillip V. Kaplan, Gregory X. Marrujo, David W. Johnstone, Mario G. Gasparri, Arturo A. Meade, Christopher A. Hergott, Chakravarthy Reddy, Richard A. Mularski, Amy Hajari Case, Samir S. Makani, Ray W. Shepherd, Benson Chen, Gregory E. Holt, and Simon Martel. 2019. Improving Lung Function in Severe Heterogenous Emphysema with the Spiration Valve System (EMPROVE). A Multicenter, Open-Label Randomized Controlled Clinical Trial. American Journal of Respiratory and Critical Care Medicine 200(11):135462. doi: 10.1164/rccm.201902-0383OC.
- Donohue, James F. 2005. Minimal Clinically Important Differences in COPD Lung Function. COPD 2(1):11124. doi: 10.1081/copd-200053377.
- Garner, Justin, Samuel V. Kemp, Tudor P. Toma, David M. Hansell, Michael I. Polkey, Pallav L. Shah, and Nicolas S. Hopkinson. 2016. Survival after Endobronchial Valve Placement for Emphysema: A 10-Year Follow-up Study. American Journal of Respiratory and Critical Care Medicine 194(4):51921. doi: 10.1164/rccm.201604-0852LE.
- Garner, Justin L., Samuel V. Kemp, Karthi Srikanthan, Cielito Caneja, Zaid Zoumot, Cara Roberts, Winston Banya, Rekha Chaudhuri, Stephen Bicknell, Ewen Ross, Adam S. LaPrad, and Pallav L. Shah. 2020. 5-Year Survival after Endobronchial Coil Implantation: Secondary Analysis of the First Randomised Controlled Trial, RESET. Respiration; International Review of Thoracic Diseases 99(2):15462. doi: 10.1159/000505274.
- van Geffen, Wouter H., Dirk-Jan Slebos, Felix J. Herth, Samuel V. Kemp, Walter Weder, and Pallav L. Shah. 2019. Surgical and Endoscopic Interventions That Reduce Lung Volume for Emphysema: A Systemic Review and Meta-Analysis. The Lancet. Respiratory Medicine 7(4):31324. doi: 10.1016/S2213-2600(18)30431-4.
- Hartman, Jorine E., Nick H. T. ten Hacken, Karin Klooster, H. Marike Boezen, Mathieu H. G. de Greef, and Dirk-Jan Slebos. 2012. The Minimal Important Difference for Residual Volume in Patients with Severe Emphysema. European Respiratory Journal 40(5):113741. doi: 10.1183/09031936.00219111.
- Holland, Anne E., Martijn A. Spruit, Thierry Troosters, Milo A. Puhan, Véronique Pepin, Didier Saey, Meredith C. McCormack, Brian W. Carlin, Frank C. Sciurba, Fabio Pitta, Jack Wanger, Neil MacIntyre, David A. Kaminsky, Bruce H. Culver, Susan M. Revill, Nidia A. Hernandes, Vasileios Andrianopoulos, Carlos Augusto Camillo, Katy E. Mitchell, Annemarie L. Lee, Catherine J. Hill, and Sally J. Singh. 2014. An Official European Respiratory Society/American Thoracic Society Technical Standard: Field Walking Tests in Chronic Respiratory Disease. European Respiratory Journal 44(6):142846. doi: 10.1183/09031936.00150314.
- Jones, Paul W., Kai M. Beeh, Kenneth R. Chapman, Marc Decramer, Donald A. Mahler, and Jadwiga A. Wedzicha. 2014. Minimal Clinically Important Differences in Pharmacological Trials. American Journal of Respiratory and Critical Care Medicine 189(3):25055. doi: 10.1164/rccm.201310-1863PP.
- Klooster, Karin, Nick H. T. ten Hacken, Jorine E. Hartman, Huib A. M. Kerstjens, Eva M. van Rikxoort, and Dirk-Jan Slebos. 2015. Endobronchial Valves for Emphysema without Interlobar Collateral Ventilation. New England Journal of Medicine 373(24):232535. doi: 10.1056/NEJMoa1507807.
- Li, Shiyue, Guangfa Wang, Changhui Wang, Xinglin Gao, Faguang Jin, Huaping Yang, Baohui Han, Rui Zhou, Chengshui Chen, Liangan Chen, Chunxue Bai, Huahao Shen, Felix J. F. Herth, and Nanshan Zhong. 2019. The REACH Trial: A Randomized Controlled Trial Assessing the Safety and Effectiveness of the Spiration® Valve System in the Treatment of Severe Emphysema. Respiration; International Review of Thoracic Diseases 97(5):41627. doi: 10.1159/000494327.
- Singh, Sally J., Milo A. Puhan, Vasileios Andrianopoulos, Nidia A. Hernandes, Katy E. Mitchell, Catherine J. Hill, Annemarie L. Lee, Carlos Augusto Camillo, Thierry Troosters, Martijn A. Spruit, Brian W. Carlin, Jack Wanger, Véronique Pepin, Didier Saey, Fabio Pitta, David A. Kaminsky, Meredith C. McCormack, Neil MacIntyre, Bruce H. Culver, Frank C. Sciurba, Susan M. Revill, Veronica Delafosse, and Anne E. Holland. 2014. An Official Systematic Review of the European Respiratory Society/American Thoracic Society: Measurement Properties of Field Walking Tests in Chronic Respiratory Disease. The European Respiratory Journal 44(6):144778. doi: 10.1183/09031936.00150414.
Evidence tables
Evidence table for systematic review of RCTs and observational studies (intervention studies)
Research question: lungvolume reduction
Evidence table for intervention studies (randomized controlled trials and non-randomized observational studies (cohort studies, case-control studies, case series))
Research question: longvolume reduction
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Criner, 2019 |
Type of study: prospective, multicenter, open-label, randomized, controlled Trial (EMPROVE)
Setting and country: Between October 2013 and May 2017; 41 investigational sites in USA and Canada
Funding and conflicts of interest: supported by Spiration Inc. d.b.a. Olympus Respiratory America funding of the EMPROVE trial. Spiration Inc. d.b.a. Olympus Respiratory America helped with trial design and review and clarification of the methods of the manuscript. |
Inclusion criteria: 40 years of age or older, met ATS/ERS criteria for management of stable COPD; were able to perform 6MWT >140 m; >40% emphysema destruction in the target lobe (assessed at 2920 Hounsfield units) and a >10% disease emphysema severity difference with the ipsilateral lobe. The target and ipsilateral lobes were required to be separated by an intact fissure, estimated visually to be >90% complete with no segmental vessels crossing between adjacent lobes; FEV1 <45% of pred, after bronchodilators; TLC >100%; RV >150% of pred
Exclusion criteria: not mentioned
N total at baseline: Intervention: 113 Control: 59
Important prognostic factors2: For example age ± SD: I: 66.7 ± 6.6 C: 86.1 ± 6.4
Sex: I: 47.8% M C: 64.4% M
Groups comparable at baseline? yes
|
Describe intervention (treatment/procedure/test): Bronchoscopic placement of Spiration Valve System
|
Describe control (treatment/procedure/test): Optimal medical management
|
Length of follow-up: 6 months
Loss-to-follow-up: Intervention: N 17 (15%) Reasons: 10 died, 6 missed visit, 1 withdrew Control: N 16 (17%) Reasons: 4 died, 2 missed visits, 10 withdrew
Incomplete outcome data: unknown
|
Outcome measures and effect size (include 95%CI and p-value if available):
FEV1 (change from baseline to 12 mo ± SD) I: 0.067L ± 0.167 (N = 86) C: -0.032L ± 0.114 (N = 39) Between group difference: 0.088L (95% CI 0.037 to 0.137)
RV (% change from baseline to 6 mo ± SD) I: -0.402L ± 0.85 (N = 105) C: -0.042L ± 0.58 (N = 50) Between group difference: -0.361 (95% CI -0.59 to 20.13)
SGRQ (change from baseline to 6 mo) I: -8.1 ± 17.1 (N = 105) C: 4.8 ± 10.6 (N = 50) Between group difference: -13.0 (95% CI -17.4 to 28.5)
6MWT (change from baseline to 6 mo ± SD) I: -4.4 ± 76.7 (N = 102) C: -11.3 ± 51.4 (N = 48) Between group difference: 6.9 (95% CI -14.2 to 28.2)
SGRQ (change from baseline to 12 mo ± SD) I: -5.8 ± 16.8 (N = 95) C: 3.7 ± 10.9 (N = 41) Between group difference: -9.5 (95% CI -14.4 to -4.7)
thoracic SAEs (0-6 mo ± SD) I: 31.0 %± ? (N = 35/113 ) C: 11.9% ± ? (N = 7/59 ) Between group difference: 19.1% (95% CI 5.9 to 29.7)
Mortality 0-6 mo I: 5.3% ± ? (N = 6/113) C: 1.7% ± ? (N = 1/59) Between group difference: 3.6 (95% CI -3.9 to 8.9)
|
Author’s conclusion: In patients with severe heterogeneous emphysema, the SVS shows significant improvement in multiple efficacy outcomes, with an acceptable safety profile. |
|
Li, 2019 |
Type of study: multicenter, prospective, unblinded, randomized, parallel assignment, controlled Trial (REACH trial)
Setting and country: 12 clinical sites in China, year?
Funding and conflicts of interest: Nanshan Zhong has no conflict of interest to disclose. Herth MD has acted in a consultant capacity for Spiration Inc./Olympus Respiratory America. All other coauthors have no conflicts of interest to disclose. Spiration Inc./Olympus Respiratory America funded the REACH trial. Spiration was involved in the design of the study. N. Zhong, S. Li, and G. Wang had full access to all the data. N. Zhong had final responsibility to submit the paper for publication. |
Inclusion criteria: Patients with severe dyspnea mMRC scale: 2, severe airflow obstruction (post- FEV1 ≤ 45%), hyperinflation (TLC ≥100% and RV ≥150%); HRCT inclusion criteria: a highly diseased target lobe (≥40% emphysema involvement), high heterogeneity compared to the ipsilateral lobe (≥15% difference), and an intact interlobar fissure (≥90% complete). Visual assessment of HRCT imaging was independently evaluated by both the lead clinical site and a core laboratory (MedQIA, Los Angeles, CA, USA). Screening/baseline CT imaging from all sites was assessed by these same two reviewers to ensure consistency across the study sites. Any reviewer disagreement was arbitrated with the aid of quantitative CT (QCT) software
Exclusion criteria: not mentioned
N total at baseline: Intervention: 72 Control: 35
Important prognostic factors2: age ± SD: I: 63.5±6.7 C: 62.4±6.9
Sex: I: 100% M C: 97% M
Groups comparable at baseline? Yes
|
Describe intervention (treatment/procedure/test): Spiration valve system and standard medical care
|
Describe control (treatment/procedure/test): Standard medical care
|
Length of follow-up: 12 months (primary endpoint: 3 months)
Loss-to-follow-up: Intervention: N=9 Reasons (describe) Withdrew upon randomization (N=5) Procedure aborted due to tumor discovery (N=1) Subject withdrew due to AE (N=3)
Control: N=3 (8.6%) Reasons (describe) Withdrew upon randomization (N=2) Subject died (N=1)
Incomplete outcome data: Intervention: N=9 Reasons (describe) Subject did not attend visit (N=9) (data imputed)
Control: N=6 Reasons (describe) Subject did not attend visit (N=6) data imputed
|
Outcome measures and effect size (include 95%CI and p-value if available):
FEV1 change from baseline to– 6 mo I: 0.091 ± 0.156 (N = 63) C: –0.024 ± 0.142 (N = 33) P < 0.001
RV (change from baseline to 6 mo) I: –0.42 ± 1.84 (N = 63) C: –0.05 ± 1.33 (N = 33) P 0.114
6MWT (change from baseline to 6 mo) I: 20.82 ± 86.65 (N = 63) C: –15.58 ± 71.91 (N = 33) P 0.042
SGRQ (change from baseline to 6 mo) I: –8.39 ± 17.43 (N = 63) C: 2.11 ± 17.24 (N = 32) P 0.007
Total SAEs (baseline to 6 mo) I: 22 in 66 patients C: 8 in 33 patients
Mortality 0-6 mo I: 0 in 66 patients) C: 1 in 33 patients |
Authors conclusion: The SVS represents a novel approach for the treatment of severe emphysema with a clinically acceptable risk-benefit profile.
|
Notes:
- Prognostic balance between treatment groups is usually guaranteed in randomized studies, but non-randomized (observational) studies require matching of patients between treatment groups (case-control studies) or multivariate adjustment for prognostic factors (confounders) (cohort studies); the evidence table should contain sufficient details on these procedures
- Provide data per treatment group on the most important prognostic factors ((potential) confounders)
- For case-control studies, provide sufficient detail on the procedure used to match cases and controls
- For cohort studies, provide sufficient detail on the (multivariate) analyses used to adjust for (potential) confounders
Risk of bias tables
Table of quality assessment for systematic reviews of RCTs and observational studies
Research question lung volume reduction
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Van Geffen, 2019 |
Yes |
Yes Medline and Embase were searched
|
Yes |
Yes Most important characteristics were described. However, mean age was missing |
Not applicable |
Yes Risk of bias was assessed using the Cochrane risk of bias tool for randomised controlled trials. Major flaw with most of the studies was the non-blinding of participants (performance bias) and investigators (detection bias), Four of the 18 datasets had a slightly higher loss to follow-up in the intervention than control arms, and have therefore been deemed to be of uncertain quality for attrition bias. No other bias was found in the reported studies. No specific bias was detected across studies. |
Yes I2 was used for assessing heterogeneity |
Yes Publication bias was assessed in a funnel plot |
No Source of funding was only reported for the systematic review (no funding) |
Risk of bias table for intervention studies (randomized controlled trials)
Research question: lung volume reduction
|
Study reference
(first author, publication year) |
Was the allocation sequence adequately generated? a
Definitely yes Probably yes Probably no Definitely no |
Was the allocation adequately concealed?b
Definitely yes Probably yes Probably no Definitely no |
Blinding: Was knowledge of the allocated interventions adequately prevented?c
Were patients blinded?
Were healthcare providers blinded?
Were data collectors blinded?
Were outcome assessors blinded?
Were data analysts blinded?
Definitely yes Probably yes Probably no Definitely no |
Was loss to follow-up (missing outcome data) infrequent?d
Definitely yes Probably yes Probably no Definitely no |
Are reports of the study free of selective outcome reporting?e
Definitely yes Probably yes Probably no Definitely no |
Was the study apparently free of other problems that could put it at a risk of bias?f
Definitely yes Probably yes Probably no Definitely no |
Overall risk of bias If applicable/necessary, per outcome measureg
LOW Some concerns HIGH
|
|
Criner, 2019 |
Definitely yes;
Reason: Randomization occurred within the electronic data capture system using a blocked randomization scheme with blocks of randomly varying sizes |
Definitely yes;
Reason: Randomization occurred within the electronic data capture system using a blocked randomization scheme with blocks of randomly varying sizes |
Definitely no;
Reason: only the treatment group underwent bronchoscopy |
Probably yes;
Reason: : imputation methods were used |
Definitely yes;
Reason: all relevant outcomes were reported |
No information
|
LOW (FEV1; RV; mortality) Some concerns: 6MWT, AEs HIGH (QoL.)
|
|
LI, 2020
|
Definitely yes;
Reason: a computer-generated randomization schema with a random permuted block size of 6 stratified by site was created by an independent group |
Definitely yes;
Reason: stratification was created by an independent group, was assigned study wide, |
Definitely no;
Reason: the study was unblinded |
Definitely yes;
Reason: Loss to follow up is comparable in intervention and control group, imputation methods were used |
Definitely yes;
Reason: all relevant outcomes were reported |
No information(Criner et al. 2019) |
LOW (FEV1; RV; mortality) Some concerns: 6MWT, AEs HIGH (QoL. )
|
- Randomization: generation of allocation sequences have to be unpredictable, for example computer generated random-numbers or drawing lots or envelopes. Examples of inadequate procedures are generation of allocation sequences by alternation, according to case record number, date of birth or date of admission.
- Allocation concealment: refers to the protection (blinding) of the randomization process. Concealment of allocation sequences is adequate if patients and enrolling investigators cannot foresee assignment, for example central randomization (performed at a site remote from trial location). Inadequate procedures are all procedures based on inadequate randomization procedures or open allocation schedules..
- Blinding: neither the patient nor the care provider (attending physician) knows which patient is getting the special treatment. Blinding is sometimes impossible, for example when comparing surgical with non-surgical treatments, but this should not affect the risk of bias judgement. Blinding of those assessing and collecting outcomes prevents that the knowledge of patient assignment influences the process of outcome assessment or data collection (detection or information bias). If a study has hard (objective) outcome measures, like death, blinding of outcome assessment is usually not necessary. If a study has “soft” (subjective) outcome measures, like the assessment of an X-ray, blinding of outcome assessment is necessary. Finally, data analysts should be blinded to patient assignment to prevents that knowledge of patient assignment influences data analysis.
- If the percentage of patients lost to follow-up or the percentage of missing outcome data is large, or differs between treatment groups, or the reasons for loss to follow-up or missing outcome data differ between treatment groups, bias is likely unless the proportion of missing outcomes compared with observed event risk is not enough to have an important impact on the intervention effect estimate or appropriate imputation methods have been used.
- Results of all predefined outcome measures should be reported; if the protocol is available (in publication or trial registry), then outcomes in the protocol and published report can be compared; if not, outcomes listed in the methods section of an article can be compared with those whose results are reported.
- Problems may include: a potential source of bias related to the specific study design used (e.g. lead-time bias or survivor bias); trial stopped early due to some data-dependent process (including formal stopping rules); relevant baseline imbalance between intervention groups; claims of fraudulent behavior; deviations from intention-to-treat (ITT) analysis; (the role of the) funding body. Note: The principles of an ITT analysis implies that (a) participants are kept in the intervention groups to which they were randomized, regardless of the intervention they actually received, (b) outcome data are measured on all participants, and (c) all randomized participants are included in the analysis.
- Overall judgement of risk of bias per study and per outcome measure, including predicted direction of bias (e.g. favors experimental, or favors comparator). Note: the decision to downgrade the certainty of the evidence for a particular outcome measure is taken based on the body of evidence, i.e. considering potential bias and its impact on the certainty of the evidence in all included studies reporting on the outcome.
Beoordelingsdatum en geldigheid
Publicatiedatum : 15-09-2023
Beoordeeld op geldigheid : 31-08-2023
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2020 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met COPD.
Samenstelling van de werkgroep
Werkgroep
- Dr. F. (Folkert) Brijker, longarts, werkzaam in het Spaarne Gasthuis te Haarlem, NVALT (voorzitter, vanaf oktober 2022)
- Dr. J.S. (Jaring) van der Zee, longarts, NVALT (voorzitter, tot oktober 2022)
- Dr. W.H. (Wouter) van Geffen, longarts, werkzaam in het Medisch Centrum Leeuwarden te Leeuwarden, NVALT
- Drs. R. (Renée) van Snippenburg, werkzaam bij Ksyos en waarnemend longarts, NVALT
- Dr. J.C.C.M. (Hans) in ’t Veen, longarts, werkzaam in het Franciscus Gasthuis & Vlietland te Rotterdam, NVALT
- M. (Moniek) Wouters, longarts, werkzaam in het Ziekenhuis Gelderse Vallei te Arnhem, NVALT
- Prof. H.A.M. (Huib) Kerstjens, hoogleraar longziekten, longarts, werkzaam in het UMCG te Groningen, NVALT (vanaf oktober 2022)
- J. (Jeanine) Antons, longarts, werkzaam in het RadboudUMC te Nijmegen, NVALT (vanaf oktober 2022)
- Drs C.L.Y. (Chantal) Knoops, AIOS longgeneeskunde, werkzaam in het Catharina Ziekenhuis te Eindhoven (vanaf oktober 2022)
- Prof. J.W.M. (Jean) Muris, huisarts, werkzaam bij de Universiteit Maastricht, lid van de NHG-Expertgroep CAHAG, NHG
- Drs. E.R. (Erik) van der Meijs, apotheker, KNMP
- W.J.M. (Walter) van Litsenburg, verpleegkundig specialist longgeneeskunde, Catharina Ziekenhuis te Eindhoven, V&VN
- Dr. M.J.H. (Maurice) Sillen, fysiotherapeut, werkzaam bij CIRO, KNGF
- R.A. (Renée) Kool, projectleider, Longfonds
- R. (Ramona) Leysner, diëtiste, Nederlandse Vereniging van Diëtisten (NVD)
- Drs. M. (Menno) Wagenaar, patiëntvertegenwoordiger, Longfonds
- J. (Johan) Smit, patiëntvertegenwoordiger, Longfonds
Met ondersteuning van
- Dr. M. (Margriet) Moret, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Drs. N. (Nicole) Verheijen, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten en longarts
- Dr. T. (Tim) Christen, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Inbreng patiëntenperspectief
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Brijker (voorzitter, vanaf oktober 2022) |
Longarts Spaarne Gasthuis |
Voorzitter sectie COPD NVALT. Dit is een onbetaalde functie binnen de longartsenvereniging NVALT. Lid regionale kwaliteitscommissie COPD/astma. Deze Commissie heeft 2x per jaar vergadering a 2 uur per keer in de avonduren en hiervoor ontvang ik onkostenvergoeding. Docent CASPIR cursussen. dit betreft scholing voor spirometrie voor huisartsen en POH-ers in de regio. Dit vindt een aantal keer per jaar plaats (<5 keer) in de avonduren en hiervoor ontvang ik een onkostenvergoeding |
Geen |
Geen |
|
*Van der Zee (voorzitter, tot oktober 2022) |
Longarts OLVG Amsterdam 0,2FTE tot 1-1-2020 Longarts Amsterdam UMC, locatie AMC, 0,2 FTE |
Lid MEC-U Locatie Nieuwegein, onkosten vergoeding Lid Gezondheidsraad Commissie Gespoten PUR, onkosten vergoeding Incidenteel medische expertises (o.a. DAS, ARAG, Triage, de Rechtspraak), betaald 2019 Speakers fee, Astra-Zeneca, Novartis, Chiesi 2019 1x Ad hoc Advies m.b.t. biologicals bij astma, GSK, betaald |
Geen |
Geen advieswerk tijdens het richtlijnontwikkeltraject |
|
Van Geffen |
Longarts Medisch Centrum Leeuwarden, maatschap Friese Longartsen |
Editorial board Cochrane Airways: Onbetaald Commisie Bronkhorst Nvalt: Onbetaald Richtlijn Commissie NVALT NSCLC: Onbetaald |
Deelname aan een investigator initiated onderzoek firma Novartis. financiering is overgemaakt aan UMCG (2017 beëindigd). Voor de bedrijven Chiesi, Roche, Boehringer en AstraZeneca deelname aan adviesraden betreffende oncologie. Deze gingen niet over COPD of biologicals. De hiervoor gebruikelijke CGR vergoeding werd geweigerd. Chiesi en Boehringer waren wel COPD, maar niet in de laatste 1.5 jaar. |
Geen advieswerk op gebied van COPD of biologicals tijdens het richtlijnontwikkeltraject |
|
In 't Veen |
Longarts bij In 't Veen Longarts BV. Verbonden aan de vakgroep longziekten en STZ expertisecentrum Astma, COPD & Respiratoire Allergie van het Franciscus Gasthuis en Vlietland, Rotterdam. |
Onbetaald: Opleider longziekten Franciscus Gasthuis en Vlietland Lid Concilium Opleiding NVALT Lid Vrij Ademen Akkoord namens NVALT Betrokken longarts bij Schone Lucht Akkoord Lid Move2Improve Lid werkgroep Ziektelastmeter; Generiek en COPD (afgerond) Voorzitter StichtingRoLeX (Rotterdam Leeuwarden eXpertise voor obstructieve longzieken), een stichting die nascholing voor longartsen (i.o.) verzorgd. Bestuurslid LAN Betaald: Longfunctiebeoordelaar Huisartsenlaboratorium STAR-SHL NHG richtlijn COPD namens NVALT Adviseurschap m.b.t. astma: Sanofi, GSK, Boehringer Ingelheim, Chiesi. (laatste 2 jaar (datum invullen 30-6-19) geen persoonlijke betrokkenhied als adviseur bij COPD gerelateerde issues, mede vanwege mijn betrokkenheid bij de NHG richtlijn). Speakers Bureau: Chiesie, Novartis, Boehringer Ingelheim, Inhalatie Technologie Werkgroep Health Agency Stichting RoLeX Sanofi |
Ik beoordeel longfuncties voor een huisarts laboratorium, en heb adviseurschap verricht voor diverse farmaceutische firma's. Er is nooit advies gegeven door mij over medicamenteuze COPD-behandeling, ook niet over biologicals. het genoemde adviseurschap is inmiddels meer dan 3-4 jaar geleden beëindigd. Zie eerder. Research faculty grants, (subsidiegevers Boehringer, Chiesi, Teva, Franciscus wetenschapsbureau) m.b.t. onderzoek bij astma en COPD, via ons expertisecentrum. Van belang hierbij is dat al het onderzoek niet medicatie-gerelateerd is. Zie boven bij onbetaald: Ik ben betrokken bij de bevordering van luchtkwaliteit en als zodanig word ik af en toe geconsulteerd met betrekking tot het schone Lucht Akkoord, een nationaal (door de overheid in gang gezet) platform dat maatregelen hierover in kaart brengt. Voorts ben ik betrokken bij het Vrij Ademen Akkoord, dat oa vanuit LAN, Longfonds, NRS en NVALT aandacht vraagt voor de (toekomstige) patient met een longziekte. |
Geen advieswerk over COPD of biologicals tijdens ontwikkeltraject van de richtlijn. Geen uitwerking van uitgangsvragen over longmedicatie of biologicals. |
|
Van Snippenburg |
Waarnemend Longarts; |
Secretaris Sectie COPD NVALT, onbetaald Werkgroep longen Huisartsen Utrecht Stad, betaald
|
Geen |
Geen |
|
Antons (vanaf oktober 2022) |
Longarts Radboudumc, Nijmegen |
Geen |
Geen |
Geen |
|
Kerstjens (vanaf oktober 2022) |
Hoogleraar longziekten UMCG, 1,0 FTE |
"Voorzitter Noordelijke CARA Stichting. Subsidiegevend orgaan. Onbetaald - Lid RvT bureau bijwerkingen geneesmiddelen LAREB. Betaald aan UMCG - Vz Stichting BEBO. Onafhankelijke METc. Betaald aan UMCG (per 1-1-2023 vz) - Vice-vz Netherlands Respiratory Society. Stichting ter bevordering van wetenschap en wetenschapsklimaat Longziekten NL. Onbetaald. (per 1-1-2023 vz).
Op afroep (geen vaste contracten of afspraken) deelname aan adviesraden van farmaceutische industrieën, en betaling voor lezingen: AstraZeneca, Boehringer Ingelheim, Chiesi, GSK, Novartis. Alles betaald aan UMCG." |
"Geen persoonlijk financieel belang; alles wat er door mij binnenkomt wordt betaald aan UMCG. En krijg ik ook in tweede instantie nooit wat van. 2. Geen dienstverband 3. Betaald adviseurschappen zie bij overige item over nevenwerkzaamheden voor AstraZeneca, Boehringer Ingelheim, Chiesi, GSK, Novartis. 4. Geen directe fianicee belangen of via aandelen of opties. 5. Geen patenten"
"Veel gesponsord onderzoek, o.a. ZonMW VWS Innovatiefonds verzekeraars Industrie: AstraZeneca, Boehringer Ingelheim, Chiesi, GSK, Novartis." |
restricties ten aanzien van besluitvorming met betrekking tot modules over medicatie |
|
Knoops (vanaf oktober 2022) |
AIOS longziekten, Catharina Ziekenhuis Eindhoven |
Geen |
Geen |
Geen |
|
Tazmi (tot oktober 2020) |
Verpleegkundig specialist - werkzaam bij Laurens locatie Intermezzo |
Geen |
Geen |
Geen |
|
Van Jaarsveld |
Adviseur Zorg bij Longfonds |
Geen |
Geen |
Geen |
|
Muris |
Hoogleraar huisartsgeneeskunde, Universiteit Maastricht |
Vervangende werkzaamheden huisartspraktijk Geulle (betaald) |
Geen |
Geen |
|
Van der Meijs |
Apotheker, sinds 1 februari niet meer praktiserend lid namens de KNMP |
SIG-long (SIG = specialist interest group) van KNMP – vacatiegeld |
Geen |
Geen |
|
Van Litsenburg (vanaf oktober 2020) |
Verpleegkundig specialist astma en COPD 36 uur per week 24-uurs thuiszorgverpleegkundige 24 uur per week |
Bestuurslid IMIS (inhalatiemedicatie instructie school) 2u per week Coördinator IMIS Zuid Nederland IMIS trainer Docent Hogeschool Arnhem en Nijmegen Kernteam Picasso voor COPD (momenteel niet actief) Werkgroeplid palliatieve richtlijn COPD |
Kernteamlid Picasso (niet actief) |
Geen |
|
Leysner |
dietist Merem medische revalidatie in Hilversum" |
Incidenteel scholing geven aan studenten hogeschool Holland; betaald |
Geen |
Geen |
|
Wouters |
Bij aanvang AIOS longziekten, Rijnstate Ziekenhuis en thans longarts Ziekenhuis Gelderse Vallei Ede |
Geen |
Geen |
Geen |
|
Wagenaar |
Longervaringsdeskundige bij het Longfonds Geen betaalde functies |
Geen |
Geen |
Geen |
|
Kool |
Projectleider Zorgveld, Longfonds |
Geen |
Geen |
Geen |
|
Sillen |
Resultaatverantwoordelijk fysiotherapeut CIRO+, expertisecentrum voor chronisch orgaanfalen Horn |
Bestuurslid Vereniging voor Hart-, Vaat- en Longfysiotherapie (vacatievergoeding) Extern adviseur Fontys Hogeschool Eindhoven (betaald) Gastdocent Saxion Hogeschool, Enschede en Hogeschool van Amsterdam (betaald) |
Geen |
Geen |
|
Smit |
Longervaringsdeskundige Longfonds (vrijwilligerswerk) |
Geen |
Geen |
Geen |
Implementatie
Er werd aandacht besteed aan het patiëntenperspectief doordat een afgevaardigde patiëntenvereniging zitting nam in de werkgroep. De inbreng van de afgevaardigden is tevens verwerkt in de verslagen hiervan. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan het Longfonds en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerden de werkgroep de knelpunten in de zorg voor patiënten met COPD. De werkgroep beoordeelde de aanbevelingen uit de eerdere richtlijn (NVALT, 2010) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door de NVALT, V&VN Longverpleegkundigen, het Longfonds, NHG, NAPA en KNMP via een invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
De werkgroep heeft uitgebreid over de belangrijkste uitkomstmaten voor de te bespreken interventies gediscussieerd. Het werd wenselijk geacht de set uitkomsten over de verschillende modules waar mogelijk hetzelfde te houden, en zeker met de zelfde minimale klinisch relevante verschillen. Bij specifieke interventies werden soms specifieke relevante uitkomsten toegevoegd. Voor sommige parameters kon geen referentie gevonden worden en werd als onderstaand beschreven een consensus standpunt ingenomen. De werkgroep onderkent dat de absolute risico reductie klinisch beter interpretabel is dan de relatieve, maar kon voor onvoldoende studies die getallen er bij vinden en hield dus vast aan de relatieve risico’s, met toelichting waar mogelijk.
• Exacerbation reduction: ≥20% (Jones, 2014; Chapman 2013)
• Pneumonia: ≥20% difference in relative risk
• Hospital admissions: ≥20% difference in relative risk
• Mortality: ≥10% difference in relative risk
• SGRQ-score: ≥4 units (Jones, 2014)
• CAT-score: >2 units (Kon 2014)
• CCQ-score: >0.4 units
• FEV1: >100 ml (Donohue 2005; Jones, 2014)
• Adverse events: ≥25% difference in relative risk
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur en de beoordeling van de risk-of-bias van de individuele studies is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/) De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
Definitie |
|
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE-methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming blijkt dat er waarschijnlijk geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
|
Module |
Uitkomst kwalitatieve raming |
Toelichting |
|
Module 1.1 Gebruik van inhalatiecorticosteroïden (ICS) bij COPD |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar is (>40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 1.2 Triple therapie in 1 vs in meerdere devices bij COPD |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar is (>40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 1.3 Onderhoudsantibiotica bij COPD
|
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 1.4 Poliklinische behandeling van een COPD-longaanval |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar is (>40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 1.5 Biologicals bij COPD |
Geen substantiële financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten) en zal daarom naar verwachting geen substantiële financiële gevolgen hebben voor de collectieve uitgaven
|
|
Module 2.1 Fysiotherapie in de eerste lijn
|
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 2.2 tweede en derdelijnsrevalidatie bij COPD
|
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 2.3 Voeding bij COPD
|
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar is (>40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 3.1 Zuurstoftherapie bij COPD
|
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar is (>40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 3.2 Longvolumereductie |
geen substantiële financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten) en zal daarom naar verwachting geen substantiële financiële gevolgen hebben voor de collectieve uitgaven.
|
|
Module 3.3 Chronische beademing bij COPD
|
n.v.t. |
Verwijzing naar andere richtlijn |
|
Module 4 COPD zelfmanagement
|
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt ook uit de toetsing het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht.
|
|
Module 5 E-health
|
Geen substantiële financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten) en dat het een nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Het inzetten van digitale zorgtoepassingen zal zijn georganiseerd op lokaal/regionaal niveau en daarom worden op landelijk niveau geen substantiële financiële gevolgen verwacht.
|
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Chapman KR, Bergeron C, Bhutani M, et al. Do we know the minimal clinically important
difference (MCID) for COPD exacerbations? COPD 2013;10(2):243-9.
DOI:10.3109/15412555.2012.733463.
Donohue JF. Minimal clinically important differences in COPD lung function. COPD
2005;2(1):111-124. (http://www.ncbi.nlm.nih.gov/pubmed/17136971).
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Jones PW, Beeh KM, Chapman KR, Decramer M, Mahler DA, Wedzicha JA. Minimal clinically
important differences in pharmacological trials. Am J Respir Crit Care Med
2014;189(3):250-5. DOI: 10.1164/rccm.201310-1863PP.
Kon SS, Canavan JL, Jones SE, et al. Minimum clinically important difference for the COPD
Assessment Test: a prospective analysis. Lancet Respir Med 2014;2(3):195-203. DOI:
10.1016/S2213-2600(14)70001-3.
Kocks JW, Tuinenga MG, Uil SM, van den Berg JW, Stahl E, van der Molen T. Health status
measurement in COPD: the minimal clinically important difference of the Clinical
COPD Questionnaire. Respir Res 2006;7(1):62.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, Glasziou P, Jaeschke R, Vist GE, Williams JW Jr, Kunz R, Craig J, Montori VM, Bossuyt P, Guyatt GH; GRADE Working Group. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008 May 17;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008 May 24;336(7654). doi: 10.1136/bmj.a139.
Schünemann, A Holger J (corrected to Schünemann, Holger J). PubMed PMID: 18483053; PubMed Central PMCID: PMC2386626.
Wessels M, Hielkema L, van der Weijden T. How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. J Med Libr Assoc. 2016 Oct;104(4):320-324. PubMed PMID: 27822157; PubMed Central PMCID: PMC5079497.
Zoekverantwoording
Table of excluded studies
|
Author and year |
Reason for exclusion |
|
|
Dransfield |
2020 |
uses post hoc data of LIBERATE trial (Criner 2018) |
|
Garner |
2020 |
wrong population |
|
Hartman |
2018 |
does not fit PICO |
Literature search strategy
Algemene informatie
|
Richtlijn: Herziening COPD |
|
|
Uitgangsvraag: Welke COPD-patiënten komen in aanmerking voor een longvolumereductie behandeling?
|
|
|
Database(s): Ovid/Medline, Embase |
Datum:5-5-2021 |
|
Periode: 2018- |
Talen: nvt |
|
Literatuurspecialist: Ingeborg van Dusseldorp |
|
|
BMI zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Bij gebruikmaking van een volledig zoekblok zal naar de betreffende link op de website worden verwezen. |
|
|
Toelichting: Deze vraag is een update van de volgende SR: Surgical and endoscopic interventions that reduce lung volume for emphysema: a systemic review and meta-analysis van Geffen W.H., Slebos D.-J., Herth F.J., Kemp S.V., Weder W., Shah P.L. The Lancet Respiratory Medicine (2019) 7:4 (313-324). Date of Publication: 1 Apr 2019
Er is gezocht met de volgende elementen:
COPD EN longvolumereductie
|
|
|
Te gebruiken voor richtlijnen tekst: In de databases Embase en Ovid/Medline is op 2021 met relevante zoektermen gezocht naar systematische reviews, RCTs en observationele studies over (uitgangsvraag). De literatuurzoekactie leverde … unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SRs |
41 |
17 |
41 |
|
RCTs |
124 |
68 |
128 |
|
Observationele studies |
|
|
|
|
Overig |
|
|
|
|
Totaal |
|
|
169 |
Zoekstrategie
Embase
|
No. |
Query |
Results |
|
#71 |
#70 NOT #69 |
104 |
|
#70 |
#66 AND #68 |
124 |
|
#69 |
#66 AND #67 |
41 |
|
#68 |
('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it |
2557886 |
|
#67 |
('meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) NOT ('conference abstract'/it OR 'conference review'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) |
557459 |
|
#66 |
#65 AND (1-5-2018)/sd NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
555 |
|
#65 |
#63 AND #64 |
5104 |
|
#64 |
'lung resection'/exp OR 'endobronchial valve'/exp OR 'endobronchial coil'/exp OR 'lung volume reduction*':ab,ti,kw OR (((bronchoscop* OR endobronchial OR intrabronchial) NEAR/3 (intervention* OR valve* OR coil* OR stent*)):ti,ab,kw) OR aeriseal*:ab,ti,kw OR 'lung resection':ti,ab,kw OR 'pneumectomy':ti,ab,kw OR 'pneumonectomy':ti,ab,kw OR 'pneumonic resection':ti,ab,kw OR 'pneumoresection':ti,ab,kw OR 'pulmonary resection':ti,ab,kw OR 'pulmonectomy':ti,ab,kw OR 'resected lung':ti,ab,kw OR zephyr:ti,ab,kw OR spiration:ti,ab,kw OR 'airway sizing kit':ti,ab,kw |
48242 |
|
#63 |
'chronic obstructive lung disease'/exp OR ('chronic obstructive' NEAR/2 (lung OR pulmonary OR airway)) OR 'copd':ab,ti,kw OR 'chronic bronchitis':ab,ti,kw OR emphysem*:ab,ti,kw OR aecopd:ti,ab,kw |
210269 |
Ovid/Medline
|
# |
Searches |
Results |
|
9 |
5 and 7 |
68 |
|
8 |
5 and 6 |
17 |
|
7 |
(exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) |
2113580 |
|
6 |
(meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf.) not (comment/ or editorial/ or letter/ or ((exp animals/ or exp models, animal/) not humans/)) |
494009 |
|
5 |
4 not ((exp animals/ or exp models, animal/) not humans/) not (letter/ or comment/ or editorial/) |
274 |
|
4 |
limit 3 to yr="2018 -Current" |
302 |
|
3 |
1 and 2 |
1995 |
|
2 |
(lung volume reduction* or ((bronchoscop* or endobronchial or intrabronchial) adj3 (intervention* or valve* or coil* or stent*)) or aeriseal* or lung resection or pneumectomy or pneumonectomy or pneumonic resection or pneumoresection or pulmonary resection or pulmonectomy or resected lung or zephyr or spiration or airway sizing kit).ti,ab,kf. |
22093 |
|
1 |
exp Pulmonary Disease, Chronic Obstructive/ or ('chronic obstructive' adj2 (lung or pulmonary or airway)).ab,ti,kf. or copd.ab,ti,kf. |
92249 |