Behandeling met foto(chemo)therapie CE
Uitgangsvraag
Is er plaats voor foto(chemo)therapie in de behandeling van CE?
Aanbeveling
Fototherapie kan worden toegepast indien lokale therapieën onvoldoende effect hebben.
De effectiviteit van NB-UVB-therapie wordt momenteel (vanaf feb 2023) onderzocht in een Nederlandse multicenter trial. Breng uw patiënt op de hoogte van deze studie. Zie voor meer informatie https://www.zorgevaluatienederland.nl/evaluations/update
Fototherapie zou moeten worden toegepast onder verantwoordelijkheid van een ervaren behandelaar.
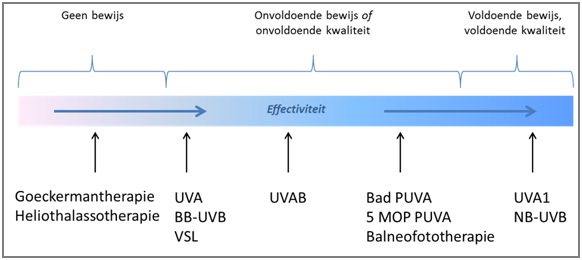
Op basis van beperkt onderzoek verdienen NB-UVB en (cold light) UVA1 de voorkeur. Vanwege de betere beschikbaarheid, de mindere warmte ontwikkeling en de minder tijds- en arbeidsintensiteit beveelt de werkgroep NB-UVB aan boven UVA1.
5-MOP PUVA, bad PUVA en balneofototherapie lijken niet minder effectief te zijn, maar voldoende kwalitatief goede studies ontbreken. UVAB is minder effectief dan UVA1.
Voor BB-UVA, BB-UVB en VSL bestaat onvoldoende bewijs van goede kwaliteit en deze vormen van fototherapie kunnen daarom niet worden aanbevolen in de behandeling van CE.
Bij de behandeling van kinderen met CE is er onvoldoende evidence voor een goed effect van fototherapie.
Overwegingen
Fototherapie is door regelmatige ziekenhuisbezoeken belastend voor de patiënt en vergt goede instructie en begeleiding. Om deze keuze voor deze belastende therapieën te ondersteunen is behoefte aan kwalitatieve studies van voldoende omvang (voldoende aantallen patiënten), voldoende kwaliteit en een goede duur met een ruime follow up periode. Helaas ontbreekt het hieraan voor de meeste soorten fototherapie. Daarnaast hebben veel studies het gebruik van topicale corticosteroïden toegestaan om het gebruik te meten als uitkomstmaat [Jekler 1990, Jekler 1988, Jekler 1991, Reynolds 2001, Jekler 1991, Valkova 2004, Granlund 2001]. Het totaal excluderen van topicale corticosteroïden zal waarschijnlijk niet vaak worden uitgevoerd in de praktijk, maar in klinische trials ziet men wel graag totale exclusie of een adequate en volledige monitoring van de gebruikte steroïden.
Van de relatief goed onderzochte UVA1 en NB-UVB therapie zijn de lange termijn effecten bij patiënten met CE nog onbekend. Daarnaast is UVA1 therapie slechts zeer beperkt beschikbaar in Nederland. UVA1 is bovendien erg tijds- en arbeidsintensief en gaat gepaard met meer warmteontwikkeling dan UVB therapie, hetgeen door sommige patiënten met CE als onprettig ervaren wordt. In het algemeen wordt van smalspectrum UVB therapie aangenomen dat deze relatief veilig zou zijn. Deze modaliteit is op vele plaatsen in Nederland voorhanden, de belichtingstijden zijn relatief kort en de warmteontwikkeling gering. Eventuele thuisbehandeling met UV voor CE zou nader onderzocht moeten worden.
Onderbouwing
Fototherapie is een van oudsher bekende therapie voor de behandeling van CE [Gambichler 2009]. Deze therapie wordt zowel voor de behandeling van acute exacerbaties als voor de behandeling van het chronisch eczeem toegepast bij volwassenen. In de behandeling van kinderen is men terughoudend in het gebruik van fototherapie.
De gedachte is dat de werking berust op verschillende factoren. Ten eerste kan fototherapie een verbetering van het huidbeeld geven door een immunosuppressieve actie te induceren met suppressie van de antigeen-presenterende functie van de Langerhanscellen en de inductie van apoptose in infiltrerende T cellen [Majoie 2009]. Daarnaast kan fototherapie leiden tot een reductie van de kolonisatie met Staphylococcus aureus en Pityrosporum orbiculare [Faergemann 1987, Ring 2012]. Ook een door fototherapie geïnduceerde toegenomen dikte van het stratum corneum zou door een gereduceerd antigeen presentatie leiden tot mildere eczeemklachten [Jekler 1990].
Verschillende typen van foto(chemo)therapie zijn beschreven: breedspectrum UVB (280-315 nm), smalspectrum UVB (311-313 nm, ook bekend als TL-01), breedband-UVA (BB-UVA) (315-400 nm), UVA1 (340-400 nm), cold light UVA1 (met een koelsysteem dat golflengten >530nm elimineert, resulterend in een lagere warmteproductie), UVAB (280-400 nm), volledig spectrum licht (VSL, 320-5000 nm, exclusief UVB maar inclusief UVA, zichtbaar licht en infrarood licht), zoutwater baden plus UVB (balneofototherapie), koolteer plus UVB licht (Goeckerman) en psoraleen plus UVA (PUVA) [Gambichler 2009, Meduri 2007, Scheinfeld 2003]. UVA1 fototherapie kan worden toegepast in hoge doseringen (High Dose (HD), 130J/cm2), matige doseringen (Medium Dose (MD), 50 J/cm2) en lage doseringen (Low Dose (LD), 10J/cm2). Behandeling met 308-nm monochromatic excimer licht en de pulsed-dye laser bij CE is ook beschreven [Ring 2012].
|
Niveau 1 |
UVA1 en NB-UVB zijn de meest en de best onderzochte fototherapie mogelijkheden voor de behandeling van CE. Beide therapieën zijn even effectief voor de reductie van CE volgens de SASSAD, LSS en SCORAD en voor de reductie van jeukklachten.
A1 Garritsen 2013 A2 Gambichler 2008, von Kobyletzki 1999 B Reynolds 2001, Majoie 2009, Krutmann 1992, Krutmann 1998, Legat 2003, Tzaneva 2001, Dittmar 2001 |
|
Niveau 2 |
Hoge doseringen UVA1 (130 J / cm2) hebben geen statistisch significant voordeel boven gemiddelde doseringen (50 J / cm2).
B Tzaneva 2001, Dittmar 2001 |
|
Niveau 2 |
Op basis van enkele individuele studies van wisselende kwaliteit zijn bad PUVA, 5-MOP PUVA en balneofototherapie niet minder effectief dan UVA1 en NB-UVB voor de reductie van de SCORAD.
A2 Heinlin 2011 B Der-Petrossian 2000, Tzaneva 2010 |
|
Niveau 2 |
Op basis van 3 studies is UVAB minder effectief dan UVA1 voor de reductie van de SCORAD en COSTA scores. A2 Von Kobyletzki 1999 |
|
Niveau 2 |
De resultaten van de studies naar BB-UVA, BB-UVB en VSL geven, gecombineerd met de matige kwaliteit en kleine omvang van deze studies, onvoldoende draagkracht om deze therapeutische opties te adviseren in de behandeling van CE. B Byun 2010, Jekler 1988, Jekler 1990, Jekler 1991, Jekler 1991, Reynolds 2001,Valkova 2004 |
|
Niveau 4 |
Gerandomiseerde onderzoeken met het focus op kinderen ontbreken , waardoor geen conclusies of adviezen gegeven kunnen worden over fototherapie bij kinderen. D Mening werkgroep |
|
Niveau 4 |
Op basis van de gerandomiseerde studies kan gezien de korte follow-up duur geen uitspraak worden gedaan over de kans op recidief na staken van de behandeling D Mening werkgroep |
Een totaal van 19 gerandomiseerde studies met 905 patiënten met CE werd geselecteerd voor data analyse. Daarnaast werden middels de aanvullende search nog 5 niet gerandomiseerde studies over balneofototherapie en heli thalassotherapie toegevoegd.
Ondanks de beschikbaarheid van vele ultraviolette behandelingen is het aantal gerandomiseerde studies per UV therapie voor CE gering en vaak van matige kwaliteit. Het betreft voornamelijk links-rechts vergelijkende studies uit het begin van de negentiger jaren, onder relatief kleine groepen patiënten (in de gerandomiseerde studies N= 9 tot 180, gemiddeld 47.63 patiënten) verricht in enkele onderzoekscentra (zie Evidence tabellen). De meeste studies zijn uitgevoerd met het relatief nieuwe UVA1.
Als primaire uitkomstmaten werd gekeken naar de klinische verschijnselen en symptomen (jeuk en verstoorde slaap) middels scoresystemen zoals de Leicester Sign Score (LSS) of de Scoring Atopic Dermatitis (SCORAD) [Finlay 1996, Task Force on Atopic Dermatitis, Schmitt 2012]. Secundaire uitkomstmaten waren kwaliteit van leven (zoals gemeten middels de Dermatology Life Quality Index [DLQI] of de Skindex-29), de gerapporteerde milde en serieuze bijwerkingen en de lange termijn controle van exacerbaties [Finlay 1994, Sampogna 2011].
Effectiviteit
Fototherapie versus placebo zichtbaar licht
Jekler et al. toonde in een links-rechts vergelijkende studie van 28 patiënten aan dat UVB statistisch significant beter is dan zichtbaar licht (beide 3 keer per week voor 8 weken) voor de reductie van de klinische scores en pruritus direct na de behandeling (p<0,001). In deze studie waren milde klasse topicale corticosteroïden toegestaan. De genoemde bijwerkingen waren mild en acceptabel. 13 patiënten ervaarden een gevoel van verbranding na de UVB therapie. In de placebo groep werd dit niet genoemd. Xerosis cutis werd in beide groepen een aantal malen genoemd, zonder statistisch significante verschillen tussen de groepen [Jekler 1988].
De studie van Reynolds et al. vergeleek Narrow Band-UVB (NB-UVB) (n=24) met placebo zichtbaar licht (n=22) en met BB-UVA (n=23). Zij concludeerden dat NB-UVB beter is dan zichtbaar licht (beide 2 keer per week voor 24 behandelingen) voor de reductie van de uitgebreidheid van het eczeem (daling van ~10 versus ~2) en de afname van pruritus (38% meer in NB-UVB) en slaapproblemen (35% meer in NB-UVB) direct na de behandeling. De uitgebreidheid van het eczeem blijft tevens lager in de NB-UVB groep na een follow up periode van 3 maanden. Er wordt niet vermeld of deze verschillen statistisch significant zijn. Zij zagen verder dat placebo zichtbaar licht beter was voor de reductie van de uitgebreidheid van het eczeem dan BB-UVA, maar dat BB-UVA beter was voor de reductie van jeukklachten (11% meer in BB-UVA) en slaapproblemen (16% meer in BB-UVA). Er wordt ook hiervan niet vermeld of deze verschillen statistisch significant zijn. Genoemde bijwerkingen zijn verbranding (1 NB-UVB, 1 placebo licht)en een exacerbatie van CE (1 NB-UVB, 2 BB-UVA en 1 placebo licht) [Reynolds 2001].
UVA(1) versus (NB / BB-)UVB fototherapie
Drie studies, 2 kleine links-rechts vergelijkende studies [Majoie 2009, Legat 2003] en een grotere cross-over studie [Gambichler 2008], hebben MD-UVA1 vergeleken met NB-UVB in een studieopzet van driemaal per week tot een duur van 8 weken. Er werden geen significante verschillen gezien voor de reductie van SASSAD, SCORAD, jeukklachten of de verbetering van de Skindex-29 direct na behandeling [Majoie 2009, Legat 2003, Gambichler 2008], of na een follow up periode van 4 weken [Majoie 2009]. NB-UVB was significant beter dan UVA1 voor de afname van de LSS in een studie (p=0,02) [Legat 2003], maar niet in de andere studie [Majoie 2009]. Mild erytheem werd gezien in 1 UVA1 patiënt [Gambichler 2008] en in 3 NB-UVB patiënten [Gambichler 2008].
Reynolds et al. vergeleken NB-UVB met BB-UVA (beide 2 keer per week voor 24 behandelingen) en toonden aan dat NB-UVB meer reductie geeft van jeukklachten (daling van 90% versus 63%) en slaapproblemen (daling van 71% versus 53%) direct na de behandeling. De uitgebreidheid blijft ook na een follow up periode van 3 maanden lager bij NB-UVB. Er werd niet vermeld of deze verschillende statistisch significant waren. Het gebruik van matige tot potente topicale corticosteroïden was in deze studie toegestaan. Genoemde bijwerkingen zijn verbranding (1 NB-UVB) en een exacerbatie van CE (1 NB-UVB, 2 BB-UVA) [Reynolds 2001].
Jekler et al. onderzochten de effectiviteit van BB-UVA versus BB-UVB, beide 3 keer per week voor 8 weken. Er werd significant meer verbetering van de klinische uitkomstparameters (p<0,01) en een significant grotere afname in de uitgebreidheid van CE (p<0,05) gezien met BB-UVA dan met BB-UVB. Er werd geen statistisch significant verschil gevonden in de verbetering van jeukklachten. De enige genoemde bijwerkingen zijn droogheid van de huid (8 UVA patiënten en 15 UVB patiënten) en verbranding (2 UVA en 13 UVB patiënten) [Jekler 1991].
BB-UVA en UVA1
Von Kobyletzky et al. vergeleek MD-UVA1 met cold light MD-UVA (beide 5 keer per week voor 3 weken) en zag een beter resultaat bij cold light MD-UVA1 voor de reductie van de SCORAD direct na behandeling. Ook na een follow up periode van 4 weken was de SCORAD in de cold light MD-UVA1 groep lager, maar er wordt niet vermeld of deze verschillende statistisch significant zijn [Von Kobyletzky 1999].
Een kleine links-rechts vergelijkende studie van Tzaneva et al. en een iets grotere studie van Dittmar et al. keken naar het effect van dosering van UVA1. Beide studies vonden geen statistisch significant verschil tussen MD-UVA1 en HD-UVA1 (beide 5 keer per week voor 3 weken) voor de afname van de SCORAD direct na behandeling en na een follow up periode oplopend tot 6 maanden. Er werden geen ernstige bijwerkingen, zoals eczema herpeticum, waargenomen. De enige gevonden bijwerkingen (aantallen onbekend) waren voorbijgaand erytheem en het gevoel van warmte [Tzaneva 2001, Dittmar 2001).
Krutmann et al. toonden aan dat HD-UVA1 statistisch significant beter is dan fluocortolone 0,5% crème (beide dagelijks gedurende 10 dagen) voor de afname van de COSTA score (eenvoudig scoringsysteem ontwikkeld door Costa en collegae) direct na de 10 daagse therapie (p<0,002) [Krutmann 1998].
Balneofototherapie en heli thalassotherapie
Balneofototherapie (zout water baden met NB-UVB) is volgens de goed uitgevoerde, gerandomiseerde, vergelijkende studie met 180 patiënten van Heinlin et al. statistisch significant beter dan alleen NB-UVB (beide 3 tot 5 keer per week tot 35 sessies) voor de reductie van SCORAD direct na de behandeling (p<0,004) of na een follow up periode van 6 maanden (p<0,04). Geen significante verschillen worden gezien voor de verbetering van de kwaliteit van leven (FLQA-d). Er werden 8 serieuze bijwerkingen waargenomen (2 balneofototherapie en 6 NB-UVB) die volgens de auteurs geen relatie hadden met de studie interventie. De meest voorkomende bijwerkingen die wél gerelateerd waren aan de studie therapieën waren erytheem (5,7% balneofototherapie, 2,2% NB-UVB) en licht dermatosen (2,3% balneofototherapie en 3,4% NB-UVB). Tijdens de follow up werd in beide groepen geen toename van melanocytaire naevis gezien [Heinlin 2011].
De gecontroleerde prospectieve studie van Dittmar et al. 1999 vergeleek UVAB monotherapie (n=12) met UVAB therapie gecombineerd met zoutwater baden (balneofototherapie) (n=16) en toonde na 20 behandelingen een significante reductie van de SCORAD van 69,5 voor therapie tot 36,8 na therapie in de balneofototherapie groep (p<0,0015). Opvallend in deze studie was dat er in de UVAB groep geen significante verbetering werd gezien, wat impliceert dat het baden in het zoute water de cruciale behandel component was in deze studie. Dit is in tegenspraak met andere, eerder genoemde studies, die het effect van UVAB lieten zien. Er werden in beide groepen geen bijwerkingen gezien [Dittmar 1999].
De open, ongecontroleerde, prospectieve studie van Autio et al. stuurde 216 CE patiënten voor 2- of 3-weekse heliothalasso-trips (klimatotherapie en spabehandeling) naar de Canarische Eilanden. De gemiddelde SCORAD daalde met 70% van 40 naar 12 na 2 weken heli thalassotherapie en was nog steeds 45% lager (22) dan bij de start, 3 maanden na de therapie (p<0,0001). Er werd geen significant verschil gezien tussen de 2- en 3-weekse therapieën. Ook het gebruik van topicale steroïden was na 3 maanden nog significant lager (p<0,0001). Kwaliteit van leven van patiënten werd gemeten door aan patiënten één vraag te stellen. 99% van de patiënten was van mening dat de heliotherapie een positief effect had op hun leven [Autio 2002].
Harari et al. onderzochten in hun retrospectieve single arm studie 1718 patiënten en concludeerden dat behandelingen in de Dode Zee in Israël van >4 weken zorgden voor een eczeem verbetering van >95%. Zij gebruikten hiervoor een zelf opgesteld scoringssysteem. 20.8% van de patiënten beschreef achteraf een remissie periode langer dan 10 maanden, 45,2% beschreef een remissie periode van 5-10 maanden en 34% van de benaderde patiënten ervoer een remissie van minder dan 5 maanden. Een duidelijke uitkomstmaat werd hiervoor niet gebruikt en significantie werd niet vermeld. Er werden geen bijwerkingen gezien [Harari 2000].
De ongecontroleerde single arm multicenter studie van Schiffner et al. combineerde NB-UVB met zout water baden. De analyse werd gebaseerd op 2 groepen: groep 1 (de ‘klinische trial’ groep) met patiënten die strikt het studieprotocol gevolgd hadden zonder uitval of non-compliance en groep 2 (de ‘dagelijkse praktijk’ groep), bestaande uit iedereen die minimaal eenmalig de behandeling ontvangen had. Er werd een significante(p<0,05) verbetering gezien van de SCORAD na 35 sessies bij 55% van de patiënten uit groep 1 en bij 41% van de patiënten uit groep 2. De kwaliteit van leven was volgens 54% van de patiënten na de therapie verbeterd, volgens 37% niet veranderd en volgens 9% verslechterd. Volgens de auteurs is deze vorm van therapie geschikt voor patiënten met een chronische vorm van CE, met een hoge compliance en met voldoende vrije tijd om de therapie te kunnen volgen. Bijwerkingen die gezien waren zijn erythema (7,3%), verbranding (3,6%), circulatiestoornissen (<1%) en claustrofobie (<1%) [Schiffner 2002].
De niet gerandomiseerde prospectieve studie van Adler-Cohen et al. bekeek het effect op CE en op de kwaliteit van leven van Dode Zee klimatotherapie. Ze behandelden 49 volwassenen met UVB expositie en vervolgens met baden in de Dode Zee in Israël. Het protocol in deze studie is niet duidelijk beschreven, maar de gemiddelde UVB doses was 1.664 J/m2 en het gemiddelde maximale aantal zonuren was 3,2. Patiënten verbleven gemiddeld 31 dagen bij de Dode Zee. De gemiddelde SCORAD waarde verbeterde met 39 punten (p<0,001). De overall Skindex-29 verbeterde met een gemiddelde waarde van 33 punten van 63 naar 30 (p<0,001). De eind SCORAD meting werd beïnvloed door de start-SCORAD en door het aantal zonuren per dag. De Skindex-29 score na behandeling werd beïnvloed door de start-Skindex-29 waarde en door de leeftijd van de patiënten. In deze studie zonder follow up periode worden geen bijwerkingen beschreven [Adler-Cohen 2012].
UVAB
Drie studies [Krutmann 1992, Krutmann 1998,von Kobyletzky 1999) vergeleken UVA1 met UVAB, beide dagelijks tot 15 dagen. In deze studies was UVA1 significant beter dan UVAB voor de reductie van COSTA (p<0,01 [Krutmann 1992] en p<0,0001 [Krutmann 1998]) en voor SCORAD (p<0,05) [von Kobyletzky 1999] direct na de behandeling Het is niet duidelijk of het verschil dat von Kobyletzki et al. beschrijven na een follow up periode van 4 weken in het voordeel van UVA1 statistisch significant is. Beschreven bijwerkingen waren xerosis cutis in UVA1 patiënten (aantal onbekend) [Krutmann 1992] zweten (5 UVA1 patiënten) [von Kobyletzki 1999] en erytheem in UVAB patiënten (aantal onbekend) [Krutmann 1992].
Von Kobyletzki et al vergeleek daarnaast UVAB ook met cold light MD-UVA1 (5 keer per week voor 3 weken) en zag dat de laatstgenoemde statistisch significant beter was voor de afname van de SCORAD direct na behandeling (p<0,05). Ook voor deze vergelijking was het niet duidelijk of het beschreven verschil na een follow up periode van 4 weken in het voordeel van cold light MD-UVA1 nog steeds significant is.
Jekler et al. voerden een aantal kleine links-rechts vergelijkende studies uit met UVAB, waarin zij het gebruik van topicale corticosteroïden toestonden. In 1991 concludeerden zij dat UVAB statistisch significant beter is dan BB-UVA (beide 5 keer per week voor 3 weken) voor de reductie van de klinische score (p<0,05), de algemene evaluatie score (p<0,01) en de healing score (p<0,01). Er wordt geen statistisch significant verschil gezien voor de reductie van jeukklachten. Genoemde bijwerkingen zijn een droge huid (7 UVA en 8 UVAB patiënten) en erytheem (4 UVA en 7 UVAB patiënten). In 1990 en 1991 vergeleken zij UVAB met BB-UVB (beide 3 keer per week voor 8 weken) en zagen dat UVAB significant beter was voor de reductie van de klinische scores en pruritus. Daarnaast was UVAB statistisch significant beter dan BB-UVB voor de afname van de uitgebreidheid van het eczeem volgens één studie [Jekler 1991], maar niet volgens de andere studie [Jekler 1990]. Ernstige xerosis cutis werd gezien in 9 UVB en 6 UVAB patiënten [Jekler 1990, Jekler 1991]. Overbehandelings verbranding werd gezien bij 8 UVB patiënten en bij 2 UVAB patiënten [Jekler 1990, Jekler 1991].
Volgens de studie van Krutmann et al. is fluocortolone 0,5% crème statistisch significant beter dan UVAB (beide dagelijks gedurende 10 dagen) voor de reductie van de COSTA score direct na de tiendaagse behandeling (p<0,0001) [Krutmann 1998].
Valkova et al. vergeleken in hun studie UVAB (17 patiënten) met UVAB gecombineerd met topicale corticosteroïden (14 patiënten). Zij zagen dat UVAB + topicale corticosteroïden statistisch significant beter is dan UVAB alleen (beide 5 keer per week tot klinische verbetering) voor de reductie van de behandelingsduur (p<0,02), maar er werden geen statistisch significante verschillende waargenomen tussen de 2 groepen voor de verbetering van de COSTA score (p=0,904) of de duur van de remissie perioden (p=0,39). Bijwerkingen die gezien werden zijn erytheem (5 UVAB, 4 UVAB+CS), verbranding (5 UVAB, 2 UVAB+CS), droge huid (10 UVAB, 5 UVAB+CS), warme (3 UVAB) en intens transpireren (3 UVAB, 4 UVAB+CS) [Valkova 2004].
Granlund et al. toonden in hun grote studie met 72 patiënten aan dat ciclosporine (4 mg/kg/dag) statistisch significant beter is dan UVAB (2-3 keer per week gedurende 8 weken) voor de snelle reductie van de SCORAD (p<0,001 in week 2,4 en 6 van behandelcyclus 1), de duur van de remissie (p<0,01) en de verbetering van de kwaliteit van leven na de eerste 4 weken (p<0,01). Geen statistisch significante verbetering wordt gezien voor de verbetering van kwaliteit van leven aan het einde van de studie na 5 behandelcycli van 8 weken. In deze studie werden topicale steroïden die niet sterker waren dan hydrocortisone-17-butyrate toegestaan. Bijwerkingen werden in 35 ciclosporine patiënten en in 32 UVAB patiënten genoemd. Er werden geen ernstige bijwerkingen genoemd. Gastro-intestinale bijwerkingen werden vaker gezien in de ciclosporine groep, terwijl zonnebrand vaker in de UVAB werd waargenomen. Infecties werden in beide groepen vermeld (29 ciclosporine patiënten, 25 UVAB) [Granlund 2001].
Foto(chemo)therapie en volledig spectrum licht (VSL)
Byun et al. vergeleken VSL (2 keer per week voor 4 weken) bij 20 patiënten met een behandeling met emolliens bij 18 patiënten. VSL zorgde voor een significante daling van de SCORAD direct na behandeling (reductie van 23,1%, p<0,01) en na een follow up periode van 4 weken (reductie 35,7%, p-waarde niet genoemd). In de controle groep met emolliens zag men geen significantie daling van de SCORAD waarden (p=0,26). In de VSL groep werd erytheem bij 6 patiënten gezien (30%), jeuk in 4 patiënten (20%) en branderig gevoel in 2 patiënten (10%). Een exacerbatie van CE werd gezien in 6 (20% VSL patiënten [Byun 2011].
De kleine links-rechts vergelijkende studie van der Petrossian et al. (12 patiënten) vond geen significant verschil tussen bad PUVA en NB-UVB (beide 3 keer per week tot complete remissie of gedurende maximaal 6 weken) voor een reductie van de SCORAD direct na de behandeling of na een follow up periode oplopend tot een jaar (week 2, p=0,09; week 4, p=0,51; week 6, p=0,48; 1 jaar, p-waarde niet genoemd). Wel werd er een snellere respons op bad-PUVA gezien in de eerste 2 weken. Er werden geen serieuze bijwerkingen (zoals ernstig foto toxisch erytheem of een eczema herpeticum) of onplezierige bijwerkingen waargenomen [Petrossian 2000].
5-MOP PUVA (3 keer per week gedurende 5 weken) bleek volgens de cross-over studie van Tzaneva et al. statistisch significant beter te zijn dan MD-UVA1 (5 maal gedurende 3 weken) voor de reductie van de SCORAD (p=0,041) en de duur van de remissie (p=0,012). Beide therapieën werden goed verdragen en er werden slechts milde bijwerkingen vermeld: mild palmoplantair erytheem (2 UVA1 en 9 PUVA patiënten), folliculitis (1 UVA1 en 2 PUVA), verbranding (7 UVA1) en foto-onycolyse (2 PUVA) [Tzaneva 2010].
Bijwerkingen
Alle behandelingen werden goed verdragen en er werden geen serieuze bijwerkingen vermeld. Milde bijwerkingen, zoals xerosis cutis en door behandeling geïnduceerd erytheem, werden bij de meeste behandelopties gezien. Minder vaak voorkomende bijwerkingen zijn toegenomen jeukklachten (bij UVA1 en VSL), gastro-intestinale klachten (bij balneofototherapie met NB-UVB), exacerbaties van eczeem (bij BB-UVA, NB-UVB, placebo zichtbaar licht en VSL), folliculitis (bij UVA1 en PUVA) en foto-onycolyse (bij PUVA). De exacte aantallen staan vermeld in de resultaten sectie. Gegevens over bijwerkingen moeten voorzichtig geïnterpreteerd worden, omdat niet alle studies bijwerkingen beschreven hebben en sommige studies alleen de aanwezigheid van de bijwerkingen noemden zonder de exacte getallen te vermelden. Daarnaast betreft het alleen bijwerkingen op de korte termijn, omdat lange termijn veiligheidsdata niet beschikbaar zijn.
Samenvatting
De geïncludeerde gerandomiseerde studies zijn over het algemeen van heterogene opzet, van korte duur zonder lange termijn follow up en bevatten vaak weinig patiënten. Desalniettemin kan worden geconcludeerd dat foto(chemo)therapie een goede therapeutische optie kan zijn voor patiënten met eczeem. Klinisch eczeem scores, jeukklachten en slaapproblemen verbeteren, remissie perioden tot 6 maanden worden vermeld en geen serieuze korte termijn bijwerkingen werden gedocumenteerd. Helaas zijn goede lange termijn data voor de meeste vergelijkingen niet beschikbaar.
Het meeste bewijs van voldoende kwaliteit is beschikbaar voor UVA1 en NB-UVB. Beide behandelopties zijn effectief voor de reductie van klinische symptomen van CE. Studies die beide opties direct met elkaar vergeleken lieten geen significante verschillen zien. Aan de hand van de beschikbare gerandomiseerde studies kan geen voorkeur worden uitgesproken voor het gebruik van NB-UVB of UVA1, noch voor de behandeling van acuut versus chronisch CE.
Bad-PUVA en 5-MOP PUVA lijken niet van mindere effectiviteit te zijn, maar worden slechts in individuele studies bestudeerd. Voor balneofototherapie en heli thalassotherapie geldt dat er slechts één gerandomiseerde studie beschikbaar is die balneofototherapie direct vergelijkt met NB-UVB monotherapie. De overige bekeken studies zijn niet gerandomiseerd, gebruiken allemaal een ander behandel protocol en vergelijken niet direct met fototherapie als monotherapie. Het blijft daarom onduidelijk of baden in zout water gecombineerd met licht expositie daadwerkelijk beter is dan mono-foto(chemo)therapie.
Op basis van één studie van goede kwaliteit lijkt cold light MD-UVA1 beter te zijn dan de reguliere UVA1 voor de reductie van SCORAD (von Kobyletzki 1999). Op basis van de resultaten van een zeer klein aantal studies van matige kwaliteit lijken UVAB, BB-UVA, BB-UVB en VSL minder effectieve behandelopties. UVAB lijkt beter te werken dan BB-UVA en BB-UVB, maar is volgens 3 studies niet effectiever dan het eerder genoemde UVA1 voor de reductie van SCORAD en de COSTA scores [von Kobyletzki 1999, Krutmann 1992, Krutmann 1998].
Omdat er geen gerandomiseerde of vergelijkende studies voor de combinatie steenkoolteer in combinatie met UV-B (vroeger geduid als Goeckerman therapie) beschikbaar zijn, blijft de rol van deze behandeloptie onduidelijk.
Kinderen
Vergelijkende gerandomiseerde studies bij kinderen ontbreken. Een mogelijke oorzaak hiervan is de bekende lange termijn bijwerkingen van ultraviolette straling op de huid. In de gevonden gerandomiseerde studies werden geen ernstige bijwerkingen gezien, maar lange termijn follow up studies in psoriasis patiënten laten een toegenomen risico op huidkanker zien na het gebruik van PUVA (Archier 2012). Volgens een recente uitgebrachte review zijn er nog geen directe verbanden gevonden tussen het gebruik van BB-UVB, NB-UVB en UVA1 en het ontstaan van huidkanker, maar ook hiervoor geldt dat langer termijn follow up studies ontbreken [Hofbuaer 2013].
De in 2014 verschenen Amerikaanse richtlijn (‘AD, management and treatment with phototherapy and systemic agents’) stemt hier mee overeen. Daarin spreekt men een voorkeur uit voor NB-UVB. De Amerkanen voegen er nog aan toe dat de lampen en machines die bij foto(chemo)therapie worden gebruikt voor kinderen bedreigend kunnen zijn. De dosis en frequentie zouden per individu moeten worden bepaald [Guidelines of care JAAD 2014].
Thuisbelichting
De werkgroep heeft geen hier geen aparte search naar gedaan. In de in 2014 verschenen Amerikaanse richtlijn is een alinea opgenomen over thuisbelichting bij patiënten met CE. Het grootste bezwaar van foto(chemo)therapie is het veelvuldig bezoek aan een kliniek. Thuisbelichting komt aan dit bezwaar geheel tegemoet. Er zijn echter geen studies verricht naar de effectiviteit en veiligheid van thuisbelichting bij patiënten met CE. Die zijn wel verricht bij patiënten met psoriasis. Daarbij is gebleken dat de thuisbelichting gelijkwaardig is aan een behandeling in de kliniek [Guide Lines of care JAAD 2014].
Lasers en extra corporale fotochemotherapie
De werkgroep heeft geen hier geen aparte search naar gedaan. In de in 2014 verschenen Amerikaanse richtlijn is een alinea opgenomen over behandeling met laser en foto dynamische therapie bij patiënten met CE. Er zijn meerdere publicaties waarin diverse vormen van foto dynamische therapie zijn beschreven. Het zijn over het algemeen kleine studies met een net vergelijkende opzet en magere resultaten. Incidenteel zijn er wel positieve resultaten beschreven, maar al met al zijn die resultaten niet zodanig dat deze therapie kan worden aanbevolen. Mogelijk is er wel een plek voor deze behandeling bij patiënten met een erytrodermie op basis van CE [Guidelines of care JAAD 2014].
Figuur 1 Effectiviteit
- Adler-Cohen C, Czarnowicki T, Dreiher J, et al. Climatotherapy at the Dead Sea: an effective treatment modality for atopic dermatitis with significant positive impact on quality of life. Dermatitis. 2012;23:75-80.
- Archier E, Devaux S, Castela E, et al. Carcinogenic risks of psoralen UV-A therapy and narrowband UV-B therapy in chronic plaque psoriasis: a systematic literature review. J Eur Acad Dermatol Venereol. 2012;26 Suppl 3:22-31.
- Autio P, Komulainen P, Larni HM, et al. Heliotherapy in atopic dermatitis: a prospective study on climatotherapy using the SCORAD index. Acta Derm Venereol. 2002;82:436-440.
- Brenninkmeijer EE, Schram ME, Leeflang MM, et al. Diagnostic criteria for atopic dermatitis: a systematic review. Br J Dermatol. 2008;158:754-65.
- Byun HJ, Lee HI, Kim B, et al. Full-spectrum light phototherapy for atopic dermatitis. Int J Dermatol. 2001;50:94-101.
- Der-Petrossian M, Seeber A, Hönigsmann H, et al. Half-side comparison study on the efficacy of 8-methoxypsoralen bath-PUVA versus narrow-band ultraviolet B phototherapy in patients with severe chronic atopic dermatitis. Br J Dermatol. 2000;142:39-43.
- Dittmar HC, Pflieger D, Schempp CM et al. Comparison of balneophototherapy and UVA/B mono-phototherapy in patients with subacute atopic dermatitis. Hautartz. 1999;50:649-653.
- Dittmar HC, Pflieger D, Schöpf E, et al. Pilot study of dose finding in acute exacerbated atopic dermatitis. Hautarzt. 2001;52:423-7.
- Faergemann J, Larkö O. The effect of UV light on human skin microorganisms. Acta Derm Venereol (Stockh) 1987;67:69-72.
- Finlay AY, Khan GK (1994) Dermatology Life Quality Index (DLQI) a simple practical measure for routine clinical use. Clin Exper Dermatol 19:210216
- Finlay AY. Measurement of disease activity and outcome in atopic dermatitis. Br J Dermatol 1996;135:509-15.
- Gambichler T, Othlinghaus N, Tomi NS, et al. Medium-dose ultraviolet (UV) A1 vs. narrowband UVB phototherapy in atopic eczema: a randomized crossover study. Br J Dermatol. 2009;160:652-8.
- Gambichler T. Management of atopic dermatitis using photo(chemo)therapy. Arch Dermatol Res. 2009;301:197-203.
- Global resource for eczema trials. Beschikbaar op: http://www.greatdatabase.org.uk/. Geraadpleegd op 10 Oktober 2012.
- Granlund H, Erkko P, Remitz A, et al. Comparison of cyclosporin and UVAB phototherapy for intermittend one-year treatment of atopic dermatitis. Acta Derm Venereol. 2001;81:22-7.
- Harari M, Shani J, Seidl V, et al. Climatotherapy of atopic dermatitis at the Dead Sea: demographic evaluation and cost-effectiveness. Int J Dermatol. 2000;39:59-69.
- Heinlin J, Schiffner-Rohe J, Schiffner R, et al. A first prospective randomized controlled trial on the efficacy and safety of synchronous balneophototherapy vs. narrow-band UVB monotherapy for atopic dermatitis. J Eur Acad Dermatol Venereol. 2011;25:765-73.
- Hofbauer G. Phototherapy and carcinogenesis. Hautartz. 2013;64:349-53.
- Jekler J, Larkö O. UVB phototherapy of atopic dermatitis. Br J Dermatol. 1988;119:697-705.16.
- Jekler J, Larkö O. Combined UVA-UVB versus UVB phototherapy for atopic dermatitis: a paired-comparison study. J Am Acad Dermaol. 1990;22:49-53.
- Jekler J, Larkö O. UVA solarium versus UVB phototherapy of atopic dermatitis: a paired-comparison study. Br J Dermatol. 1991;125:569-72.
- Jekler J, Larkö O. Phototherapy for atopic dermatitis with ultraviolet A (UVA), low-dose UVB and combined UVA and UVB: two paired-comparison studies. Photodermatol Photoimmunol Photomed. 1991;8:151-6.
- Krutmann J, Czech W, Diepgen T, et al. High-dose UVA1 therapy in the treatment of patients with atopic dermatitis. J Am Acad Dermatol. 1992;26:225-30.
- Krutmann J, Diepgen TL, Luger TA, et al. High-dose UVA1 therapy for atopic dermatitis: results of a multicenter trial. J Am Acad Dermatol. 1998;38:589-93.
- Legat FJ, Hofer A, Brabek E, et al. Narrowband UV-B vs medium dose UV-A1 phototherapy in chronic atopic dermatitis. Arch Dermatol. 2003;139:223-4.
- Majoie IM, Oldhoff JM, van Weelden H, et al. Narrowband ultraviolet B and medium-dose ultraviolet A1 are equally effective in the treatment of moderate to severe atopic dermatitis. J Am Acad Dermatol. 2009;60:77-84.
- Meduri NB, Vandergriff T, Rasmussen H, et al. Phototherapy in the management of atopic dermatitis: a systematic review. Photodermatol Photoimmunol Photomed. 2007;23:106-12.
- Reynolds NJ, Franklin V, Gray JC, et al. Narrow-band ultraviolet B and broad-band ultraviolet A phototherapy in adult atopic eczema: a randomised controlled trial. Lancet. 2001;357:2012-6.
- Ring J, Alomar A, Bieber T et al. Guidelines for treatment of atopic eczema (atopic dermatitis) part II. J Eur Acad Dermatol Venereol 2012 Sep;26:1176-93.
- Sampogna F, Abeni D. Interpretation of Skindex-29 scores. J Invest Dermatol. 2011;131:1790-2.
- Scheinfeld NS, Tutrone WD, Weinberg JM, et al. Phototherapy of atopic dermatitis. Clin Dermatol. 2003;21:241-8.
- Schiffner R, Schiffner-Rohe J, Gerstenhauer M, et al. Dead Sea treatment principe for outpatient use in atopic dermatitis: safety and efficacy of synchronous balneophototherapy using narrowband UVB and bathing in Dead Sea salt solution. Eur J Dermatol. 2002;12:543-548.
- Schmitt J, Spuls P, Boers M, et al. Towards global consensus on outcome measures for atopic eczema research: results of the HOME II meeting. Allergy. 2012;67:1111-7.
- Severity scoring of atopic dermatitis: the SCORAD index. Consensus Report of the European Task Force on Atopic Dermatitis. Dermatology 1993;186:23-31.
- Sidbury R, Davis DM, Cohen DE et al. American Academy of Dermatology. Guidelines of care for the management of atopic dermatitis: section 3. Management and treatment with phototherapy and systemic agents. J Am Acad Dermatol. 2014 Aug;71(2):327-49.
- Tzaneva S, Seeber A, Schwaiger M, et al. High-dose versus medium-dose UVA1 phototherapy for patients with severe generalized atopic dermatitis. J Am Acad Dermatol. 2001;45:503-7.
- Tzaneva S, Kittler H, Holzer G, et al. A. 5-Methoxypsoralen plus ultraviolet (UV) A is superior to medium-dose UVA1 in the treatment of severe atopic dermatitis: a randomized cross-over trial. Br J Dermatol. 2010;162:655-60.
- Valkova S, Velkova A. UVA/UVB phototherapy for atopic dermatitis revisited. J Dermatolog Treat. 2004;15:239-44.
- Von Kobyletzki G, Pieck C, Hoffmann K, et al. Medium-dose UVA1 cold-light phototherapy in the treatment of severe atopic dermatitis. J Am Acad Dermatol. 1999;41:931-7.
- Sidbury R, Davis DM, Cohen DE et al. American Academy of Dermatology. Guidelines of care for the management of atopic dermatitis: section 3. Management and treatment with phototherapy and systemic agents. J Am Acad Dermatol. 2014 Aug;71(2):327-49
|
Auteur, jaartal |
Mate van bewijs |
Type onderzoek |
Aantal patiënten |
Patiëntenpopulatie (evt in/exclusiecriteria) |
AD criterium |
Follow-up duur na behandeling |
Interventie groep |
Controle groep |
Uitkomst |
Resultaten |
Opmerkingen over studie kwaliteit |
|
Adler-Cohen, 2012 |
C |
OS |
49 |
Leeftijd 18-71, duur CE 3-59 jaar. Gem SCORAD van 66. |
H&R |
NB |
Climatotherapie |
Nvt |
SCORAD, Skindex-29 |
Significante reductie van SCORAD (p<0.0001) en van Skindex-29 (p<0.0001) na behandeling bij Dode Zee |
Niet gerandomiseerd, single arm studie. Grote uitval van patiënten (12 van de 61). Protocol en methoden slecht beschreven. Eerst UVB therapie, daarna zee-therapie. Effecten niet uitgesplitst. Geen follow up. Geen bijwerkingen beschreven. |
|
Autio, 2002 |
C |
OS |
216 |
Leeftijd >18 jaar, matig-ernstig eczeem |
NB |
3 maanden |
Heliothalassotherapie Canarisch eilanden |
Nvt |
SCORAD |
Significante reductie SCORAD 2 weken en 3 maanden na behandeling (p<0.0001) |
Niet gerandomiseerd, single arm studie, geen patiënten kenmerken genoteerd, geen standaard meting van kwaliteit van leven. |
|
Byun, 2011 |
B |
RCT |
38 |
Gem SCORAD 47.87 (VSL) en 39.79 (controle), 25-48 jr, huidtype IV of V |
H&R |
4 wkn |
VSL |
Emolliens |
SCORAD |
VLS significante reductie in week 4 (p<0.01). Emolliens geen significatie reductie in week 4 en 8 (p=0.236)
|
Randomisatieproces en allocation concealment onduidelijk. Niet geblindeerd. Geen uitvallers. Geen washout periode voor topicale steroïden. Bijwerkingen gemeld. |
|
Der-Petrossian, |
B |
RCT |
12 |
Chronisch ernstig CE, gem SCORAD 67.9, leeftijd gem 27 jr |
H&R |
Tot 1 jaar |
Bad-PUVA vs smal spectrum UVB |
Nvt |
SCORAD |
Geen significantie verschillen (p=0.09 in week 2, p=0.51 in week 4, p=0.48 in week 6). Wel snellere respons op bad-PUVA in week 2. |
Randomisatieproces en allocation concealment onduidelijk. Patiënten niet geblindeerd. Twee uitvallers, bijwerkingen gemeld. Geen wash-out periode voor topicale steroïden, geen exclusie criteria studiedeelname gemeld. Geen exacte data gemeld, alleen percentages en een kleine figuur. a |
|
Auteur, jaartal |
Mate van bewijs |
Type onderzoek |
Aantal patiënten |
Patiëntenpopulatie (evt in/exclusiecriteria) |
AD criterium |
Follow-up duur na behandeling |
Interventie groep |
Controle groep |
Uitkomst |
Resultaten |
Opmerkingen over studie kwaliteit |
|
Dittmar, 1999 |
B |
OS |
28 |
Subactuut eczeem, gem leeftijd 34. |
H&R |
NB |
UVAB monotherapie versus balneofototherapie |
Nvt |
SCORAD |
Significante daling van SCORAD in balneophototherapie groep (p<0.0015), geen daling gezien in UVAB groep. |
Niet gerandomiseerd. Vergelijkende studie, bijwerkingen vermeld. Protocol duidelijk beschreven. |
|
Dittmar, 2001 |
B |
RCT |
34 |
SCORAD >30, ernst CE, 18-57 jr |
H&R |
NB |
UVA-1 hoge, gemiddelde en lage dosering |
Nvt |
SCORAD |
Hoge dosis = gemiddelde dosis |
Randomisatie en blindering niet besproken. 10 uitvallers, reden van uitval gemeld, bijwerkingen gemeld, geen effect op jeuk. Geen wash-out periode voor topicale steroïden. |
|
Gambichler, 2008 |
A2 |
RCT |
47 |
Uitgebreid CE, gem SASSAD >40, leeftijd 18-83 jr |
H&R |
2 mnd. |
UVA1 vs NB-UVB |
nvt |
SASSAD, pruritus, Skindex-29 |
Geen significantie verschillen tussen UVA1 en NB-UVB voor uitkomstmaten. Geen significante invloed van behandelvolgorde op resultaten (p=0.81) |
Carry-over effect van crossover studie goed beschreven. Randomisatie-proces en allocation concealment adequeaat benoemd. ITT analyse van 28 patiënten uitgevoerd. |
|
Granlund, 2001 |
B |
RCT |
72 |
R&L 7-9, ernst CE via H&R, > 18 jr |
H&R |
NB |
UVAB |
Cyclo |
SCORAD, EDI, dagen remissie |
CyA>UVAB |
Randomisatieproces en allocation concealment onduidelijk. Niet geblindeerd. 24 uitvallers, reden van uitval gemeld, bijwerkingen gemeld, korte wash-out periode voor fototherapie, topicale steroïden toestaan. |
|
Harari, 2000 |
C |
OS |
1718 |
Volwassenen en kinderen (>2 jaar). |
NB |
Tot >10maanden |
Dode zee verblijf Israël |
Nvt |
Zelf ontwikkeld systeem |
Verbetering van 95% bij verblijf >4 weken. |
Niet gerandomiseerd, single arm studies, geenpatiënten kenmerken, geen standaard meting eczeem verbetering. |
|
Heinlin, 2011 |
A2 |
RCT |
180 |
SCORAD>35, causasische achtergrond, leeftijd gem 41 jr |
H&R |
6 mnd. |
Balneofoto-therapie vs NB-UVB |
Nvt |
SCORAD, FLQA-d |
Significant groter daling SCORAD in balneofototherapie (p<0.0001). Geen verschillen bij FLQA-d |
Randomisatie en allocation concealment goed toegepast. ITT analyse van 169 patiënten. Blindering niet mogelijk. Bijwerkingen genoemd. |
|
Auteur, jaartal |
Mate van bewijs |
Type onderzoek |
Aantal patiënten |
Patiëntenpopulatie (evt in/exclusiecriteria) |
AD criterium |
Follow-up duur na behandeling |
Interventie groep |
Controle groep |
Uitkomst |
Resultaten |
Opmerkingen over studie kwaliteit |
|
Jekler, 1988 |
B |
RCT |
28 |
Ernst CE nb, gem leeftijd 24.9 jr, |
H&R |
NB |
UVB |
Placebo zichtbaar licht |
Totale score, pruritus |
UVB> placebo zichtbaar licht (p<0.0001 voor alle uitkomstmaten) |
Links-rechts vergelijking. 11 uitvallers. Randomisatieproces en blindering niet benoemd. Hydrocortison topicaal toegestaan. Bijwerkingen genoemd. |
|
Jekler, 1990 |
B |
RCT |
39 |
ErnstCE nb> 18jr |
H&R |
NB |
UVB vs UVAB |
nvt |
Totale score, pruritus |
Uvab>uvb (p=0,002 voor totale score, p=0.04 voor pruritus) |
Links-rechts vergelijking. 9 uitvallers. Randomisatieproces en blindering niet benoemd. Hydrocortison topicaal toegestaan. Bijwerkingen genoemd. |
|
Jekler, 1991 |
B |
RCT |
33 |
Ernst CE nb, gem leeftijd 23.3 jr |
H&R |
NB |
UVA vs UVB |
nvt |
Totale score, pruritus |
Uva>uvb voor totale score (p<0.02). Geen verschil voor pruritus. |
Links-rechts vergelijking. 12 uitvallers. Randomisatieproces en blindering niet benoemd. Hydrocortison topicaal toegestaan. Bijwerkingen genoemd. |
|
Jekler, 1991A |
B |
RCT |
20 |
Ernst CE nb, gem leeftijd 28.3 jr |
H&R |
NB |
UVB vs UVAB |
nvt |
Totale score, pruritus |
UVAB > UVB (p=0.001 voor alle uitkomstmaten)
|
Links-rechts vergelijking. 2 uitvallers. Randomisatieproces en blindering niet benoemd. Hydrocortison topicaal toegestaan. Bijwerkingen genoemd. |
|
28 |
Ernst CE nb, gem leeftijd 24.0 jr |
H&R |
NB |
UVA vs UVAB |
nvt |
Totale score, pruritus |
Significante reductie in voordeel van UVAB voor totale score (p<0.05). Voor pruritus geen veschil. |
Links-rechts vergelijking. 3 uitvallers. Randomisatieproces en blindering niet benoemd. Hydrocortison topicaal toegestaan. Bijwerkingen genoemd. |
|||
|
Kruttmann, 1992 |
B |
RCT |
25 |
Acute exacerbaties, leeftijd 19-35 jr |
H&R |
NB |
UVA1 vs UVAB |
nvt |
COSTA |
UVA1 > UVAB (p<0,01) |
Randomisatieproces en blindering niet benoemd. 1 uitvaller. Bijwerkingen genoemd. |
|
Auteur, jaartal |
Mate van bewijs |
Type onderzoek |
Aantal patiënten |
Patiëntenpopulatie (evt in/exclusiecriteria) |
AD criterium |
Follow-up duur na behandeling |
Interventie groep |
Controle groep |
Uitkomst |
Resultaten |
Opmerkingen over studie kwaliteit |
|
Krutmann, 1998 |
A2 |
RCT |
53 |
Ernstig CE, COSTA > 40, leeftijd gem 26-28 jr |
H&R |
NB |
HD-UVA1, UVAB |
Dermato-corticosteroïden |
COSTA |
UVA1 > fluocortolone (p<0.002) UVA1 > UVAB (p<0.0001) Fluocortolone > UVAB (p<0.0001) |
Randomisatieproces en blindering niet benoemd. geen uitvallers. Bijwerkingen genoemd. Geen exacte data gemeld, alleen percentages en een kleine figuur. |
|
Legat, 2003 |
B |
RCT |
9 |
Chronisch CE, 23-41 jr |
H&R |
NR |
UVA1 vs NB-UVB |
nvt |
LSS, COSTA, pruritus |
LSS afname sterker in NB-UVB (p=0.02), COSTA afname sterker in UVA1 (ns), pruritus afname geen significante verschillen |
Links-recht vergelijking, lage aanvangsdosering UVA1, 2 uitvallers, reden van uitval gemeld, bijwerkingen niet gemeld. Randomisatie en blindering niet besproken. Geen baseline kenmerken vermeld.
|
|
Majoie, 2009 |
B |
RCT |
13 |
Ernst CR nb, gem leeftijd 25 jr |
H&R |
4 wkn |
UVA1 vs NB-UVB |
nvt |
LSS, pruritus |
Geen significante verschillen tussen beide behandelingen. |
Links-rechts vergelijking, geen uitvallers. Patiënten niet geblindeerd. Randomisatieproces en allocation concealment onduidelijk. Geen bijwerkingen beschreven. |
|
Reynolds, 2001 |
B |
RCT |
73 |
Activity >10, leeftijd gem 25-29 jr |
H&R |
12 wkn |
NB-UVB vs UVA |
Placebo zichtbaar licht |
Score van Sowden en collegae, pruritus, slaapproblemen |
NB-UVB > UVA > placebo licht |
Randomisatieproces en allocation concealment goed uitgevoerd. 26 uitvallers, reden van uitvallen gemeld, evenals bijwerkingen. Corticosteroïden topicaal toegestaan. |
|
Auteur, jaartal |
Mate van bewijs |
Type onderzoek |
Aantal patiënten |
Patiëntenpopulatie (evt in/exclusiecriteria) |
AD criterium |
Follow-up duur na behandeling |
Interventie groep |
Controle groep |
Uitkomst |
Resultaten |
Opmerkingen over studie kwaliteit |
|
Schiffner, 2002 |
C |
OS |
615 |
SCORAD >35, gem leeftijd 37 jaar. |
NB |
NB |
NB-UVB met zoutwaterbaden |
Nvt |
SCORAD, zelf ontwikkelde vragenlijst voor QoL |
SCORAD significant (p<0.05) gedaald bij 55% van de patiënten. Kwaliteit van leven verbeterd bij 54% van patiënten. |
Open, niet gerandomiseerde, multicenter trial, niet gecontroleerd. Hoge uitval. Bijwerkingen genoemd. |
|
Tzaneva, 2001 |
B |
RCT |
10 |
SCORAD 45-90, leeftijd 22-58 |
H&R |
Tot 6 mnd. |
HD UVA1 vs MD-UVA1 |
Nvt |
SCORAD |
Geen significante verschillen op alle tijdspunten |
Randomisatieproces en allocation concealment onduidelijk. Geen uitvallers, patiënten niet geblindeerd. Bijwerkingen genoemd. |
|
Tzaneva, 2010 |
B |
RCT |
40 |
SCORAD>45, leeftijd gem 32.9 jr |
H&R |
Tot 1 jaar |
UVA1 vs 5-MOP PUVA |
Nvt |
SCORAD, remissieduur |
SCORAD sterker gedaald in PUVA (p=0.041), remissie langer in PUVA (p=0.012)
|
Allocation concealment niet gemeld. Randomisatieproces wel vermeld (muntje opgooien). Crossover study, cary-over effect niet beschreven. Slechts 15 deelnemers studie volbracht. Bijwerkingen beschreven. |
|
Valkova, 2004 |
B |
RCT |
31 |
COSTA gem 670. Leeftijd gem 19 jr |
H&R |
3-6mdn |
UVAB vs UVAB+CS |
Nvt |
COSTA, pruritus, slaapproblemen |
Geen significante verschillen tussen twee groepen voor COSTA (p=0.904) of remissie perioden (p=0.39). Significant verschil in aantal behandelingen in voordeel van UVAB+CS (p=0.02) en hoogte van UVB (p=0.03) |
Randomisatieproces en allocation concealment onduidelijk. Geen blindering. Bijwerkingen genoemd. |
|
Von Kobyletzki |
A2 |
RCT |
120 |
Ernstig CE, leeftijd van 18-61 |
H&R |
4 wkn |
UVA1 vs Cold-light UVA1 vs UVAB |
Nvt |
SCORAD |
Significante reductie in voordeel van beide UVA1 groepen vergeleken met UVAB (p<0.05). Significante reductie in voordeel van cold-light UVA1 vergelen met UVA1 (p<0.03). |
Randomisatieproces en allocation concealment onduidelijk. Patiënten niet geblindeerd. 16 uitvallers, redenen gemeld. Bijwerkingen genoemd. |
RCT=randomised controlled trial; H&R=constitutioneel eczeem volgens criteria van Hanifin en Rajka; CE=constitutioneel eczeem; uv=ultraviolet; PUVA=ultraviolet a en orale psoralenen; UVA1=langgolvig UVA; Med=minimal erythema dose; cold light uva-1= gekoelde uva-1 therapie; nb=smal spectrum; Cycl=CyA=ciclosporinA; Iga=investigator global assesment; SCORAD=European clinical severety score for atopic dermatitis; o.s=open niet gerandomiseerde studie nb=niet bekend of niet beschreven R&L=ziekte ernst volgens Rajka en Langeland 1989; gem=gemiddeld; nvt=niet van toepassing; ITT = intention to treat; EDI = eczema disability index; LSS= Leicester score
Beoordelingsdatum en geldigheid
Publicatiedatum : 09-06-2015
Beoordeeld op geldigheid : 01-01-2014
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep uit 2014 gedeeltelijk in stand gehouden. Op modulair niveau is een onderhoudsplan beschreven. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt van de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update).
De Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) is regiehouder van deze richtlijn(modules) en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn(modules). De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door arts-onderzoekers van de NVDV en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijn.
Doel en doelgroep
Doel
Deze richtlijn over constitutioneel eczeem is een document met aanbevelingen ter ondersteuning van de dagelijkse praktijkvoering. De richtlijn berust op de resultaten van wetenschappelijk onderzoek en aansluitende meningsvorming gericht op het vaststellen van goed medisch handelen. De richtlijn geeft aanbevelingen over begeleiding en behandeling van patiënten met constitutioneel eczeem.
Doelgroep
De richtlijn is bestemd voor alle zorgverleners die betrokken zijn bij de zorg voor patiënten met constitutioneel eczeem. Zoals dermatologen, gespecialiseerd verpleegkundigen, huisartsen, bedrijfsartsen, jeugdgezondheidsartsen, allergologen, kinderartsen, klinische chemici, apothekers en psychologen. Voor patiënten is een afgeleide tekst van de richtlijn beschikbaar op de website van de NVDV (www.nvdv.nl) en op www.thuisarts.nl.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2007 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met constitutioneel eczeem en patiëntenvertegenwoordiger(s) vanuit de Huidpatiënten Nederland en Vereniging voor mensen met Constitutioneel Eczeem (VMCE) (zie voor het overzicht van de werkgroepleden de tabellen hieronder). Wetenschappelijke verenigingen en beroepsverenigingen zoals de NVK, NVZA, NVvA, V&VN, NHG, NVAB en NIP en stakeholders zoals VIG, ZN, NVZ, en NFU werden voor de knelpuntenanalyse en commentaarronde uitgenodigd. Voor de modulaire update in 2018 van de richtlijn werden bovenstaande partijen weer uitgenodigd.
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname.
De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
Werkgroepleden – (modulaire) herziening 2019
|
Werkgroeplid |
Affiliatie en vereniging |
|
Dhr. B.W.M. Arents |
VMCE |
|
Mw. Dr. M.A. Breukels, kinderarts |
Elkerliek ziekenhuis, NVK |
|
Mw. Dr. M.S. de Bruin-Weller, dermatoloog (voorzitter) |
UMC Utrecht, NVDV |
|
Mw. Drs. Y.Y. Chung, arts-onderzoeker (secretaris) (tot december 2017) |
Bureau NVDV, Utrecht, NVDV (tot 2018) |
|
Dhr. Dr. J.J.E. van Everdingen, dermatoloog n.p. |
Directeur NVDV |
|
Mw. Dr. F.M. Garritsen, AIOS dermatologie |
UMC Utrecht |
|
Mw. Drs. M.F. Hofhuis, arts-onderzoeker (secretaris) (vanaf januari 2018) |
Bureau NVDV, Utrecht, NVDV (vanaf 2018) |
|
Dhr. Drs. W.N.M. Kouwenhoven |
VMCE |
|
Dhr. Dr. T. Rustemeyer, dermatoloog |
VUMC, NVDV |
|
Mw. Drs. A.A.J. van der Sande, arts-onderzoeker (secretaris) (tot december 2017) |
Bureau NVDV, Utrecht, NVDV (tot 2018) |
|
Mw. Dr. M.L.A. Schuttelaar, dermatoloog |
UMC Groningen, NVDV |
|
Mw. Drs. L. Teligui, arts-onderzoeker (secretaris) (januari tot december 2018) |
Bureau NVDV, Utrecht, NVDV (vanaf 2018) |
|
Dhr. Dr. R. Tupker, dermatoloog |
St. Antonius ziekenhuis Nieuwegein, NVDV |
|
Werkgroep vroege introductie voedingsallergenen |
Affiliatie en vereniging |
|
Mw. Dr. M. de Graaf dermatoloog |
UMC Utrecht, NVDV |
|
Mw. Dr. I. M. Haeck, dermatoloog |
Reinier de Graaf Groep, NVDV |
|
Dhr. Dr. A.C. Knulst, dermatoloog |
UMC Utrecht, NVDV |
|
Mw. Dr. T. M. Le, dermatoloog |
UMC Utrecht, NVDV |
|
Mw. Prof. dr. S.G.M.A. Pasmans, dermatoloog |
Erasmus MC, NVDV |
|
Mw. Drs. L.S. van der Schoot, arts-onderzoeker (secretaris), vanaf april 2019 |
Bureau NVDV, Utrecht, NVDV (vanaf 2019) |
Werkgroepleden – versie 2014
|
Werkgroeplid |
Affiliatie en vereniging |
|
Mw. Dr. M.A. Breukels, kinderarts |
NVK |
|
Mw. Prof. dr. C.A.F.M. Bruijnzeel-Koomen, dermatoloog (voorzitter) |
NVDV |
|
Mw. Dr. M.S. de Bruin-Weller, dermatoloog |
NVDV |
|
Mw. Drs. C.A.M. Eggen, arts-onderzoeker (secretaris) |
Bureau NVDV, Utrecht, NVDV (tot 2014) |
|
Dhr. Dr. J.J.E. van Everdingen, dermatoloog n.p. |
Directeur NVDV |
|
Dhr. Dr. F. Jungbauer, bedrijfsarts |
NVAB |
|
Dhr. Drs. W.N.M. Kouwenhoven |
VMCE |
|
Mw. Drs, R.A. Kuin, arts-onderzoeker (secretaris) |
Bureau NVDV, Utrecht, NVDV (vanaf 2014) |
|
Dhr. Prof. dr. A. Oranje, dermatoloog |
NVDV |
|
Mw. Dr. J.N.G. Oude Elberink, internist-allergoloog |
Vakgroep Allergologie (+NVvA) |
|
Mw. Dr. H. van Os-Medendorp |
V&VN |
|
Mw. Prof. dr. S. G.M.A. Pasmans, dermatoloog |
NVDV |
|
Dhr. Dr. T. Rustemeyer, dermatoloog |
NVDV |
|
Mw. Dr. M.L.A. Schuttelaar, dermatoloog |
NVDV |
|
Mw. Prof. dr. P.I. Spuls, dermatoloog |
NVDV |
|
Dhr. Dr. R.A. Tupker, dermatoloog |
NVDV |
|
Mw. Drs. C.J.H. de Vries, huisarts |
NHG (RL) |
|
Mw. Drs. W. Zijlstra |
NIP |
|
Ondersteuning werkgroep |
Affiliatie en vereniging |
|
Mw. Drs. K.B. Fieten |
NAD |
|
Mw. C. Frima |
student UMCU |
|
Mw. Drs. F.M. Garritsen |
AIOS UMCU |
|
Mw. Drs K. Hiemstra |
student UMCU |
|
Mw. Drs. E. Roekevisch |
AIOS AMC |
|
Mw. Drs. J.L. Thijs |
student UMCU |
|
Mw. Dr. S.G.A. van Velsen |
AIOS VUmc |
|
Dhr. Drs. G. Weststrate |
student UMCU |
|
Mw. Dr. M.J. Wiegman |
AIOS UMCG |
Werkgroepleden – versie 2007
|
Werkgroeplid (kernwerkgroep) |
Affiliatie en vereniging |
|
Mw. Prof. dr. C.A.F.M. Bruijnzeel-Koomen, dermatoloog (voorzitter) |
UMC Utrecht, NVDV |
|
Mw. drs. P.C.M. Eland-de Kok, verpleegkundig specialist |
UMC Utrecht |
|
Dhr. Dr. J.J.E. van Everdingen, dermatoloog |
CBO, secretaris vanaf 1 januari 2006 |
|
Mw. dr.ir. C.W.P.M. Hukkelhoven, epidemioloog, |
CBO, secretaris tot 1 januari 2006 |
|
Dr. J.P.C. Jaspers stafmedewerker vakinhoudelijke ontwikkeling |
UMC Groningen |
|
Dhr. Dr. J.H. Sillevis Smitt, dermatoloog |
AMC Amsterdam |
|
Werkgroep |
|
|
B.W.M. Arents |
VMCE (tot 27 november 2005) |
|
Mw. Drs. F.S. Boukes, huisarts |
NHG |
|
Mw. Dr. M.S. de Bruin-Weller, dermatoloog |
UMC Utrecht |
|
Dr. B.J.G. Daemen, apotheker |
Den Haag, KNMP/WINAP |
|
Mw. drs. P.C. Dirven-Meijer, huisarts |
Huisartsenpraktijk Renswoude |
|
Dr. M.O. Hoekstra, kinderarts |
UMC Utrecht |
|
Drs. E.J. Jansen, verpleegkundig consulent |
UMC Groningen |
|
Dr. E.J.M. van Leent, dermatoloog |
AMC Amsterdam |
|
Mw. Dr. J.N.G. Oude Elberink, internist-allergoloog |
UMC Groningen |
|
Drs. W.P. Piebenga, bedrijfsarts |
Velp |
|
Mw. drs. J.G.M. Rijntjes, kinderarts |
Emma Kinderziekenhuis, Amsterdam |
|
Dr. K.H. Tjiam, dermatoloog |
Renier de Graaf Groep, Delft |
|
Dr. A.W. van Toorenenbergen, klinisch chemicus |
Erasmus MC, Rotterdam |
|
Dr. R.A. Tupker, dermatoloog |
Sint Antonius Ziekenhuis, Nieuwegein |
|
Mw. Y. de Vries, hulplijn/columnist |
VMCE |
|
Mw. drs. C.L. Wensing-Souren, jeugdarts |
Huisartsenpraktijk Chaam |
Belangenverklaringen
Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen is opgenomen in bijlage A. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van de NVDV.
Inbreng patiëntenperspectief
Er is aandacht besteed aan het patiëntenperspectief door deelname van vertegenwoordigers vanuit de patiëntenvereniging VMCE in de werkgroep (zie ook samenstelling van de werkgroep). De deelnemers zijn betrokken geweest bij het opstellen van de conceptteksten. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de VMCE.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn(module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren, zoals het niet meer vergoeden van bepaalde behandelingen (lichttherapie en (ureumhoudende) indifferente middelen) en de introductie van nieuwe systemische medicatie (dupilumab). Het implementatieplan is te vinden op de richtlijnen database (RLDB) onder aanverwante producten. Omdat de maatschappelijke impact van het gebruik van het nieuwe geneesmiddel dupilumab als groot werd ingeschat, is in 2019 een doorrekening van de gewijzigde kosten bij integrale implementatie van de richtlijn gerealiseerd in een zogenaamde Budget Impact Analyse (BIA). De volledige rapportage is opgenomen in de aanverwante producten.
Werkwijze
De werkgroep constitutioneel eczeem heeft de vraag- en doelstellingen van deze richtlijn met elkaar afgestemd en uitgewerkt. De eerste versie van de richtlijn stamt uit 2007. De richtlijn is in 2012-2014 herzien op een groot aantal onderdelen, de hoofdstukken ‘diagnostiek’, ‘lokale therapie’ en ‘overige systemische therapie’ gedeeltelijk herzien. Per hoofdstuk staat aangegeven in welk jaartal deze al dan niet herzien is.
De ontwikkeling van de modulaire herziening in 2019 is o.a. gebaseerd op de update van de systematische review van Roekevisch et al. over de effectiviteit en veiligheid van systemische immunomodulerende middelen bij patiënten met matig tot ernstig constitutioneel eczeem. [Roekevisch 2014] Ook is gebruik gemaakt van de ‘Guidelines of care for the management of atopic dermatitis, section 3. Management and treatment with phototherapy and systemic agents‘. [Sidbury 2014]
Hieronder wordt de werkwijze van de richtlijnontwikkeling toegelicht.
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. [Medisch Specialistische Richtlijnen] Dit rapport is gebaseerd op het AGREE II-instrument (Appraisal of Guidelines for Research & Evaluation II), dat een internationaal breed geaccepteerd instrument is. [Brouwers 2010] Voor een stap-voor-stapbeschrijving hoe een evidence-based richtlijn tot stand komt, wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van Medisch Specialisten.
Knelpuntenanalyse
In de eerste vergadering zijn knelpunten en wensen ten aanzien van de richtlijn geïnventariseerd door de werkgroepleden. De werkgroep heeft de aanbevelingen beoordeeld uit de eerdere richtlijn (NVDV, 2014) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door de patiëntenvereniging. Tevens zijn de VIG, ZN, NVZ en NFU uitgenodigd om knelpunten aan te dragen tijdens de eerste bijeenkomst.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep uitgangsvragen opgesteld. Per uitgangsvraag zijn klinisch relevante uitkomstmaten opgesteld, waarbij zowel naar gewenste als ongewenste effecten is gekeken. De werkgroep heeft deze uitkomstmaten gewaardeerd volgens hun relatieve klinisch belang bij de besluitvorming rondom aanbevelingen. Specifieke uitkomstmaten per uitkomstvraag worden in de betreffende paragrafen uitgewerkt. Klinische uitkomstmaten zoals het proportie patiënten die IGA response (clear/almost clear) behaalt en de reductie in ernst van het constitutioneel eczeem (EASI50 en SCORAD50). Maar ook patiënt gerapporteerde uitkomsten zoals afname en/of controle van symptomen (NRS-jeuk), verandering in DLQI score. Met betrekking tot daily practice research is drug survival de meest gebruikte uitkomstmaat. Deze werd meegenomen voor de lange-termijnveiligheid van systemische therapie.
Strategie voor zoeken en selecteren van literatuur
Voor de afzonderlijke uitgangsvragen is aan de hand van specifieke zoektermen een systematische zoekstrategie uitgevoerd in (verschillende) elektronische databases Embase, MEDLINE en Cochrane. In eerste instantie is gezocht naar studies met de hoogste mate van bewijs. De gevonden studies zijn steeds door twee arts-onderzoekers van de NVDV dan wel werkgroepleden onafhankelijk van elkaar geselecteerd op basis van titel en abstract en vooraf opgestelde selectiecriteria. De beoordeling en uiteindelijke selectie op basis van volledige tekst is gedaan door arts-onderzoekers van de NVDV en werkgroepleden. De geselecteerde studies zijn gebruikt om de uitgangsvraag te beantwoorden. De zoekstrategie is te vinden in bijlage B.
Kwaliteitsbeoordeling wetenschappelijk bewijs
De beoordeling van de kwaliteit van het wetenschappelijk bewijs en onderzoeksgegevens is in de (modulaire herziening van de) richtlijn voor het grootste deel tot stand gekomen met de EBRO-methode. De paragraaf ‘Dupilumab’ uit het hoofdstuk ‘systemische immunosuppressieve therapie’ is met de GRADE-methode uitgewerkt net als de paragraaf ‘effectiviteit van ureum bij patiënten met constitutioneel eczeem’ uit het addendum Ureum.
Kwaliteitsbeoordeling wetenschappelijk bewijs middels GRADE
Bij de GRADE-methode (Grading Recommendations Assessment, Development and Evaluation) worden individuele studies systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. [Schünemann 2013]
Tabel 1 geeft een kort overzicht van de indeling van methodologische kwaliteit van het wetenschappelijk bewijs volgens GRADE. De beoordelingen van de methodologische kwaliteit kunt u vinden in de Risk of Bias (RoB)-tabellen, deze zijn op te vragen via de NVDV en/of terug te vinden in bijlage C. Hiervoor is gebruikgemaakt van de Cochrane risk of bias tool. [Higgins 2011] GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag (tabel 1). Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie. [Schünemann, 2013] De kwaliteit van het bewijs per interventie per uitkomstmaat is te vinden in de tabellen met de Summary of Findings (zie bijlage C).
Een volledige uitleg over de GRADE-methode valt buiten het bestek van deze richtlijn, zie hiervoor het ‘GRADE handbook’. [Schünemann 2013, www.gradeworkinggroup.org]
Tabel 1. Indeling van kwaliteit van wetenschappelijk bewijs volgens GRADE
|
GRADE-systeem |
||
|
Kwaliteitsindeling bewijs |
Hoog |
|
|
Redelijk |
|
|
|
Laag |
|
|
|
Zeer laag |
|
|
|
Startkwalificatie |
- Gerandomiseerd onderzoek = hoog - Observationele studie = laag |
|
|
Factoren die de kwaliteit van bewijs kunnen verlagen* |
- Ernstige of zeer ernstige beperkingen in de kwaliteit van de studie - Indirectheid van het bewijs - Belangrijke inconsistentie tussen studies - Imprecisie - Grote kans op ‘publicatiebias’ |
|
|
Factoren die de kwaliteit van bewijs kunnen verhogen** |
- Sterk bewijs voor een associatie – significant relatief risico van > 2 (< 0,5) gebaseerd op consistent bewijs uit twee of meer observationele studies, zonder plausibele ‘confounders’ (+1) - Zeer sterk bewijs voor een associatie – significant relatief risico van > 5 (< 0,2) gebaseerd op direct bewijs zonder belangrijke bedreigingen voor de validiteit (+2) - Bewijs voor een dosis respons gradiënt (+1) - Alle plausibele ‘confounders’ zonder het effect te hebben verminderd (+1) |
|
* Elk criterium kan de kwaliteit verminderen met 1 stap of bij zeer ernstige beperkingen met 2 stappen.
** Verhogen kan alleen indien er geen beperkingen zijn t.a.v. de studiekwaliteit, imprecisie, inconsistentie, indirectheid en publicatiebias
Beoordelen van het niveau van het wetenschappelijke bewijs middels EBRO
Bij de EBRO-methode (Evidence Based RichtlijnOntwikkeling) wordt een andere classificatie voor de beoordeling van de kwaliteit van studies aangehouden (zie tabel 2). [van Everdingen 2004] Hierbij ligt de belangrijkheid van de uitkomstmaten niet van tevoren vast en is er geen vastgelegde procedure voor upgraden en downgraden van bewijs, zoals die bij GRADE geldt.
Tabel 2. Indeling van methodologische kwaliteit van individuele studies volgens EBRO
|
Kwaliteit |
Interventie |
Diagnostisch accuratesse- onderzoek |
Schade/ bijwerkingen*, etiologie, prognose |
|
A1 |
Systematische review van ten minste twee onafhankelijk van elkaar uitgevoerde onderzoeken van A2-niveau |
||
|
A2
|
Gerandomiseerd dubbelblind vergelijkend klinisch onderzoek van goede kwaliteit van voldoende omvang |
Onderzoek ten opzichte van een referentietest (een ‘gouden standaard’) met tevoren gedefinieerde afkapwaarden en onafhankelijke beoordeling van de resultaten van test en gouden standaard, betreffende een voldoende grote serie van opeenvolgende patiënten die allen de index- en referentietest hebben gehad |
Prospectief cohortonderzoek van voldoende omvang en follow-up, waarbij adequaat gecontroleerd is voor ‘confounding’ en selectieve follow-up voldoende is uitgesloten. |
|
B |
Vergelijkend onderzoek, maar niet met alle kenmerken als genoemd onder A2 (hieronder valt ook patiënt-controleonderzoek, cohortonderzoek) |
Onderzoek ten opzichte van een referentietest, maar niet met alle kenmerken die onder A2 zijn genoemd |
Prospectief cohortonderzoek, maar niet met alle kenmerken als genoemd onder A2 of retrospectief cohortonderzoek of patiënt-controleonderzoek |
|
C |
Niet-vergelijkend onderzoek |
||
|
D |
Mening van deskundigen |
||
*Deze classificatie is alleen van toepassing in situaties waarin om ethische of andere redenen gecontroleerde trials niet mogelijk zijn. Zijn die wel mogelijk dan geldt de classificatie voor interventies.
Bij het werken volgens de EBRO-methode zijn op basis van de beschikbare literatuur een of meerdere conclusies geformuleerd. Afhankelijk van het aantal onderzoeken en de mate van bewijs is een niveau van bewijskracht toegekend aan de conclusie (zie tabel 3). [van Everdingen 2004]
Tabel 3. Niveau van conclusies volgens EBRO
|
Niveau |
Conclusie gebaseerd op |
|
1 |
Onderzoek van niveau A1 of ten minste 2 onafhankelijk van elkaar uitgevoerde onderzoeken van niveau A2 |
|
2 |
1 onderzoek van niveau A2 of ten minste 2 onafhankelijk van elkaar uitgevoerde onderzoeken van niveau B |
|
3 |
1 onderzoek van niveau B of C |
|
4 |
Mening van deskundigen |
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde studies zijn overzichtelijk weergegeven als ‘karakteristieken en resultaten van geïncludeerde studies’ zie bijlage C. De belangrijkste bevindingen uit de literatuur met betrekking op de vooraf opgestelde uitkomstmaten zijn beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies zijn de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Formuleren van conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de EBRO- of GRADE-methode. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten werden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overige overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn voor zowel de GRADE- en EBRO-methodiek gebaseerd op het beschikbare wetenschappelijke bewijs, de belangrijkste overige overwegingen en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht of het niveau van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling.
Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht (zie bijlage G).
Commentaar- en autorisatiefase
De conceptrichtlijn is aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren zijn verzameld in een commentaarformulier/tabel en besproken met de werkgroep. Naar aanleiding van de commentaren is de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn is aan de betrokken (wetenschappelijke) verenigingen en (patiënt)organisaties voorgelegd ter autorisatie en door hen geautoriseerd dan wel geaccordeerd. Zie daarvoor paragraaf ‘Autorisatie’.
Autorisatie
In 2014 werd de gehele richtlijn geautoriseerd door: Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV), Nederlandse Vereniging voor Kindergeneeskunde (NVK), Nederlandse Vereniging voor Allergologie (NVvA), Nederlands Huisartsen Genootschap (NHG), Nederlands Instituut van Psychologen (NIP), Nederlandse Vereniging voor Arbeids- en Bedrijfsgeneeskunde (NVAB), Verpleegkundigen & Verzorgenden Nederland (V&VN) en de Vereniging voor Mensen met Constitutioneel Eczeem (VMCE)
De in 2019 herziene modules in deze richtlijn werden geautoriseerd door: Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV), Nederlandse Vereniging voor Allergologie (NVvA) en de Vereniging voor Mensen met Constitutioneel Eczeem (VMCE) op 15 november 2019. De V&VN en HPN onderschrijven de richtlijn Het Nederlands Huisartsen Genootschap (NHG) gaf een verklaring van geen bezwaar af. De Nederlandse Vereniging voor Kindergeneeskunde (NVK) heeft de richtlijn geautoriseerd onder voorwaarde dat de module over monitoring en dosering van systemische en immunosuppressieve therapie bij kinderen herzien wordt conform de aanbevelingen van het Kinderformularium én de NVK richtlijn Medicamenteuze behandeling van kinderen met juveniele idiopathische artritis.
Literatuur
- Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
- Higgins JPT, Green S (editors). Cochrane Handbook for Systematic Reviews of Interventions Version 5.1.0 [updated March 2011]. The Cochrane Collaboration, 2011. Available from https://training.cochrane.org/handbook
- Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwaliteit. Online beschikbaar op http://richtlijnendatabase.nl/
- van Everdingen JJE, Burgers JS, Assendelft WJJ, et al. Evidence-based richtlijnontwikkeling. Bohn Stafleu Van Loghum 2004.
- Roekevisch E, Spuls PI, Kuester D, et al. Efficacy and safety of systemic treatments for moderate-to-severe atopic dermatitis: A systematic review. J Allergy Clin Immunol 2014;133(2):429-438
- Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
- Sidbury R, Davis DM, Cohen DE et al. American Academy of Dermatology. Guidelines of care for the management of atopic dermatitis: section 3. Management and treatment with phototherapy and systemic agents. J Am Acad Dermatol. 2014 Aug;71(2):327-49.



