Uitgebreidheid primaire resectie CC
Uitgangsvraag
Deze module omvat de volgende deelvragen:
- Wat is de meerwaarde van complete mesocolische excisie (CME)?
- Hoe uitgebreid dient de lymfklierdissectie in verticale richting te worden uitgevoerd (D2 of D3)?
- Is er een indicatie voor profylactische adnexextripatie?
- Welke implicaties hebben erfelijke predispositie (BRCA of MSH2 kiembaan mutatie) en inflammatoire darmziekten voor de uitgebreidheid van de resectie?
- Wanneer is een multiviscerale resectie geïndiceerd?
Aanbeveling
Voer een volledige inspectie en zo mogelijk palpatie uit van de buikholte bij aanvang van een geplande colonresectie voor coloncarcinoom ter uitsluiting van synchrone peritoneale metastasen, ovariummetastasen en levermetastasen. Bepaal de PCI score en neem een biopt indien peritoneale metastasen worden gevonden.
Voer de colonresectie uit volgens het CME principe, met dissectie in de anatomische scheidingsvlakken ter verkrijging van een intact mesenterium, en met centrale ligate van de segmentele vaten resulterend in een D2 lymfklierdissectie.
Breidt de resectie van rechtszijdig coloncarcinoom uit met een centrale lymfklierdissectie (D3) tot de links laterale zijde van de a. mesenterica superior uitsluitend bij pathologische klieren in het D3 gebied op preoperatieve CT. In dergelijke gevallen is relevante expertise vereist met zo nodig verwijzing naar een tertiair centrum.
Voer dubbelzijdige adnexextirpatie uit bij macroscopisch afwijkend aspect. Overweeg profylactische adnexextirpatie bij hoog risico groepen (BRCA of MSH2 kiembaan mutatie) in een gedeeld besluitvormingsproces. Voer profylactische adnexextirpatie in afwezigheid van risicofactoren alleen uit in studieverband. Voor overwegingen rondom oppertunistische salpingectomie wordt verwezen naar de richtlijn “het vergrote ovarium” (cluster benigne gynaecologie).
Verricht voor een coloncarcinoom bij Colitis Ulcerosa een sub-totale colectomie of proctocolectomie volgens CME principes. Overweeg een segmentresectie volgens CME voor een coloncarcinoom bij Crohnse colitis als alternatief voor (procto)colectomie binnen gedeelde besluitvorming.
Voer een en bloc multiviscerale resectie uit van aangrenzende structuren die adhesief of door tumor ingroei verbonden zijn met het colon en vermeld dit in de PA aanvraag.
Overwegingen
CME is een initiatief voor standaardisatie van de chirurgische behandeling van het coloncarcinoom. Dissectie in de embryologische scheidingsvlakken mag als standaard worden verondersteld in de huidige colorectale chirurgie en is daarom geen noviteit maar ‘good surgical practice’. In een vergelijkende studie van standaard colon resectie in Leeds met de CME techniek van Erlangen (West, 2010) hadden CME preparaten vaker een intact mesocolon en een groter mesocolisch oppervlakte. De pathologische gradering van het mesocolon, in analogie aan die van het TME preparaat, bleek geassocieerd met overleving (West, 2008).
In de Nederlands praktijk streven we naar CME met een niveau D2 lymfklierdissectie. Het beste bewijs hiervoor komt uit een studie waarin uitkomsten tussen vier Deense ziekenhuizen werd vergeleken, waarbij één Deens ziekenhuis CME uitvoerde en drie ziekenhuizen een ‘standaard’ resectie voor rechtszijdig coloncarcinoom uitvoerden (Bertelsen, 2019). Daarin bleek de 5,2-jaar cumulatieve incidentie van recidief 9,7% na CME en 17,9% na beperkt mesocolische resectie, en een reductie in recidief kans werd voor zowel stadium 1, 2, als 3 gezien. Dit toont aan dat verbetering in oncologische uitkomsten van CME onafhankelijk is van lymfklierstatus. Pathofysiologisch kan dit mogelijk verklaard worden door beschadiging of transectie van het mesocolon op relatief korte afstand van de primaire tumor bij een ‘non-CME’ resectie, ter plaatse waar tumorcellen zich kunnen bevinden in de vorm van EMVI, tumor deposities of perineurale invasie. Dit kan vervolgens tumor spill veroorzaken met uitgroei tot locoregionaal recidief inclusief peritoneale metastasen. Hoewel er een 5% verschil in algehele overleving werd gevonden, was dit niet statistisch significant. In de Duitse RESECTAT populatie studie werd CME (gedocumenteerde dissectie van de v. mesenterica superior) met non-CME vergeleken in 1004 patiënten met rechtszijdig coloncarcinoom uit 53 centra, waarbij 88% een open resectie onderging (Benz, 2022). Voor stadium 1-3 samen werd een vergelijkbare 5-jaar algehele overleving gevonden (81% vs 78%), en voor stadium 3 een significant betere 5-jaar overleving voor CME (78% vs. 65%, HR 0,61 (0,39-0,95). Bij een grote Nederlandse multicenter inventarisatie (Grüter, 2024) bleek nog een kwaliteitsslag te behalen bij rechtszijdig coloncarcinoom aangezien in slechts 23% sprake was van een optimaal CME preparaat (Benz 0). Een Deense studie met postoperatieve beeldvorming (Munkedal, 2017) heeft laten zien dat nog een resterende segmentele arteriële stomp kon worden gevonden met een mediane lengte van 49 mm voor rechtszijdige en 31 mm voor linkszijdige colonresecties. Daarmee blijkt in de praktijk een intentionele D2 vaak uit te monden in een dissectie op het niveau ergens tussen D1 en D2 in. Incomplete mesocolische excisie lijkt met name een probleem voor rechtszijdige resecties, vanwege de vereiste dissectie in het vlak ventraal van het duodenum en de pancreas kop, en van de v. mesenterica superior en veneuze takken van de lis van Henle om een optimale D2 dissectie te verkrijgen. Adequate training en proctoring lijkt hiervoor relevant, en daarom is in Nederland het RIGHT project opgezet (Grüter, 2023).
Hoewel er in een beperkt percentage centrale lymfkliermetastasen worden gevonden na een D3 dissectie, is het de vraag of resectie hiervan een onafhankelijke invloed heeft op oncologische uitkomst naast andere kenmerken van een tumor met dergelijke vergevorderde lymfkliermetastasering. De Chinese RELARC trial randomiseerde 1072 patiënten tussen CME D2 of CME D3 resectie (Lu, 2024). Er werd geen significant verschil in 3-jaar DFS en OS gevonden. Aangezien centrale lymfklierdissectie extra morbiditeit met zich mee kan brengen, met name bij rechtszijdige tumoren (Bertelsen, 2016), en geen doorslaggevend bewijs is geleverd voor de oncologische meerwaarde, wordt aanbevolen om niet routinematige D3 dissecties uit te voeren over de mesenterica superior vaten. Alleen in de zeldzame gevallen (<2%) dat er pathologische klieren in het D3 gebied worden gezien op preoperatieve CT, kan worden overwogen om de verticales dissectie wel uit te breiden tot D3 niveau voor locoregionale controle (Sammour, 2020). Hiervoor lijkt verwijzing naar een centrum met desbetreffende expertise geïndiceerd.
Voor het uitvoeren van een preventieve adnexextirpatie (ovariëctomie inclusief de tubae) worden als argumenten de reductie in kans op ovariële metastasen, reductie in kans op het ontstaan van ovariumcarcinoom, en de minimale chirurgische procedure met kleine kans op chirurgische morbiditeit genoemd. Er is één oude kleine RCT gepubliceerd waarin 155 patiënten met colorectaal carcinoom werden gerandomiseerd tussen wel of niet profylactische ovariectomie (Young-Fadok, 1998). De studie was underpowered om verschil in overleving aan te tonen. Ongeveer 1,3% van de vrouwen ontwikkelt in haar leven ovariumcarcinoom, meestal ontstaan in de tubae. Vanwege zeer langzame vooruitgang in curatie van ovariumcarcinoom, komt steeds meer nadruk op primaire preventie te liggen.
Preventief verwijderen van de tubae (zonder ovarium) wordt opportunistische salpingectomie genoemd. Dit kan besproken worden bij vrouwen die een abdominale ingreep ondergaan vanwege het risico-reducerend effect op eierstokkanker (hoewel nog bewijs van lage kwaliteit) zonder dat dit chirurgische complicaties verhoogd. De effecten op lange termijn ovariële reserve zijn nog niet bekend. Het verwijderen van zowel de tubae als het ovarium bij postmenopauzale patiënten met een colorectaal carcinoom om ook het optreden van ovarium metastasen te reduceren wordt onderzocht in een Nederlandse patiënt preferentie studie (van der Meer, 2022). Argumenten tegen preventieve adnexextirpatie zijn de hoge number ‘needed to treat’, de niet aangetoonde coloncarcinoom specifieke overlevingswinst, en de hormonale verstoring (vooral premenopausaal, maar ook postmenopausaal) met secundaire gevolgen (onder andere hart- en vaatziekten en sexuele functie verstoringen). Bij oudere patienten moet specifiek de resterende levensverwachting en resterend life-time risico op ovariumcarcinoom worden meegewogen in een beslissing over preventieve adnexextirpatie. Bij hoog risico groepen (erfelijke predispositie zoals BRCA mutatie, MSH2 mutatie) zou in een gedeelde besluitvorming met patiënten een preventieve adnexextirpatie samen met de electieve resectie van het coloncarcinoom kunnen worden besproken (Berek, 2010). Bij zowel pre- als postmenopauzale vrouwen zonder risicofactoren moet terughoudend met profylactische adnexextirpatie worden omgegaan bij afwezigheid van bewezen oncologisch voordeel, en zou dit bij voorkeur in studieverband moeten plaatsvinden.
Indien één ovarium macroscopisch afwijkend is, dient een dubbelzijdige adnexextirpatie te worden uitgevoerd.
Voor resectie van een cT4N0-2M0 coloncarcinoom is, zoals voor iedere oncologische resectie, de R0 status een belangrijke voorspeller voor de overleving. Aangezien tumorinfiltratie peroperatief moeilijk is te onderscheiden van reactieve benigne adhesies wordt geadviseerd om bij twijfel een multiviscerale resectie uit te voeren.
Patiënten met inflammatoire darmziekten (IBD) die een coloncarcinoom ontwikkelen, hebben een verhoogde kans op lokalisaties van hooggradige dysplasie of zelfs invasieve groei elders in het colon of rectum. Slechts bij uitzondering betreft het een sporadisch carcinoom niet in het kader van IBD. Daarom wordt in de Europese richtlijnen geadviseerd om een protocolectomie te doen. Maar meer recente studies tonen aan dat dit risico voorheen misschien te hoog werd ingeschat. Als alternatief kan worden overwogen om een colectomie met ileo-rectale anastomose of zelfs een segmentele resectie te doen met goede endoscopisch follow-up van het rectum en eventueel resterend colon. De voor- en nadelen moeten dan goed worden besproken met de patiënt.
Samenvatting van nationale data en populatiestudies
Vanuit de Eindhovense kankerregistratie werd gerapporteerd dat het aantal peroperatief gevonden peritoneale metastasen ten tijde van resectie van de primaire tumor 1,4% bedroeg voor laparoscopische resecties, 5,0 % voor open resecties en 3,3% voor geconverteerde resecties (Thomassen, 2014). Ook na correctie voor confounders bleef laparoscopische resectie significant geassocieerd met een lagere kans op het detecteren van peritoneale metastasen (OR 0,42). Derhalve wordt expliciet geadviseerd om onafhankelijk van de chirurgische benadering een zorgvuldige inspectie van het abdomen uit te voeren.
Onderbouwing
Achtergrond
Ter verbetering van de oncologische uitkomsten van segmentele oncologische resectie van een cT1-4 N0/+ coloncarcinoom is het concept complete mesocolische excisie (CME) geïntroduceerd. Dit is analoog aan totale mesorectale excisie (TME) voor de behandeling van het rectumcarcinoom, waarbij met scherpe dissectie in de embryologische scheidingsvlakken een compleet en intact mesorectum wordt verkregen.
CME is geïntroduceerd samen met een centrale lymfklierdissectie (D3), wat tot veel verwarring in terminologie heeft geleid. CME voor coloncarcinoom omvat de volgende 3 componenten:
- vrijmaken van het mesocolon door middel van een scherpe dissectie over het retroperitoneum waarbij de mesocolische fascie intact blijft;
- centraal ligeren van de segmentele vaten: (a. en v. ileocolica, rechter v. colica en eventueel aanwezige a. colica dextra, relevante zijtakken of hoofdstam van a. en v. colica media, a. colica sinistra of sigmoidale aftakkingen en v. mesenterica inferior);
- resectie van voldoende lengte colon proximaal en distaal van de tumor (tenminste 5 cm) voor het verwijderen van de pericolische lymfklieren (longitudinale disseminatie).
De lymfklierdissectie in verticale richting tot aan de basis van de segmentele aftakkingen (D2), als onderdeel van CME, kan worden uitgebreid met een centrale lymfklierdissectie (D3), waarbij ook al het mesocolische vet ventraal van de v. mesenterica superior en a. mesenterica superior (rechtszijdig) of ter plaatse van de a. mesenterica inferior tussen de a. colica sinistra en aorta (linkszijdig) wordt meegenomen. De toegevoegde waarde van een D3 dissectie dient apart beoordeeld te worden van de meerwaarde van een CME D2 dissectie.
Voor wat betreft uitgebreidheid van de resectie voor coloncarcinoom is er discussie over het preventief meenemen van extra-intestinale organen (zoals de adnexen) om uitgroei van occulte metastasen ter plaatse te kunnen voorkómen. Daarnaast kan de uitgebreidheid bepaald worden door erfelijke predispositie of bijkomende ziekten (Crohn, Colitis Ulcerosa) of door lokale tumordoorgroei in omliggende weefsels.
Conclusies / Summary of Findings
Samenvatting literatuur
Samenvatting van internationale richtlijnen en consensusdocumenten
CME en niveau van verticale lymfklierdissectie (D2 vs D3)
De SIGN richtlijn (2016) beveelt radicale resectie volgens CME principes aan met ‘flush’ ligatie van de colische vaten. Er wordt geen specifieke uitspraak over de uitgebreidheid van de verticale mesocolische lymfklierdissectie gedaan.
De ASCRS richtlijn (Vogel, 2022) beschrijft dat het mesocolon van het tumor bevattende segment verwijderd moet worden tot aan de basis van de voedende vaten. Verder wordt geconcludeerd dat er onvoldoende literatuur is die een routinematige D3 dissectie rechtvaardigt indien er klinisch geen verdenking is op verdachte centrale lymfklieren. Wel wordt aanbevolen om klinisch verdachte D3 lymfklieren te reseceren.
In een Nederlandse Delphi studie onder 76 chirurgen uit 43 centra werd >80% consensus bereikt over de uitgebreidheid van resectie bij een rechtszijdige coloncarcinoom, bestaande uit een CME D2 dissectie met vrijleggen van de v. mesenterica superior en de lis van Henle met centrale ligatie van de segmentele vaten (Grüter, 2024).
Profylactische adnexextirpatie
De ASCRS richtlijn (Vogel, 2022) beveelt alleen ovariëctomie aan indien macroscopisch afwijkend of bij directe tumor doorgroei. Routinematige profylactische ovariëctomie wordt niet aanbevolen, maar zou wel kunnen worden overwogen bij erfelijke predispositie voor ovariumcarcinoom of postmenopauzale vrouwen.
Erfelijke predispositie en inflammatoire darmziekten
Overwegingen voor segmentele colonresectie of totale colectomie bij patiënten met Lynch syndroom en een coloncarcinoom staan beschreven in de richtlijn erfelijk darmkanker. Bij coloncarcinoom in het kader van familiaire adenomateuze polyposis (FAP) is proctocolectomie de voorkeursbehandeling, maar voor de andere polyposis syndromen (atypische familiaire adenomateuze polyposis (AFAP), MUTYH-associated polyposis (MAP), serrated polyposis) worden geen uitspraken gedaan over de uitgebreidheid van resectie. De ECCO richtlijn (Adamina, 2024) suggereert dat voor patiënten met een coloncarcinoom bij een Crohnse colitis, een proctocolectomie kan worden uitgevoerd, maar dat de hoge kans op metachrone carcinomen na segmentele resectie voorheen waarschijnlijk is overschat. Daarom is segmentele resectie met endoscopische surveillance ook een optie in geselecteerde patiënten na gedeelde besluitvorming of in geval van hoog operatie risico.
De ECCO richtlijn (Øresland, 2015) adviseert een proctocolectomie met centrale ligatie van alle segmentele vaten voor patiënten met een coloncarcinoom bij colitis ulcerosa. In geselecteerde gevallen kan na gedeelde besluitvorming voor een colectomie worden gekozen, bijvoorbeeld bij een proximaal carcinoom met milde ziekte in het rectum.
Multiviscerale resectie
De ASCRS richtlijn (Vogel, 2022) adviseert een en-bloc resectie van aangrenzende organen indien deze adhesief zijn of macroscopisch geïnfiltreerd door het coloncarcinoom, gezien er in 34-84% daadwerkelijke pathologische invasie wordt aangetoond.
Samenvatting van systematische reviews en meta-analyses
PICO 1 (CME versus standaard chirurgie)
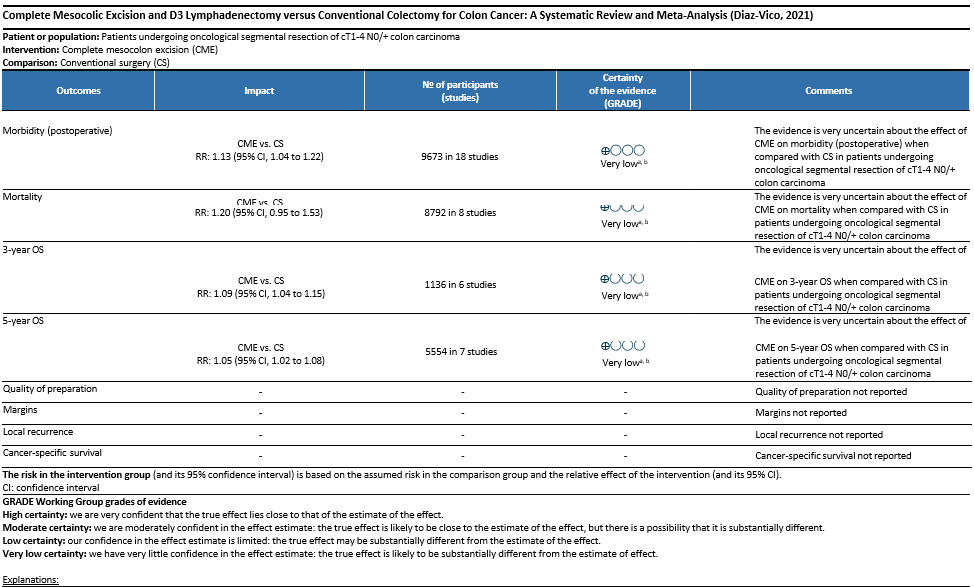
Diaz-Vico verrichtte een systematische review van 27 studies (Diaz Vico, 2021). Er werd meer postoperatieve morbiditeit na CME (RR 1.13 (1.04-1.22) gevonden, maar vergelijkbaar risico op naadlekkage (RR 1.11 (0.89–1.38)) en mortaliteit (RR 1.20 (0.95; 1.53)). CME chirurgie resulteerde in meer gereseceerde darmlengte (RR 0.15 (0.01; 0.30), groter mesocolisch oppervlakte (RR 1.07 (0.78; 1.35)) en hoger aantal lymfklieren (RR 0.76 (0.66; 0.85)). Er werd een langere 3-jaar en 5-jaar algehele overleving gevonden na CME (respectievelijk RR 1.09 (1.04–1.15)) en RR 1.05, ( 1.02–1.08), p = 0.02), met een lagere kans op lokaal recidief (RR 0.35 (0.24-0.51)) en afstand metastasen (RR 0.71 (0.60–0.85)).
PICO 2 (D3 dissectie versus D2 dissectie)
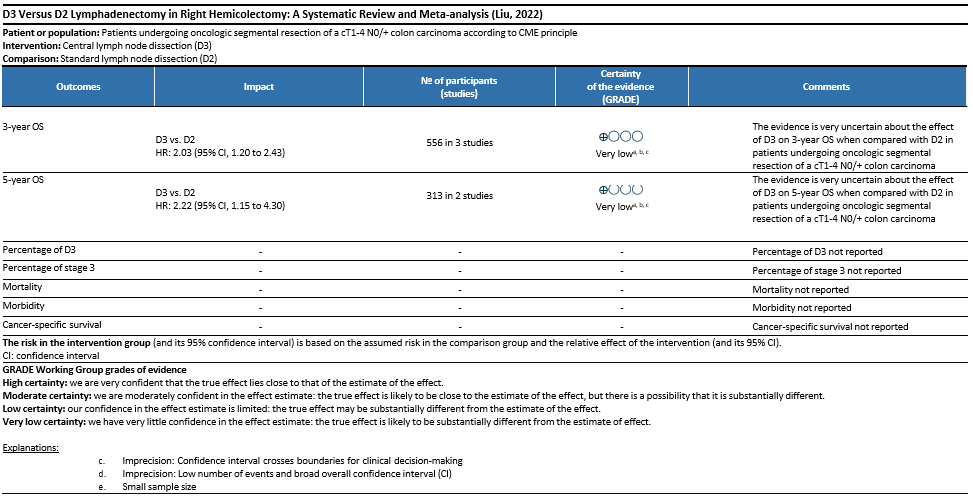
Een systematische review van 7 cohort studies (Liu, 2022) suggereert dat er een betere ziektevrije en algehele overleving wordt gevonden na D3 dissectie in vergelijking met D2 dissectie, maar dat RCTs nodig zijn.
PICO 3 (profylactische adnexextirpatie)
Een meta-analyse van Yoon (Yoon, 2016) laat zien dat dubbelzijdige tubectomie in de algemene populatie leidt tot een afname van 50% tot 70% in het optreden van
ovariumcarcinoom. Er werd geen vervroegde overgang gezien vanwege het in situ laten van het ovarium. Een literatuuronderzoek van Van der Meer (2021) onderzocht de incidentie van ovariummetastasen bij vrouwen met colorectaal carcinoom onder de leeftijd van 50 jaar. Op basis van 12 retrospectieve en 2 prospectieve studies, werden bij 157 van totaal 3379 jonge patienten (4,6%) op enig moment ovarium metastasen gevonden (synchroon danwel metachroon). Het is niet duidelijk of deze ovariummetastasen gediagnosticeerd werden op basis van beeldvorming, macroscopisch verdacht aspekt of lokale doorgroei met ovariele betrokkenheid tijdens operatie, of als occulte laesie tijdens pathologisch onderzoek van een profylactisch verwijderd ovarium. Een meta-analyse van Wei (2023) laat zien dat in 13 van 16 studies de seksuele functie was verminderd door profylactische salpingo-oophorectomie.
Zoeken en selecteren
PICO 1 (CME versus standaard colonresectie)
| P: | Patiënten die een oncologische segmentele resectie van een cT1-4 N0/+ coloncarcinoom ondergaan |
| I: | Complete mesocolische excisie (CME) |
| C: | ‘standaard’ resectie |
| O: | Kwaliteit van het preparaat, marges, morbiditeit, mortaliteit, locoregionaal recidief, kanker-specifieke overleving, totale overleving |
PICO 2 (Centrale (D3) versus standaard dissectie (D2))
| P: | Patiënten die een oncologische segmentele resectie van een cT1-4 N0/+ coloncarcinoom ondergaan volgens CME principe |
| I: | Centrale lymfklierdissectie (D3) |
| C: | Standaard lymfklier dissectie (D2) |
| O: | Percentage (geïsoleerde) tumor-positieve centrale lymfklieren (D3), percentage stadium 3, morbiditeit, mortaliteit, locoregionaal recidief, kanker-specifieke overleving, totale overleving |
PICO 3 (profylactische adnexextirpatie)
| P: | Patiënten die een in opzet curatieve resectie van een coloncarcinoom ondergaan |
| I: | Profylactische adnexextirpatie (ovarium en tuba) |
| C: | Geen adnexextirpatie |
| O: | Percentage ovariummetastasen, incidentie van ovariumcarcinoom, morbiditeit, kanker-specifieke overleving, totale overleving |
Uitkomstmaten
- Kwaliteit van het preparaat uitgedrukt in niveau van de resectie (mesocolische fascie, intramesocolisch en muscularis propria) en compleetheid van het preparaat (bijvoorbeeld volgens Benz classificatie) (Benz, 2019).
- Afstand van de tumor tot het dichtstbijzijnde transversale snijvlak, radiaire snijvlak tegenover de tumor, en het proximale of distale resectievlak.
- Percentage positieve centrale lymfklieren in het geval van een D3 dissectie, al dan niet in combinatie met positieve D1-2 lymfklieren.4Postoperatieve morbiditeit.
- Postoperatieve mortaliteit.
- Locoregionaal recidief.
- Kankerspecifieke overleving.
- Totale overleving.
Referenties
- Adamina M, Minozzi S, Warusavitarne J, Buskens CJ, Chaparro M, Verstockt B, Kopylov U, Yanai H, Vavricka SR, Sigall-Boneh R, Sica GS, Reenaers C, Peros G, Papamichael K, Noor N, Moran GW, Maaser C, Luglio G, Kotze PG, Kobayashi T, Karmiris K, Kapizioni C, Iqbal N, Iacucci M, Holubar S, Hanzel J, Sabino JG, Gisbert JP, Fiorino G, Fidalgo C, Ellu P, El-Hussuna A, de Groof J, Czuber-Dochan W, Casanova MJ, Burisch J, Brown SR, Bislenghi G, Bettenworth D, Battat R, Atreya R, Allocca M, Agrawal M, Raine T, Gordon H, Myrelid P. ECCO Guidelines on Therapeutics in Crohn's Disease: Surgical Treatment. J Crohns Colitis. 2024 Oct 15;18(10):1556-1582. doi: 10.1093/ecco-cc/jjae089. PMID: 38878002.
- Benz SR, Feder IS, Vollmer S, Tam Y, Reinacher-Schick A, Denz R, Hohenberger W, Lippert H, Tannapfel A, Stricker I. Complete mesocolic excision for right colonic cancer: prospective multicentre study. Br J Surg. 2022 Dec 13;110(1):98-105. doi: 10.1093/bjs/znac379. PMID: 36369986; PMCID: PMC10364501.
- Benz S, Tannapfel A, Tam Y, Grünenwald A, Vollmer S, Stricker I. Proposal of a new classification system for 20 complete mesocolic excison in right-sided colon cancer. Tech Coloproctol. 2019 Mar;23(3):251-257. doi:10.1007/s10151-019-01949-4. Epub 2019 Mar 5. PMID: 30838463.
- Berek JS, Chalas E, Edelson M, Moore DH, Burke WM, Cliby WA, Berchuck A;Society of Gynecologic Oncologists Clinical Practice Committee. Prophylactic and risk-reducing bilateral salpingo-oophorectomy: recommendations based on risk of ovarian cancer. Obstet Gynecol. 2010 Sep;116(3):733-43. doi:10.1097/AOG.0b013e3181ec5fc1. Review. PubMed PMID: 20733460.
- Bertelsen CA, Kirkegaard-Klitbo A, Nielsen M, Leotta SM, Daisuke F, Gögenur I. Pattern of Colon Cancer Lymph Node Metastases in Patients Undergoing Central Mesocolic Lymph Node Excision: A Systematic Review. Dis Colon Rectum. 2016 Dec;59(12):1209-1221. Review. PubMed PMID: 27824707.
- Bertelsen CA, Neuenschwander AU, Jansen JE, Kirkegaard-Klitbo A, Tenma JR, Wilhelmsen M, Rasmussen LA, Jepsen LV, Kristensen B, Gögenur I; Copenhagen Complete Mesocolic Excision Study (COMES); Danish Colorectal Cancer Group (DCCG). Short-term outcomes after complete mesocolic excision compared with 'conventional' colonic cancer surgery. Br J Surg. 2016 Apr;103(5):581-9. doi:10.1002/bjs.10083. Epub 2016 Jan 18. PubMed PMID: 26780563.
- Bertelsen CA, Neuenschwander AU, Jansen JE, Tenma JR, Wilhelmsen M, Kirkegaard-Klitbo A, Iversen ER, Bols B, Ingeholm P, Rasmussen LA, Jepsen LV, Born PW, Kristensen B, Kleif J. 5-year outcome after complete mesocolic excision for right-sided colon cancer: a population-based cohort study. Lancet Oncol. 2019 Nov;20(11):1556-1565. doi: 10.1016/S1470-2045(19)30485-1. Epub 2019 Sep 13. Erratum in: Lancet Oncol. 2020 Aug;21(8):e372. doi:10.1016/S1470-2045(20)30378-8. PMID: 31526695.
- Díaz-Vico T, Fernández-Hevia M, Suárez-Sánchez A, García-Gutiérrez C, Mihic-Góngora L, Fernández-Martínez D, Álvarez-Pérez JA, Otero-Díez JL, Granero-Trancón JE, García-Flórez LJ. Complete Mesocolic Excision and D3 Lymphadenectomy versus Conventional Colectomy for Colon Cancer: A Systematic Review and Meta- Analysis. Ann Surg Oncol. 2021 Dec;28(13):8823-8837. doi: 10.1245/s10434-021-10186-9. Epub 2021 Jun 4. PMID: 34089109.
- Grüter AAJ, Coblijn UK, Toorenvliet BR, Tanis PJ, Tuynman JB; Right Collaborators Group. National implementation of an optimal standardised technique for right-sided colon cancer: protocol of an interventional sequential cohort study (Right study). Tech Coloproctol. 2023 Nov;27(11):1083-1090. doi: 10.1007/s10151-023-02801-6. Epub 2023 Apr 25. PMID: 37097330; PMCID: PMC10562307.
- Grüter AAJ, Jongsma WA, Leone N, Barai H, Toorenvliet BR, Tanis PJ, Tuynman JB; RIGHT Collaborators Group. Nationwide variations in the execution of minimally invasive right hemicolectomy and short-term outcomes: first phase of the RIGHT study. Br J Surg. 2024 Oct 30;111(11):znae291. doi: 10.1093/bjs/znae291. PMID: 39556596; PMCID: PMC11572717.
- Grüter AAJ, Toorenvliet BR, Belgers EHJ, Belt EJT, van Duijvendijk P, Hoff C, Hompes R, Smits AB, van de Ven AWH, van Westreenen HL, Bonjer HJ, Tanis PJ, Tuynman JB; Right collaborators group. Nationwide standardization of minimally invasive right hemicolectomy for colon cancer and development and validation of a video-based competency assessment tool (the Right study). Br J Surg. 2024 Jan 3;111(1):znad404. doi: 10.1093/bjs/znad404. PMID: 38103184; PMCID: PMC10763527.
- Liu S, Li L, Sun H, Chen B, Yu M, Zhong M. D3 Versus D2 Lymphadenectomy in Right Hemicolectomy: A Systematic Review and Meta-analysis. Surg Innov. 2022 Jun;29(3):416-425. doi: 10.1177/15533506211060230. Epub 2022 Feb 1. PMID: 35102792.
- Lu J, Xing J, Zang L, Zhang C, Xu L, Zhang G, He Z, Sun Y, Feng Y, Du X, Hu S, Chi P, Huang Y, Wang Z, Zhong M, Wu A, Zhu A, Li F, Xu J, Kang L, Suo J, Deng H, Ye Y, Ding K, Xu T, Zhang Y, Zhang Z, Zheng M, Su X, Xiao Y; RELARC study group. Extent of Lymphadenectomy for Surgical Management of Right-Sided Colon Cancer:The Randomized Phase III RELARC Trial. J Clin Oncol. 2024 Nov 20;42(33):3957-3966. doi:10.1200/JCO.24.00393. Epub 2024 Aug 27. PMID: 39190853.
- Munkedal DLE, Rosenkilde M, Nielsen DT, Sommer T, West NP, Laurberg S. Radiological and pathological evaluation of the level of arterial division after colon cancer surgery. Colorectal Dis. 2017 Jul;19(7):O238- O245. doi: 10.1111/codi.13756. PubMed PMID: 28590033.
- Øresland T, Bemelman WA, Sampietro GM, Spinelli A, Windsor A, Ferrante M, Marteau P, Zmora O, Kotze PG, Espin-Basany E, Tiret E, Sica G, Panis Y, Faerden AE, Biancone L, Angriman I, Serclova Z, de Buck van Overstraeten A, Gionchetti P, Stassen L, Warusavitarne J, Adamina M, Dignass A, Eliakim R, Magro F, D'Hoore A; European Crohn's and Colitis Organisation (ECCO). European evidence based consensus on surgery for ulcerative colitis. J Crohns Colitis. 2015 Jan;9(1):4-25. doi: 10.1016/j.crohns.2014.08.012. PubMed PMID: 25304060.
- Sammour T, Malakorn S, Thampy R, Kaur H, Bednarski BK, Messick CA, Taggart M, Chang GJ, You YN. Selective central vascular ligation (D3 lymphadenectomy) in patients undergoing minimally invasive complete mesocolic excision for colon cancer: optimizing the risk-benefit equation. Colorectal Dis. 2020 Jan;22(1):53-61. doi: 10.1111/codi.14794. Epub 2019 Aug 18. PMID: 31356721.
- Scottish Intercollegiate Guidelines Network (SIGN). Diagnosis and management of colorectal cancer. Edinburgh: SIGN; 2011 (revised 2016). (SIGN publication no. 126). Available form: http://www.sign.ac.uk.
- Thomassen, I; van Gestel, YRBM; Aalbers, AGJ; van Oudheusden, TR; Wegdam, JA; Lemmens, VEPP; de Hingh, IHJT Peritoneal carcinomatosis is less frequently diagnosed during laparoscopic surgery compared to open surgery in patients with colorectal cancer. Eur J Surg Oncol, 2014 vol. 40(5) pp. 511-514.
- Van der Meer R, de Hingh IHJT, Bloemen JG, Janssen L, Roumen RMH. Role Of Ovarian Metastases In Colorectal Cancer (ROMIC): a Dutch study protocol to evaluate the effect of prophylactic salpingo-oophorectomy in postmenopausal women. BMC Womens Health. 2022 Nov 11;22(1):441. doi: 10.1186/s12905-022-02040-PMID: 36369055; PMCID: PMC9652988.
- van der Meer R, Bakkers C, Rostamkhan E, de Hingh I, Roumen R. Ovarian metastases from colorectal cancer in younwomen: a systematic review of the literature. Int J Colorectal Dis. 2021 Dec;36(12):2567-2575. doi:10.1007/s00384-021-04012-7. Epub 2021 Aug 25. PMID: 34432125.
- Vogel JD, Felder SI, Bhama AR, Hawkins AT, Langenfeld SJ, Shaffer VO, Thorsen AJ, Weiser MR, Chang GJ, Lightner AL, Feingold DL, Paquette IM. The American Society of Colon and Rectal Surgeons Clinical Practice Guidelines for the Management of Colon Cancer. Dis Colon Rectum. 2022 Feb 1;65(2):148-177. doi:10.1097/DCR.0000000000002323. PMID: 34775402.
- Wei X, Oxley S, Sideris M, Kalra A, Brentnall A, Sun L, Yang L, Legood R, Manchanda R. Quality of life after risk- reducing surgery for breast and ovarian cancer prevention: a systematic review and meta-analysis. Am J Obstet Gynecol. 2023 Oct;229(4):388-409.e4. doi: 10.1016/j.ajog.2023.03.045. Epub 2023 Apr 12. PMID:37059410.
- West NP, Hohenberger W, Weber K, Perrakis A, Finan PJ, Quirke P. Complete mesocolic excision with central vascular ligation produces an oncologically superior specimen compared with standard surgery for carcinoma of the colon. J Clin Oncol. 2010 Jan 10;28(2):272-8. doi: 10.1200/JCO.2009.24.1448. Epub 2009 Nov 30. PubMed PMID: 19949013.
- West NP, Morris EJ, Rotimi O, Cairns A, Finan PJ, Quirke P. Pathology grading of colon cancer surgical resection and its association with survival: a retrospective observational study. Lancet Oncol. 2008 Sep;9(9):857-65. doi: 10.1016/S1470-2045(08)70181-5. Epub 2008 Jul 28. PubMed PMID: 18667357.
- Yoon SH, Kim SN, Shim SH, Kang SB, Lee SJ. Bilateral salpingectomy can reduce the risk of ovarian cancer in the general population: A meta-analysis. Eur J Cancer. 2016 Mar;55:38-46. doi: 10.1016/j.ejca.2015.12.003. Epub 2016 Jan 8. Review. PubMed PMID: 26773418.
- Young-Fadok TM, Wolff BG, Nivatvongs S, Metzger PP, Ilstrup DM. Prophylactic oophorectomy in colorectal carcinoma: preliminary results of a randomized, prospective trial. Dis Colon Rectum. 1998 Mar;41(3):277- 83; discussion 283-5. PubMed PMID: 9514421.
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 13-03-2026
Beoordeeld op geldigheid : 13-03-2026
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodules werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodules.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met colorectaal carcinoom. Deze werkgroep is ingesteld in het kader van het cluster oncologie onderste tractus digestivus.
De huidige samenstelling van de werkgroep
- Prof. dr. P.J. (Pieter) Tanis, gastrointestinaal en oncologisch chirurg, Erasmus MC, Rotterdam, NVvH (voorzitter)
- Dr. M. (Myriam) Chalabi, internist, Antoni van Leeuwenhoek, Amsterdam, NIV/NVMO
- Dr. E.C. (Elske) Gootjes, medisch oncoloog, Radboud UMC, Nijmegen, NIV
- Dr. D.J.A. (Derk Jan) de Groot, internist-oncoloog, UMC Groningen, Groningen, NIV/NVMO
- Dr. M.P.W. (Martijn) Intven, radiotherapeut, UMC Utrecht, Utrecht, NVRO
- Dr. M. (Miranda) Kusters, colorectaal chirurg, Amsterdam UMC, Amsterdam, NVvH
- Dr. M. M. (Miangela) Laclè, patholoog, UMC Utrecht, Utrecht, NVVPathologie
- Dr. M.M. (Marilyne) Lange, patholoog, Amsterdam UMC, Amsterdam, NVvPathologie
- Dr. M. (Monique) Maas, radioloog, Nederlands Kanker Instituut, Amsterdam, NVvR (vice-voorzitter)
- Dr. L. (Leon) Moons, MDL-arts, UMC Utrecht, Utrecht, NVMDL
- Prof. dr. I.D. (Iris) Nagtegaal, patholoog, Radboud UMC, Nijmegen, NVvPathologie
- Dr. M. (Mark) Roef, nucleair geneeskundige, Catharina Ziekenhuis, Eindhoven, NVNG
- Dr. J.M.L. (Jeanine) Roodhart, internist-oncoloog, UMC Utrecht, Utrecht, NIV/NVMO
- Dr. M. (Maarten) Smits, radioloog, UMC Utrecht, Utrecht, NVvR
- (Iris) van der Veeken Msc., coloncare verpleegkundige, Flevoziekenhuis, Almere, V&VN
- Prof. dr. C. (Kees) Verhoef, oncologisch chirurg, Erasmus MC, Rotterdam, NVvH
- Dr. K.S. (Kathelijn) Versteeg, internist-oncoloog, Amsterdam UMC, Amsterdam, NIV/NVMO
- Dr. M. (Marianne) de Vries, abdominaal radioloog, Erasmus MC, Rotterdam, NVvR
- Dr. M.L. (Miriam) Wumkes, internist, Jeroen Bosch Ziekenhuis, ’s-Hertogenbosch, NIV/NVMO
- S. (Silvie) Dronkers, stichting Darmkanker † (in herinnering)
Voormalig betrokken werkgroepleden
- Dr. M.E. (Marije) Hamaker, klinisch geriater, Diakonessenhuis, Utrecht, NVKG
- Dr. H.M.W. (Henk) Verheul, internist-oncoloog, Radboudumc, Nijmegen, NIV/NVMO
- Dr. H.L. (Erik) van Westreenen, chirurg, Isala Zwolle/ Isala Diaconessenhuis, Zwolle/Meppel, NVvH
- Dr. P. (Petur) Snaebjornsson, patholoog, Nederlands Kanker Instituut, Amsterdam, NVvP
Met medewerking van
- Dr. H.M.U. (Heike) Peulen, radiotherapeut-oncoloog, Catharina Ziekenhuis, Eindhoven
- Drs. F. (Floor) Piquer, PhD kandidaat, Catharina ziekenhuis
- dr. J.W.A. (Pim) Burger, chirurg, Catharina Ziekenhuis, Eindhoven, NVvH
Met ondersteuning van
- dr. D. (Dagmar) Nieboer, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. R.J.S. (Rayna) Anijs, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- I. (Ingeborg) van Dusseldorp, medisch informatiespecialist, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke Financiële Belangen |
Persoonlijke Relaties |
Extern gefinancierd onderzoek |
Intell. belangen en reputatie |
Overige belangen |
Ondernomen acties |
|
Prof. Dr. P.J. (Pieter) Tanis |
Chirurg, Erasmus MC |
Lid clinical audit board Dutch ColoRectal Audit, onbetaald Bestuurslid Stichting Opsporing Erfelijke Tumoren, onbetaald Lid medische adviesraad Lynch Polyposis vereniging, onbetaald Associate Editor Colorectal Disease, onbetaald |
Geen |
Geen |
Meerdere klinische multicenter trials: * KWF - COLOPEC-2: vroegdetectie peritoneale metastasen CRC - Projectleider * KWF - BIOPEX-2: transpositielap voor sluiting perineale wond APR voor rectumcarcinoom - Projectleider * KWF - IMARI: preventie en optimale behandeling naadlekkage na rectumcarcinoom resectie - Projectleider * KWF - Predicitiemodel longlaesies bij CRC - Projectleider * KWF - Snapshot complex coloncarcinoom - Geen projectleider KWF-COLOPEC-2: vroegdetectie peritoneale metastasen CRC-projectleider KWF-CAIRO-6: perioperatieve chemotherapie bij CRS-HIPEC voor peritoneale metastasen van CRC-geen projectleider KWF-BIOPEX-2: transpositielap voor sluiting perineale wond APR voor rectumcarcinoom- projectleider KWF- IMARI: preventie en optimale behandeling naadlekkage na rectumcarcinoom resectie-projectleider KWF-AI voor karakterisatie / predictie van longlaesies bij CRC-projectleider KWF-Snapshot complex coloncarcinoom-projectleider KWF-Snapshot rectumcarcinoom 2016-geen projectleider ZonMw CROSSROADS: behandelstrategie na lokale excisie pT1-2 coloncarcinoom, gestratificeerd voor lymfkliermetastase risico- geen projectleider Zorgverzekeraars (ZN)-DICA 2.0, pilot DCRA: verdiepingsmodules, videoregistratie-projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. M. (Myriam) Chalabi |
Internist-oncoloog, Antoni van Leeuwenhoek |
Geen |
Geen |
Geen |
* BMS - neoadjuvante immuuntherapie bij coloncarcinoom (Projectleider JA) * roche - neoadjuvante radiotherapie,immuuntherapie en bevacizumab bijrectumcarcinoom (Projectleider JA) * agenus - neoadjuvante immuuntherapie pan-cancer (Projectleider, ) * roche - neoadjuvante immuuntherapie bij slokdarm/maagcarcinoom (Projetleider JA) * MSD - neoadjuvante immuuntherapie bij lokaal irresectabele colorectale (Projectleider JA) carcinomen
|
Geen |
Geen |
Geen acties ondernomen |
|
Dr. E.C. (Elske) Gootjes |
Medisch oncoloog, Radboud UMC |
Geen |
Geen |
Geen |
* KWF - ORCHESTRA, lokale behandeling bij mCRC - Geen projectleider * Roche - ORCHESTRA, lokale behandeling bij MCRC - Geen projectleider * Stichting Blokker Verwer - ORCHESTRA, lokale behandeling bij mCRC - Geen projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
S.Y.A. (Silvie) Dronkers MA (overleden 18-12-2025)
|
Stichting Darmkanker Coördinator Patiënten Participatie Onderzoek en Belangenbehartiging
onbetaald |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. D.J.A. (Derk-Jan) de Groot |
Internist oncoloog, UMC Groningen |
Geen |
Geen |
Geen |
zie onder: * Hoffman-La Roche - Fase 2 klinische geneesmiddelen studie - Projectleider * GE - Fase 2 klinische studie - Geen projectleider * Siemens - Beurs om PET onderzoek te doen |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. E.C. (Elske) Gootjes
|
Medisch oncoloog RadboudUMC |
Geen |
Geen |
Geen |
* KWF - ORCHESTRA, lokale behandeling bij mCRC - Geen projectleider * Roche - ORCHESTRA, lokale behandeling bij MCRC - Geen projectleider * Stichting Blokker Verwer - ORCHESTRA, lokale behandeling bij mCRC - Geen projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
Prof. Dr. M.P.W. (Martijn) Intven |
Radiotherapeut-Oncoloog UMC Utrecht |
- Voorzitter Nederlandse Vereniging voor radiotherapie en Oncologie, onbetaald - Lid redactieraad NTVO, onbetaald |
Geen |
Geen |
KWF - Pancreascarcinoom - Projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
dr. M. (Miranda) Kusters |
Colorectaal chirurg, Amsterdam UMC |
Geen |
Geen |
Geen |
KWF - Snapshot rectumcarcinoom - Projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. M.M. (Miangela) Laclè
|
Patholoog, UMC Utrecht |
Geen |
Geen |
Geen |
KWF - PATCH (validatie studie predictiemodel gesteelde T1 CRCs) - Projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
dr. M.M. (Marilyne) Lange |
Patholoog Amsterdam UMC |
Geen betaalde nevenwerkzaamheden |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. M. (Monique) Maas |
Radioloog bij NKI-AVL |
Redacteur nascholingsblad 'Imago'; hiervoor ontvang ik een vergoeding 1x per jaar |
Geen |
Geen |
KWF – Near complete response in rectal cancer – projectleider/PI |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. L.M.G. (Leon Moons) |
MDL arts, UMC Utrecht |
Geen |
Consultant voor Boston Scientific |
Geen persoonlijke relaties met een belang |
Alleen KWF, ZonMW en MLDS gesponsorde onderzoeken: * KWF - MATILDA-studie: EMR vs ESD voor grote linkszijdige poliepen - Projectleider * KWF - STAR-studie: cluster gerandomiseerde studie naar het effect van training in EMR in het verlagen - Projectleider * MLDS - STONE-studie: risicofactoen voor lymfkliermetastasen bij T1 CRCs * ZonMW - TRIASSIC-studie: ESD vs TAMIS voor rectum poliepenoor - Geen projectleider ZonMw CROSSROADS: behandelstrategie na lokale excisie pT1-2 coloncarcinoom, gestratificeerd voor lymfkliermetastase risico- projectleider |
Voorzitter T1 CRC werkgroep bestuurslid DCCG Voorzitter richtlijn Poliepectomie in het rectum en colon |
Geen |
Geen acties ondernomen |
|
Prof. Dr. I.D. (Iris) Nagtegaal |
Hoogleraar Pathologie, Radboudumc |
Voorzitter Stichting Palga (detachering) Expert patholoog BVO darmkanker (detachering) Onbetaalde functies: |
Geen |
Geen |
ja diverse wetenschappelijke projecten van verschillende fondsen: * KWF - Microbiome and metastases - Geen projectleider * Hanarth Foundation - Cancer of unknown primary - Projectleider * KWF - Implementation Al in pathology * ZonMW - Covid19 and cancer - Geen projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. M. (Mark) Roef |
Nucleair geneeskundige, Catharina Ziekenhuis Eindhoven |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
dr. J.M.L. (Jeanine) Roodhart |
internist-oncoloog, UMC Utrecht |
ONCODE clinical advisory board KWF wetenschappelijke raad, exploratie kamer bestuurslid stichting Hubrecht Organoid Biobank
allen onbetaald. |
Geen persoonlijke; geen betalingen aan mij als persoon voor deelname adviesraden, wel betalingen aan afdeling voor adviesraden/spreken door diverse farma en onderzoeksprojecten betaald door farma. |
nee |
ja: * KWF - ACTOR studie, organoids anuscarcinoom als predictieve biomarker en platform voor ontwikkelen nieuwe - Projectleider * GSK - MIRROR, analyse behandeling en uitkomsten MSI vs MSS rectumcarcinoom - Projectleider * HUB - OPTIC studie, voorspellende waarde organoids - Projectleider * Xilis - POSTED, MOS screeningsplatform als predictieve biomarker - Projectleider * Pierre Fabre - BRIDGE, real life treatment patterns en uitkomsten per moleculaire subgroep - Projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
dr. M.L.K. (Maarten) Smits |
Interventieradioloog, UMC Utrecht |
- Voorzitter wetenschapscommissie Nederlandse Vereniging voor Interventieradiologie (onbetaald) - Lid kernwerkgroep Kwaliteitsnormen in de Interventieradiologie - Consultant voor Philips (begunstigde UMC Utrecht) - Consultant voor Terumo / Quirem Medical (begunstigde UMC Utrecht) - Consultant voor Medtronic (begunstigde UMC Utrecht) - Consultant voor Swedish Orphan Biovitrum (eenmalige zitting in advisory board in 2021, begunstigde UMC Utrecht) |
Geen |
Geen |
* Terumo / Quirem Medical - HEPAR primary study, radioembolization for patients with hepatocellular carcinoma - Geen projectleider * Zorginstituut Nederland - CAIRO7-studie: radioembolisation for frail or elderly patients with colorectal liver metastases - Geen projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
I. (Iris) van Veeken |
verpleegkundige - Flevoziekenhuis |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
Prof. Dr. C. (Kees) Verhoef |
Hoofd Gastro-Intestinale en Oncologische Chirurgie, Erasmus MC |
Bestuur Familiehuis, onbetaald Bestuur DCCG, onbetaald Ass Editor Sarcoma, Cancers and Digestive Surgery, onbetaald Dagvoorzitter expertmeeting Johnson en Johnon, betaald |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
dr. K.S. (Kathelijn) Versteeg |
Internist-oncoloog en ouderengeneeskunde Amsterdam UMC |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
dr. M. (Marianne) de Vries |
Erasmus MC Radiologie Rotterdam: Radioloog (betaald) |
Geen |
Geen |
Geen |
Alleen meewerken aan multicenter studies maar niet als hoofdonderzoeker en krijg daar geen geld voor (bijvoorbeeld SNAPshot studie AVL of PELVEX studie) |
Geen |
Geen |
Geen acties ondernomen |
|
dr. M.L. (Miriam) Wumkes
|
Internist-oncoloog Jeroen Bosch ziekenhuis (vrijgevestigd, betaald) |
Voorzitter oncologiecommissie JBZ, betaald LId netwerkoncologiecommissie EMBRAZE, betaald Lid Regiocommissie Onco-oost, betaald Lid wetenschappelijke commissie DPCG, niet betaald Lid werkgroep organisatie van zorg DRPC, niet betaald Moleculaire diagnostiek per augustus, Zorginstituut Nederland, niet betaald. |
Geen |
Geen |
Lokale PI van onderzoek in JBZ, geen projectleider. Overigens onderzoeken niet binnen de lower tract * Overheid (vergoeding vanuit basispakket) - Periscope 2, beperkt gemetastaseerd maagcarcinoom, chemo vs chemo met CRS/HIPEC - Geen projectleider * KWF - Preopanc 3, resectabel pancreascarcinoom - Geen projectleider |
niet van toepassing. |
2019 Advies raad maagcarcinoom, Servier 2019 Adviesraad pancreascarcinoom, Servier 2020 Consensus expert Groep NTRK genfusie gerelateerde kanker. 2021: Programmacommissie en voordracht indian Summerschool voor jonge klaren, Servier
Vanaf 2022: Wetenschappelijk comite Waddenworkshop MDL, sponsoring verschillende farma (beschreven op de site welke farma voor welk jaar, https://www.waddenworkshoponcologie.nl/mdl-tumoren )
Voordracht masterclass GE oncologie stichting oncowijs |
Geen acties ondernomen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door het uitnodigen van Stichting Darmkanker en de Nederlandse Federatie van Kankerpatiëntenorganisaties (NFK) voor de invitational conferences in 2017 en 2023. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. Daarnaast zijn deze patiëntenorganisaties in de commentaarfase uitgenodigd om modules mee te lezen, te becommentariëren en de werkgroep van feedback vanuit het patiëntenperspectief voorzien.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
|
Module |
Uitkomst raming |
Toelichting |
|
Uitgebreidheid primaire resectie coloncarcinoom |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er worden daarom geen substantiële financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodules zijn opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 3.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase in 2017 inventariseerde de werkgroep knelpunten en de werkgroep beoordeelde de aanbevelingen uit de eerdere richtlijn (NVRO, 2014) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door verschillende partijen via een invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten. Medio 2023 is het grootste deel van de richtlijn herzien en worden nieuwe modules of herzieningen door de werkgroep besproken indien de werkgroep:
- Signalen krijgt van (nieuwe) knelpunten in de zorg voor patiënten met colorectaal carcinoom die geadresseerd dienen te worden in de richtlijn.
- Signaleert dat er nieuwe onderzoeksresultaten zijn die relevant zijn voor de richtlijn.
- Constateert dat er tekstuele verbeteringen of aanvullingen nodig zijn in de richtlijn om de bruikbaarheid of volledigheid van de richtlijn te verbeteren.
De werkgroep bespreekt welke aanvullingen of herzieningen geprioriteerd dienen te worden en stelt evt. passende (nieuwe) uitgangsvragen op. De werkroep bepaalt de prioriteit van aanvullingen of herzieningen op basis van: (1) klinische relevantie, (2) de beschikbaarheid van nieuwe evidence, (3) en de te verwachten impact op de kwaliteit van zorg, patiëntveiligheid en (macro)kosten.
Uitkomstmaten
De werkgroep inventariseerde per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij men zowel naar gewenste als ongewenste effecten keek. De werkgroep baseerde de keuze voor uitkomstmaten mede op basis van de “core outcome set” gepubliceerd door Zerillo (2017). De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden. Hiervoor sloot de werkgroep zich, waar mogelijk, aan bij de grenzen voor klinische besluitvorming volgens de PASKWIL criteria uit 2023. Wanneer er geen grenzen voor klinische besluitvorming conform de PASKWIL criteria geformuleerd konden worden (bijvoorbeeld bij non-inferioriteitsvraagstukken) werden de standaard GRADE grenzen gehanteerd, tenzij anders vermeld.
Strategie voor zoeken en selecteren van literatuur
De werkgroep raadpleegde voor de afzonderlijke uitgangsvragen reeds gepubliceerde systematische reviews (SRs). SRs kwamen in aanmerking indien: i) systematisch was gezocht in één of meerdere databases; ii) transparante in- en exclusiecriteria zijn toegepast en iii) idealiter de kwaliteit van de geïncludeerde literatuur was beoordeeld. De voor de uitgangsvragen relevante internationale richtlijnen en consensusdocumenten werden eveneens geraadpleegd. Overige literatuur, waar niet systematisch naar werd gezocht, is als bewijsvoering in de overwegingen opgenomen.
Relevante beschikbare populatiegegevens uit Nederland werden gebruikt voor het bepalen van knelpunten, praktijkvariatie en externe validiteit van internationale richtlijnen en gepubliceerde literatuur.
Kwaliteitsbeoordeling individuele studies
De (risk of bias) kwaliteitsbeoordelingen van de individuele studies uit de gebruikte SRs werden gebruikt, tenzij deze afwezig waren of onbruikbaar waren voor het beoordelen van de kracht van het wetenschappelijke bewijs. Indien afwezig of onbruikbaar werd aangenomen dat er een risico op bias aanwezig zou kunnen zijn. In enkele gevallen, wanneer studies informatie verschaften over de cruciale uitkomstma(a)t(en), werd er een nieuwe kwaliteitsbeoordeling van individuele studies uitgevoerd.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van de geselecteerde SRs werden weergegeven in ‘Summary of Findings’ tabellen. De belangrijkste bevindingen uit de literatuur werden kort beschreven onder “Samenvatting literatuur” (kopjes “Samenvatting van internationale richtlijnen en consensusdocumenten” en “Samenvatting van systematische reviews en meta-analyses”) en onder “Overwegingen”. Bestaande meta-analyses uit de gebruikte systematische reviews werden beschreven. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek (te vinden in de ‘Summary of Findings’ tabellen). De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de cruciale uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje Overwegingen.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello, 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE-methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE- methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling beargumenteerd hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Indicatorontwikkeling
De werkgroep ontwikkelde geen interne kwaliteitsindicatoren om het toepassen van de richtlijn in de praktijk te volgen en te versterken. De werkgroep conformeert zich aan de SONCOS normen en de DICA-DCRA indicatoren.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule wordt aan de betrokken wetenschappelijke verenigingen en (patiënt)organisaties voorgelegd ter commentaar. De commentaren worden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren wordt de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule wordt aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi:
10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol.
2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html.
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi:10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zerillo JA, Schouwenburg MG, van Bommel ACM, Stowell C, Lippa J, Bauer D, Berger AM, Boland G, Borras JM, Buss MK, Cima R, Van Cutsem E, van Duyn EB, Finlayson SRG, Hung-Chun Cheng S, Langelotz C, Lloyd J, Lynch AC, Mamon HJ, McAllister PK, Minsky BD, Ngeow J, Abu Hassan MR, Ryan K, Shankaran V, Upton MP, Zalcberg J, van de Velde CJ, Tollenaar R; Colorectal Cancer Working Group of the International Consortium for Health Outcomes Measurement (ICHOM). An International Collaborative Standardizing a Comprehensive Patient-Centered Outcomes Measurement Set for Colorectal Cancer. JAMA Oncol. 2017 May 1;3(5):686-694. doi: 10.1001/jamaoncol.2017.0417. PubMed PMID: 28384684.