Lokale therapie mCRC lever
Uitgangsvraag
Welke vormen van lokale therapie kunnen worden ingezet bij niet-resectabele levermetastasen?
Aanbeveling
De aanbevelingen in deze module zijn overgenomen uit de 2014 richtlijn en in 2019 door de werkgroep beoordeeld als actueel. De aanbevelingen zijn eventueel tekstueel aangepast, maar inhoudelijk niet veranderd.
Voer een partiële leverresectie uit indien voldaan aan de criteria voor resectabiliteit.
Geef niet standaard perioperatieve of adjuvante chemotherapie bij primair resectabele levermetastasen.
Hanteer de volgende criteria voor resectabiliteit:
- Bij normaal leverparenchym en indien er geen sprake is van neoadjuvante systemische therapie, dient minimaal 20 procent van de lever over te blijven na resectie (=rest volume), indien er uitgebreide resecties worden overwogen,
- Indien er primair onvoldoende leverparenchym zou overblijven na resectie zou inductie systemische therapie en/of vena-porta embolisatie en/of “two-stage” resecties moeten worden overwogen.
- Geen absolute contra-indicaties zijn; bilobaire levermetastasen, aantal metastasen, grootte van de metastasen, wel of niet synchroniciteit, extra-hepatische metastasen, stadium primaire tumor, leeftijd en waarde van het serum CEA.
- Geen contra-indicatie is een te verwachten krappe resectiemarge. In centra met veel expertise is er de mogelijkheid om resecties uit te voeren direct grenzend aan grote vaat- en/of galwegstructuren met kleinere marges. Omdat het echter moeilijk is op voorhand de marge te bepalen, wordt een ruime marge van 10 mm geadviseerd.
Overweeg gelijktijdig opereren van de primaire tumor en synchrone metastasen alleen na zorgvuldige selectie en bij voldoende beschikbare expertise bij patiënten met synchrone levermetastasen.
Opereer zo parenchymsparend mogelijk.
Beschouw lokale thermale ablatie als een belangrijke component in de multidisciplinaire behandeling van patiënten met colorectale levermetastasen van een relatief beperkte omvang (tot 3 cm).
Pas lokale thermale ablatie toe in combinatie met resectie om bij geselecteerde patiënten lokale behandeling mogelijk te maken.
Pas percutane lokale thermale ablatie toe als lokale behandeling bij patiënten met colorectale levermetastasen die minder geschikt zijn voor chirurgische resectie door hoge leeftijd, comorbiditeit, een ongunstige locatie van de laesie voor resectie of een geschiedenis van uitgebreide abdominale chirurgie.
MW ablatie is mogelijk een goed alternatief voor RFA, met name bij tumor lokalisaties waarbij een negatief effect van grote bloedvaten is te verwachten (heatsink).
Overweeg radio-embolisatie als salvage therapie bij patiënten met metastasen beperkt tot de lever. In een vroegere fase is de waarde ten opzichte van palliatieve systemische therapie onvoldoende bekend.
Overweeg stereotactische radiotherapie voor patiënten met irresectabele colorectale levermetastasen waarbij de ligging voor RFA ongunstig is.
Chirurgische behandeling
Iedere patiënt met colorectale levermetastasen dient te worden besproken met een centrum met expertise ten aanzien van leverchirurgie, lokale behandelingstechnieken van de lever en het (gemetastaseerde) colorectale carcinoom.
Partiële leverresectie heeft de voorkeur boven alleen systemische therapie bij patiënten die voldoen aan de criteria voor resectabiliteit.
Leverresecties en combinatiebehandelingen dienen te worden uitgevoerd in centra waar:
- expertise aanwezig is
- geschikte apparatuur beschikbaar is en
- ervaring is opgebouwd met
- systemische therapie voor het colorectale carcinoom
- lokale behandelingstechnieken voor de lever (operatieve en percutane behandelingen)
- intensive care en
- anesthesie op dit vlak.
Criteria voor resectabiliteit
Bij normaal leverparenchym en indien er geen sprake is van neoadjuvante systemische therapie, dient minimaal 20% van de lever over te blijven na resectie (=rest volume), indien er uitgebreide resecties worden overwogen,
Indien er primair onvoldoende leverparenchym zou overblijven na resectie zou inductie systemische therapie en/of vena-portae embolisatie en/of ‘two-stage’ resecties moeten worden overwogen.
Geen absolute contra-indicaties zijn; bilobaire levermetastasen, aantal metastasen, grootte van de metastasen, wel of niet synchroniciteit, extra-hepatische metastasen, stadium primaire tumor, leeftijd en waarde van het serum CEA.
Geen contra-indicatie is een te verwachten krappe resectiemarge. In centra met veel expertise is er de mogelijkheid om resecties uit te voeren direct grenzend aan grote vaat- en/of galwegstructuren met kleinere marges. Omdat het echter moeilijk is op voorhand de marge te bepalen, wordt een ruime marge van 10 mm geadviseerd.
Gelijktijdig opereren van de primaire tumor en synchrone metastasen is geen standaard bij patiënten met synchrone levermetastasen. De werkgroep is van mening dat deze behandeling na zorgvuldige selectie in centra met veel ervaring op zowel colorectale chirurgie als leverchirurgie kan worden overwogen.
Er dient zo parenchymsparend mogelijk te worden geopereerd.
Bij patiënten met nieuwe levermetastasen na eerdere leverchirurgie, wordt re-resectie geadviseerd indien patiënt voldoet aan de criteria voor resectabiliteit.
De radicaliteit is het belangrijkste en de gewenste marge is afhankelijk van de patiëntgebonden situatie.
Een beperkte marge is geen contra-indicatie voor (het aanbieden van) resectie.
Bij patiënten met beperkte extrahepatische metastase(n) kan een resectie worden overwogen. Dit moet geschieden in expertise centra en het liefst in studieverband.
Leeftijd is geen absolute contra-indicatie voor partiële leverresectie.
Overwegingen
Radio Frequentie Ablatie en Microwave ablatie
Bij patiënten met resectabele levermetastasen blijft chirurgische resectie eerste keus. Bij patiënten die minder geschikt zijn voor chirurgische resectie door hoge leeftijd, comorbiditeit, ongunstige locatie van de laesie voor resectie, of waar een geschiedenis is van uitgebreide abdominale chirurgie kan bij beperkte tumorload in de lever en afwezigheid van of bij stabiele extra-hepatische ziekte ablatie in de vorm van (percutane) RFA een goede lokale behandelingsoptie zijn met goede klinische uitkomsten. Door chirurgische resectie te combineren met RFA kan het aantal resecties van levermetastasen toenemen.
Trans arteriële chemo embolisatie
Partiële leverresectie is de gouden standaard. TACE voor colorectale levermetastasen moet (nog) gezien worden als experimentele behandeling en dient in studieverband te worden verricht.
De rol van TACE bij patiënten met niet-resectabele colorectale levermetastasen in vergelijking met andere lokale behandeltechnieken of systemische behandeling moet adequaat onderzocht worden in gerandomiseerde studies. Op dit moment zijn er geen data die de voor– en nadelen van TACE hebben vergeleken met andere, lokale niet-chirurgische technieken en er is te weinig evidence om TACE toe te passen indien er nog systemische behandelingsopties zijn.
Stereotactische radiotherapie
De rol van stereotactische radiotherapie in vergelijking met andere lokale behandeltechnieken als RFA moet onderzocht worden in gerandomiseerde studies. Op dit moment zijn er geen data die de voor– en nadelen van SRT hebben vergeleken met andere, lokale niet-chirurgische technieken.
Onderbouwing
Achtergrond
Indien de colorectale levermetastase(n) primair niet resectabel worden geacht door lokalisatie en dit is niet veranderd na vena portae embolisatie en/of inductie systemische therapie, dan kunnen alternatieve lokale behandelingen van de lever in aanmerking komen. De lokale therapieën kunnen worden onderverdeeld in drie categorieën: Lokaal ablatieve thermale therapie, lokaal vasculaire behandelingen en lokaal niet-vasculaire behandelingen.
Chirurgische behandeling
De behandeling van patiënten met colorectale levermetastasen (CRLM) heeft zich in de laatste 20 jaar aanzienlijk ontwikkeld. Dit geldt zowel voor de systemische als de lokale behandelingsmogelijkheden. Momenteel blijft chirurgische resectie de gouden standaard bij patiënten die voldoen aan de criteria voor resectabiliteit. Het merendeel van de patiënten met CRLM is echter geen kandidaat voor resectie. De ontwikkeling van lokale therapieën voor de lever en de verbetering van de effectiviteit van de systemische therapie hebben erin geresulteerd dat het percentage patiënten dat in aanmerking komt voor primaire of secundaire (na downsizing d.m.v. systemische therapie) resectie is gestegen tot 20%-30%. De selectie, de volgorde en de integratie van interventies dient in een multidisciplinair team plaats te vinden, waarin expertise op alle relevante deelgebieden vertegenwoordigd dient te zijn.
In deze module hoofdstuk worden de momenteel beschikbare en meest gebruikte lokale therapieën voor de lever in Nederland besproken. Voor de opties ten aanzien van de systemische therapieën wordt verwezen naar de betreffende modules.
Conclusies
Radio Frequentie Ablatie en Microwave ablatie
Er is bewijs van lage kwaliteit dat RFA bij open buik, laparoscopisch en percutaan kan worden toegepast. Het is een veilige techniek met een geringe kans op complicaties en een korte opname duur. Er zijn meerdere niet gerandomiseerde studies beschikbaar die laten zien dat RFA een techniek is met een relatief lage local recurrence en een positief effect op de overleving.
Niveau: laag Weng 2012 (57); Cirocchi 2012 (11)
Er is bewijs van matige kwaliteit dat de kans op lokale recidieven na RFA toeneemt bij toename van de grootte van de leverlaesie.
Niveau: matig Solbiati 2001 (48); Solbiati 2001 (50); Berber 2005 (7)
Bij patiënten met niet-resectabele colorectale levermetastasen is er bewijs van zeer lage kwaliteit dat de toevoeging van RFA op systemische chemotherapie de Progression Free Survival verbetert, zonder een aantoonbaar effect op de Overall Survival.
Niveau: zeer laag Ruers 2012 (42)
Er is bewijs van zeer lage kwaliteit dat cryotherapie een betere of slechtere lokale controle of overleving heeft dan RFA bij patiënten met colorectale levermetastasen. Cryotherapie is een ablatietherapie waarbij door bevriezing celdood optreedt en lijkt gepaard te gaan met meer complicaties dan RFA.
Niveau: zeer laag Pathak 2011 (40)
Er is bewijs van zeer lage kwaliteit dat MW ablatie minder last heeft van ineffectieve ablaties door koeling nabij grote bloedvaten (heatsink). MW ablatie is een veilige thermische ablatie techniek, waarbij nog onvoldoende bewijs is dat het in de praktijk betere lokale controle en overleving geeft dat RFA.
Niveau: zeer laag Pathak 2011 (40); Livraghi 2012 (34)
Geïsoleerde leverperfusie
Er is bewijs van lage kwaliteit dat geïsoleerde leverperfusie voor tot de lever beperkte colorectale levermetastasen in een respons percentage bij een geselecteerde groep patiënten resulteert, vergelijkbaar met de moderne chemotherapie.
Niveau: laag Alexander 2000 (4); Bartlett 2001 (6); Rothbarth 2003 (41)
Trans arteriële chemo embolisatie
Er is bewijs van lage kwaliteit dat TACE een veilige techniek met een geringe kans op complicaties en een korte opnameduur is.
Niveau: laag Fiorentini 2012 (16)
Er is bewijs van lage kwaliteit dat TACE een hoge kans op lokale controle voor patiënten met niet resectabele colorectale levermetastasen biedt.
Niveau: laag Fiorentini 2012 (16)
Er is bewijs van zeer lage kwaliteit dat dat TACE een toegevoegde waarde heeft ten opzichte van systemische chemotherapie ten aanzien van de progressie vrije overleving en mogelijk op de algehele overleving bij patiënten met niet-resectabele colorectale levermetastasen.
Niveau: zeer laag Fiorentini 2012 (16)
Stereotactische radiotherapie
Er is bewijs van matige kwaliteit dat voor patiënten met irresectabele colorectale levermetastasen met beperkte risico’s van toxiciteit en zonder een negatieve beïnvloeding in de kwaliteit van leven, stereotactische radiotherapie een hoge kans van lokale controle biedt.
Niveau: matig Van der Pool 2010 (54); Mendez Romero 2008 (60)
Chirurgische behandeling
Er is een enorme variatie in prognostische factoren voor de overleving na in opzet curatieve resectie van de colorectale levermetastasen. Er bestaan zogenaamde Clinical Risk Scores om de prognose in te schatten. Over marges bij de resectie van de colorectale levermetastasen bestaat er geen duidelijkheid.
Niveau 4: D Mening van de werkgroep
Het medisch beleid bij synchrone levermetastasen en extrahepatische afwijkingen is niet eenduidig. Er is een enorme variatie in uitvoering van resecties (anatomische vs. niet-anatomische, vena cava reconstructie, two-stage, na porta-embolisatie, na inductie systemische therapie, etc.).
Niveau 4: D Mening van de werkgroep
Eenduidige resultaten over de effectiviteit van combinatiebehandelingen met (neo)-adjuvante systemische therapie ontbreken.
Niveau 4: D Mening van de werkgroep
Er is geen eenduidigheid over de criteria van resectabiliteit.
Niveau 4: D Mening van de werkgroep
Resectie van colorectale levermetastasen leidt in geselecteerde patiëntengroepen tot een 5-jaars overleving van 25% – 60%.
Niveau 3: C Yin 2013 (39); Li 2013 (26); Slesser 2013 (34)
Als gevolg van lokale irresectabiliteit, extrahepatische uitbreiding of door aanwezige comorbiditeit komt slechts tot 30% van de patiënten in aanmerking voor een in opzet curatieve resectie.
Niveau 3: C Yin 2013 (39); Li 2013 (26); Slesser 2013 (34)
Er zijn aanwijzingen dat bij normaal leverparenchym maximaal 80% van het levervolume kan worden verwijderd met beperkt gevaar op postoperatief leverfalen.
Niveau 3: C De Beare 1996 (13); Kokudo 2001 (22); Kubota 1997 (24); Sneider 2004 (32); Adballa 2006 (1)
Er zijn aanwijzingen dat bij diffuse parenchymafwijkingen zoals bij cirrose of uitgebreide steatose, het maximaal te verwijderen volume beperkt is en ook het vermogen tot leverregeneratie en daarmee de mogelijkheid tot herstel van leverfunctie veel kleiner is.
Niveau 3: C Schneider 2004 (32); Abdalla 2006 (1)
Er is geen eenduidig bewijs met betrekking tot marges in relatie tot kans op recidief, progressievrije of totale overleving bij resectie.
Niveau 3: C Andreou 2013 (7)
Er zijn aanwijzingen dat patiënten met extrahepatische afwijkingen een slechtere prognose hebben in vergelijking tot patiënten zonder extrahepatische afwijkingen.
Niveau 3: C Chua 2012 (12)
Er zijn aanwijzingen dat een selecte groep van patiënten met extrahepatische ziekten een 5-jaarsoverleving hebben tussen de 19 en 36%.
Niveau 3: C Chua 2012 (12)
Er zijn aanwijzingen dat een oudere leeftijd (>70 en/of 80 jaar) geen absolute contra-indicatie is voor resectie.
Niveau 3: C Adam 2010 (2)
Er zijn aanwijzingen dat synchroniciteit geen contra-indicatie is voor resectie.
Niveau 3: C Lyass 2001 (27); Vogt 1991 (38); Fujita 2000 (17)
Er zijn aanwijzingen dat overleving bij gelijktijdig opereren van primaire tumor en synchrone metastasen vergelijkbaar is met opereren van synchrone levermetastasen na 2 of 3 maanden.
Niveau 3: C Yin 2013 (39); Li 2013 (26); Slesser 2013 (34)
Samenvatting literatuur
Radio Frequentie Ablatie
Principe van de techniek
RFA is een techniek die gebruik maakt van lokale applicatie van hitte door middel van hoogfrequente wisselstroom. Met deze techniek wordt weefsel verhit tot een temperatuur boven de 50°C, waardoor denaturatie van intracellulaire eiwitten en vernietiging van celmembranen (coagulatie necrose) optreedt (35; 13; 48). De tumor wordt aangeprikt met een naald (open buik, laparoscopisch of percutaan). Het aanprikken van de tumor gebeurt meestal echografisch, maar zo nodig met CT. De naald is een gedeeltelijke geïsoleerde schacht (14-17,5 gauge diameter) met een niet-geïsoleerde distale tip. Er zijn verschillende typen RFA-naalden verkrijgbaar. Zodra de naald correct is gepositioneerd wordt de RFA-procedure gestart waarbij hoogfrequente wisselstroom, vanuit de tip, het omliggende weefsel instromen. Hierdoor vindt de applicatie plaats van thermale energie, totdat een adequate temperatuur wordt bereikt.
Complicaties
Een uitgebreide review van Mulier, waarin 82 artikelen met 3.670 patiënten vanaf 1990 tot 2002 werden geëvalueerd, meldde een morbiditeit van 8,9% en mortaliteit van 0,5% (38). Een systematische review van Decadt, waarin 44 artikelen met 1.931 patiënten vanaf 1995 tot 2003 werden geëvalueerd, meldde vergelijkbare resultaten: morbiditeit in 137 (7,1%) en mortaliteit in 10 patiënten (0,5%) (14).
Er blijken bij RFA significant minder complicaties op te treden dan bij chirurgische resectie (3,9 vs. 18,3%) en een significant kortere opnameduur (3,9 vs. 9,2 dagen).
Lokale controle en overleving
Lokale controle is volgens Solbiati beter te bereiken bij tumoren kleiner dan 3 cm (48). Een andere studie van Solbiati vermeldt ook dat het recidiefpercentage hoger is bij grote laesies (21% bij laesies ≤2,5 cm, 52,8% bij laesies van 2,6- 4,0 cm en 68,4% bij laesies ≥4 cm) (50). Dit blijkt ook uit een uitgevoerd prospectieve studie, waarin Berber (2005) een mediane overleving van 38, 32 en 21 maanden voor laesies <3 cm, 3-5 cm en >5 cm rapporteerde.
De meeste studies rapporteren kleine patiëntengroepen [(18; 39; 1; 58) of het betreft studies met gecombineerde data van primaire levertumoren en metastasen van verschillende origine (12; 30; 8; 47; 33; 25). Er zijn een aantal publicaties met lange termijn gegevens over overleving van grote groepen patiënten met colorectale levermetastasen die behandeld zijn met RFA, echter geen gerandomiseerde trials.
In een prospectieve studie van Solbiati, werden 117 patiënten (179 metastasen variërend van 0,6 tot 9,6 cm) gevolgd die met RFA voor metachrone colorectale levermetastasen werden behandeld (48). Eventuele lokale recidieven werden opnieuw met RFA behandeld. In deze studie werd een 1-, 2- en 3-jaars overleving gemeld van respectievelijk 93%, 69% en 46% en een mediane overleving van 36 maanden. Dezelfde auteurs hebben hun data geüpdatet (166 patiënten met 378 metastasen) met een 1, 2, 3, 4 en 5-jaars overleving van respectievelijk 96%, 64%, 45%, 36% en 22% (49; 32) met 423 patiënten en 615 metastasen, variërend van 0,5 tot 5,0 cm, rapporteerde 1, 2, 3, 4 en 5-jaars overleving van 86%, 63%, 47%, 29% en 24% respectievelijk. Ook Gillams liet vergelijkbare resultaten zien met een 1, 3 en 5-jaars van 91%, 40% en 17% en een mediane overleving van 32 maanden in 167 patiënten behandeld (17).
In een Cochrane review werden 18 studies bekeken waarbij RFA werd vergeleken met andere behandelingsopties bij resectabele en niet-resectabele levermetastasen. Hierbij was er slechts 1 prospectief gerandomiseerde studie waarbij RFA gecombineerd met systemische chemotherapie werd vergeleken met alleen chemotherapie bij 119 patiënten met niet-resectabele levermetastasen. In deze studie vond men een significant betere progressievrije overleving bij 3 jaar van 27,6% voor de combinatie behandeling t.o.v. 10,6% voor chemotherapie alleen (HR 0,60; 95%BI: 0,42-0,95). De 30 maanden OS van 61,7% (95%BI: 48,2-73,9) voor de combinatiebehandeling verschilde echter niet significant met die van chemotherapie alleen (57,6%, 95%BI: 44,1-70,4).
Bij 17 studies was geen sprake van randomisatie, met een sterk verhoogd risico op selectie bias en onvergelijkbaarheid door verschillende inclusiecriteria van de diverse studies. Lokale ablatie wordt in de klinische praktijk veelal toegepast bij patiënten die minder geschikt zijn voor chirurgische resectie, wat kan resulteren in slechtere uitkomsten. In klinieken met een succesvol RFA-programma wordt bij patiënten met een hoger risico vaak voor een minder invasieve behandeling gekozen, zoals RFA, met een striktere selectie voor chirurgische resectie en betere resultaten tot gevolg.
Circa 20% van de patiënten met colorectale levermetastasen komt in aanmerking voor chirurgische resectie. In de literatuur is geen bewijs dat RFA de chirurgische resectie van colorectale levermetastasen kan vervangen. Chirurgische resectie blijft de gouden standaard bij resectabele ziekte (9; 14; 36; 5; 19) [Laz 2004]. Door hoge leeftijd, comorbiditeit, ongunstige locatie of een geschiedenis van uitgebreide abdominale chirurgie kunnen patiënten minder geschikt zijn voor een leverresectie (10; 23; 27; 31). Bij dergelijke patiënten kan bij beperkte tumorload in de lever en afwezigheid van of stabiele extra-hepatische ziekte ablatie, de vorm van RFA een goede lokale behandelingsoptie zijn met goede klinische uitkomsten (10; 37; 43; 44; 31).
De mogelijkheden van uitgebreidere leverchirurgie nemen toe met de zich verder ontwikkelende chirurgische technieken. RFA kan gebruikt worden als complementaire tool bij resectie van levermetastasen, om meer patiënten chirurgische therapie te kunnen bieden (45; 55; 59). Waar voorheen lokalisatie van metastasen in zowel de linker als rechter leverkwab een contra-indicatie was voor chirurgische resectie kan een patiënt nu, met een (extended) hemihepatectomie en een RFA wel lokaal worden behandeld.
Cryotherapie
Principe van de techniek
Door het bevriezen van cellen vindt formatie van intra- en extracellulaire ijskristallen plaats. Dit heeft schade aan de celmembranen en intracellulaire structuren tot gevolg waardoor celdood optreedt. Dit wordt bereikt door snel vriezen of te vriezen tot een heel lage temperatuur (2; 26; 3). Het plaatsen van een probe vindt echogeleid plaats. Vervolgens wordt vloeibare stikstof of argon in de tumor gebracht en de tumor wordt bevroren met een marge van 1 cm.
Complicaties
De beschreven complicaties van cryotherapie zijn relatief frequent. Voorbeelden zijn intra-operatieve hypothermie, hartritmestoornissen, scheurvorming in leverkapsel door het uitzetten van het bevroren weefsel, pulmonale complicaties, abcesvorming, galwegfistelvorming en het cryoshock syndroom (3; 46). Ernstige complicaties worden in de literatuur beschreven variërend van 21%-66% (40). In verband met het hoge complicatierisico is cryotherapie door veel gebruikers verlaten en vervangen door andere ablatieve technieken.
Lokale controle en overleving
Er zijn geen prospectieve gerandomiseerde studies die cryotherapie vergelijken met andere vormen van ablatieve technieken, chirurgie of systemische behandelingen. Er is geen meta-analyse gedaan naar de resultaten van cryotherapie. In een recente systematische review werd een lokaal recidief percentage variërend van 23%-39% gerapporteerd met een 5-jaars overleving van 0%-44% (40).
Microwave ablatie
Principe van de techniek
Een meer recente ontwikkeling in de thermische ablatietechnieken is de Microwave (MW) ablatie. De techniek is vergelijkbaar met RFA maar maakt gebruik van microgolven (0,9-2,4 GHz). De probe wordt op vergelijkbare wijze als bij RFA in de tumor geplaatst, maar het gebruik van grounding pads is niet nodig. Oscillatie van watermoleculen leidt door wrijving tot lokale verhitting en celdood. MW ablatie heeft een theoretisch voordeel ten opzichte van RFA. Een snellere en effectievere verhitting maakt de techniek minder gevoelig voor het heatsink effect nabij grotere bloedvaten, waardoor een betere ablatie plaats kan vinden nabij deze structuren. Daarnaast is de techniek minder gevoelig voor lokale verdroging en verkoling van het weefsel (40; 22).
Complicaties
Livraghi rapporteerde de complicaties van MW ablatie bij 736 patiënten met 1.037 laesies. Zij concludeerden dat MW ablatie van de lever veilig is met 2,9% majeure complicaties en 7,3% mineure complicaties (23).
Lokale controle en overleving
In een kleine gerandomiseerde prospectieve studie werd MW ablatie vergeleken met chirurgische resectie bij patiënten met resectabele colorectale levermetastasen. Voor de MW groep van 14 patiënten was de 1, 2 en 3-jaars overleving 71%, 57% en 14% met een mediane overleving van 25 maanden. Bij de resectiegroup was dit 69%, 56%, 23% en 23 maanden. In een systematische review werden 13 studies geïncludeerd. De 1, 3 en 5 jaar overleving was 40%-92%, 0%-57% en 14%-32% met een mediane overleving van 21-43 maanden en een lokaal recidief percentage van 2%-13% (58).
Geïsoleerde leverperfusie
De geïsoleerde leverperfusie is ontwikkeld ten tijde van de relatief ineffectieve ‘oude’ systemische chemotherapie, die een laag responspercentage gaf bij patiënten met een gemetastaseerd colorectaal carcinoom (55). De huidige systemische therapie is veel effectiever in vergelijking met historische chemotherapie, met dezelfde respons percentages als de geïsoleerde leverperfusie (52). Mede gezien de belasting voor de patiënt, wordt daarom de geïsoleerde leverperfusie voor patiënten met colorectale levermetastasen zelden tot nooit meer toegepast.
Trans arteriële chemo embolisatie
Trans Arteriële Chemo Embolisatie (TACE) is een methode waarbij men de colorectale levermetastase probeert te vernietigen door zowel de bloedtoevoer naar de metastase af te sluiten, als door zeer lokaal in de tumor chemotherapie te geven. Dit gebeurt door chemotherapeutica zeer selectief toe te dienen in de arterie of meerdere arteriën die de metastase(n) van bloed voorziet/voorzien. Recent is hier de TACE DEBIRI bijgekomen; dit is een TACE met zogenaamde ‘drug eluting beads of irinotecan’. Tegelijkertijd vindt embolisatie plaats van desbetreffende arterie/arteriën. Hierdoor ontstaat enerzijds een verminderde aanvoer van zuurstof en voeding voor de metastase waardoor de tumorcellen beschadigd raken. Anderzijds vindt er een grotere opname plaats van het chemotherapeuticum door de vertraagde bloedstroom en de hogere directe concentratie. Het effect van de chemotherapie neemt hierdoor toe. In Nederland doet de interventie radioloog dit op een percutane manier.
De literatuur van TACE voor patiënten met colorectale levermetastasen is zeer beperkt. Tot 2013 zijn er 6 case series beschreven en 1 fase 3 trial. De studie van Florentini, randomiseerde 75 patiënten tussen chemo-embolisatie met irinotecan eluting beads (DEBIRI) of FOLFIRI (16). Na 50 maanden was de algehele overleving significant beter in de groep van patiënten die behandeld waren met DEBIRI ten opzichte van de patiënten die behandeld waren met FOLFIRI (p=0,031) HR 0,60 (95%BI: 0,37-0,97). De mediane overleving was 22 maanden (95%BI: 21-23), voor DEBIRI en 15 maanden (95%BI: 12-18) voor de FOLFIRI groep. Belangrijkste tekortkoming van de studie was de onduidelijke randomisatie en daardoor de mogelijkheid van een ingeslopen bias.
Yttrium-90-radio-embolisatie
Intra-arteriële Yttrium-90 radio-embolisatie (90Y-RE) is een nieuwe behandeling voor salvage patiënten met colorectale levermetastasen (CRCLM). Het gaat hierbij om patiënten waarbij de uitzaaiingen beperkt zijn tot de lever, de primaire tumor verwijderd is en patiënt progressief is na standaard chemotherapie lijnen (oxaliplatin en irinotecan). Studies waarin CRCLM patiënten in salvage setting worden behandeld met radio-embolisatie rapporteren een mediane overleving van 10,0 maanden (21). De potentiële voordelen van de behandeling met 90Y-RE ten opzichte van best-supportive care, voor de uitkomstenmaat totale overleving zijn onderzocht in 3 gerandomiseerde studies (20; 21; 53). Er zijn geen resultaten uit RCT’s beschikbaar die 90Y vergelijken met 1e of 2e lijn chemotherapie. Een dergelijk studie is momenteel wel gaande.
Stereotactische radiotherapie
Bij stereotactische radiotherapie (SRT) wordt hoge bestralingsdoses gegeven met hoge precisie in een klein aantal fracties. Er zijn geen strikte criteria qua aantal metastasen en maximale tumordiameter voor SRT. Kandidaten voor een ablatieve behandeling met SRT zijn over het algemeen patiënten met één tot vier metastasen, met een maximale tumordiameter van 5 tot 6 cm, in redelijk goede conditie en indien extra-hepatische ziekte aanwezig is moet deze potentieel behandeld kunnen worden (10; 5; 19; 27; 37; 43; 44; 55; 59; 22; 24; 28; 29; 50). Patiënten die in aanmerking komen voor SRT hebben irresectabele levermetastasen en vaak liggen deze ongunstig voor radiofrequentie ablatie (RFA).
De lokale controle bij 1 en 2 jaar na SRT in gepubliceerde series met alleen colorectale levermetastasen varieerde tussen 67%-100% en 55%-78% (24; 29; 51; 12; 54)*. De overleving bij 1 en 2 jaar varieerde tussen 53-100% en 38-83% (29; 51; 12; 54). De gerapporteerde mediane overleving lag tussen 25 en 34 maanden in twee gepubliceerde series (29; 54). Toxiciteit gerelateerd aan de behandeling met SRT voor levermetastasen is over het algemeen beperkt. Verhoogde geïsoleerde leverenzymen, misselijkheid, vermoeidheid, gastritis en huidtoxiciteit zijn gerapporteerd (19; 31; 44; 54; 24; 54).
Een prospectieve studie heeft de impact geanalyseerd van SRT op de kwaliteit van leven van 28 patiënten met levertumoren, vooral patiënten met levermetastasen (60). Gemiddelde waarden van QoL-5D (EQ-5D) index, EQ-VAS score en EORTC-QLQ C-30 global health status namen toe na de behandeling maar er was geen significant verschil tussen de waarden voor de behandeling en één, drie en zes maanden daarna.
*) Met betrekking tot Hoyer 2006; personal communication over data betreffend lokale controle van levermetastasen op 2 jaar was 78%.
Chirurgische behandeling
Resectie van colorectale levermetastasen leidt in de meer recente studies bij geselecteerde patiëntengroepen tot een 5-jaars overleving van 30% tot 60%, echter slechts 15-30% van de patiënten met levermetastasen zijn uiteindelijk resectabel met curatieve intentie (21). Er zijn geen klinische studies die patiënten randomiseren tussen resectie en systemische chemotherapie. Er zijn ook geen prospectieve studies uitgevoerd waarbij patiënten met een beperkt aantal en resectabele colorectale levermetastasen behandeld zijn met moderne systemische therapie. Voor patiënten met uitgebreide colorectale levermetastasen zijn er een tweetal case-control series beschreven. De grootste serie is van Broquet (2011). Deze vergelijkt 2 groepen patiënten met dezelfde patiënten karakteristieken behandeld met alleen systemische chemotherapie (n=62, groep 1) versus systemische chemotherapie gevolgd door resectie (n=65, groep 2). In groep 1 werden alleen patiënten geïncludeerd die respondeerden op systemische chemotherapie. Beide groepen hadden mediaan 6 colorectale levermetastasen (range 2-18) en waren verder ook vergelijkbaar op alle andere karakteristieken. Groep 2 had een langere overleving (5-jaars overleving 15% vs. 51%)
Ook Kopetz liet een vergelijkbaar resultaat zien in hun retrospectieve serie van patiënten die een resectie hebben ondergaan versus alleen systemische therapie (23). Er is dus geen bewijs van hoog niveau dat lokale therapie een langere overleving oplevert ten opzichte van systemische therapie. De overleving na partiële leverresectie is dermate overtuigend ten opzichte van het resultaat van systemische behandelingen dat dit de behandeling van voorkeur is.
Criteria voor resectabiliteit
Gezien de eventuele toepassing van effectieve systemische chemotherapie, de verbeterde technieken en toegenomen mogelijkheden van lokale therapieën voor patiënten met colorectale levermetastasen en de toegenomen mogelijkheden voor behandeling van het eventuele recidief, zijn de ‘klassieke prognostische factoren’ niet meer van toepassing (11; 31).
Voldoende rest- leverweefsel na resectie
De mogelijkheid om resectie van een groot deel van het levervolume uit te voeren, zonder risico op postoperatieve insufficiëntie van de restlever, wordt mede bepaald door de kwaliteit van het parenchym. Bij normaal leverparenchym kan maximaal tot 80% van het levervolume worden verwijderd met gering gevaar op postoperatief leverfalen (13; 22; 24; 32; 1). Bij aangedaan leverweefsel na systemische therapie en/of cirrose wordt dit percentage kleiner (1). De normale lever heeft een aanzienlijk vermogen tot regeneratie waardoor de levercapaciteit postoperatief zal toenemen. Echter als het te reseceren deel meer dan 80 procent van het functionerend leverweefsel betreft worden de morbiditeit en mortaliteit duidelijk hoger als gevolg van postoperatieve leverinsufficiëntie. Dit houdt in dat als er uitgebreide resecties worden overwogen waarbij slechts 20% van de lever overblijft na resectie, er een combinatiebehandeling moet worden overwogen. Bij diffuse parenchymafwijkingen, zoals bij cirrose of uitgebreide steatose, is het maximaal te verwijderen volume echter veel beperkter (32). Ook het vermogen tot leverregeneratie en daarmee de mogelijkheid tot herstel van leverfunctie, is veel kleiner.
Een van de mogelijkheden om de toekomstige restleverfunctie te vergroten is het uitvoeren van een preoperatieve selectieve vena portae embolisatie aan de aangedane zijde. Hierdoor wordt hypertrofie geïnduceerd in het contralaterale deel van de lever zodat deze een grotere functionele capaciteit krijgt en de resectie veiliger kan worden verricht. Een van de problemen is dat niet altijd het effect van deze procedure voorspeld kan worden en dat metingen van de werkelijke leverfunctie lastig zijn.
Volumetrie van de lever
Het meten van het volume van de toekomstige lever na resectie gebeurt door middel van volumetrie van de al verkregen diagnostische spiraal CT of MRI data. De minimale grootte van de restlever ten opzichte van het totale volume van een gezonde lever dient 20% te zijn om een veilige leverresectie uit te voeren bij patiënten die niet zijn voorbehandeld met systemische therapie en/of levercirrose. Dit komt ongeveer overeen met een resectie van minder dan 6 leversegmenten. Voor patiënten met een chronische ziekte geldt hiervoor een grens van 50%-60% ofwel 4-5 segmenten. Het volume van de lever correleert echter niet altijd goed met de werkelijke functie van de lever. Er zijn een tweetal technieken om de leverfunctie te bepalen: Indocyaninegroen (ICG)-test en hepatobiliaire scintigrafie. Met zowel de ICG-klaringstest als hepatobiliaire scintigrafie meet men uiteraard de functie van de gehele lever. Er bestaat echter tot op heden geen manier om de functie van de toekomstige restlever te bepalen.
Met betrekking tot de kans op het optreden van postoperatieve leverinsufficiëntie en de complicaties die daarvan het gevolg zijn wordt een voorspelling gedaan op basis van de volgende gegevens:
- de geschatte functie van de lever,
- het volume van de toekomstige restlever,
- de aan- en afwezigheid van steatose of fibrose,
- de algemene toestand van de patiënt.
De resultaten van re-chirurgie indien het tijdsinterval van hernieuwde metastasen <6 maanden is, lijken slechter dan indien het tijdsinterval >6 maanden is.
Vena portae embolisatie
Mortaliteit en morbiditeit na leverresecties worden voor een belangrijk deel bepaald door de functie van het deel van de restlever. Een te kleine restlever kan leiden tot postoperatieve leverinsufficiëntie. Hierdoor kan de patiënt in een hepatisch coma raken en is de kans op overlijden groot (80%).
Vena portae embolisatie (VPE) is een methode met als doel het vergroten van het volume van de toekomstige restlever voordat de resectie plaatsvindt. De literatuur laat een gemiddelde stijging van het volume van de toekomstige restlever na embolisatie ten opzichte van de toekomstige restlever voor embolisatie van 37,9% (35). Voor patiënten met een normale leverfunctie is een periode van 2-4 weken voldoende om adequate hypertrofie te bereiken. Voor patiënten met een cirrotische lever of met diabetes mellitus geldt hiervoor een periode van 6-8 weken. Vooral cirrose heeft een negatieve invloed op de mate van hypertrofie. Dit geldt in mindere mate voor schade aan de lever door cholestase en chemotherapie (35). Het volume van de lever correleert echter niet altijd goed met de werkelijke functie van de lever. Er zijn tweetal technieken om de leverfunctie te bepalen: Indocyaninegroen (ICG)-test en hepatobiliaire scintigrafie. 99mTC-mebrofenin hepatobiliaire scintigrafie kan worden toegepast om het risico op postoperatief leverfalen in te schatten (15).
Op basis van gegevens over de geschatte functie van de lever en het volume van de toekomstige restlever, de aan- en afwezigheid van steatose of fibrose en de algemene toestand van de patiënt wordt een voorspelling gedaan met betrekking tot de kans op het optreden van postoperatieve leverinsufficiëntie en de complicaties die daarvan het gevolg zijn.
De meest toegepaste technieken die worden gebruikt om toegang tot de vena portae te verkrijgen zijn directe cannulatie van de vena ileocolica, de percutane toegangsweg en peroperatief chirurgisch als blijkt dat het te reseceren volume groter is dan preoperatief voorspeld. De percutane techniek kan zowel ipsilateraal als contralateraal worden toegepast en heeft als voordeel dat er geen laparotomie hoeft plaats te vinden met de bijbehorende risico’s. Deze techniek minimaliseert het risico van trombose van de vena portae hoofdstam en schade aan de contralaterale vasculatuur.
Er zijn verschillende middelen beschreven waarmee de embolisatie kan worden uitgevoerd zoals n-butyl cyanoacrylaat met ethiodide olie, gelfoam, polidocanol, fibrinelijm, coils, polyvinyl alcohol (PVA), microsferen, ethanol, Amplatzer plugs, of een combinatie van middelen. De optimale (combinatie) van embolisatiemateriaal voor porta-embolisatie is niet duidelijk. Bij tijdelijke (absorbeerbare) materialen bestaat de kans op rekanalisatie met minder hypertrofie als gevolg (36). N-butyl cyanoacrylaat heeft mogelijk het beste effect, echter in een recente meta-analyse werd geen statistisch verschil aangetoond tussen de verschillende embolisatiematerialen (35). De preoperatieve mortaliteit varieert van 0-6,5% voor patiënten zonder cirrose en 6-7% voor patiënten met cirrose. Bij minder dan 15% van de patiënten traden complicaties op. Dit percentage is gelijk aan of lager dan het percentage complicaties na partiële resectie zonder VPE.
Een mogelijk nadeel van VPE is dat na resectie, de regeneratieve capaciteit van de restlever is uitgeput en dat een relatief tekort niet meer kan worden gecompenseerd.
Vrij recent is er een nieuwe techniek beschreven waar het leverparenchym wordt doorgenomen en de vena portae wordt geligeerd, maar de leverkwab wordt niet direct gereseceerd (Associating liver partition and portal vein ligation for staged hepatectomy: ALPPS) (33). Dit gebeurde na mediaan 9 dagen waarbij er een volume toename werd gezien van de ‘rest-lever’ van 73%. Deze techniek moet gezien worden als experimenteel en heeft nog geen vaste plaats in de behandeling van patiënten met colorectale levermetastasen.
Tumorvrije marge na resectie metastasen
Over het algemeen wordt een marge van minimaal 10 mm gehanteerd, echter door de technische ontwikkelingen, de ontwikkelingen van de systemische therapie en ervaring van chirurgen is het mogelijk om bij marges van kleiner dan 10 mm te reseceren zonder vitale structuren (vaat/galweg) te bedreigen. Er is geen eenduidige literatuur over de grootte van de marge (retrospectieve series). In het algemeen kan men zeggen dat 1 mm voldoende is bij een gelijke overleving ten opzichte van grotere marges (9). In het tijdperk van moderne/effectieve chemotherapie lijkt een marge van 0 mm te voldoen, afhankelijk van de respons op de chemotherapie (9; 7).
Inductie systemische therapie
Patiënten met primair irresectabele maar potentieel resectabele metastasen dienen behandeld te worden met inductie systemische therapie. Het doel is een zodanige tumorreductie te verkrijgen dat een radicale resectie alsnog mogelijk wordt. Kenmerken van deze inductiebehandeling zijn dat een schema met een zo groot mogelijke kans op een objectieve respons wordt gekozen, en dat de duur van de behandeling wordt beperkt ter voorkoming van chirurgische complicaties. Een resectie dient dus plaats te vinden zodra metastasen resectabel zijn geworden. De bevinding dat metastasen in complete radiologische remissie in de meeste gevallen nog vitale tumorcellen bevatten is een tweede argument om niet de maximale tumorrespons af te wachten (10). Op grond van huidige gegevens kan echter geen duidelijke voorkeur worden uitgesproken om lokalisatie van radiologisch niet meer aantoonbare metastasen chirurgisch te verwijderen dan wel intact te laten. Voor meer gedetailleerde bespreking van de keuze van systemische therapie wordt verwezen naar de betreffende module.
Extrahepatische tumorgroei (inclusief hilus lymfklieren)
Vele studies laten zien dat patiënten met extrahepatische afwijkingen een slechtere prognose hebben dan patiënten zonder extrahepatische afwijkingen (12). Meerdere studies laten echter ook zien, dat een lange termijn overleving behaald kan worden bij een selectie van de patiënten. Dit zijn retrospectieve series, waarbij specifieke lokalisaties zeer beperkte overlevingsgetallen laten zien na resectie (bijvoorbeeld bijniermetastasen, para-aortale of truncus coeliacus klieren). Een meta-analyse bij 1.152 patiënten met gelijktijdige extrahepatische metastasen, laat ook zien dat lange termijn overleving behaald kan worden na resectie van hepatische en extrahepatische metastasen (12). Als er metastasen in één extrahepatisch orgaan zijn, lijkt de overleving beter na resectie dan de overlevingsgetallen van patiënten die behandeld zijn met systemische therapie alleen. Indien er metastasen in meer dan één extrahepatisch orgaan zijn, is de toegevoegde waarde van resectie mogelijk zeer beperkt en lijkt de overleving gelijk aan alleen systemische therapie.
Leeftijd
Twee patiëntkenmerken zijn belangrijk voor de bepaling van de operabiliteit: leeftijd en lichamelijke conditie. Om vast te stellen of een patiënt een operatie kan ondergaan, is een preoperatieve evaluatie belangrijk. Zowel de leeftijd als de algemene conditie zullen maatgevend zijn voor risico’s op complicaties. Uit meerdere studies blijkt dat bij patiënten ouder dan 70 jaar, en zelfs 80 jaar, een 5 jaars-overleving hebben die conform de jongere leeftijd is (2).
Synchrone vs. metachrone levermetastasen
Er zijn geen studies die overleving van patiënten met synchrone levermetastasen vergelijken met patiënten met metachrone levermetastasen in prospectieve setting, rekening houdend met andere factoren zoals: aantal, grootte, uni-of bilobaire locatie, etc. In diverse retrospectieve studies wordt een 5-jaarsoverleving gerapporteerd conform de overleving na resectie van metachrone levermetastasen, ook bij een lokaal uitgebreide primaire tumor (39; 26; 34). Synchroniciteit is daarom geen contra-indicatie is voor partiële leverresectie (27; 38; 17).
Verschillende reviews en meta-analyses zijn uitgevoerd ten aanzien van timing van resectie van synchrone levermetastasen (39; 26; 34). Opgemerkt moet worden dat het hier niet gaat om prospectieve of gerandomiseerde studies. De mogelijkheden zijn synchrone resectie van primaire tumor en metastasen of metachrone resectie waarbij de primaire tumor eerst wordt geopereerd en 2 tot 3 maanden later de metastasen.
De laatste jaren is er een opkomst van de ‘Liver first approach’ waarbij eerst de lever wordt geopereerd en 2 tot 3 maanden later de primaire tumor. De literatuur over de ‘Liver first approach’ is zeer beperkt, er is een meta-analyse verricht en is er één artikel gepubliceerd met de lange termijns overleving (25; 8; 41). Op basis van de reviews en meta-analyse is er geen absolute voorkeur uit te spreken voor één van deze drie benaderingen. Uit de literatuur is wel te concluderen dat de synchrone resectie wordt uitgevoerd bij patiënten met een beperkt aantal metastasen en een lokaal beperkte tumor. Dit omdat anders wordt verwacht dat morbiditeit en zelfs mortaliteit zal toenemen (3). Timing is afhankelijk van expertise van het centrum.
Chirurgische anatomie van de lever
De functionele, anatomische indeling van de lever in acht segmenten (I-VIII) door de Franse chirurg Couinaud betekende een belangrijke stap voorwaarts in de ontwikkeling van de leverchirurgie. Ieder segment vormt een functionele eenheid met gescheiden arteriële en portale aanvoerende vaten en een eigen galweg. De drie levervenen (respectievelijk de rechter en linker levervenen, en de centrale levervene) verdelen de lever in vier sagittale sectoren en draineren in de suprahepatisch gelegen vena cava. Het vlak tussen de twee middelste sectoren vormt de anatomische scheiding tussen rechter en linker leversegmenten (het anatomische midden van de lever) en wordt bepaald door de centrale levervene (zie figuur 1).
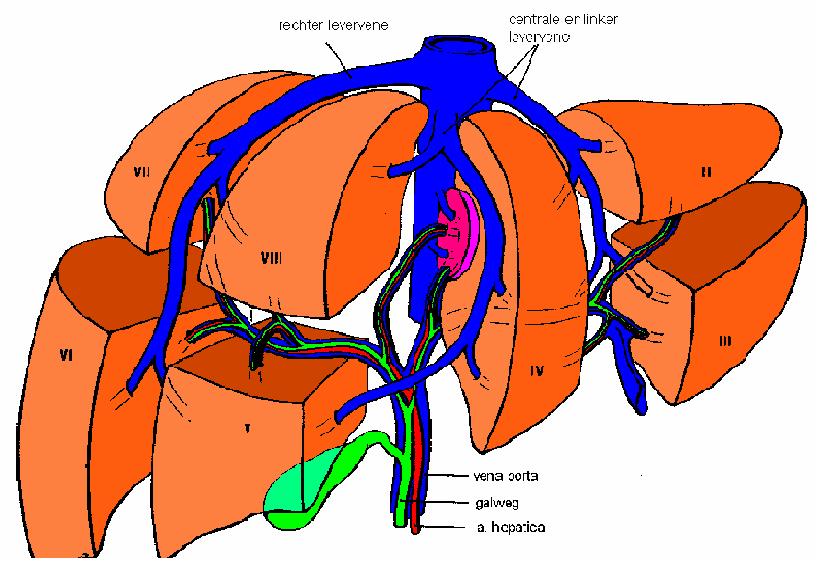
Figuur 1. Chirurgische anatomie van de lever
Soorten partiële leverresectie
Een type resectie wordt benoemd naar de segmenten die bij de resectie worden verwijderd. De klassieke, anatomische resecties zijn de rechtszijdige en linkszijdige hemihepatectomie waarbij respectievelijk, de segmenten 5, 6, 7 en 8 of de segmenten 2, 3 en 4 worden gereseceerd. Deze resecties kunnen worden uitgebreid door van de contralaterale zijde, één of twee segmenten extra te reseceren: een uitgebreide (extended) hemihepatectomie rechts omvat dan excisie van de segmenten 5, 6, 7, 8 en 4 (in de Engelstalige literatuur ook wel trisegmentectomy genoemd) terwijl een uitgebreide (extended) hemihepatectomie links excisie van de segmenten 1, 2, 3, 4 en daarbij nog de segmenten 5 en 8 betekent.
Kleinere resecties zijn de bisegmentectomieën zoals een segment 2/3 resectie of segment 6/7 resectie, meestal voor perifeer gelegen tumoren. De keuze van een resectie wordt bepaald door de locatie, aantal en grootte van de tumor(en) als ook de nabijheid van belangrijke vasculaire structuren. Over het algemeen wordt gestreefd naar zo klein mogelijk resecties, met behoud van zoveel mogelijk parenchym. Indien mogelijk zal men segmentele resecties uitvoeren of zelfs een deel van een segment (subsegmentele resectie). Oppervlakkige gelegen tumoren kunnen lokaal worden gereseceerd (wigexcisie).
Er blijkt geen verschil in overleving te zijn tussen anatomische en niet-anatomische resecties, waarbij het resectievlak door een segment loopt. Bovendien is de morbiditeit en mortaliteit niet hoger in de niet-anatomische groep.
Complicaties na leverresectie
De meest voorkomende complicaties na leverresecties zijn bloedverlies, gallekkage, sepsis en insufficiëntie van de restlever. Vooral de mate van bloedverlies tijdens de operatie en het aantal verwijderde segmenten zijn gecorreleerd met het optreden van complicaties na de ingreep. Veel van de maatregelen die worden toegepast bij leverresecties zijn dan ook gericht op het zoveel mogelijk beperken van het bloedverlies. Overmatig bloedverlies tijdens partiële leverresecties kan worden beperkt door:
- Tijdelijke occlusie van de afferente bloedvaten naar de lever. De Pringle-manoeuvre waarbij zowel de vena portae als de arteria hepatica worden afgeklemd is de klassieke methode om bloedtoevoer naar de lever tijdelijk uit te schakelen. Er zijn twee manieren om dit uit te voeren: intermitterend afklemmen en continue afklemmen.
- Volledige vasculaire exclusie van de lever. Bij resecties waar ook een deel van de vena cava dient te worden verwijderd, kan totale vasculaire exclusie van de lever worden toegepast waarbij naast de Pringle-manoeuvre, ook de vena cava craniaal en caudaal van de lever wordt afgeklemd.
- Het laag houden van de centraal veneuze druk (<4 cm Hg) beperkt het retrograad bloedverlies uit de levervenen en het capillaire bed. Onder deze omstandigheden kunnen de meeste leverresecties zonder groot bloedverlies worden uitgevoerd.
Het toepassen van technieken voor dissectie van het leverparenchym. Voor de parenchymale dissectie kunnen verschillende technieken worden gebruikt om met zo min mogelijk bloedverlies het parenchym te klieven. Er lijkt geen verschil te zijn in uitkomst, tussen de verschillende technieken van parenchymdissectie. Een veel toegepaste methode is de CUSA (Cavitron Ultrasonic Surgical Aspirator) waarbij het parenchym selectief wordt verwijderd zodat kleine bloedvaten en galtakken kunnen worden afgebonden. Het toepassen van hemostatische middelen aan het einde van de operatie lijkt geen invloed te hebben op post operatieve complicaties. Twee RCT’s lieten geen verschil zien in het optreden van post-operatieve resectievlak gerelateerde complicaties [Fiqueras 2007] (40).
Re-resecties
Indien patiënten eerder een leverresectie hebben ondergaan en opnieuw levermetastasen ontwikkelen bestaat er een optie voor chirurgische behandeling. Uit series waarin, na zorgvuldige selectie van patiënten (voldoende rest leverparenchym, voldoende tumorvrije marge, afwezigheid van extrahepatische ziekte en klinische toestand van de patiënt) reresectie werd uitgevoerd, bleek dit een veilige procedure met goede lange termijn resultaten, conform de uitkomst van de resectie (6; 4; 16; 19; 28; 29; 30). Ook de mortaliteit en morbiditeit van reresectie blijken beperkt (42). De resultaten van re-chirurgie als het tijdsinterval van hernieuwde metastasen <6 maanden is, lijken slechter dan wanneer het tijdsinterval >6 maanden is (37).
Two stage resections
Patiënten die irresectabele afwijkingen hebben, vanwege bilobaire distributie van tumoren, kunnen in aanmerking komen voor second-stage resectie. Second-stage resectie houdt in complete resectie van de tumor in een helft van de lever, gevolgd door in tweede instantie resectie van de tumor in de contralaterale helft. De bedoeling is om het risico op leverfalen te reduceren door het uitvoeren van een tweede complete resectie nadat regeneratie is opgetreden. Dit kan gecombineerd worden met vena portae embolisatie en/of systemische therapie (18). In combinatie met portae embolisatie wordt in eerste instantie kleine laesies uit de toekomstige restlever verwijderd en in tweede instantie de vena portae embolisatie en resectie worden toegepast (5; 20). Broquet (2011) vergelijkt 2 groepen patiënten, met dezelfde patiënten karakteristieken behandeld, met alleen systemische chemotherapie (n=62, groep 1) versus systemische chemotherapie gevolgd door second stage resectie (n=65, groep 2). In groep 1 werden alleen patiënten geïncludeerd die respondeerden op systemische chemotherapie. Beide groepen hadden mediaan 6 colorectale levermetastasen (range 2-18) en waren verder ook vergelijkbaar op alle andere karakteristieken. Groep 2 had een evidente langere overleving (5-jaars overleving 15% vs. 51%).
Zoeken en selecteren
| PICO |
P |
Patienten met een stadium IV colorectaal carcinoom en metastasen in de lever |
|
Patienten met een stadium IV colorectaal carcinoom en metastasen in de longen |
||
|
I |
Lokale therapie (resectie (long/lever), RFA (lever), RT (long/lever), itriumbolletjes (lever)) |
|
|
|
||
|
C |
Systemische therapie |
|
|
O |
Lokale controle |
Referenties
- Abdalla EK, Vauthey JN, Ellis LM, et al. Recurrence and outcomes following hepatic resection, radiofrequency ablation, and combined resection/ablation for colorectal liver metstases. Ann Surg. 2004 Jun;239(6):818-25.
- Adam R, Akpinar E, Johann M, et al. Place of cryosurgery in the treatment of malignant liver tumors. Ann Surg 1997;225:39-8.
- Adam R, Hagopian EJ, Linhares M, et al. A comparison of percutaneous cryosurgery and percutaneous radiofrequency for unresectable hepatic malignancies. Arch Surg. 2002 Dec;137(12):1332-9; discussion 1340.
- Alexander HR, Libutti SK, Bartlett DL, et al. A phase I-II study of isolated hepatic perfusion using melphalan with or without tumor necrosis factor for patients with ocular melanoma metastatic to liver. Clin Cancer Res 2000;6:3062-70.
- Ambrosino G, Polistina F, Costantin G, et al. Image-guided robotic stereotactic radiosurgery for unresectable liver metastases: preliminary results. Anticancer Res 2009 Aug;29(8):3381-4.
- Bartlett DL, Libutti SK, Figg WD, et al. Isolated hepatic perfusion for unresectable hepatic metastases from colorectal cancer. Surgery. 2001 Feb;129(2):176-87.
- Berber E, Pelley R, Siperstein AE. Predictors of Survival After Radiofrequency Thermal Ablation of Colorectal Cancer Metastases to the Liver: A Prospective Study. J Clin Oncol 2005;23:1358-1364.
- Bleicher RJ, Allegra DP, Nora DT, et al. Radiofrequency ablation in 447 complex unresectable liver tumors: lessons learned. Ann Surg Oncol 2003;10:52-8.
- Blomgren H, Lax I, Göranson H, et al. Radiosurgery for Tumors in the Body: Clinical Experience Using a New Method. Journal of Radiosurgery 1998;1(1):63-74.
- Blomgren H, Lax I, Naslund I, et al. Stereotactic high dose fraction radiation therapy of extracranial tumors using an accelerator. Clinical experience of the first thirty-one patients. Acta Oncol 1995;34(6):861-70.
- Cirocchi R, Trastulli S, Boselli C, et al. Radiofrequency ablation in the treatment of liver metastases from colorectal cancer. Cochrane Database Syst Rev. 2012 Jun 13;6:CD006317.
- Chang DT, Swaminath A, Kozak M, et al. Stereotactic body radiotherapy for colorectal liver metastases: a pooled analysis. Cancer 2011 Sep 1;117(17):4060-9.
- Curley SA, Izzo F, Delrio P, et al. Radiofrequency ablation of unresectable primary and metastatic hepatic malignancies: results in 123 patients. Ann Surg. 1999 Jul;230(1):1-8.
- Dawson LA, McGinn CJ, Normolle D, et al. Escalated focal liver radiation and concurrent hepatic artery fluorodeoxyuridine for unresectable intrahepatic malignancies. J Clin Oncol 2000 Jun;18(11):2210-8.
- Decadt B, Siriwardena AK. Radiofrequency ablation of liver tumours: systematic review. Lancet Oncol 2004;5:550-60.
- Fiorentini G, Aliberti C, Tilli M, et al. Intra-arterial infusion of irinotecan-loaded drug-eluting beads (DEBIRI) versus intravenous therapy (FOLFIRI) for hepatic metastases from colorectal cancer: final results of a phase III study. Anticancer Res. 2012 Apr;32(4):1387-95.
- Gillams AR, Lees WR. Radio-frequency ablation of colorectal liver metastases in 167 patients. Eur Radiol 2004;14:2261-7.
- Gillams AR, Lees WR. Survival after percutaneous, image-guided, thermal ablation of hepatic metastases from colorectal cancer. Dis Colon Rectum. 2000 May;43(5):656-61.
- Goodman KA, Wiegner EA, Maturen KE, et al. Dose-escalation study of single-fraction stereotactic body radiotherapy for liver malignancies. Int J Radiat Oncol Biol Phys 2010 Oct 1;78(2):486-93.
- Gray B, Van Hazel G, Hope M, et al. Randomised trial of SIR-Spheres plus chemotherapy vs. chemotherapy alone for treating patients with liver metastases from primary large bowel cancer. Ann Oncol. 2001 Dec;12(12):1711-20.
- Hendlisz A, Van den Eynde M, Peeters M, et al. Phase III trial comparing protracted intravenous fluorouracil infusion alone or with yttrium-90 resin microspheres radioembolization for liver-limited metastatic colorectal cancer refractory to standard chemotherapy. J Clin Oncol. 2010 Aug 10;28(23):3687-94. doi: 10.1200/JCO.2010.28.5643. Epub 2010 Jun 21.
- Herfarth KK, Debus J. Stereotactic radiation therapy for liver metastases. Chirurg 2005 Jun;76(6):564-9.
- Herfarth KK, Debus J, Lohr F, et al. Stereotactic single-dose radiation therapy of liver tumors: results of a phase I/II trial. J Clin Oncol 2001 Jan 1;19(1):164-70.
- Hoyer M, Roed H, Traberg HA, et al. Phase II study on stereotactic body radiotherapy of colorectal metastases. Acta Oncol 2006;45(7):823-30.
- Jiang HC, Liu LX, Piao DX, et al. Clinical short-term results of radiofrequency ablation in liver cancers. World J Gastroenterol 2002;8:624-30.
- Johnson LB, Krebs TL, Van Echo D, et al. Cytoablative therapy with combined resection and cryosurgery for limited bilobar hepatic colorectal metastases. Am J Surg. 1997 Dec;174(6):610-3.
- Katz AW, Carey-Sampson M, Muhs AG, et al. Hypofractionated stereotactic body radiation therapy (SBRT) for limited hepatic metastases. Int J Radiat Oncol Biol Phys 2007 Mar 1;67(3):793-8.
- Kavanagh BD, McGarry RC, Timmerman RD. Extracranial radiosurgery (stereotactic body radiation therapy) for oligometastases. Semin Radiat Oncol 2006 Apr;16(2):77-84.
- Kim MS, Kang JK, Cho CK, et al. Three-fraction stereotactic body radiation therapy for isolated liver recurrence from colorectal cancer. Tumori. 2009 Jul-Aug;95(4):449-54.
- Kuvshinoff BW, Ota DM. Radiofrequency ablation of liver tumors: influence of technique and tumor size. Surgery. 2002 Oct;132(4):605-11; discussion 611-2.
- Lee MT, Kim JJ, Dinniwell R, et al. Phase I study of individualized stereotactic body radiotherapy of liver metastases. J Clin Oncol 2009 Apr 1;27(10):1585-91.
- Lencioni R, Crocetti L, Cioni D, et al. Percutaneous radiofrequency ablation of hepatic colorectal metastases: technique, indications, results, and new promises. Invest Radiol. 2004 Nov;39(11):689-97.
- Lencioni R, Donati F, Cioni D et al. Detection of colorectal liver metastases: prospective comparison of unenhanced and ferumoxides-enhanced magnetic resonance imaging at 1.5 T, dual-phase spiral CT, and spiral CT during arterial portography. MAGMA 1998;7:76-87.
- Livraghi T, Meloni F, Solbiati L, et al; Collaborative Italian Group using AMICA system. Complications of microwave ablation for liver tumors: results of a multicenter study. Cardiovasc Intervent Radiol. 2012 Aug;35(4):868-74.
- McGahan JP, Browning PD, Brock JM, et al. Hepatic ablation using radiofrequency electrocautery. Invest Radiol 1990;25:267-70.
- McGinn CJ, Ten Haken RK, Ensminger WD, et al. Treatment of intrahepatic cancers with radiation doses based on a normal tissue complication probability model. J Clin Oncol 1998 Jun;16(6):2246-52.
- Mendez Romero A, Wunderink W, Hussain SM, et al. Stereotactic body radiation therapy for primary and metastatic liver tumors: A single institution phase i-ii study. Acta Oncol 2006;45(7):831-7.
- Mulier S, Mulier P, Ni Y, et al. Complications of radiofrequency coagulation of liver tumours. Br J Surg 2002;89:1206-22.
- Oshowo A, Gillams A, Harrison E, et al. Comparison of resection and radiofrequency ablation for treatment of solitary colorectal liver metastases. Br J Surg. 2003 Oct;90(10):1240-3.
- Pathak S, Jones R, Tang JM, et al. Ablative therapies for colorectal liver metastases: a systematic review. Colorectal Dis. 2011 Sep;13(9):e252-65.
- Rothbarth J, Pijl ME, Vahrmeijer AL, et al. Isolated hepatic perfusion with high-dose melphalan for the treatment of colorectal metastasis confined to the liver. Br J Surg 2003;90:1391-7.
- Ruers T, Punt C, Van Coevorden F, et al; EORTC Gastro-Intestinal Tract Cancer Group, Arbeitsgruppe Lebermetastasen und?tumoren in der Chirurgischen Arbeitsgemeinschaft Onkologie (ALM-CAO) and the National Cancer Research Institute Colorectal Clinical Study Group (NCRI CCSG). Radiofrequency ablation combined with systemic treatment versus systemic treatment alone in patients with non-resectable colorectal liver metastases: a randomized EORTC Intergroup phase II study (EORTC 40004). Ann Oncol. 2012 Oct;23(10):2619-26.
- Rule W, Timmerman R, Tong L, et al. Phase I Dose-Escalation Study of Stereotactic Body Radiotherapy in Patients With Hepatic Metastases. Ann Surg Oncol. 2011 Apr;18(4):1081-7. doi: 10.1245/s10434-010-1405-5. Epub 2010 Nov 3.
- Rusthoven KE, Kavanagh BD, Cardenes H, et al. Multi-institutional phase I/II trial of stereotactic body radiation therapy for liver metastases. J Clin Oncol 2009 Apr 1;27(10):1572-8.
- Schefter TE, Kavanagh BD, Timmerman RD, et al. A phase I trial of stereotactic body radiation therapy (SBRT) for liver metastases. Int J Radiat Oncol Biol Phys 2005 Aug 1;62(5):1371-8.
- Seifert JK, Morris DL. Prognostic factors after cryotherapy for hepatic metastases from colorectal cancer. Ann Surg 1998; 228:201-8.
- Solbiati L, Ierace T, Goldberg SN, et al. Percutaneous US-guided radio-frequency tissue ablation of liver metastases: treatment and follow-up in 16 patients. Radiology. 1997 Jan;202(1):195-203.
- Solbiati L, Ierace T, Tonolini M, et al. Radiofrequency thermal ablation of hepatic metastases. Eur J Ultrasound 2001;13:149-158.
- Solbiati L, Ierace T, Tonolini M. Long-term survival of patients treated with radiofrequency ablation for liver colorectal metastases: improved outcome with increasing experience. Radiology 2003 S;229,:411.
- Solbiati L, Livraghi T, Goldberg SN, et al. Percutaneous radio-frequency ablation of hepatic metastases from colorectal cancer: long-term results in 117 patients. Radiology. 2001 Oct;221(1):159-66.
- Stintzing S, Hoffmann RT, Heinemann V, et al. Frameless single-session robotic radiosurgery of liver metastases in colorectal cancer patients. Eur J Cancer 2010 Apr;46(6):1026-32.
- van Iersel LB, Koopman M, van de Velde CJ, et al. Management of isolated nonresectable liver metastases in colorectal cancer patients: a case-control study of isolated hepatic perfusion with melphalan versus systemic chemotherapy. Ann Oncol. 2010 Aug;21(8):1662-7. doi: 10.1093/annonc/mdp589. Epub 2010 Jan 28.
- Van Hazel G, Blackwell A, Anderson J, et al. Randomised Phase 2 Trial of SIR-Spheres1 Plus Fluorouracil/Leucovorin Chemotherapy Versus Fluorouracil/Leucovorin Chemotherapy Alone in Advanced Colorectal Cancer. J Surg Oncol. 2004 Nov 1;88(2):78-85.
- Van der Pool AE, Mendez RA, Wunderink W, et al. Stereotactic body radiation therapy for colorectal liver metastases. Br J Surg 2010 Mar;97(3):377-82.
- Vautravers-Dewas C, Dewas S, Bonodeau F, et al. Image-guided robotic stereotactic body radiation therapy for liver metastases: is there a dose response relationship? Int J Radiat Oncol Biol Phys. 2011 Nov 1;81(3):e39-47. doi: 10.1016/j.ijrobp.2010.12.047. Epub 2011 Mar 4.
- Verhoef C, de Wilt JH, Brunstein F, et al. Isolated hypoxic hepatic perfusion with retrograde outflow in patients with irresectable liver metastases; a new simplified technique in isolated hepatic perfusion. Ann Surg Oncol. 2008 May;15(5):1367-74. doi: 10.1245/s10434-007-9714-z. Epub 2008 Feb 1.
- Weng M, Zhang Y, Zhou D, et al. Radiofrequency ablation versus resection for colorectal cancer liver metastases: a meta-analysis. PLoS One. 2012;7(9):e45493.
- White TJ, Roy-Choudhury SH, Breen DJ, et al. Percutaneous radiofrequency ablation of colorectal hepatic metastases - initial experience. An adjunct technique to systemic chemotherapy for those with inoperable colorectal hepatic metastases. Dig Surg 2004;21:314-20.
- Wulf J, Guckenberger M, Haedinger U, et al. Stereotactic radiotherapy of primary liver cancer and hepatic metastases. Acta Oncol 2006;45(7):838-47.
- Méndez Romero A, Wunderink W, van Os RM, et al. Quality of life after stereotactic body radiation therapy for primary and metastatic liver tumors. Int J Radiat Oncol Biol Phys. 2008 Apr 1;70(5):1447-52. Epub 2007 Nov 8.
Verantwoording
Autorisatiedatum en geldigheid
Laatst beoordeeld : 29-10-2019
Laatst geautoriseerd : 29-10-2019
Geplande herbeoordeling : 01-04-2020
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep in stand gehouden voor een periode van 3 jaar, met optionele verlenging van 3 jaar. De werkgroep zal halfjaarlijks bijeen komen voor een herbeoordeling van de geldigheid van de modules in deze richtlijn. De geldigheid van richtlijnmodules zal bij herbeoordeling komen te vervallen wanneer nieuwe ontwikkelingen aanleiding geven om een herzieningstraject te starten. De Nederlandse Vereniging voor Heelkunde (NVvH) is regiehouder van deze richtlijn en eindverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijnmodules. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied. Per module is aangegeven welke wetenschappelijke vereniging de eerstverantwoordelijke is voor de actualiteitsbeoordeling (zie de Algemene inleiding).
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijn.
Doel en doelgroep
Doel
Het beschrijven van het beleid bij patiënten met een colorectaal carcinoom: gestandaardiseerd en op hun wensen afgestemd in alle fasen van de ziekte.
Doelgroep
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen die betrokken zijn bij de zorg voor patiënten met colorectaal carcinoom in de tweede en derde lijn.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2017 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met colorectaal carcinoom te maken hebben. De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
De huidige samenstelling van de werkgroep
- Prof. dr. P.J. (Pieter) Tanis, gastrointestinaal en oncologisch chirurg, Erasmus MC, Rotterdam, NVvH (voorzitter)
- Prof. dr. G.L. (Geerard) Beets, gastrointestinaal en oncologisch chirurg, Antoni van Leeuwenhoek, Amsterdam, NVvH
- Prof. dr. R.G.H. (Regina) Beets-Tan, radioloog, Nederlands Kanker Instituut, Amsterdam, NVvR
- S. Dokter (Simone) MSc., verpleegkundig specialist, Antoni van Leeuwenhoek, Amsterdam, V&VN
- C.M.J. (Christel) Gielen MSc., verpleegkundig specialist, Maastricht UMC+, Maastricht, V&VN
- Dr. D.J.A. (Derk Jan) de Groot, internist-oncoloog, UMC Groningen, Groningen, NIV/NVMO (vanaf december 2018)
- Dr. M.E. (Marije) Hamaker, klinisch geriater, Diakonessenhuis, Utrecht, NVKG
- Dr. C.J. (Corneline) Hoekstra, nucleair geneeskundige, Jeroen Bosch Ziekenhuis, ’s-Hertogenbosch, NVNG
- Dr. M.P.W. (Martijn) Intven, radiotherapeut, UMC Utrecht, Utrecht, NVRO
- Dr. O.J.L. (Olaf) Loosveld, internist-oncoloog, Amphia Ziekenhuis, Brede, NIV/NVMO
- Dr. M. (Monique) Maas, radioloog, Nederlands Kanker Instituut, Amsterdam, NVvR
- Prof. dr. C.A.M. (Corrie) Marijnen, radiotherapeut, Leids Universiteit Medisch Centrum, Leiden, NVRO
- Dr. M. (Martijn) Meijerink, interventieradioloog, Amsterdam UMC locatie VUmc, Amsterdam, NVvR (vanaf november 2018)
- Dr. L. (Leon) Moons, MDL-arts, UMC Utrecht, Utrecht, NVMDL
- Prof. dr. I.D. (Iris) Nagtegaal, patholoog, Radboud UMC, Nijmegen, NVvP
- Dr. P. (Petur) Snaebjornsson, patholoog, Nederlands Kanker Instituut, Amsterdam, NVvP
- Dr. H.M.W. (Henk) Verheul, internist-oncoloog, Radboudumc, Nijmegen, NIV/NVMO
- Prof. dr. C. (Kees) Verhoef, oncologisch chirurg, Erasmus MC, Rotterdam, NVvH
- Dr. M. (Marianne) de Vries, abdominaal radioloog, Erasmus MC, Rotterdam, NVvR (vanaf november 2018)
- Dr. H.L. (Erik) van Westreenen, chirurg, Isala Zwolle/ Isala Diaconessenhuis, Zwolle/Meppel, NVvH
Voormalig betrokken werkgroepleden
- Prof. dr. C.J.A. (Kees) Punt, medisch oncoloog, NIV/NVMO
- Prof. dr. J. (Jaap) Stoker, abdominaal radioloog, NVvR
- Dr. A.J. (Albert Jan) ten Tije, internist oncoloog, NIV/NVMO
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van Medisch Specialisten.
De werkgroep heeft bij aanvang van het richtlijnontwikkelingstraject geconstateerd dat sommige werkgroepleden betrokken zijn bij wetenschappelijk onderzoek dat wordt gefinancierd door overheid, onafhankelijke subsidieverstrekkers, of commerciële partijen (in het laatste geval: unrestricted scientific grants). Om te voorkomen dat indirecte belangen (waaronder reputatie en kennisvalorisatie) de richtlijnaanbevelingen onbedoeld zouden kunnen beïnvloeden, heeft de werkgroep besloten dat geen van de modules/aanbevelingen worden opgesteld door één werkgroeplid met dergelijke indirecte belangen. Tenminste één ander werkgroeplid met hetzelfde specialisme of tenminste één ander werkgroeplid met vergelijkbare inhoudelijke kennis van het betreffende onderwerp zijn verantwoordelijk voor de inhoud (vier-ogen-principe).
De werkgroep zag in de gemelde (on)betaalde nevenfuncties geen aannemelijke reden voor onbedoelde beïnvloeding door belangenverstrengeling ten aanzien van de onderwerpen die in de richtlijn aan bod komen.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Prof. Dr. P.J. (Pieter) Tanis
|
Gastrointestinaal en oncologisch chirurg |
Voorzitter Dutch Colorectal Cancer Group (onbetaald)
Bestuurslid Dutch Peritoneal Oncology Group (onbetaald)
Bestuurslid Dutch Colorectal Audit (onbetaald)
Medische adviesraad Lynch Polyposis vereniging (onbetaald)
Associate Editor Colorectal Disease (onbetaald)
Coordinerend auteur hoofdstuk tumoren van de dunne en dikke darm, leerboek Oncologie (onbetaald) |
PI van COLOPEC 1 en 2 trials gefinancierd door ZonMW en KWF.
Steering committee van de CAIRO6 studie gefinancierd door KWF en unrestricted scientific grant Roche.
PI van de BIOPEX 1 studie, gefinancierd door unrestricted scientific grant van LifeCell.
PI van de BIOPEX 2 studie gefinancierd door KWF.
|
Geen actie ondernomen.
Biopex 1 is gepubliceerd in 2013 (verjaard).
Overige subsidies zijn van ZonMW en KWF, onwaarschijnlijk dat dit een belang oplevert. Daarom geen actie ondernomen. |
|
Dr. H.L. (Erik) Van Westreenen
|
Gastrointestinaal en oncologisch chirurg |
Penningmeester werkgroep Coloproctologie (onbetaald) |
PI Limeric study (endoscopisch geassisteerde laparoscopische wigresectie van het colon).
Locale PI en mede aanvrager FORCE study (Zon-MW) (Randomisatie tussen best-supportive care of bekkenfysiotherapie na low-anterior resectie)
Locale PI TESAR study
Locale PI StarTrec study
Locale PI FIT trial |
Geen actie ondernomen.
Mede-aanvrager van ZonMW subsidie, onwaarschijnlijk dat dit een belang oplevert. Daarom geen actie ondernomen. |
|
Prof. dr. C.J.A. (Kees) Punt
|
Medisch oncoloog |
Voorzitter werkgroep medische oncologie, Dutch Colorectal Cancer Group (DCCG) (onbetaald).
Voorzitter Dutch Oncology Research Platform (onbetaald). |
Lid raad van advies SPKS
Unrestricted scientific grants van Roche en Amgen voor DCCG CAIRO5 studie.
Adviseur Nordic Pharma. |
Om mogelijk te maken dat geen van de modules/ aanbevelingen worden opgesteld door één werkgroeplid met indirecte belangen door sponsoring uit derde geldstroom van private instellingen, zijn extra werkgroepleden toegevoegd aan de werkgroep. |
|
Dr. M.E. (Marije) Hamaker
|
Klinisch geriater |
Geen |
Roche: lid van werkgroep e-learning colorectaal carcinoom (niet relevant voor de richtlijn)
Astra Zeneca: financiering van onderzoek over dialyse bij ouderen |
Geen actie ondernomen. |
|
Dr. L. (Leon) Moons
|
MDL-arts |
Consultant voor Boston Scientific (consultancy over specifieke apparatuur voor MDL-artsen, niet relevant voor de richtlijn) |
Voorzitter van T1 CRC werkgroep.
PI van een gerandomiseerde studie (piecemeal EMR vs. ESD), gefinancierd door KWF.
PI van een studie naar risicomodellen voor het voorspellen van lymfekliermetastasen en lokale recidieven van T1 CRCs, gefinancierd door de MLDS.
PI van een studie naar tumor seedings tijdens coloscopie, gefinancierd door de Sacha Swarttouw-Hijmans stichting. |
Om mogelijk te maken dat geen van de modules/ aanbevelingen worden opgesteld door één werkgroeplid met indirecte belangen door sponsoring uit derde geldstroom van private instellingen, zijn extra werkgroepleden toegevoegd aan de werkgroep. |
|
Prof. dr. C.A.M. (Corrie) Marijnen
|
Radiotherapeut / Afdelingshoofd radiotherapie LUMC |
Voorzitter wetenschapscommissie NVRO
Redactielid leerboek Oncologie |
Geen. |
Geen actie ondernomen. |
|
Dr. M.P.W. (Martijn) Intven
|
Radiotherapeut |
Lid redactieraad van het Nederlands tijdschrift voor oncologie |
Geen. |
Geen actie ondernomen. |
|
Prof. dr. I.D. (Iris) Nagtegaal
|
Patholoog / Detachering als Expert Pathologie t.b.v. het bevolkingsonderzoek darmkanker bij FSB |
Voorzitter PALGA (Nederlands Digitale Pathologie Archief) (vacatiegelden naar afdeling Pathologie van RadboudUMC)
Lid adviesraad KWF (onbetaald)
Voorzitter European Taskforce for synoptic reporting in pathology (onbetaald)
Voorzitter Nederlands TNM committee (onbetaald) |
Amgen 2014: Discordance in mutation statis is not an issue for molecular testing in CRC (80.000 euro) |
Geen van de modules/ aanbevelingen zijn opgesteld door één werkgroeplid met indirecte belangen door sponsoring uit derde geldstroom van private instellingen. |
|
Dr. P. (Petur) Snaebjornsson
|
Patholoog |
Bestuurslid Dutch Colorectal Cancer Group (onbetaald)
Lid Dutch peritoneal Oncology Group (onbetaald)
Tot en met 2017: Organisator van Dodo couperclub regio Noord-Holland (onbetaald). |
Betrokken bij COLOPEC trials en CAIRO6 trial. |
Geen actie ondernomen. |
|
Prof. dr. R.G.H. (Regina) Beets-Tan
|
Radioloog / Hoofd radiologie NKI/AVL |
Geen. |
Geen. |
Geen actie ondernomen. |
|
Dr. A.J. (Bert Jan) ten Tije |
Internist-oncoloog |
Geen. |
Geen. |
Geen actie ondernomen. |
|
Dr. Martijn Meijerink
|
Interventieradioloog, Amsterdam UMC locatie VUmc |
Voorzitter WCIR (wetenschapscommissie interventieradiologie), onbetaald.
Voortzitter SIO (Soc. Interv. Oncol.) Research Committee, onbetaald.
Raad van advies SPKS (stichting voor patiënten met kanker aan het spijsverteringskanaal), onbetaald.
Ambassadeur SBBvK en OZS, onbetaald |
Consultant Angiodynamics B.V. (vergoeding voor presentaties, workshops, proctorships) op het gebied van irreversibele electroporatie.
Research grants: Collision Trial (Medtronic) Diverse trials (Angiodynamics B.V.)
|
Om mogelijk te maken dat geen van de modules/ aanbevelingen worden opgesteld door één werkgroeplid met indirecte belangen door sponsoring uit derde geldstroom van private instellingen, zijn extra werkgroepleden toegevoegd aan de werkgroep. |
|
Dr. Marianne de Vries
|
Radioloog Erasmus MC Rotterdam |
Geen. |
Geen. |
Geen actie ondernomen. |
|
Dr. Monique Maas |
Radioloog |
Redactielid blad IMAGO (onkostenvergoeding) |
Geen. |
Geen actie ondernomen. |
|
Dr. Derk Jan de Groot
|
Internist-oncoloog Universitair Medisch Centrum Groningen |
Geen. |
Klinische studies: Ipsen (betaling aan het instituut) |
Geen actie ondernomen. |
|
C.M.J. (Christel) Gielen MSc.
|
Verpleegkundig specialist Coloncare MUMC |
Geen. |
Werkt mee aan de inclusie voor de ENCORE studie (energie voor het leven na colorectaalkanker). |
Geen actie ondernomen. |
|
S. Dokter (Simone) MSc. |
Verpleegkundig specialist MDL |
Geen. |
Geen. |
Geen actie ondernomen. |
|
Dr. C.J. (Corneline) Hoekstra
|
Nucleair geneeskundige |
Geen. |
Geen. |
Geen actie ondernomen. |
|
Prof. dr. C. (Kees) Verhoef
|
Oncologisch chirurg |
Wetenschappelijke adviesraad KWF (onbetaald).
Wetenschappelijk raad Livermetsurvey (onbetaald).
Voorzitter Nederlandse Vereniging voor Chirurgische Oncologie (onbetaald).
Lid Algemeen Bestuur Nederlandse Vereniging van Heelkunde (onbetaald).
Voorzitter "Dutch chapter E-AHPBA" (onbetaald).
Nederlands TNM comite (onbetaald).
Adviesraad IKNL (onbetaald).
Nederlandse wetenschappelijke Sarcoom Werkgroep (onbetaald).
Bestuur Dutch Hepatocellular Carcinoma Group (onbetaald).
Bestuur Familiehuis, Daniel den Hoed Kliniek (onbetaald). |
Geen. |
Geen actie ondernomen. |
|
Prof. dr. G.L. (Geerard) Beets
|
Chirurg / Afdelingshoofd AVL |
Medisch consultant bij Champalimaud Foundation, oncologisch ziekenhuis in Lissabon, Portugal (betaalde functie) |
Geen. |
Geen actie ondernomen. |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door het uitnodigen van de Stichting voor Patiënten met Kanker aan het Spijsverteringskanaal (SPKS) voor de invitational conference. Daarnaast hebben dr. L. Meerman en mw. A. van Heijst (Stomavereniging, Nederlandse Federatie van Kankerpatiëntenorganisaties, NFK) modules meegelezen en de werkgroep van feedback vanuit het patiëntenperspectief voorzien. De conceptrichtlijn is tevens ter commentaar voorgelegd aan SPKS en NFK. In verbrand met de zeer verslechterde gezondheidstoestand en het overlijden van mw A. van Heijst wordt vanaf maart 2020 feedback vanuit het patiëntperspectief gegeven door dr. L. Meerman en mw. M. v.d. Bosch-Scholts.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de herziene richtlijnmodules en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten. De werkgroep heeft geen interne kwaliteitsindicatoren ontwikkeld, omdat interne en externe kwaliteitsindicatoren al ontwikkeld worden binnen de Dutch Colorectal Audit (DCRA), de clinical audit board betreffend colorectaal carcinoom onder de Dutch Institute for Clinical Auditing (DICA).
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseurs de knelpunten. De werkgroep beoordeelde de aanbevelingen uit de eerdere richtlijn (NVRO, 2014) op noodzaak tot revisie. De werkgroep stelde vervolgens een long list met knelpunten op en prioriteerde de knelpunten op basis van: (1) klinische relevantie, (2) de beschikbaarheid van nieuwe evidence, (3) en de te verwachten impact op de kwaliteit van zorg, patiëntveiligheid en (macro)kosten. Tevens zijn er knelpunten aangedragen door verschillende partijen via een invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en werkgroepleden concept-uitgangsvragen opgesteld. Gedurende het richtlijnherzieningstraject heeft de werkgroep de definitieve uitgangsvragen in een hernieuwd raamwerk (de inhoudsopgave, zie ook de algemene inleiding) van de richtlijn vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep baseerde de keuze voor uitkomstmaten mede op basis van de “core outcome set” gepubliceerd door Zerillo (2017). De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden. Hiervoor sloot de werkgroep zich, waar mogelijk, aan bij de grenzen voor klinische besluitvorming volgens de PASKWIL criteria uit 2016. Wanneer er geen grenzen voor klinische besluitvorming conform de PASKWIL criteria geformuleerd konden worden (bijvoorbeeld bij non-inferioriteitsvraagstukken) werden de standaard GRADE grenzen gehanteerd, tenzij anders vermeld.
Strategie voor zoeken en selecteren van literatuur
De werkgroep raadpleegde voor de afzonderlijke uitgangsvragen reeds gepubliceerde systematische reviews (SRs). SRs kwamen in aanmerking indien: i) systematisch was gezocht in één of meerdere databases; ii) transparante in- en exclusiecriteria zijn toegepast en iii) idealiter de kwaliteit van de geïncludeerde literatuur was beoordeeld. De voor de uitgangsvragen relevante internationale richtlijnen en consensusdocumenten werden eveneens geraadpleegd. Overige literatuur, waar niet systematisch naar werd gezocht, is als bewijsvoering in de overwegingen opgenomen.
Relevante beschikbare populatiegegevens uit Nederland werden gebruikt voor het bepalen van knelpunten, praktijkvariatie en externe validiteit van internationale richtlijnen en gepubliceerde literatuur.
Kwaliteitsbeoordeling individuele studies
De (risk of bias) kwaliteitsbeoordelingen van de individuele studies uit de gebruikte SRs werden gebruikt, tenzij deze afwezig waren of onbruikbaar waren voor het beoordelen van de kracht van het wetenschappelijke bewijs. Indien afwezig of onbruikbaar werd aangenomen dat er een risico op bias aanwezig zou kunnen zijn. In enkele gevallen, wanneer studies informatie verschaften over de cruciale uitkomstma(a)t(en), werd er een nieuwe kwaliteitsbeoordeling van individuele studies uitgevoerd.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van de geselecteerde SRs werden weergegeven in ‘Summary of Findings’ tabellen. De belangrijkste bevindingen uit de literatuur werden kort beschreven onder “Samenvatting literatuur” (kopjes “Samenvatting van internationale richtlijnen en consensusdocumenten” en “Samenvatting van systematische reviews en meta-analyses”) en onder “Overwegingen”. Bestaande meta-analyses uit de gebruikte systematische reviews werden beschreven. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013). Het resultaat van de gradering van het wetenschappelijk bewijs werd opgenomen in de ‘Summary of Findings’ tabellen.
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk* |
|
|
Laag |
|
|
Zeer laag |
|
*in 2017 heeft het Dutch GRADE Network bepaalt dat de voorkeursformulering voor de op een na hoogste gradering ‘redelijk’ is in plaats van ‘matig’.
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008), en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek (te vinden in de ‘Summary of Findings’ tabellen). De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de cruciale uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje Overwegingen.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje Overwegingen.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Aanbevelingen uit de richtlijn Colorectaal carcinoom 2014
De werkgroep beoordeelde alle aanbevelingen in de richtlijn Colorectaal carcinoom uit 2014 op geldigheid. De werkgroep heeft aanbevelingen gehandhaafd die als nog steeds geldig werden beschouwd. De werkgroep heeft deze aanbevelingen tekstueel opgefrist met als doel de implementeerbaarheid te vergroten. De aanbevelingen zijn niet inhoudelijk veranderd. De werkgroep heeft in het modulair onderhoudsschema vastgesteld wanneer herziening van deze modules gepland is. De werkgroep verwacht dat eind 2020 de gehele richtlijn is herzien.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van Zorg.
Indicatorontwikkeling
Er werden geen interne kwaliteitsindicatoren ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken. De werkgroep conformeert zich aan de SONCOS normen en de DICA-DCRA indicatoren.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de Kennislacunes beschreven (onder aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en patiëntorganisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers, M. C., Kho, M. E., Browman, G. P., Burgers, J. S., Cluzeau, F., Feder, G., ... & Littlejohns, P. (2010). AGREE II: advancing guideline development, reporting and evaluation in health care. Canadian Medical Association Journal, 182(18), E839-E842.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van Medisch Specialisten.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann, H. J., Oxman, A. D., Brozek, J., Glasziou, P., Jaeschke, R., Vist, G. E., ... & Bossuyt, P. (2008). Rating Quality of Evidence and Strength of Recommendations: GRADE: Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ: British Medical Journal, 336(7653), 1106.
Wessels, M., Hielkema, L., & van der Weijden, T. (2016). How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. Journal of the Medical Library Association: JMLA, 104(4), 320.
Zerillo JA, Schouwenburg MG, van Bommel ACM, Stowell C, Lippa J, Bauer D, Berger AM, Boland G, Borras JM, Buss MK, Cima R, Van Cutsem E, van Duyn EB, Finlayson SRG, Hung-Chun Cheng S, Langelotz C, Lloyd J, Lynch AC, Mamon HJ, McAllister PK, Minsky BD, Ngeow J, Abu Hassan MR, Ryan K, Shankaran V, Upton MP, Zalcberg J, van de Velde CJ, Tollenaar R; Colorectal Cancer Working Group of the International Consortium for Health Outcomes Measurement (ICHOM). An International Collaborative Standardizing a Comprehensive Patient-Centered Outcomes Measurement Set for Colorectal Cancer. JAMA Oncol. 2017 May 1;3(5):686-694. doi: 10.1001/jamaoncol.2017.0417. PubMed PMID: 28384684.

