Orale corticosteroïden
Uitgangsvraag
Wat is de effectiviteit en veiligheid van orale corticosteroïden bij de behandeling van patiënten met chronische spontane urticaria?
Aanbeveling
Bij exacerbaties van chronische spontane urticaria kunnen kortdurend orale corticosteroïden worden ingezet met een mogelijk goed klinisch effect. Behandeling met orale corticosteroiden is geen aparte stap in het voorgestelde stepped care model, maar wordt aanbevolen als aanvulling op alle stappen.
Bij resistente chronische spontane urticaria ondanks (opgedoseerde) 2de generatie antihistaminica kunnen kortdurend orale corticosteroïden worden ingezet, waarbij op basis van de literatuur in sommige gevallen lang aanhoudende remissie werd bereikt.
Het wordt aanbevolen om orale corticosteroïden in principe alleen kortdurend (maximaal drie weken) te gebruiken bij de behandeling van chronische spontane urticaria. De aangewezen dosering is 20-50mg prednison (of een equivalent hiervan) per dag, op geleide van de klachten.
Overwegingen
Volgens de internationale richtlijn van Zuberbier et al. (2014) zijn, indien orale corticosteroïden worden gebruikt, doses tussen 20-50 mg / dag benodigd om de klachten te onderdrukken. Echter, dose finding studies ontbreken en dit advies is gebaseerd op expert opinion. Langdurig gebruik is echter gezien het bijwerkingenprofiel van prednison ongewenst en het is te verwachten dat bij CSU na het staken van de prednison de klachten zullen terugkeren (Zuberbier et al. 2014).
Augey et al. (2008) hebben in een prospectieve studie het effect bestudeerd van het stoppen met orale corticosteroïden. Daarnaast onderzochten zij het vermogen om de ziekte onder controle te houden zonder corticosteroïden, bij 17 patiënten met verschillende vormen van CU, die 3-30 dagen per maand orale corticosteroïden gebruikten. 47% had een kortdurende verslechtering van symptomen na het stoppen van orale corticosteroïden, 35% had een complete remissie bij 12 maanden en 47% had een partiële remissie met alleen behandeling met een antihistaminicum.
Meerdere studies toonden aan dat de kwaddel bij priktesten met histamine minder groot is na lokaal gebruik van clobetasolproprionaatzalf 1-2dd (Dunsky et al., 1979; Narasimha, Srinivas & Mathew, 2005). Barlow et al. (1995) toonden aan dat de urtica bij het provoceren van een vertraagde druk urticaria significant kleiner was na het aanbrengen van clobetasolpropionaatzalf 0.05% ten opzichte van het vehiculum. Histologisch werd er een afname gezien in het aantal mestcellen na het smeren van clobetasolproprionaatzalf. Deze afname was niet significant (P=0,059).
Deze gegevens pleiten vóór een positief effect van corticosteroïden op het ontwikkelen van urticae.
Veiligheid
Er zijn tot op heden geen langdurige studies uitgevoerd met monotherapie corticosteroïden al dan niet in combinatie met een antihistaminicum bij patiënten met CSU. Het bijwerkingenprofiel maakt langdurig gebruik van orale corticosteroïden ook onwenselijk.
Vanuit de literatuur is slechts bewijs voor kortdurend gebruik van orale corticosteroïden bij patiënten met therapieresistente chronische urticaria; de duur van de behandeling in de studies varieert echter. Op basis de behandelduur in deze studies en expert opinion zou men een behandelduur van maximaal drie weken kunnen aanhouden om de symptomen te verminderen.
Gegevens over de veiligheid van corticosteroïden zijn in meerdere dermatologische richtlijnen beschreven. De voor- en nadelen van gebruik moeten worden afgewogen op individueel niveau. Bijwerkingen van orale corticosteroïden zijn bekend en worden in de beschikbare dermatologische richtlijnen besproken.
Kosten therapie
De kosten van orale corticosteroïden zijn laag, zeker in vergelijking met geregistreerde middelen als ciclosporine en omalizumab. Een tablet prednisolon kost circa 53 eurocent per stuk. Men moet hierbij echter aantekenen dat door langdurig gebruik de kosten kunnen stijgen door de vaak optredende bijwerkingen zoals bij bijvoorbeeld slecht gereguleerde diabetes of osteoporose.
Afweging gewenste / ongewenste effecten
Hoewel geen gerandomiseerde dubbel blinde prospectieve studies zijn gedaan naar de effectiviteit van orale corticosteroïden bij patiënten met CSU, zijn er multipele kleinere studies uitgevoerd die duiden op effectiviteit van deze middelen op de klachten van patiënten. Orale corticosteroïden hebben een bekend bijwerkingenprofiel, maar kunnen een gunstig effect hebben om de klachten kortdurend te onderdrukken.
Behandeling met orale corticosteroïden kan van belang zijn bij patiënten met acute exacerbaties.
Patiëntenperspectief
Corticosteroïden werken snel en zijn over het algemeen effectief bij het doorbreken van klachten van spontane chronische urticaria. Het kan patiënten met een grote ziektelast de gewenste verbetering van kwaliteit van leven geven.
Organisatie van zorg
Het kortdurend gebruik van corticosteroïden kan worden opgestart door zowel dermatoloog als huisarts. Beide hebben uitgebreide ervaring bij het gebruik van deze middelen en bekend met de potentiële bijwerkingen / contra-indicaties.
Onderbouwing
Achtergrond
Corticosteroïden worden vaak voorgeschreven aan patiënten met chronische urticaria. Orale corticosteroïden zijn sinds lange tijd verkrijgbaar en voldoen niet aan de strenge eisen voor de huidige registratie. Hoewel het gebruik van deze middelen wereldwijd beschouwd wordt als een effectieve therapie bij chronische urticaria, is de wetenschappelijke onderbouwing mager.
Conclusies / Summary of Findings
|
Niveau 3 |
Er zijn aanwijzingen dat bij de behandeling van antihistaminica resistente chronische spontane urticaria een korte kuur met orale corticosteroïden effectief kan zijn. Grote gerandomiseerde klinische trials ontbreken echter. |
Samenvatting literatuur
Beschrijving studies
Slechts één retrospectieve ongecontroleerde studie onderzocht de effectiviteit van orale corticosteroïden bij patiënten met chronische urticaria (Asero & Tedeschi, 2010). Van de 750 patiënten die werden behandeld met 10mg van het antihistaminicum cetirizine reageerden 90 patiënten onvoldoende op deze therapie. Van deze 90 patiënten waren vier patiënten lost to follow-up. Een reden hiervoor werd niet nader genoemd. Gedurende tien dagen werden de therapieresistente 86 patiënten behandeld met prednison in een afbouwschema, beginnend met 25mg / dag gedurende drie dagen, dan 12,5mg / dag gedurende drie dagen en 6,25mg / dag gedurende vier dagen waarna stop van de behandeling. Gedurende de prednisonkuur bleven de patiënten hun antihistaminicum gebruiken. Patiënten met recidief na staken van de eerste prednison kuur, kregen nog een tweede kuur aangeboden bij hun controle bezoek na vier weken.
Paradis et al. (1996) gaven patiënten met CIU in een dubbelblinde gerandomiseerde studie zeven dagen 32mg methylprednison waarna er via de skin chamber techniek de hoeveelheid vrijgekomen histamine en histamine-releasing factor werd bestudeerd. Alleen de histamine-releasing factor toonde een significante daling. Tijdens deze studie hielden patiënten echter ook een urticaria activiteit score bij waarbij een significante daling werd gezien van de score na zeven dagen prednison ten opzichte van de placebo groep. Veel patiënten bemerkte al na 48 uur verbetering. Twee van de tien patiënten ondervonden geen enkele verbetering bij gebruik van methylprednisolon.
Er werd echter niet gekeken naar de recidiefkans na het staken van de therapie. De studie werd namelijk opgezet met een ander doel dan het aantonen van effectiviteit van orale corticosteroïden bij chronisch spontane urticaria.
In de studie van Grattan et al. (2003) werden zeven CSU patiënten gevraagd om een UAS bij te houden. Op dagtweevan de studie startten de onderzoekers met loratadine en op dag 12 van deze 14-daagse studie startten zij met prednisolon 0,5mg / kg, tot maximaal 40 mg / dd. Er werd hierbij een significante daling van de UAS gezien bij het gebruik van alleen loratadine maar ook een verdere daling na toevoegen van drie dagen prednison. In deze studie werden ook de effecten van prednisolon op de hoeveelheid basofielen en eosinofielen granulocyten en lymfocyten in chronische urticaria patiënten.
Ook in deze studie werd niet gekeken naar het percentage recidieven na staken van de therapie.
Kwaliteit van bewijs
De studie van Asero & Tedeschi (2010) is een retrospectieve ongecontroleerde studie bij patiënten met therapieresistente chronische urticaria (>17 jaar). Patiënten met fysische urticaria werden geëxcludeerd. Van de 90 patiënten zijn vier patiënten lost to follow-up, waar geen verklaring voor wordt gegeven. De behandeling met orale corticosteroïden werd als succesvol gezien bij geen of minimale urticaria gedurende vier weken na het stoppen met de corticosteroïden, met alleen een eenmalige dagelijkse dosis van een niet sederend antihistaminicum.
De uitkomstmaat voor ‘complete respons’ werd subjectief bepaald, waardoor een bias kan zijn veroorzaakt. In deze retrospectieve studie kon de objectieve of subjectieve ziekteactiviteit niet worden vastgesteld. De ernst van de aandoening bij deze patiënten kon dus niet worden geobjectiveerd.
Patiënten werden geïncludeerd indien zij minimaal zes weken klachten hadden. Er is echter niet gespecificeerd wat de gemiddelde duur van klachten was bij de patiëntengroep. De baseline karakteristieken van de patiënten werden niet genoemd, waardoor de groep niet duidelijk werd gedefinieerd, wat de wetenschappelijke waarde van de studie beperkt. Het is niet onmogelijk dat de klachten verbeterden, niet door het gebruik van orale steroïden, maar door het natuurlijk beloop en het gebruik van het antihistaminicum.
De relatief kleine studies van Paradis et al. (1996) en Grattan et al. (2003) waren niet primair opgezet om de effectiviteit van prednison bij CIU aan te tonen. Een bias was niet uit te sluiten. In beide studies was een activiteitsscore gebruikt om het effect van orale corticosteroïden te evalueren, wat in de studie van Asero & Tedeschi (2010) ontbreekt.
Gewenste effecten
Van de 86 patiënten in de studie van Asero & Tedeschi (2010) bereikten 40 patiënten complete remissie. Complete remissie is hierbij omschreven als geen of minimale urticaria vier weken na het stoppen van de behandeling met prednison met alleen een eenmalige dosis van een tweede generatie antihistaminicum. 35 van de 86 patiënten hadden een goede respons op behandeling met prednison maar kregen een terugval na het afbouwen of stoppen van de prednison. Aan deze 35 patiënten werd een tweede prednisonkuur aangeboden. 23 van deze patiënten gebruikte de prednison, waarna alsnog acht patiënten een complete remissie toonden.
Ongewenste effecten
De bijwerkingen van orale corticosteroïden in de behandeling van chronische urticaria werden niet in de studies van Asero & Tedeschi (2010), Grattan et al. (2003) en Paradis et al. (1996) beschreven.
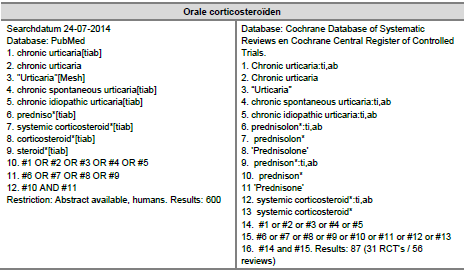
Zoeken en selecteren
Om de uitgangsvraag te beantwoorden is een systematische search verricht met behulp van de databases PubMed en Cochrane (Cochrane Database of Systematic Reviews en Cochrane Central Register of Controlled Trials). De searchstrategie is bijgevoegd in de Zoekverantwoording. De search leverde 600 artikelen op uit PubMed en 87 artikelen uit Cochrane. Hiervan zijn uiteindelijktweestudies geïncludeerd die de effectiviteit en veiligheid van orale corticosteroïden bij chronische urticaria hebben onderzocht. Na het lezen van de full-teksten is één studie alsnog geëxcludeerd op basis van de kwaliteit van het artikel. Hierdoor bleef er slechts één retrospectieve ongecontroleerde studie over (Asero & Tedeschi, 2010). Ook zijn er uiteindelijk twee studies geïncludeerd waarbij de effectiviteit van orale corticosteroïden niet het primaire onderzoeksdoel was, maar deze wel wordt beschreven (Grattan et al., 2003; Paradis et al., 1996).
De evidencetabellen hiervan kunt u terugvinden onder Evidence tabellen. Voor de uitgangsvraag is tevens kennis genomen van de internationale richtlijn van Zuberbier et al. uit 2014.
Referenties
- Asero R, & Tedeschi A. 2010. Usefulness of a short course of oral prednisone in antihistamine-resistant chronic urticaria: a retrospective analysis. J. Investig. Allergol. Clin. Immunol. 20 (5): 386-390.
- Augey F, Guillot-Pouget I, Gunera-Saad N, Berard F, and Nicolas JF. 2008. [Impact of corticosteroid withdrawal in chronic urticaria: a prospective study of 17 patients]. Ann. Dermatol. Venereol. 135 (1): 21-25.
- Barlow RJ, Macdonald DM, Black AK, and Greaves MW. 1995. The effects of topical corticosteroids on delayed pressure urticaria. Arch. Dermatol. Res. 287 (3-4): 285-288.
- Dunsky EH, Zweiman B, Fischler E, and Levy DA. 1979. Early effects of corticosteroids on basophils, leukocyte histamine, and tissue histamine. J. Allergy Clin. Immunol. 63 (6): 426-432.
- Grattan CE, Dawn G, Gibbs S, and Francis DM. 2003. Blood basophil numbers in chronic ordinary urticaria and healthy controls: diurnal variation, influence of loratadine and prednisolone and relationship to disease activity. Clin. Exp. Allergy 33 (3): 337-341.
- Kim S, Baek S, Shin B, Yoon SY, Park SY, Lee T, Lee YS, Bae YJ, Kwon HS, Cho YS, Moon HB, and Kim TB. 2013. Influence of initial treatment modality on long-term control of chronic idiopathic urticaria. PLoS. One. 8 (7): e69345.
- Narasimha SK, Srinivas CR, and Mathew AC. 2005. Effect of topical corticosteroid application frequency on histamine-induced wheals. Int. J. Dermatol. 44 (5): 425-427.
- Paradis L, Lavoie A, Brunet C, Bedard PM, and Hebert J. 1996. Effects of systemic corticosteroids on cutaneous histamine secretion and histamine-releasing factor in patients with chronic idiopathic urticaria. Clin. Exp. Allergy 26 (7): 815-820.
- Zuberbier T, Aberer W, Asero R, Bindslev-Jensen C, Brzoza Z, Canonica GW, Church MK, Ensina LF, Gimenez-Arnau A, Godse K, Goncalo M, Grattan C, Hebert J, Hide M, Kaplan A, Kapp A, Abdul Latiff AH, Mathelier-Fusade P, Metz M, Nast A, Saini SS, Sanchez-Borges M, Schmid-Grendelmeier P, Simons FE, Staubach P, Sussman G, Toubi E, Vena GA, Wedi B, Zhu XJ, and Maurer M. 2014. The EAACI / GA2LEN / EDF / WAO Guideline for the definition, classification, diagnosis, and management of urticaria: the 2013 revision and update. Allergy 69(7): 868887.
Evidence tabellen
|
Auteur, jaartal |
Mate van bewijs |
Studie opzet |
N= |
Patiëntenpopulatie |
Interventie (incl. duur) |
Controle (incl. duur) |
Uitkomstmaten |
Follow-up duur |
Resultaten |
Overige opmerkingen |
|
Asero et al. 2010 |
C |
Retrospectief on- gecontroleerd |
86 |
Ptn met CU . Fysische urticaria uitgesloten
16 mannen/ 74 vrouwen Leeftijd 22-85 jaar, gemiddelde 51 jaar. |
Prednison 25mg/dag op dag 1,2 en 3; 12.5mg/dag op dag 4,5 en 6; 6.25 mg/dag op dag 7, 8,9,10. Duur 10 dagen
Co-medicatie: Cetirizine 10mg, loratadine 10mg, ebastine 10mg, desloratadine 5mg of levocetirizine 5mg dagelijks. |
n.v.t. |
Effectiviteit: Complete remissie (geen of minimale urticaria 4 wkn na stop prednison met alleen nog standaard dosering ns H1-AH) |
4 wkn (na stop prednison) |
In 40/86 (47%) ptn complete remissie 4 wkn na stop prednison.
35 ptn hadden goede respons maar vielen terug bij afbouwen dosis of na stop therapie. 9% resulteerde in complete remissie na tweede kuur prednison. |
Uitkomstmaat niet-valide en subjectief bepaald.
Alleen ptn niet reagerend op standaard dosering ns H1-AH.
4 ptn lost to follow-up.
Studie uitgevoerd in een enkele perifere kliniek. |
|
Paradis et al. 1996 |
|
Prospectief, dubbelblind, gerandomisee rd |
19 |
14 /5 man met CSU zonder systemische steroïden gedurende 1 maand, klassieke H1 of H2 blokkers gedurende 72h en astemizole voor 6 wkn.
leeftijd mediaan 43 |
Verkrijgen materiaal voor histamine secretie en histamine-releasing factor na m ethylprednisolon 32mg 1 dd of placebo gedurende 7 dagen |
n.v.t. |
Symptoomscore
Hoeveelheid histamin-releasing factor (HRF) en histamine secretie in de huid |
Geen |
Significante daling symptoomscore na 7 dgn prednisolon. Onveranderde hoeveelheid histamine in placebo vs prednisolon; significante verlaging HRF in prednisolon groep |
Symptoomscore niet gevalideerd
Studie niet gericht op bepaling effectiviteit systemisch corticosteroïden maar op histamine en HRF in de huid bij CSU ptn.
Lage ptn-aantallen |
|
Auteur, jaartal |
Mate van bewijs |
Studie opzet |
N= |
Patiëntenpopulatie |
Interventie (incl. duur) |
Controle (incl. duur) |
Uitkomstmaten |
Follow-up duur |
Resultaten |
Overige opmerkingen |
|
Grattan et al, 2003 |
|
Prospectief, gecontroleerd e, open studie |
17 |
CU ptn: 5 vrouw, 2 man, mediaan 35 jaar;
|
Antihistaminica gestaakt 7 dgn voor start studie, start loratadine van dag 2 tot 14; start prednisolon 0.6mg/kg max 40mg 1dd dag 12 tm 14.
Duur studie: 14 dagen |
10 gezonde controle (6 vrouw, 4 man, mediaan 39 jaar) bestaande uit medewerker s ziekenhuis |
Ptn hielden een dagelijkse UAS bij en ondergingen op dag dat 1, 8 en 14 meerdere venapuncties ter bepaling van de variatie van basofielen aantallen in het bloed over de dag en onder invloed van de geneesmiddelen.
UAS score ASST BHRA Manual basophilcount |
Geen |
Significante verbetering van UAS na inname loratadine en verdere verbetering na inname prednisolon. Basofielen in bloed bij CU ptn in baseline al verlaagd, maar significante stijging hiervan na gebruik van prednisolon. Negatieve correlatie tussen UAS en aantallen circulerende basofielen. |
Studie niet primair gericht op bepaling effectiviteit systemisch corticosteroïden
Lage ptn-aantallen |
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 21-12-2015
Beoordeeld op geldigheid : 03-12-2015
Algemene gegevens
Deelnemende verenigingen/instanties:
Nederlandse Vereniging voor Allergologie (NVvA)
Nederlands Huisartsen Genootschap (NHG)
Nederlandse Vereniging voor Kindergeneeskunde (NVK) - Huidpatiënten Nederland (HPN).
Financiering
Deze richtlijn is tot stand gekomen met financiële steun vanuit het SKMS-programma
Deze richtlijn is geautoriseerd door (beoogd):
Nederlandse Vereniging voor Allergologie (NVvA)
Nederlandse Vereniging voor Kindergeneeskunde (NVK)
Huidpatiënten Nederland (HPN)
Zorgverzekeraars Nederland (ZN)
Nefarma.
Aanleiding
Urticaria wordt gekenmerkt door het plotseling optreden van urticae (kwaddels), angio-oedeem of beide. Bij continue of terugkerende klachten van urticae en / of angio-oedeem gedurende meer dan zes weken wordt er gesproken van chronische urticaria. Chronische urticaria kan een zeer belastende aandoening zijn. Het is een huidziekte die resulteert in rode jeukende, soms verheven kwaddels (urticae) op de huid van verschillende omvang en vorm, meestal gepaard gaand met heftige jeuk. Ook kan er sprake zijn van diepe zwellingen (angio-oedeem). Patiënten met chronische urticaria kunnen vele kwaddels ontwikkelen en elke dag klachten hebben. Het kan vele jaren duren en kan grote invloed hebben op de kwaliteit van leven, zowel lichamelijk als emotioneel, alsook voor diens omgeving. De ziektelast van deze aandoening kan aanzienlijk zijn. Deze richtlijn bespreekt de huidige stand van zaken omtrent de nomenclatuur, bepaling van de ziektelast van chronische urticaria en de behandeling van chronische spontane urticaria.
Doel en doelgroep
Doel
Deze richtlijn is een document met aanbevelingen ter ondersteuning van de dagelijkse praktijkvoering en dient als leidraad voor de dagelijkse praktijk om zo de kwaliteit van de zorg voor alle patiënten met chronische urticaria te bevorderen. De richtlijn berust op de resultaten van wetenschappelijk onderzoek (‘evidence- based’) en aansluitende meningsvorming gericht op het vaststellen van goed medisch handelen. Deze richtlijn en de daarvan afgeleide documenten geven aanbevelingen over de nomenclatuur, bepaling van de ziektelast en behandeling van chronische spontane urticaria. Het doel van deze richtlijn is meer uniformiteit wat betreft laatstgenoemde aspecten te creëren, waardoor een betere afstemming, begeleiding en follow-up van patiënten door zorgaanbieders wordt bereikt. De ontwikkeling van deze richtlijn zal gefaseerd gelopen; in eerste instantie zullen alleen de nomenclatuur, de vragenlijsten omtrent kwaliteit van leven en ziekteactiviteit en de behandeling van chronische spontane urticaria aan bod komen.
Doelgroep
De doelgroep wordt gevormd door alle zorgaanbieders die werkzaam zijn op het gebied van chronische urticaria of betrokken zijn bij de behandeling van patiënten met chronische spontane urticaria. Dit betreft zowel de medische, paramedische als verpleegkundige beroepsgroepen.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn werd in 2014 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die met patiënten met chronische urticaria te maken hebben. Deelnemende verenigingen in de werkgroep zijn de Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV), de Nederlandse Vereniging voor Allergologie (NVvA), de Nederlandse Vereniging voor Kindergeneeskunde (NVK), het Nederlands Huisartsen Genootschap (NHG) en Huidpatiënten Nederland (HPN).
|
Werkgroepleden |
Vereniging |
|
Dr. A.C. Knulst (voorzitter) |
NVDV |
|
Dr. C. Nieuwhof |
NVvA |
|
Drs. M. Stadermann |
NVK |
|
Dr. R.A. Tupker |
NVDV |
|
Dr. M.B.A. van Doorn |
NVDV |
|
Drs. S.M. Franken |
NVDV |
|
Mevr. F. Das |
HPN |
|
Ds. W. Poldervaart |
HPN |
|
Drs. C. de Vries |
NHG |
|
Drs. M. van den Elzen |
Arts-onderzoeker UMCU |
|
Drs. E.J. van Zuuren |
NVDV |
|
Dr. J.J.E. van Everdingen |
Directeur NVDV |
|
Drs. M.C. Urgert (t / m half januari 2015) |
Arts-onderzoeker NVDV (secretariaat) |
|
Drs. W.R. Veldkamp (vanaf half januari 2015) |
Arts-onderzoeker NVDV (secretariaat) |
|
Drs. G.E. van der Kraaij (vanaf half maart 2015) |
Arts-onderzoeker NVDV (secretariaat) |
Inbreng patiëntenperspectief
Tijdens het vaststellen van de uitkomstmaten en het graderen hiervan volgens GRADE was er een patiënt aanwezig. Deze heeft ook actief bijgedragen tijdens de pressurecooker, met als doel het formuleren van de aanbevelingen.
Methode ontwikkeling
Evidence based
Implementatie
Bij het opstellen van deze richtlijn is veel aandacht besteed aan de implementatie en de praktische uitvoerbaarheid, effectiviteit, nut en noodzaak. De richtlijn wordt via het web verspreid onder alle relevante beroepsgroepen en ziekenhuizen en er zal in verschillende specifieke vaktijdschriften aandacht worden besteed aan de richtlijn. Tevens zal een samenvatting en patiëntenversie worden gemaakt. De voorlichtingsfolder van de NVDV zal worden afgestemd op de richtlijn.
Werkwijze
De werkgroep startte in 2014. In de voorbereidingsfase werd een ‘stakeholdersbijeenkomst’ georganiseerd. Hiervoor werden behalve de bovengenoemde partijen ook Zorgverzekeraars Nederland (ZN) en Nefarma uitgenodigd. Tijdens deze bijeenkomst werden de door de werkgroep opgestelde uitgangsvragen besproken en nader geëxpliceerd. Voor de ontwikkeling van deze richtlijn is gebruik gemaakt van zowel de EBRO-criteria als de GRADE-methode. Gekozen is om de therapeutische uitgangsvragen ciclosporine en omalizumab uit te werken volgens de GRADEmethode. Bij de GRADE-methode wordt wetenschappelijk bewijs beoordeeld aan de hand van uitkomstmaten. GRADE veronderstelt dat de werkgroep in het beginstadium van de richtlijnontwikkeling uitkomstmaten vaststelt. Een volledig uitleg over de GRADE-methode valt buiten het bestek van deze richtlijn, zie hiervoor het ‘GRADE handbook’ (Schünemann et al., 2013). Voor de twee uitgangsvragen die volgens GRADE zijn uitgewerkt, zijn tijdens de invitational conference patiënt-relevante uitkomstmaten bepaald en vervolgens ingedeeld in kritieke, belangrijke en minder belangrijke uitkomstmaten. De gekozen uitkomstmaten zijn als volgt:
- Verbetering ziekteactiviteit in vergelijking tot de baseline (cruciaal)
- Verbetering kwaliteit van leven in vergelijking tot de baseline (cruciaal)
- Proportie patiënten met bijwerkingen (cruciaal)
- Proportie patiënten met complete respons (belangrijk)
- Proportie patiënten met een partiële respons (belangrijk)
- Proportie angio-oedeem vrije dagen (belangrijk)
- Proportie patiënten met remissie binnen 1 maand (van beperkt belang).
Wetenschappelijke onderbouwing
Per uitgangsvraag werd een systematische search verricht in de databases PubMed, de Cochrane Database of Systematic Reviews en Cochrane Central Register of Controlled Trials), tenzij anders aangegeven. Ook werden relevante nationale en internationale richtlijnen aangaande chronische urticaria geraadpleegd, met name de recente internationale richtlijn ‘EAACI / GA2LEN / EDF / WAO guideline on urticaria, 2014’, ontwikkeld volgens AGREE methode, en de Amerikaanse richtlijn ‘The diagnosis and management of acute and chronic urticaria: 2014 update’ (Bernstein et al., 2014; Zuberbier et al., 2014). De zoekstrategie en resultaten van de searches zijn terug te vinden onder Zoekverantwoording en Evidencetabellen.
De volgende inclusie / exclusiecriteria zijn gebruikt, tenzij anders aangegeven:
|
Inclusiecriteria: |
Exclusiecriteria: |
|
Chronische spontane / idiopathische urticaria |
Acute urticaria |
|
Alle leeftijden |
Andere vormen van chronische urticaria |
|
Behandeling met het betreffende geneesmiddel |
Narrative reviews |
|
|
Case series / observationele studies met minder dan vijf patiënten |
|
|
Studies in andere taal dan Engels |
|
|
Studies met onvoldoende informatie over effectiviteit en / of veiligheid |
|
|
In vitro onderzoek |
|
|
Dubbele publicaties |
|
|
Onderzoek bij dieren. |
Na selectie van de literatuur bleven artikelen over die als onderbouwing bij de verschillende conclusies staan vermeld. De werkgroepleden beoordeelden de kwaliteit en inhoud ervan. Vervolgens schreven de werkgroepleden een paragraaf of module voor de conceptrichtlijn, waarin de beoordeelde literatuur werd verwerkt.
Bij de uitwerking van de uitgangsvragen volgens de GRADE-methode zijn de stappen beschreven in het ‘GRADE handbook’ nauwkeurig gevolgd (Schünemann et al. 2013). Tevens is gebruik gemaakt van ‘the Cochrane Handbook for Systematic Reviews of Intervention’ voor het uitwerken van de uitgangsvragen en voor het verrichten van de meta-analyses (Higgins and Green 2011).
Elke module van de richtlijn is volgens een vast stramien opgebouwd, dat onderstaand is weergegeven. Een van de doelen is om een richtlijn zo transparant mogelijk te laten zijn, zodat elke gebruiker kan zien op welke literatuur en overwegingen bepaalde aanbevelingen zijn gebaseerd.
Uitgangsvraag
Een uitgangsvraag is een klinisch relevante vraag waarop tijdens de richtlijnontwikkeling een antwoord wordt geformuleerd.
Inleiding
Een korte introductie op de achtergrond van de uitgangsvraag.
Wetenschappelijke onderbouwing
Per uitgangsvraag is beknopt de zoekstrategie en de uitkomst hiervan beschreven. Meer gedetailleerde informatie over de zoekstrategie is beschreven in de Zoekverantwoording.
Samenvatting van de literatuur
De antwoorden op de uitgangsvragen zijn voor zover mogelijk gebaseerd op gepubliceerd wetenschappelijk onderzoek. De geselecteerde artikelen zijn door de schrijvende werkgroepleden beoordeeld op kwaliteit van het onderzoek en gegradeerd naar mate van bewijs, waarbij gebruik gemaakt is van de GRADE-methode en van de EBRO-methode. Voor de indeling van methodologische kwaliteit van studies volgens EBRO en GRADE zie tabel 1 en 4. Beschrijving en beschouwing van de gepubliceerde artikelen zijn indien van toepassing te vinden onder het kopje ‘samenvatting van de literatuur’. Meer gedetailleerde informatie is beschreven in de Evidencetabellen.
Conclusie
Het wetenschappelijk materiaal is samengevat in een conclusie, waarbij het niveau van het meest relevante bewijs is weergegeven. Voor het niveau van conclusies volgens EBRO en GRADE zie tabel 2 en 5.
Overige overwegingen
Voor het komen tot een aanbeveling zijn er naast het wetenschappelijke bewijs vaak andere aspecten van belang, bijvoorbeeld: patiënten voorkeuren, beschikbaarheid van speciale technieken of expertise, organisatorische aspecten, maatschappelijke consequenties of kosten. Ook bijwerkingen werden hierin meegenomen, voor zover die niet reeds uit wetenschappelijke literatuur waren gedestilleerd en waarvoor dan wel andere bronnen beschikbaar waren. In de overige overwegingen worden de conclusies op basis van de literatuur geplaatst in de context van de dagelijkse praktijk en vindt een afweging plaats van de voor- en nadelen van de verschillende beleidsopties.
Aanbeveling
De uiteindelijk geformuleerde aanbeveling is het resultaat van het beschikbare bewijs in combinatie met deze overwegingen. Het volgen van deze procedure en het opstellen van de richtlijn in dit ‘format’ heeft als doel de transparantie van de richtlijn te verhogen. Het biedt ruimte voor een efficiënte discussie tijdens de werkgroep vergaderingen en vergroot bovendien de helderheid voor de gebruiker van de richtlijn. Voor de gebruikte niveaus van aanbevelingen volgens EBRO en GRADE zie tabel 3 en 6.
Uitwerking volgens de EBRO-methode
Tabel 1: Indeling van methodologische kwaliteit van individuele studies volgens EBRO
|
Kwaliteit |
Interventie |
Diagnostisch accuratesse onderzoek |
Schade / bijwerkingen*, etiologie, prognose |
|
A1 |
Systematische review van tenminste twee onafhankelijk van elkaar uitgevoerde onderzoeken van A2-niveau |
||
|
A2
|
Gerandomiseerd dubbelblind vergelijkend klinisch onderzoek van goede kwaliteit van voldoende omvang |
Onderzoek ten opzichte van een referentietest (een ‘gouden standaard’) met tevoren gedefinieerde afkapwaarden en onafhankelijke beoordeling van de resultaten van test en gouden standaard, betreffende een voldoende grote serie van opeenvolgende patiënten die allen de index- en referentietest hebben gehad |
Prospectief cohort onderzoek van voldoende omvang en follow-up, waarbij adequaat gecontroleerd is voor ‘confounding’ en selectieve follow-up voldoende is uitgesloten. |
|
B |
Vergelijkend onderzoek, maar niet met alle kenmerken als genoemd onder A2 (hieronder valt ook patiënt-controle onderzoek, cohortonderzoek) |
Onderzoek ten opzichte van een referentietest, maar niet met alle kenmerken die onder A2 zijn genoemd |
Prospectief cohort onderzoek, maar niet met alle kenmerken als genoemd onder A2 of retrospectief cohort onderzoek of patiënt-controle onderzoek |
|
C |
Niet-vergelijkend onderzoek |
||
|
D |
Mening van deskundigen |
||
* Deze classificatie is alleen van toepassing in situaties waarin om ethische of andere redenen gecontroleerde trials niet mogelijk zijn. Zijn die wel mogelijk dan geldt de classificatie voor interventies.
Tabel 2: Niveau van conclusies volgens EBRO
|
Niveau |
Conclusie gebaseerd op |
|
1 |
Onderzoek van niveau A1 of tenminste twee onafhankelijk van elkaar uitgevoerde onderzoeken van niveau A2 |
|
2 |
Eén onderzoek van niveau A2 of tenminste twee onafhankelijk van elkaar uitgevoerde onderzoeken van niveau B |
|
3 |
Eén onderzoek van niveau B of C |
|
4 |
Mening van deskundigen |
Tabel 3: Niveau van aanbeveling volgens EBRO
|
Aanbeveling |
Balans |
|
Sterk positief |
De interventie doet duideljk meer goed dan kwaad: Doe…. |
|
Zwak positief |
Het is onzeker of alle patienten gebaat zijn bij de interventie: doe bij voorkeur…. |
|
Zwak negatief |
Het is onzeker of alle patienten gebaat zijn bij de interventie: doe bij voorkeur niet…. |
|
Sterk negatief |
De interventie doet meer kwaad dan goed: doe niet…. |
Uitwerking volgens de GRADE-methode
Tabel 4: Indeling van methodologische kwaliteit van studies volgens GRADE
|
|
GRADE systeem |
|
Type bewijs |
Gerandomiseerd onderzoek = hoog Observationele studie = laag Elk ander bewijs = zeer laag |
|
Factoren die de kwaliteit van bewijs kunnen verlagen*: |
- Ernstige of zeer ernstige beperkingen in de kwaliteit van de studie - Indirectheid van het bewijs - Belangrijke inconsistentie tussen studies - Imprecisie - Grote kans op ‘publicatiebias’ |
|
Factoren die de kwaliteit van bewijs kunnen verhogen**: |
- Sterk bewijs voor een associatie—significant relatief risico van > 2 ( < 0,5) gebaseerd op consistent bewijs uit twee of meer observationele studies, zonder plausibele ‘confounders’ (+1) - Zeer sterk bewijs voor een associatie—significant relatief risico van > 5 ( < 0,2) gebaseerd op direct bewijs zonder belangrijke bedreigingen voor de validiteit (+2) - Bewijs voor een dosis respons gradiënt (+1) - Alle plausibele ‘confounders’ zouden het effect hebben verminderd (+1) |
*Elk criterium kan de kwaliteit verminderen met 1 stap of bij zeer ernstige beperkingen met twee stappen. ** Verhogen kan alleen indien er geen beperkingen zijn t.a.v. de studiekwaliteit, imprecisie, inconsistentie, indirectheid en publicatiebias.
Tabel 5: Niveau van conclusies volgens GRADE
|
Conclusie - Hoog = nader onderzoek zal zeer onwaarschijnlijk het vertrouwen in de inschatting van een effect veranderen - Middelmatig = nader onderzoek zal waarschijnlijk een belangrijke invloed hebben op het vertrouwen in de inschatting van een effect en kan de inschatting van een effect veranderen - Laag = nader onderzoek zal zeer waarschijnlijk een belangrijke invloed hebben op het vertrouwen in de inschatting van een effect en zal waarschijnlijk de inschatting van een effect veranderen - Zeer laag = elke inschatting van een effect is zeer onzeker |
Tabel 6: Niveau van aanbevelingen volgens GRADE
|
Klinische aanbeveling - Sterk voor/tegen = als clinici, gebaseerd op het beschikbare bewijs, zeer zeker zijn dat de voordelen de nadelen of risico’s overtreffen, of andersom, dan zal er een sterke aanbeveling worden gedaan - Zwak voor/tegen = als clinici, gebaseerd op het beschikbare bewijs, denken dat de voordelen en de nadelen of risico’s in balans zijn of als er een bepaalde onzekerheid bestaat over de grootte van de voordelen en risico’s, moeten ze een zwakke aanbeveling maken |
Zoekverantwoording