Antihistaminica
Uitgangsvraag
Wat is de effectiviteit en veiligheid van het voorschrijven van tweede generatie antihistaminica tot viermaal de geregistreerde dosis bij de behandeling van chronische spontane urticaria?
Aanbeveling
Het verhogen van de dosering 2de generatie antihistaminica (cetirizine, desloratadine, ebastine, fexofenadine, levocetirizine en rupatadine) tot maximaal 4x de standaarddosering past als tweede stap in het voorgestelde stepped care model van de behandeling van chronische spontane urticaria, na de geregistreerde dosis 2de generatie antihistaminica. Dit wordt als veilig en effectief beschouwd. In het geval van bijwerkingen kan overwogen worden te switchen naar een ander antihistaminicum voordat de dosering verhoogd wordt.
Het voorschrijven van hoge dosis 2de generatie antihistaminica is off-label en dient altijd gepaard te gaan met uitleg over de ingestelde therapie en mogelijke bijwerkingen. Een deel van de patiënten ontwikkelt slaperigheid, vermoeidheid, duizeligheid, droge mond, hoofdpijn en faryngitis.
In individuele gevallen kan switchen van het ene naar het andere 2de generatie H1-antihistaminicum uitkomst bieden als behandeling van chronische spontane urticaria. Dit is geen aparte stap in het voorgestelde stepped-care model, maar wordt aanbevolen als aanvulling op de tweede stap (opdoseren 2de generatie antihistaminica) ondanks de lage kwaliteit van bewijs.
Bij ernstige nachtelijke jeuk (met verstoring van de slaap) kan een kortdurende en intermitterende behandeling met een 1ste generatie antihistaminicum (zoals dimetindeen of hydroxyzine) vóór de nacht overwogen worden.
Overwegingen
Uit de Cochrane Review van Sharma et al. (2014) bleek dat het niet mogelijk is om op basis van de huidige literatuur een voorkeur voor een specifiek tweede generatie antihistaminicum uit te spreken.
Het opdoseren van tweede generatie antihistaminica heeft in de praktijk vaak bewezen effectief te zijn in de behandeling van CSU. Echter moet ook vermeld worden dat hogere doseringen niet geregistreerd zijn voor de behandeling van chronische spontane urticaria. De geregistreerde tweede generatie antihistaminica hebben een veiligheidsdossier van doseringen tot tenminste 4x de standaarddosering. Echter de dosisafhankelijke bijwerkingen per tweede generatie antihistaminicum variëren. Als wordt gekeken naar de bijwerkingen en het bewijs over de effectiviteit van het opdoseren tot 4x de geregistreerde dosis, kan tot een aanbeveling worden gekomen om opdoseren tot 4x de geregistreerde dosis te overwegen als tweede keus in het algoritme van de behandeling van CSU (voor stepped-care model zie de module stepped-care behandeling). Deze dosering kan in 2 dd 2 tabletten of 4 dd 1 tablet worden voorgeschreven, afhankelijk van de wensen van de patiënt. Hiervoor is geen onderbouwing in de literatuur. Men moet zich er hierbij wel van bewust zijn dat de compliance verlaagd wordt door het moeten innemen van veel tabletten.
De snelheid van het opdoseren dient per patiënt te worden bepaald. Bijwerkingen, met name sufheid en slaperigheid, van deze hogere doseringen tweede generatie antihistaminica lijken in de praktijk vaker voor te komen dan gemeld. Dit wordt dus niet niet door evidence ondersteund. Niet duidelijk is of deze bijwerkingen kunnen worden toegeschreven aan slapeloosheid ten gevolge van de ziekte of aan een mogelijk sederend effect van de hoog-gedoseerde medicatie. In het geval van bijwerkingen kan overwogen worden eerst te switchen alvorens de dosering tweede generatie antihistaminica op te hogen.
De ervaring van de werkgroepleden is dat een kortdurende en intermitterende behandeling met eerste generatie antihistaminica bij volwassen patiënten met CSU in sommige gevallen bij kan dragen aan het bevorderen van de nachtrust, indien deze disproportioneel verstoord wordt door jeukklachten.
Er is één studie waaruit bleek, in een subanalyse, dat switchen tussen tweede generatie antihistaminica (levocetirizine en desloratadine) effectief kan zijn (Staevska et al., 2010). Er is aanzienlijk meer bewijs voor het opdoseren van een tweede generatie antihistaminica, zoals in eerdere modules beschreven.
De ervaring van de werkgroepleden is dat switchen tussen verschillende tweede generatie antihistaminica in specifieke gevallen wel effectief kan zijn en zou dit, ondanks de lage kwaliteit van bewijs, willen aanbevelen als aanvulling op de tweede stap (opdoseren tweede generatie antihistaminica).
Als wordt gekeken naar de kosten van tweede generatie antihistaminica zijn deze veel goedkoper in vergelijking met andere behandelingen zoals ciclosporine en omalizumab (zie hiervoor de desbetreffende modules leukotriënenreceptorantagonisten en omalizumab). De kosten voor cetirizine 10mg zijn €0,18-€0,84 / dag, voor ebastine 10mg €0,26 / dag, voor rupatadine 10mg €0,28 / dag, voor fexofenadine 180mg €0,11-€0,37 / dag en voor levocetirizine en desloratadine 5mg €0,03-€0,20 / dag (www.medicijnkosten.nl).
Onderbouwing
Achtergrond
De belangrijkste behandeling gericht op symptoomverlichting is het verminderen van het effect van mestcelmediatoren zoals histamine. Veel symptomen van urticaria worden primair gemedieerd door de werking van histamine op H1-receptors op endotheelcellen en op sensorische zenuwen. Behandeling met H1-antihistaminica is van zeer groot belang bij de behandeling van urticaria. Continu gebruik van H1-anthistaminica bij chronische urticaria wordt niet alleen ondersteund door de resultaten van klinische trials (Grob et al., 2009; Weller et al., 2013) maar ook door het werkingsmechanisme van deze medicatie. Moderne tweede generatie antihistaminica in doses waarvoor een vergunning is verstrekt, zijn eerstelijns behandelingen bij urticaria en opdosering wordt in de recente internationale richtlijn aanbevolen als tweedelijns behandeling (Zuberbier et al., 2014).
Eerste en tweede generatie H1-antihistaminica
Antihistaminica zijn sinds de jaren 50 van de vorige eeuw beschikbaar voor de behandeling ziekten die gepaard gaan met histamine gemedieerde klachten. De oudere eerste generatie antihistaminica hebben echter uitgesproken anticholinerge effecten en sedatieve werking op het centrale zenuwstelsel (CZS) die langer dan 12 uur duren terwijl het antipruritisch effect slechts 4 - 6 uur duurt. Oude eerste generatie H1-antihistaminica vormen een speciaal probleem bij ouderen bij wie zij het risico op belemmerde cognitie, aandachtsproblemen, gedesorganiseerde spraak, veranderd bewustzijn en valpartijen vergroten. Bovendien kan de eerste generatie antihistaminica interfereren met de rapid eye movement (REM) slaap en invloed hebben op leren en prestaties. De bovengenoemde bijwerkingen worden in de recente GA²LEN position paper (Church et al., 2010) onderschreven: hierin wordt met klem aanbevolen om bij allergie bij volwassenen en met name bij kinderen geen eerste generatie antihistaminica meer te gebruiken. Dit standpunt wordt gedeeld door de WHO-richtlijn ARIA (Bousquet et al., 2008). Ook in de internationale CSU richtlijn wordt tegen het gebruik van deze eerste generatie antihistaminica geadviseerd voor de routinebehandeling van chronische urticaria als eerstelijns middelen, met uitzondering van de weinige plaatsen ter wereld waar tweede generatie antihistaminica niet beschikbaar zijn (Zuberbier et al., 2014). Deze aanbeveling is gebaseerd op sterk bewijs met betrekking tot mogelijke ernstige bijwerkingen van oude eerste generatie antihistaminica (lethale overdoses zijn gemeld) en de beschikbaarheid van tweede generatie antihistaminica wereldwijd voor lage kosten die niet alleen deze bijwerkingen niet hebben maar ook een hogere werkzaamheid en een langere werkingsduur hebben. Gezien dit advies adviseert de werkgroep ook bij urticaria terughoudend te zijn met het gebruik van eerste generatie antihistaminica bij CSU. Bij ernstige nachtelijke jeuk (met verstoring van de slaap) kan een kortdurende en intermitterende behandeling met een eerste generatie antihistaminicum (zoals dimetindeen of hydroxyzine) vóór de nacht overwogen worden (conform de richtlijn constitutioneel eczeem).
Verdere progressie met betrekking tot de geneesmiddelveiligheid werd bereikt door de ontwikkeling van de nieuwere tweede generatie antihistaminica cetirizine (metaboliet van hydroxyzine), loratadine en fexofenadine, waarvan sommige tweede generatie metabolieten zijn van eerdere 1e generatie antihistaminica. Meer recent zijn onder andere bilastine, desloratadine, de actieve metaboliet van loratadine, ebastine, levocetirizine en rupatadine (Kubo et al., 2011) toegevoegd aan de lijst van tweede generatie antihistaminica. Veel van deze antihistaminica zijn onvoldoende bestudeerd bij urticaria en er zijn aanzienlijke klinische verschillen tussen deze antihistaminica. Zes ervan (cetirizine, ebastine, rupatadine, fexofenadine desloratadine en levocetirizine) zijn voldoende onderzocht bij urticaria. Samen moeten tweede generatie antihistaminica worden beschouwd als de eerstelijns symptomatische behandeling voor urticaria vanwege het goede veiligheidsprofiel. Er is echter een groot gebrek aan up-to-date, goed ontworpen klinische trials ter vergelijking (head-to-head) van de werkzaamheid en veiligheid van tweede generatie H1-antihistaminica bij CSU (Sharma et al., 2014).
Conclusies / Summary of Findings
|
Niveau 2 |
Het is aannemelijk dat het opdoseren van cetirizine naar 20mg effectief is bij de behandeling van chronische spontane urticaria bij patiënten die niet reageren op standaarddosering. Echter, studies naar de effectiviteit van hogere doseringen cetirizine laten wisselende resultaten zien.
B: Kameyoshi et al., 2007; B: Okubo et al., 2013; B: Juhlin et al., 1998; C: Asero, 2007 |
|
Niveau 3 |
Er zijn aanwijzingen dat het opdoseren van ebastine tot vier maal de geregistreerde dosis effectief is bij patiënten met therapieresistente chronische spontane urticaria.
C: Godse et al., 2011 |
|
Niveau 1 |
Het is aangetoond dat het opdoseren van rupatadine naar 20mg per dag effectief is bij de behandeling chronische spontane urticaria.
A1: Sharma et al., 2014; A1: Gimenez-Arnau et al., 2009 |
|
Niveau 1 |
Fexofenadine doseringen van 60, 120 en 240mg 2dd laten een vergelijkbare effectiviteit zien bij de behandeling van chronische spontane urticaria. Wel is een lineaire trend zichtbaar wat betreft verbetering van symptomen bij hogere doseringen.
A2: Nelson et al., 2000; A2: Finn et al., 1999 |
|
Niveau 2 |
Het is aannemelijk dat desloratadine en levocetirizine 20mg effectiever zijn dan de standaarddosering van 5mg in de behandeling van therapieresistente chronische spontane urticaria. Het opdoseren van levocetirizine en desloratadine tot 4x de geregistreerde dosis is effectief bij circa 75% van de patiënten met resistente chronische spontane urticaria.
A2: Staevska et al., 2010 |
|
Niveau 3 |
Er zijn aanwijzingen dat vanuit patiënten perspectief het opdoseren van 2de generatie antihistaminica effectief is, zonder significante toename van de bijwerkingen.
C: Weller et al., 2011 |
|
Niveau 2 |
Het is aannemelijk dat switchen in individuele gevallen tussen desloratadine en levocetirizine effectief kan zijn.
A2: Staevska et al., 2010 |
|
Niveau 1 |
Er is geen verschil in het risico op het staken van een middel door bijwerkingen tussen 10mg en 20mg cetirizine.
A1: Sharma et al., 2014 |
|
Niveau 2 |
Het is aannemelijk dat het opdoseren van cetirizine naar 30mg en opdoseren van rupatadine naar 20mg gepaard kan gaan met slaperigheid of vermoeidheid.
C: Asero, 2007; A2: Dubertret et al., 2007; A1: Ginenez-Arnau et al., 2007 |
Samenvatting literatuur
Beschrijving studies
De geïncludeerde studies bestonden uit twee observationele studies, negen gecontroleerde studies, één studie met gepoolde resultaten en één retrospectieve survey. De behandelduur in de studies was tussen de twee en zes weken. Het aantal patiënten varieerde van zes tot 439 patiënten met chronische spontane urticaria. In één studie was de patiëntenpopulatie niet nader omschreven (Okubo et al., 2013). In een studie namen tevens patiënten met een positieve ASST (Asero, 2007) en in een studie andere namen patiënten met symptomatisch dermografisme en drukurticaria deel (Staevska et al., 2010). Antihistaminica waarvan de effectiviteit van een hogere dosering dan de geregistreerde dosis is onderzocht zijn cetirizine, ebastine, rupatadine, fexofenadine, levocetirizine en desloratadine.
Hiernaast is er kennis genomen van de systematische Cochrane review van Sharma et al. (2014).
Uitkomstmaten die zijn gebruikt om de effectiviteit te bepalen zijn de ziekteactiviteit, totale symptoom score, kwaliteit van leven en bijwerkingen. De geïncludeerde studies zijn moeilijk te vergelijken gezien de verschillende interventies. De resultaten zullen dan ook worden uitgesplitst per antihistaminicum.
Kwaliteit van bewijs
Onder de studies waren zeven gerandomiseerde studies. Het randomisatieproces werd slechts in één van de studies duidelijk beschreven (Weller et al., 2013). Ook de methode om een adequate ‘concealment of allocation’ te waarborgen was slechts in twee studies duidelijk beschreven (Staevska et al., 2010; Weller et al., 2013). Zeven studies gaven aan dubbelblind te zijn uitgevoerd. In vijf studies was de methode van blindering echter niet duidelijk beschreven. Drie studies waren open-label studies. De grootte van de studiepopulaties varieerde van erg klein (n=6) tot een gepoolde studie met 538 patiënten. Zes studies gaven aan een intention-to-treat (ITT) analyse te hebben uitgevoerd. Meer informatie vindt u terug in de Evidencetabellen.
Effectiviteit
Cetirizine
In de Cochrane Review van Sharma et al. (2014) is beschreven dat 10mg cetirizine bij meer patiënten tot complete remissie leidt dan placebo. Over het effect van 20mg cetirizine of hoger werd niet gesproken.
In een open studie van Kameyoshi et al. (2007) werden 21 patiënten met CIU en inadequate respons op 10mg cetirizine 1-2 weken behandeld met 20mg cetirizine. Patiënten werden gerandomiseerd om óf nog 1-2 weken cetirizine 10mg te krijgen, of 20mg cetirizine voor 1-2 weken. Beide groepen lieten verbetering in UAS zien tijdens de behandeling met 20mg. De groep behandeld met 20mg cetirizine liet blijvende verbetering in UAS zien, waar de groep met lagere dosering juist een terugval liet zien.
In een andere open studie van Asero (2007) werden 22 patiënten met resistente CIU behandeld met 10mg cetirizine gedurende één week, en vervolgens met 30mg (3dd 10mg) gedurende één week. Slechts één patiënt liet een verbetering in VAS-score zien bij de verhoogde dosis. Alle andere patiënten hadden uiteindelijk aanvullende therapie nodig in de vorm van corticosteroïden, ciclosporine of cyclofosfamide.
De effectiviteit van een dubbele dosering cetirizine was onderzocht in een gerandomiseerde, niet-geblindeerde studie van Okubo et al. (2013) onder 51 patiënten met chronische urticaria. In fase A kregen alle patiënten 10mg cetirizine gedurende een week. Alleen patiënten niet reagerend op deze dosering werden gerandomiseerd om behandeld te worden met óf cetirizine 20mg óf olopatadine 10mg. Zes van de negen patiënten bereikten remissie (verbetering of verdwijnen van alle symptomen in vergelijking met de baseline). Een significante verbetering in ziekteactiviteit en jeuk werd gezien in de groep met cetirizine 20mg, in vergelijking met de baseline. De groepen lieten onderling geen verschil zien.
In een kleine dubbelblinde studie onder 30 patiënten met CIU, werden zes patiënten die niet reageerden op cetirizine 10mg of placebo onderverdeeld in cetirizine 10mg of 20mg. Van de drie patiënten bemerkte één patiënt uitstekende (91-100%), één gemiddelde (31-50%) en één patiënt slechte(<30%) verbetering van symptomen in vergelijking met de baseline.
Ebastine
Godse et al. (2011) hebben in een open studie bij 30 patiënten met CIU de dosering ebastine opgehoogd van 10mg tot 40mg in vier weken. De effectiviteit werd bepaald middels de UAS7. Alleen symptomatische patiënten kregen een hogere dosering ebastine. De UAS zakte van 4,6 (baseline) naar <1 na vier weken behandeling. 17, acht en twee patiënten waren symptoomvrij na behandeling met 10mg, 20mg en 40mg ebastine respectievelijk.
Rupatadine
Sharma et al. (2014) concludeerden dat 10mg en 20mg rupatidine ten opzichte van placebo goede of excellente respons geven in de bij patiënten met CSU. Of er verschil is in het effect van de verschillende doses, lieten zij in het midden.
In een gerandomiseerde, dubbelblinde, placebogecontroleerde studie onder 329 patiënten met CIU werd 10mg rupatadine vergeleken met 20mg gedurende zes weken. Beide doseringen gaven een significante verbetering in symptomen in vergelijking met placebo. Tussen de twee doseringen werd echter geen significant verschil gevonden (Gimenez-Arnau et al., 2007).
In een andere gerandomiseerde, dubbelblinde placebogecontroleerde studie van Dubertret et al. (2007) werd het effect van 5mg, 10mg en 20mg rupatadine onderzocht gedurende vier weken bij 277 patiënten met CIU. De dosering met 20mg was significant effectiever dan 5mg (P<0,001) en 10mg (P<0,05) wat betreft de jeukscore. Wat betreft totale symptoomscore was 20mg alleen significant effectiever dan 5mg rupatadine (P<0,01).
Een studie waarin gepoolde analyse is verricht van de twee eerder genoemde studies concludeert dat zowel 10mg als 20mg rupatadine significant effectiever is dan placebo. Rupatadine 20mg liet een significant hoger percentage responders (75% symptoomvermindering in vergelijking met de baseline) zien in vergelijking met rupatadine 10mg (P<0,01) (Gimenez-Arnau et al., 2009).
Fexofenadine
In een gerandomiseerde, dubbelblinde, placebo gecontroleerde studie van Nelson et al. (2000) werden 418 patiënten behandeld met 20, 60, 120 of 240mg fexofenadine 2dd of placebo gedurende vier weken. Alle doseringen waren significant effectiever dan placebo. Een dosering van 60mg of hoger was effectiever dan de lage dosering van 20mg, hoewel de drie hoogste doseringen onderling niet verschilden. Een vergelijkbare studie van Finn et al. (1999) onder 439 patiënten toonde dezelfde resultaten. Wel was een lineaire trend zichtbaar wat betreft verbetering van symptomen bij hogere doseringen.
Levocetirizine / Desloratadine
Staevska et al. (2010) hebben 80 patiënten met CIU behandeld met desloratadine of levocetirizine in een gerandomiseerde, dubbelblinde studie. De startdosering was 5mg per dag, en dit werd bij resistente patiënten wekelijks opgehoogd tot 10 of 20mg per dag. Patiënten die niet reageerden op 20mg van het ene middel werden behandeld met 20mg van het andere middel. 13 patiënten werden symptoomvrij na behandeling met 5mg en 21 patiënten na 10mg en 20 mg. De hogere doseringen waren significant effectiever voor zowel levocetirizine (P<0,001) en desloratadine (P=0,002). Zeven patiënten die niet op desloratadine 20mg reageerden, reageerden wel op 20mg levocetirizine.
Verhoogde doseringen lieten een verbeterde kwaliteit van leven zien. 75% van de patiënten werden geclassificeerd als ‘responders to higher doses’.
Weller et al. (2013) hebben de effectiviteit onderzocht van on-demand desloratadine 5mg en 20mg in een dubbelblinde, gerandomiseerde studie. De grootte van het gebied met urticae werd bepaald met behulp van thermografische beeldvorming, vijf uur na het toedienen van medicatie. Zowel 5 als 20mg lieten een reductie van de grootte van het gebied zien in vergelijking met placebo, er was echter geen verschil tussen beide doseringen desloratadine.
Patiënten perspectief
Een retrospectieve observationele survey met vragenlijsten onder 319 patiënten met gediagnosticeerde CSU heeft het perspectief van patiënten over de effectiviteit en veiligheid van het opdoseren van verschillende tweede generatie antihistaminica onderzocht. Uit deze survey bleek dat 75% van de patiënten een hogere dosering kregen vanwege onvoldoende effectiviteit van de geregistreerde dosis. 40%, 42% en 54% rapporteerde een significant voordeel van twee, drie of vier tabletten per dag respectievelijk (Weller et al., 2011).
Dosering
Standaarddosering die in Nederland wordt gebruikt bij de behandeling van chronische urticaria is voor cetirizine, ebastine en rupatadine 10mg / dag. Voor fexofenadine is dit 180mg / dag en voor levocetirizine en desloratadine 5mg / dag.
Gezien het offlabel gebruik dient men zich bewust te zijn van de farmacodynamiek, farmacokinetiek en de metabolisatie via de lever hetzij nieren.
Bijwerkingen
Veelvoorkomende bijwerkingen (1-10%) van tweede generatie antihistaminica zijn slaperigheid, vermoeidheid, duizeligheid, droge mond, hoofdpijn en faryngitis (Informatorium medicamentorum, kennisbank KNMP).
Uit de retrospectieve survey van Weller et al. (2011) bleek dat het aantal bijwerkingen dat patiënten ervaren bij hogere doseringen tweede generatie antihistaminica niet significant te verschillen van bijwerkingen bij standaarddoseringen. Ook bleek uit de Cochrane Review van Sharma et al. (2014) dat er geen verschil zat in het risico op het staken van een middel door bijwerkingen tussen 10mg en 20mg cetirizine.
Echter, in de studie van Kameyoshi et al. (2007) gaven twee van de tien patiënten klachten aan van slaperigheid bij cetirizine 20mg, die verdwenen bij het verlagen van de dosering naar 10mg. 13 patiënten (59%) rapporteerden vermoeidheid en slaperigheid tijdens het gebruik van cetirizine 30mg (Asero, 2007). Ook in de studie van Okubo et al. (2013) werd bij drie van de 59 patiënten slaperigheid gerapporteerd.
Eén van de tien patiënten rapporteerde milde sedatie bij het gebruik van 40mg ebastine (Godse, 2011). In de studie van Gimenez-Arnau et al. (2007) bleek rupatadine 10mg een gunstiger bijwerkingenprofiel te hebben dan rupatadine 20mg; 20mg gaf in vergelijking met 10mg met meer klachten van hoofdpijn (8,3% vs. 4,5%) en slaperigheid (8,3% vs. 2,7%). Het optreden van slaperigheid varieerde in de studie van Dubertret et al. (2007) van 4,3% bij 5mg tot 21,4% bij 20mg rupatadine. Voor hoofdpijn liep dit uiteen van 2,86% voor 5mg tot 4,29% voor 20mg. Eenmaal is een voorbijgaand verhoogd serum creatine kinase gesignaleerd bij een patiënt. In beide studies die de effectiviteit en veiligheid van fexofenadine in verschillende doseringen hebben onderzocht, werd in alle behandelgroepen een vergelijkbaar aantal bijwerkingen gemeld. In de studie van Staevska et al. (2010) rapporteerden 17 van de 80 patiënten bijwerkingen, waarbij geen duidelijke relatie werd gezien met de hogere doseringen levocetirizine of desloratadine.
Zoeken en selecteren
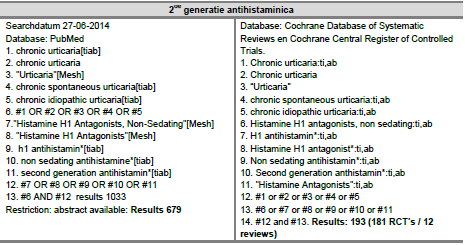
Voor deze uitgangsvraag is een systematische search verricht in de databases PubMed, the Cochrane Database of Systematic Reviews en Cochrane Central Register of Controlled Trials. De searchstrategie is bijgevoegd onder Zoekverantwoording. De search leverde 679 artikelen op uit PubMed en 193 artikelen uit Cochrane, hiervan zijn uiteindelijk 12 bruikbare studies geïncludeerd die de effectiviteit en veiligheid van het opdoseren van tweede generatie antihistaminica bij CSU hebben onderzocht (Asero, 2007; Dubertret et al., 2007; Finn et al., 1999; Gimenez-Arnau et al., 2007; Gimenez-Arnau, Izquierdo & Maurer, 2009; Godse, 2011; Juhlin and Arendt, 1988; Nelson, Reynolds & Mason, 2000; Okubo et al., 2013; Staevska et al., 2010; Weller et al., 2011; Weller et al., 2013). Een aanvullende handsearch leverde nog één bruikbaar artikel op (Kameyoshi et al., 2007). Ook is er kennis genomen van de Cochrane Review van Sharma et al. (2014), die na de searchdatum is gepubliceerd.
Referenties
- Asero R. 2007. Chronic unremitting urticaria: is the use of antihistamines above the licensed dose effective? A preliminary study of cetirizine at licensed and above-licensed doses. Clin. Exp. Dermatol. 32 (1): 34-38.
- Bousquet J, Khaltaev N, Cruz AA, Denburg J, Fokkens WJ, Togias A, Zuberbier T, Baena-Cagnani CE, Canonica GW, van WC, Agache I, Ait-Khaled N, Bachert C, Blaiss MS, Bonini S, Boulet LP, Bousquet PJ, Camargos P, Carlsen KH, Chen Y, Custovic A, Dahl R, Demoly P, Douagui H, Durham SR, van Wijk RG, Kalayci O, Kaliner MA, Kim YY, Kowalski ML, Kuna P, Le LT, Lemiere C, Li J, Lockey RF, Mavale-Manuel S, Meltzer EO, Mohammad Y, Mullol J, Naclerio R, O'Hehir RE, Ohta K, Ouedraogo S, Palkonen S, Papadopoulos N, Passalacqua G, Pawankar R, Popov TA, Rabe KF, Rosado-Pinto J, Scadding GK, Simons FE, Toskala E, Valovirta E, van CP, Wang DY, Wickman M, Yawn BP, Yorgancioglu A, Yusuf OM, Zar H, Annesi-Maesano I, Bateman ED, Ben KA, Boakye DA, Bouchard J, Burney P, Busse WW, Chan-Yeung M, Chavannes NH, Chuchalin A, Dolen WK, Emuzyte R, Grouse L, Humbert M, Jackson C, Johnston SL, Keith PK, Kemp JP, Klossek JM, Larenas-Linnemann D, Lipworth B, Malo JL, Marshall GD, Naspitz C, Nekam K, Niggemann B, Nizankowska-Mogilnicka E, Okamoto Y, Orru MP, Potter P, Price D, Stoloff SW, Vandenplas O, Viegi G, and Williams D. 2008. Allergic Rhinitis and its Impact on Asthma (ARIA) 2008 update (in collaboration with the World Health Organization, GA(2)LEN and AllerGen). Allergy 63 Suppl 86: 8-160.
- Church MK, Maurer M, Simons FE, Bindslev-Jensen C, van CP, Bousquet J, Holgate ST, and Zuberbier T. 2010. Risk of first-generation H(1)-antihistamines: a GA(2)LEN position paper. Allergy 65 (4): 459-466.
- Dubertret L, Zalupca L, Cristodoulo T, Benea V, Medina I, Fantin S, Lahfa M, Perez I, Izquierdo I, and Arnaiz E. 2007. Once-daily rupatadine improves the symptoms of chronic idiopathic urticaria: a randomised, double-blind, placebo-controlled study. Eur. J. Dermatol. 17 (3): 223-228.
- Finn AF Jr., Kaplan AP, Fretwell R, Qu R, and Long J. 1999. A double-blind, placebo-controlled trial of fexofenadine HCl in the treatment of chronic idiopathic urticaria. J. Allergy Clin. Immunol. 104 (5): 1071-1078.
- Gimenez-Arnau A, Izquierdo I, and Maurer M. 2009. The use of a responder analysis to identify clinically meaningful differences in chronic urticaria patients following placebo- controlled treatment with rupatadine 10 and 20 mg. J. Eur. Acad. Dermatol. Venereol. 23 (9): 1088-1091.
- Gimenez-Arnau A, Pujol RM, Ianosi S, Kaszuba A, Malbran A, Poop G, Donado E, Perez I, Izquierdo I, and Arnaiz E. 2007. Rupatadine in the treatment of chronic idiopathic urticaria: a double-blind, randomized, placebo-controlled multicentre study. Allergy 62 (5): 539-546.
- Godse KV. 2011. Ebastine in chronic spontaneous urticaria in higher doses. Indian J. Dermatol. 56 (5): 597-598.
- Grob JJ, Auquier P, Dreyfus I, and Ortonne JP. 2009. How to prescribe antihistamines for chronic idiopathic urticaria: desloratadine daily vs PRN and quality of life. Allergy 64 (4): 605-612.
- Juhlin L, and Arendt C. 1988. Treatment of chronic urticaria with cetirizine dihydrochloride a non-sedating antihistamine. Br. J. Dermatol. 119 (1): 67-71.
- Kameyoshi Y, Tanaka T, Mihara S, Takahagi S, Niimi N, and Hide M. 2007. Increasing the dose of cetirizine may lead to better control of chronic idiopathic urticaria: an open study of 21 patients. Br. J. Dermatol. 157 (4): 803-804.
- Kubo N, Senda M, Ohsumi Y, Sakamoto S, Matsumoto K, Tashiro M, Okamura N, and Yanai K. 2011. Brain histamine H1 receptor occupancy of loratadine measured by positron emission topography: comparison of H1 receptor occupancy and proportional impairment ratio. Hum. Psychopharmacol. 26 (2): 133-139.
- Nelson HS, Reynolds R, and Mason J. 2000. Fexofenadine HCl is safe and effective for treatment of chronic idiopathic urticaria. Ann. Allergy Asthma Immunol. 84 (5): 517-522.
- Okubo Y, Shigoka Y, Yamazaki M, and Tsuboi R. 2013. Double dose of cetirizine hydrochloride is effective for patients with urticaria resistant: a prospective, randomized, non-blinded, comparative clinical study and assessment of quality of life. J. Dermatolog. Treat. 24 (2): 153-160.
- Staevska M, Popov TA, Kralimarkova T, Lazarova C, Kraeva S, Popova D, Church DS, Dimitrov V, and Church MK. 2010. The effectiveness of levocetirizine and desloratadine in up to 4 times conventional doses in difficult-to-treat urticaria. J. Allergy Clin. Immunol. 125 (3): 676-682.
- Weller K, Ardelean E, Scholz E, Martus P, Zuberbier T, and Maurer M. 2013. Can on-demand non-sedating antihistamines improve urticaria symptoms? A double-blind, randomized, single-dose study. Acta Derm. Venereol. 93 (2): 168-174.
- Weller K, Ziege C, Staubach P, Brockow K, Siebenhaar F, Krause K, Altrichter S, Church MK, and Maurer M. 2011. H1-antihistamine up-dosing in chronic spontaneous urticaria: patients' perspective of effectiveness and side effects--a retrospective survey study. PLoS. One. 6 (9): e23931.
- Zuberbier T, Aberer W, Asero R, Bindslev-Jensen C, Brzoza Z, Canonica GW, Church MK, Ensina LF, Gimenez-Arnau A, Godse K, Goncalo M, Grattan C, Hebert J, Hide M, Kaplan A, Kapp A, Abdul Latiff AH, Mathelier-Fusade P, Metz M, Nast A, Saini SS, Sanchez-Borges M, Schmid-Grendelmeier P, Simons FE, Staubach P, Sussman G, Toubi E, Vena GA, Wedi B, Zhu XJ, and Maurer M. 2014. The EAACI / GA2LEN / EDF / WAO Guideline for the definition, classification, diagnosis, and management of urticaria: the 2013 revision and update. Allergy 69(7): 868887.
Evidence tabellen
Opdoseren 2de generatie antihistaminica
|
Auteur, jaartal |
Mate van bewijs |
Studie type |
Patiëntenpopulatie In/exclusie |
Studieopzet / Dosering /
|
Behandel duur |
Followup duur |
Uitkomstmaten |
Bijwerking en |
Resultaten |
|
Conclusie |
Studie Limitaties* |
Overige opmerkingen |
|
Cetirizine |
|
|
|
|
|
|
|
|
|
|
|||
|
Kameyo shi et al. 2007 |
B |
Open Label trial. |
21 ptn met CIU (>1maand), niet reagerend op cetirizine 10 mg
Leeftijd A:42,5 ± 14,1 vs. B:36,9 ± 16,7
M / V verhouding niet bekend |
Cetirizine 10mg vs. 20 mg (2dd10mg)
(A:20mg 2-4 wkn (n=11), B: 20mg 1-2 wkn, daarna 10mg 1-2 wkn (n=10))
Comedicatie: geen, echter 2 ptn bleven montelukast 10mg naast cetirizine 20mg gebruiken. |
2-4 wkn
|
- |
Gem. TSS (aantal kwaddels, duur, jeuk 0-9) |
2 ptn met slaperighei d bij 20 mg. |
Significante verbetering (P <0,01) TSS bij 20mg in vergelijking tot de baseline. |
Opdoseren lijkt effectief |
Kleine open studie. Randomisatie niet beschreven. Concealment of allocation niet beschreven. Duur CIU onbekend Korte duur studie. Variabele behandelduur. Loss to follow-up/ ITT niet beschreven.
|
||
|
Asero et al. 2007 |
C |
Open Label trial |
22 ptn met resistente CU (2-480 maanden)
3 mannen / 19 vrouwen. Leeftijd 28-67 jaar |
Cetirizine 10mg vs. 30mg (3dd 10mg)
Comedicatie: 21 ptn gebruikten corticosteroïden aan het eind van week2 . |
2 wkn (1 week 10mg, 1 eek 30mg) |
4 wkn |
Ziekteactiviteit (VAS-score) |
13 ptn (59%) rapporteer den vermoeidh eid en slaperighei d bij 30mg. |
Slechts 1 patiënt verbetering door opdoseren. Alle andere ptn moesten corticosteroïden/cicl osporine gebruiken, waarmee ziekte onder controle kwam. |
Opdoseren niet effectief |
Kleine open studie Korte duur studie Tevens ptn met positieve ASST. Ziekteactiviteit bepaald met VAS. |
||
|
Auteur, jaartal |
Mate van bewijs |
Studie type |
Patiëntenpopulatie In/exclusie |
Studieopzet / Dosering /
|
Behandel duur |
Followup duur |
Uitkomstmaten |
Bijwerking en |
Resultaten |
Conclusie |
Studie Limitaties* |
Overige opmerkingen |
|
Okubo et al. 2013 |
B |
RCT Open label
|
51 ptn met CU (gem. duur urticaria 7mnd). Alleen ptn resistent voor 10mg cetirizine werden gerandomiseerd (n=18)
16 mannen / 35 vrouwen 17-81 jaar |
Cetirizine 10mg vs. 20mg 1dd
(Fase 1: cetirizine 10mg, Fase 2: cetirizine 20mg(n=9) vs. olopatadine 10mg (n=9))
Comedicatie: geen, washout periode tenminste 3 dagen. |
2 wkn (1 week 10mg cetirizine, 1 week cetirizine 10mg vs. olopatadin e) |
- |
Ziekteactiviteit (Ernst urticae (03)) Jeuk (VAS) Kwaliteit van leven (Skindex) |
Slaperighei d bij 3 ptn (2 in 10mg groep, 1 in 20mg groep) |
significante verbetering in jeuk en urticae bij cetirizine 20mg in vergelijking met de baseline. Tussen de groepen geen significant verschil.
Verbetering QoL bij 20mg in vergelijking tot de baseline. |
Opdoseren lijkt effectief bij ptn resistent voor standaard dosering. |
Niet geblindeerd. Randomisatieproces niet beschreven. Concealment niet beschreven. Slechts 9 ptn behandeld met 20mg. 2/9 dropouts in olopatadine groep, reden niet beschreven Patiëntenpopulatie, in- exclusiecriteria niet omschreven Alleen ptn resistent voor 10mg werden gerandomiseerd. Jeuk bepaald met VAS. Geen gevalideerd scoresysteem voor ziektelast. |
|
|
Juhlin et al. 1988 |
B |
DB PC trial |
6 ptn met CIU 11mannen / 19 vrouwen 15-70 jaar |
Cetirizine 10mg 1dd vs. 10mg 2dd
(Fase 1: cetirizine 10mg vs. placebo (n=30), Fase 2: cetirizine 10mg (n=3) vs. 20mg (n=3))
Comedicatie: geen |
? |
- |
% verbetering symptomen in vergelijking tot de baseline: uitstekend (91100), erg goed (71-90), goed (51-70), gemiddeld(31- 50), slecht(<30) |
Geen bijwerkinge n |
1/3 ptn bemerkte uitstekende, 1/3 gemiddelde, 1/3 slechte verbetering symptomen bij 20mg cetirizine. |
|
Randomisatie niet beschreven. Cross-over. Blindering niet beschreven. Alleen ptn niet reagerend op studie fase I kwamen in studie fase II: Slechts 6 ptn, waarvan 3 cetirizine 20mg. Loss to follow-up niet beschreven. Geen statistiek verricht. Behandelduur niet duidelijk beschreven. |
|
|
Auteur, jaartal |
Mate van bewijs |
Studie type |
Patiëntenpopulatie In/exclusie |
Studieopzet / Dosering /
|
Behandel duur |
|
Followup duur |
|
Uitkomstmaten |
Bijwerking en |
Resultaten |
Conclusie |
Studie Limitaties* |
Overige opmerkingen |
|
|
Ebastine |
|
|
|
|
|
|
|
|
|
|
|||||
|
Godse et al. 2011 |
C |
Open Label Cohort |
30 ptn met CIU (range 3 mnd – 2 jaar)
14 mannen / 16 vrouwen Gem. leeftijd 30.2 jr. |
Ebastine 10mg - 40mg
Comedicatie: geen, 1 dag washout.
|
4 wkn |
|
- |
|
Ziekteactiviteit (UAS7) Sedatie (0-3) |
Milde sedatie bij 1 patiënt met 40mg. |
Baseline UAS 4.6, na 1 wk UAS 2.2, na 2 wk UAS 1.1, na 4 wk UAS < 1.0. 17, 8 en 2 ptn symptoomvrij na 10, 20 en 40mg respectievelijk. |
Opdoseren effectief |
Kleine open studie. Relatief korte duur. Alleen resistente ptn kregen hogere dosering Ebastine (20mg n=10, 40mg n=2). Onduidelijk over welke groep de UAS is bepaald. 3 ptn lost to follow-up vanwege geen respons. Geen statistiek verricht. |
||
|
Rupatadine |
|
|
|
|
|
|
|
|
|
|
|||||
|
Gimene z- Arnau et al. 2009 |
A1 |
Gepoo lde data 2 DB PC RCT’s |
538 ptn met CIU.
Resultaat gepoolde data studies Dubertret et al. 2007 en Gimenez-Arnau et al. 2007. |
Rupatadine 10mg vs. 20mg vs. placebo |
4 wkn |
- |
|
Jeuk (MPS) Nr. kwaddels (MNW) UAS (MPS+MNW)
Respons 50% of 75% symptoomverbeterin g in vergelijking met baseline. |
- |
20mg hoger percentage responders met 75% symptoomverminde ring dan 10mg (P<0,01) 10mg en 20mg significant effectiever dan placebo (P<0,0001).
|
Opdoseren effectief. |
Kwaliteitsbeoordeling RCT’s niet beschreven. ‘aangepaste’ UAS gebruikt. |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Auteur, jaartal |
Mate van bewijs |
Studie type |
Patiëntenpopulatie In/exclusie |
Studieopzet / Dosering /
|
Behand elduur |
Follow -up duur |
Uitkomstmaten |
Bijwerking en |
Resultaten |
Conclusie |
Studie Limitaties* |
Overige opmerkingen |
|
Dubertet et al. 2007 |
A2 |
RCT DB PC
|
283 ptn met matige tot ernstige CIU 12-65 jaar. Jeukscore ≥2 |
Rupatadine 5mg vs. 10mg vs 20mg vs. placebo 1dd
Comedicatie: geen |
4 wkn |
- |
Jeuk (MPS) Nr. kwaddels (MNW) MTSS (MPS+MNW) Invloed op ADL Invloed op slaap
|
Meest frequent slaperighei d en hoofdpijn |
Reductie MPS 10mg en 20mg vs. placebo significant.
20mg significant effectiever dan 5mg (P<0,001) en 10mg(P<0,05) wat betreft jeuk en significante effectiever dan 5mg wat betreft MTSS(P<0,01). 10 en 20mg significante effectiever dan placebo wat betreft MPS en MTSS. |
OPdoseren effectief op jeuk en totale symptoomsc ore.
|
Randomisatie, concealment en blindering niet beschreven. Modified ITT analyse. 283 gerandomiseerd, 277 in analyse. 39 loss to follow-up Drop-out goed beschreven. Sample size berekend. |
|
|
Gimene z-Arnau et al. 2007 |
A2 |
RCT DB PC MC |
329 ptn met CIU (10mg n=112, 20mg n=109, placebo n=113) Volwassenen Jeukscore ≥2 |
Rupatadine 10mg vs. 20mg vs. placebo 1dd
Comedicatie: geen |
4 en 6 wkn |
- |
Jeuk (MPS) Nr. kwaddels (MNW) MTSS (MPS+ MNW) QoL (DLQI) Discomfort (VAS) |
Meest frequent slaperighei d en hoofdpijn |
Significante vermindering MPS 10mg en 20mg vergeleken met placebo.
10mg vs. 20mg geen significant verschil |
Geen verschil 10mg vs. 20mg. 10mg gunstiger bijwerkingen profiel. |
Randomisatie en concealment d.m.v. ‘centralized computergenerated randomization code provided by the sponsor’. Blindering niet beschreven. Modified ITT analyse. 400 ptn gerandomiseerd, 329 in analyse. Loss to follow-up 12.3%, redelijk verdeeld over de groepen. Sample size berekend. |
|
|
Auteur, jaartal |
Mate van bewijs |
Studie type |
Patiëntenpopulatie In/exclusie |
Studieopzet / Dosering /
|
Behand elduur |
Follow -up duur |
Uitkomstmaten |
Bijwerking en |
Resultaten |
Conclusie |
Studie Limitaties* |
Overige opmerkingen |
|
Fexofenadine |
||||||||||||
|
Nelson et al. 2000 |
A2 |
RCT DB PC MC |
468 ptn met CIU (≥3 dagen/week gedurende 6 wkn) Matige tot ernstige jeuk 12-65 jaar
Exclusie: ptn niet reagerend op H1AH. |
Fexofenadine 20 vs. 60 vs. 120 vs. 240mg 2dd
Comedicatie: geen |
4 wkn |
- |
Jeuk (MPS) Nr. kwaddels (MNW) Impact op slaap en ADL (0-3)
|
Gelijke incidentie bijwerkinge n alle groepen.
|
Alle doseringen significante effectiever dan placebo met significante lineaire trend zichtbaar.
Hoger dan 60mg effectiever dan 20mg. Onderling echter geen verschil. |
Dosering van 60mg lijkt meest effectief.
|
Randomisatie, concealment en blindering niet beschreven. Modified ITT analyse. 468 ptn gerandomiseerd, 418 in analyse. Loss to follow-up 29%.N=36 dropout in placebo. Geen baseline disbalans.
|
|
|
Finn et al. 1999 |
A2 |
RCT DB PC MC |
439 ptn met CIU (≥3 dagen/week gedurende 6 wkn)
12-65 jaar |
Fexofenadine 20 vs. 60 vs. 120 vs. 240mg 2dd
Comedicatie: geen |
4 wkn |
- |
Jeuk (MPS) Nr. kwaddels (MNW) MTSS Impact slaap en ADL (0-3)
|
Gelijke incidentie bijwerkinge n alle groepen.
|
Alle doseringen significante effectiever dan placebo met significante lineaire trend zichtbaar.
Hoger dan 60mg effectiever dan 20mg. Onderling echter geen verschil. |
Dosering van 60mg lijkt meest effectief.
|
Randomisatie, concealment en blindering niet beschreven. Modified ITT analyse. 476 ptn gerandomiseerd, 439 in analyse. Loss to follow- up 103 ptn (22%); 30% plc, 26% 20mg, 21% 60mg, 14% 120mg en 17% 240mg.
|
|
|
Auteur, jaartal |
Mate van bewijs |
Studie type |
Patiëntenpopulatie In/exclusie |
Studieopzet / Dosering /
|
Behand elduur |
Follow -up duur |
Uitkomstmaten |
Bijwerking en |
Resultaten |
Conclusie |
Studie Limitaties* |
Overige opmerkingen |
|
Levocetirizine / Desloratadine |
|
|
|
|
|
|
|
|
|
|||
|
Staesvk a et al. 2010 |
A2 |
RCT DB Crossover |
80 ptn met resistente CIU ondanks standaard dosering H1-AH. (≥3 dagen/week gedurende 6 wkn)
27 mannen / 52 vrouwen
19-67 jaar |
Levocetirizine vs. desloratadine (levo n=40 / des n=40) 5mg, 10mg, 20 mg 1dd Alleen resistente ptn kregen hogere dosering.
|
1- 4 wkn |
- |
Aantal ptn symptoomvrij VAS QoL (DLQI) |
Bijwerking en bij 17/80 ptn geen duidelijk verschil doseringen .
|
Des 5mg vs. 20mg P0,002, lev 5mg vs. 20mg P<0,001.
7/28 resistent voor 20mg desloratadine reageerden op 20mg levocetirizine.
Bij verhoogde dosering verbeterde symptoomscores |
Opdoseren tot 4x standaarddo sering effectief bij ca. 75% van ptn met resistente urticaria. Switchen kan zinvol zijn. |
3 dropouts desloratadinegroep, goed beschreven. Randomisatiemethode niet beschreven. Blindering beschreven, echter: ptn niet geblindeerd voor verhoging dosering. Ook ptn met symptomatisch dermografisme, drukurticaria en positieve ASST. Na korte symptoomvrije periode (3dgn) kunnen ptn trial verlaten. |
|
|
Weller et al. 2013 |
A2 |
RCT DB |
34 ptn met CSU 18-75 jaar 13 mannen / 16 vrouwen |
Desloratadine On-demand behandeling 5mg (n=13) vs. 20mg (n=16)
Noodmedicatie: cetirizine 10mg en clemastine 1mg z.n. |
3 wkn |
- |
Grootte gebied urticae ‘grootte van hyperthermisch gebied’ Aantal kwaddels
|
Geen bijwerkinge n gerapporte erd of geobserve erd. |
5mg vs. 20mg. niet verschillend.
5 en 20mg effectief in reduceren hyperthermisch gebied.
Aantal kwaddels verminderd na 20mg. |
Effectiviteit on-demand therapie beperkt. Geen verschil beide doseringen. |
Randomisatie en blindering beschreven. Modified ITT bij 29 ptn. Kleine studiegroep. Alleen on-demand behandeling. |
|
|
Auteur, jaartal |
Mate van bewijs |
Studie type |
Patiëntenpopulatie In/exclusie |
Studieopzet / Dosering /
|
Behand elduur |
Follow -up duur |
Uitkomstmaten |
Bijwerking en |
Resultaten |
Conclusie |
Studie Limitaties* |
Overige opmerkingen |
|
Overig |
|
|
|
|
|
|
|
|
|
|
|
|
|
Weller et al. 2011 |
C |
Surve y Retros pectief observ atione el |
319 ptn met CSU (gediagnosticeerd) Leeftijd 18-76 248 vrouwen / 71 mannen |
Vragenlijsten retrospectief over patiëntenperspectief effectiviteit en veiligheid opdoseren |
- |
- |
- |
Bijwerking en hogere dosis nsAH n.s. in vergelijkin g tot standaard dosering |
75% van de ptn had ervaring met opdoseren. 40%, 42% en 54% rapporteerde significant voordeel van 2, 3, of4 tabletten respectievelijk. |
Ondersteuni ng aanbeveling om nsAH op te doseren. |
Retrospectieve studie (recall bias) |
|
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 21-12-2015
Beoordeeld op geldigheid : 03-12-2015
Algemene gegevens
Deelnemende verenigingen/instanties:
Nederlandse Vereniging voor Allergologie (NVvA)
Nederlands Huisartsen Genootschap (NHG)
Nederlandse Vereniging voor Kindergeneeskunde (NVK) - Huidpatiënten Nederland (HPN).
Financiering
Deze richtlijn is tot stand gekomen met financiële steun vanuit het SKMS-programma
Deze richtlijn is geautoriseerd door (beoogd):
Nederlandse Vereniging voor Allergologie (NVvA)
Nederlandse Vereniging voor Kindergeneeskunde (NVK)
Huidpatiënten Nederland (HPN)
Zorgverzekeraars Nederland (ZN)
Nefarma.
Aanleiding
Urticaria wordt gekenmerkt door het plotseling optreden van urticae (kwaddels), angio-oedeem of beide. Bij continue of terugkerende klachten van urticae en / of angio-oedeem gedurende meer dan zes weken wordt er gesproken van chronische urticaria. Chronische urticaria kan een zeer belastende aandoening zijn. Het is een huidziekte die resulteert in rode jeukende, soms verheven kwaddels (urticae) op de huid van verschillende omvang en vorm, meestal gepaard gaand met heftige jeuk. Ook kan er sprake zijn van diepe zwellingen (angio-oedeem). Patiënten met chronische urticaria kunnen vele kwaddels ontwikkelen en elke dag klachten hebben. Het kan vele jaren duren en kan grote invloed hebben op de kwaliteit van leven, zowel lichamelijk als emotioneel, alsook voor diens omgeving. De ziektelast van deze aandoening kan aanzienlijk zijn. Deze richtlijn bespreekt de huidige stand van zaken omtrent de nomenclatuur, bepaling van de ziektelast van chronische urticaria en de behandeling van chronische spontane urticaria.
Doel en doelgroep
Doel
Deze richtlijn is een document met aanbevelingen ter ondersteuning van de dagelijkse praktijkvoering en dient als leidraad voor de dagelijkse praktijk om zo de kwaliteit van de zorg voor alle patiënten met chronische urticaria te bevorderen. De richtlijn berust op de resultaten van wetenschappelijk onderzoek (‘evidence- based’) en aansluitende meningsvorming gericht op het vaststellen van goed medisch handelen. Deze richtlijn en de daarvan afgeleide documenten geven aanbevelingen over de nomenclatuur, bepaling van de ziektelast en behandeling van chronische spontane urticaria. Het doel van deze richtlijn is meer uniformiteit wat betreft laatstgenoemde aspecten te creëren, waardoor een betere afstemming, begeleiding en follow-up van patiënten door zorgaanbieders wordt bereikt. De ontwikkeling van deze richtlijn zal gefaseerd gelopen; in eerste instantie zullen alleen de nomenclatuur, de vragenlijsten omtrent kwaliteit van leven en ziekteactiviteit en de behandeling van chronische spontane urticaria aan bod komen.
Doelgroep
De doelgroep wordt gevormd door alle zorgaanbieders die werkzaam zijn op het gebied van chronische urticaria of betrokken zijn bij de behandeling van patiënten met chronische spontane urticaria. Dit betreft zowel de medische, paramedische als verpleegkundige beroepsgroepen.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn werd in 2014 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die met patiënten met chronische urticaria te maken hebben. Deelnemende verenigingen in de werkgroep zijn de Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV), de Nederlandse Vereniging voor Allergologie (NVvA), de Nederlandse Vereniging voor Kindergeneeskunde (NVK), het Nederlands Huisartsen Genootschap (NHG) en Huidpatiënten Nederland (HPN).
|
Werkgroepleden |
Vereniging |
|
Dr. A.C. Knulst (voorzitter) |
NVDV |
|
Dr. C. Nieuwhof |
NVvA |
|
Drs. M. Stadermann |
NVK |
|
Dr. R.A. Tupker |
NVDV |
|
Dr. M.B.A. van Doorn |
NVDV |
|
Drs. S.M. Franken |
NVDV |
|
Mevr. F. Das |
HPN |
|
Ds. W. Poldervaart |
HPN |
|
Drs. C. de Vries |
NHG |
|
Drs. M. van den Elzen |
Arts-onderzoeker UMCU |
|
Drs. E.J. van Zuuren |
NVDV |
|
Dr. J.J.E. van Everdingen |
Directeur NVDV |
|
Drs. M.C. Urgert (t / m half januari 2015) |
Arts-onderzoeker NVDV (secretariaat) |
|
Drs. W.R. Veldkamp (vanaf half januari 2015) |
Arts-onderzoeker NVDV (secretariaat) |
|
Drs. G.E. van der Kraaij (vanaf half maart 2015) |
Arts-onderzoeker NVDV (secretariaat) |
Inbreng patiëntenperspectief
Tijdens het vaststellen van de uitkomstmaten en het graderen hiervan volgens GRADE was er een patiënt aanwezig. Deze heeft ook actief bijgedragen tijdens de pressurecooker, met als doel het formuleren van de aanbevelingen.
Methode ontwikkeling
Evidence based
Implementatie
Bij het opstellen van deze richtlijn is veel aandacht besteed aan de implementatie en de praktische uitvoerbaarheid, effectiviteit, nut en noodzaak. De richtlijn wordt via het web verspreid onder alle relevante beroepsgroepen en ziekenhuizen en er zal in verschillende specifieke vaktijdschriften aandacht worden besteed aan de richtlijn. Tevens zal een samenvatting en patiëntenversie worden gemaakt. De voorlichtingsfolder van de NVDV zal worden afgestemd op de richtlijn.
Werkwijze
De werkgroep startte in 2014. In de voorbereidingsfase werd een ‘stakeholdersbijeenkomst’ georganiseerd. Hiervoor werden behalve de bovengenoemde partijen ook Zorgverzekeraars Nederland (ZN) en Nefarma uitgenodigd. Tijdens deze bijeenkomst werden de door de werkgroep opgestelde uitgangsvragen besproken en nader geëxpliceerd. Voor de ontwikkeling van deze richtlijn is gebruik gemaakt van zowel de EBRO-criteria als de GRADE-methode. Gekozen is om de therapeutische uitgangsvragen ciclosporine en omalizumab uit te werken volgens de GRADEmethode. Bij de GRADE-methode wordt wetenschappelijk bewijs beoordeeld aan de hand van uitkomstmaten. GRADE veronderstelt dat de werkgroep in het beginstadium van de richtlijnontwikkeling uitkomstmaten vaststelt. Een volledig uitleg over de GRADE-methode valt buiten het bestek van deze richtlijn, zie hiervoor het ‘GRADE handbook’ (Schünemann et al., 2013). Voor de twee uitgangsvragen die volgens GRADE zijn uitgewerkt, zijn tijdens de invitational conference patiënt-relevante uitkomstmaten bepaald en vervolgens ingedeeld in kritieke, belangrijke en minder belangrijke uitkomstmaten. De gekozen uitkomstmaten zijn als volgt:
- Verbetering ziekteactiviteit in vergelijking tot de baseline (cruciaal)
- Verbetering kwaliteit van leven in vergelijking tot de baseline (cruciaal)
- Proportie patiënten met bijwerkingen (cruciaal)
- Proportie patiënten met complete respons (belangrijk)
- Proportie patiënten met een partiële respons (belangrijk)
- Proportie angio-oedeem vrije dagen (belangrijk)
- Proportie patiënten met remissie binnen 1 maand (van beperkt belang).
Wetenschappelijke onderbouwing
Per uitgangsvraag werd een systematische search verricht in de databases PubMed, de Cochrane Database of Systematic Reviews en Cochrane Central Register of Controlled Trials), tenzij anders aangegeven. Ook werden relevante nationale en internationale richtlijnen aangaande chronische urticaria geraadpleegd, met name de recente internationale richtlijn ‘EAACI / GA2LEN / EDF / WAO guideline on urticaria, 2014’, ontwikkeld volgens AGREE methode, en de Amerikaanse richtlijn ‘The diagnosis and management of acute and chronic urticaria: 2014 update’ (Bernstein et al., 2014; Zuberbier et al., 2014). De zoekstrategie en resultaten van de searches zijn terug te vinden onder Zoekverantwoording en Evidencetabellen.
De volgende inclusie / exclusiecriteria zijn gebruikt, tenzij anders aangegeven:
|
Inclusiecriteria: |
Exclusiecriteria: |
|
Chronische spontane / idiopathische urticaria |
Acute urticaria |
|
Alle leeftijden |
Andere vormen van chronische urticaria |
|
Behandeling met het betreffende geneesmiddel |
Narrative reviews |
|
|
Case series / observationele studies met minder dan vijf patiënten |
|
|
Studies in andere taal dan Engels |
|
|
Studies met onvoldoende informatie over effectiviteit en / of veiligheid |
|
|
In vitro onderzoek |
|
|
Dubbele publicaties |
|
|
Onderzoek bij dieren. |
Na selectie van de literatuur bleven artikelen over die als onderbouwing bij de verschillende conclusies staan vermeld. De werkgroepleden beoordeelden de kwaliteit en inhoud ervan. Vervolgens schreven de werkgroepleden een paragraaf of module voor de conceptrichtlijn, waarin de beoordeelde literatuur werd verwerkt.
Bij de uitwerking van de uitgangsvragen volgens de GRADE-methode zijn de stappen beschreven in het ‘GRADE handbook’ nauwkeurig gevolgd (Schünemann et al. 2013). Tevens is gebruik gemaakt van ‘the Cochrane Handbook for Systematic Reviews of Intervention’ voor het uitwerken van de uitgangsvragen en voor het verrichten van de meta-analyses (Higgins and Green 2011).
Elke module van de richtlijn is volgens een vast stramien opgebouwd, dat onderstaand is weergegeven. Een van de doelen is om een richtlijn zo transparant mogelijk te laten zijn, zodat elke gebruiker kan zien op welke literatuur en overwegingen bepaalde aanbevelingen zijn gebaseerd.
Uitgangsvraag
Een uitgangsvraag is een klinisch relevante vraag waarop tijdens de richtlijnontwikkeling een antwoord wordt geformuleerd.
Inleiding
Een korte introductie op de achtergrond van de uitgangsvraag.
Wetenschappelijke onderbouwing
Per uitgangsvraag is beknopt de zoekstrategie en de uitkomst hiervan beschreven. Meer gedetailleerde informatie over de zoekstrategie is beschreven in de Zoekverantwoording.
Samenvatting van de literatuur
De antwoorden op de uitgangsvragen zijn voor zover mogelijk gebaseerd op gepubliceerd wetenschappelijk onderzoek. De geselecteerde artikelen zijn door de schrijvende werkgroepleden beoordeeld op kwaliteit van het onderzoek en gegradeerd naar mate van bewijs, waarbij gebruik gemaakt is van de GRADE-methode en van de EBRO-methode. Voor de indeling van methodologische kwaliteit van studies volgens EBRO en GRADE zie tabel 1 en 4. Beschrijving en beschouwing van de gepubliceerde artikelen zijn indien van toepassing te vinden onder het kopje ‘samenvatting van de literatuur’. Meer gedetailleerde informatie is beschreven in de Evidencetabellen.
Conclusie
Het wetenschappelijk materiaal is samengevat in een conclusie, waarbij het niveau van het meest relevante bewijs is weergegeven. Voor het niveau van conclusies volgens EBRO en GRADE zie tabel 2 en 5.
Overige overwegingen
Voor het komen tot een aanbeveling zijn er naast het wetenschappelijke bewijs vaak andere aspecten van belang, bijvoorbeeld: patiënten voorkeuren, beschikbaarheid van speciale technieken of expertise, organisatorische aspecten, maatschappelijke consequenties of kosten. Ook bijwerkingen werden hierin meegenomen, voor zover die niet reeds uit wetenschappelijke literatuur waren gedestilleerd en waarvoor dan wel andere bronnen beschikbaar waren. In de overige overwegingen worden de conclusies op basis van de literatuur geplaatst in de context van de dagelijkse praktijk en vindt een afweging plaats van de voor- en nadelen van de verschillende beleidsopties.
Aanbeveling
De uiteindelijk geformuleerde aanbeveling is het resultaat van het beschikbare bewijs in combinatie met deze overwegingen. Het volgen van deze procedure en het opstellen van de richtlijn in dit ‘format’ heeft als doel de transparantie van de richtlijn te verhogen. Het biedt ruimte voor een efficiënte discussie tijdens de werkgroep vergaderingen en vergroot bovendien de helderheid voor de gebruiker van de richtlijn. Voor de gebruikte niveaus van aanbevelingen volgens EBRO en GRADE zie tabel 3 en 6.
Uitwerking volgens de EBRO-methode
Tabel 1: Indeling van methodologische kwaliteit van individuele studies volgens EBRO
|
Kwaliteit |
Interventie |
Diagnostisch accuratesse onderzoek |
Schade / bijwerkingen*, etiologie, prognose |
|
A1 |
Systematische review van tenminste twee onafhankelijk van elkaar uitgevoerde onderzoeken van A2-niveau |
||
|
A2
|
Gerandomiseerd dubbelblind vergelijkend klinisch onderzoek van goede kwaliteit van voldoende omvang |
Onderzoek ten opzichte van een referentietest (een ‘gouden standaard’) met tevoren gedefinieerde afkapwaarden en onafhankelijke beoordeling van de resultaten van test en gouden standaard, betreffende een voldoende grote serie van opeenvolgende patiënten die allen de index- en referentietest hebben gehad |
Prospectief cohort onderzoek van voldoende omvang en follow-up, waarbij adequaat gecontroleerd is voor ‘confounding’ en selectieve follow-up voldoende is uitgesloten. |
|
B |
Vergelijkend onderzoek, maar niet met alle kenmerken als genoemd onder A2 (hieronder valt ook patiënt-controle onderzoek, cohortonderzoek) |
Onderzoek ten opzichte van een referentietest, maar niet met alle kenmerken die onder A2 zijn genoemd |
Prospectief cohort onderzoek, maar niet met alle kenmerken als genoemd onder A2 of retrospectief cohort onderzoek of patiënt-controle onderzoek |
|
C |
Niet-vergelijkend onderzoek |
||
|
D |
Mening van deskundigen |
||
* Deze classificatie is alleen van toepassing in situaties waarin om ethische of andere redenen gecontroleerde trials niet mogelijk zijn. Zijn die wel mogelijk dan geldt de classificatie voor interventies.
Tabel 2: Niveau van conclusies volgens EBRO
|
Niveau |
Conclusie gebaseerd op |
|
1 |
Onderzoek van niveau A1 of tenminste twee onafhankelijk van elkaar uitgevoerde onderzoeken van niveau A2 |
|
2 |
Eén onderzoek van niveau A2 of tenminste twee onafhankelijk van elkaar uitgevoerde onderzoeken van niveau B |
|
3 |
Eén onderzoek van niveau B of C |
|
4 |
Mening van deskundigen |
Tabel 3: Niveau van aanbeveling volgens EBRO
|
Aanbeveling |
Balans |
|
Sterk positief |
De interventie doet duideljk meer goed dan kwaad: Doe…. |
|
Zwak positief |
Het is onzeker of alle patienten gebaat zijn bij de interventie: doe bij voorkeur…. |
|
Zwak negatief |
Het is onzeker of alle patienten gebaat zijn bij de interventie: doe bij voorkeur niet…. |
|
Sterk negatief |
De interventie doet meer kwaad dan goed: doe niet…. |
Uitwerking volgens de GRADE-methode
Tabel 4: Indeling van methodologische kwaliteit van studies volgens GRADE
|
|
GRADE systeem |
|
Type bewijs |
Gerandomiseerd onderzoek = hoog Observationele studie = laag Elk ander bewijs = zeer laag |
|
Factoren die de kwaliteit van bewijs kunnen verlagen*: |
- Ernstige of zeer ernstige beperkingen in de kwaliteit van de studie - Indirectheid van het bewijs - Belangrijke inconsistentie tussen studies - Imprecisie - Grote kans op ‘publicatiebias’ |
|
Factoren die de kwaliteit van bewijs kunnen verhogen**: |
- Sterk bewijs voor een associatie—significant relatief risico van > 2 ( < 0,5) gebaseerd op consistent bewijs uit twee of meer observationele studies, zonder plausibele ‘confounders’ (+1) - Zeer sterk bewijs voor een associatie—significant relatief risico van > 5 ( < 0,2) gebaseerd op direct bewijs zonder belangrijke bedreigingen voor de validiteit (+2) - Bewijs voor een dosis respons gradiënt (+1) - Alle plausibele ‘confounders’ zouden het effect hebben verminderd (+1) |
*Elk criterium kan de kwaliteit verminderen met 1 stap of bij zeer ernstige beperkingen met twee stappen. ** Verhogen kan alleen indien er geen beperkingen zijn t.a.v. de studiekwaliteit, imprecisie, inconsistentie, indirectheid en publicatiebias.
Tabel 5: Niveau van conclusies volgens GRADE
|
Conclusie - Hoog = nader onderzoek zal zeer onwaarschijnlijk het vertrouwen in de inschatting van een effect veranderen - Middelmatig = nader onderzoek zal waarschijnlijk een belangrijke invloed hebben op het vertrouwen in de inschatting van een effect en kan de inschatting van een effect veranderen - Laag = nader onderzoek zal zeer waarschijnlijk een belangrijke invloed hebben op het vertrouwen in de inschatting van een effect en zal waarschijnlijk de inschatting van een effect veranderen - Zeer laag = elke inschatting van een effect is zeer onzeker |
Tabel 6: Niveau van aanbevelingen volgens GRADE
|
Klinische aanbeveling - Sterk voor/tegen = als clinici, gebaseerd op het beschikbare bewijs, zeer zeker zijn dat de voordelen de nadelen of risico’s overtreffen, of andersom, dan zal er een sterke aanbeveling worden gedaan - Zwak voor/tegen = als clinici, gebaseerd op het beschikbare bewijs, denken dat de voordelen en de nadelen of risico’s in balans zijn of als er een bepaalde onzekerheid bestaat over de grootte van de voordelen en risico’s, moeten ze een zwakke aanbeveling maken |
Zoekverantwoording