Behandeling/Stepped-care - Spontane urticaria
Uitgangsvraag
Wat is de behandeling van chronische spontane urticaria, en kan hier een stepped care model voor worden gemaakt?
Aanbeveling
Samenvatting aanbevelingen behandeling chronische spontane urticaria
Op basis van analyse van de beschikbare literatuur en de overige overwegingen van de werkgroep van de onderliggende hoofdstukken beveelt de werkgroep het volgende stepped-care model aan voor de behandeling van CSU (zie de onderstaande afbeelding).
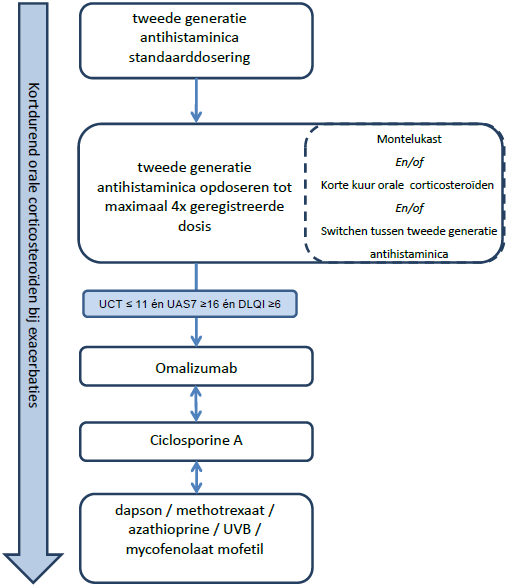
Stepped-care model
- Stap 1: geregistreerde dosis tweede generatie antihistaminica: goede werkzaamheid, zeer goed veiligheidsprofiel, lage kosten
- Stap 2: maximaal 4 keer geregistreerde dosis tweede generatie antihistaminicum. Goede kwaliteit van bewijs voor effectiviteit, goed veiligheidsprofiel, lage kosten. Offlabel
- Ter overweging toevoegen aan stap 2: Montelukast: zeer lage kwaliteit van bewijs voor matige effectiviteit, goede veiligheid, lage kosten. Offlabel
- Ter overweging kortdurend toe te voegen aan alle stappen: orale corticosteroïden: goede werkzaamheid tijdens inname, goed veiligheidsprofiel bij een korte kuur, lage kosten. Aanzienlijke bijwerkingen zijn te verwachten bij langdurige behandeling
- Switchen van tweede generatie antihistaminicum: zeer lage kwaliteit van bewijs voor effectiviteit, in individuele gevallen werkzaam (expert opinion werkgroep), goed veiligheidsprofiel, lage kosten. In het geval van bijwerkingen kan overwogen worden eerst te switchen alvorens op te doseren.
- Stap 3: Omalizumab: hoge kwaliteit van bewijs voor effectiviteit, goed veiligheidsprofiel op korte termijn, hoge kosten.
- Aanbevolen wordt om niet eerder dan zes maanden na de eerste manifestatie van CSU met omalizumab te starten
- Stap 4: Ciclosporine A: lage kwaliteit van bewijs voor effectiviteit, matig veiligheidsprofiel en hoge kosten. Offlabel.
- Stap 5: Overige therapieën: dapson, methotrexaat, azathioprine, UVB en mycofenolaat mofetil: Zeer lage kwaliteit van bewijs voor effectiviteit.
Het wordt aanbevolen om vanaf stap 3 in het stepped-care model de effectiviteit van de therapie elke 3-6 maanden te herevalueren. Voor nadere informatie wordt verwezen naar de hoofdstukken waarin de betreffende middelen worden behandeld.
Overwegingen
In de internationale richtlijn (Zuberbier et al., 2014) wordt in het stepped care plan geen verschil gemaakt tussenbehandeling met montelukast als add-on medicatie bij tweede generatie antihistaminica en omalizumab en ciclosporine A (CsA). Uit een enkele blinde, gerandomiseerde studie (Wan, 2009) blijkt mogelijke effectiviteit van montelukast als een additionele optie bij tot 2x de geregistreerde dosis tweede generatie antihistaminica. Daarnaast is de veiligheid hoog en de kosten relatief laag, in vergelijking met omalizumab en CsA.
Ook wordt in de internationale richtlijn het additioneel geven van een korte kuur orale corticosteroïden bij opgedoseerde tweede generatie antihistaminica (losstaand van het geven van dit middel bij exacerbaties) in dezelfde stap genoemd als omalizumab en CsA. Er zijn aanwijzingen dat met een korte kuur add-on corticosteroïden de ziekte mogelijk voor langere tijd (deels) onderdrukt kan worden, (matige kwaliteit van bewijs in de literatuur (Asero & Tedeschi, 2010)) en zo dus voorkomen kan worden dat een volgende stap in het stepped care model onnodig doorlopen wordt. Net als montelukast zijn orale corticosteroïden relatief goedkoop.
Tenslotte wordt er in de internationale richtlijn niet gesproken over het al dan niet switchen tussen de diverse tweede generatie antihistaminica. In de literatuur zijn aanwijzingen dat het switchen tussen desloratadine en levocetirizine een positief effect kan hebben op de klachten. Echter het bewijs hiervoor berust op een subanalyse van één studie (Staevska et al., 2010), en is daardoor van mindere kwaliteit dan het opdoseren tot 4x de geregistreerde dosis. De ervaring van de werkgroepleden is dat switchen tussen de andere tweede generatie antihistaminica bij sommige patiënten ook effectief kan zijn. In het geval van bijwerkingen kan overwogen worden te switchen naar een ander antihistaminicum voordat de dosering verhoogd wordt.
Op basis van de bovengenoemde argumenten pleit de werkgroep ervoor het voorschrijven van montelukast of een korte kuur orale corticosteroïden, of het switchen tussen de verschillende tweede generatie antihistaminica in het stepped care plan op te nemen als optionele ‘side-step’ naast een opgedoseerde tweede generatie antihistaminicum. Daarmee wordt ervoor gekozen af te wijken van de internationale richtlijn.
De internationale richtlijn geeft als derde stap in de behandeling de keuze tussen onder andere ciclosporine en omalizumab, maar geeft hier verder geen richting aan. Op basis van ons aanvullende literatuuronderzoek volgens de GRADE methodiek naar zowel de effectiviteit en veiligheid van CsA en omalizumab bij CSU, heeft de werkgroep gemeend er goed aan te doen het stepped-care model verder uit te werken. Qua effectiviteit is er lage kwaliteit van bewijs voor een gunstig effect van CsA tegen hoge kwaliteit van bewijs voor een gunstig effect van omalizumab. Qua veiligheid is er lage kwaliteit van bewijs voor weinig bijwerkingen bij CsA en hoge kwaliteit van bewijs voor weinig bijwerkingen bij omalizumab. CsA is qua directe kosten goedkoper dan omalizumab, maar zijn er aanwijzingen dat de indirecte kosten (o.a. gerelateerd aan de bijwerkingen van het voorgeschreven middel) bij CsA hoger liggen dan bij omalizumab. Tenslotte is omalizumab geregistreerd voor CSU terwijl CsA offlabel voorgeschreven moet worden.
Op basis van deze argumenten is er gekozen omalizumab vóór CsA te stellen, maar waarbij op basis van uitgesproken persoonlijke wensen van de patiënt wel ruimte is voor behandeling met CsA.
De werkgroep vindt dat in het doorlopen van de stap van opgedoseerde tweede generatie antihistaminica naar omalizumab (of CsA) de ziekte-ernst in acht genomen moet worden. Op basis van nationale en internationale expert opinion en de te verwachtte grootte van de verbetering van kwaliteit van leven en klachtenverbetering stelt de werkgroep dat het pas nuttig lijkt met deze middelen te behandelen vanaf matige ziekte-ernst. De afkapwaarden die hiervoor in de literatuur genoemd worden zijn een UCT lager dan 12, een UAS7 van 16 of hoger en een DLQI van 6 of hoger.
De werkgroep adviseert niet te snel te starten met omalizumab vanwege de kans op spontane remissie, het ontbreken van bewijs van effectiviteit en veiligheid op de lange termijn en de kosten.
Over het algemeen wordt niet aanbevolen binnen een halfjaar na de eerste manifestatie van de ziekte te starten met omalizumab gezien de kans op spontane remissie.
In de internationale en Amerikaanse richtlijn (Zuberbier et al., 2014; Bernstein et al., 2014) wordt niets genoemd over het eventuele moment van staken van omalizumab. Gezien de kosten en de kans een eventuele spontane remissie onder omalizumab heeft de werkgroep besloten hier wel enkele (expert opinion) aanbevelingen over te doen.
Bij aanvang van de therapie en vervolgens om de drie maanden dient de UAS7 afgenomen te worden.
Bij een (vrijwel) complete remissie wordt aanbevolen de therapie aan te passen. Bij gebrek aan bewijs in de literatuur beveelt de werkgroep aan, op basis van expert opinion, om het interval tussen de behandelingen met stappen van één week te verlengen tot 8 weken en vervolgens de therapie te staken.
Is er na drie maanden geen effect van de behandeling met omalizumab dan moet worden overwogen de behandeling aan te passen. De expert opinion van de werkgroep is om in dit geval de dosis te verhogen of het interval te verkorten.
Omalizumab is een add-on therapie. De verhoogde dosis antihistaminica is de basis van de behandeling en wordt tijdens de behandeling met omalizumab gecontinueerd, mits dit door de patiënt verdragen wordt.
Mochten omalizumab en CsA (stap 3 en 4) gecontra-indiceerd zijn, bijwerkingen hebben of onvoldoende effect sorteren, dan kan er als alternatief gekozen worden voor één van de overige middelen als diafenylsulfon (Dapson), methotrexaat, UVB, azathioprine, intraveneuze immunoglobulinen en mycofenolaat mofetil.
Indien er bij patiënten op systemische immuunsuppressiva besloten wordt om te switchen naar omalizumab, kan worden overwogen eerst omalizumab te starten en in tweede instantie de immuunsuppressiva af te bouwen, om een exacerbatie te voorkomen.
Onderbouwing
Achtergrond
In deze modules presenteert de werkgroep de aanbevolen stepped-care behandeling van CSU. De werkgroep heeft de effectiviteit en veiligheid zo veel mogelijk per behandelmogelijkheid in kaart gebracht. Voor de meest gangbare behandelmogelijkheden van CSU zijn aparte sub uitgangsvragen gedefinieerd, die in aparte modules worden besproken.
Behandeldoel
Het behandeldoel van CSU wordt besproken in de recente internationale richtlijn chronische urticaria (Zuberbier et al., 2014). De aanbeveling om altijd te streven naar complete controle van symptomen wordt door de werkgroep niet overgenomen. Deze aanbeveling is gebaseerd op de huidige definitie van de WHO waarin wordt gesteld dat gezondheid ’een toestand van volledig fysiek, geestelijk en sociaal welbevinden en niet louter het ontbreken van ziekte of gebrek is‘.
De werkgroep is echter van mening dat per patiënt en in overleg met de patiënt bepaald dient te worden wat het behandeldoel is en wanneer dit behandeldoel behaald is. De symptomen van een patiënt met een chronische aandoening die met medicatie wordt onderdrukt kan immers ook een hoge kwaliteit van leven hebben als de symptomen niet volledig worden onderdrukt. Het is altijd een afweging van voor- en nadelen, waarbij de nadelen in de vorm van bijwerkingen, patiënten ongemak en kosten verbonden aan medicatie, soms groter zijn dan de voordelen van volledige onderdrukking.
Om tot een advies voor de behandeling van CSU te komen is deze uitgangsvraag uitgesplitst in de volgende (sub)uitgangsvragen:
- Wat is de effectiviteit en veiligheid van het opdoseren van tweede generatie antihistaminica tot vier maal de standaard dosering bij de behandeling van chronische spontane urticaria?
- Wat is de effectiviteit en veiligheid van leukotriënen antagonisten in de behandeling van chronische spontane urticaria?
- Wat is de effectiviteit en veiligheid van ciclosporine in de behandeling van chronische spontane urticaria?
- Wat is de effectiviteit en veiligheid van omalizumab in de behandeling van chronische spontane urticaria?
- Wat is de effectiviteit en veiligheid van orale corticosteroïden in de behandeling van chronische spontane urticaria?
De uitwerkingen van deze vragen zijn in de submodules terug te vinden.
Conclusies / Summary of Findings
Voor de conclusies per behandelmodaliteit wordt verwezen naar de onderliggende modules.
Referenties
- Asero R, & Tedeschi A. 2010. Usefulness of a short course of oral prednisone in antihistamine-resistant chronic urticaria: a retrospective analysis. J. Investig. Allergol. Clin. Immunol. 20 (5): 386-390.
- Bernstein JA, Lang DM, Khan DA, Craig T, Dreyfus D, Hsieh F, Sheikh J, Weldon D, Zuraw B, Bernstein DI, Blessing-Moore J, Cox L, Nicklas RA, Oppenheimer J, Portnoy JM, Randolph CR, Schuller DE, Spector SL, Tilles SA, and Wallace D. 2014. The diagnosis and management of acute and chronic urticaria: 2014 update. J. Allergy Clin. Immunol. 133 (5): 1270-1277.
- Staevska M, Popov TA, Kralimarkova T, Lazarova C, Kraeva S, Popova D, Church DS, Dimitrov V, and Church MK. 2010. The effectiveness of levocetirizine and desloratadine in up to 4 times conventional doses in difficult-to-treat urticaria. J. Allergy Clin. Immunol. 125 (3): 676-682.
- Wan KS. 2009. Efficacy of leukotriene receptor antagonist with an anti-H1 receptor antagonist for treatment of chronic idiopathic urticaria. J. Dermatolog. Treat. 20 (4): 194-197.
- Zuberbier T, Aberer W, Asero R, Bindslev-Jensen C, Brzoza Z, Canonica GW, Church MK, Ensina LF, Gimenez-Arnau A, Godse K, Goncalo M, Grattan C, Hebert J, Hide M, Kaplan A, Kapp A, Abdul Latiff AH, Mathelier-Fusade P, Metz M, Nast A, Saini SS, Sanchez-Borges M, Schmid-Grendelmeier P, Simons FE, Staubach P, Sussman G, Toubi E, Vena GA, Wedi B, Zhu XJ, and Maurer M. 2014. The EAACI / GA2LEN / EDF / WAO Guideline for the definition, classification, diagnosis, and management of urticaria: the 2013 revision and update. Allergy 69(7): 868887.
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 21-12-2015
Beoordeeld op geldigheid : 03-12-2015
Algemene gegevens
Deelnemende verenigingen/instanties:
Nederlandse Vereniging voor Allergologie (NVvA)
Nederlands Huisartsen Genootschap (NHG)
Nederlandse Vereniging voor Kindergeneeskunde (NVK) - Huidpatiënten Nederland (HPN).
Financiering
Deze richtlijn is tot stand gekomen met financiële steun vanuit het SKMS-programma
Deze richtlijn is geautoriseerd door (beoogd):
Nederlandse Vereniging voor Allergologie (NVvA)
Nederlandse Vereniging voor Kindergeneeskunde (NVK)
Huidpatiënten Nederland (HPN)
Zorgverzekeraars Nederland (ZN)
Nefarma.
Aanleiding
Urticaria wordt gekenmerkt door het plotseling optreden van urticae (kwaddels), angio-oedeem of beide. Bij continue of terugkerende klachten van urticae en / of angio-oedeem gedurende meer dan zes weken wordt er gesproken van chronische urticaria. Chronische urticaria kan een zeer belastende aandoening zijn. Het is een huidziekte die resulteert in rode jeukende, soms verheven kwaddels (urticae) op de huid van verschillende omvang en vorm, meestal gepaard gaand met heftige jeuk. Ook kan er sprake zijn van diepe zwellingen (angio-oedeem). Patiënten met chronische urticaria kunnen vele kwaddels ontwikkelen en elke dag klachten hebben. Het kan vele jaren duren en kan grote invloed hebben op de kwaliteit van leven, zowel lichamelijk als emotioneel, alsook voor diens omgeving. De ziektelast van deze aandoening kan aanzienlijk zijn. Deze richtlijn bespreekt de huidige stand van zaken omtrent de nomenclatuur, bepaling van de ziektelast van chronische urticaria en de behandeling van chronische spontane urticaria.
Doel en doelgroep
Doel
Deze richtlijn is een document met aanbevelingen ter ondersteuning van de dagelijkse praktijkvoering en dient als leidraad voor de dagelijkse praktijk om zo de kwaliteit van de zorg voor alle patiënten met chronische urticaria te bevorderen. De richtlijn berust op de resultaten van wetenschappelijk onderzoek (‘evidence- based’) en aansluitende meningsvorming gericht op het vaststellen van goed medisch handelen. Deze richtlijn en de daarvan afgeleide documenten geven aanbevelingen over de nomenclatuur, bepaling van de ziektelast en behandeling van chronische spontane urticaria. Het doel van deze richtlijn is meer uniformiteit wat betreft laatstgenoemde aspecten te creëren, waardoor een betere afstemming, begeleiding en follow-up van patiënten door zorgaanbieders wordt bereikt. De ontwikkeling van deze richtlijn zal gefaseerd gelopen; in eerste instantie zullen alleen de nomenclatuur, de vragenlijsten omtrent kwaliteit van leven en ziekteactiviteit en de behandeling van chronische spontane urticaria aan bod komen.
Doelgroep
De doelgroep wordt gevormd door alle zorgaanbieders die werkzaam zijn op het gebied van chronische urticaria of betrokken zijn bij de behandeling van patiënten met chronische spontane urticaria. Dit betreft zowel de medische, paramedische als verpleegkundige beroepsgroepen.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn werd in 2014 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die met patiënten met chronische urticaria te maken hebben. Deelnemende verenigingen in de werkgroep zijn de Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV), de Nederlandse Vereniging voor Allergologie (NVvA), de Nederlandse Vereniging voor Kindergeneeskunde (NVK), het Nederlands Huisartsen Genootschap (NHG) en Huidpatiënten Nederland (HPN).
|
Werkgroepleden |
Vereniging |
|
Dr. A.C. Knulst (voorzitter) |
NVDV |
|
Dr. C. Nieuwhof |
NVvA |
|
Drs. M. Stadermann |
NVK |
|
Dr. R.A. Tupker |
NVDV |
|
Dr. M.B.A. van Doorn |
NVDV |
|
Drs. S.M. Franken |
NVDV |
|
Mevr. F. Das |
HPN |
|
Ds. W. Poldervaart |
HPN |
|
Drs. C. de Vries |
NHG |
|
Drs. M. van den Elzen |
Arts-onderzoeker UMCU |
|
Drs. E.J. van Zuuren |
NVDV |
|
Dr. J.J.E. van Everdingen |
Directeur NVDV |
|
Drs. M.C. Urgert (t / m half januari 2015) |
Arts-onderzoeker NVDV (secretariaat) |
|
Drs. W.R. Veldkamp (vanaf half januari 2015) |
Arts-onderzoeker NVDV (secretariaat) |
|
Drs. G.E. van der Kraaij (vanaf half maart 2015) |
Arts-onderzoeker NVDV (secretariaat) |
Inbreng patiëntenperspectief
Tijdens het vaststellen van de uitkomstmaten en het graderen hiervan volgens GRADE was er een patiënt aanwezig. Deze heeft ook actief bijgedragen tijdens de pressurecooker, met als doel het formuleren van de aanbevelingen.
Methode ontwikkeling
Evidence based
Implementatie
Bij het opstellen van deze richtlijn is veel aandacht besteed aan de implementatie en de praktische uitvoerbaarheid, effectiviteit, nut en noodzaak. De richtlijn wordt via het web verspreid onder alle relevante beroepsgroepen en ziekenhuizen en er zal in verschillende specifieke vaktijdschriften aandacht worden besteed aan de richtlijn. Tevens zal een samenvatting en patiëntenversie worden gemaakt. De voorlichtingsfolder van de NVDV zal worden afgestemd op de richtlijn.
Werkwijze
De werkgroep startte in 2014. In de voorbereidingsfase werd een ‘stakeholdersbijeenkomst’ georganiseerd. Hiervoor werden behalve de bovengenoemde partijen ook Zorgverzekeraars Nederland (ZN) en Nefarma uitgenodigd. Tijdens deze bijeenkomst werden de door de werkgroep opgestelde uitgangsvragen besproken en nader geëxpliceerd. Voor de ontwikkeling van deze richtlijn is gebruik gemaakt van zowel de EBRO-criteria als de GRADE-methode. Gekozen is om de therapeutische uitgangsvragen ciclosporine en omalizumab uit te werken volgens de GRADEmethode. Bij de GRADE-methode wordt wetenschappelijk bewijs beoordeeld aan de hand van uitkomstmaten. GRADE veronderstelt dat de werkgroep in het beginstadium van de richtlijnontwikkeling uitkomstmaten vaststelt. Een volledig uitleg over de GRADE-methode valt buiten het bestek van deze richtlijn, zie hiervoor het ‘GRADE handbook’ (Schünemann et al., 2013). Voor de twee uitgangsvragen die volgens GRADE zijn uitgewerkt, zijn tijdens de invitational conference patiënt-relevante uitkomstmaten bepaald en vervolgens ingedeeld in kritieke, belangrijke en minder belangrijke uitkomstmaten. De gekozen uitkomstmaten zijn als volgt:
- Verbetering ziekteactiviteit in vergelijking tot de baseline (cruciaal)
- Verbetering kwaliteit van leven in vergelijking tot de baseline (cruciaal)
- Proportie patiënten met bijwerkingen (cruciaal)
- Proportie patiënten met complete respons (belangrijk)
- Proportie patiënten met een partiële respons (belangrijk)
- Proportie angio-oedeem vrije dagen (belangrijk)
- Proportie patiënten met remissie binnen 1 maand (van beperkt belang).
Wetenschappelijke onderbouwing
Per uitgangsvraag werd een systematische search verricht in de databases PubMed, de Cochrane Database of Systematic Reviews en Cochrane Central Register of Controlled Trials), tenzij anders aangegeven. Ook werden relevante nationale en internationale richtlijnen aangaande chronische urticaria geraadpleegd, met name de recente internationale richtlijn ‘EAACI / GA2LEN / EDF / WAO guideline on urticaria, 2014’, ontwikkeld volgens AGREE methode, en de Amerikaanse richtlijn ‘The diagnosis and management of acute and chronic urticaria: 2014 update’ (Bernstein et al., 2014; Zuberbier et al., 2014). De zoekstrategie en resultaten van de searches zijn terug te vinden onder Zoekverantwoording en Evidencetabellen.
De volgende inclusie / exclusiecriteria zijn gebruikt, tenzij anders aangegeven:
|
Inclusiecriteria: |
Exclusiecriteria: |
|
Chronische spontane / idiopathische urticaria |
Acute urticaria |
|
Alle leeftijden |
Andere vormen van chronische urticaria |
|
Behandeling met het betreffende geneesmiddel |
Narrative reviews |
|
|
Case series / observationele studies met minder dan vijf patiënten |
|
|
Studies in andere taal dan Engels |
|
|
Studies met onvoldoende informatie over effectiviteit en / of veiligheid |
|
|
In vitro onderzoek |
|
|
Dubbele publicaties |
|
|
Onderzoek bij dieren. |
Na selectie van de literatuur bleven artikelen over die als onderbouwing bij de verschillende conclusies staan vermeld. De werkgroepleden beoordeelden de kwaliteit en inhoud ervan. Vervolgens schreven de werkgroepleden een paragraaf of module voor de conceptrichtlijn, waarin de beoordeelde literatuur werd verwerkt.
Bij de uitwerking van de uitgangsvragen volgens de GRADE-methode zijn de stappen beschreven in het ‘GRADE handbook’ nauwkeurig gevolgd (Schünemann et al. 2013). Tevens is gebruik gemaakt van ‘the Cochrane Handbook for Systematic Reviews of Intervention’ voor het uitwerken van de uitgangsvragen en voor het verrichten van de meta-analyses (Higgins and Green 2011).
Elke module van de richtlijn is volgens een vast stramien opgebouwd, dat onderstaand is weergegeven. Een van de doelen is om een richtlijn zo transparant mogelijk te laten zijn, zodat elke gebruiker kan zien op welke literatuur en overwegingen bepaalde aanbevelingen zijn gebaseerd.
Uitgangsvraag
Een uitgangsvraag is een klinisch relevante vraag waarop tijdens de richtlijnontwikkeling een antwoord wordt geformuleerd.
Inleiding
Een korte introductie op de achtergrond van de uitgangsvraag.
Wetenschappelijke onderbouwing
Per uitgangsvraag is beknopt de zoekstrategie en de uitkomst hiervan beschreven. Meer gedetailleerde informatie over de zoekstrategie is beschreven in de Zoekverantwoording.
Samenvatting van de literatuur
De antwoorden op de uitgangsvragen zijn voor zover mogelijk gebaseerd op gepubliceerd wetenschappelijk onderzoek. De geselecteerde artikelen zijn door de schrijvende werkgroepleden beoordeeld op kwaliteit van het onderzoek en gegradeerd naar mate van bewijs, waarbij gebruik gemaakt is van de GRADE-methode en van de EBRO-methode. Voor de indeling van methodologische kwaliteit van studies volgens EBRO en GRADE zie tabel 1 en 4. Beschrijving en beschouwing van de gepubliceerde artikelen zijn indien van toepassing te vinden onder het kopje ‘samenvatting van de literatuur’. Meer gedetailleerde informatie is beschreven in de Evidencetabellen.
Conclusie
Het wetenschappelijk materiaal is samengevat in een conclusie, waarbij het niveau van het meest relevante bewijs is weergegeven. Voor het niveau van conclusies volgens EBRO en GRADE zie tabel 2 en 5.
Overige overwegingen
Voor het komen tot een aanbeveling zijn er naast het wetenschappelijke bewijs vaak andere aspecten van belang, bijvoorbeeld: patiënten voorkeuren, beschikbaarheid van speciale technieken of expertise, organisatorische aspecten, maatschappelijke consequenties of kosten. Ook bijwerkingen werden hierin meegenomen, voor zover die niet reeds uit wetenschappelijke literatuur waren gedestilleerd en waarvoor dan wel andere bronnen beschikbaar waren. In de overige overwegingen worden de conclusies op basis van de literatuur geplaatst in de context van de dagelijkse praktijk en vindt een afweging plaats van de voor- en nadelen van de verschillende beleidsopties.
Aanbeveling
De uiteindelijk geformuleerde aanbeveling is het resultaat van het beschikbare bewijs in combinatie met deze overwegingen. Het volgen van deze procedure en het opstellen van de richtlijn in dit ‘format’ heeft als doel de transparantie van de richtlijn te verhogen. Het biedt ruimte voor een efficiënte discussie tijdens de werkgroep vergaderingen en vergroot bovendien de helderheid voor de gebruiker van de richtlijn. Voor de gebruikte niveaus van aanbevelingen volgens EBRO en GRADE zie tabel 3 en 6.
Uitwerking volgens de EBRO-methode
Tabel 1: Indeling van methodologische kwaliteit van individuele studies volgens EBRO
|
Kwaliteit |
Interventie |
Diagnostisch accuratesse onderzoek |
Schade / bijwerkingen*, etiologie, prognose |
|
A1 |
Systematische review van tenminste twee onafhankelijk van elkaar uitgevoerde onderzoeken van A2-niveau |
||
|
A2
|
Gerandomiseerd dubbelblind vergelijkend klinisch onderzoek van goede kwaliteit van voldoende omvang |
Onderzoek ten opzichte van een referentietest (een ‘gouden standaard’) met tevoren gedefinieerde afkapwaarden en onafhankelijke beoordeling van de resultaten van test en gouden standaard, betreffende een voldoende grote serie van opeenvolgende patiënten die allen de index- en referentietest hebben gehad |
Prospectief cohort onderzoek van voldoende omvang en follow-up, waarbij adequaat gecontroleerd is voor ‘confounding’ en selectieve follow-up voldoende is uitgesloten. |
|
B |
Vergelijkend onderzoek, maar niet met alle kenmerken als genoemd onder A2 (hieronder valt ook patiënt-controle onderzoek, cohortonderzoek) |
Onderzoek ten opzichte van een referentietest, maar niet met alle kenmerken die onder A2 zijn genoemd |
Prospectief cohort onderzoek, maar niet met alle kenmerken als genoemd onder A2 of retrospectief cohort onderzoek of patiënt-controle onderzoek |
|
C |
Niet-vergelijkend onderzoek |
||
|
D |
Mening van deskundigen |
||
* Deze classificatie is alleen van toepassing in situaties waarin om ethische of andere redenen gecontroleerde trials niet mogelijk zijn. Zijn die wel mogelijk dan geldt de classificatie voor interventies.
Tabel 2: Niveau van conclusies volgens EBRO
|
Niveau |
Conclusie gebaseerd op |
|
1 |
Onderzoek van niveau A1 of tenminste twee onafhankelijk van elkaar uitgevoerde onderzoeken van niveau A2 |
|
2 |
Eén onderzoek van niveau A2 of tenminste twee onafhankelijk van elkaar uitgevoerde onderzoeken van niveau B |
|
3 |
Eén onderzoek van niveau B of C |
|
4 |
Mening van deskundigen |
Tabel 3: Niveau van aanbeveling volgens EBRO
|
Aanbeveling |
Balans |
|
Sterk positief |
De interventie doet duideljk meer goed dan kwaad: Doe…. |
|
Zwak positief |
Het is onzeker of alle patienten gebaat zijn bij de interventie: doe bij voorkeur…. |
|
Zwak negatief |
Het is onzeker of alle patienten gebaat zijn bij de interventie: doe bij voorkeur niet…. |
|
Sterk negatief |
De interventie doet meer kwaad dan goed: doe niet…. |
Uitwerking volgens de GRADE-methode
Tabel 4: Indeling van methodologische kwaliteit van studies volgens GRADE
|
|
GRADE systeem |
|
Type bewijs |
Gerandomiseerd onderzoek = hoog Observationele studie = laag Elk ander bewijs = zeer laag |
|
Factoren die de kwaliteit van bewijs kunnen verlagen*: |
- Ernstige of zeer ernstige beperkingen in de kwaliteit van de studie - Indirectheid van het bewijs - Belangrijke inconsistentie tussen studies - Imprecisie - Grote kans op ‘publicatiebias’ |
|
Factoren die de kwaliteit van bewijs kunnen verhogen**: |
- Sterk bewijs voor een associatie—significant relatief risico van > 2 ( < 0,5) gebaseerd op consistent bewijs uit twee of meer observationele studies, zonder plausibele ‘confounders’ (+1) - Zeer sterk bewijs voor een associatie—significant relatief risico van > 5 ( < 0,2) gebaseerd op direct bewijs zonder belangrijke bedreigingen voor de validiteit (+2) - Bewijs voor een dosis respons gradiënt (+1) - Alle plausibele ‘confounders’ zouden het effect hebben verminderd (+1) |
*Elk criterium kan de kwaliteit verminderen met 1 stap of bij zeer ernstige beperkingen met twee stappen. ** Verhogen kan alleen indien er geen beperkingen zijn t.a.v. de studiekwaliteit, imprecisie, inconsistentie, indirectheid en publicatiebias.
Tabel 5: Niveau van conclusies volgens GRADE
|
Conclusie - Hoog = nader onderzoek zal zeer onwaarschijnlijk het vertrouwen in de inschatting van een effect veranderen - Middelmatig = nader onderzoek zal waarschijnlijk een belangrijke invloed hebben op het vertrouwen in de inschatting van een effect en kan de inschatting van een effect veranderen - Laag = nader onderzoek zal zeer waarschijnlijk een belangrijke invloed hebben op het vertrouwen in de inschatting van een effect en zal waarschijnlijk de inschatting van een effect veranderen - Zeer laag = elke inschatting van een effect is zeer onzeker |
Tabel 6: Niveau van aanbevelingen volgens GRADE
|
Klinische aanbeveling - Sterk voor/tegen = als clinici, gebaseerd op het beschikbare bewijs, zeer zeker zijn dat de voordelen de nadelen of risico’s overtreffen, of andersom, dan zal er een sterke aanbeveling worden gedaan - Zwak voor/tegen = als clinici, gebaseerd op het beschikbare bewijs, denken dat de voordelen en de nadelen of risico’s in balans zijn of als er een bepaalde onzekerheid bestaat over de grootte van de voordelen en risico’s, moeten ze een zwakke aanbeveling maken |
Zoekverantwoording
