Systemische corticosteroïden bij chronische rhinosinusitis
Uitgangsvraag
Hoe vaak mag je systemische corticosteroïden voorschrijven per jaar bij patiënten met chronische rhinosinusitis?
Aanbeveling
Behandel patiënten met chronische rhinosinusitis in het algemeen zo weinig mogelijk met systemische corticosteroïden.
Overweeg bij patiënten met chronische rhinosinusitis met neuspoliepen/primaire diffuse type2 en ernstige aanhoudende klachten ondanks voorgaande therapie een behandeling met systemische corticosteroïden bij voorkeur niet vaker dan twee keer per jaar.
Bespreek de voor- en nadelen van de behandeling met de patiënt.
Voor de plaats van deze aanbeveling zie stroomdiagram.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Er is literatuuronderzoek gedaan naar de voor- en nadelen van behandeling met korte kuren van systemische corticosteroïden ten opzichte van standaardbehandeling bij patiënten met chronische rhinosinusitis (CRS). Er werden alleen studies gevonden over patiënten met CRSwNP. Op basis van de geïncludeerde RCT’s geven systemische corticosteroïden mogelijk geen verbetering in patiënt gerapporteerde uitkomstmaten (PROMs) ten opzichte van placebo, in dit geval total nasal symptom score (TNSS) op middellange termijn (10-12 weken). Behandeling leek wel te resulteren in een lagere poliepscore op korte (1-3 weken) en middellange termijn. Door de zeer lage bewijskracht is het onduidelijk of er verbetering is in reukscore op korte of middellange termijn. Er leek geen verschil te zijn in neveneffecten (adverse events) tussen behandeling met corticosteroïden en placebo. De totale bewijskracht van het bewijs, de laagste bewijskracht voor de cruciale uitkomstmaten, is laag. Op het gebied van de uitkomst kwaliteit van leven is er sprake van een kennislacune. Op basis van de poliepscore is er een lichte voorkeur voor behandeling met systemische corticosteroïden ten opzichte van placebobehandeling.
Er is geen literatuur beschikbaar die de frequentie van systemische corticosteroïden bij patiënten met CRS onderzoekt. Er wordt gekeken naar het effect van een systemische corticosteroïden kuur van 14 tot 20 dagen bij patiënten met CRS met neuspoliepen. Hier worden geen neveneffecten van behandeling met systemische corticosteroïden gerapporteerd op korte termijn. Voor een overzicht van de bijwerkingen verwijst de werkgroep naar het farmacotherapeutisch kompas. Voor bijwerkingen op de (middel-)-lange termijn verwijst de werkgroep naar het overzicht van Hox (2020).Derhalve, op basis van expert opinion, wordt geadviseerd niet meer dan twee kuren systemische corticosteroïden per jaar voor te schrijven voor patiënten met CRS en neuspoliepen. Indien meer dan twee kuren per jaar noodzakelijk zijn, wordt geadviseerd naar verdere behandeling te kijken (zie stroomdiagram).
Er is geen literatuur beschikbaar over het effect van korte kuren (tot 14 dagen) van systemische corticosteroïden bij patiënten met CRS zonder neuspoliepen die voldeed aan de inclusiecriteria.
Sinds 2020 adviseert de EPOS een nieuwe indeling: type 2 en non type 2 CRS (Fokkens, 2020). Het is aannemelijk dat systemische corticosteroïden effectiever zijn bij patiënten met het primaire diffuse type 2 CRS. Westerse patiënten met neuspoliepen vallen overwegend in deze groep. De werkgroep adviseert maximaal twee kuren per jaar voor te schrijven bij deze patiënten. De werkgroep is van mening dat behandeling met systemische corticosteroiden niet is geindiceerd bij patienten met een non type 2 CRS.
Alvorens te behandelen met systemische corticosteroïden adviseert de werkgroep te starten met neusspoelen en/of topicale corticosteroïden. Indien dit geen of te weinig effect heeft kunnen systemische corticosteroïden voorgeschreven worden.
Er is beperkt bewijs dat een systemische corticosteroïden kuur voorafgaand aan endoscopische neusbijholtenchirurgie een gunstig effect heeft in termen van bloedverlies, kwaliteit van het chirurgisch veld en operatietijd (Hox, 2020; Pundir, 2016). Een eventuele kuur voorafgaand aan een chirurgische behandeling wordt door de werkgroep ter overweging gegeven. Voor behandeling met systemische corticosteroïden aansluitend aan chirurgie is er beperkt en conflicterend bewijs t.a.v. een eventueel aanvullend effect (zeker op de lange termijn) (Chang, 2021; Pundir, 2016). De werkgroep adviseert om dit niet routinematig in te zetten.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Het belangrijkste doel van de interventie is om patiënten klachtenvrij of op een acceptabel klachtenniveau te krijgen. Het gebruik van systemische corticosteroïden kan hier aan bijdragen bij patiënten met CRS en neuspoliepen (primaire diffuse type2 CRS). Systemische corticosteroïden kunnen een gunstig effect op poliepen op de korte- en middellange termijn hebben. Het kan een tijdelijke verbetering van de reuk geven. Er worden geen neveneffecten gerapporteerd in de literatuur bij korte follow-up. Wel zijn er aanwijzingen dat cumulatieve doseringen over langere tijd relevante bijwerkingen kunnen hebben (Hox, 2020).
Kosten (middelenbeslag)
De directe kosten voor systemische corticosteroïden zijn laag en hebben geen invloed op het ziekenhuis en/of afdelingsbudget. De behandeling heeft een kortdurend effect op indirecte kosten. Er is geen uitspraak te doen over het exacte effect op deze kosten.
Aanvaardbaarheid, haalbaarheid en implementatie
Er zijn geen voorwaarden aan de haalbaarheid van de interventie. De verantwoordelijkheid voor het innemen van de medicatie ligt bij de patiënt. Iedereen in Nederland heeft toegang tot de medicatie, de zorg is verzekerd. Er zijn geen belemmerende factoren op het gebied van implementatie en er zal een hoge acceptatie en therapietrouw zijn bij patiënten die baat hebben bij de behandeling.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Het belangrijkste doel van de interventie is om patiënten klachtenvrij of op een acceptabel klachtenniveau te krijgen. De directe kosten van een kuur systemische corticosteroïden zijn laag en een kuur heeft een kortdurend effect op de indirecte kosten. Systemische corticosteroïden kunnen een gunstig effect op poliepen op de korte- en middellange termijn hebben en een tijdelijke verbetering van de reuk geven. In de literatuur worden geen bijwerkingen gerapporteerd op de korte termijn. Er is echter niet gekeken naar mogelijke effecten op de lange termijn. Ook is er geen literatuur beschikbaar voor patiënten met CRS zonder neuspoliepen (primaire diffuse non-type2 CRS) die voldoet aan de inclusie criteria.
Op basis van de beschikbare literatuur die aan de inclusiecriteria voldeed en expert opinion adviseert de werkgroep patiënten met CRS met neuspoliepen/ primaire diffuse type2 CRS niet vaker dan twee keer per jaar te behandelen met een kuur systemische corticosteroïden.
Onderbouwing
Op dit moment is er geen (inter)nationale consensus over de frequentie van behandeling met systemische corticosteroïden bij patiënten met chronische rhinosinusitis (CRS). Bewijs in de literatuur is laag en er is een grote praktijkvariatie. Afhankelijk van de klachten van de patiënt kan meerdere keren per jaar worden behandeld met systemische corticosteroïden.
|
Low GRADE |
In patients with chronic rhinosinusitis with nasal polyps, short courses (14-20 days) of systemic corticosteroid therapy may result in little to no difference in total symptom score at 10 to 12 weeks follow-up when compared with usual care.
Sources: (Kirtreesakul, 2012; Vaidyanathan, 2011; Van Zele, 2010) |
|
Low GRADE |
In patients with chronic rhinosinusitis with nasal polyps, short courses (14-20 days) of systemic corticosteroid therapy may improve nasal polyp score at 1 to 3 weeks and at 10 to 12 weeks follow-up when compared with usual care.
Sources: (Ecevit, 2015; Kirtreesakul, 2012; Vaidyanathan, 2011; Van Zele, 2010) |
|
Very low GRADE |
It is unclear whether short courses (14-20 days) of systemic corticosteroid therapy improve olfactory function at 1 to 2 weeks follow-up when compared with usual care in patients with chronic rhinosinusitis with nasal polyps
Sources: (Ecevit, 2015; Vaidyanathan, 2011) |
|
Low GRADE |
In patients with chronic rhinosinusitis with nasal polyps, short courses (14-20 days) of systemic corticosteroid therapy may not affect adverse events when compared with usual care on short term.
Sources: (Ecevit, 2015) |
Description of studies
Main study characteristics are presented in table 1. Further details are summarized in the evidence tables.
Table 1. Main study characteristics
|
Study |
Population |
Intervention |
Control |
Follow-up |
|
Ecevit, 2015 |
23 patients with nasal polyposis |
Oral prednisolone in descending (60-10 mg) doses for 17 days (n=11) |
Placebo for 17 days (n=12) |
17 days |
|
Kirtsreesakul, 2012 |
114 patients with CRSwNP |
Oral prednisolone (50 mg/day) for 14 days followed by mometasone furoate nasal spray for 10 weeks (n=67) |
Placebo for 14 days followed by mometasone furoate nasal spray for 10 weeks (n=47) |
12 weeks |
|
Vaidyanathan, 2011 |
51 patients with CRSwNP |
Oral prednisolone (25 mg/day) for 2 weeks, followed by fluticasone propionate nasal drops for 8 weeks then fluticasone propionate nasal spray for a further 18 weeks (n=27) |
Placebo tablets followed by fluticasone propionate identical to intervention group (n=24) |
28 weeks |
|
Van Zele, 2010 |
33 patients with CRSwNP |
Oral methylprednisolone in descending (32-8 mg/day) doses for 20 days (n=14) |
Placebo (n=19) |
12 weeks |
|
Hissaria, 2006 |
40 patients with CRSwNP |
Oral prednisolone 50 mg/day for 14 days (n=20) |
Placebo (n=20) |
14 days |
Results
Patient reported outcomes (critical outcome)
Quality of life as determined by the SNOT-22 score was not reported in the included literature.
Three studies reported total symptom score at 10 to 12 weeks. Taken together, the standardized mean difference (SMD) between systemic corticosteroid therapy (n=108) and placebo (n=92) was -0.13 (95% CI -0.41 to 0.15) in favour of corticosteroid therapy, as presented in figure 1. Xu (2020) reported total symptom score at day 7, and found -7.3±1.1 (n=40) in the intervention group versus -4.10±0.9 (n=39) n the control group (P=0.039). The differences were not clinically relevant.
Figure 1. Total symptom score at 10-12 weeks after systemic corticosteroid therapy versus placebo.
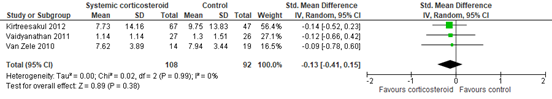
Standardized mean difference, random effects model. Lower score is better. Z: p-value of pooled effect; df: degrees of freedom; I2: statistical heterogeneity; CI: confidence interval.
Level of evidence of the literature
The level of evidence for the outcome total symptom score was based on randomized studies and therefore started at high. The quality of evidence was downgraded by 2 levels to low due to heterogeneity of the studies (variation is medication dose and the presence of adjuvant therapy) and the limited number of included patients (imprecision).
Polyp score
Five studies reported nasal polyp score (figure 2). At 1 to 3 weeks, the SMD (95% CI) in 5 RCTs between systemic corticosteroid (n=120) and control therapy (n=107) was -1.51 (-2.12 to -0.90) in favour of corticosteroid therapy. At 10 to 12 weeks, the SMD was -0.50 (-0.79 to -0.21) in 108 versus 95 patients. These differences were considered clinically relevant.
Figure 2. Nasal polyp score after systemic corticosteroid therapy versus placebo.
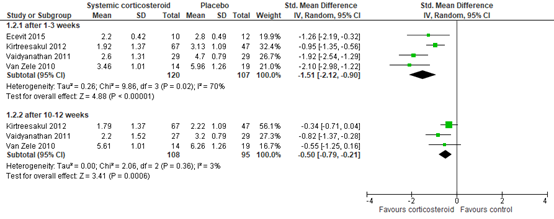
Standardized mean difference, random effects model. Lower score is better. Z: p-value of pooled effect; df: degrees of freedom; I2: statistical heterogeneity; CI: confidence interval.
Level of evidence of the literature
The level of evidence for the outcome polyp score was based on randomized studies and therefore started at high. The quality of evidence was downgraded by 2 level to low due to heterogeneity of the studies (variation is medication dose and presence of adjuvant therapy) and the limited number of included patients (imprecision).
Olfactory function
Two studies reported olfactory scores. Ecevit (2015) reported a VAS score (0-10, lower is better) of 5.5±3.6 (n=10) after systemic corticosteroid therapy versus 8.5±2.2 (n=12) in the placebo group at day 17. Vaidyanathan (2011) reported a mean (95% CI) VAS score (0-100) of 1.03 (0.40 to 1.67) versus 3.22 (1.86 to 4.57) at 2 weeks, 27.24 (17.41 to 39.25) versus 38.12 (26.31 to 52.10) at 10 weeks, and 29.27 (19.84 to 40.53) versus 41.33 (28.96 to 55.92) at 28 weeks, in oral prednisolone group (n=27) and the placebo group (n=24), respectively. These differences are considered clinically relevant.
Level of evidence of the literature
The level of evidence for the outcome olfactory function was based on randomized studies and therefore started at high. The quality of evidence was downgraded by 3 levels to very low due to heterogeneity of the studies (variation is medication dose and presence of adjuvant therapy), the limited number of included patients and because the CI overlapped with the limit of clinical decision-making (both imprecision).
Adverse events
Only one study reported adverse events at patient level. Ecevit (2015) found no adverse events in either the prednisolone group (n=10) or the placebo group (n=12).
Level of evidence of the literature
The level of evidence for the outcome adverse events was based on randomized studies and therefore started at high. The quality of evidence was downgraded by 2 levels to low due to the very low number of events (imprecision).
A: Systematic review of the literature was performed to answer the following question:
P: Patients with chronic rhinosinusitis, with or without nasal polyps.
I: Systemic corticosteroids.
C: Placebo/usual care.
O: Disease-related quality of life (SNOT-score), total symptom score, nasal polyp score, sense of smell/olfactory dysfunction, (serious) adverse event (short and long term).
Relevant outcomes
The guideline development group considered patient reported outcome measures (PROMs) as critical outcomes for decision making; and the outcomes nasal polyp score, sense of smell/olfactory dysfunction, and (serious) adverse events as important outcomes for decision making.
A priori, the working group considered disease-related quality of life, as assessed by the Sino-Nasal Outcome Test (SNOT-22) score, the preferred outcome. This is a quality of life score specifically for CRS patients, in which patients score the burden of disease for 22 symptoms and social/emotional consequences from 0 (“no problem”) to 5 (“problem as bad as it can be”), resulting in a total score from 0 to 110. In case SNOT-22 was not reported, symptom severity as described by total nasal symptom score was preferred over the use of a visual analogue score (VAS). The important outcomes nasal polyp score and sense of smell/olfactory dysfunction could be assessed by any validated score. Adverse events were not defined a priori.
For the SNOT-22 score the working group defined 12.0 as a minimal clinically (patient) important difference (MCID) in medically managed patients with CRS, as described in literature (Phillips, 2018). For total symptom score, polyp score and VAS scores, the working group defined 15% of the maximum score as MCID, and 0.5 for standardized mean differences. For adverse events (risk ratio, RR), the working group defined 25% as a MCID.
Search and select (Methods)
The meta-analysis of the EPOS position paper (Fokkens, 2020) was followed, and updated with papers published more recently (2019 and later). The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms until July 22, 2021. The detailed search strategy is depicted under the ‘Methods’ tab. The systematic literature search resulted in 372 hits. Studies were eligible for inclusion if they were (1) randomized controlled trials (RCTs) or meta-analyses of RCTs, (2) comparing systemic corticosteroids (any dose or duration, but excluding postoperative therapy) with placebo, (3) in patients with chronic rhinosinusitis, with or without nasal polyps. Based on title and abstract screening, eleven studies were initially selected. After reading the full text, nine studies were excluded (see the table with reasons for exclusion under the ‘Methods’ tab) and two were included.
Results
For analysis of the literature, five articles analysed by the EPOS position paper were included. Important study characteristics of all studies and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
- Ecevit MC, Erdag TK, Dogan E, Sutay S. Effect of steroids for nasal polyposis surgery: A placebo-controlled, randomized, double-blind study. Laryngoscope. 2015 Sep;125(9):2041-5. doi: 10.1002/lary.25352. Epub 2015 May 6. PMID: 25945691.
- Chang MT, Noel J, Ayoub NF, Qian ZJ, Dholakia S, Nayak JV, Patel ZM, Hwang PH. Oral Corticosteroids Following Endoscopic Sinus Surgery for Chronic Rhinosinusitis Without Nasal Polyposis: A Randomized Clinical Trial. JAMA Otolaryngol Head Neck Surg. 2021 May 1;147(5):434-441. doi: 10.1001/jamaoto.2021.0011. PMID: 33662124; PMCID: PMC7934078.
- Fokkens WJ, et al. European Position Paper on Rhinosinusitis and Nasal Polyps 2020 (EPOS). Rhinology. 2020 Feb 20;58(Suppl S29):1-464. doi: 10.4193/Rhin20.600. PMID: 32077450.
- Hox V, Lourijsen E, Jordens A, Aasbjerg K, Agache I, Alobid I, Bachert C, Boussery K, Campo P, Fokkens W, Hellings P, Hopkins C, Klimek L, Mäkelä M, Mösges R, Mullol J, Pujols L, Rondon C, Rudenko M, Toppila-Salmi S, Scadding G, Scheire S, Tomazic PV, Van Zele T, Wagemann M, van Boven JFM, Gevaert P. Benefits and harm of systemic steroids for short- and long-term use in rhinitis and rhinosinusitis: an EAACI position paper. Clin Transl Allergy. 2020 Jan 3;10:1. doi: 10.1186/s13601-019-0303-6. Erratum in: Clin Transl Allergy. 2020 Sep 28;10:38. PMID: 31908763; PMCID: PMC6941282.
- Hissaria P, Smith W, Wormald PJ, Taylor J, Vadas M, Gillis D, Kette F. Short course of systemic corticosteroids in sinonasal polyposis: a double-blind, randomized, placebo-controlled trial with evaluation of outcome measures. J Allergy Clin Immunol. 2006 Jul;118(1):128-33. doi: 10.1016/j.jaci.2006.03.012. Epub 2006 May 19. PMID: 16815148.
- Kirtsreesakul V, Wongsritrang K, Ruttanaphol S. Does oral prednisolone increase the efficacy of subsequent nasal steroids in treating nasal polyposis? Am J Rhinol Allergy. 2012 Nov-Dec;26(6):455-62. doi: 10.2500/ajra.2012.26.3820. PMID: 23232195; PMCID: PMC3903103.
- Phillips KM, Hoehle LP, Caradonna DS, Gray ST, Sedaghat AR. Minimal clinically important difference for the 22-item Sinonasal Outcome Test in medically managed patients with chronic rhinosinusitis. Clin Otolaryngol. 2018 Oct;43(5):1328-1334. doi: 10.1111/coa.13177. Epub 2018 Jul 26. PMID: 29953729.
- Pundir V, Pundir J, Lancaster G, Baer S, Kirkland P, Cornet M, Lourijsen ES, Georgalas C, Fokkens WJ. Role of corticosteroids in Functional Endoscopic Sinus Surgery--a systematic review and meta-analysis. Rhinology. 2016 Mar;54(1):3-19. doi: 10.4193/Rhino15.079. PMID: 26970247.
- Vaidyanathan S, Barnes M, Williamson P, Hopkinson P, Donnan PT, Lipworth B. Treatment of chronic rhinosinusitis with nasal polyposis with oral steroids followed by topical steroids: a randomized trial. Ann Intern Med. 2011 Mar 1;154(5):293-302. doi: 10.7326/0003-4819-154-5-201103010-00003. PMID: 21357906.
- Van Zele T, Gevaert P, Holtappels G, Beule A, Wormald PJ, Mayr S, Hens G, Hellings P, Ebbens FA, Fokkens W, Van Cauwenberge P, Bachert C. Oral steroids and doxycycline: two different approaches to treat nasal polyps. J Allergy Clin Immunol. 2010 May;125(5):1069-1076.e4. doi: 10.1016/j.jaci.2010.02.020. PMID: 20451040.
Evidence table for intervention studies (randomized controlled trials and non-randomized observational studies [cohort studies, case-control studies, case series])1
This table is also suitable for diagnostic studies (screening studies) that compare the effectiveness of two or more tests. This only applies if the test is included as part of a test-and-treat strategy – otherwise the evidence table for studies of diagnostic test accuracy should be used.
Research question: What are the favourable and unfavourable effects of systemic corticosteroid therapy compared with placebo/usual care in patients with chronic rhinosinusitis?
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Ecevit, 2015 |
Type of study: RCT
Setting and country: Single-centre, Turkey
Funding and conflicts of interest: The authors have no funding, financial relationships, or conflicts of interest to disclose. |
Inclusion criteria: Nasal polyposis; 18-65 years old; Endoscopic stage II or III nasal polyposis; no response to 6 weeks of fluticasone nasal drops.
Exclusion criteria: Hypertension, type I or II diabetes mellitus, signs of systemic infection, pregnancy/lactation, any type of tuberculosis infection, peptic ulcer, viral infection, myasthenia gravis, stage I nasal polyposis, aspirin intolerance, previous major head trauma.
N total at baseline: Intervention: 10 Control: 12
Important prognostic factors2: Age, mean ± SD: I: 45.6±11.5 C: 19.2±3.1
Sex: I: 90% M C: 67% M
Groups were comparable at baseline. |
Oral prednisolone, 60 mg for 7 days, followed by 10 mg every other day for 10 days.
N=10
|
Oral placebo.
N=12 |
Length of follow-up: 17 days
Loss-to-follow-up: None.
Incomplete outcome data: Not specified.
|
Values are mean ± SD after treatment
Polyp score (data taken from EPOS position paper): OCS: 2.2±0.42 (n=10) Placebo: 2.8±0.49 (n=12) Mean difference -1.26 [95% CI -2.19, -0.32]
Smell (VAS, higher is worse) OCS: 5.5±3.6 Placebo: 8.5±2.2
Adverse effects were not observed in either group. |
Authors’ conclusions: Preoperative administration of systemic corticosteroids improves perioperative visibility by reducing blood loss and results in the shortening of the operation time. We advise utilization of preoperative corticosteroid for the safety of patients being treated for nasal polyposis. The optimal dose and duration of medication to use in these cases require additional study. |
|
Kirtsreesakul, 2012 |
Type of study: RCT
Setting and country: Single-centre, Thailand
Funding and conflicts of interest: Funded by the Faculty of Medicine, Prince of Songkla University. The authors have no conflicts of interest to declare pertaining to this article |
Inclusion criteria: Patients with benign bilateral nasal polyps diagnosed clinically and confirmed by nasal endoscopy were included in the study.
Exclusion criteria: Patients with symptoms or physical signs suggestive of renal disease, hepatic disease, diabetes mellitus, cataract, glaucoma, cardiovascular disease, unstable asthma, cystic fibrosis, mucociliary disorders, immunocompromise, severe septal deviation, or acute infection within the previous 2 months; patients who had used nasal, inhaled, or systemic steroids within 2 months, an antihistamine within 2–7 days, and/or a decongestant within 2 days or had had previous sinonasal surgery.
N total at baseline: Intervention: 69 Control: 48
Important prognostic factors2: Age, mean (range): I: 45.3 (18-65) C: 46.4 (18-65)
Sex: I: 64% male C: 62% male
Mean duration of symptoms (yr): I: 7.9 C: 7.7
Total nasal polyp score, mean ± SD: I: 3.37 ± 1.37 C: 3.13 ± 1.09
Groups were comparable at baseline. |
Oral Behandel patiënten met chronische rhinosinusitis in het algemeen zo weinig mogelijk met systemische corticosteroïden.
Overweeg bij patiënten met prednisolone, 50 mg daily for 14 days
|
Placebo for 14 days
followed in both groups by administration of mometasone furoate nasal spray (MFNS) at 200 µg twice daily for 10 weeks.
|
Length of follow-up: 12 weeks
Loss-to-follow-up: Intervention: 2/69 (3%) Logistical reasons
Control: 1/48 (2%) Logistical reasons
Incomplete outcome data: None
|
Outcome measures and effect size (include 95%CI and p-value if available):
Total symptom score (data from EPOS position paper) mean±SD OCS: 7.73±14.16 (n=67) C: 9.75±13.83 (n=47) Mean difference -2.02 [95% CI -7.23, 3.19]
Polyp score (data from EPOS position paper) mean±SD At 2 weeks OCS: 1.92±1.37 C: 3.13±1.09 Mean difference -1.21 [95% CI -1.66, -0.76]
At 12 weeks OCS: 1.79±1.37 C: 2.22±1.09 Mean difference -0.43 [95% CI -0.88, 0.02]
Adverse effects (specified per event, not per person) OCS vs C: Gastrointestinal disturbance: 11 vs 1 Dyspepsia: 5 vs 1 Throat irritation: 4 vs 3 Headache: 3 vs 3 Nasal irritation: 2 vs 2 Increased appetite: 1 vs 0 Fatigue: 1 vs 0 Acne: 1 vs 0 Insomnia: 1 vs 0
|
Authors’ conclusions: Combined oral and nasal steroid therapy was more effective over 12 weeks than nasal steroid therapy alone in improving hyposmia, polyps size, and nasal airflow in nasal polyposis. |
|
Vaidyanathan, 2011 |
Type of study: RCT
Setting and country: Single-centre, Scotland
Funding and conflicts of interest: Chief Scientist Office, Scotland; National Health Service Tayside Small Grants Scheme; and an Anonymous Trust grant from University of Dundee. |
Inclusion criteria: Nonsmoking adults who had CRS with nasal polyposis, with or without asthma, from a single-centre specialty clinic in Tayside, Scotland, to which patients were referred for assessment by their primary care physicians. Inclusion criteria were the presence on nasoendoscopy of bilateral moderate-sized to large nasal polyps (grade >1) according to the Lildholdt scale and at least 2 of anterior or posterior nasal discharge, nasal obstruction, or decreased sense of smell for more than 12 weeks.
Exclusion criteria: Treatment with an oral corticosteroid in the past 3 months, sinus surgery in the past year, recent upper respiratory tract infection, mechanical nasal airway obstruction of more than 50% due to septal deviation, or pregnancy or lactation.
N total at baseline: Intervention: 30 Control: 30
Important prognostic factors2: Age mean (range): I: 49 (24–70) C: 52 (17–78)
Sex: I: 47% M C: 67% M
Duration of CRS, mean±SD (years) I: 11±11 C: 17±15
Groups were comparable at baseline. |
Oral prednisolone 25mg/day for 2 weeks
N=29
|
Placebo tablets for 2 weeks.
N=29
followed in both groups by fluticasone propionate nasal drops 400 µg twice daily, for 8 weeks and then fluticasone propionate nasal spray, 200 µg twice daily, for a further 18 weeks.
|
Length of follow-up: 28 weeks
Loss-to-follow-up: Intervention: 3/30 (10%) 1 withdrew for personal reasons, 2 did not receive follow-up medication (nasal spray)
Control: 6/30 (20%) 1 withdrew for personal reasons, 1 was lost to follow-up, 2 discontinued placebo intervention due to nausea or asthma exacerbation, 2 did not receive follow-up medication (nasal spray).
Incomplete outcome data: I: 3% of the data for polyp grading were missing at 2 weeks, 7% at 10 weeks, and 4% at 28 weeks. C: 7% of the data were missing at 2 weeks, 7% at 10 weeks, and 4% at 28 weeks.
|
Total symptom score mean (95% CI) At 2 weeks I: 1.03 (0.40 to 1.67) C: 3.22 (1.86 to 4.57) Predicted Mean difference 0.15 (0.02 to 0.40) P=0.001
At 10 weeks I: 1.14 (0.69 to 1.59) C: 1.30 (0.69 to 1.91) Predicted Mean difference 1.86 (0.85 to 3.98) P=0.07
At 28 weeks I: 1.00 (0.58 to 1.41) C: 1.54 (0.95 to 2.14) Predicted Mean difference 0.80 (0.26 to 2.15) P=0.81
Polyp score mean (95% CI) At 2 weeks I: 2.6 (2.1 to 3.1) C: 4.7 (4.4 to 5.0) Predicted Mean difference -1.8 (–2.4 to –1.2) P<0.001
At 10 weeks I: 2.2 (1.6 to 2.8) C: 3.2 (2.8 to 3.5) Predicted Mean difference -1.1 (–1.7 to –0.4) P=0.110
At 28 weeks, mean (95% CI) I: 2.8 (2.2 to 3.4) C: 3.3 (2.8 to 3.7) Predicted Mean difference -0.8 (–1.8 to 0.2) P=0.11
Hyposmia VAS (0–100 mm, lower score equals better smell) At 2 weeks I: 27.52 (18.37 to 38.53) C: 54.55 (41.29 to 69.64) Predicted Mean difference -28.33 (–42.71 to –13.96) P=0.002
At 10 weeks I: 27.24 (17.41 to 39.25) C: 38.12 (26.31 to 52.10) Predicted Mean difference -16.06 (–30.99 to –1.13) P=0.03
At 28 weeks I: 29.27 (19.84 to 40.53) C: 41.33 (28.96 to 55.92) Predicted Mean difference -12.13 (–30.55 to 6.29) P=0.19 |
Authors’ conclusions: Initial oral steroid therapy followed by topical steroid therapy seems to be more effective over 6 months than topical steroid therapy alone in decreasing polyp size and improving olfaction in patients referred for specialty care of CRS with at least moderate nasal polyposis. |
|
Van Zele, 2010 |
Type of study: RCT
Setting and country: Multicentre, Belgium, Germany, Australia, the Netherlands
Funding and conflicts of interest: Supported by a grant from the Flemish Scientific Research Board, FWO Nr. A12/5-HBKH 3 (holder of a Fundamenteel Klinisch Mandaat), by a postdoctoral grant from the Research Foundation Flanders (FWO), and by postdoctoral mandate from the Research Foundation Flanders (FWO). Disclosure of potential conflict of interest: P. J. Wormald has received royalties from Medtronic ENT, is a consultant for NeilMed, and has received research support from the Garnett Passe and RodneyWilliams Foundation.W. Fokkens has received research support from GlaxoSmithKline and Stallergenes. A. Beule has received research support from the European Union. The rest of the authors have declared that they have no conflict of interest. |
Inclusion criteria: Patients with recurrent bilateral nasal polyps after surgery or massive bilateral nasal polyps (grade 3 or 4) in good health, and free of diseases that would interfere with the study.
Exclusion criteria: Women must not be pregnant, breast-feeding, or premenarcheal. Subjects who have required a burst of oral corticosteroids within the 3 months before screening are excluded from the study. Subjects with systemic fungoid infections, known allergic reaction on methylprednisolone or tetracyclines, hypertension, diabetes (type 1 and 2), glaucoma, tuberculosis, herpes infection, or zona ophtalmica are excluded, and children are excluded. For all criteria see supplemental table E2 of the article.
N total at baseline: Intervention: 14 Control: 19
Important prognostic factors2: Age, mean (SEM): I: 48.89 (3.23) C: 54.67 (3.07)
Sex: I: 85.7% M C: 78.9% M
Total polyp score, mean (SEM): I: 5.86 (0.27) C: 6.16 (0.29)
Groups were comparable at baseline. |
Group 1. Oral methylprednisolone (32 mg/d on days 1-5; 16 mg/d on days 6-10; and 8 mg/d on days 11-20).
Group 2*. oral doxycycline
*group 2 was not considered in this analysis
|
Oral placebo
|
Length of follow-up: 12 weeks
Loss-to-follow-up: Intervention: 0/14
Control: 7/19 (37%) after week 4. Reasons for withdrawal included unsatisfactory therapeutic effects, withdrawal of consent, and serious adverse events
Incomplete outcome data: Not specified
|
Total symptom score (data from EPOS position paper) Mean±SD at 12 weeks I: 7.62±3.89 (n=14) C: 7.94±3.44 (n=9) Mean difference -0.32 [95% CI -2.88, 2.24]
Polyp score (data from EPOS position paper) Mean±SD At 1 week I: 3.46±1.01 C: 5.96±1.26 Mean difference -2.50 [95% CI -3.28, -1.72]
At 12 weeks I: 5.61±1.01 C: 6.26±1.26 Mean difference -0.65 [95% CI -1.43, 0.13]
Adverse events: 48.5% of the subjects in the study reported at least 1 adverse event. There were no significant differences in the number or type of adverse events between treatment groups or between treatment and placebo groups. |
Authors’ conclusions: This study highlights the need for long-term studies with doxycycline to establish their therapeutic role in the treatment of nasal polyposis and to improve treatment standards. Treatment of nasal polyps with oral corticosteroids is of limited value unless it is associated with surgery or therapy with intranasal corticosteroids. |
|
Hissaria, 2006 |
Type of study: RCT
Setting and country: Single-centre, Australia
Funding and conflicts of interest: Funding not stated. P. Wormwald receives royalties from Medtronic Xomed for instruments designed. The rest of the authors have declared that they have no conflict of interest.
|
Inclusion criteria: Patients aged 18 to 65 years who had symptomatic polyp disease diagnosed on nasendoscopy.
Exclusion criteria: Previous use of oral steroids, unstable asthma, recent sinus surgery, acute infection within 1 month of recruitment, polyps caused by cystic fibrosis or mucociliary disorders, diabetes mellitus, cataract, glaucoma, fungal sinusitis, contraindications for MRI scanning, or any other significant comorbid condition that contraindicated the use of systemic corticosteroids.
N total at baseline: Intervention: 20 Control: 21
Important prognostic factors2: For example Age, mean ± SD: I: 49±13 C: 48±12
Sex: I: 35% M C: 60% M
Previous polyp operations I: 8/20 C: 13/20
Groups were comparable at baseline. |
Oral prednisolone, 50 mg daily for 14 days |
Oral placebo
|
Length of follow-up: 2 weeks
Loss-to-follow-up: Intervention: 0
Control: One subject (5%) (in the placebo group) withdrew within the first week because of a lack of efficacy
Incomplete outcome data: Not specified.
|
Nasendoscopy polyp score at 14 days (%) I: 52% C: 93%
Adverse events (specified per event, not per person) Events, I vs C: Insomnia, 8 vs 2 Mood disturbance, 5 vs 2 Headache, 2 vs 0 Dyspepsia, 3 vs 2 Increased appetite, 2 vs 0 Fatigue, 2 vs 0 Backache, 1 vs 0 Diarrhea/GI disturbance, 2 vs 1 Acne, 1 vs 0 Edema feet, 1 vs 0 |
Authors’ conclusions: This trial clearly establishes clinically significant improvement in the symptoms and pathology of sinonasal polyposis with a short course of systemic corticosteroids. |
Notes:
- Prognostic balance between treatment groups is usually guaranteed in randomized studies, but non-randomized (observational) studies require matching of patients between treatment groups (case-control studies) or multivariate adjustment for prognostic factors (confounders) (cohort studies); the evidence table should contain sufficient details on these procedures
- Provide data per treatment group on the most important prognostic factors [(potential) confounders]
- For case-control studies, provide sufficient detail on the procedure used to match cases and controls
- For cohort studies, provide sufficient detail on the (multivariate) analyses used to adjust for (potential) confounders
Risk of bias table for intervention studies (randomized controlled trials; based on Cochrane risk of bias tool and suggestions by the CLARITY Group at McMaster University)
Research question:
|
Study reference
(first author, publication year) |
Was the allocation sequence adequately generated? a
Definitely yes Probably yes Probably no Definitely no |
Was the allocation adequately concealed?b
Definitely yes Probably yes Probably no Definitely no |
Blinding: Was knowledge of the allocated interventions adequately prevented?c
Were patients blinded?
Were healthcare providers blinded?
Were data collectors blinded?
Were outcome assessors blinded?
Were data analysts blinded?
Definitely yes Probably yes Probably no Definitely no |
Was loss to follow-up (missing outcome data) infrequent?d
Definitely yes Probably yes Probably no Definitely no |
Are reports of the study free of selective outcome reporting?e
Definitely yes Probably yes Probably no Definitely no |
Was the study apparently free of other problems that could put it at a risk of bias?f
Definitely yes Probably yes Probably no Definitely no |
Overall risk of bias If applicable/necessary, per outcome measureg
LOW Some concerns HIGH
|
|
Ecevit, 2015 |
Probably yes;
Reason: The hospital pharmacy department performed the drug/placebo randomization, but the randomization method was not specified. |
Definitely yes;
Reason: The hospital pharmacy department performed the drug/placebo randomization, and the identity of the contents in the boxes was not disclosed to any clinicians interacting with patients throughout the study. |
Definitely yes;
Reason: The hospital pharmacy department performed the drug/placebo randomization, and the identity of the contents in the boxes was not disclosed to any clinicians interacting with patients throughout the study. |
Definitely yes;
Reason: no loss to follow-up. |
Probably yes;
Reason: All relevant outcomes were reported |
Probably yes;
Reason: No other problems noted |
LOW |
|
Kirtsreesakul, 2012 |
Probably yes;
Reason: assumed but not specified. |
Probably yes;
Reason: assumed but not specified. |
Definitely yes;
Patients and study personnel were not informed of the treatment modality of the patients until all assessments were completed. |
Definitely yes;
Loss to follow-up was limited and similar between the groups. |
Probably yes;
Reason: All relevant outcomes were reported |
Probably yes;
Reason: No other problems noted |
LOW |
|
Vaidyanathan, 2011 |
Definitely yes;
An independent, off-site clinical trials pharmacist used a computer-generated random allocation sequence to randomize the trial, using block randomization with a block size of 4. |
Definitely yes;
Medication and placebo tablets were distributed in sealed opaque envelopes at the research unit, in sequential order, by a laboratory technician who was not directly involved with the study. |
Definitely yes;
An independent, off-site clinical trials pharmacist masked and blinded the 25-mg prednisolone tablet and an identical placebo tablet to double-blind the study from the investigator and participants. |
Probably no;
For the measurements at later time points, loss to follow-up was considerable and uneven between the study groups. |
Probably yes;
Reason: All relevant outcomes were reported |
Probably yes;
Reason: No other problems noted |
Some concerns for outcomes at longer follow-up. |
|
Van Zele, 2010 |
Probably yes;
Reason: assumed but not specified. |
Probably yes;
Reason: Eligible patients were randomly assigned to 3 groups by individuals not involved in the study. Study medication was provided in in unlabeled capsules. |
Definitely yes;
Study personnel and participants were blinded for the duration of the study. |
Probably no;
For the measurements at later time points, loss to follow-up was considerable and uneven between the study groups. |
Probably yes;
Reason: All relevant outcomes were reported |
Probably yes;
Reason: No other problems noted |
Some concerns for outcomes at longer follow-up. |
|
Hissaria, 2006 |
Probably yes;
Reason: assumed but not specified. |
Definitely yes;
Patients were randomized by the hospital pharmacy to receive the study medication, which consisted of prednisolone or placebo and were blinded to their treatment status. |
Definitely yes;
Patients were blinded to their treatment status and observers of imaging were blinded to treatment status. |
Definitely yes;
Loss to follow-up was limited and similar between the groups. |
Probably yes;
Reason: All relevant outcomes were reported |
Probably yes;
Reason: No other problems noted |
LOW |
- Randomization: generation of allocation sequences have to be unpredictable, for example computer generated random-numbers or drawing lots or envelopes. Examples of inadequate procedures are generation of allocation sequences by alternation, according to case record number, date of birth or date of admission.
- Allocation concealment: refers to the protection (blinding) of the randomization process. Concealment of allocation sequences is adequate if patients and enrolling investigators cannot foresee assignment, for example central randomization (performed at a site remote from trial location). Inadequate procedures are all procedures based on inadequate randomization procedures or open allocation schedules..
- Blinding: neither the patient nor the care provider (attending physician) knows which patient is getting the special treatment. Blinding is sometimes impossible, for example when comparing surgical with non-surgical treatments, but this should not affect the risk of bias judgement. Blinding of those assessing and collecting outcomes prevents that the knowledge of patient assignment influences the process of outcome assessment or data collection (detection or information bias). If a study has hard (objective) outcome measures, like death, blinding of outcome assessment is usually not necessary. If a study has “soft” (subjective) outcome measures, like the assessment of an X-ray, blinding of outcome assessment is necessary. Finally, data analysts should be blinded to patient assignment to prevents that knowledge of patient assignment influences data analysis.
- If the percentage of patients lost to follow-up or the percentage of missing outcome data is large, or differs between treatment groups, or the reasons for loss to follow-up or missing outcome data differ between treatment groups, bias is likely unless the proportion of missing outcomes compared with observed event risk is not enough to have an important impact on the intervention effect estimate or appropriate imputation methods have been used.
- Results of all predefined outcome measures should be reported; if the protocol is available (in publication or trial registry), then outcomes in the protocol and published report can be compared; if not, outcomes listed in the methods section of an article can be compared with those whose results are reported.
- Problems may include: a potential source of bias related to the specific study design used (e.g. lead-time bias or survivor bias); trial stopped early due to some data-dependent process (including formal stopping rules); relevant baseline imbalance between intervention groups; claims of fraudulent behavior; deviations from intention-to-treat (ITT) analysis; (the role of the) funding body. Note: The principles of an ITT analysis implies that (a) participants are kept in the intervention groups to which they were randomized, regardless of the intervention they actually received, (b) outcome data are measured on all participants, and (c) all randomized participants are included in the analysis.
- Overall judgement of risk of bias per study and per outcome measure, including predicted direction of bias (e.g. favors experimental, or favors comparator). Note: the decision to downgrade the certainty of the evidence for a particular outcome measure is taken based on the body of evidence, i.e. considering potential bias and its impact on the certainty of the evidence in all included studies reporting on the outcome.
Table of excluded studies
|
Author and year |
Reason for exclusion |
|
Arancibia, 2020 |
Postoperative therapy |
|
Chang, 2021 |
Postoperative therapy |
|
Cherian, 2020 |
Not the PICO comparison |
|
Lin, 2020 |
Postoperative therapy |
|
Ma, 2021 |
Postoperative therapy |
|
Papadakis, 2021 |
Not placebo-controlled |
|
Shen, 2019 |
Already in Fokkens (2020) |
|
Xu, 2020 |
Not placebo-controlled |
|
Yang, 2021 |
Postoperative therapy |
|
Zhang, 2019 |
Meta-analysis, less recent than Fokkens (2020) |
|
Zhang, 2019 (2) |
Not the PICO comparison |
Beoordelingsdatum en geldigheid
Publicatiedatum : 19-09-2023
Beoordeeld op geldigheid : 07-09-2023
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2021 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met chronische rhinosinusitis met/zonder neuspoliepen.
Werkgroep
- Dr. R. van Weissenbruch, KNO-arts, Wilhelmina Ziekenhuis Assen, Assen, NVKNO
- Dr. S. Reitsma, KNO-arts, Amsterdam Universitair Medisch Centrum, Amsterdam, NVKNO
- Drs. D.F. Eijkenboom, KNO-arts, Antonius Ziekenhuis, Sneek, NVKNO
- Drs. G.E. Joustra, AIOS, Universitair Medisch Centrum Groningen, Groningen, NVKNO
- Dr. G.J. Braunstahl, longarts, Franciscus Gasthuis, Rotterdam, NVALT
- Dr. M.B. Ekkelenkamp, arts-microbioloog, Universitair Medisch Centrum Utrecht, Utrecht, NVMM
- Drs. J. Vister, radioloog, Universitair Medisch Centrum Groningen, Groningen, NVvR
- Dhr. T. Jonkergouw, adviseur patiëntenbelang, Patiëntenfederatie Nederland (tot maart 2023)
- Mevr. M. Broere, adviseur patiëntenbelang, Patiëntenfederatie Nederland (vanaf maart 2023)
- Mevr. K.M. Jaarsma-Osseweijer, voorzitter Reuksmaakstoornis.nl
Met ondersteuning van
- Dr. M.S. Ruiter, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Drs. B.L. Gal-de Geest, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Van Weissenbruch |
KNO-arts Wilhelmina Ziekenhuis Assen |
Geen voor CRS 2018-2019 bij en nascholing voor huisartsen en KNO-artsen voor ALK en Sanofi College en algemene KNO |
Geen |
Geen restricties. |
|
Braunstahl |
Longarts, Franciscus Gasthuis & Vlietland Rotterdam |
Nul-aanstelling ErasmusMC voor onderzoek: onbetaald |
Vergoeding: Presentaties en incidenteel advieswerk voor Boehringer Ingelheim, Sanofi, Novartis, GSK, AstraZeneca, ALK, MEDA en Chiesi. Onderwerp relevant voor de richtlijn is behandeling met biologicals.
Deelname richtlijn ernstige astma. Deelname klankbordgroep van het project ‘Obesitas volwassenen’
Geen vergoeding: Redactie NTvAAKI Bestuur RoLeX astma/COPD nascholingen Bestuur Rapsodi, ernstig astma database NL Voorzitter astmasectie NVALT Wetenschappelijke adviescommissie Longfonds |
Geen advieswerk voor industrie op gebied van CRS gedurende de looptijd van de richtlijn, restricties ten aanzien van besluitvorming voor module(s) over behandeling met biologicals. |
|
Ekkelenkamp |
Arts-microbioloog, UMC Utrecht |
Schrijver / columinst als ZZP’er, betaald |
Geen |
Geen restricties. |
|
Reitsma |
KNO-arts/rhinoloog, Amsterdam UMC |
Lid medische adviesraad patiëntenvereniging CRSwNP (crs-np.nl) onbetaald Lid bestuur stichting AERO (stichtinggaero.org) onbetaald |
Op incidentele basis de afgelopen 36 maanden: betaald adviseurschap voor Sanofi betaald adviseurschap voor Novartis. Onderwerp relevant voor de richtlijn is behandeling met biologicals. Op de afdeling KNO van het Amsterdam UMC, locatie AMC, wordt onderzoek verricht dat mede gefinancierd is met gelden van ZonMw, Mylan, Chordate Medical Systems, ALK, Allergy diagnostics, Sanofi, Novartis, GSK. Op ten minste 1 daarvan ben ik PI. Onderwerp relevant voor de richtlijn is behandeling met biologicals. Boegbeeldfunctie binnen de Nederlandse KNO-vereniging gezien voorzitterschap van de kerngroep Rhinologie
Lid van rhinologie-team Amsterdam UMC, locatie AMC, waar bijzondere/unieke expertise in behandeling van CRS patiënten is, in het bijzonder met het oog op biologicals; dit centrum heeft een landelijke tertiaire functie
Lid stuurgroep herziening Europese richtlijn voor CRS (EPOS; zie epos2020.com) waarin nieuwe theoretische concepten worden neergelegd |
Geen advieswerk voor industrie op gebied van CRS gedurende de looptijd van de richtlijn, restricties ten aanzien van besluitvorming voor module(s) over behandeling met biologicals. |
|
Eijkenboom |
KNO-arts Antonius ziekenhuis Sneek + Emmeloord |
Geen |
Deelname aan IPAS studie (ALICE) de afdeling KNO in het Antonius Ziekenhuis Sneek participeert sinds kort in de IPAS studie van ALK. IPAS staat voor "Itulazax Post-Authorisation Study". Het is een fase IV studie waarbij nog uitvoeriger gekeken wordt naar de bijwerkingen van een al in de normale praktijk voor te schrijven medicijn. Het betreft waarschijnlijk kleine patiënten aantallen (<10 in 2 jaar) met daarbij een beperkte vergoeding per patiënt. Safety studie. Geen PI. |
Geen restricties. |
|
Joustra |
Arts-assistent / promovendus KNO UMCG |
Geen |
Geen |
Geen restricties. |
|
Vister |
Neuro- en Hoofhalsradioloog UMCG |
Geen |
Geen |
Geen restricties. |
|
Jonkergouw |
Junior adviseur patiëntbelang bij Patiëntenfederatie Nederland |
Geen |
Geen |
Geen restricties. |
|
Jaarsma |
Voorzitter van de vereniging Reuksmaakstoornis |
project fondsenwerver stichting Fier (Betaald) Wethouder gemeente Krimpen aan den IJssel (betaald) |
Geen |
Geen restricties. |
|
Gal-de Geest |
Adviseur bij Kennisinstituut van de Federatie Medisch Specialisten |
Geen |
Geen |
Geen restricties. |
|
Ruiter |
Adviseur bij Kennisinstituut van de Federatie Medisch Specialisten |
Geen |
Geen |
Geen restricties. |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door het uitnodigen van de Patiëntenfederatie Nederland en patiëntenorganisatie CRS voor de schriftelijke knelpuntenanalyse en deelname van de Patiëntenfederatie Nederland en Reuksmaakstoornis.nl aan de werkgroep.
De conceptrichtlijn is tevens voor commentaar voorgelegd aan de Patiëntenfederatie Nederland en Reuksmaakstoornis.nl en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Implementatie
Wet kwaliteit, klachten en geschillen zorg (Wkkgz) & Kwalitatieve raming van mogelijke substantiële financiële gevolgen
Bij de richtlijn is conform de Wkkgz een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming blijkt dat er geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
Module |
Uitkomst raming |
Toelichting |
|
Module Kwantificeren van nasendoscopische beelden |
geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, en het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Module Beeldvorming bij CRS |
geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Module Diagnostiek onderste luchtwegen bij CRS |
geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Module Behandeling onderste luchtwegen bij CRS |
geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Module Langdurige antibiotica bij CRS |
geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Module Systemische corticosteroïden bij CRS |
geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Module Biologicals |
geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten) en zal daarom naar verwachting geen substantiële financiële gevolgen hebben voor de collectieve uitgaven. |
|
Module Chirurgie bij CRS |
geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Module Postoperatief corticosteroïdenimplantaat |
geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten) en zal daarom naar verwachting geen substantiële financiële gevolgen hebben voor de collectieve uitgaven. |
|
Module Ballondilatatie |
geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten) en zal daarom naar verwachting geen substantiële financiële gevolgen hebben voor de collectieve uitgaven. |
|
Module Organisatie van zorg |
geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft]. Er worden daarom geen financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten met chronische rhinosinusitis met/zonder neuspoliepen. De werkgroep beoordeelde de aanbevelingen uit de eerdere richtlijn (NVKNO, 2009) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door ZKN, het Longfonds, de NVvR en de NVKNO via enquête. Een verslag hiervan is opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten, welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor het zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder ‘Onderbouwing’. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek, spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen, moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs, ook andere aspecten belangrijk en worden meegewogen. Dit kunnen aanvullende argumenten zijn uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg. Hieronder vallen alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg, zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur. Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module ‘Organisatie van zorg’.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/uploaded/docs/Medisch_specialistische_richtlijnen_2-0_-_tot_2023_-_verouderd.pdf?u=1aYjPr
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Literature search strategy
Algemene informatie
|
Richtlijn: NVKNO chronische rhinosinusitis en neuspoliepen |
|
|
Uitgangsvraag: Hoe vaak mag je systemische corticosteroïden voorschrijven per jaar? |
|
|
Database(s): Ovid/Medline, Embase |
Datum: 22-7-2021, 26-7-2021 |
|
Periode: 2019- |
Talen: nvt |
|
Literatuurspecialist: Ingeborg van Dusseldorp |
|
|
BMI zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Bij gebruikmaking van een volledig zoekblok zal naar de betreffende link op de website worden verwezen. |
|
|
Toelichting:
26-7-2021 Geconstateerd dat het deel neuspoliepen ontbrak in de zoekstrategie. Dit deel is alsnog toegevoegd. Uiteindelijk is in deze vraag gezocht met de volgende elementen:
Rhinosinusitis OF neuspoliepen EN corticosteroiden
22-7-2021
Voor deze vraag is gezocht met de volgende elementen: Chronische rhinosinusitis EN corticosteroiden Voor de chronische rhinosinusitis is de zoekstrategie van de positioneringspaper gebruikt:
Fokkens WJ, et al. European Position Paper on Rhinosinusitis and Nasal Polyps 2020 (EPOS). Rhinology. 2020 Feb 20;58(Suppl S29):1-464. doi: 10.4193/Rhin20.600. PMID: 32077450. Zoekstrategie vanaf p454
Het sleutelartikel van Hox wordt niet gevonden vanwege het studiedesign. De positioneringspaper wordt niet gevonden omdat in title/abstract/keyword/trefwoord de corticosteroïden ontbreken.
Vanwege de hoge aantallen in Embase is in deze database gebruik gemaakt van een specifiek RCT filter. In Ovid/Medline is gebruik gemaakt van het algemene RCT filter. |
|
|
Te gebruiken voor richtlijnen tekst: In de databases Embase en Ovid/Medline is tm 26 juli 2021 met relevante zoektermen gezocht naar systematische reviews en RCTs over het gebruik van corticosteroïden bij chronische rhinosinusitis en neuspoliepen. De literatuurzoekactie leverde 372 unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SRs |
126 |
17 |
128 |
|
RCTs |
250 |
66 |
236 |
|
Observationele studies |
|
|
|
|
SR neuspoliepen |
1 |
0 |
1 |
|
RCTs neuspoliepen |
6 |
2 |
7 |
|
Overig |
|
|
372 |
|
Totaal |
|
|
364 |
Zoekstrategie
Embase 26-7-2021
|
No. |
Query |
Results |
|
#27 |
#26 NOT #25 |
6 |
|
#26 |
#18 AND #24 |
7 |
|
#25 |
#17 AND #24 |
1 |
|
#24 |
#15 AND #23 |
69 |
|
#23 |
#22 AND [1-1-2019]/sd NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
902 |
|
#22 |
#21 NOT #13 |
8554 |
|
#21 |
('nose polyp'/exp OR (((nose OR nasal OR nasi OR rhino* OR sinus* OR sinonasal) NEAR/3 (papilloma* OR polyp*)):ti,ab,kw) OR rhinopolyp*:ti,ab,kw OR crswnp*:ti,ab,kw OR crssnp*:ti,ab,kw OR ecrs:ti,ab,kw OR (crs:ti,ab,kw AND (sinonas* OR nasal OR naso* OR rhin* OR ent)) OR ((kartagener* NEAR/2 syndrom*):ti,ab,kw) OR 'primary ciliary dyskinesi*':ti,ab,kw) NOT ((copd:ti OR thoracic:ti OR pulmonary:ti) AND disease:ti OR bronchiectas*:ti) |
21498 |
|
#20 |
#16 AND #18 |
253 |
|
#19 |
#16 AND #17 |
126 |
|
#18 |
('randomized controlled trial'/exp OR random*:ti,ab OR (((pragmatic OR practical) NEAR/1 'clinical trial*'):ti,ab) OR ((('non inferiority' OR noninferiority OR superiority OR equivalence) NEAR/3 trial*):ti,ab)) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) NOT ('conference abstract'/it OR 'conference review'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) |
1198048 |
|
#17 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
733409 |
|
#16 |
#14 AND #15 |
1295 |
|
#15 |
'corticosteroid'/exp AND 'oral drug administration'/exp OR 'glucocorticoid'/exp OR 'prednisone'/exp OR 'prednisolone derivative'/exp OR 'dexamethasone derivative'/exp OR 'betamethasone derivative'/exp OR glucocorticoid*:ti,ab,kw OR glucocorticosteroid*:ti,ab,kw OR glucocortoid*:ti,ab,kw OR glycocorticoid*:ti,ab,kw OR glycocorticosteroid*:ti,ab,kw OR predniso*:ti,ab,kw OR dexamethason*:ti,ab,kw OR bethamethason*:ti,ab,kw OR celeston*:ti,ab,kw |
847887 |
|
#14 |
#13 AND [1-1-2019]/sd NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
12263 |
|
#13 |
#8 OR #12 |
119380 |
|
#12 |
#9 OR #10 OR #11 |
15181 |
|
#11 |
ars:ti,kw AND (sinonas* OR nasal OR naso* OR rhin* OR ent) |
19 |
|
#10 |
((upper NEAR/4 (respiratory OR airway) NEAR/2 infection*):ti,kw) OR urti:ti,kw |
2964 |
|
#9 |
'common cold'/de OR 'common cold':ti,ab,kw OR 'common colds':ti,ab,kw OR 'coryza':ti,ab,kw OR 'natural cold':ti,ab,kw OR 'natural colds':ti,ab,kw |
12563 |
|
#8 |
#3 OR #4 OR #5 OR #6 OR #7 |
106083 |
|
#7 |
((inflamm* OR microb*) NEAR/5 (rhino* OR sinus OR sinuses OR sinusal)):ti,kw |
865 |
|
#6 |
sinusit*:ti,kw OR rhinit*:ti,kw OR ozena*:ti,kw OR rhinosinusit*:ti,kw OR nasosinusit*:ti,kw OR pansinusit*:ti,kw OR ethmoidit*:ti,kw OR sphenoidit*:ti,kw |
42052 |
|
#5 |
'paranasal sinus disease'/mj OR ('paranasal sinus'/de AND 'respiratory tract disease'/de) |
2515 |
|
#4 |
'rhinitis'/de OR 'rhinitis':ti,ab,kw OR 'atrophic rhinitis'/de OR 'vasomotor rhinitis'/de |
56313 |
|
#3 |
'sinusitis'/exp OR 'pansinusitis':ti,ab,kw OR 'sinusitis':ti,ab,kw OR 'sphenoid sinusitis':ti,ab,kw OR 'sphenoidal sinusitis':ti,ab,kw OR 'rhino-sinusitis':ti,ab,kw OR 'rhinosinusitis':ti,ab,kw |
54567 |
|
#2 |
benefits AND harm AND of AND systemic AND steroids AND for AND short- AND 'long term' AND use AND in AND rhinitis AND rhinosinusitis AND hox |
2 |
|
#1 |
european AND position AND paper AND on AND rhinosinusitis AND nasal AND polyps AND 2020 |
13 |
Embase 22-7-2021
|
No. |
Query |
Results |
|
#24 |
#20 AND #21 |
1 |
|
#23 |
#19 AND #21 |
0 |
|
#22 |
#16 AND #21 |
4 |
|
#21 |
#1 OR #2 |
15 |
|
#20 |
#16 AND #18 |
250 |
|
#19 |
#16 AND #17 |
126 |
|
#18 |
('randomized controlled trial'/exp OR random*:ti,ab OR (((pragmatic OR practical) NEAR/1 'clinical trial*'):ti,ab) OR ((('non inferiority' OR noninferiority OR superiority OR equivalence) NEAR/3 trial*):ti,ab)) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) NOT ('conference abstract'/it OR 'conference review'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) |
1198048 |
|
#17 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
733409 |
|
#16 |
#14 AND #15 |
1295 |
|
#15 |
'corticosteroid'/exp AND 'oral drug administration'/exp OR 'glucocorticoid'/exp OR 'prednisone'/exp OR 'prednisolone derivative'/exp OR 'dexamethasone derivative'/exp OR 'betamethasone derivative'/exp OR glucocorticoid*:ti,ab,kw OR glucocorticosteroid*:ti,ab,kw OR glucocortoid*:ti,ab,kw OR glycocorticoid*:ti,ab,kw OR glycocorticosteroid*:ti,ab,kw OR predniso*:ti,ab,kw OR dexamethason*:ti,ab,kw OR bethamethason*:ti,ab,kw OR celeston*:ti,ab,kw |
847887 |
|
#14 |
#13 AND [1-1-2019]/sd NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
12222 |
|
#13 |
#8 OR #12 |
119380 |
|
#12 |
#9 OR #10 OR #11 |
15181 |
|
#11 |
ars:ti,kw AND (sinonas* OR nasal OR naso* OR rhin* OR ent) |
19 |
|
#10 |
((upper NEAR/4 (respiratory OR airway) NEAR/2 infection*):ti,kw) OR urti:ti,kw |
2964 |
|
#9 |
'common cold'/de OR 'common cold':ti,ab,kw OR 'common colds':ti,ab,kw OR 'coryza':ti,ab,kw OR 'natural cold':ti,ab,kw OR 'natural colds':ti,ab,kw |
12563 |
|
#8 |
#3 OR #4 OR #5 OR #6 OR #7 |
106083 |
|
#7 |
((inflamm* OR microb*) NEAR/5 (rhino* OR sinus OR sinuses OR sinusal)):ti,kw |
865 |
|
#6 |
sinusit*:ti,kw OR rhinit*:ti,kw OR ozena*:ti,kw OR rhinosinusit*:ti,kw OR nasosinusit*:ti,kw OR pansinusit*:ti,kw OR ethmoidit*:ti,kw OR sphenoidit*:ti,kw |
42052 |
|
#5 |
'paranasal sinus disease'/mj OR ('paranasal sinus'/de AND 'respiratory tract disease'/de) |
2515 |
|
#4 |
'rhinitis'/de OR 'rhinitis':ti,ab,kw OR 'atrophic rhinitis'/de OR 'vasomotor rhinitis'/de |
56313 |
|
#3 |
'sinusitis'/exp OR 'pansinusitis':ti,ab,kw OR 'sinusitis':ti,ab,kw OR 'sphenoid sinusitis':ti,ab,kw OR 'sphenoidal sinusitis':ti,ab,kw OR 'rhino-sinusitis':ti,ab,kw OR 'rhinosinusitis':ti,ab,kw |
54567 |
|
#2 |
benefits AND harm AND of AND systemic AND steroids AND for AND short- AND 'long term' AND use AND in AND rhinitis AND rhinosinusitis AND hox |
2 |
|
#1 |
european AND position AND paper AND on AND rhinosinusitis AND nasal AND polyps AND 2020 |
13 |
|
# |
Searches |
Results |
|
39 |
21 and 37 |
2 |
|
38 |
20 and 37 |
0 |
|
37 |
18 and 36 |
11 |
|
36 |
35 not ((exp animals/ or exp models, animal/) not humans/) not (letter/ or comment/ or editorial/) |
841 |
|
35 |
limit 34 to yr="2019 -Current" |
927 |
|
34 |
33 not 15 |
8486 |
|
33 |
25 or 26 or 27 or 28 or 29 or 30 or 31 or 32 |
17179 |
|
32 |
((adenoid* adj2 (hypertroph* or obstruct*)) or adenoidit*).tw,kf. |
1212 |
|
31 |
adenoids/ab or (adenoids/ and hypertrophy/) |
1060 |
|
30 |
(kartagener* syndrom* or primary ciliary dyskinesi*).mp. not (COPD or thoracic or pulmonary disease or bronchiectas*).ti,ot. |
2268 |
|
29 |
ECRS.tw,kf. or (CRS.tw,kf. and (sinonas* or nasal or naso* or rhin* or ENT).mp.) |
3754 |
|
28 |
CRSSNP*.tw,kf. |
529 |
|
27 |
(rhinopolyp* or CRSwNP*).tw,kf. |
1319 |
|
26 |
((nose or nasal or nasi or rhino* or sinus* or sinonasal) adj3 (papilloma* or polyp*)).tw,kf. |
9400 |
|
25 |
nasal polyps/ |
6983 |
|
24 |
23 not 22 |
66 |
|
23 |
19 and 21 |
73 |
|
22 |
19 and 20 |
17 |
|
21 |
(exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) |
2144182 |
|
20 |
(meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf.) not (comment/ or editorial/ or letter/ or ((exp animals/ or exp models, animal/) not humans/)) |
508830 |
|
19 |
17 and 18 |
291 |
|
18 |
exp Prednisone/ or exp Prednisolone/ or exp Dexamethasone/ or exp Betamethasone/ or exp Glucocorticoids/ or (exp Adrenal Cortex Hormones/ and exp Administration, Oral/) or glucocorticoid*.ti,ab,kf. or glucocorticosteroid*.ti,ab,kf. or glucocortoid*.ti,ab,kf. or glycocorticoid*.ti,ab,kf. or glycocorticosteroid*.ti,ab,kf. or predniso*.ti,ab,kf. or dexamethason*.ti,ab,kf. or bethamethason*.ti,ab,kf. or celeston*.ti,ab,kf. |
280338 |
|
17 |
16 not ((exp animals/ or exp models, animal/) not humans/) not (letter/ or comment/ or editorial/) |
9040 |
|
16 |
limit 15 to yr="2019 -Current" |
9725 |
|
15 |
8 or 14 |
78805 |
|
14 |
or/9-13 |
17389 |
|
13 |
ARS.tw,kf. and (sinonas* or nasal or naso* or rhin* or ENT).mp. |
214 |
|
12 |
((upper adj4 (respiratory or airway) adj2 infection*) or URTI).tw,kf. |
10470 |
|
11 |
coryza.tw,kf. |
694 |
|
10 |
((common or head) adj cold*).tw,kf. |
4448 |
|
9 |
common cold/ |
4294 |
|
8 |
or/1-7 |
63329 |
|
7 |
(rhinorr*.ti,ot,kf. not (ci.fs. or (CSF or ((leak* or fluid*) and cerebr*) or safet*).ti,ot,kf.)) or (purulent adj3 rhinorr*).tw,kf. |
619 |
|
6 |
nasal muc?us.tw,kf. |
898 |
|
5 |
((inflamm* or microb*) adj5 (rhino* or sinus or sinuses or sinusal)).tw,kf. |
2572 |
|
4 |
(sinusit* or rhinit* or ozena* or rhinosinusit* or nasosinusit* or pansinusit* or ethmoidit* or sphenoidit*).tw,kf. |
53121 |
|
3 |
exp paranasal sinuses/mi or (exp paranasal sinuses/ and (respiratory tract infections/ or chronic disease/)) |
2868 |
|
2 |
rhinitis/ or rhinitis, atrophic/ or rhinitis, vasomotor/ |
14672 |
|
1 |
exp sinusitis/ |
21518 |
Ovid/Medline 22-7-2021
Search Strategy:
|
# |
Searches |
Results |
|
25 |
Nasal Mucosa/ |
18563 |
|
24 |
23 not 22 |
66 |
|
23 |
19 and 21 |
73 |
|
22 |
19 and 20 |
17 |
|
21 |
(exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) |
2143366 |
|
20 |
(meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf.) not (comment/ or editorial/ or letter/ or ((exp animals/ or exp models, animal/) not humans/)) |
508472 |
|
19 |
17 and 18 |
291 |
|
18 |
exp Prednisone/ or exp Prednisolone/ or exp Dexamethasone/ or exp Betamethasone/ or exp Glucocorticoids/ or (exp Adrenal Cortex Hormones/ and exp Administration, Oral/) or glucocorticoid*.ti,ab,kf. or glucocorticosteroid*.ti,ab,kf. or glucocortoid*.ti,ab,kf. or glycocorticoid*.ti,ab,kf. or glycocorticosteroid*.ti,ab,kf. or predniso*.ti,ab,kf. or dexamethason*.ti,ab,kf. or bethamethason*.ti,ab,kf. or celeston*.ti,ab,kf. |
280271 |
|
17 |
16 not ((exp animals/ or exp models, animal/) not humans/) not (letter/ or comment/ or editorial/) |
9040 |
|
16 |
limit 15 to yr="2019 -Current" |
9716 |
|
15 |
8 or 14 |
78796 |
|
14 |
or/9-13 |
17388 |
|
13 |
ARS.tw,kf. and (sinonas* or nasal or naso* or rhin* or ENT).mp. |
214 |
|
12 |
((upper adj4 (respiratory or airway) adj2 infection*) or URTI).tw,kf. |
10469 |
|
11 |
coryza.tw,kf. |
694 |
|
10 |
((common or head) adj cold*).tw,kf. |
4448 |
|
9 |
common cold/ |
4294 |
|
8 |
or/1-7 |
63321 |
|
7 |
(rhinorr*.ti,ot,kf. not (ci.fs. or (CSF or ((leak* or fluid*) and cerebr*) or safet*).ti,ot,kf.)) or (purulent adj3 rhinorr*).tw,kf. |
619 |
|
6 |
nasal muc?us.tw,kf. |
898 |
|
5 |
((inflamm* or microb*) adj5 (rhino* or sinus or sinuses or sinusal)).tw,kf. |
2572 |
|
4 |
(sinusit* or rhinit* or ozena* or rhinosinusit* or nasosinusit* or pansinusit* or ethmoidit* or sphenoidit*).tw,kf. |
53114 |
|
3 |
exp paranasal sinuses/mi or (exp paranasal sinuses/ and (respiratory tract infections/ or chronic disease/)) |
2868 |
|
2 |
rhinitis/ or rhinitis, atrophic/ or rhinitis, vasomotor/ |
14668 |
|
1 |
exp sinusitis/ |
21511 |

