Leefstijl en dieetmaatregelen bij CNS
Uitgangsvraag
Is er bewijs om bij patiënten met chronische nierschade een gezonde leefstijl na te streven (dat wil zeggen een gezond lichaamsgewicht, voldoende lichamelijke inspanning, stoppen met roken en zout te beperken), teneinde progressie van chronische nierschade te voorkomen?
Is specifiek bij patiënten met chronische nierschade bariatrische chirurgie te overwegen in geval van ernstige obesitas, teneinde progressie van chronische nierschade te voorkomen?
Aanbeveling
Patiënten met chronische nierschade moeten worden gestimuleerd om:
- een gezond lichaamsgewicht na te streven (d.w.z. BMI 18,5-24,9 kg/m2);
- lichamelijke inspanning te leveren in overeenstemming met de adviezen vanuit de Norm Gezond Bewegen;
- roken te stoppen;
- zoutinname te beperken tot maximaal 6 gram (keukenzout (natriumchloride)) per dag.
Voor voedingsadviezen wordt verwezen naar de Richtlijnen Goede Voeding van de Gezondheidsraad [Gezondheidsraad, 2015].
Een verminderde nierfunctie vormt geen contra-indicatie voor het uitvoeren van bariatrische chirurgie. Voor indicaties voor bariatrische chirurgie wordt verwezen naar de richtlijn morbide obesitas. Er is geen extra meerwaarde aangetoond bij patiënten met chronische nierschade, maar ook geen extra risico.
Overwegingen
De kwaliteit van het bewijs is laag en de effecten zijn niet bewezen of beperkt. Desalniettemin zijn er goede argumenten die pleiten voor een gezonde leefstijl, bijvoorbeeld met betrekking tot algeheel welbevinden, cardiovasculaire en pulmonale effecten. Ook lijkt roken te zijn geassocieerd met progressie van nierschade.
Onderbouwing
Conclusies / Summary of Findings
|
laag |
Gewichtsverlies (door dieet of fysieke inspanning) bij patiënten met chronische nierschade is niet aantoonbaar van invloed op de nierfunctie. Bolignano, 2013; Huffel, 2014 |
|
laag |
Roken door patiënten met chronische nierschade leidt waarschijnlijk tot progressie van de nierschade. Het staat echter niet evident vast dat stoppen met roken de nierfunctie van patiënten met chronische nierschade verbetert. Elihimas, 2014; Johnson, 2004 |
|
laag |
Zoutbeperking door patiënten met chronische nierschade leidt waarschijnlijk niet tot een verbetering van de nierfunctie, maar mogelijk wel tot vermindering van de mate van albuminurie. McMahon, 2015 |
|
laag |
De effectiviteit van bariatrische chirurgie bij patiënten met chronische nierschade en morbide obesitas op de nierfunctie is niet goed bekend; de resultaten van de verschillende onderzoeken variëren van afwezig tot gunstig. Bolignano, 2013; Hou, 2013; Stephenson, 2013 |
|
laag |
Bariatrische chirurgie lijkt bij patiënten met chronische nierschade niet onveiliger te zijn dan bij patiënten zonder chronische nierschade, wanneer gekeken wordt naar uitkomsten 30 dagen postoperatief. Saleh, 2015 |
Samenvatting literatuur
Gewichtsverlies (dieet en fysieke inspanning)
Van Huffel et al. publiceerden in 2014 een systematische review over dieetbeperkingen en inspanning voor patiënten met diabetes mellitus en CNS [Huffel, 2014]. In deze studie werden RCT’s en observationele onderzoeken opgenomen met diverse interventies (bijv. 500 kcal reductie in calorieënintake, 3 maal per week 45 minuten training) bij patiënten met diabetes mellitus en CNS stadium 3-5. De geïncludeerde studies waren van lage tot matige kwaliteit (bijv. door gebrek aan blindering en onduidelijkheden in randomisatie) en vanwege heterogene populaties en interventies was meta-analyse van de resultaten niet mogelijk. De systematische review kon op basis van de gegevens uit de individuele studies geen uitspraak doen over de relatie tussen gewichtsverlies en/of lichamelijke inspanning en mortaliteit en/of cardiovasculaire events. Een aantal van de geïncludeerde studies geven wel resultaten op het gebied van nierfunctie. Zo wordt in één van de geïncludeerde studies (Morales et al, 2003 in Huffel, 2014) onder 30 patiënten met een BMI > 27kg/m2 een verschil van 11 ml/min/1,73 m2 in eGFR gevonden tussen de interventie- en controlegroep, waarbij de interventiegroep een dieet volgde met 500 kcal reductie gedurende 5 maanden (p<0,05) De BMI was na deze interventie gemiddeld 31,6 kg/m2 in de interventie- en 35 kg/m2 in de controlegroep (p<0,05). Een hypocalorisch dieet (1410 kcal) gedurende 12 maanden werd prospectief onderzocht bij 24 patiënten met CNS, diabetes mellitus en obesitas, waarbij de eGFR met 12 ml/min/1,73m2 (p=0,01) verbeterde en de BMI met 7,3 kg/m2 afnam (Solerte et al, 1989 in Huffel, 2014). De auteurs geven hierbij aan dat dit waarschijnlijk te verklaren is door verminderde eiwitintake en spierafbraak. Een laatste onderzoek bestudeerde het effect van 4 maal per week een laagcalorisch dieet (740-940 kcal) bij patiënten met diabetische nefropathie met overgewicht (BMI gemiddeld 30,4 kg/m2), waarbij geen significant resultaat op de nierfunctie werd gevonden (Saiti et al, 2005 in Huffel, 2014). De duur van de interventie is hierbij niet weergegeven. De BMI van deze patiënten nam met gemiddeld 2,2 kg/m2 af.
Bolignano et al. publiceerden in 2013 een systematische review over het effect van gewichtsvermindering op de nierfunctie bij obese patiënten met CNS [Bolignano, 2013]. In deze systematische review werden 31 randomized controlled trials en observationele onderzoeken geïncludeerd, gericht op gewichtsvermindering, door middel van dieet, inspanning, medicatie en bariatrische chirurgie. Ook in deze systematische review konden geen data gepoold worden in een meta-analyse en ook hier waren de geïncludeerde studies van lage tot matige kwaliteit. Ten opzichte van de review van Huffel et al. zijn aanvullende resultaten te melden. In een prospectief onderzoek onder 37 obese patiënten met CNS liet een dieet van 4 weken met 500 kcal vermindering een significante reductie van ernstig verhoogde albuminurie (p<0,001) en albuminurie (p=0,01) zien in de groep patiënten met diabetes mellitus (n=24); de grootte van het effect en de aanwezigheid van gewichtsverlies zijn niet weergegeven (Vasquez et al, 1984 in Bolignano, 2013). In een ander prospectief onderzoek onder 17 vrouwen met micro-albuminurie en obesitas resulteerde een interventie van drie maanden met dieet en inspanning bij 8/17 vrouwen in normo-albuminurie (Gilardini et al, 2010 in Bolignano, 2013). Effect op de eGFR werd niet gevonden; de BMI nam significant af (grootte van het effect niet vermeld). Een derde prospectief onderzoek onder 63 obese patiënten met ernstig verhoogde albuminurie evalueerde het effect van 24 maanden dieet met 500 kcal reductie en aerobe inspanning gedurende 3 keer per week (Shen et al, 2010 in Bolignano, 2013). Na 6 maanden werd 35% reductie van ernstig verhoogde albuminurie en 8,3% reductie van de BMI gezien en na 24 maanden 51% respectievelijk 9,2% (p<0,00001). Een randomized controlled trial onder 13 patiënten met CNS stadium 2-4 en obesitas en diabetes mellitus liet geen verschil in eGFR en lichaamsgewicht zien bij vergelijking van 18 weken 3 maal per week aerobe training met standaardzorg of met de situatie voor de training (Leehey et al, 2009 in Bolignano, 2013).
De systematische review van Sah et al. bleek bij bestudering van de fulltekst geen uitspraken te doen over renale en cardiovasculaire uitkomsten als effect van fysieke inspanning door patiënten met CNS [Sah, 2015]. Datzelfde geldt voor de systematische review van Heiwe et al. die zich met name richt op inspanningsvermogen [Heiwe, 2014], en die van Barcellos et al. die weliswaar als secundaire uitkomst kijkt naar progressie van CNS, maar hier eigenlijk geen uitspraak over doet [Barcellos, 2015]. De review van Painter et al. ten slotte bleek een narratieve in plaats van een systematische review te zijn [Painter, 2013]. Deze artikelen zijn daarom niet verder geanalyseerd.
Bariatrische chirurgie
In de eerder beschreven systematische review includeerden Bolignano et al. 7 prospectieve en 6 retrospectieve onderzoeken die het effect van bariatrische chirurgie evalueerden [Bolignano, 2013]. De chirurgische technieken varieerden tussen de onderzoeken (intestinal bypass, gastroplasty, bilio-pancreatic diversion, Roux-en-Y gastric bypass, sleeve gastrectomy). Patiënten in de onderzoeken hadden morbide obesitas (BMI gemiddeld 45-55 kg/m2). De resultaten konden vanwege heterogeniteit niet gepoold worden in een meta-analyse en de individuele onderzoeken kennen vanwege het observationele en deels retrospectieve design een behoorlijk risico op vertekening. De eGFR daalde in 6 studies, maar steeg in één. Ook met betrekking tot serum creatinine werden wisselende resultaten gevonden. De mate van albuminurie verminderde in 6 van de geïncludeerde studies en ernstig verhoogde albuminurie in 5 studies.
Na de studie van Bolignano et al. verscheen nog een aantal onderzoeken waarin het effect van bariatrische chirurgie bij patiënten met CNS werd onderzocht. In het onderzoek van Saleh et al. werd gekeken naar de veiligheid van bariatrische chirurgie gestratificeerd naar eGFR-klasse [Saleh, 2015]. Er is gebruik gemaakt van data van de American College of Surgeons National Surgical Quality Improvement Program, waarbij alle volwassen patiënten met een BMI ≥ 30 kg/m2 die een vorm van bariatrische chirurgie ondergingen, geïncludeerd zijn. Patiënten met een acute slechte gezondheid voor de ingreep werden geëxcludeerd. In de studie zijn 64.589 patiënten geïncludeerd (62% eGFR ≥ 90, 32% eGFR 60-89,9, 5% eGFR 30-59,9 en 1% eGFR < 30 ml/min/1,73 m2). Eindpunten waren de morbiditeit (overall en major) en de mortaliteit 30 dagen postoperatief. De resultaten laten een trend zien naar meer complicaties bij ernstigere nierschade, maar deze bevindingen zijn niet statistisch significant na correctie voor hypertensie, diabetes mellitus, leeftijd en BMI. De auteurs concluderen dat gevorderde nierschade niet geassocieerd is met een verhoogd risico op postoperatieve complicatie na bariatrische chirurgie.
Hou et al. beschreven de resultaten van bariatrische chirurgie bij 233 patiënten een jaar na de ingreep (uit een cohort van 450 patiënten, van wie laboratoriumwaarden bekend waren voor de ingreep) [Hou, 2013]. Van deze patiënten had 17% CNS stadium 2 en 3% stadium 3 CNS voor chirurgie. De gemiddelde eGFR in de stadium-2-groep steeg van 77 (sd: 17) naar 93 (sd: 20) (p<0,05) ml/min/1,73 m2 en in de stadium-3-groep van 50 (sd: 7) naar 67 (sd: 19) ml/min/1,73 m2 (p<0,05).
De retrospectieve studie van Stephenson et al. onderzocht de invloed van bariatrische chirurgie (laparoscopic gastric banding) bij patiënten met diabetes mellitus en micro- of macro-albuminurie op de mate van albuminurie [Stephenson, 2013]. In deze studie werden 23 patiënten geïncludeerd, van wie 16 met micro-albuminurie en 7 met macro-albuminurie. 2/7 patiënten met macro-albuminurie had 36 maanden na bariatrische chirurgie normo-albuminurie en 2/7 had micro-albuminurie. Bij 3/7 persisteerde de macro-albuminurie. Bij de patiënten met micro-albuminurie voorafgaand aan de chirurgie had na 36 maanden 9/16 normo-albuminurie, 6/16 microalbuminurie en 1/16 macro-albuminurie.
In het onderzoek van Amor et al. is gekeken naar de invloed van bariatrische chirurgie op de mate van albuminurie, maar hierbij is in de resultaten geen onderscheid gemaakt tussen patiënten met en zonder CNS bij baseline (27% had ACR ≥ 30 mg/g, gemiddelde ACR bij baseline 55,05 (sd 139,1), zodat de resultaten van deze studie niet kunnen worden gebruikt voor deze richtlijn [Amor, 2013]. Datzelfde geldt voor de studie van Fenske et al., die een prospectief onderzoek hebben gedaan naar de effecten van bariatrische chirurgie op de nierfunctie en de bloeddruk [Fenske, 2013], die van Ruiz-Tovar et al. uit 2015 over gastrectomie bij patiënten met morbide obesitas ouder dan 40 jaar [Ruiz-Tovar, 2015], en die van Jose et al. over het effect van biliopancreatic diversion chirurgie op de nierfunctie [Jose, 2013]. Het onderzoek van Tham et al. bleek bij bestudering van de fulltekst een narratieve review te zijn en wordt hier niet verder besproken.
Stoppen met roken
Elihimas et al. onderzochten de relatie tussen roken en CNS in een systematische review uit 2014 [Elihimas, 2014]. In deze review zijn 5 patiënt-controle onderzoeken en 7 cohortonderzoeken geïncludeerd. Zes van de geïncludeerde studies laten een relatie zien tussen roken en progressie van CNS. Vijf van de geïncludeerde studies laten een dosis-effectrelatie zien tussen roken en de progressie van CNS. In de review zijn geen studies opgenomen die het effect van stoppen met roken bij patiënten met nierschade evalueren.
Clase beschreef de evidence rondom diverse medicamenteuze en leefstijlinterventies bij patiënten met CNS [Clase, 2011]. Uit deze systematische review blijkt dat er geen randomized controlled trials zijn die het effect van stoppen met roken bij patiënten met CNS onderzocht hebben.
Johnson komt in een systematische review in 2004 tot dezelfde conclusie, maar beschrijft wel een patiënt-controle onderzoek dat laat zien dat (huidig) roken een onafhankelijke risicofactor is voor ernstig verhoogde albuminurie en afname van de nierfunctie [Johnson, 2004] (Bleyer et al, 2000 in Johnson, 2004). Uit dezelfde studie bleek dat ex-rokers dit verhoogde risico niet hadden, wat suggereert dat stoppen met roken geassocieerd zou zijn met een verminderd risico op progressie van nierschade. Uit een andere studie in deze review kwam naar voren dat stoppen met roken geassocieerd is met een vermindering van albumine-excretie en progressie van nierschade bij patiënten met diabetes mellitus (Sawicki et al, 1994 in Johnson, 2004).
Zoutbeperking
In 2015 verscheen een Cochrane systematische review over gewijzigde zoutintake bij patiënten met CNS [McMahon, 2015]. In deze prima opgezette systematische review werden 8 randomized controlled trials geïncludeerd. De onderliggende studies waren van wisselende kwaliteit, vanwege bijvoorbeeld problemen met randomisatie en blindering. Ook was er sprake van heterogeniteit in populatie en interventies en waren de studies vaak van relatief korte duur. In de review zijn diverse (vooraf vastgestelde) uitkomstmaten bestudeerd; voor deze richtlijn is met name gekeken naar de eGFR en endogene creatinineklaring op basis van de 24-uurs urine. De resultaten, bij een beperkt aantal patiënten, zijn weergegeven in onderstaande figuren.

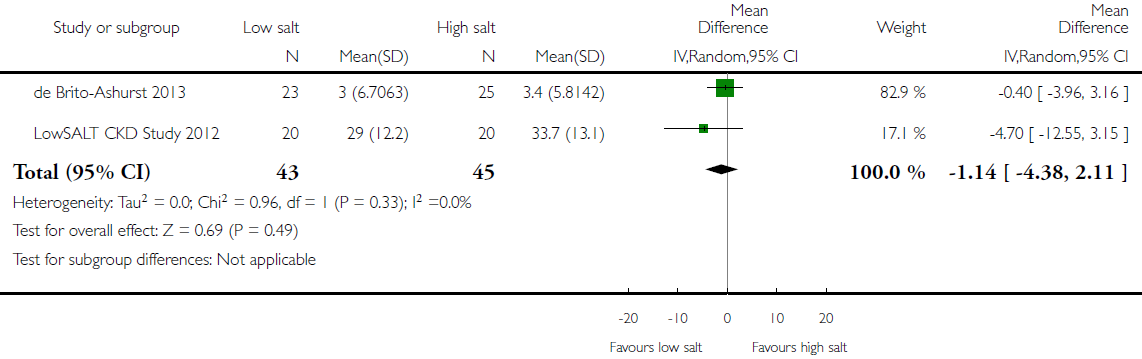
Figuur 1. Meta-analyse van zoutbeperking versus normale zoutintake en het effect op de eGFR (ml/min/1,73 m2)

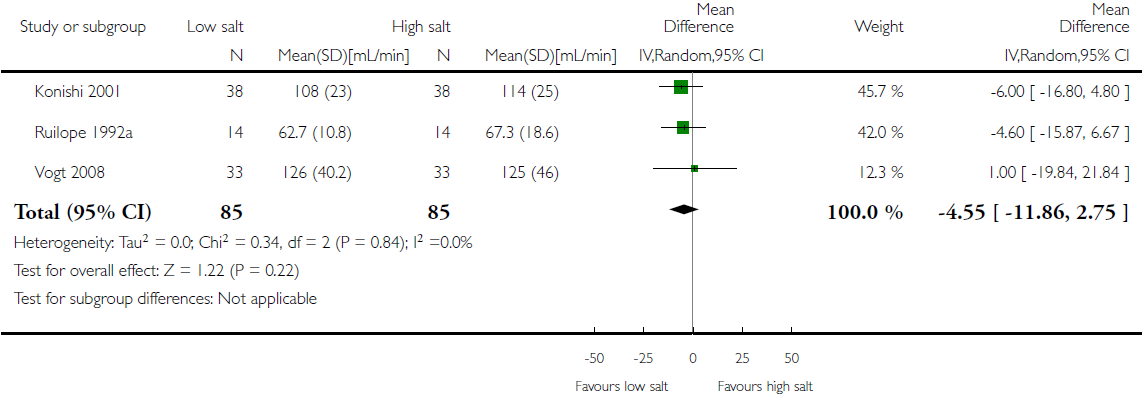
Figuur 2. Meta-analyse van zoutbeperking versus normale zoutintake en het effect op de creatinineklaring (ml/min)
Beide vergelijkingen laten geen statistisch significant effect zien. In de review zijn geen gepoolde resultaten opgenomen voor wat betreft vermindering van albuminurie, maar de auteurs beschrijven dat de geïncludeerde studies reductie van albuminurie laten zien bij zoutrestrictie.
Het onderzoek van Ash et al., een systematische review over voedingsadviezen bij patiënten met CNS, rapporteerde geen effecten van zoutrestrictie op renale uitkomstmaten [Ash, 2014].
Zoeken en selecteren
Voor een antwoord op deze uitgangsvragen is op twee manieren naar literatuur gezocht. Voor de leefstijladviezen is op 8 februari 2016 naar literatuur gezocht in PubMed. Dit leverde 82 abstracts op. Aanvullend is gezocht naar literatuur over stoppen met roken bij patiënten met CNS op 19 februari 2016. Dit leverde 42 abstracts op. Voor de vraag rondom bariatrische chirurgie is op 8 februari 2016 gezocht in Medline (zie de literatuursearches bij de zoekverantwoording). Dit leverde (ontdubbeld) 229 abstracts op. Deze abstracts zijn op onderwerp (sluit het artikel aan bij de uitgangsvraag?) en op research design (systematische reviews) geselecteerd, wat resulteerde in 16 artikelen, die fulltekst zijn beoordeeld. Voor het onderwerp bariatrische chirurgie is naar aanvullende evidence gezocht, verschenen na de laatste systematische review. De evidence is volgens de principes van de GRADE methodiek beoordeeld.
Referenties
- Amor A, Jimenez A, Moizé V, Ibarzabal A, Flores L, Lacy AM, Vidal J. Weight loss independently predicts urinary albumin excretion normalization in morbidly obese type 2 diabetic patients undergoing bariatric surgery. Surg Endosc 2013; 27: 2046-51.
- Ash S, Campbell KL, Bogard J, Millichamp A. Nutrition prescription to achieve positive outcomes in chronic kidney disease: a system-atic review. Nutrients 2014; 6: 416-51.
- Barcellos FC, Santos IS, Umpierre D, Bohlke M, Hallal PC. Effects of exercise in the whole spectrum of chronic kidney disease: a systematic review. Clin Kidney J 2015; 8: 753-65.
- Bolignano D, Zoccali C. Effects of weight loss on renal function in obese CKD patients: a systematic review. Nephrol Dial Transplant 2013; 28: iv82-98.
- Clase C. Renal failure (chronic). Clin Evid 2011; 05: 2004
- Elihimas UF, Elihimas, HCdS, Lemos VM, Albuquerque Leao M de, Barros de Oliveria S MP, Tenorio de Franca EE, et al. Smoking as a risk factor for chronic kidney disease: systematic review. J Bras Nefrol 2014; 36:519-28.
- Fenske WK, Dubb S, Bueter M, Seyfried F, Patel K, Tam FWK, et al. Effect of bariatric surgery-induced weight loss on renal and sys-temic inflammation and blood pressure: a 12-month prospective study. Surg Obes Relat Dis2013; 9: 559-68.
- Gezondheidsraad. Richtlijnen goede voeding. Den Haag: Gezondheidsraad, 2015; publicatienr. 2015/24.
- Heiwe S, Jacobson SH. Exercise training in adults with CKD: a systematic review and meta-analysis. Am J Kidney Dis 2014; 64: 383-93.
- Hou C-C, Shyu R-S, Lee W-J, Ser K-H, Lee Y-C, Chen S-C. Improved renal function 12 months after bariatric surgery. Surg Obes Relat Dis 2013; 9: 202-6.
- Huffel L van, Tomson CRV, Ruige J, Nistor I, Biesen W van, Bolignano D. Dietary restriction and exercise for diabetic patients with chronic kidney disease: a systematic review. PLOS One 2014; 9: e113667.
- Johnson DW. Evidence-based guide to slowing the progression of early renal insufficiency. Int Med J 2004; 34: 50-7
- Jose B, Ford S, Super P, Thomas GN, Dasgupta I, Taheri S. The effect of biliopancreatic diversion surgery on renal function a retro-spective study. Obes Surg 2013; 23: 634-7.
- McMahon EJ, Campbell KL, Bauer JD, Mudge DW. Altered dietary salt intake for people with chronic kidney disease. Cochrane Data-base of Systematic Reviews 2015, Issue 2. Art. No.: CD010070. DOI: 10.1002/14651858.CD010070.pub2.
- Nederlands Huisartsen Genootschap. Multidisciplinaire richtlijn Cardiovasculair risicomanagement. NHG, 2011.
- Painter P, Roshanravan B. The association of physical activity and physical function with clinical outcomes in adults with chronic kidney disease. Curr Opin Nephrol Hypertens 2013; 22: 615-23.
- Ruiz-Tovar J, Giner L, Sarro-Sobrin F, Alsina ME, Paz Marco M, Craver L. Laparoscopic sleeve gastrectomy prevents the deterioration of renal function in morbidly obese patients over 40 years. Obes Surg 2015; 25: 796-9.
- Sah SK, Siddiqui MA, Darain H. Effect of progressive resistive exercise training in improving mobility and functional ability of middle adulthood patients with chronic kidney disease. Saudi J Kidney Dis Transpl 2015; 26: 912-23.
- Saleh F, Kim SJ, Okrainec A, Jackson TD. Bariatric surgery in patients with reduced kidney function: an analysis of short-term out-comes. Surg Obes Relat Dis 2015; 11: 828-35.
- Stephenson DT, Jandeleit-Dahm K, Balkau B, Cohen N. Improvement in albuminuria in patients with type 2 diabetes after laparoscopic adjustable gastric banding. Diab Vasc Dis Res 2013; 10: 514-9.
- Tham JC, Le Roux CW, Docherty NG. Cardiovascular, renal and overall health outcomes after bariatric surgery. Curr Cardiol Rep 2015; 17: 34.
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 06-04-2018
Beoordeeld op geldigheid : 18-01-2018
Jaarlijks wordt door de initiatiefnemers van de ontwikkeling van deze richtlijn bepaald of actualisatie van de richtlijn nodig is. Indien actualisatie gewenst is, spannen de initiatiefnemers zich in om de hiervoor noodzakelijke voorwaarden (bijvoorbeeld financiering, samenstelling werkgroep) te realiseren. Nieuwe of nog niet behandelde knelpunten kunnen aanleiding zijn tot actualisatie van de richtlijn.
Algemene gegevens
Deze richtlijn is ontwikkeld in samenwerking met:
- Koninklijke Nederlandse Maatschappij ter Bevordering der Pharmacie
- Nederlandse Federatie voor Nefrologie
- Nederlandse Vereniging van Diëtisten / Diëtisten Nierziekten Nederland
- Nederlandse Vereniging van Ziekenhuisapothekers
- Nederlandse Vereniging voor Klinische Chemie en Laboratoriumgeneeskunde
- Nierpatiënten Vereniging Nederland
Met ondersteuning van:
- Nederlands Huisartsen Genootschap
- Nederlandse Internisten Vereniging
- PROVA
De ontwikkeling van deze richtlijn is gefinancierd vanuit een projectbudget door de Stichting Kwaliteitsgelden Medisch Specialisten en het Nederlands Huisartsen Genootschap.
Doel en doelgroep
Doel
Het doel van deze richtlijn is de kwaliteit van zorg en patiëntveiligheid van patiënten met CNS te waarborgen en waar mogelijk te verbeteren. In deze richtlijn zijn aanbevelingen geformuleerd die professionals in de zorg hiertoe handvaten geven. Daarbij is het doel bovendien de zorg in de eerste en tweede lijn zoveel mogelijk op elkaar af te stemmen en daarbij uitdrukkelijk het patiëntenperspectief een plaats te geven.
Doelgroep
De doelgroep van deze richtlijn zijn professionals die zich bezig houden met de zorg voor patiënten met CNS. Hieronder worden in ieder geval verstaan: huisartsen, internisten, internist-nefrologen, apothekers, laboratoriumspecialisten klinische chemie en diëtisten. Ook andere professionals, zoals andere medisch specialisten, verpleegkundigen en maatschappelijk werkenden, kunnen hun voordeel doen met deze richtlijn.
Samenstelling werkgroep
Voor de ontwikkeling van deze richtlijn is een multidisciplinaire werkgroep ingesteld, onder voorzitterschap van dhr. dr. Marc Hemmelder, internist-nefroloog, en mw. drs. Jacintha van Balen, huisarts. In de werkgroep hebben gemandateerde vertegenwoordigers van de volgende beroepsverenigingen zitting:
- Koninklijke Nederlandse Maatschappij ter Bevordering der Pharmacie
- Nederlands Huisartsen Genootschap
- Nederlandse Internisten Vereniging / Nederlandse Federatie voor Nefrologie
- Nederlandse Vereniging van Diëtisten / Diëtisten Nierziekten Nederland
- Nederlandse Vereniging van Ziekenhuisapothekers
- Nederlandse Vereniging voor Klinische Chemie en Laboratoriumgeneeskunde
Om het patiëntenperspectief in de werkgroep te waarborgen, hadden twee vertegenwoordigers van de Nierpatiënten Vereniging Nederland zitting in de werkgroep. De werkgroep werd procedureel en methodologisch ondersteund door PROVA. Logistieke ondersteuning is gegeven door de Nederlandse Internisten Vereniging en het Nederlands Huisartsen Genootschap. Het secretariaat is gevoerd door het Nederlands Huisartsen Genootschap.
Synchroon aan de ontwikkeling van deze multidisciplinaire richtlijn zijn de NHG-Standaard Chronische Nierschade en aanvullende NIV-modules Chronische Nierschade ontwikkeld. De werkgroepleden van de Standaardwerkgroep en van de NIV-werkgroep maakten deel uit van de werkgroep van de multidisciplinaire richtlijn, om zo alle trajecten zo veel mogelijk op elkaar af te stemmen.
- Mw. drs. Jacintha van Balen, huisarts, Nederlands Huisartsen Genootschap, Utrecht, namens het Nederlands Huisartsen Genootschap – voorzitter
- Dhr. dr. Marc Hemmelder, internist-nefroloog, Nefrovisie, Utrecht, namens de Nederlandse Internisten Vereniging en de Nederlandse Federatie voor Nefrologie – voorzitter
- Mw. drs. Mariska Tuut, epidemioloog, PROVA, Varsseveld – secretaris
- Dhr. Peter van Cuijk, Apeldoorn, ervaringsdeskundige, namens de Nierpatiënten Vereniging Nederland
- Dhr. prof. dr. Ron Gansevoort, internist-nefroloog, UMC Groningen, namens de Nederlandse Internisten Vereniging en de Nederlandse Federatie voor Nefrologie
- Dhr. dr. Wim de Grauw, huisarts te Berghem, Radboudumc, Nijmegen, namens het Nederlands Huisartsen Genootschap
- Mw. Inez Jans, diëtist, Ziekenhuis Gelderse Vallei, Ede, namens Nederlandse Vereniging van Diëtisten en Diëtisten Nierziekten Nederland
- Mw. dr. Birgit Koch, ziekenhuisapotheker-klinisch farmacoloog, Erasmus MC, Rotterdam, namens de Nederlandse Vereniging van Ziekenhuisapothekers
- Mw. drs. Karen de Leest, apotheker, Apotheek de Roerdomp, Nieuwegein, namens de Koninklijke Nederlandse Maatschappij ter Bevordering der Pharmacie
- Mw. drs. Karen Prantl, Bussum, coördinator kwaliteit & onderzoek, Nierpatiënten Vereniging Nederland, namens de Nierpatiënten Vereniging Nederland
- Dhr. dr. Paul Schenk, laboratoriumspecialist klinische chemie / klinisch chemicus, LUMC, Leiden, namens de Nederlandse Vereniging voor Klinische Chemie en Laboratoriumgeneeskunde
- Mw. dr. Nynke Scherpbier, huisarts, Radboudumc, Nijmegen, namens het Nederlands Huisartsen Genootschap
- Mw. drs. Judith Tjin-A-Ton, huisarts, Amstelveen, namens het Nederlands Huisartsen Genootschap
- Mw. dr. Neelke van der Weerd, internist-nefroloog, AMC, Amsterdam, namens de Nederlandse Internisten Vereniging en de Nederlandse Federatie voor Nefrologie
Belangenverklaringen
|
Naam |
Namens |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Reputatie-management |
Extern gefinancierd onderzoek |
Kennis-valorisatie |
Overige belangen |
|
Jacintha van Balen |
NHG |
Huisarts 0,6 FTE; Teamleider afdeling Richtlijnen en Wetenschap |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
|
Marc Hemmelder |
NIV / NFN |
Internist-nefroloog Medisch Centrum Leeuwarden (0,6 FTE) Uitvoerend bestuurder Nefrovisie (0,4 FTE) |
Geen |
Geen |
Geen |
Geen |
Dolomites studie van Astellas |
Renine, registratie van patiënten met nierfunctievervaning in Nederland. Onderdeel van Nefrovisie |
Geen |
|
Mariska Tuut |
onafhankelijk |
Eigenaar PROVA, adviesbureau voor procesmatige en methodologische ondersteuning bij de ontwikkeling van evidence-based richtlijnen en andere kwaliteitsinstrumenten |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
|
Peter van Cuijk |
NVN |
Ruim 35 jaar gewerkt in de Jeugdhulpverlening als orthopedagoog en manager. Ervaring in diverse settingen en diverse functie's, zowel inhoudelijk, uitvoerend en in de aansturing/management. |
bestuursfunctie (penningmeester) amateur-theatervereniging De Apeldoornse Komedie |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
|
Ron Gansevoort |
NIV / NFN |
Internist-nefroloog, UMCG |
Lid bestuur Nederlandse Federatie voor Nefrologie (sectie Wetenschap); Lid Wetenschappelijke Adviesraad Nierstichting; Lid redactie wetenschappelijke tijdschriften: American Journal of Kidney Diseases, Clinical Journal of the American Society of Neprology, European Medical Journal Nephrology, Journal of Nephrology, Nephrology Dialysis and Transplantation, Nephron Clinical Practice (alle functies onbetaald) |
Geen |
Geen |
Lid wetenschappelijke adviesraad Nierstichting |
Geen |
Geen |
Geen |
|
Wim de Grauw |
NHG |
Huisarts te Berghem (0,7 fte); Senior staflid huisarts-onderzoeker afdeling Eerstelijns Geneeskunde Radboudumc Nijmegen (0,3 fte) |
Herder bij diverse professionele begrazingsbedrijven |
Geen |
Geen |
Onderzoek op het gebied van Chronische Nierschade is een belangrijk onderdeel van de onderzoekslijn vaatschade van de afdeling Eerstelijnsgeneeskunde Radboudumc in samenwerking met de afdeling Nefrologie Radboudumc |
De afdeling Eerstelijns Geneeskunde ontvangt subsidie van de Nierstichting Nederland voor onderzoek op het gebied van Chronische Nierschade |
Afdeling Eerstelijnsgeneeskunde Radboudumc heeft samen met de afdeling Nefrologie Radboudumc en Zorgdomein Telenefrologie ontwikkeld, een e-health applicatie voor consultatie tussen huisarts en nefroloog |
Geen |
|
Inez Jans |
NVD / DNN |
Diëtist, aandachtsgebied nierziekten en voedingsteam, Ziekenhuis Gelderse Vallei (fulltime dienstverband) |
Extern assessor Hogeschool van Arnhem en Nijmegen, opleiding Voeding en Diëtetiek (flex contract); Actief lid Diëtisten Nierziekten Nederland (voorzitter DNN werkgroep kwaliteit; lid DNN werkgroep richtlijnen); vanuit die rol lid van de werkgroep multidisciplinaire richtlijn chronisch nierfalen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
|
Birgit Koch |
NVZA |
Ziekenhuisapotheker-klinisch farmacoloog 0,85 FTE |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
ZonMw: PK/PD antipsychotica; Stichting Coolsingel: middelenmisbruik zwangerschap |
n.v.t. |
n.v.t. |
|
Karen de Leest |
KNMP |
Apotheker, Apotheek de Roerdomp, Nieuwegein, 24 uur/week |
Wetenschappelijk medewerker KNMP, 10 uur/week |
Geen |
Geen |
Redactielid Vascuzine, tijdschrift v.d. Vasculitis patiënten vereniging, vrijwilligerswerk, geen boegbeeldfunctie |
Geen |
Geen |
Nee |
|
Karen Prantl |
NVN |
Beleidsmedewerker kwaliteit |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
|
Paul Schenk |
NVKC |
Klinisch chemicus/ laboratoriumspecialist Klinische chemie, LUMC Leiden (voltijds, loondienst) |
Geen nevenwerkzaamheden buiten LUMC |
Geen persoonlijke financiële belangen |
Geen relevante persoonlijke relaties als hier bedoeld |
Geen relevante posities als hier bedoeld |
Geen relevant extern gefinancierd onderzoek |
Geen relevante valorisatie |
Nee, geen relevante overige belangen |
|
Nynke Scherpbier |
NHG |
Opleidingsdirecteur extramurale vervolgopleidingen RadboudUMC 0,8 FTE; huisarts 0,2 FTE |
Council member EURACT, Europese organisatie voor opleiden in de huisartsgeneeskunde (onbetaald) |
Geen |
Geen |
Geen |
Ik ben co-promotor van een promotietraject dat wordt gefinancierd door de Nierstichting met als doel te onderzoeken: 1. wat belemmerende en bevorderende factoren zijn in het naleven van de LTA; 2. hoe patiënten de voorlichting over CNS ervaren; 3. of het mogelijk is om veilige wijze bepaalde patiënten terug te verwijzen vanuit de tweede naar de eerste lijn |
Afdeling Eerstelijnsge-neeskunde Radbou-dumc heeft samen met de afdeling Nefro-logie Radboudumc en Zorgdomein Telenefrologie ontwikkeld, een e-health applicatie voor consultatie tus-sen huisarts en nefroloog |
Geen |
|
Judith Tjin-A-Ton |
NHG |
Huisarts |
Kaderhuisarts hart- en vaatziekten: kwaliteitscommissie en werkgroep HVZ bij Amstellandzorg BV (betaald) |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
|
Neelke van der Weerd |
NIV / NFN |
Internist-nefroloog AMC Amsterdam |
- |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
Methode ontwikkeling
Evidence based
Implementatie
Gedurende het hele proces van richtlijnontwikkeling is rekening gehouden met implementatie van de richtlijn in de praktijk, bijvoorbeeld bij de samenstelling van de werkgroep, de brede knelpunteninventarisatie en de uitgebreide commentaarronde. De werkgroep heeft adviezen voor implementatie (implementatieplan) en indicatoren geformuleerd. Deze zijn opgenomen onder de aanverwante producten.
Na autorisatie van de richtlijn wordt deze ten minste op de website van de Nederlandse Internisten Vereniging en het Nederlands Huisartsen Genootschap gepubliceerd. Ook andere deelnemende partijen zijn vrij de richtlijn op hun website te publiceren. De richtlijn wordt ter publicatie aangeboden aan www.richtlijnendatabase.nl. Daarnaast wordt getracht samenvattingen van de richtlijn in Nederlandse tijdschriften te publiceren, aandacht aan de richtlijn te besteden op congressen, en nascholingsmateriaal en voorlichtingsmateriaal te ontwikkelen, om zo de implementatie van de richtlijn te bevorderen.
Een voor patiënten begrijpelijke samenvatting van de aanbevelingen uit deze richtlijn komt beschikbaar via www.thuisarts.nl. Een verdieping daarvan komt beschikbaar via de website van de Nierstichting/Nederlandse Vereniging van Nierpatiënten.
Werkwijze
Knelpunteninventarisatie
De richtlijnwerkgroep heeft in de eerste werkgroepvergadering knelpunten benoemd in de zorg voor patiënten met CNS. Deze knelpunten zijn in een invitational conference voorgelegd aan belanghebbenden, waarbij ook is gediscussieerd over aanvullende knelpunten. Voor deze invitational conference zijn, naast vertegenwoordigers van verenigingen die in de werkgroep afgevaardigd zijn, de volgende partijen uitgenodigd:
- Federatie Medisch Coördinerende Centra
- Inspectie voor de Gezondheidszorg
- Nederlandse Federatie van Universitair Medische Centra
- Nederlandse Vereniging van Ziekenhuizen
- Nederlandse Zorgautoriteit
- Nierstichting Nederland
- Patiëntenfederatie Nederland
- Vereniging Innovatieve Geneesmiddelen
- Vereniging Maatschappelijk Werk Nefrologie
- Verpleegkundigen & Verzorgenden Nederland
- ZorgInstituut Nederland
- Zorgverzekeraars Nederland
De richtlijnwerkgroep heeft de input vanuit de knelpunteninventarisatie geanalyseerd en in de tweede werkgroepvergadering de knelpunten en uitgangsvragen vastgesteld.
Uitwerking knelpunten en uitgangsvragen in conceptrichtlijn
Per knelpunt werd door de werkgroep vooraf bepaald op welke wijze dit knelpunt zou worden behandeld: met behulp van systematisch literatuuronderzoek (evidence-based) of meer op basis van bestaande richtlijnen en professionele expertise in de werkgroep. Er was financiering voor de uitwerking van een beperkt aantal vragen met behulp van systematisch literatuuronderzoek. Om toch ook de andere belangrijke knelpunten een plaats te geven in deze richtlijn, is voor uitwerking van de resterende knelpunten voor een minder arbeidsintensieve wijze gekozen. De wijze van uitwerking van de knelpunten/uitgangsvragen staat per uitgangsvraag vermeld in de verschillende modules van deze richtlijn. De keuze van de knelpunten die met systematisch literatuuronderzoek zijn beantwoord is gemaakt door de gezamenlijke werkgroep, op basis van verwachting dat het literatuuronderzoek mogelijk tot nieuwe inzichten zou leiden en de afwezigheid van recente internationale richtlijnen over de specifieke uitgangsvraag.
De uitwerking van de knelpunten in conceptteksten werd voorbereid door de epidemioloog die bij de ontwikkeling van de richtlijn betrokken was. Per knelpunt werd deze inhoudelijk bijgestaan door een aantal werkgroepleden, afhankelijk van het onderwerp. De conceptteksten werden plenair tijdens de werkgroepvergaderingen besproken, en na discussie bijgesteld. De richtlijnwerkgroep is 9 maal bijeen geweest, alvorens de conceptrichtlijn is vastgesteld.
Bij veel uitgangsvragen is voor de onderbouwing gebruik gemaakt van internationale richtlijnen op het gebied van CNS. De KDIGO richtlijn en de NICE richtlijn over chronische nierschade zijn op kwaliteit beoordeeld bij aanvang van de ontwikkeling van deze multidisciplinaire richtlijn. De wijze van onderbouwing van deze internationale richtlijnen werd door de richtlijnwerkgroep als adequaat beoordeeld. Beide richtlijnen maakten gebruik van de GRADE methodiek.
Voor de uitgangsvragen die met behulp van systematisch literatuuronderzoek zijn uitgewerkt, is gebruik gemaakt van de principes van de GRADE Working Group. Voor achtergrondinformatie over deze methodiek wordt verwezen naar het Dutch GRADE Network (www.dutchgradenetwork.org). Vanwege de verschillende totstandkoming van de diverse aanbevelingen heeft de werkgroep ervoor gekozen om het graderen van aanbevelingen, zoals dit wordt gepropageerd in de GRADE-methodiek, niet door te voeren in deze richtlijn. Hiermee is eenheid in de formulering van aanbevelingen gecreëerd.
De module ‘Samenwerking bij CNS’ bevat samenwerkingsafspraken: aanbevelingen voor consultatie en verwijzing tussen eerste en tweede lijn, en aanbevelingen voor samenwerking met laboratoriumspecialisten klinische chemie, diëtisten en apothekers. Hierbij zijn geen specifieke uitgangsvragen genoemd, maar is uitgegaan van eerdere samenwerkingsafspraken en uitgangspunten en aanbevelingen uit de modules ‘Diagnostiek en stadiëring bij CNS’ en ‘Beleid en behandeling bij CNS’.
Daar waar in deze richtlijn ‘hij’ genoemd staat, kan ook ‘zij’ gelezen worden.
Commentaar en autorisatie
De conceptrichtlijn is ter commentaar aangeboden aan alle partijen die bij de knelpunteninventarisatie om input gevraagd zijn. Het binnengekomen commentaar is door de werkgroep beoordeeld en verwerkt in de richtlijn. Daarbij is beargumenteerd welke commentaren wel en welke niet zijn overgenomen.
Daarna is de richtlijn ter autorisatie voorgelegd aan de partijen die in de werkgroep vertegenwoordigd zijn. De richtlijn is geautoriseerd door de Nederlandse Internisten Vereniging, het Nederlands Huisartsen Genootschap, de Nederlandse Vereniging voor Diëtisten, de Nederlandse Vereniging voor Ziekenhuisapothekers en de Nederlandse Vereniging voor Klinische Chemie en Laboratoriumgeneeskunde. Ook is de richtlijn goedgekeurd door de Nierpatiënten Vereniging Nederland.
Juridische betekenis van richtlijnen
Richtlijnen zijn geen wettelijke voorschriften, maar op ‘evidence' gebaseerde inzichten en aanbevelingen waaraan zorgverleners moeten voldoen om kwalitatief goede zorg te verlenen. Na autorisatie van de richtlijn door een beroepsvereniging, wordt de richtlijn gezien als deel van de ‘professionele standaard'. Aangezien de aanbevelingen hoofdzakelijk gebaseerd zijn op de ‘gemiddelde patiënt', kunnen zorgverleners op basis van hun professionele autonomie waar nodig afwijken van de richtlijn. Afwijken van richtlijnen kan in bepaalde situaties zelfs noodzakelijk zijn. Wanneer van de richtlijn wordt afgeweken, dient dit beargumenteerd en gedocumenteerd te worden.
Zoekverantwoording
Leefstijladviezen, d.d. 8 februari 2016
("renal insufficiency, chronic"[MeSH Major Topic] OR chronic renal failure[tiab] OR chronic kidney failure[tiab] OR chronic kidney disease[tiab] OR renal insufficiency[tiab]) AND (healthy lifestyle[tiab] OR (lifestyle modification[tiab] OR lifestyle modifications[tiab]) OR healthy weight[tiab] OR salt intake[tiab] OR exercise[tiab] OR weight loss[tiab] OR smoking cessation[tiab]) AND ((meta analaysis[tiab] OR meta analise[tiab] OR meta analises[tiab] OR meta analisis[tiab] OR meta analitic[tiab] OR meta analiyze[tiab] OR meta analogs[tiab] OR meta analogue[tiab] OR meta analogues[tiab] OR meta analsis[tiab] OR meta analsysis[tiab] OR meta analyis[tiab] OR meta analyisis[tiab] OR meta analysable[tiab] OR meta analyse[tiab] OR meta analysed[tiab] OR meta analysei[tiab] OR meta analysen[tiab] OR meta analysers[tiab] OR meta analyses[tiab] OR meta analysescohort[tiab] OR meta analysespublication[tiab] OR meta analysestype[tiab] OR meta analysi[tiab] OR meta analysia[tiab] OR meta analysic[tiab] OR meta analysing[tiab] OR meta analysis[tiab] OR meta analysis's[tiab] OR meta analysis,[tiab] OR meta analysisdagger[tiab] OR meta analysises[tiab] OR meta analysisevaluating[tiab] OR meta analysisintroduction[tiab] OR meta analysisjr[tiab] OR meta analysismoderate[tiab] OR meta analysisof[tiab] OR meta analyst[tiab] OR meta analysticians[tiab] OR meta analysts[tiab] OR meta analysys[tiab] OR meta analytic[tiab] OR meta analytical[tiab] OR meta analytically[tiab] OR meta analytics[tiab] OR meta analyzable[tiab] OR meta analyze[tiab] OR meta analyzed[tiab] OR meta analyzes[tiab] OR meta analyzing[tiab]) OR systematic review[tiab] OR systematic[sb]) NOT (child[tiab] OR children[tiab]) AND (hasabstract[text] AND ("2000/01/01"[PDAT] : "3000/12/31"[PDAT]) AND (English[lang] OR Dutch[lang] OR French[lang] OR German[lang]))
Stoppen met roken, d.d. 19 februari 2016
("renal insufficiency, chronic"[MeSH Major Topic] OR chronic renal failure[tiab] OR chronic kidney failure[tiab] OR chronic kidney disease[tiab] OR renal insufficiency[tiab]) AND ("smoking"[MeSH Terms] OR "smoking"[All Fields]) AND ((meta analaysis[tiab] OR meta analise[tiab] OR meta analises[tiab] OR meta analisis[tiab] OR meta analitic[tiab] OR meta analiyze[tiab] OR meta analogs[tiab] OR meta analogue[tiab] OR meta analogues[tiab] OR meta analsis[tiab] OR meta analsysis[tiab] OR meta analyis[tiab] OR meta analyisis[tiab] OR meta analysable[tiab] OR meta analyse[tiab] OR meta analysed[tiab] OR meta analysei[tiab] OR meta analysen[tiab] OR meta analysers[tiab] OR meta analyses[tiab] OR meta analysescohort[tiab] OR meta analysespublication[tiab] OR meta analysestype[tiab] OR meta analysi[tiab] OR meta analysia[tiab] OR meta analysic[tiab] OR meta analysing[tiab] OR meta analysis[tiab] OR meta analysis's[tiab] OR meta analysis,[tiab] OR meta analysisdagger[tiab] OR meta analysises[tiab] OR meta analysisevaluating[tiab] OR meta analysisintroduction[tiab] OR meta analysisjr[tiab] OR meta analysismoderate[tiab] OR meta analysisof[tiab] OR meta analyst[tiab] OR meta analysticians[tiab] OR meta analysts[tiab] OR meta analysys[tiab] OR meta analytic[tiab] OR meta analytical[tiab] OR meta analytically[tiab] OR meta analytics[tiab] OR meta analyzable[tiab] OR meta analyze[tiab] OR meta analyzed[tiab] OR meta analyzes[tiab] OR meta analyzing[tiab]) OR systematic review[tiab] OR systematic[sb]) NOT (child[tiab] OR children[tiab]) AND (hasabstract[text] AND ("2000/01/01"[PDAT] : "3000/12/31"[PDAT]) AND (English[lang] OR Dutch[lang] OR French[lang] OR German[lang]))
Bariatrische chirurgie, d.d. 8 februari 2016
Searchstring
Database: Ovid MEDLINE(R) In-Process & Other Non-Indexed Citations, Ovid MEDLINE(R) Daily and Ovid MEDLINE(R) <1946 to Present>
Search Strategy:
--------------------------------------------------------------------------------
1 "chronische nierschade".ti. (0)
2 renal insufficiency, chronic/ (9710)
3 exp kidney failure, chronic/ (81692)
4 kidney diseases/ and chronic.ti,ab. (10847)
5 ((chronic or progressive) adj2 (renal or kidney)).ti,ab. (61110)
6 (chronic adj (kidney or renal) adj insufficienc*).ti,ab. (4615)
7 CKD.ti,ab. (15408)
8 ((chronic or progressive) adj2 (renal or kidney)).kf. (2874)
9 (chronic adj (kidney or renal) adj insufficienc*).kf. (45)
10 CKD.kf. (656)
11 diabetic nephropathies/ (20775)
12 exp glomerulonephritis/ (42203)
13 exp proteinuria/ (34278)
14 acidosis, renal tubular/ (2595)
15 exp hypertension, renal/ (18844)
16 (diabetic adj (kidney or renal) adj (disease* or failure)).ti,ab. (1635)
17 ((renal or renovascular) adj2 hypertensi*).ti,ab. (12636)
18 (glomerulosclerosis or glomerulonephritis or nephropath* or proteinuria* or albuminuria or microalbuminuria).ti,ab. (97882)
19 (glomerular adj (sclerosis or nephritis)).ti,ab. (1854)
20 ((renal or distal or proximal or tubul*) adj2 acidos*).ti,ab. (2868)
21 hyperuricemia/ or hyperuric?emi*.ti,ab. (6571)
22 exp hyperparathyroidism, secondary/ (7470)
23 (renal adj2 (osteo* or hyperparathyroidism)).ti,ab. (3258)
24 or/2-23 (265852)
25 ureteral obstruction/ (12014)
26 exp urethral obstruction/ (9755)
27 ((uropath* or ureter* or urethra*) adj obstruct*).ti,ab. (6011)
28 (renal of kidney or chronic).ti,ab. (885588)
29 (25 or 26 or 27) and 28 (1248)
30 24 or 29 (266546)
31 (transplant* or donor* or graft* or allograft*).ti. (342377)
32 pregnan*.ti. (190096)
33 *renal dialysis/ not (predialysis or pre dialysis or ("not" adj4 dialysis)).ti. (53408)
34 30 not (31 or 32 or 33) (220044)=P
35 "P voor chronische nierschade".ti. (0)
36 exp Bariatric Surgery/ (17066)
37 Gastroenterostomy/ (3252)
38 (billroth or bariatric or gastroenterostom*).ti. (6671)
39 (billroth or bariatric or gastroenterostom*).kf. (1607)
40 or/36-39 (22454)
41 exp Obesity/ (156903)
42 (obesit? or obese).ti. (86631)
43 (obesit? or obese).kf. (16258)
44 (morbid adj3 obes*).ti. (2481)
45 (morbid adj3 obes*).kf. (283)
46 or/41-45 (173164)=obesity
47 Bariatrics/ (221)
48 40 or 47 (22531)
49 34 and 46 and 48 (139)
50 34 and 48 (176)
51 49 (139)
52 limit 51 to yr="2000 -Current" (129)
53 "sensitief filter voor RCT's van Cochrane".ti. (0)
54 randomized controlled trial.pt. (406810)
55 controlled clinical trial.pt. (90107)
56 (randomized or randomised).ab. (401346)
57 placebo.ab. (166328)
58 drug therapy.fs. (1819122)
59 randomly.ab. (242221)
60 trial.ab. (347038)
61 groups.ab. (1515463)
62 or/54-61 (3666040)
63 62 not (exp animals/ not humans/) (3153556)= rct
64 "filter rct cochrane sensitief".ti. (0)
65 "filter systematic reviews".ti. (0)
66 meta analysis.pt. (61482)
67 (meta-anal$ or metaanal$).af. (109047)
68 (quantitativ$ adj10 (review$ or overview$)).tw. (5511)
69 (systematic$ adj10 (review$ or overview$)).tw. (85866)
70 (methodologic$ adj10 (review$ or overview$)).tw. (7364)
71 medline.tw. and review.pt. (50587)
72 (pooled adj3 analy*).tw. (10524)
73 or/66-72 (196938)
74 "filter systematic reviews".ti. (0)
75 "cochrane$".fc_jour. (11827)
76 73 or 75 (198264)=systrev
77 52 and 76 (3)
78 52 and 63 (19) trials
79 su.fs. (1675263)
80 48 or 79 (1682398)
81 34 and 46 and 76 and 80 (4) med20160208 ckd obesity surgery systrev
82 49 not (78 or 81) (117)rest
83 obesity/su or obesity, morbid/su (12373)
84 bariatric surgery/ or gastric bypass/ or gastroplasty/ or jejunoileal bypass/ or lipectomy/ (17066)
85 ((bariatric adj3 surg*) or (gastric adj3 bypass*) or gastroplast* or (jejunoi* adj3 bypass*) or lipect*).tw. (15627)
86 ((bariatric adj3 surg*) or (gastric adj3 bypass*) or gastroplast* or (jejunoi* adj3 bypass*) or lipect*).kf. (1289)
87 83 or 84 or 85 or 86 (24372)
88 34 and 87 (242)
89 limit 88 to yr="2000 -Current" (218)
90 89 and 73 (5)extra systrev
91 89 and 63 (38)extra rct
92 89 not (73 or 63) (176)
93 92 (176)
94 *obesity/su or *obesity, morbid/su (8778)
95 *bariatric surgery/ or *gastric bypass/ or *gastroplasty/ or *jejunoileal bypass/ or *lipectomy/ (13797)
96 ((bariatric adj3 surg*) or (gastric adj3 bypass*) or gastroplast* or (jejunoi* adj3 bypass*) or lipect*).ti. (10338)
97 86 or 94 or 95 or 96 (18806)
98 93 and 97 (125) med20160212 CKD obesity surgery focus rest extra
99 Kidney Failure, Chronic/dh (1182)
100 Kidney Failure, Chronic/th (36716)
101 Diet, Protein-Restricted/ (2276)
102 ((reduc* adj3 protein adj3 intake) or (protein adj3 restric*) or (low-protein adj3 diet)).tw. (7565)
103 ((reduc* adj3 protein adj3 intake) or (protein adj3 restric*) or (low-protein adj3 diet)).kf. (75)
104 Glomerular Filtration Rate/ (35168)
105 "glomerular filtration rate (GFR)".kw. (35)
106 gfr.kf. (207)
107 gfr.tw. (15552)
108 (G3?? or moderat* or medium or decreas*).tw. (2542655)
109 glomerular filtration rate.tw. (30143)
110 104 or 105 or 106 or 107 or 109 (50422)
111 108 and 110 (15249)
112 (moderate adj3 protein).tw. (832)
113 (moderate adj3 protein).kf. (1)
114 Dietary Proteins/ (33657)
115 Dietary Proteins/ad (13590)
116 99 or 101 or 102 or 103 or 112 or 113 or 115 (21690)
117 34 and 111 and 116 and 76 (6)
118 34 and 110 and 116 and 76 (20) systrev
119 34 and 110 and 116 and 63 (201)
120 limit 119 to yr="2000 -Current" (89) rct
121 120 not 118 (77)
122 34 and 111 and 116 (191)
123 122 (191)
124 limit 123 to yr="2000 -Current" (84)
125 124 not (120 or 118) (36) rest
Resultaat bariatrische chirurgie
|
Naam file |
aantal |
|
med20160208 ckd obesity surgery systrev |
4 |
|
med20160212 CKD obesity surgery systrev extra |
2 |
|
med20160208 ckd obesity surgery trials |
19 |
|
med20160212 CKD obesity surgery rct extra |
18 |
|
med20160212 CKD obesity surgery focus rest extra |
123 |
|
med20160208 ckd obesity surgery rest |
23 |
|
med20160212 CKD obesity surgery rest extra |
40 |
