Operatietechniek bij volwassenen bij chirurgische behandeling van obesitas
Uitgangsvraag
Welke chirurgische techniek leidt bij volwassenen met ernstige obesitas tot de beste uitkomsten?
Aanbeveling
Kies bij volwassenen met indicatie voor metabole chirurgie voor die procedure die de voorkeur van patiënt en behandelaar het dichtst bij elkaar brengt, rekening houdend met de volgende factoren:
- BMI;
- leeftijd;
- co-morbiditeit;
- GERD;
- eerdere buikoperaties;
- medicatie.
Overwegingen
De onderstaande overwegingen en aanbevelingen gelden voor het overgrote deel van de populatie waarop de uitgangsvraag betrekking heeft.
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
- In termen van cruciale uitkomstmaten zijn er nauwelijks overwegingen die de keuze voor een specifieke techniek van metabole chirurgie bij volwassenen onderbouwen.
- Vrijwel alle cruciale uitkomstmaten, waaronder ook Excess Weight Loss op langere termijn en kwaliteit van leven zijn vergelijkbaar tussen de verschillende technieken.
- Het aantal revisie operaties na sleeve gastrectomie is hoger dan na RYGB.
Er zijn in de literatuur slechts een beperkt aantal studies die de uitkomsten van de verschillende operatietechnieken vergelijken. Een bijkomend probleem is dat er niet altijd sprake is van een eenvormige techniek van de verschillende ingrepen. Bij zowel Sleeve gastrectomie als Roux-en-Y Gastric bypass bestaat er grote variatie in de uitvoering en daarmee in de resultaten. Bovendien beschrijven de meeste vergelijkende studies gewichtsuitkomsten van de eerste 2 tot 3 jaar na operatie. Die zijn voor de meeste technieken vergelijkbaar. Hoewel gewichtsverlies na 2 jaar zeker van belang is gaat het bij een chronische aandoening als obesitas meer om lange termijn resultaten. Van RYGB zijn die beter bekend dan van gastric sleeve en van OAGB, omdat dat veel jongere technieken zijn. Vergelijkende studies voor de lange termijn zijn er dan ook niet. De meeste vergelijkende studies hebben gewichtsverlies als primaire uitkomstmaat maar zijn daardoor under powered voor zaken als co-morbiditeit of kwaliteit van leven. Daardoor is het lastig om daarover uitspraken te doen. Bijkomend probleem bij de beoordeling van effecten op langere termijn, is het fenomeen dat patiënten niet vervolgd kunnen worden (loss to follow-up). Ook in het relatief goed georganiseerde en in centra gecentraliseerde zorg aanbod in Nederland is de uitval ondanks landelijke registratie plicht groot. Dat vertroebelt het zicht op feitelijke resultaten sterk. Toch zijn er wel degelijk verschillen tussen de verschillende technieken die bij de keuze voor de juiste techniek een rol spelen. Een uitgebreide beschrijving van standaard technieken is beschikbaar in het consensus document van de Amerikaanse bariatrische chirurgen (Bhandari, 2019).
De bewijskracht voor cruciale uitkomstmaten overall is zeer laag. Alleen voor het verhoogd aantal revisie operaties en voor de kwaliteit van leven na SG versus RYGB is redelijke bewijskracht. De voornaamste oorzaken voor de gebrekkige bewijskracht is het gebrek aan vergelijkende studies, de beperkte kwaliteit van de studies en het beperkt aantal geïncludeerde patiënten.
Op grond van de belangrijke uitkomstmaten is geen duidelijke uitspraak te doen over het type metabole operatie dat bij een volwassene het meest succesvol is. De klinische ervaring van chirurgen lijkt te contrasteren met het gebrek aan bewijs voor het voordeel in gewichtsreductie dat met bypass operaties boven sleeve operaties kan worden behaald, zowel op korte als op langere termijn. Er zijn wel degelijk verschillen aanwijsbaar tussen ingrepen, die mede bepalen of de ingreep meer of minder geschikt is voor een bepaalde patiënt. Factoren die daar een rol spelen zijn onder andere: BMI, eerdere operaties, leeftijd, co-morbiditeit en de aanwezigheid van GERD.
Zonder een duidelijke waardering wordt hieronder per ingreep een aantal van de aandachtspunten bij de keuze van de techniek genoemd:
Laparoscopische sleeve gastrectomie (SG)
- Veilig en bij vrijwel iedereen uitvoerbaar.
- Passageklachten direct postoperatief komen wat vaker voor.
- Lange termijn gewichtsresultaten (5 tot 10 jaar) nog niet goed bekend.
- Mogelijk wat hogere kans op weight regain dan bij gastric bypass procedures.
- Aanzienlijke kans op het optreden van GERD (76%) en Barret’s oesofagus (19%) na 5 jaar. Daarom relatief gecontraíndiceerd bij pre-existente reflux en hiatus hernia diafragmatica (Sebastianelli, 2019).
- Het ontstaan van Barrett’s oesofagus is een potentieel risico voor het ontstaan van slokdarmkanker. Daarom is levenslange gastroscopische controle mogelijk aangewezen.
- Geschikt bij eerdere uitgebreide buikchirurgie.
- Ook bij Crohn patiënten veilig.
- Geschikt als eerste procedure in een stapsgewijze behandeling bijvoorbeeld bij extreme obesitas (BMI > 60 kg/m2), dan gevolgd door een hypo-abortieve ingreep zoals duondenal switch of SADI-S.
Laparoscopische Roux-en-Y gastric bypass (RYGB)
- Veilig en bij de meeste mensen uitvoerbaar.
- Uitgebreide data over lange termijn uitkomsten bekend.
- Lange termijn gewichtsverlies mogelijk wat hoger dan bij SG.
- Zeer goede resolutie van co-morbiditeit, ook van reflux klachten.
- Waarschijnlijk wat beter effect op resolutie van T2 diabetes dan SG.
- Meer klachten van ‘dumping’ na de maaltijd (10 tot 15%).
- Meer chronische buikklachten dan na SG.
- Er is een kans op het ontstaan van inwendige hernia.
- De kans op galstenen is mogelijk hoger dan bij SG.
- Minder geschikt bij: eerdere uitgebreide buikchirurgie, ziekte van Crohn, Oxalaat nierstenen.
- Technisch lastiger dan SG bij extreme buikobesitas.
Laparoscopische one anastomosis gastric bypass (OAGB)
- Veilig en bij de meeste mensen uitvoerbaar.
- Zeer goed gewichtsverlies op korte en middellange termijn, mogelijk zelfs beter dan bij RYGB en SG.
- Zeer goede resolutie van co-morbiditeiten; voor T2DM mogelijk zelfs beter dan voor RYGB.
- De OAGB is de jongste van de genoemde technieken. Er is nog niet veel bekend over resultaten op lange termijn.
- De techniek van de OAGB kent vele varianten. Met name bij een langere biliopancretische lis (>150cm) is er kans op malnutritie.
- Bij de OAGB is er een kans op (biliaire) reflux en een verhoogde kans op het ontstaan van ulcers. De kans op reflux is groter dan bij RYGB maar kleiner dan bij SG>.
- Ulcers als gevolg van biliaire reflux en H pylori vormen bij de BII maagresectie een risico op het ontwikkelen van een zogenaamd maagstompcarcinoom na 25 tot 30 jaar. Het is onbekend of dit voor de OAGB ook geldt.
- Na OAGB is er een kans op inwendige hernia, maar mogelijk kleiner dan bij RYGB.
- Bij OAGB gelden dezelfde relatieve contra-indicaties als bij RYGB (eerdere buikoperaties, M. Crohn, oxalaatstenen).
Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)
Het hoofddoel van de meeste patiënten is reductie van gewicht, verbeteren van kwaliteit van leven en in voorkomende gevallen verminderen van (risico op) co-morbiditeit. Voor wat deze doelen betreft kan geen onderbouwing worden gevonden voor het ondersteunen van een voorkeur voor type ingreep. De sleeve gastrectomie geeft mogelijk aanleiding tot meer revisie operaties vanwege weight regain, maar daar staat tegenover dat het aantal reoperaties bij gastric bypass op langere termijn vanwege complicaties weer wat hoger is. Dat is geen onderwerp geweest van deze onderzoeksvraag. De bevindingen na sleeve gastrectomie van reflux en Barret’s oesofagus zijn van relatief recente datum en hebben mogelijk hun impact op de kwaliteit van leven en de beoordeling van de ingreep door patiënten. Al deze argumenten moeten een onderdeel zijn van het proces van shared decision making dat bij de keuze voor de juiste operatie wordt gevolgd.
Kosten (middelenbeslag)
De genoemde ingrepen ontlopen elkaar niet wat betreft operatiekosten en opnameduur. De kosten effectiviteit van metabole chirurgie in het algemeen staat niet ter discussie. Over de differentiatie van de kosten effectiviteit tussen de verschillende ingrepen kan worden gesteld dat een hoger aantal revisie operaties een negatief effect op de kosten effectiviteit heeft. Uit de zoekvraag lijkt het aantal revisieoperaties voor weight regain na sleeve gastrectomie hoger dan na bypass operaties. Daar staat tegenover dat het aantal operaties vanwege late complicaties na gastric bypass operaties hoger is dan na SG. Hoe die twee uitkomsten zich precies verhouden is niet bekend.
Aanvaardbaarheid voor de overige relevante stakeholders
Er bestaan geen overtuigende bezwaren tegen elk van de genoemde ingrepen. Zowel SG als RYGB en OAGB zijn door de beroepsgroep erkende metabole operaties. Er zijn bij zowel SG als OAGB theoretische bezwaren over het risico op het ontstaan van maligne ziekte op zeer lange termijn (Slokdarmcarcinoom en Barret’s na SG en maagstompcarcinoom na OAGB). De wetenschappelijke bewijsvoering hiervoor ontbreekt echter en binnen de beroepsgroep is dit nog een punt van discussie. Vooralsnog zijn er dan ook geen morele bezwaren die de keuze voor een bepaalde ingreep bepalen.
Haalbaarheid en implementatie
De benodigde inzet van middelen en capaciteit is onafhankelijk van de keuze van een metabole chirurgische techniek. Een verschuiving van de keuze van een operatie naar een andere heeft dan ook geen invloed op de totale aantallen.
Rationale/ balans tussen de argumenten voor en tegen de interventie
De literatuur geeft niet veel aanknopingspunten als het gaat om de juiste keuze van metabole ingreep voor de juiste patiënt. Helaas worden met name de lange termijn uitkomsten van metabole chirurgie in de huidige vergelijkende studies onvoldoende belicht. Binnen de beroepsgroep bestaan evenwel beargumenteerde voorkeuren voor een bepaald type ingreep bij bepaalde patiënten. Meerdere factoren zijn van invloed op die keuze waaronder: BMI, leeftijd, co-morbiditeit met name diabetes mellitus type 2, aanwezigheid van reflux, eerdere buikoperaties en medicijngebruik.
Onderbouwing
Uitgangspunt voor het verrichten van metabole chirurgie is optimaliseren van gewichtsverlies en daarmee verbeteren van (risico op) co-morbiditeiten, levensverwachting en kwaliteit van leven. Voor het bewerkstelligen van deze eindpunten, moet gekozen worden welke procedure de beste kans van slagen heeft. Daartegenover staat het risico op operatieve complicaties en nadelige effecten van de ingreep. Tussen de verschillende ingrepen (Roux-en-Y gastric bypass, one anastomosis/mini-gastric bypass, sleeve gastrectomie) bestaan wezenlijke technische en anatomische verschillen en er zijn verschillen in de lange termijn resultaten. Met welke ingreep het beste de balans tussen positieve en negatieve gevolgen bereikt wordt, is niet bekend. In de dagelijkse praktijk kiezen behandelaars en hun patiënten vaak op basis van eigen ervaring, ervaring uit de omgeving en persoonlijke overtuiging. De uitgangsvraag is bedoeld om ten aanzien van deze keuze in een zo objectief mogelijke onderbouwing te voorzien.
Uitkomstmaat 1. Excess weight loss na 5 jaar (cruciaal)
Vergelijking: LRYGB versus LSG
|
Laag GRADE |
Er is mogelijk geen klinisch relevant verschil in excess weight loss 5 jaar na operatie bij volwassen patiënten tussen laparoscopische Roux-en-Y gastric bypass en laparoscopische sleeve gastrectomie.
Bronnen: (Ignat, 2017; Salminen, 2018; Zhang, 2014) |
Uitkomstmaat 2. Bloedingen en naadlekkages (cruciaal)
Vergelijking: LRYGB versus LSG
|
Zeer laag GRADE |
Uitkomst: Ernstige complicaties: bloedingen
Het is onduidelijk of laparoscopische Roux-en-Y gastric bypass meer of minder bloedingen geeft bij volwassen patiënten vergeleken met laparoscopische sleeve gastrectomie.
Bronnen: (Ignat, 2017;, Salminen, 2018; Zhang, 2014; Kehagias, 2011; Peterli, 2018) |
Uitkomstmaat 2. Bloedingen en naadlekkages (cruciaal)
Vergelijking: LMGB versus LRYGB en LMGB versus LSG
|
Zeer laag GRADE |
Uitkomst: Ernstige complicaties: bloedingen
Het is onduidelijk of laparoscopische mini-gastric bypass meer of minder bloedingen geeft bij volwassen patiënten vergeleken met laparoscopische Roux-en-Y gastric bypass of laparoscopische sleeve gastrectomie.
Bronnen: (Lee, 2005; Shivakumar, 2018) |
Uitkomstmaat 2. Bloedingen en naadlekkages (cruciaal)
Vergelijking: LRYGB versus LSG
|
Zeer laag GRADE |
Uitkomst: Ernstige complicaties: naadlekkages
Het is onduidelijk of laparoscopische Roux-en-Y gastric bypass meer of minder naadlekkages geeft bij volwassenen vergeleken met laparoscopische sleeve gastrectomie.
Bronnen: (Ignat, 2017; Salminen, 2018; Zhang, 2014; Kehagias, 2011; Peterli, 2018) |
Uitkomstmaat 2. Bloedingen en naadlekkages (cruciaal)
Vergelijking: LMGB versus LRYGB en LMGB versus LSG
|
Zeer laag GRADE |
Uitkomst: Ernstige complicaties: naadlekkages
Het is onduidelijk of laparoscopische mini-gastric bypass meer of minder naadlekkages geeft bij volwassenen vergeleken met laparoscopische Roux-en-Y gastric bypass of laparoscopische sleeve gastrectomie.
Bronnen: (Lee, 2005; Shivakumar, 2018) |
Uitkomstmaat 3. Reflux (GERD "gastroesophageal reflux disease")
Vergelijking: LRYGB versus LSG & LMGB versus LRYGB & LMGB versus LSG
|
Zeer laag GRADE |
Uitkomst: Ernstige complicaties: refluxklachten
Het is onduidelijk of er een verschil is in het vóórkomen van refluxklachten bij volwassen patiënten tussen verschillende metabole operatietechnieken.
Bronnen: (Ignat, 2017; Salminen, 2018; Zhang, 2014; Kehagias, 2011; Peterli, 2018; Shivakumar, 2018; Lee, 2005) |
Uitkomstmaat 4. Passageklachten (cruciaal)
Vergelijking: LRYGB versus LSG & LMGB versus LRYGB & LMGB versus LSG
|
Zeer laag GRADE |
Uitkomst: Ernstige complicaties: passageklachten
Het is onduidelijk of er een verschil is in het vóórkomen van passageklachten bij volwassen patiënten tussen verschillende metabole operatietechnieken.
Bronnen: (Ignat, 2017; Salminen, 2018; Zhang, 2014; Kehagias, 2011; Peterli, 2018; Shivakumar, 2018; Lee, 2005) |
Uitkomstmaat 5. Inwendige herniaties (cruciaal)
Vergelijking: LRYGB versus LSG & LMGB versus LRYGB
|
Zeer laag GRADE |
Uitkomst: Ernstige complicaties: inwendige herniaties
Het is onduidelijk of er een verschil is in het vóórkomen van inwendige herniaties bij volwassen patiënten tussen verschillende metabole operatietechnieken.
Bronnen: (Ignat, 2017; Salminen, 2018; Zhang, 2014; Kehagias, 2011; Peterli, 2018; Lee, 2005) |
Uitkomstmaat 6. Galstenen (cruciaal)
Vergelijking: LMGB versus LSG
|
Zeer laag GRADE |
Uitkomst: Galstenen
Het is onduidelijk of galstenen vaker voorkomen na laparoscopische mini-gastric bypass of na laparoscopische sleeve gastrectomie bij volwassenen.
Bronnen: (Shivakumar, 2018) |
Uitkomstmaat 7. Revisie operatie (cruciaal)
Vergelijking: LRYGB versus LSG
|
redelijk GRADE |
Uitkomst: Revisie operatie
Volwassenen die een laparoscopische sleeve gastrectomie hebben ondergaan hebben waarschijnlijk (veel) vaker een revisie operatie nodig vergeleken met volwassenen die een laparoscopische Roux-en-Y gastric bypass hebben ondergaan.
Bronnen: (Ignat, 2017; Salminen, 2018; Zhang, 2014; Kehagias, 2011; Peterli, 2018) |
Uitkomstmaat 7. Revisie operatie (cruciaal)
Vergelijking: LRYGB versus LSG en LMGB versus LSG
|
Zeer laag GRADE |
Uitkomst: Revisie operatie
Het is onduidelijk of laparoscopische mini-gastric bypass leidt tot meer of minder revisie operaties bij volwassenen vergeleken met patiënten die een laparoscopische Roux-en-Y gastric bypass of laparoscopische sleeve gastrectomie hebben ondergaan.
Bronnen: (Lee, 2005; Shivakumar, 2018) |
Uitkomstmaat 8. Kwaliteit van leven (cruciaal)
Vergelijking: LRYGB versus LSG
|
Redelijk GRADE |
Uitkomst: Kwaliteit van leven
Volwassen die laparoscopische Roux-en-Y gastric bypass of laparoscopische sleeve gastrectomie hebben ondergaan ervaren waarschijnlijk hetzelfde niveau van kwaliteit van leven vijf jaar na de operatie.
Bronnen: (Zhang, 2014; Ignat, 2017; Salminen, 2018; Peterli, 2018) |
Uitkomstmaat 8. Kwaliteit van leven (cruciaal)
Vergelijking: LMGB versus LRYGB
|
Zeer laag GRADE |
Uitkomst: Kwaliteit van leven
Het is onduidelijk of er een verschil is in de ervaren kwaliteit van leven bij volwassen na laparoscopische mini-gastric bypass vergeleken met laparoscopische sleeve gastrectomie
Bronnen: (Lee, 2005) |
Uitkomstmaat 9. Excess weight loss, 2 tot 3 jaar na metabole operatie (belangrijk)
Vergelijking: LRYGB versus LSG
|
Laag GRADE |
Uitkomst: Excess weight loss twee of drie jaar na metabole chirurgie
Er is mogelijk geen klinisch relevant verschil in excess weight loss twee of drie jaar na operatie bij volwassen patiënten tussen laparoscopische Roux-en-Y gastric bypass en laparoscopische sleeve gastrectomie.
Bronnen: (Ignat, 2017; Kehagias, 2011; Salminen, 2018; Zhang, 2014) |
Uitkomstmaat 9. Excess weight loss, 2 tot 3 jaar na metabole operatie (belangrijk)
Vergelijking: LMGB versus LSG
|
Laag GRADE |
Uitkomst: Excess weight loss twee of drie jaar metabole chirurgie
Er is mogelijk geen klinisch relevant verschil in excess weight loss twee of drie jaar na operatie tussen laparoscopische mini-gastric bypass en laparoscopische sleeve gastrectomie.
Bronnen: (Shivakumar, 2018) |
Uitkomstmaat 10. Hypertensie (belangrijk)
Vergelijking: (L)RYGB versus LSG
|
Laag GRADE |
Uitkomst: remissie van hypertensie
Er lijkt geen klinisch relevant verschil te zijn in het bereiken van remissie van hypertensie tussen laparoscopische Roux-en-Y gastric bypass en laparoscopische sleeve gastrectomie.
Bronnen: (Kehagias, 2011; Paluszkiewicz, 2012; Peterli, 2018; Salminen, 2018; Zhang, 2014) |
Uitkomstmaat 10. Hypertensie (belangrijk)
Vergelijking: LMYGB versus LSG
|
GRADE |
Uitkomst: remissie van hypertensie
Het is onduidelijk of er een klinisch relevant verschil is in het bereiken van remissie van hypertensie tussen laparoscopische mini-gastric bypass en laparoscopische sleeve gastrectomie.
Bronnen: (Shivakumar, 2018) |
Uitkomstmaat 11. Dislipidemie (belangrijk)
Vergelijking: (L)RYGB versus LSG
|
Laag GRADE |
Uitkomst: remissie van dislipidemie
Er lijkt een klinisch relevant verschil te zijn in het bereiken van remissie van dislipidemie tussen (laparoscopische) Roux-en-Y gastric bypass en laparoscopische sleeve gastrectomie in het voordeel van laparoscopische) Roux-en-Y gastric bypass.
Bronnen: (Paluszkiewicz, 2012; Peterli, 2018; Salminen, 2018) |
Uitkomstmaat 12. Slaapapneu (belangrijk)
Vergelijking: LRYGB versus LSG
|
Zeer laag GRADE |
Uitkomst: remissie van slaapapneu
Het is onduidelijk of er een verschil bestaat in het bereiken van remissie van slaapapneu tussen laparoscopische Roux-en-Y gastric bypass en laparoscopische sleeve gastrectomie.
Bronnen: (Kehagias, 2011; Peterli, 2018) |
Overige uitkomsten
|
- GRADE |
Er zijn geen studies over:
|
Beschrijving studies
Vijf RCT’s vergeleken laparoscopische Roux-en-Y gastric bypass (LRYGB) met laparoscopische sleeve gastrectomie (LSG) met in totaal 694 patiënten (Zhang, 2014; Salminen, 2018; Peterli, 2018; Kehagias, 2011; Ignat, 2017). In de studie van Paluszkiewicz (2012) werd Roux-en-Y gastric bypass ook vergeleken met LSG, maar werd in tegenstelling tot de overige artikelen de gastric bypass niet laparoscopisch uitgevoerd (n=72). Eén RCT vergeleek gastric mini-bypass met (laparoscopische) Roux-en-Y gastric bypass (Lee, 2005; n=80) en één RCT vergeleek gastric mini-bypass met sleeve gastrectomie (Shivakumar, 2018; n=200). Deze laatste studie hanteerde als enige studie een single-blind design (patiënten waren geblindeerd voor operatietype), de rest van de studies waren niet geblindeerd.
(laparoscopische) Roux-en-Y gastric bypass versus laparoscopische sleeve gastrectomie
Paluszkiewicz (2012) vergeleek de effectiviteit van de Roux-en-Y gastric bypass (RYGB) met de laparoscopische sleeve gastrectomie (LSG). 72 patiënten werden één op één gerandomiseerd naar de operatietechnieken. De inclusiecriteria waren een BMI van boven de 40 kg/m2 of een BMI boven de 35 kg/m2 met tenminste één co-morbide aandoening en een leeftijd tussen de 18 en de 60 jaar. De studie rapporteerde onder andere vroege en late complicaties, remissie van co-morbiditeiten en vitamine B12 en ijzerdeficiënties.
Zhang (2014) includeerde 64 patiënten in een gerandomiseerd onderzoek naar de effectiviteit van laparoscopische Roux-en-Y gastric bypass (LRYGB) (n=32) bypass vergeleken met een LSG (n=32). De studie hanteerde een lager afkappunten voor BMI dan gebruikelijk in Westerse landen, namelijk een BMI tussen de 32 en de 50. De studie rapporteerde vroege en late complicaties, evenals excessive weight loss (EWL) drie en vijf jaar na operatie en remissie van co-morbiditeiten.
Salminen (2018) rapporteerde de recentste resultaten van de SLEEPASS trial waarin patiënten werden gerandomiseerd naar laparoscopische sleeve gastrectomie (n= 121) of laparoscopische Roux-en-Y gastric bypass (n=119). De volgende inclusiecriteria werden gehanteerd: een BMI van boven de 40 kg/m2 of een BMI boven de 35 kg/m2 met tenminste één co-morbide aandoening, een leeftijd tussen de 18 en de 60 jaar en het eerder gevolgd hebben van een beweeg- en dieetprogramma zonder succes. De studie rapporteerde resultaten over korte en lange termijn complicaties, EWL drie en vijf jaar na operatie, remissie en verbetering van co-morbiditeiten en kwaliteit van leven.
Peterli (2018) rapporteerde de resultaten van SM-BOSS RCT waarin patiënten werden gerandomiseerd naar laparoscopische sleeve gastrectomie (n= 112) of laparoscopische Roux-en-Y gastric bypass (n=113). De studie hanteerde als inclusiecriteria een BMI van boven de 40 kg/m2 of een BMI boven de 35 kg/m2 met tenminste één co-morbide aandoening. De studie rapporteerde onder andere resultaten met betrekking tot vroege en late complicaties, remissie en verbetering van co-morbide aandoeningen.
Kehagias (2011) rekruteerde 60 patiënten met een BMI van onder de 50 van een wachtlijst voor metabole chirurgie. De patiënten werden één op één gerandomiseerd naar LRYGB en LSG. De studie rapporteerde onder andere vroege en late complicaties, EWL drie jaar na de operatie en remissie van co-morbiditeiten.
Ignat (2017) includeerde patiënten met een BMI tussen de 40 kg/m2 en de 60 kg/m2 en randomiseerde hen naar LRYGB (n=45) of LSG (n=55). De studie rapporteerde complicaties, EWL drie en vijf jaar na operatie en kwaliteit van leven.
Laparoscopische mini-gastric bypass versus laparoscopische Roux-en-Y gastric bypass
Lee (2005) vergeleek de effectiviteit van de laparoscopische mini-gastric bypass (LMGB) met LRYGB. De studie hanteerde de volgende inclusiecriteria: tenminste 5 jaar obesitas, BMI van boven de 40 kg/m2 of een BMI boven de 35 kg/m2 met tenminste één co-morbide aandoening, een leeftijd tussen de 18 en de 59, geregistreerde pogingen om gewicht te verliezen en een goede motivatie om metabole chirurgie te ondergaan. Tachtig patiënten werden één op één gerandomiseerd naar LMGB en LRYGB. De studie rapporteerde korte en lange termijn complicaties, EWL twee jaar na de operatie en kwaliteit van leven.
Mini-gastric bypass/OAGB versus laparoscopische sleeve
Shivakumar (2018) vergeleek de effectiviteit van de laparoscopische mini-gastric bypass (LMGB, n=101) met LSG (n=100). De studie hanteerde als inclusiecriteria een BMI tussen de 35 en de 60 kg/m2 en een leeftijd van 18 tot 60 jaar. De studie rapporteerde korte en lange termijn complicaties, EWL drie jaar na chirurgie en remissie van co-morbiditeiten.
Resultaten - kritieke uitkomsten
Uitkomstmaat 1. Excess weight loss na 5 jaar (cruciaal)
Ignat (2017), Salminen (2018) en Zhang (2014) rapporteerden het gemiddelde percentage excess weight loss (EWL) na vijf jaar naar type metabole chirurgie. Figuur 1 geeft de gepoolde data weer. LRYGB geeft gemiddeld 8% meer EWL vergeleken met sleeve gastrectomie (gemiddeld verschil 8,0%, 95% BI: 7,5 tot 8,5), hetgeen geen klinisch relevant verschil betreft.
Figuur 1 Uitkomstmaat EWL na 5 jaar vergelijking LRYGB versus LSG
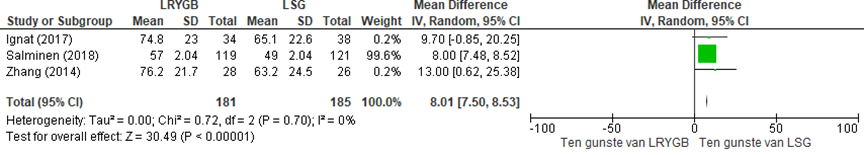
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Ernstige complicaties op korte termijn (≤ 30 dagen)
Uitkomstmaat 2. Bloedingen en naadlekkages
Vijf studies (Ignat, 2017; Salminen,2018; Zhang, 2014; Kehagias, 2011; Peterli,2018) rapporteerden de prevalentie van bloedingen en naadlekkages bij LRYGB versus LSG, één LMGB versus LRYGB en één LMGB versus LSG. Het aantal events was te laag om te betrouwbare conclusies over te trekken. Zie voor meer achtergrond de evidencetabellen.
Ernstige complicaties op lange termijn (>30 dagen)
Uitkomstmaat 3. Reflux (GERD "gastroesophageal reflux disease")
Vijf studies onderzochten het vóórkomen van refluxklachten bij LRYGB versus LSG (Ignat, 2017; Salminen, 2018; Zhang, 2014; Kehagias, 2011 en Peterli, 2018). In geen van de vijf geïncludeerde studies kwam een geval van reflux voor in de LRYGB-behandelarm. In totaal kwam in de LSG-behandelarm 17 gevallen (5%) van reflux voor. Gezien het ontbreken van events in de LRYGB-groep zijn de resultaten niet gepoold. In de studies naar LMGB versus LRYGB en LMGB versus LSG werd niets over reflux gerapporteerd (Lee, 2005; Shivakumar, 2018).
Uitkomstmaat 4. Passageklachten (cruciaal)
Vijf studies onderzochten het vóórkomen van passageklachten bij LRYGB versus LSG (Ignat, 2017; Salminen, 2018; Zhang, 2014; Kehagias, 2011 en Peterli, 2018). Het aantal events was te laag om betrouwbare conclusies over te trekken. Zie voor meer achtergrond de evidencetabellen. In de studies naar de vergelijking tussen LMGB versus LRYGB (Lee, 2005) en LMGB versus LSG (Shivakumar, 2018) kwamen geen gevallen van passageklachten voor.
Uitkomstmaat 5. Inwendige herniaties (cruciaal)
Vijf studies onderzochten het vóórkomen van inwendige herniaties bij LRYGB (Ignat, 2017; Salminen, 2018; Zhang, 2014; Kehagias, 2011 en Peterli, 2018) in de studies naar LRYGB versus LSG. In totaal kwam in de LRYGB-behandelarmen 27 (8,1%) gevallen van herniaties voor. In de studie naar LMGB versus LRYGB werd niets over inwendige herniaties gerappporteerd (Lee, 2005).
Uitkomstmaat 6. Galstenen (cruciaal)
Enkel de studie naar LMGB versus LSG rapporteerde over de uitkomstmaat galstenen (Shivakumar, 2018). Drie personen in de LMGB-groep en twee personen in de LSG-groep hadden symptomatische galstenen (2,8% en 1,9%, respectievelijk).
Uitkomstmaat 7. Revisie operatie (cruciaal)
Vijf studies onderzochten hoe vaak revisie operaties noodzakelijk waren in de vergelijking LRYGB versus LSG (Ignat, 2017; Salminen, 2018; Zhang, 2014; Kehagias, 2011 en Peterli, 2018). In geen van de geïncludeerde studies was een revisie operatie nodig voor de LRYGB-behandelarm. In totaal kwamen in de LSG-behandelarm 23 (6,8%) revisie operaties voor. Bij 17 personen was revisie operatie noodzakelijk door ernstige reflux, bij vijf personen door onvoldoende gewichtsverlies en bij één persoon door mid gastric twist. Twee personen ondergingen een revisie operatie naar biliopancreatic diversion duodenal switch, de rest onderging revisie operatie naar gastric bypass. Gezien het ontbreken van events in de LRYGB-behandelarm zijn de resultaten niet gepoold.
In de studie naar LMGB versus LRYGB onderging in totaal één persoon in de LRYGB-groep revisie operatie door onvoldoende gewichtsverlies (Lee, 2005). In de studie naar LMGB versus LSG onderging ook in totaal één persoon een revisie operatie (Shivakumar, 2018). De persoon uit de LSG-groep onderging een revisie operatie naar LMGB vanwege onvoldoende resultaat in termen van zowel gewichtsverlies als verbetering in diabetes mellitus status.
Uitkomstmaat 8. Kwaliteit van leven (cruciaal)
Tabel 1 geeft een overzicht van de uitkomst kwaliteit van leven na metabole operatie weer. Geen van de studies rapporteerde een significant verschil in kwaliteit van leven tussen de verschillende operatiegroepen.
Tabel 1 Overzicht uitkomstmaat kwaliteit van leven na metabole operatie
|
Vergelijking: LRYGB versus. LSG |
|||
|
Referentie |
Vragenlijst |
Tijdsmoment |
Resultaten, gemiddelde (SD) |
|
Zhang (2014) |
Moorehead-Ardelt Questionnaire II |
5 jaar na operatie |
LRYGB: 1,58 (0,71) |
|
Ignat (2017) |
Moorehead-Ardelt Questionnaire II |
5 jaar na operatie |
LRYGB: 1,4 (1,0) LSG: 1,2 (1,1), p>0,05 |
|
|
Gastrointestinal Quality of Life Index (GIQLI) |
5 jaar na operatie |
LRYGB: 111,7 (17,8) LSG: 113,0 (16,6), p>0,05 |
|
Salminen (2018) |
Moorehead-Ardelt Questionnaire I |
5 jaar na operatie |
LRYGB: 0,76 (1,01) LSG: 0,85 (1,08), p=0,85 |
|
Peterli (2018) SM-BOSS |
Gastrointestinal Quality of Life Index (GIQLI) |
5 jaar na operatie |
LRYGB: 117,9 (114,8 - 121,0) |
|
|
Bariatric Analysis and Reporting Outcome System (BAROS) |
5 jaar na operatie |
LRYGB: 1,7 (1,5 – 1,9) LSG: 1,4 (1,1 - 1,7), p=0,66 |
|
Vergelijking: LMGB versus. LRYGB |
|||
|
Lee (2005) |
Gastrointestinal Quality of Life Index (GIQLI) |
1 jaar na operatie |
LMGB: 113,9 (17,0) LSG: 113,3 (16,1) |
Resultaten - belangrijke uitkomsten
Uitkomstmaat 9. Excess weight loss, 2 tot 3 jaar na metabole operatie (belangrijk)
Vier studies vergeleken EWL drie jaar na LRYGB met LSG. De studies konden niet worden gepoold vanwege het ontbreken van een spreidingsmaat (Kehegias, 2011; Zhang 2014).
De studie van Ignat (2017) en Zhang (2014) rapporteerde een klinisch relevant verschil: in de studie van Ignat (2017) bedroeg de EWL 83,0% (SD 14,3) voor LRYGB en 66,3% (SD 26,8), voor LSG (p=0,024) en in de studie van Zhang (2014) bedroeg de EWL 79,8% voor LRYGB en 68,0% voor LSG (p<0,05). Salminen (2018) rapporteerde een verschil van 8,4% (95% BI: 3,5 - 13,3) ten gunste van LRYGB, hetgeen echter niet klinisch relevant is. In tegenstelling tot de andere studies, rapporteerde Kehagias (2011) een grotere EWL voor LSG dan voor LRYGB. Dit verschil was echter niet statistisch significant of klinisch relevant (LRYGB: 62,1%; LSG: 68,5%, p=0,74).
In de studie naar LMGB versus LSG (Shivakumar, 2018) werd een EWL van 66,5% (SD 15,7) voor LMGB en 61,2% (SD 25,3) voor LSG gerapporteerd, hetgeen niet klinisch relevant of statistisch significant van elkaar verschilde.
Remissie van co-morbiditeiten anders dan diabetes mellitus
Uitkomstmaat 10. Hypertensie (belangrijk)
Figuur 2 geeft de gepoolde resultaten van vergelijking tussen (L)RYGB en LSG voor de uitkomstmaat remissie hypertensie weer. Remissie van hypertensie bleek niet te verschillen tussen beiden behandelgroepen (RR: 1,17 (BI: 0,88 tot 1,56). De studie naar LMGB versus LSG (Shivakumar, 2018) rapporteerde nagenoeg dezelfde rate voor remissie van hypertensie in de LMGB-groep (37/53) als de LSG-groep (39/56) 3 jaar na de operatie.
Figuur 2 Uitkomstmaat remissie hypertensie vergelijking LRYGB versus LSG
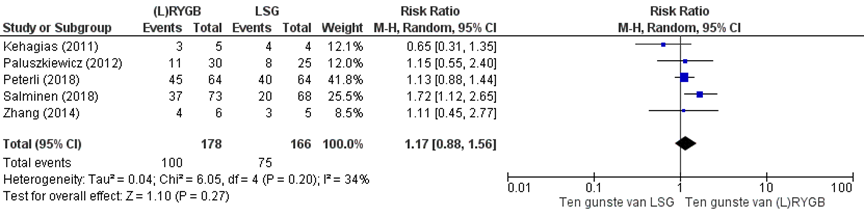
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Uitkomstmaat 11. Dislipidemie (belangrijk)
Figuur 3 geeft de gepoolde resultaten van vergelijking tussen (L)RYGB en LSG voor de uitkomstmaat remissie van dislipidemie weer. Remissie van dislipidemie werd 1,47 (1,13 tot 1,93) keer zo vaak bewerkstelligd middels LRYGB vergeleken met LSG, hetgeen een klinisch relevant verschil betreft.
Figuur 3 Uitkomstmaat remissie dislipidemie vergelijking LRYGB versus LSG
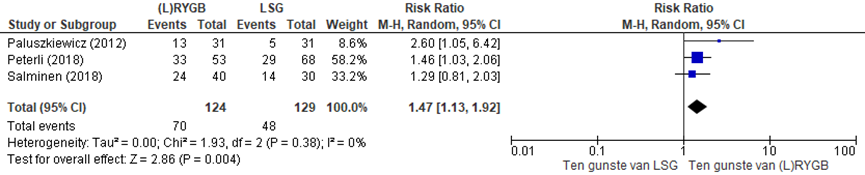
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Uitkomstmaat 12. Slaapapneu (belangrijk)
Twee studies onderzochten de remissie van slaapapneu tussen LRYGB en LSG (Kehagias,
2011; Peterli, 2018). In beide studies was er even vaak sprake van remissie in beide operatie
techniek groepen (gepoold: LRYGB: 21 uit 46 en LSG: 26 uit 54).
Bewijskracht van de literatuur
Volgens GRADE start de bewijskracht van RCT’s op ‘hoog’.
Cruciale uitkomstmaten
LRYGB versus LSG: EWL na 5 jaar
De bewijskracht voor de uitkomstmaat EWL na 5 jaar is met twee niveaus verlaagd tot ‘laag’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan blindering en loss-to-follow-up bias, één niveau aftrekken) en het doorkruisen van de grens voor klinisch relevantie (imprecisie, één niveau aftrekken).
LRYGB versus LSG: bloedingen
De bewijskracht voor de uitkomstmaat bloedingen is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan blindering, één niveau aftrekken) en het geringe aantal patiënten (imprecisie: betrouwbaarheidsinterval overlapt beide grenzen voor klinische relevantie, twee niveaus aftrekken).
LMGB versus LRYGB en LMGB versus LS: bloedingen
De bewijskracht voor de uitkomstmaat bloedingen is met drie niveaus verlaagd tot ‘zeer laag’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan (dubbel)blindering, één niveau aftrekken) en het vrijwel ontbreken van events (imprecisie, twee niveaus aftrekken).
LRYGB versus LSG: naadlekkages
De bewijskracht voor de uitkomstmaat naadlekkages is met drie niveaus verlaagd tot ‘zeer laag’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan blindering, één niveau aftrekken) en de hoge mate van inconsistentie (heterogeniteit, twee niveaus aftrekken).
LMGB versus LRYGB en LMGB versus LSG: naadlekkages
De bewijskracht voor de uitkomstmaat naadlekkages is met drie niveaus verlaagd tot ‘zeer laag’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan (dubbel)blindering, één niveau aftrekken) en gezien het nagenoeg ontbreken van events (imprecisie, twee niveaus aftrekken).
LMGB versus LRYGB & LMGB versus LRYGB & LMGB versus LSG: Reflux (GERD "gastroesophageal reflux disease")
De bewijskracht voor de uitkomstmaat reflux is met drie niveaus verlaagd tot ‘zeer laag’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan (dubbel)blindering, één niveau aftrekken) en gezien het nagenoeg ontbreken van events (imprecisie, twee niveaus aftrekken).
LMGB versus LRYGB & LMGB versus LRYGB & LMGB versus LSG: Passageklachten
De bewijskracht voor de uitkomstmaat passageklachten is met drie niveaus verlaagd tot ‘zeer laag’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan (dubbel)blindering, één niveau aftrekken) en gezien het nagenoeg ontbreken van events (imprecisie, twee niveaus aftrekken).
LMGB versus LRYGB & LMGB versus LRYGB & LMGB versus LSG: Inwendige herniaties
De bewijskracht voor de uitkomstmaat inwendige herniaties is met drie niveaus verlaagd tot ‘zeer laag’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan (dubbel)blindering, één niveau aftrekken) en gezien het nagenoeg ontbreken van events (imprecisie, twee niveaus aftrekken).
LRYGB versus LSG: Revisie operatie
De bewijskracht voor de uitkomstmaat revisie operatie is met één niveau verlaagd tot ‘redelijk’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan blindering).
LMGB versus LRYGB en LMGB versus LSG: Revisie operatie
De bewijskracht voor de uitkomstmaat revisie operatie is met drie niveaus verlaagd tot ‘zeer laag’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan (dubbel)blindering) en het geringe aantal patiënten/events (imprecisie, twee niveaus aftrekken).
LRYGB versus LSG en LMGB versus LRYGB: Galstenen
Er zijn geen studies gevonden over galstenen voor de vergelijkingen LRYGB versus LSG en LMGB versus LRYGB bij volwassenen.
LMGB versus LSG: Galstenen
De bewijskracht voor de uitkomstmaat galstenen is met drie niveaus verlaagd tot ‘zeer laag’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan (dubbel)blindering) en het geringe aantal patiënten/events (imprecisie, twee niveaus aftrekken).
LRYGB versus LSG: Kwaliteit van leven
De bewijskracht voor de uitkomstmaat kwaliteit van leven is met één niveau verlaagd tot ‘redelijk’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan blindering, loss-to-follow-up bias).
LMGB versus LRYGB: Kwaliteit van leven
De bewijskracht voor de uitkomstmaat kwaliteit van leven is met drie niveaus verlaagd tot ‘zeer laag’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan blindering) en het geringe aantal patiënten (imprecisie, twee graderingen aftrekken).
LMGB versus LSG: Kwaliteit van leven
Er zijn geen studies over kwaliteit van leven voor de vergelijkingen LRYGB versus LSG bij volwassenen.
Belangrijkrijke uitkomstmaten
LRYGB versus LSG: EWL na 2 of 3 jaar
De bewijskracht voor de uitkomstmaat EWL na 2 to 3 jaar is met twee niveaus verlaagd tot ‘laag’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan blindering, één niveau aftrekken) en inconsistentie (heterogeniteit, één niveau aftrekken).
LMYGB versus LSG: EWL na 2 of 3 jaar
De bewijskracht voor de uitkomstmaat EWL na 2 of 3 jaar is met twee niveaus verlaagd tot ‘laag’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan (dubbel)blindering, één niveau aftrekken) en het doorkruisen van de grenzen voor klinische relevantie (imprecisie, één niveau aftrekken).
LMGB versus LRYGB: EWL na 2 of 3 jaar
Er zijn geen studies over EWL na 2 of 3 jaar voor de vergelijking LMYGB versus LRYGB.
LRYGB versus LSG: remissie van hypertensie
De bewijskracht voor de uitkomstmaat remissie van hypertensie is met twee niveaus verlaagd tot ‘laag’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan blindering, één niveau aftrekken) en inconsistentie relevantie (heterogeniteit, één niveau aftrekken).
LMGB versus LRYGB: remissie van hypertensie
Er zijn geen studies naar remissie van hypertensie voor de vergelijking LMYGB versus LRYGB.
LMGB versus LSG: remissie van hypertensie
De bewijskracht voor de uitkomstmaat remissie van hypertensie is met drie niveaus verlaagd tot ‘zeer laag’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan (dubbel) blindering, één niveau aftrekken) en het geringe aantal patiënten (imprecisie, twee niveaus aftrekken).
LRYGB versus LSG: remissie van dislipidemie
De bewijskracht voor de uitkomstmaat remissie van dislipidemie is met twee niveaus verlaagd tot ‘laag’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan blindering, één niveau aftrekken) en het doorkruisen van de grens van klinische relevantie (imprecisie, één niveau aftrekken).
LMGB versus LRYGB
Er zijn geen studies naar remissie van dislipidemie voor de vergelijkingen LMGB versus LRYGB.
LRYGB versus LSG: remissie van slaapapneu
De bewijskracht voor de uitkomstmaat remissie van slaapapneu is met drie niveaus verlaagd tot ‘zeer laag’ gezien beperkingen in de onderzoeksopzet (risk of bias: gebrek aan blindering, één niveau aftrekken) en het geringe aantal patenten (imprecisie, twee niveaus aftrekken).
LMGB versus LRYGB & LRYGB versus LSG: remissie van slaapapneu
Er zijn geen studies naar remissie van slaapapneu voor de vergelijkingen LMYGB versus LRYGB & LRYGB versus LSG.
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag (vragen):
Welke chirurgische techniek leidt bij volwassenen met ernstige obesitas tot de beste uitkomsten?
P: volwassenen (18 tot 65 jaar) met ernstige obesitas die in aanmerking komen voor metabole chirurgie;
I/C: (laparoscopische) gastric bypass, one anastomosis /mini-gastric bypass, sleeve gastrectomie en andere varianten behalve gastric banding;
O: complicaties op korte termijn en lange termijn, gewichtsverlies na 2 tot 3 jaar en ≥ 5 jaar; remissie of verbetering van co-morbiditeiten: hypertensie, slaapapneu, dislipidemie; cardiovasculaire events en kwaliteit van leven.
Relevante uitkomstmaten
De werkgroep achtte gewichtsverlies na ≥ 5 jaar, ernstige complicaties en algehele kwaliteit van leven voor de besluitvorming cruciale uitkomstmaten; en gewichtsverlies na 2 tot 3 jaar, remissie van hypertensie, dislipidemie en slaapapneu voor de besluitvorming belangrijke uitkomstmaten.
Ernstige complicaties dienden tenminste graad IIIB volgens de Clavien-Dinco classificatie (interventie onder algehele anesthesie) te zijn of het artikel beschreef dat er chirurgische interventie voor de ernstige complicatie noodzakelijk was. Heroperaties, nabloedingen en naadlekkages werden door de werkgroep als ernstige complicaties op korte termijn (≤ 30) beschouwd en reflux (GERD "gastroesophageal reflux disease"), inwendige herniaties (bij gastric bypass), passageklachten, revisie operatie en galstenen als relevante complicaties op lange termijn (> 30 dagen). De werkgroep hanteerde de in de studies gebruikte definities voor deze complicaties. De werkgroep hanteerde de door de internationale GRADE-working group voorgestelde default grenzen gehanteerd voor klinische relevantie: een verschil in relatief risico van 25% bij dichotome uitkomstmaten.
Gewichtsverlies diende te zijn uitgedrukt in percentage excess weight loss (EWL). De werkgroep beschouwde een verschil van ≥ 10% EWL tussen beide operatietechnieken als klinisch relevant.
De remissie en/of verbetering van co-morbiditeiten en kwaliteit van leven diende ten minste na één jaar follow-up te zijn vastgesteld. De werkgroep hanteerde de in de studies gebruikte definities voor remissie en verbetering.
Algehele kwaliteit van leven diende te zijn vastgesteld middels gevalideerde vragenlijsten. De werkgroep definieerde niet a priori een klinisch relevant verschil voor kwaliteit van leven, maar hanteerde in de studie gebruikte definities.
Zoeken en selecteren
In de databases Medline (via Pubmed), Embase (via Embase.com) en de Cochrane Library (via Wiley) is met relevante zoektermen gezocht naar systematische reviews, gerandomiseerde studies en observationeel onderzoek. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie voor de subgroep leverde 1.953 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria:
- (een systematische review van) randomised controlled trials (RCT’s).
- Artikel full-tekst beschikbaar in het Engels of Nederlands.
Artikelen die niet-laparoscopisch uitgevoerde metabole operaties onderzochten konden worden geïncludeerd in de literatuuranalyse. Echter, voor deze studies werd de uitkomst complicaties niet meegenomen, aangezien het reeds bekend is dat deze operatietechniek meer complicaties geeft vergeleken met laparoscopisch uitgevoerde operaties.
Op basis van titel en abstract werden in eerste instantie 32 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 25 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording). Eén relevante studie werd gevonden middels cross-referencing (Lee, 2005).
Acht onderzoeken werd opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidencetabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk of bias tabellen.
Resultaten
Acht onderzoeken zijn opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidencetabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk-of-biastabellen.
- Bhandari M, Fobi MAL, Buchwald JN; and the Bariatric Metabolic Surgery Standardization (BMSS) Working Group:. Standardization of Bariatric Metabolic Procedures: World Consensus Meeting Statement. Obes Surg. 2019 Jul;29(Suppl 4):309-345. doi: 10.1007/s11695-019-04032-x. PubMed PMID: 31297742.
- Ignat, M., Vix, M., Imad, I., D'urso, A., Perretta, S., Marescaux, J., & Mutter, D. (2017). Randomized trial of Roux‐en‐Y gastric bypass versus sleeve gastrectomy in achieving excess weight loss. British Journal of Surgery, 104(3), 248-256.
- Kehagias, I., Karamanakos, S. N., Argentou, M., & Kalfarentzos, F. (2011). Randomized clinical trial of laparoscopic Roux-en-Y gastric bypass versus laparoscopic sleeve gastrectomy for the management of patients with BMI< 50 kg/m 2. Obesity surgery, 21(11), 1650-1656
- Lee, W. J., Yu, P. J., Wang, W., Chen, T. C., Wei, P. L., & Huang, M. T. (2005). Laparoscopic Roux-en-Y versus mini-gastric bypass for the treatment of morbid obesity: a prospective randomized controlled clinical trial. Annals of surgery, 242(1), 20.
- Paluszkiewicz, R., Kalinowski, P., Wróblewski, T., Bartoszewicz, Z., Białobrzeska-Paluszkiewicz, J., Ziarkiewicz-Wróblewska, B., ... & Krawczyk, M. (2012). Prospective randomized clinical trial of laparoscopic sleeve gastrectomy versus open Roux-en-Y gastric bypass for the management of patients with morbid obesity. Videosurgery and Other Miniinvasive Techniques, 7(4), 225.
- Peterli, R., Wölnerhanssen, B. K., Peters, T., Vetter, D., Kröll, D., Borbély, Y., ... & Nett, P. (2018). Effect of laparoscopic sleeve gastrectomy versus laparoscopic Roux-en-Y gastric bypass on weight loss in patients with morbid obesity: the SM-BOSS randomized clinical trial. Jama, 319(3), 255-265.
- Salminen, P., Helmiö, M., Ovaska, J., Juuti, A., Leivonen, M., Peromaa-Haavisto, P., ... & Victorzon, M. (2018). Effect of laparoscopic sleeve gastrectomy versus laparoscopic Roux-en-Y gastric bypass on weight loss at 5 years among patients with morbid obesity: the SLEEVEPASS randomized clinical trial. Jama, 319(3), 241-254
- Sebastianelli L, Benois M, Vanbiervliet G, Bailly L, Robert M, Turrin N, Gizard E, Foletto M, Bisello M, Albanese A, Santonicola A, Iovino P, Piche T, Angrisani L, Turchi L, Schiavo L, Iannelli A. Systematic Endoscopy 5 Years After Sleeve Gastrectomy Results in a High Rate of Barrett's Esophagus: Results of a Multicenter Study. Obes Surg. 2019 May;29(5):1462-1469. doi: 10.1007/s11695-019-03704-y. PubMed PMID: 30666544.
- Shivakumar, S., Tantia, O., Goyal, G., Chaudhuri, T., Khanna, S., Ahuja, A., ... & Majumdar, K. (2018). LSG versus MGB-OAGB—3 Year Follow-up Data: a Randomised Control Trial. Obesity surgery, 28(9), 2820-2828.
- Zhang, Y., Zhao, H., Cao, Z., Sun, X., Zhang, C., Cai, W., ... & Qin, M. (2014). A randomized clinical trial of laparoscopic Roux-en-Y gastric bypass and sleeve gastrectomy for the treatment of morbid obesity in China: a 5-year outcome. Obesity surgery, 24(10), 1617-1624.
Evidence table for intervention studies (randomized controlled trials and non-randomized observational studies (cohort studies, case-control studies, case series))1
This table is also suitable for diagnostic studies (screening studies) that compare the effectiveness of two or more tests. This only applies if the test is included as part of a test-and-treat strategy – otherwise the evidence table for studies of diagnostic test accuracy should be used.
Research question: Welke chirurgische techniek leidt bij volwassenen met ernstige obesitas tot de beste uitkomsten?
Comparison: LRYGB versus. LSG
Research question: Welke chirurgische techniek leidt bij volwassenen met ernstige obesitas tot de beste uitkomsten?
Comparison: LMGB versus LRYGB
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C)
|
Follow-up |
Outcome measures and effect size |
Comments |
|
Lee (2005) |
Type of study: RCT
Setting and country: Taiwan
Funding and conflicts of interest: |
Inclusion criteria: a history of obesity of _5 years’ duration; BMI _ 40 kg/m2 or BMI _ 35 kg/m2 with comorbidities; documented weight loss attempts in the past; and good motivation for surgery. The age was restricted to patients from 18 to 59 years of age.
Exclusion criteria: previous obesity surgery, previous gastric surgery, large abdominal ventral hernia, pregnancy, psychiatric illness, or BMI > 60 kg/m2.
N total at baseline: Intervention: 40 Control: 40
Important prognostic factors2: Age, mean ± SD: LMGBP: 30.7 ± 8.4 LRYGBP: 31.1 ±9.1
Sex, F: M ratio I: 27:13 C: 28:12
BMI: I: 44.8 ± 8.8
Groups comparable at baseline? Yes
|
Describe intervention (treatment/procedure/test):
laparoscopic mini-gastric bypass (LMGBP)
|
Describe control (treatment/procedure/test):
laparoscopic Roux-en-Y gastric bypass (LRYGBP)
|
Length of follow-up: minimum postoperative follow-up was 2 years (mean, 31.3 months)
Loss-to-follow-up: 0 Incomplete outcome data: 0
|
Outcome measures and effect size (include 95%CI and p-value if available):
Excess weight reduction (EWL),% 1 year post surgery LRYGBP: 58.7 ± 16.4
EWL,% 2 years post surgery LRYGBP: 64.4 ± 8.8
Early complications Bleedings: I:0 C:0
LMGBP: 7.5% 3 minor complications LRYGBP: 20% Two of the 8 complications in the LRYGBP group were major, and both were related to anastomotic leakage. Six patients in the LRYGBP group developed minor complications, including upper gastrointestinal bleeding, ileus, and leakage from the drainage tube. All of them recovered after conservative treatment.
Increase in Quality of life 1 year after surgery Gastrointestinal Quality of Life Index (GIQLI) (GIQLI) |
|
Research question: Welke chirurgische techniek leidt bij volwassenen met ernstige obesitas tot de beste uitkomsten?
Comparison: LMGB versus LSG
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C)
|
Follow-up |
Outcome measures and effect size |
Comments |
|
Shivakumar (2018) |
Type of study: RCT
Setting and country: India
Funding and conflicts of interest: Funding: not reported
The authors declare that they have no conflict of interest. |
Inclusion criteria: Patients between 18 to 60 years, with BMI > 35 kg/m2 and less than 60 kg/m2
Exclusion criteria: Patients younger than 18 years, older than 60 years, history of psychiatric illness, pregnancy, previous bariatric surgery, non-compliant, non-willing to be part of the RCT and lost for follow-up
N total at baseline: Intervention: 100 Control: 101
Important prognostic factors2: Age ± SD: I: 39.89 ± 11.75 C: 42.89 ± 14.02
Sex M:F ratio I: 35/65 C: 39/62
BMI ± SD: I: 44.57 ± 7.16 C: 44.32 ± 7.88
Groups comparable at baseline? Yes
|
Describe intervention (treatment/procedure/test):
laparoscopic sleeve gastrectomy (LSG)
|
Describe control (treatment/procedure/test):
one anastomosis gastric bypass (MGB-OAGB) |
Length of follow-up: minimum 3 years
Loss-to-follow-up: LSG Year 2: 5 Year 3: 3
OAGB Year 2: 4 Year 3: 4
Incomplete outcome data: LSG: 2 -died
OAGB: 3 -refused follow up (2x) -died
|
Outcome measures and effect size (include 95%CI and p-value if available):
EWL 3 years post surgery LSG: 61.15 ± 25.27 OAGB: 66.48 ± 15.72
Short term readmissions LSG: 10 OAGB: 7
Long term re-admisson (>30 days) LSG: 3 OAGB: 5 Revision:
Diabetes mellitus remission at 3 years LSG: 82% OAGB: 89%
HbA1c at 3 years LSG: 6.32 ± 0.31 OAGB: 6.13 ± 0.27
Hypertension remission at 3 years OAGB: 74% P=1.00
|
|
Risk of bias assessment
Risk of bias table for intervention studies (randomized controlled trials)
Research question:
|
Study reference
(first author, publication year) |
Describe method of randomisation |
Bias due to inadequate concealment of allocation?
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?
(unlikely/likely/unclear) |
Bias due to loss to follow-up?
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?
(unlikely/likely/unclear) |
|
Paluszkiewicz, 2012 |
“Simple randomization” |
Unclear |
Unclear |
Likely |
Unclear |
Unlikely |
Unlikely |
Unlikely |
|
Zhang, 2014 |
Computer-generated random numbers were used to allocate the type of procedure (LRYGB or LSG), which was written on a card and sealed in a completely opaque envelop. |
Unlikely |
Unclear |
Likely |
Unclear |
Unlikely |
Unlikely |
Unlikely |
|
Peterli (2018) |
closed envelope |
Unlikely |
Likely |
Likely |
Likely |
Unlikely |
Unlikely |
Unlikely |
|
Kehagias (2011) |
Computer-generated random numbers |
Unlikely |
Likely |
Likely |
Likely |
Unlikely |
Unlikely |
Unlikely |
|
Lee (2005) |
sealed envelopes |
Unlikely |
Likely |
Likely |
Likely |
Unlikely |
Unlikely |
Unlikely |
|
Ignat (2017) |
closed envelopes |
Unlikely |
Likely |
Likely |
Likely |
Unlikely |
Likely, considerable loss-to-follow-up |
Unlikely |
|
Salminen (2018) |
opaque, sealed, closed-envelope |
Unlikely |
Likely |
Likely |
Likely |
Unlikely |
Unlikely, Loss-to-FU same in both groups and missing data are imputed |
Unlikely |
|
Shivakumar (2018) |
computer-generated sequence consisting of permuted blocks of six patients |
Unlikely |
Unlikely |
Likely |
Likely |
Unlikely |
Loss to FU is considerable 3 years after surgery |
Likely |
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Helmiö (2012) |
Salminen (2018) betreft dezelfde trial en recentere uitkomsten en de uitkomsten uit deze studie mee |
|
Helmiö (2014) |
Salminen (2018) betreft dezelfde trial en recentere uitkomsten en de uitkomsten uit deze studie mee |
|
Vix (2013) |
Geen uitkomstmaten volgens PICO |
|
Vix (2014) |
Geen uitkomstmaten volgens PICO |
|
Karamanakos (2008) |
Geen uitkomstmaten volgens PICO |
|
de Barros (2015) |
Geen uitkomstmaten volgens PICO |
|
Osland (2016)a |
Onvolledig systematische review |
|
Osland (2016)b |
Onvolledig systematische review |
|
Ramón (2012) |
Geen uitkomstmaten volgens PICO |
|
Woelnerhanssen (2011) |
Geen uitkomstmaten volgens PICO |
|
Li (2016) |
Onvolledig systematische review |
|
Kalinowski (2017) |
Geen uitkomstmaten volgens PICO |
|
Praveen (2012) |
Niet juiste operatietechniek |
|
Schneider (2016) |
Geen uitkomstmaten volgens PICO |
|
Capristo (2018) |
Geen uitkomstmaten volgens PICO |
|
Peterli (2012) |
Geen uitkomstmaten volgens PICO |
|
Peterli (2009) |
Geen uitkomstmaten volgens PICO |
|
Spuntarelli (2015) |
Congres abstract |
|
Woelnerhanssen (2011) |
Geen uitkomstmaten volgens PICO |
|
Arman (2015) |
Geen uitkomstmaten volgens PICO |
|
Fischer (2015) |
Geen uitkomstmaten volgens PICO |
|
Jerraya (2015) |
Geen uitkomstmaten volgens PICO |
|
Li (2014) |
Geen uitkomstmaten volgens PICO |
|
Seetharamaiah (2017) |
Oud systematische review met cohortstudies |
|
Svanevik (2015) |
Niet juiste vergelijking volgens PICO |
Beoordelingsdatum en geldigheid
Publicatiedatum : 28-10-2020
Beoordeeld op geldigheid : 28-10-2020
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep niet in stand gehouden. Uiterlijk in 2025 bepaalt het bestuur van de Nederlandse Vereniging voor Heelkunde of de modules van deze richtlijn nog actueel zijn. Op modulair niveau is een onderhoudsplan beschreven. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De Nederlandse Vereniging voor Heelkunde is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
|
Module1 |
Regiehouder(s)2 |
Jaar van autorisatie |
Eerstvolgende beoordeling actualiteit richtlijn3 |
Frequentie van beoordeling op actualiteit4 |
Wie houdt er toezicht op actualiteit5 |
Relevante factoren voor wijzigingen in aanbeveling6 |
|
Operatiekeuze bij Volwassenen |
NVvH |
2020 |
2022 |
1x per 2 jaar |
NVvH |
Veel ontwikkelingen op het gebied van de mini-bypass |
|
[1] Naam van de module 2 Regiehouder van de module (deze kan verschillen per module en kan ook verdeeld zijn over meerdere regiehouders) 3 Maximaal na vijf jaar 4 (half)Jaarlijks, eens in twee jaar, eens in vijf jaar 5 regievoerende vereniging, gedeelde regievoerende verenigingen, of (multidisciplinaire) werkgroep die in stand blijft 6 Lopend onderzoek, wijzigingen in vergoeding/organisatie, beschikbaarheid nieuwe middelen |
||||||
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS) en/of andere bron. De financier heeft geen enkele invloed gehad op de inhoud van de richtlijn.
Doel en doelgroep
Doel
Doel van deze herziening is om tot een richtlijn te komen waarin de meest recente kennis omtrent de chirurgische zorg voor patiënten met obesitas is vastgelegd.
Doelgroep
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen die betrokken zijn bij de zorg voor patiënten met obesitas.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2017 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met ernstige obesitas (zie hiervoor de samenstelling van de werkgroep).
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
Werkgroep
- Dr. F.J. Berends, chirurg, Nederlandse Vereniging voor Heelkunde (voorzitter)
- Dr. I.F. Faneyte, chirurg, ZiekenhuisGroep Twente, Almelo/Hengelo, Nederlandse Vereniging voor Heelkunde
- Dr. R. Schouten, chirurg, Flevoziekenhuis, Almere, Nederlandse Vereniging voor Heelkunde
- Dr. F.M.H. van Dielen, chirurg, Máxima Medisch Centrum, Veldhoven/Eindhoven, Nederlandse Vereniging voor Heelkunde
- Prof. dr. L.W.E. van Heurn, hoogleraar kinderchirurgie, chirurg, Amsterdam UMC locatie AMC, Amsterdam, plaats, Nederlandse Vereniging voor Heelkunde
- Dr. S. Bouma- de Jongh, kinderarts, De Kinderartsenpraktijk, Nederlandse Vereniging voor Kindergeneeskunde
- Dr. A.C.E. Vreugdenhil, kinderarts, MUMC+, Maastricht, Nederlandse Vereniging voor Kindergeneeskunde
- Dr. A.P. van Beek, internist, UMCG, Groningen, Nederlandse Internisten Vereniging
- Dr. J.S. Burgerhart, internist i.o., Erasmus MC, Rotterdam tot 31 december 2019, vanaf 1 januari 2020 internist-vasculair geneeskundige, Ziekenhuis St Jansdal, Harderwijk, Nederlandse Internisten Vereniging
- Dr. M.J.M. Groenen, MDL-arts, Rijnstate, Arnhem, Nederlandse Vereniging van Maag-Darm-Leverartsen
- Dr. S.V. Koenen, gynaecoloog, Elisabeth-TweeSteden-Ziekenhuis, Tilburg, Nederlandse Vereniging voor Obstetrie en Gynaecologie
- Drs. M.S.Q. Kortenhorst, gynaecoloog i.o. UMC Utrecht, Utrecht, Nederlandse Vereniging voor Obstetrie en Gynaecologie
- Dr. R.C. Painter, gynaecoloog, Amsterdam UMC, locatie AMC, Nederlandse Vereniging voor Obstetrie en Gynaecologie
- Dr. J.O.E.H. van Laar, gynaecoloog, Máxima Medisch Centrum, Veldhoven/Eindhoven, Nederlandse Vereniging voor Obstetrie en Gynaecologie
- N.G. Cnossen, patiëntvertegenwoordiger, Nederlandse Stichting Over Gewicht
- Dr. C. Hinnen, klinisch psycholoog, LUMC, Leiden, Nederlands Instituut van Psychologen
- E. Govers BSc., diëtist, Amstelring, Amsterdam, Nederlandse Vereniging van Diëtisten
Klankbordgroep
- Prof. dr. E.F.C. van Rossum, internist, Erasmus MC, Rotterdam, Nederlandse Internisten Vereniging
Met ondersteuning van
- Dr. A. Bijlsma, adviseur, Kennisinstituut van de Federatie Medisch Specialisten (vanaf oktober 2018)
- Dr. J. Buddeke, adviseur, Kennisinstituut van de Federatie Medisch Specialisten (vanaf oktober 2018)
- Dr. W.A. van Enst, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten (tot oktober 2018)
- Dr. S.N. Hofstede, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten (vanaf oktober 2018)
- Drs. A.A. Lamberts, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten (vanaf oktober 2018)
- J.C.F. Ket, medisch informatiespecialist, Van Dusseldorp, Delvaux & Ket
- I. van Dusseldorp, medisch informatiespecialist, Van Dusseldorp, Delvaux & Ket
- E. Delvaux, medisch informatiespecialist, Van Dusseldorp, Delvaux & Ket
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in de onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van Medisch Specialisten.
|
Achternaam WG-lid |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Getekend op |
Actie (voorstel) |
|
Berends (voorzitter) |
Freelance chirurg |
Consultant Johnson & Johnson tot september 2018 (betaald) |
De firma Johnson & Johnson heeft een "baratric and metabolic board" waarvan ik lid ben. (Betaald) |
geen |
geen |
|
geen |
24-11-2017 |
Geen. Er staan geen producten van Johnson in deze richtlijn. |
|
Hinnen |
Oncologisch centrum, LUMC, afdeling medische psychologie en ziekenhuis-psychiatrie, MC Slotervaart |
Bestuur Nederlandse Behavioral Medicine Federatie (onbetaald) |
geen |
geen |
geen |
geen |
geen |
31-10-2017 |
Geen |
|
Schouten |
Chirurg, Flevoziekenhuis te Almere |
geen |
geen |
geen |
geen |
geen |
geen |
8-11-2017 |
Geen |
|
Groenen |
Maag Darm Leverarts, werkzaam in Rijnstate Ziekenhuis te Arnhem |
Concilium Gastroenterolgicum, onbetaald |
geen |
geen |
Betrokken bij onderzoek betreffende Chronische darmontsteking (Crohn en Colitis Ulcerosa) waarbij ondersteuning door industrie. |
geen |
geen |
9-11-2017 |
Geen, gefinancierde onderzoeken/ training gaan niet over obesitas |
|
Faneyte |
Chirurg 75% ZiekenhuisgroepTwente |
geen |
geen persoonlijke financiële belangen behoudens eigen werk als vrijgevestigd bariatrisch chirurg |
geen |
geen |
geen |
geen |
9-11-2017 |
Geen |
|
Govers |
Diëtist, Stichting Amstelring (inmiddels niet meer werkzaam) |
Voorzitter Kenniscentrum Diëtisten Overgewicht en Obesitas, Amsterdam, |
geen |
geen |
geen |
geen |
- |
26-11-2017 |
Geen |
|
Van Laar |
gynaecoloog |
Assistant professor TU/e |
geen |
geen |
geen |
geen |
geen |
1-12-2017 |
Geen |
|
Koenen |
Gynaecoloog, UMC Utrecht (vanaf 1 januari 2018 ETZ, Tilburg) 1,0 FTE werkzaam |
Voorzitter Werkgroep Otterlo NVOG (werkgroep die verantwoordelijk is voor richtlijnen over de Verloskunde). Onbetaald |
geen |
geen |
geen |
geen |
nee |
12-12-2017 |
Geen |
|
Painter |
Gynaecoloog, Afdeling Verloskunde, AMC, Amsterdam 0,9 FTE |
• Affiliatie: Gynaecoloog Amsterdam UMC • lid van de werkgroep modulaire richtlijn Zwangerschap en Obesitas (NVOG). • vice voorzitter van de NVOG Pijler FMG Wetenschapscommissie • voorzitter SIG NVOG Diabetes, Obesitas en Zwangerschap • lid van de Koepel Wetenschap NVOG • lid van de RIVM Commissie Programma Nationale Hielprik Screening (namens de NVOG) • lid stuurgroep James Lind Alliance PSP 'Hyperemesis Gravidarum' |
geen |
geen |
CVON/ Nederlandse Hartstichting, WOMB project (hoofdaanvrager prof Roseboom) AMC-VuMc Alliantie OiO (mede aanvrager dr AE Budding) |
Lid Wetenschappelijke Advies Raad Stichting ZEHG (Hyperemesis Gravidarum patiënten vereniging) |
geen |
29-11-2017 |
Geen, de onderzoeken betreffen onderwerpen die buiten de afbakening van de richtlijn vallen. |
|
Kortenhorst |
Gynaecoloog-in-opleiding Wilhelmina Kinderziekenhuis |
geen |
geen |
geen |
geen |
geen |
geen |
1-12-2017 |
Geen |
|
Cnossen |
Ervaringsdeskundige werkgroep bariatrie van de Nederlandse stichting Over Gewicht -(Onbetaald) |
geen |
geen |
geen |
geen |
geen |
geen |
19-1-2018 |
Geen |
|
Burgerhart |
internist- vasculair geneeskundig i.o. in opleiding Erasmus MC Rotterdam t/m 31-12-2019. Vanaf 1-1-2020 internist-vasculair geneeskundige, Ziekenhuis St Jansdal, Harderwijk |
geen |
geen |
geen |
geen |
geen |
geen |
18-5-2018 |
Geen |
|
Heurn |
Kinderchirurg, hoogleraar kinderchirurgie AMC en VUMC |
geen |
geen |
geen |
geen |
Hoofdonderzoeker BASIC trial: onderzoek naar bariatrische |
geen |
28-2-2018 |
Geen, onderzoek wordt op dit moment gefinancierd door het ziekenhuis zelf. Funding wordt nog wel gezocht. Resultaten nog niet bekend |
|
Beek |
internist-endocrinoloog (100%) in het UMC Groningen. |
geen |
geen |
geen |
Select studie. Effecten op cardiovasculaire uitkomsten bij patiënten met overgewicht of obesitas (Novo Nordisk). Het betreft een multicenter trial waarbij in totaal 17500 patiënten worden geïncludeerd. Mijn centrum zal 25 patiënten includeren en NL in totaal 250. Ik ben National Leader in deze studie die is gestart 24-10-2018. Uitkomsten worden verwacht in 2023. Geen belangen verstrengeling zowel inhoudelijk (resultaten nog niet bekend) als financieel. |
geen |
geen |
13-7-2018 |
Geen
Uitkomsten van de studie worden verwacht in 2023. Redelijkerwijs zal deze studie dus geen belangenverstrengeling opleveren omdat er geen uitkomsten nog van de studie zijn. |
|
Dielen |
Bariatrisch chirurg |
0.0 fte aanstelling in het Mumc+ als gastoperateur voor de BASIC trial. Betaald |
geen |
geen |
geen |
Gastroperateur van de BASIC trial en derhalve hierbij actief betrokken. - Principal investigator van een internationale multicenter prospectief gerandomiseerde studie gastric sleeve versus. gastric bypass in adolescenten. (TEEN-Best). Voorlopige startdatum 1 september 2018 |
geen |
6-3-2018 |
Geen, onderzoek wordt op dit moment gefinancierd door het ziekenhuis zelf. Funding wordt nog wel gezocht. Resultaten nog niet bekend |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door een afgevaardigde van de Stichting Over Gewicht (voorheen Nederlandse Obesitas Vereniging) plaats te laten nemen in de werkgroep. De volgende patiëntenorganisaties zijn uitgenodigd voor de Invitational conference: Patiëntenfederatie Nederland, Hart en Vaatgroep, Diabetesvereniging en Stichting Over Gewicht. Een verslag van deze bijeenkomst is besproken in de werkgroep en de belangrijkste knelpunten zijn verwerkt in de richtlijn. Tijdens de oriënterende zoekactie (uitgevoerd op 18 december 2017) werd gezocht op literatuur naar patiëntenperspectief (zie Strategie voor zoeken en selecteren van literatuur). De conceptrichtlijn is tevens voor commentaar voorgelegd aan de Patiëntenfederatie Nederland, Hart en Vaatgroep, Diabetesvereniging en Stichting Over Gewicht.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van de Federatie Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens zijn er knelpunten aangedragen door verschillende stakeholders tijdens een Invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar bestaande buitenlandse richtlijnen (GIN-database), systematische reviews, literatuur over patiëntvoorkeuren en patiëntrelevante uitkomstmaten (Medline, Comet-initiative en COSMIN database). Vervolgens werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens is aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie voor de oriënterende zoekactie en patiëntenperspectief zijn opgenomen onder aanverwante producten.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR - voor systematische reviews; Cochrane - voor gerandomiseerd gecontroleerd onderzoek; Newcastle-Ottowa - voor observationeel onderzoek; QUADAS II - voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk* |
|
|
Laag |
|
|
Zeer laag |
|
*in 2017 heeft het Dutch GRADE Network bepaalt dat de voorkeursformulering voor de op een na hoogste gradering ‘redelijk’ is in plaats van ‘matig’
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008), en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de cruciale uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van Zorg.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in het aanverwante product Kennislacunes beschreven.
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers, M. C., Kho, M. E., Browman, G. P., Burgers, J. S., Cluzeau, F., Feder, G., ... & Littlejohns, P. (2010). AGREE II: advancing guideline development, reporting and evaluation in health care. Canadian Medical Association Journal, 182(18), E839-E842.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html
Kennisinstituut. Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van Medisch Specialisten. 2015
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann, H. J., Oxman, A. D., Brozek, J., Glasziou, P., Jaeschke, R., Vist, G. E., ... & Bossuyt, P. (2008). Rating Quality of Evidence and Strength of Recommendations: GRADE: Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ: British Medical Journal, 336(7653), 1106.
Wessels, M., Hielkema, L., & van der Weijden, T. (2016). How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. Journal of the Medical Library Association: JMLA, 104(4), 320.
Zoekverantwoording
|
Uitgangsvraag: Welke operatietechniek is voor welke indicatie geïndiceerd?
Algemeen: P: mensen die in aanmerking komen voor metabole chirurgie I: gastric bypass C: gastric sleeve O: beter resultaat, etc.
Subgroepen: P: vrouwen met een kinderwens P: kinderen P: ouderen P: reflux P: diabetes P: overige |
|
|
Database(s): PubMed |
Datum: 25-6-2018 |
|
Periode: geen restrictie, voor 2000 slechts 10 referenties meer in PubMed, zie #16 en #29 |
Talen: geen restrictie |
|
Opmerking: Op verzoek is deze vraag behandeld als 1 uitgangsvraag met een aantal subgroepen. In de uitwerking is onderscheid gemaakt tussen de verschillende subgroepen en zijn de resultaten van de verschillende groepen ontdubbeld. NB. Als gevolg van het ontdubbelen worden studies waarin meerdere groepen met elkaar worden vergeleken, slechts bij 1 subgroep getoond. Dus, een studie waarin zowel diabetes als reflux wordt genoemd wordt alleen zichtbaar in 1 van de 2 subgroepen en niet bij beide. Daarom zijn bij elke subgroep alle abstracts doorlopen. |
|
PubMed
|
Search |
Query |
Items found |
|
#62 |
#41 AND #44 overig epidemiologisch |
626 |
|
#61 |
#41 AND #43 overig RCT |
223 |
|
#60 |
#41 AND #42 overig SR |
248 |
|
#47 |
#35 AND #44 diabetes epidemiologisch |
514 |
|
#46 |
#35 AND #43 diabetes RCT |
215 |
|
#45 |
#35 AND #42 diabetes SR |
201 |
|
#59 |
#39 AND #44 ouderen epidemiologisch |
229 |
|
#58 |
#39 AND #43 ouderen RCT |
61 |
|
#57 |
#39 AND #42 ouderen SR |
53 |
|
#53 |
#37 AND #44 kinderen epidemiologisch |
168 |
|
#52 |
#37 AND #43 kinderen RCT |
51 |
|
#51 |
#37 AND #42 kinderen SR |
59 |
|
#50 |
#36 AND #44 reflux epidemiologisch |
155 |
|
#49 |
#36 AND #43 reflux RCT |
46 |
|
#48 |
#36 AND #42 reflux SR |
73 |
|
#56 |
#38 AND #44 vrouwen met een kinderwens epidemiologisch |
15 |
|
#55 |
#38 AND #43 vrouwen met een kinderwens RCT |
2 |
|
#54 |
#38 AND #42 vrouwen met een kinderwens SR |
6 |
|
#44 |
(("Epidemiologic Studies"(Mesh) OR "Prognosis"(Mesh) OR cohort(tiab) OR (case(tiab) AND (control(tiab) OR controll*(tiab) OR comparison(tiab) OR referent(tiab))) OR risk(tiab) OR causation(tiab) OR causal(tiab) OR "odds ratio"(tiab) OR etiol*(tiab) OR aetiol*(tiab) OR "natural history"(tiab) OR predict*(tiab) OR prognos*(tiab) OR outcome(tiab) OR course(tiab) OR retrospect*(tiab) OR follow up(tiab) OR followup(tiab) OR prognos*(tiab))) |
6426112 |
|
#43 |
(("Randomized Controlled Trial"(Publication Type) OR "Controlled Clinical Trial"(Publication Type) OR random*(tiab) OR placebo(tiab) OR "Drug Therapy"(Subheading) OR trial(tiab) OR groups(tiab))) |
4468366 |
|
#42 |
(((review(tiab) OR "Review"(Publication Type) OR "Meta-Analysis as Topic"(Mesh) OR meta-analysis(tiab) OR "Meta-Analysis "(Publication Type)) NOT ("Letter"(Publication Type) OR "Editorial"(Publication Type) OR "Comment"(Publication Type)))) |
2921053 |
|
#41 |
#16 NOT #40 |
886 |
|
#40 |
#35 OR #36 OR #37 OR #38 OR #39 |
1011 |
|
#39 |
#16 AND #34 |
245 |
|
#38 |
#16 AND #31 |
18 |
|
#37 |
#16 AND #30 |
199 |
|
#36 |
#16 AND #28 |
189 |
|
#35 |
#16 AND #17 |
645 |
|
#34 |
("Aged"(Mesh) OR "Aged, 80 and over"(Mesh) OR "Frail Elderly"(Mesh) OR "Geriatrics"(Mesh) OR "Geriatric Psychiatry"(Mesh) OR "Geriatric Nursing"(Mesh) OR "Geriatric Dentistry"(Mesh) OR "Dental Care for Aged"(Mesh) OR "Health Services for the Aged"(Mesh)) OR (elder*(tw) OR eldest(tw) OR frail*(tw) OR geriatri*(tw) OR old age*(tw) OR oldest old*(tw) OR senior*(tw) OR senium(tw) OR very old*(tw) OR septuagenarian*(tw) OR octagenarian*(tw) OR octogenarian*(tw) OR nonagenarian*(tw) OR centarian*(tw) OR centenarian*(tw) OR supercentenarian*(tw) OR older people(tw) OR older subject*(tw) OR older patient*(tw) OR older age*(tw) OR older adult*(tw) OR older man(tw) OR older men(tw) OR older male*(tw) OR older woman(tw) OR older women(tw) OR older female*(tw) OR older population*(tw) OR older person*(tw)) |
3004680 |
|
#31 |
"Pregnancy"(Mesh) OR "Pregnant Women"(Mesh) OR "Preconception Care"(Mesh) OR pregnan*(tiab) OR gravidit*(tiab) OR gestation*(tiab) OR placentat*(tiab) OR prepregnan*(tiab) OR conception*(tiab) OR preconception*(tiab) |
1006196 |
|
#30 |
child*(tw) OR schoolchild*(tw) OR infan*(tw) OR adolescen*(tw) OR pediatri*(tw) OR paediatr*(tw) OR neonat*(tw) OR boy(tw) OR boys(tw) OR boyhood(tw) OR girl(tw) OR girls(tw) OR girlhood(tw) OR youth(tw) OR youths(tw) OR baby(tw) OR babies(tw) OR toddler*(tw) OR "Mental Disorders Diagnosed in Childhood"(MeSH) OR teen(tw) OR teens(tw) OR teenager*(tw) OR newborn*(tw) OR postneonat*(tw) OR postnat*(tw) OR perinat*(tw) OR puberty(tw) OR preschool*(tw) OR suckling*(tw) OR picu(tw) OR nicu(tw) OR "Arthritis, Juvenile"(Mesh) OR "Myoclonic Epilepsy, Juvenile"(Mesh) OR "Leukemia, Myelomonocytic, Juvenile"(Mesh) OR "Xanthogranuloma, Juvenile"(Mesh) OR "Juvenile Delinquency"(Mesh) OR "Corneal Dystrophy, Juvenile Epithelial of Meesmann"(Mesh) |
4049936 |
|
#28 |
(("Gastroesophageal Reflux"(Mesh)) OR "Bile Reflux"(Mesh)) OR "Duodenogastric Reflux"(Mesh) OR reflux*(tiab) |
58129 |
|
#17 |
"Diabetes Mellitus"(Mesh) OR "Hypoglycemic Agents"(Mesh) OR "Hypoglycemic Agents" (Pharmacological Action) OR diabetes(tiab) OR diabetic*(tiab) OR insulin*(tiab) OR metformin*(tiab) OR rosiglitazon*(tiab) OR troglitazon*(tiab) OR pioglitazon*(tiab) OR hypoglycem*(tiab) OR hypoglycaem*(tiab) |
857247 |
|
#29 |
#14 AND #15 Filters: Publication date from 2000/01/01 |
1887 |
|
#16 |
#14 AND #15 |
1897 |
|
#15 |
"Gastric Balloon"(Mesh) OR gastric sleev*(tiab) OR sleeve gastrectom*(tiab) OR stomach stapl*(tiab) OR gastric balloon*(tiab) |
4643 |
|
#14 |
"Gastric Bypass"(Mesh) OR gastric bypass*(tiab) OR roux en y*(tiab) OR gastroileal bypass*(tiab) OR gastrojejunostom*(tiab) OR jejunoileal bypass*(tiab) OR jejuno ileal bypass*(tiab) OR ileojejunal bypass*(tiab) OR intestinal bypass*(tiab)OR omega loop*(tiab) |
17611 |
Embase.com
|
No. |
Query |
Results |
|
#68 |
#48 AND ((cohort:ti,ab,kw OR (case:ti,ab,kw AND (control:ti,ab,kw OR controll*:ti,ab,kw OR comparison:ti,ab,kw OR referent:ti,ab,kw)) OR risk:ti,ab,kw OR causation:ti,ab,kw OR causal:ti,ab,kw OR 'odds ratio':ti,ab,kw OR etiol*:ti,ab,kw OR aetiol*:ti,ab,kw OR 'natural history':ti,ab,kw OR predict*:ti,ab,kw OR prognos*:ti,ab,kw OR outcome:ti,ab,kw OR course:ti,ab,kw OR retrospect*:ti,ab,kw OR 'epidemiology'/de OR follow) AND up:ti,ab,kw OR followup:ti,ab,kw OR predict*:ti,ab,kw OR prognos*:ti,ab,kw) Overig, Epidemiologisch, |
325 |
|
#67 |
#48 AND ('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) Overig RCT |
200 |
|
#66 |
#48 AND (('meta analysis'/de OR cochrane:ab OR embase:ab OR psychlit:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de), Overig SR |
86 |
|
#48 |
(#23 OR #24 OR #25 OR #26 OR #43) NOT (#30 OR #31 OR #32 OR #33 OR #34 OR #35 OR #36 OR #37 OR #38 OR #39 OR #40 OR #41 OR #42) |
493 |
|
#47 |
#23 OR #24 OR #25 OR #26 OR #43 |
891 |
|
#46 |
#43 AND ('clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR ('prospective study'/de NOT 'randomized controlled trial'/de) OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (case:ab,ti AND ((control NEAR/1 (study OR studies)):ab,ti)) OR (follow:ab,ti AND ((up NEAR/1 (study OR studies)):ab,ti)) OR ((observational NEAR/1 (study OR studies)):ab,ti) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti Kinderwens, epidemiologisch |
12 |
|
#45 |
#43 AND ('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti Kinderwens, RCT |
1 |
|
#44 |
#43 AND (('meta analysis'/de OR cochrane:ab OR embase:ab OR psychlit:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp)) Kinderwens, SR |
0 |
|
#43 |
(((('gastric bypass surgery' OR 'gastric bypass*':ti,ab OR 'roux en y':ti,ab OR 'gastroileal bypass*':ti,ab OR 'gastrojejunostom*':ti,ab OR 'jejunoileal bypass*':ti,ab OR 'jejuno ileal bypass*':ti,ab OR 'ileojejunal bypass*':ti,ab OR 'intestinal bypass*':ti,ab) AND ('gastric balloon'/exp OR 'gastric sleev*':ti,ab OR 'sleeve gastrectom*':ti,ab OR 'gastric balloon*':ti,ab)) AND (1-1-2000)/sd) NOT 'conference abstract'/it) AND ('pregnancy'/exp OR 'pregnant woman'/exp OR 'female infertility'/exp OR 'pregnancy disorder'/exp OR 'reproductive health'/exp OR 'female fertility'/exp OR pregnan*:ti,ab,kw OR gravidit*:ti,ab,kw OR gestation*:ti,ab,kw OR placentat*:ti,ab,kw OR prepregnan*:ti,ab,kw OR conception*:ti,ab,kw OR preconception*:ti,ab,kw OR (('fertility'/de OR 'infertility'/de OR fertil*:ti,ab,kw OR infertil*:ti,ab,kw) AND ('female'/exp OR woman:ti,ab,kw OR women:ti,ab,kw OR female*:ti,ab,kw))) |
19 |
|
#42 |
'pregnancy'/exp OR 'pregnant woman'/exp OR 'female infertility'/exp OR 'pregnancy disorder'/exp OR 'reproductive health'/exp OR 'female fertility'/exp OR pregnan*:ti,ab,kw OR gravidit*:ti,ab,kw OR gestation*:ti,ab,kw OR placentat*:ti,ab,kw OR prepregnan*:ti,ab,kw OR conception*:ti,ab,kw OR preconception*:ti,ab,kw OR (('fertility'/de OR 'infertility'/de OR fertil*:ti,ab,kw OR infertil*:ti,ab,kw) AND ('female'/exp OR woman:ti,ab,kw OR women:ti,ab,kw OR female*:ti,ab,kw)) |
1288988 |
|
#41 |
#26 AND ('clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR ('prospective study'/de NOT 'randomized controlled trial'/de) OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (case:ab,ti AND ((control NEAR/1 (study OR studies)):ab,ti)) OR (follow:ab,ti AND ((up NEAR/1 (study OR studies)):ab,ti)) OR ((observational NEAR/1 (study OR studies)):ab,ti) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti)) Ouderen, epidemiologisch |
132 |
|
#40 |
#26 AND ('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) Ouderen, RCT |
41 |
|
#39 |
#26 AND (('meta analysis'/de OR cochrane:ab OR embase:ab OR psychlit:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp)) Ouderen SR |
3 |
|
#38 |
#25 AND ('clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR ('prospective study'/de NOT 'randomized controlled trial'/de) OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (case:ab,ti AND ((control NEAR/1 (study OR studies)):ab,ti)) OR (follow:ab,ti AND ((up NEAR/1 (study OR studies)):ab,ti)) OR ((observational NEAR/1 (study OR studies)):ab,ti) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti)) Kinderen, epidemiologisch |
98 |
|
#37 |
#25 AND ('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) Kinderen, RCT |
46 |
|
#36 |
#25 AND (('meta analysis'/de OR cochrane:ab OR embase:ab OR psychlit:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp)) Kinderen, SR |
18 |
|
#35 |
#24 AND ('clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR ('prospective study'/de NOT 'randomized controlled trial'/de) OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (case:ab,ti AND ((control NEAR/1 (study OR studies)):ab,ti)) OR (follow:ab,ti AND ((up NEAR/1 (study OR studies)):ab,ti)) OR ((observational NEAR/1 (study OR studies)):ab,ti) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti)) Reflux epidemiologsch |
102 |
|
#34 |
#24 AND ('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) Reflux, RCT |
47 |
|
#33 |
#24 AND (('meta analysis'/de OR cochrane:ab OR embase:ab OR psychlit:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp)) Reflux, SR |
21 |
|
#32 |
#23 AND ('clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR ('prospective study'/de NOT 'randomized controlled trial'/de) OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (case:ab,ti AND ((control NEAR/1 (study OR studies)):ab,ti)) OR (follow:ab,ti AND ((up NEAR/1 (study OR studies)):ab,ti)) OR ((observational NEAR/1 (study OR studies)):ab,ti) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti)) Diabetes epidemiologisch |
149 |
|
#31 |
#23 AND ('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) Diabetes RCT |
119 |
|
#30 |
#23 AND (('meta analysis'/de OR cochrane:ab OR embase:ab OR psychlit:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp)) Diabetes SR |
43 |
|
#26 |
#22 AND ('aged'/exp OR 'geriatrics'/exp OR 'elderly care'/exp OR elder*:de,ab,ti OR eldest:de,ab,ti OR frail*:de,ab,ti OR geriatri*:de,ab,ti OR ((old NEXT/1 age*):de,ab,ti) OR ((oldest NEXT/1 old*):de,ab,ti) OR senior*:de,ab,ti OR senium:de,ab,ti OR ((very NEXT/1 old*):de,ab,ti) OR septuagenarian*:de,ab,ti OR octagenarian*:de,ab,ti OR octogenarian*:de,ab,ti OR nonagenarian*:de,ab,ti OR centarian*:de,ab,ti OR centenarian*:de,ab,ti OR supercentenarian*:de,ab,ti OR 'older people':de,ab,ti OR ((older NEXT/1 subject*):de,ab,ti) OR ((older NEXT/1 patient*):de,ab,ti) OR ((older NEXT/1 age*):de,ab,ti) OR ((older NEXT/1 adult*):de,ab,ti) OR 'older man':de,ab,ti OR 'older men':de,ab,ti OR 'older male*':de,ab,ti OR 'older woman':de,ab,ti OR 'older women':de,ab,ti OR 'older female*':de,ab,ti OR ((older NEXT/1 population*):de,ab,ti) OR ((older NEXT/1 person*):de,ab,ti)) |
234 |
|
#25 |
#22 AND (adolescen*:ab,ti OR 'adolescence'/exp OR 'adolescent coping orientation for problem experiences'/exp OR 'adolescent development'/exp OR 'adolescent disease'/exp OR 'adolescent health'/exp OR 'adolescent parent'/exp OR 'adolescent pregnancy'/exp OR 'adolescent smoking'/exp OR 'adolescent'/exp OR 'adolescent-family inventory of life events and changes'/exp OR babies:ab,ti OR baby:ab,ti OR 'birth weight'/exp OR boy:ab,ti OR boyhood:ab,ti OR boys:ab,ti OR 'brazelton neonatal behavioral assessment scale'/exp OR 'child abuse'/exp OR 'child advocacy'/exp OR 'child behavior checklist'/exp OR 'child behavior'/exp OR 'child care'/exp OR 'child death'/exp OR 'child health care'/exp OR 'child health'/exp OR 'child nutrition'/exp OR 'child parent relation'/exp OR 'child psychology'/exp OR 'child restraint system'/exp OR 'child safety'/exp OR 'child welfare'/exp OR child*:ab,ti OR 'child'/exp OR 'childhood disease'/exp OR 'childhood mortality'/exp OR 'childhood'/exp OR girl:ab,ti OR girlhood:ab,ti OR girls:ab,ti OR 'high risk infant'/exp OR infan*:ab,ti OR 'infant disease'/exp OR 'infant mortality'/exp OR 'infant nutrition'/exp OR 'infant welfare'/exp OR 'infanticide'/exp OR 'infantile diarrhea'/exp OR 'infantile hypotonia'/exp OR 'juvenile delinquency'/exp OR neonat*:ab,ti OR 'neonatal weight loss'/exp OR 'newborn disease'/exp OR 'newborn morbidity'/exp OR 'newborn period'/exp OR newborn*:ab,ti OR 'newborn'/exp OR nicu:ab,ti OR 'only child'/exp OR paediatr*:ab,ti OR pediatri*:de,ab,ti OR 'pediatric advanced life support'/exp OR 'pediatric anesthesia'/exp OR 'pediatric cardiology'/exp OR 'pediatric hospital'/exp OR 'pediatric intensive care nursing'/exp OR 'pediatric nurse practitioner'/exp OR 'pediatric nursing'/exp OR 'pediatric rehabilitation'/exp OR 'pediatric surgery'/exp OR 'newborn hypoxia'/exp OR 'pediatric ward'/exp OR 'pediatrics'/exp OR perinat*:ab,ti OR 'perinatal development'/exp OR 'perinatal period'/exp OR 'persistent hyperinsulinemic hypoglycemia of infancy'/exp OR picu:ab,ti OR postnat*:ab,ti OR 'postnatal care'/exp OR 'postnatal development'/exp OR 'postnatal growth'/exp OR postneonat*:ab,ti OR preschool*:ab,ti OR puberty:ab,ti OR 'runaway behavior'/exp OR 'school child':ab,ti OR schoolchild*:ab,ti OR 'severe myoclonic epilepsy in infancy'/exp OR suckling*:ab,ti OR teen:ab,ti OR teenager*:ab,ti OR teens:ab,ti OR toddler*:ab,ti OR 'transient hypogammaglobulinemia of infancy'/exp OR youth:ab,ti OR youths:ab,ti) |
205 |
|
#24 |
#22 AND ('gastroesophageal reflux'/exp OR 'duodenogastric reflux'/exp OR reflux:ti,ab) |
252 |
|
#23 |
#22 AND ('non insulin dependent diabetes mellitus'/exp OR (((diabetes OR diabetic*) NEAR/3 ('non insulin depend*' OR 'noninsulin depend*' OR noninsulindepend* OR 'non insulindepend*' OR 'maturity onset*' OR 'adult onset*' OR 'slow onset*')):ti,ab) OR dm2:ti,ab OR niddm:ti,ab OR 'dm 2':ti,ab OR t2d*:ti,ab OR 'dm type 2':ti,ab OR 'type 2 diabet*':ti,ab OR 'type two diabet*':ti,ab OR 'type ii diabet*':ti,ab OR 'dm type ii':ti,ab) |
424 |
|
#22 |
((('gastric bypass surgery' OR 'gastric bypass*':ti,ab OR 'roux en y':ti,ab OR 'gastroileal bypass*':ti,ab OR 'gastrojejunostom*':ti,ab OR 'jejunoileal bypass*':ti,ab OR 'jejuno ileal bypass*':ti,ab OR 'ileojejunal bypass*':ti,ab OR 'intestinal bypass*':ti,ab) AND ('gastric balloon'/exp OR 'gastric sleev*':ti,ab OR 'sleeve gastrectom*':ti,ab OR 'gastric balloon*':ti,ab)) AND (1-1-2000)/sd) NOT 'conference abstract'/it |
1863 |
|
#16 |
('gastric bypass surgery' OR 'gastric bypass*':ti,ab OR 'roux en y':ti,ab OR 'gastroileal bypass*':ti,ab OR 'gastrojejunostom*':ti,ab OR 'jejunoileal bypass*':ti,ab OR 'jejuno ileal bypass*':ti,ab OR 'ileojejunal bypass*':ti,ab OR 'intestinal bypass*':ti,ab) AND ('gastric balloon'/exp OR 'gastric sleev*':ti,ab OR 'sleeve gastrectom*':ti,ab OR 'gastric balloon*':ti,ab) |
4785 |
|
#15 |
'gastric balloon'/exp OR 'gastric sleev*':ti,ab OR 'sleeve gastrectom*':ti,ab OR 'gastric balloon*':ti,ab |
10979 |
|
#10 |
'gastric bypass surgery' OR 'gastric bypass*':ti,ab OR 'roux en y':ti,ab OR 'gastroileal bypass*':ti,ab OR 'gastrojejunostom*':ti,ab OR 'jejunoileal bypass*':ti,ab OR 'jejuno ileal bypass*':ti,ab OR 'ileojejunal bypass*':ti,ab OR 'intestinal bypass*':ti,ab |
29409 |
Wiley/Cochrane Library
|
Search |
Query |
Items found |
|
#1 |
("gastric balloon*" or "gastric sleev*" or "sleeve gastrectom*" or "stomach stapl*" or "gastric balloon"):ti,ab,kw AND ("gastric bypass*" or "roux en y" or "roux en ys" or "gastroileal bypass*" or "gastrojejunostom*" or "jejunoileal bypass*" or "jejuno ileal bypass*" or "intestinal bypass*" or "omega loop"):ti,ab,kw |
298 |
|
#2 |
#1 and (pregnan* or gravidit* or gestation* or placentat* or prepregnan* or conception* or preconception* or ((fertil* or infertil*) and (woman or women or female*))):ti,ab,kw |
0 |
|
#3 |
#1 and (elder* or eldest or frail* or geriatri* or "old age*" or "oldest old*" or senior* or senium or "very old*" or septuagenarian* or octagenarian* or octogenarian* or nonagenarian* or centarian* or centenarian* or supercentenarian* or "older people" or "older subject*" or "older patient*" or "older age*" or "older adult*" or "older man" or "older men" or "older male" or "older woman" or "older women" or "older female" or "older population*" or "older person*"):ti,ab,kw |
5 |
|
#4 |
#1 and (infan* or child* or adolescen* or pediatric* or paediatric* or pube* or juvenil* or school* or newborn* or "new-born*" or "neo-nat*" or neonat* or premature* or postmature* or "pre-mature*" or "post-mature*" or preterm* or "pre-term*" or baby or babies or toddler* or youngster* or preschool* or kindergart* or kid or kids or playgroup* or "play-group*" or playschool* or prepube* or preadolescen* or "junior high*" or highschool* or "senior high" or "young people*" or minors):ti,ab,kw |
37 |
|
#5 |
#1 and (diabetes or "diabetic*" or "insulin*" or "metformin*" or "rosiglitazon*" or "troglitazon*" or "pioglitazon*" or "hypoglycem*" or "hypoglycaem*"):ti,ab,kw |
132 |
|
#6 |
#1 and reflux* |
35 |
|
#7 |
#1 not (#2 or #3 or #4 or #5 or #6) |
122 |
