Tijdsbestek tussen twee cataractoperaties
Uitgangsvraag
Hoeveel tijd dient er minimaal tussen de cataractoperatie van het eerste en het tweede oog te zitten?
Aanbeveling
Simultane bilaterale cataractchirurgie (ISBCS) kan worden overwogen bij hiervoor geschikte patiënten in afwezigheid van complicatie verhogende oculaire comorbiditeit.
Indien bilaterale simultane cataractoperaties gepland worden, dienen deze beschouwd en behandeld te worden als twee afzonderlijke procedures, conform de principal practice guideline for bilateral surgery.
Bij het optreden van een complicatie bij de eerste operatie moet heroverwogen worden of het tweede oog aansluitend wordt geopereerd.
Overwegingen
De onderstaande overwegingen gelden alleen voor patiënten met cataract in beide ogen bij wie het doel is beide ogen te opereren. Voorts betreft het alleen ogen zonder verhoogd operatierisico en zonder oogheelkundige comorbiditeit. In het geval van cataractoperatie aan beide ogen op dezelfde dag worden de beide operaties beschouwd als twee afzonderlijke ingrepen. Hierbij moeten diverse logistieke aanpassingen worden verricht en specifieke procedures worden gevolgd, zoals beschreven in ‘general principles for excellence in immediate sequential bilateral cataract surgery 2009’ (bron: eye foundation of canada - principles of ISBCS).
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Voor de cruciale uitkomstmaat ‘verschil in afwijking van de doelrefractie’ kan er met redelijke zekerheid geconcludeerd worden dat er geen verschil is tussen patiënten die tegelijk aan beide ogen worden geopereerd en patiënten die op twee verschillende dagen geopereerd (redelijke bewijskracht). De cruciale uitkomstmaat unilaterale endoftalmitis komt zo weinig voor dat er met een redelijke zekerheid gesteld kan worden dat er geen verschil is in risico tussen ISBCS en DSBCS. In de studie van Arshinoff (2011) wordt geen verschil in optreden van endoftalmitis gevonden als alleen cataractextracties met intracamerale antibiotica profylaxe worden vergeleken. Wanneer alle ISBCS operaties worden vergeleken met DSBCS, onafhankelijk van antibioticagebruik, worden meer endoftalmitiden gerapporteerd in de ISBCS groep. Bij de DSBCS-groep is intracameraal antibiotica echter bij alle operaties toegepast. Om het antibioticagebruik niet te laten interveniëren met de uitkomstmaat endoftalmitis hebben we tevens een analyse gedaan binnen de ISBCS en DSBCS-groepen naar patiënten bij wie alleen intracameraal antibiotica zijn gebruikt. Tussen die twee groepen bestond geen verschil in het optreden van endoftalmitis. Adverse events lijken even vaak voor te komen bij ISBCS als bij DSCBS, de bewijskracht hiervoor is laag. Voor macula oedeem is er een hoger risico in de DSBCS groep; door de inclusie van meer ogen met comorbiditeit in de DSCBS groep. Daarom is hiervoor geen GRADE-beoordeling gedaan. Voor de serious adverse events en achterste kapselruptuur lijkt er geen verschil te zijn tussen ISBCS en DSBCS. De bewijskracht is hiervoor echter zeer laag: er is te weinig zekerheid over de resultaten. Dit komt met name doordat deze complicatie weinig voorkomt en doordat er een grote spreiding is rondom de gevonden waarde. Daarom wordt geconcludeerd dat het onduidelijk is of er een verschil is tussen de behandelmethoden voor serious adverse events en achterste kapselruptuur. Er werd geen verschil in patiënt-gerapporteerd functioneren gevonden tussen ISBCS en DSBCS op het moment dat beide ogen zijn geopereerd. Echter, in de periode tussen de twee operaties ervaren mensen die DSBCS ondergaan meer klachten van hun functioneren. Het bewijs dat is gevonden heeft alleen betrekking op patiënten zonder oogheelkundige comorbiditeit. Bij patiënten met oogheelkundige comorbiditeit wordt in de literatuur standaard gekozen voor DSBCS.
Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)
Bij het merendeel van de patiënten met cataract is er een indicatie voor een cataractoperatie aan beide ogen. Hoewel een cataractoperatie aan één oog al leidt tot herstel van functionele visus, leidt de operatie van het tweede oog (met cataract) tot een verdere verbetering in kwaliteit van leven en is het ook kosteneffectief (Frampton, 2014; Shekhawat, 2017). Voordelen voor patiënten indien beide ogen op dezelfde dag worden geopereerd zijn een verwacht verminderd aantal bezoeken aan het ziekenhuis, een makkelijker druppelschema, een mogelijk korter hersteltraject, een snellere definitieve aanpassing van refractie na de operaties en (vooral in geval van anisometropie) minder functionele beperking in de periode tussen de twee operaties. Nadelen voor de patiënt kunnen zijn een langere operatietijd, geen mogelijkheid voor subtenonale anaesthesie, verlies van gevoel van ‘veiligheid/risicoreductie’ door de operaties van beide ogen niet te scheiden. Patiënten met een hogere refractieafwijking zijn mogelijk meer gebaat bij een kortere periode tussen de twee opeenvolgende operaties vanwege de functionele beperkingen bij anisometropie en problemen met refractiecorrectie in de tussenliggende periode.
Ethische overwegingen
Vanuit technisch perspectief lijkt er weinig in de weg te staan van een bilaterale cataractoperatie in één sessie, de vraag is dan of er op andere gronden hiertegen bedenkingen zijn. We moeten ervan uitgaan dat de beslissing om überhaupt tot lensextractie van beide ogen over te gaan al goed doordacht door de maximaal geïnformeerde patiënt genomen werd zonder dat bij die beslissing andere factoren een rol speelden dan het belang van de patiënt. Het was in de Nederlandse oogheelkunde tot slechts een tiental jaren geleden een algemeen geldend principe dat er nooit aan beide ogen tegelijkertijd intracoluair of direct aansluitend intra-oculair geopereerd werd, tenzij daar een dwingende reden toe bestond. Dit was een vorm van risicobeperking die door de meeste oogartsen als zeer fundamenteel gevoeld werd. Ook aan de patiënten werd uitgelegd dat er altijd maar één oog geopereerd werd en pas het tweede wanneer duidelijk geworden was dat er geen complicaties waren. In het algemeen werd een wachtperiode van minimaal twee weken aangehouden. Deze periode werd zelfs een prestatie-indicator toen er door verzekeraars gesignaleerd werd dat men er in een aantal praktijken toe neigde de wachtperiode te verkorten of twee ogen van een patiënt op één dag wilde opereren. Ook in andere landen werd een dergelijke tendens gezien. Bij deze herziening van de richtlijn cataract werd een literatuuronderzoek verricht naar onmiddellijk consecutieve bilaterale cataractchirurgie met als resultaat dat in de aanbevelingen opgenomen werd dat chirurgie aan twee ogen in één sessie overwogen kan worden.
Dat zal echter niet betekenen dat heel oogheelkundig Nederland in het vervolg zal overstappen op deze procedure en dat alle patiënten het zullen willen ondergaan. Daarvoor zit de reserve tegen intra-oculaire ingrepen aan beide ogen in één sessie waarschijnlijk te diep en zullen er ongetwijfeld oogartsen zijn die huiverig blijven voor complicaties in geval van bilaterale consecutieve chirurgie. Het is dan ook raadzaam om enige omzichtigheid te betrachten bij het inzetten van deze procedure. Een problematisch verlopen bilaterale cataractoperatie in één sessie zou de operateur wel eens zwaarder aangerekend kunnen worden dan in geval van ingrepen met tussentijds een wachtperiode. Een ingrijpende verschuiving van inzicht over emotioneel geladen kwesties kunnen soms onverwachte en ongewenste gevolgen hebben, als bijvoorbeeld psychische of juridische.
Oogartsen en andere professioneel betrokkenen doen er verstandig aan zich kritisch op te stellen in hun handelen en het welbevinden en de autonomie van de patiënt te respecteren en het uitgangspunt van ‘primum non nocere’, ook in niet-lichamelijke betekenis, niet uit het oog te verliezen.
Kosten (middelenbeslag)
Van belang is dat de mogelijkheid om beide ogen direct na elkaar te opereren op één dag in beginsel alleen geldt voor ogen zonder bijkomende risicofactoren en voor patiënten die voor beide ogen een indicatie hebben om aan cataract geopereerd te worden. Het verschil in kosten tussen DSBCS en ISBCS zal daarom alleen gelden voor deze groep patiënten. In Nederland wordt 55% (mediaan) van de patiënten binnen 12 maanden aan beide ogen aan staar geopereerd. Naar verwachting komt 80% van de patiënten die momenteel binnen 12 maanden aan beide ogen worden geopereerd in aanmerking voor ISBCS. In 2023 is een studie gepubliceerd die de doelmatigheid van bilateraal opereren van cataract op dezelfde dag versus een periode tussen de operaties vergelijkt in de Nederlandse situatie (Spekreijse, 2023). Dit onderzoek beschrijft dat het opereren van beide ogen op dezelfde dag kosteneffectief is. Er was enerzijds sprake van een betere kwaliteit van leven (uitgedrukt in QALY’s) bij de groep patiënten die aan beide ogen op dezelfde dag was geopereerd. Anderzijds was er sprake van een kostenbesparing. In Nederland zijn de besparingen mogelijk minder hoog vergeleken met andere landen waar gekeken is naar de kosteneffectiviteit van bilateraal opereren, omdat patiënten in Nederland minder ver hoeven te reizen voor de operaties en onderzoeken. Uit het Nederlands onderzoek blijkt met name een besparing in het aantal ziekenhuisbezoeken voor patiënten die aan beide ogen op dezelfde dag worden geopereerd. In de totale operatietijd en daarmee bezetting van de operatiekamer werd geen verschil gevonden. Gezien het feit dat ook bij het opereren van twee ogen op één dag de ingreep als twee aparte ingrepen worden beschouwd wat betreft middelen is er op dit vlak alleen een kostenbesparing buiten het ziekenhuis in thuiszorgkosten en apotheekkosten na de operatie. De besparing op thuiszorg, doordat ogen tegelijkertijd gedruppeld worden, geldt alleen voor patiënten die in aanmerking komen voor thuiszorg. De patiënten die in aanmerking komen voor ISBCS zijn mogelijk niet dezelfde als voor wie thuiszorg om te druppelen nodig is, waardoor besparing op thuiszorg in praktijk ook beperkt is, zie ook: https://www.zorginstituutnederland.nl/passende-zorg/publicaties/publicatie/2023/12/18/tweezijdige-staaroperatie. De uitvoering van het opereren van twee ogen op één dag heeft implicaties voor het voorraadbeheer van de operatieafdeling en is een logistieke uitdaging om aan de gestelde vereisten van de ‘ISBCS general principles for excellence (2009)’ te voldoen. Kosten die hier mogelijk verband mee houden zijn niet meegenomen in de Nederlandse kosteneffectiviteitsstudie. De mogelijkheid, bekostiging en inrichting van het operatieve proces voor elk oog afzonderlijk zal moeten blijven bestaan. Patiënten beide mogelijkheden kunnen aanbieden speelt een belangrijke rol in het "samen beslissen" over de beste zorg op maat voor de patiënt. Het effect op kosten speelt hierbij een ondergeschikte rol.
Aanvaardbaarheid, haalbaarheid en implementatie
Onderzoek naar de haalbaarheid van bilateraal opereren van cataract op dezelfde dag loopt op dit moment in Nederland. Om te voldoen aan de principal practice guideline for bilateral surgery (www.ISBCS.org) zijn diverse logistieke aanpassingen nodig. De operatie van het tweede oog wordt als een volledig nieuwe operatie beschouwd. Extra aanpassingen omvatten onder meer het gebruik van een nieuwe instrumentenset, gesteriliseerd in een aparte sterilisatiecyclus dan die van de set die gebruikt werd tijdens de ingreep aan het eerste oog.
-
- Niet-medicamenteuze producten (zoals disposable instrumenten, visco-elasticum en BSS) die tijdens de tweede operatie gebruikt worden, dienen uit andere productie-batches afkomstig te zijn dan bij de operatie van het eerste oog, vanwege risico op TASS aangetoond bij deze producten uit dezelfde batch.
- Voor intraoculaire medicatie die in de ziekenhuisapotheek conform GMP-z (zie https://nvza.nl/voor-professionals/gmp/) worden klaargemaakt, zijn gescheiden batches geen vereiste.
- Voor alle overige intra-oculaire medicatie gebruikt op OK (zoals b.v. aprokam), dienen verschillende batches gebruikt te worden en genoteerd in het dossier. De werkwijze is vastgelegd in een lokaal protocol waarbij 1 ampul bedoeld is voor single use en dus NIET voor meerdere patiënten gebruikt mag worden (NB. dit geldt ook voor sequentiële bilaterale cataractoperaties). Zie hiervoor de nieuwe SRI richtlijn “Voor Toediening Gereed Maken (VTGM) buiten de apotheek en toediening medicatie.
- Voor extra-oculaire medicatie verwijzen we naar de SRI Richtlijn “Voor Toediening Gereed Maken (VTGM) buiten de apotheek en toediening medicatie”.
Deze logistieke aanpassingen dienen lokaal geïmplementeerd te worden.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Gezien het geringe tot geen verschil in cruciale uitkomstmaten bij patiënten met cataract aan twee ogen bij wie de cataractextractie aan beide ogen ofwel gelijktijdig (ISBCS) ofwel met een periode van minimaal twee weken tussentijd (DSBCS) geopereerd worden, kunnen beide interventies worden overwogen. Het gaat hierbij om ogen zonder oculaire comorbiditeit bij wie geen verhoogd complicatierisico is en patiënten die onder topicale dan wel algehele anaesthesie geopereerd kunnen worden. Van belang is de operaties in geval van ISCBS te beschouwen als aparte operaties en navenant de steriliteitseisen in acht te nemen conform de eye foundation of canada - principles of ISBCS.
Onderbouwing
Achtergrond
Op dit moment wordt een wachttijd van minimaal twee weken voorgeschreven tussen de opeenvolgende cataractextracties bij binoculair cataract, met een controle in de tussenliggende periode. Argumenten om minimaal twee weken te wachten met het tweede oog zijn het risico op visusbedreigende postoperatieve complicaties en dan met name het risico op endoftalmitis en het optreden van een ‘refractive surprise’. In deze gevallen is het wenselijk de operatie van het tweede oog uit dan wel bij te stellen. Met de huidige technieken en materialen lijkt de cataractprocedure zodanig veilig en precies dat overwogen kan worden twee ogen tegelijkertijd te opereren. In Nederland worden meer dan 180.000 cataractoperaties per jaar verricht. Het is aannemelijk dat door twee ogen tegelijkertijd te opereren het totale behandelings- en hersteltraject voor de patiënt verkort wordt, met sneller eindresultaat en functieherstel tot gevolg. Ook zou om die reden gelijktijdig opereren uit kosteneffectiviteitsoverwegingen gunstiger kunnen zijn en daarnaast gezondheidswinst kunnen opleveren voor de patiënt.
Conclusies / Summary of Findings
In de meeste studies worden patiënten met oculaire comorbiditeit en daarmee mogelijk verhoogd operatierisico uitgesloten voor simultane chirurgie. De onderstaande conclusies hebben daarom betrekking op patiënten met bilateraal cataract bij wie een indicatie is voor operatie van beide ogen zonder oculaire comorbiditeit. In geval van simultane chirurgie worden de operaties beschouwd als twee afzonderlijke ingrepen.
Afwijkingen van de doelrefractie
|
Redelijk GRADE |
Patiënten zonder oculaire comorbiditeit die een indicatie hebben voor bilaterale cataractchirurgie en ISBCS ondergaan hebben waarschijnlijk een vergelijkbare restrefractie (-0,02D) met die van patiënten die DSBCS ondergaan.
Bronnen: (Herrinton, 2017; Lundström, 2006 en Sarikkola, 2011) |
Endoftalmitis
|
Redelijk GRADE |
Er werd geen enkel geval van bilaterale endoftalmitis gerapporteerd in de 108.854 gevallen waarbij ISBCS werd toegepast (Arshinoff, 2011; Herrinton, 2017; Lundström, 2006; Sarikkola, 2011 en (Serrano-Aguilar (2012).
Er is waarschijnlijk geen verschil in absolute risico’s op unilaterale endoftalmitis tussen ISBCS (6/82.253 ogen = 0,0073%) en DSBCS (3/68.318 = 0,004%) bij patiënten die een indicatie hebben voor bilaterale cataract chirurgie, wanneer intracameraal antibiotica wordt toegediend.
De number needed to harm (NNH) is 30.303: er kan 1 geval van unilaterale endoftalmitis worden voorkomen bij het behandelen van 30.303 mensen wanneer wordt gekozen voor DSBCS in plaats van ISBCS.
Bronnen: (Ashinoff, 2011; Herrinton, 2017) |
Serious adverse events
|
Zeer laag GRADE |
Het is niet duidelijk of overige serious adverse events vaker voorkomen bij ISBCS of DSBCS.
Bronnen: (Herrinton, 2017; Sarikkola, 2011; Serrano-Aguilar, 2012) |
Adverse events
|
Laag GRADE |
Adverse events lijken even vaak voor te komen bij ISBCS als bij DSBCS.
Bronnen: (Kessel, 2015; Sarikkola, 2011; Serrano-Aguilar, 2012) |
Achterste kapselruptuur
|
Zeer laag GRADE |
Het is onduidelijk of er een verschil is in achterste kapselruptuur tussen ISBCS en DSBCS.
Bronnen: (Herrinton, 2017; Sarikkola, 2011; Serrano-Aguilar, 2012) |
Macula oedeem
|
- GRADE |
Het is onduidelijk of er een verschil is in macula oedeem tussen ISBCS en DSBCS.
Bronnen: (Herrinton, 2017) |
Patiënt-gerapporteerd functioneren na operatie van twee ogen
|
Laag GRADE |
Nadat beide ogen zijn geopereerd lijkt er geen verschil te zijn in patiënt-gerapporteerd functioneren tussen ISBCS en DSBCS.
Bronnen: (Kessel, 2015; Sarikkola, 2011; Serrano-Aguilar, 2012 en Lundström, 2006) |
Patiënt-gerapporteerd functioneren in de tussentijd
|
Laag GRADE |
In de periode tussen de twee operaties lijken patiënten met DSBCS hun functioneren minder goed te scoren dan wanneer beide ogen tegelijk zijn geopereerd (ISBCS).
Bronnen: (Serrano-Aguilar, 2012; Lundström, 2006) |
Samenvatting literatuur
Beschrijving studies
Herrinton (2017) beschrijft een retrospectieve observationele studie waarin de vergelijking wordt gemaakt tussen 1) ISBCS (n=3.561) en 2) DSBCS (n=13.711), uitgevoerd in de Verenigde Staten. Data van patiënten werden geïncludeerd indien 1) er informatie beschikbaar was over de postoperatieve refractie en 2) het tweede oog (in het geval van DSBCS) binnen één jaar werd geopereerd. Patiënten die door een specialistische oogarts (glaucoom, oogheelkundig plastisch chirurg of retinaspecialist werden geopereerd werden niet geïncludeerd. Ook werden eerdere gevallen van endoftalmitis niet meegenomen. De groepen waren verschillend in 1) het jaar dat het eerste oog werd geopereerd; 2) etniciteit; 3) multi- of monofocale implantlens en 4) pre-operatieve comorbiditeit zoals glaucoom, diabetische retinopathie en maculadegeneratie. Beide groepen omvatten operaties met intracamerale antibiotica (na 2013) of topicale antibiotica (vóór 2013). De postoperatieve refractie werd berekend als het sferische equivalent (sferische sterkte + (cilindersterkte/2)) in dioptrie en zo kort mogelijk, maar minstens 3 weken tot 1 jaar na de operatie. Complicaties zoals achterste kapselruptuur/vitrectomie, endoftalmitis en macula oedeem werden gerapporteerd. Voor de postoperatieve restrefractie werd er gecorrigeerd voor potentiële confounding van patiëntvariabelen, inclusief de tijd tot de postoperatieve refractie, en gekozen intra-oculaire lensformule die door de jaren heen veranderde. De type intra-oculaire lensformules zijn niet gerapporteerd.
Ashinoff (2011) beschrijft een multicenter cohortstudie waarin data over de incidentie van endoftalmitis zijn verzameld door 1) een survey onder leden van de ‘International Society of Bilateral Cataract Surgeons’ en 2) literatuuronderzoek. Data over de incidentie van endoftalmitis werd gerapporteerd voor 1) ISBCS (n=95.606) en 2) DSBCS (n=29.582). De incidentie van endoftalmitis bij gebruik van 1) geen intracamerale antibiotische profylaxe (geen intra-oculaire antibiotica of topicale antibiotica) of 2) intracamerale antibiotische profylaxe werden gerapporteerd voor ISCBS. Voor DSBCS werden alleen gevallen gerapporteerd waarbij intracamerale antibiotische profylaxe werd gegeven.
Kessel (2015) is een systematische review, inclusief GRADE-beoordeling, waarin de effectiviteit van ISBCS werd onderzocht versus DSBCS op patiënt-gerapporteerd functioneren, visus en restrefractie en adverse events bij patiënten die geen oculaire comorbiditeit hadden en geen sterk van het gemiddelde afwijkende aslengte (Lundström, 2006: < 21 mm of > 27 mm; Sarikkola, 2011: > 26 mm). Er werden alleen RCT’s geïncludeerd: Lundström (2006), Sarikkola (2011) en Serrano-Aguilar (2012). Vanwege het ontbreken van data (bijvoorbeeld SD’s) werden de data van Lundström (2006) niet voor alle uitkomstmaten meegenomen in de berekening van het gepoolde effect. Lundström (2006) includeerde 50 en 46 patiënten, Sarikkola (2011) 493 en 506 patiënten en Serrano-aguilar (2012) 834 en 780 patiënten respectievelijk in de ISBCS en de DSBCS groep. Patiënt- gerapporteerd functioneren werd in de studie van Lundström (2006) gemeten aan de hand van de Catquest questionnaire die vragen bevat over de moeilijkheid van het uitvoeren van dagelijkse activiteiten en tevredenheid met het zicht en een totaalscore geeft in de range van zeven tot 34. Er werden door deze studie geen SD’s gerapporteerd. Sarikkola (2011) onderzocht patiënt-gerapporteerd functioneren aan de hand van de visual function questionnaire-7 (VF-7) en Serrano-Aguilar (2012) aan de hand van de visual function questionnaire-14 (VF-14) (score tussen 0 en 100) waarin items zoals bijvoorbeeld ‘Hoeveel problemen ondervind je bij het lezen van de krant?’ gescoord werd op een vijf-puntsschaal: 1; geen enkele problemen - 5; hiermee gestopt in verband met zicht. Visus (gecorrigeerd) werd beschreven en serious adverse events (SAE) en adverse events (AE) werden gerapporteerd. Ontbrekende data ten aanzien van de restrefractie werden uit de afzonderlijke studies gehaald. Sarikkola (2011) gebruikte de SRK/T formule voor het berekenen van de lenssterkte. Lundström (2006) geeft geen informatie over de gebruikte lensformule.
Resultaten
1. Afwijkingen van doelrefractie
De uitkomstmaat afwijkingen van doelrefractie is door drie studies onderzocht (Herrinton, 2017; Lundström, 2006 en Sarikkola, 2011).
Herrinton (2017) vond in een subgroep (ISBCS, n=3.220; DSBCS; n=12.630) een postoperatieve refractieve afwijking (sferische equivalent) van -0,36D in de ISBCS groep en -0,39D in de DSBCS groep. Lundström (2006) rapporteerde een rest sferische equivalent van 0,53D in de ISBCS groep en 0,57D in de DSBCS groep (p=0,676) vier maanden na de operatie. Sarikkola (2011) vond een resterende sferische equivalent van 0,42±0,39D in de ISBCS groep en 0,44±0,39D in de DSBCS groep (p=0,80) en een gemiddeld verschil van -0,02 (95%BI -0,05 tot 0,01).
2. Complicaties
De uitkomstmaat complicaties wordt beschreven voor endoftalmitis, andere ernstige complicaties (SAEs), alle mogelijke ongewenste voorvallen (AEs) en nog apart voor de AEs achterste kapselruptuur en macula oedeem.
a. Endoftalmitis
Er werd geen enkel geval van bilaterale endoftalmitis gerapporteerd in de 82.253 gevallen waarbij ISBCS werd toegepast (Arshinoff, 2011; Herrinton, 2017; Lundström, 2006; Sarikkola, 2011 en Serrano-Aguilar, 2012). Het verschil in risico op unilaterale endoftalmitis tussen ISBCS en DSBCS is in twee studies onderzocht (Arshinoff, 2011; Herrinton, 2017). Gezien de lage incidentie van endoftalmitis wordt het absolute risicoverschil gerapporteerd in plaats van de risk ratio. In de groep patiënten waarbij topicale of intracamerale antibiotica werd gegeven was de incidentie van unilaterale endoftalmitis in de ISBCS groep 0,0095% (1/10.494) ogen en in de DSBCS groep 0,0052% (2/38.736) ogen (Herrinton, 2017). In de groep waarbij alleen intracamerale antibiotica werd toegepast was de incidentie van unilaterale endoftalmitis in de ISBCS groep 0,0070 (5/71.759 ogen) en in de DSBCS groep 0,0034% (1/29.582 ogen). Het gepoolde effect laat zien dat in de ISBCS groep de incidentie van endoftalmitis 0,0073% (6/82.253) ogen was en in de DSBCS groep 0,0044% (3/68.318 ogen) (figuur 1). Dit leidde tot een risicoverschil van 0 (95% BI 0 tot 0, p=0,12) met een random effect model en een lage heterogeniteit (I2 0%), hetgeen inhoudt dat er geen verschil is tussen de twee interventiegroepen. De number needed to harm (NNH) is 30.303: er kan 1 geval van unilaterale endoftalmitis worden voorkomen bij het behandelen van 30.303 mensen wanneer wordt gekozen voor DSBCS in plaats van ISBCS.
Figuur 1 Uitkomstmaat endoftalmitis
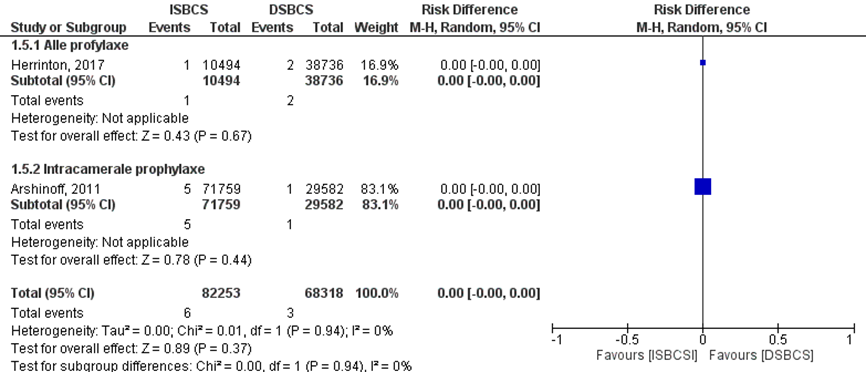
De incidentie van unilaterale endoftalmitis was 0,0073% (6/82.253 ogen) in de ISBCS en 0,0044% (3/68.318 ogen) in de DSBCS groep. Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval; ISBCS: immediate sequential bilateral cataract surgery; DSBCS: delayed sequential bilateral cataract surgery. * de DSBCS gevallen in de studie van Arshinoff (2011) zijn allemaal met intracamerale profylaxe. In de studie van Herrinton (2017) zijn de intracamerale en topicale profylaxe samen gerapporteerd. Totalen zijn # ogen
b. SAE (algemeen)
De uitkomstmaat SAE, waaronder onder andere cornea-oedeem, macula oedeem, wondlekkage (gedurende de eerste maand), irisprolaps en achterste kapselruptuur, is in drie studies onderzocht (Herrinton, 2017; Sarikkola, 2011 en Serrano-Aguilar, 2012). Het gepoolde effect laat zien dat in de ISBCS groep SAEs in 0,017% (68/6.574) van de patiënten voorkwamen en in de DSBCS groep 0,0043% (182/20.654) van de patiënten (figuur 2). Dit leidde tot een risk ratio van 1,19 (95% BI 0,76 tot 1,85, p=0,45) met een random effect model en een lage heterogeniteit (I2 22%). Hetgeen inhoudt dat er geen verschil is tussen de twee interventiegroepen. TASS werd in geen van de studies specifiek gerapporteerd.
Figuur 2 Uitkomstmaat SAE
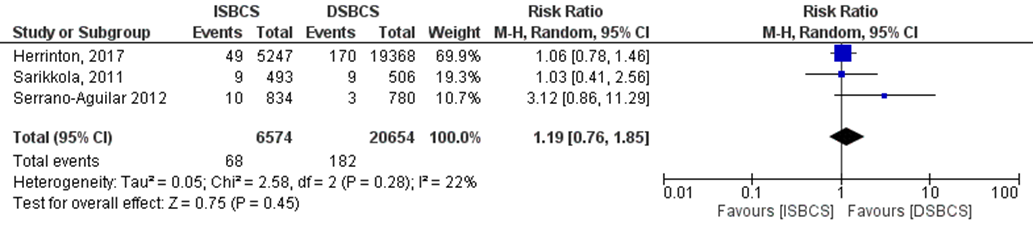
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval; ISBCS: immediate sequential bilateral cataract surgery; DSBCS: delayed sequential bilateral cataract surgery. Totalen zijn # patiënten
Herrinton (2017) rapporteert alleen gevallen van achterste kapselruptuur en/of een vitrectomie voor de beide interventie groepen apart. Deze studie vermeldde verder wel dat in 25 gevallen (0,7%) patiënten van ISBCS naar DSBCS werden veranderd aangezien de eerste operatie niet zonder complicaties verliep: waaronder achterste kapselruptuur, cornea-oedeem, intra-operatieve bloeding maar ook door apparatuur problemen.
c. AE (algemeen)
De uitkomstmaat AE, waaronder iedere complicatie is meegenomen, ook droge ogen, is in twee studies onderzocht (Sarikkola, 2011 en Serrano-Aguilar, 2012). Het gepoolde effect laat zien dat in de ISBCS groep AEs in 10,9% (145/1.327) van de patiënten voorkwamen en in de DSBCS groep 14,2% (183/1.286) van de patiënten (figuur 3). Dit leidde tot een risk ratio van 0,76 (95% BI 0,55 tot 1,07, p=0,12) met een random effect model en een gemiddelde heterogeniteit (I2 57%). Hetgeen inhoudt dat er geen verschil is tussen de twee interventiegroepen.
Figuur 3 Uitkomstmaat AE
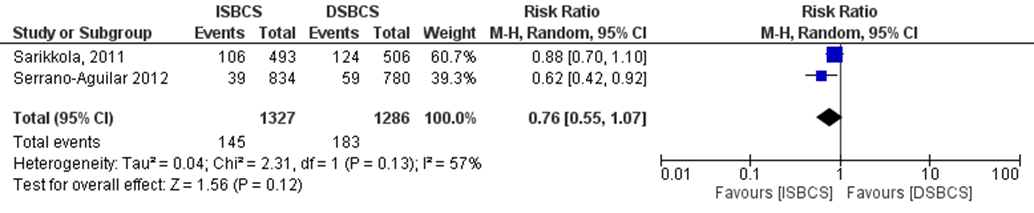
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval; ISBCS: immediate sequential bilateral cataract surgery; DSBCS: delayed sequential bilateral cataract surgery. *Totalen zijn # patiënten
d. Achterste kapselruptuur
De uitkomstmaat achterste kapselruptuur is in drie studies onderzocht (Herrinton, 2017; Sarikkola, 2011 en Serrano-Aguilar, 2012). Het gepoolde effect laat zien dat in de ISBCS groep achterste kapselruptuur in 0,73% (48/6.574) van de patiënten voorkwam en in de DSBCS groep in 0,66% (136/20.654) van de patiënten (figuur 4). Dit leidde tot een risk ratio van 1,20 (95% BI 0,86 tot 1,66, p=0,28) met een random effect model en een lage heterogeniteit (I2 0%). Hetgeen inhoudt dat er geen verschil is tussen de twee interventiegroepen.
Figuur 4 Uitkomstmaat posterior kapselruptuur
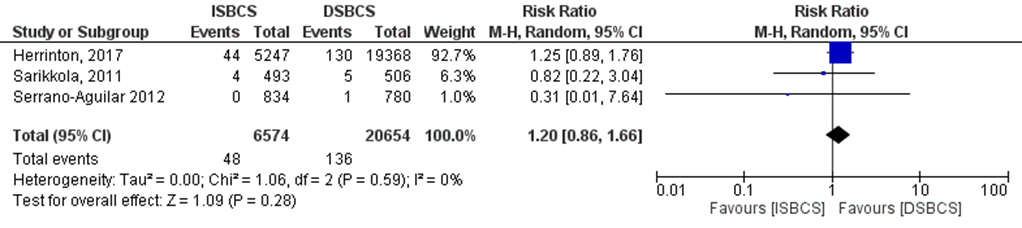
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval; ISBCS: immediate sequential bilateral cataract surgery; DSBCS: delayed sequential bilateral cataract surgery. *Totalen zijn # patiënten
e. Macula oedeem
De uitkomstmaat macula oedeem is in drie studies onderzocht (Herrinton, 2017; Sarikkola, 2011 en Serrano-Aguilar, 2012). Een belangrijk punt hierbij is dat de pre-operatieve oculaire comorbiditeit (waaronder diabetische retinopathie en maculadegeneratie) in de studie van Herrinton (2017) hoger was in de DSBCS groep dan in de ISBCS groep. Alle patiënten met een oogheelkundige comorbiditeit, en dus een verhoogd risico op macula oedeem, werden automatisch ingedeeld in de DSBCS groep. Het aantal cases in de studies van Sarikkola (2011) en Serrano-Aguilar (2012) zijn te laag om te kunnen poolen. In de studie van Herrinton (2017) komt macula oedeem in de ISBCS groep in 0,55% (29/5.247) van de patiënten voor en in de DSBCS groep bij 0,85% (165/19.368) van de patiënten (figuur 5). Dit leidde tot een risk ratio van 0,65 (95% BI 0,44 tot 0,96, p=0,03) in het voordeel van de ISBCS groep. Vanwege de selectiebias (de meerderheid van patiënten met oogheelkundige comorbiditeit werd in de DSBCS groep ingedeeld) is er geen GRADE beoordeling voor deze uitkomstmaat gedaan.
Figuur 5 Uitkomstmaat macula oedeem
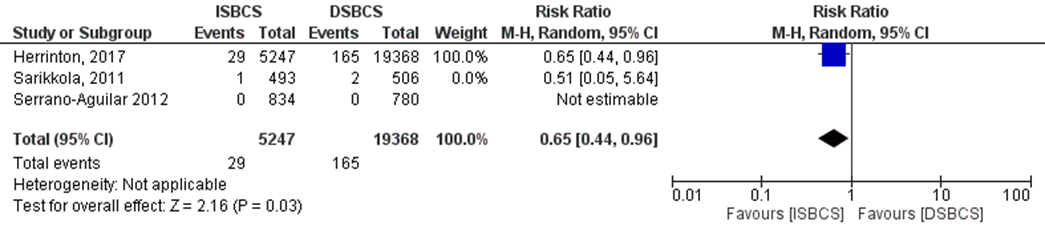
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval; ISBCS: immediate sequential bilateral cataract surgery; DSBCS: delayed sequential bilateral cataract surgery. *Totalen zijn # patiënten
3. Patiënt-gerapporteerd functioneren
a. Nadat beide ogen zijn geopereerd
Kessel (2015) rapporteert geen verschil tussen de groepen één maand nadat beide ogen zijn geopereerd. In deze systematische review is een verkeerde waarde gebruikt voor de gemiddelde score van de DSBCS groep voor de studie van Sarikkola (2011) (19,2 in plaats van 23,8). De juiste berekening van het gepoolde effect laat zien dat het gestandaardiseerde gemiddelde verschil -0,11 (95% BI -0,36 tot 0,13, p=0,37) is met een random effect model en een hoge heterogeniteit (I2 83%) (figuur 6). Hetgeen inhoudt dat er geen verschil is tussen de groepen. De studie van Lundström (2006) die subjectief functioneren met de Catquest onderzocht (met een totaalscore in de range van zeven tot 34) is niet in deze berekening meegenomen omdat de SD niet werd gerapporteerd en ook niet berekend kon worden omdat het verschil tussen de groepen nul was. Beide groepen (ISBCS en DSBCS) lieten een gemiddelde score van 7,0 zien wat statistisch niet significant verschillend was (p=0,481).
Figuur 6 Uitkomstmaat patiënt-gerapporteerd functioneren nadat beide ogen zijn geopereerd
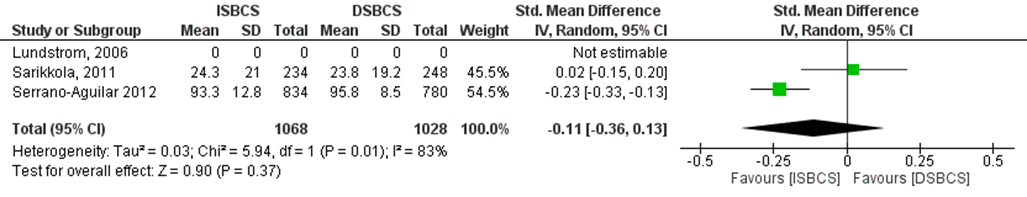
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval; ISBCS: immediate sequential bilateral cataract surgery; DSBCS: delayed sequential bilateral cataract surgery. *Totalen zijn # patiënten
b. In de tussentijd
In de tussenliggende tijd dat in de DSBCS groep het tweede oog niet was geopereerd was er wel een verschil in het voordeel van de ISBCS groep op basis van de VF-14 (score tussen 0 en 100): ISBCS: 93,3±12,8 en DSCBS: 81,3±18,3 met een gemiddeld verschil van 12,0 (95%BI 10,45 tot 13,55), p<0,001) (Serrano-Aguilar, 2012) en ISBCS: 8,0 en DSBCS: 11,0 (p<0,001) (Lundström, 2006).
Bewijskracht van de literatuur
Afwijkingen van doelrefractie
De bewijskracht voor de uitkomstmaat afwijkingen van doelrefractie is met 1 niveau verlaagd gezien beperkingen in de onderzoeksopzet (-1 risk of bias, waaronder onduidelijke allocation concealment en onduidelijk of de outcome assessor was geblindeerd). Vanwege het studiedesign is het startpunt GRADE ‘hoog’, de uiteindelijke bewijskracht komt uit op GRADE ‘redelijk’.
Endoftalmitis
De bewijskracht voor de uitkomstmaat endoftalmitis is niet verlaagd voor risk of bias omdat dit al verdisconteerd wordt in de start op een laag niveau bij observationeel onderzoek. Er wordt ook niets afgetrokken voor inconsistentie, publicatiebias, imprecisie of indirectheid. Er wordt opgewaardeerd met 1 niveau vanwege de sterke associatie (geen verschil tussen de groepen). Vanwege het studiedesign is het startpunt GRADE ‘laag’, de uiteindelijke bewijskracht komt uit op GRADE ‘redelijk’.
Serious adverse events
De bewijskracht voor de uitkomstmaat serious adverse events is met 1 niveau verlaagd op grond van overlap van het 95% betrouwbaarheidsinterval met de grenzen voor klinische besluitvorming (-1, imprecisie). Vanwege het studiedesign is het startpunt GRADE ‘laag’, de uiteindelijke bewijskracht komt uit op GRADE ‘zeer laag’.
Adverse events
De bewijskracht voor de uitkomstmaat adverse events is met 2 niveaus verlaagd op grond van beperkingen in de onderzoeksopzet (-1, risk of bias, onduidelijk of outcome assessor was geblindeerd) en overlap van het 95% betrouwbaarheidsinterval met de grenzen voor klinische besluitvorming (-1, imprecisie). Vanwege het studiedesign is het startpunt GRADE ‘hoog’, de uiteindelijke bewijskracht komt uit op GRADE ‘laag’.
Achterste kapselruptuur
De bewijskracht voor de uitkomstmaat achterste kapselruptuur is met 1 niveau verlaagd op grond van overlap van het 95% betrouwbaarheidsinterval met de grenzen voor klinische besluitvorming (-1, imprecisie). Vanwege het studiedesign is het startpunt GRADE ‘laag’, de uiteindelijke bewijskracht komt uit op GRADE ‘zeer laag’.
Macula oedeem
Er is geen GRADE-beoordeling gedaan voor de uitkomstmaat macula oedeem vanwege het feit dat er een sterke mate van selectiebias aanwezig is. Alle patiënten met een verhoogd risico op macula oedeem (degenen met oogheelkundige comorbiditeit) werden in de DSBCS groep ingedeeld.
Patiënt-gerapporteerd functioneren na operatie van twee ogen
De bewijskracht voor de uitkomstmaat patiënt-gerapporteerd functioneren is met 2 niveaus verlaagd gezien beperkingen in de onderzoeksopzet (-1, risk of bias) en tegenstrijdige resultaten (-1, inconsistentie). Vanwege het studiedesign is het startpunt GRADE ‘hoog’, de uiteindelijke bewijskracht komt uit op GRADE ‘laag’.
Patiënt-gerapporteerd functioneren in de tussentijd
De bewijskracht voor de uitkomstmaat patiënt-gerapporteerd functioneren in de tussentijd is met 2 niveaus verlaagd op grond van beperkingen in de onderzoeksopzet (-1, risk of bias) en overlap van het 95% betrouwbaarheidsinterval met de grenzen voor klinische besluitvorming (-1 imprecisie). Vanwege het studiedesign is het startpunt GRADE ‘hoog’, de uiteindelijke bewijskracht komt uit op GRADE ‘laag’.
Zoeken en selecteren
Om de uitgangsvraag te kunnen beantwoorden is een systematische literatuuranalyse verricht op basis van de volgende zoekvraag:
Wat zijn de effecten van een ‘immediate sequential’ bilaterale cataractchirurgie vergeleken met ‘delayed sequential’ bilaterale cataractchirurgie?
P: patiënten (> 18 jaar) met een indicatie voor cataractchirurgie;
I: bilaterale cataractchirurgie in onmiddellijk aansluitende sessies (immediate sequential) ISBCS;
C: bilaterale cataractchirurgie in twee sessies op verschillende dagen (delayed sequential) DSBCS;
O: Afwijkingen van de doelrefractie (cruciaal) en complicaties (zoals: endoftalmitis, achterste kapselruptuur, toxic anterior segment syndroom (TASS), macula oedeem en patiënt-gerapporteerd functioneren (belangrijk).
Relevante uitkomstmaten
De werkgroep achtte afwijkingen van de doelrefractie voor de besluitvorming cruciale uitkomstmaten en complicaties en patiënt-gerapporteerd functioneren voor de besluitvorming belangrijke uitkomstmaten.
De werkgroep definieerde de uitkomstmaten als volgt:
Afwijkingen van doelrefractie: de proportie van het aantal ogen waarbij het behaalde sferische equivalent niet binnen de 0,5 dioptrie of 1,0 dioptrie uitkwam. Met betrekking tot de uitkomstmaat patiënt-gerapporteerd functioneren definieerde de werkgroep gestandaardiseerde patiënttevredenheid vragenlijsten als geschikt instrument, zoals bijvoorbeeld de Catquest. Voor complicaties definieerde de werkgroep niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
Klinisch (patiënt) relevant verschil
De werkgroep definieerde voor afwijkingen van de doelrefractie een verschil van 5% tussen de groepen als een klinisch (patiënt) relevant verschil. Voor endoftalmitis werd een absoluut risico verschil van > 0 als een klinisch (patiënt-)relevant verschil gezien evenals voor de overige complicaties (een risk ratio van > 1). Voor patiënt-gerapporteerd functioneren werd een verschil tussen de groepen van 15% gehanteerd.
Zoeken en selecteren (Methode)
In de databases Medline (via OVID) en Embase (via Embase.com) is met relevante zoektermen gezocht naar systematische reviews, gerandomiseerd gecontroleerd onderzoek (RCT’s) en observationeel onderzoek. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 369 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria: systematische review (gezocht in ten minste twee relevante databases, risk of bias beoordeling aanwezig en de resultaten van individuele studies voldoende gepresenteerd) of RCT of observationeel onderzoek waarin een vergelijking is gemaakt tussen ISBCS en DSBCS bij > 20 (10 per arm) patiënten met een vergelijkbaar antibioticabeleid in beide groepen. Daarnaast moest tenminste één van de bovengenoemde uitkomstmaten zijn gerapporteerd.
Op basis van titel en abstract werden in eerste instantie tien studies voorgeselecteerd. Na raadpleging van de volledige tekst werd één studie uit een systematische review extra geïncludeerd en werden vervolgens vijf studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording). Zes studies werden tenslotte definitief geselecteerd.
Resultaten
Zes onderzoeken zijn opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidencetabellen. Voor de uitkomstmaat endoftalmitis werden alleen observationele studies geïncludeerd vanwege de lage incidentie van endoftalmitis. RCT’s zijn daardoor per definitie underpowered. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk-of-biastabellen.
Referenties
- Arshinoff, S. A., & Bastianelli, P. A. (2011). Incidence of postoperative endophthalmitis after immediate sequential bilateral cataract surgery. Journal of Cataract & Refractive Surgery, 37(12), 2105-2114.
- Frampton, G., Harris, P., Cooper, K., Lotery, A., & Shepherd, J. (2014). The clinical effectiveness and cost-effectiveness of second-eye cataract surgery: a systematic review and economic evaluation. Health Technology Assessment, 18(68),1-205.
- Herrinton, L. J., Liu, L., Alexeeff, S., Carolan, J., & Shorstein, N. H. (2017). Immediate sequential versus delayed sequential bilateral cataract surgery: retrospective comparison of postoperative visual outcomes. Ophthalmology, 124(8), 1126-1135.
- Kessel, L., Andresen, J., Erngaard, D., Flesner, P., Tendal, B., & Hjortdal, J. (2015). Immediate sequential bilateral cataract surgery: a systematic review and meta-analysis. Journal of ophthalmology, 2015.
- Lundström, M., Albrecht, S., Nilsson, M., & Åström, B. (2006). Benefit to patients of bilateral same-day cataract extraction: Randomized clinical study. Journal of Cataract & Refractive Surgery, 32(5), 826-830.
- Sarikkola, A. U., Uusitalo, R. J., Hellstedt, T., Ess, S. L., Leivo, T., & Kivelä, T. (2011). Simultaneous bilateral versus sequential bilateral cataract surgery: Helsinki Simultaneous Bilateral Cataract Surgery Study report 1. Journal of Cataract & Refractive Surgery, 37(6), 992-1002.
- Serrano-Aguilar, P., Ramallo-Fariña, Y., Cabrera-Hernández, J. M., Perez-Silguero, D., Perez-Silguero, M. A., Henríquez-de la Fe, F., & de Ussel, J. G. I. (2012). Immediately sequential versus delayed sequential bilateral cataract surgery: safety and effectiveness. Journal of Cataract & Refractive Surgery, 38(10), 1734-1742.
- Shekhawat, N. S., Stock, M. V., Baze, E. F., Daly, M. K., Vollman, D. E., Lawrence, M. G., & Chomsky, A. S. (2017). Impact of first eye versus second eye cataract surgery on visual function and quality of life. Ophthalmology, 124(10), 1496-1503.
- Spekreijse L, Simons R, Winkens B, van den Biggelaar F, Dirksen C, Bartels M, de Crom R, Goslings O, Joosse M, Kasanardjo J, Lansink P, Ponsioen T, Reus N, Schouten J, Nuijts R. Safety, effectiveness, and cost-effectiveness of immediate versus delayed sequential bilateral cataract surgery in the Netherlands (BICAT-NL study): a multicentre, non-inferiority, randomised controlled trial. Lancet. 2023 Jun 10;401(10392):1951-1962.
Evidence tabellen
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Herrinton, 2017 |
Type of study: retrospective observational
Setting and country: Hospital, USA
Funding and conflicts of interest: Funded by the Garfield Memorial Fund, Kaiser Permanente, and the National Eye Institute (NEI R01 EY027329). These sponsors had no role in the design or conduct of this research. Kaiser Permanente potentially derives a benefit from improvements in operating room and clinic efficiency and implementation of immediate sequential bilateral cataract surgery, and this represents a potential conflict of interest. |
Inclusion criteria: health plan members who underwent their first noncomplex phacoemulsification for cataract. Information from manifest refractions for postoperative BCVA analysis. At least 1 year of enrollment before cataract surgery on the first eye.
Exclusion criteria: complex phacoemulsification cases and cases performed by glaucoma, oculoplastic, or retinal specialists, as well as procedures by any surgeon combined with corneal transplant or glaucoma surgery. Cases with previous endophthalmitis
N total at baseline: Intervention: 3561 Control: 13711
Important prognostic factors2: For example age ≤ 74y: I:54% C:51%
Sex: I: 39% M C: 38% M
Groups comparable at baseline? Different in: -year at first surgery -Race /ethnicity -Multifocal / monofocal -Glaucoma |
Describe intervention (treatment/procedure/test):
ISBCS, with surgery in the right and left eyes performed back-to-back on the same day,
|
Describe control (treatment/procedure/test):
DSBCS, with the 2 eyes operated on separate days, the second eye within 1 year of the first
|
Length of follow-up: 1 year
Incomplete outcome data: Intervention: N =341 (9,6%) Reasons (at random)
Control: N=1081 (7.9%) Reasons (at random)
|
Outcome measures and effect size (include 95%CI and p-value if available):
Refractive error (RE): OR: 1.02 (95%CI 0.92 – 1.12), p=0.75 I: n=3220 C: n= 12630
Average postoperative RE I: -0.36D C: -0.39D
Surgical complications N=25 (0.7%) converted from ISBCS to DSBCS; due to: -Intraoperative posterior capsular rupture/ Vitrectomy (N=6) -Patient agitation or BP elevation (n=4) -Equipment problem (n=3) -Iris-related (n=3) -IOL had to be removed (n=2) Intraoperative corneal edema (n=2) -Zonular dehiscence (n=2) -Floppy capsular bag (n=1) -Ant capsular tear (n=1) -Intra-operative bleeding (n=1) à these not reported for the initial DSBCS group
Incidence Intraoperative posterior capsular rupture: I: 0.84 C: 0.67 (p=0.23)
Vitrectomy I: 0.42 C: 0.45 (p=0.82)
Post capsular rupture and/or vitrectomy: I: 0.93 (N=6 (0,2%) small post capsular rent) C: 0.88, p=0.79
Endophthalmitis (<120 days post op) I: 1/10494 eyes C: 2/38736 eyes, p=0.32
Macula edema (<120 days) (# patients), by OCT and treated with prednisolone I: 29/5247 pt = 0.55% C: 165/19368 pt = 0.85%, p=0.03 |
Postoperative RE was calculated as the spherical equivalent (sphere þ cylinder/2), measured in diopters (D); nearest the date of surgery during the interval 3 weeks to 1 year after surgery:
Emmetropia was defined as spherical error of <0.5 to 0 D, whereas eyes that were more myopic or hyperopic were defined as ametropic. |
|
Arshinoff, 2011 |
Type of study: cohort study
Setting and country: multicentre; International
Funding and conflicts of interest: Supported by the Eye Foundation of Canada (Mr. Bastianelli). |
Inclusion criteria: -Members of the iSBCS were surveyed, and the overall incidence of postoperative endophthalmitis after ISBCS was calculated from the collected data. -In addition, the literature was reviewed to determine the recent incidence of postoperative endophthalmitis in unilateral cataract surgery with and without the use of intracameral antibiotics; the data were compared with the collected results.
Exclusion criteria: All cases of postoperative endophthalmitis, irrespective of cause, were included except 2, 1 each in the vancomycin and moxifloxacin groups because in both cases the eye was noted to be clear 2 weeks postoperatively and the patients subsequently experienced trauma, causing wound rupture and then infection.
N total at baseline: Intervention: 95606 Control: 29582
Important prognostic factors2: For example age ± SD: I:NR C:NR
Sex: I: NR C: NR
Groups comparable at baseline? NR |
Describe intervention (treatment/procedure/test):
immediately sequential bilateral cataract surgery (ISBCS)
|
Describe control (treatment/procedure/test):
delayed sequential bilateral cataract surgery [DSBCS)
|
Length of follow-up:
Loss-to-follow-up: NR
Incomplete outcome data: NR
|
Outcome measures and effect size (include 95%CI and p-value if available):
Endophthalmitis incidence rate in ISBCS
NO IC agent (No IC agent (none C infusion)) :12/23847 (1/1987); 0.05%
IC profylaxis: 5/71759 (1/14352); 0.007%
All: 17/95606 (1/5759); 0.017%
In DSBCS 1/29582
|
|
|
Study reference
(first author, year of publication) |
Bias due to a non-representative or ill-defined sample of patients?1
(unlikely/likely/unclear) |
Bias due to insufficiently long, or incomplete follow-up, or differences in follow-up between treatment groups?2
(unlikely/likely/unclear) |
Bias due to ill-defined or inadequately measured outcome ?3
(unlikely/likely/unclear) |
Bias due to inadequate adjustment for all important prognostic factors?4
(unlikely/likely/unclear) |
|
Herrinton, 2017 |
Unlikely
Selection bias: patients more at risk were allocated to DSBCS |
Unlikely |
Unlikely |
Unlikely: To control for potential confounding by patient factors, the regression model also adjusted for patient-level variables, including time to postoperative refraction.
We estimated the adjusted odds ratio (OR) and 95% confidence interval (CI) for the association of ISBCS compared with DSBCS for each dichotomous outcome by fitting a conditional logistic regression model that stratified by surgeon. This approach ensured adjustment for a variety of practice variations across surgeons, including choice of formula for IOL power calculations
Note: intention-to-treat analyses, in which patients scheduled for ISBCS who were converted to DSBCS were nonetheless retained in the ISBCS group. |
|
Arshinoff, 2011 |
Unlikely |
Unlikely |
Unlikely |
Unlikely |
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Kessel, 2015 |
Yes |
Yes |
Yes |
Yes |
NA |
Yes |
Yes |
Yes, but not reported in results |
Yes |
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Dickman, 2019 |
Studiedesign voldoet niet |
|
Guber, 2015 |
Geen vergelijkende studie |
|
Leivo, 2011 |
Andere uitkomsten beschreven |
|
Malvankar-Mehta, 2015 |
Selectiecriteria van de systematische review voldoet niet en andere uitkomsten beschreven |
|
Rush, 2015 |
Studiedesign voldoet niet en kleine studie |
Verantwoording
Autorisatiedatum en geldigheid
Laatst beoordeeld : 09-11-2021
Laatst geautoriseerd : 09-11-2021
Geplande herbeoordeling : 01-01-2027
|
Module[1] |
Regiehouder(s)[2] |
Jaar van autorisatie |
Eerstvolgende beoordeling actualiteit richtlijn[3] |
Frequentie van beoordeling op actualiteit[4] |
Wie houdt er toezicht op actualiteit[5] |
Relevante factoren voor wijzigingen in aanbeveling[6] |
|
Tijdsbestek |
NOG |
2021 |
2026 |
5 |
NOG |
Wijziging in veiligheid van behandelen (minder complicaties) |
[1] Naam van de module
[2] Regiehouder van de module (deze kan verschillen per module en kan ook verdeeld zijn over meerdere regiehouders)
[3] Maximaal na vijf jaar
[4] (half)Jaarlijks, eens in twee jaar, eens in vijf jaar
[5] regievoerende vereniging, gedeelde regievoerende verenigingen, of (multidisciplinaire) werkgroep die in stand blijft
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Doel en doelgroep
Doel
Een richtlijn is in wezen de beschrijving van de actuele stand van de kennis, technieken en gerelateerde zaken rond het onderwerp van de richtlijn. Daarnaast heeft een richtlijn tot doel de beroepsbeoefenaars aanbevelingen te geven die de kwaliteit van hun werk mede op het gewenste niveau kunnen houden. Er is dus ook sprake van een beschrijving van kwalitatieve normen voor de beroepsgroep. Iedere arts is gehouden om primair te handelen in het belang van de patiënten daarbij zorg te dragen voor diens veiligheid in relatie tot het medische handelen. De Richtlijn Cataract stelt dan ook normen vast voor goede praktijkvoering, stelt standaarden voor patiëntenzorg en veiligheid en biedt een referentiepunt voor de beoordeling van de resultaten waaraan cataractchirurgie van hoge kwaliteit moet voldoen. De aanbevelingen, normen en standaarden zijn getoetst aan de resultaten van gedegen wetenschappelijk onderzoek, gepubliceerd in de wetenschappelijke literatuur. Indien zekere vraagstellingen niet goed beantwoord konden worden op basis van literatuuronderzoek, werden de meningen van erkende experts gehoord door de richtlijnwerkgroep en bij consensus verwerkt in de aanbevelingen.
Doelgroep
Deze richtlijn is geschreven voor met name oogartsen maar ook andere leden van de beroepsgroepen die direct betrokken zijn bij de zorg met cataract.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2018 een werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met cataract.
Werkgroep
- Drs. B.A.E. (Bert) van der Pol, oogarts niet praktiserend, (voorzitter) NOG
- Dr. M.C. (Marjolijn) Bartels, oogarts, Deventer Ziekenhuis, NOG
- Drs. M.M.M.J. (Margot) Dellaert, oogarts, Treant Zorggroep, NOG
- Drs. Y.P. (Ype) Henry, oogarts, VU medisch centrum, NOG
- Dr. L.V. (Long) Ly, oogarts, Bergman Clinics, NOG
- Drs. R.C.M. (Marit) Maatman, oogarts, Alrijne Ziekenhuis, NOG
- Dr. N.J. (Nic) Reus, oogarts, Amphia Ziekenhuis, NOG
- Dr. N. (Nienke) Visser, oogarts, Maastricht Universitair Medisch Centrum, NOG
- Prof. Dr. R.M.M.A. (Rudy) Nuijts, oogarts, Maastricht Universitair Medisch Centrum, NOG
Met ondersteuning van
- Dr. A.C.J. (Astrid) Balemans, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. J. (Josefien) Buddeke, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- M. (Mitchel) Griekspoor MSc, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Klankbordgroep
- H.J. (Anneke) Jansen Molenaar, Adviseur Oogzorg bij de Oogvereniging
- D. (Dana) Kamsteeg-Koerts, Optometrist, Oogziekenhuis Rotterdam
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenwerkzaamheden |
Gemelde belangen |
Actie |
|
Van der Pol |
Niet praktiserend |
Geen |
Geen |
Geen actie |
|
Dellaert |
Oogarts |
Medisch manager, onkostenvergoeding |
Geen |
Geen actie |
|
Bartels |
Zelfstandig ondernemer, via B.V. verbonden aan Verenigde Specialisten Deventer en zo aan Deventer Ziekenhuis |
Voorzitter subcommissie Richtlijnen NOG |
Deelname aan ZonMw studie IBSCS / DBSCS via UMC Maastricht (site - investigator)
Contactpersoon namens cornea werkgroep bij hoornvliespatiënten vereniging.
|
Geen trekker van de modules over ontstekings- en infectieprofylaxe bij reguliere cataractchirurgie. |
|
Henry |
Oogarts; staflid
|
Lid van de steering group van EUREQUO (ESCRS); Secretaris van NIOIC (NOG); Voorzitter van WTO (NOG) |
Geen |
Geen actie |
|
Ly |
Oogarts bij Bergman Clinics |
Geen |
Geen |
Geen actie |
|
Maatman |
Oogarts, Alrijne Ziekenhuis
|
NOG bestuur (secretaris), betaald. Tot 2016/2017 advies Bayer / Eylea, betaald
|
Geen |
Geen trekker module ontstekingsprofylaxe reguliere cataractchirurgie. |
|
Reus |
Oogarts in het Amphia Ziekenhuis, Breda/Oosterhout
|
Bestuurslid Nederlandse Intraoculaire Implant Club (NIOIC) (onbetaald) Bestuurslid European Society of Cataract and Refractive Surgeons (ESCRS) (onbetaald)
|
Bestuurslid Nederlandse Intraoculaire Implant Club (NIOIC) (onbetaald)
1.Principal Investigator van Investigator-Initiated Trial waarvoor subsidie van Alcon (unresticted grant). Het onderwerp is de helderheid van ogen na een staaroperatie. Er wordt onderzoek gedaan naar de hoeveelheid lichtverstrooiing in de ogen na een cataractoperatie en redenen waarom er meer strooilicht in het oog overblijft na een cataractoperatie dan wordt verwacht. 2.Site-Investigator van studie naar bilaterale cataractchirurgie geïnitieerd door prof. R. Nuijts, oogarts (Universiteitskliniek voor Oogheelkunde Maastricht) waarvoor subsidie van ZonMW (unresticted grant). |
Geen trekker van modules met betrekking tot infectieprofylaxe bij reguliere cataractchirurgie en IOLs. |
|
Visser |
Oogarts, aandachtsgebieden cornea- en cataract chirurgie. Werkgever: University Eye Clinic Maastricht, MUMC+
|
Young ophthalmology committee ESCRS (onbetaald)
|
EPICAT study: Effectiveness of Periocular drug Injection in CATaract surgery (gefinancierd door ESCRS, het gaat hierbij om een restricted grant, de ESCRS heeft op voorhand akkoord gegeven voor de specifieke opzet, uitvoering, en terugkoppeling van de EPICAT studie) |
Geen actie |
|
Nuijts |
Prof.dr. RMMA Nuijts, hoogleraar Corneatransplantatie en Refractiechirurgie; MUMC Maastricht
|
- Voorzitter Nederlandse IntraOculaire Implant Club, NIOIC (onbetaald) |
Abbott: NL 56878.068.16/METC162029 A randomised, subject-masked evaluation of visual function after bilateral implantation of two types of presbyopia-correcting IOLs: the Symfony-study. Period: 01-12-2016 - 01-12-2018
Alcon: VERION versus conventional, manual ink-marking in toric IOL implantation. Period: 2015 - 2016
Alcon: ILJ466-P003 Post-Market Investigation of the Clareon IOL. Period: 2018 - 2028
Alcon: The ACRYSOF IQ PanOptix Presbyopia Correcting intraocular lens (IOL) Model TFNT00. Period: 01-12-2015 - 01-12-2017
CHIESI: NL 54419.000.15/CCMO15.0538 Multinational, multicentre, prospective, open-label, uncontrolled clinical trial to assess the efficacy and safety of Autologous Cultivated Limbal Stem Cells Transplantation (ACLSCT) for restoration of corneal epithelium in patients with limbal stem cell deficiency due to ocular burns. Period: 01-12-2016 - 01-12-2018
ESCRS: European Cornea and Cell Transplantation Registry (ECCTR), European Union Third Health Programme 2014-2020 and the European Society of Cataract and Refractive Surgeons. Period: 01-04-2016 - 2019
ESCRS: The ESCRS PREMED study: PREvention of Macular EDema after cataract surgery. Period: 2012 - 2016
InSciTE: EyeScite: smart biomedical solutions for better eyesight. |
Geen trekker van de modules met betrekking tot infectie- en onstekingsprofylaxe en IOLs bij reguliere cataractchirurgie. |
|
Kamsteeg-Koerts (klankbordgroep) |
Optometrist, Oogziekenhuis Rotterdam |
- Per 25 november 2019 lid OVN ledenraad met een aanstelling voor 3 jaar - Lid OVN commissie Beroepsbelangen |
Geen
|
Geen actie |
|
Jansen-Molenaar |
Adviseur Oogzorg bij de Oogvereniging |
Geen |
Geen |
Geen actie |
Inbreng patiëntenperspectief
Een afgevaardigde van de Oogvereniging nam zitting in de klankbordgroep. Daarnaast werden de Oogvereniging en de Patiëntenfederatie uitgenodigd om deel te nemen aan de schriftelijke knelpuntenanalyse. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de betrokken patiëntenverenigingen en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Methode ontwikkeling
Evidence based
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten met cataract. De werkgroep beoordeelde de aanbeveling(en) uit de eerdere richtlijnmodule cataract (2013) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door het Nederlands Oogheelkundig Gezelschap (NOG), de Nederlandse Vereniging voor Klinische Geriatrie (NVKG), het Nederlands Huisartsen Genootschap (NHG), de Oogvereniging, Verenso en de Landelijke Vereniging van Operatieassistenten (LVO) via een schriftelijke knelpuntenanalyse. Een verslag hiervan is opgenomen in de bijlagen.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming) en belangrijk (maar niet cruciaal). Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur en de beoordeling van de risk-of-bias van de individuele studies is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet een-op-een vergelijkbaar met het minimale klinisch relevante verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden die meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello, 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs, de belangrijkste overwegingen en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE-gradering HOOG) zal niet altijd van toepassing zijn onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Zoekacties zijn opvraagbaar. Neem hiervoor contact op met de Richtlijnendatabase.

