Gebruik van de femtosecond laser bij cataractoperaties
Uitgangsvraag
Is er een meerwaarde van de femtosecond laser boven reguliere phaco-emulsificatie bij cataractchirurgie?
Aanbeveling
Vanuit effectiviteits- en veiligheidsoverwegingen is er geen reden om voor FLACS te kiezen in plaats van conventionele phaco-emulsificatie.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Voor de cruciale uitkomstmaten ‘afwijkingen van doelrefractie’ en ‘verte-gecorrigeerde visus’ kan met redelijke zekerheid geconcludeerd worden dat er geen verschil is tussen FLACS en reguliere phaco-emulsificatie (redelijke bewijskracht). De overall bewijskracht voor de cruciale uitkomstmaten is redelijk.
Voor de belangrijke uitkomstmaten is de bewijskracht laag tot zeer laag. Endotheelcelverlies lijkt niet lager te zijn na FLACS ten opzichte van reguliere phaco-emulsificatie, de bewijskracht hiervoor is echter laag. Ook is er geen gunstig effect van FLACS ten opzichte van reguliere phaco-emulsificatie gevonden op de hoogte van aberraties. De bewijskracht hiervoor is zeer laag.
Voor de uitkomstmaat ‘voorste kapselruptuur’ kan er met lage zekerheid geconcludeerd worden dat FLACS mogelijk vaker leidt tot een voorste kapselruptuur dan reguliere phaco-emulsificatie (lage bewijskracht) en dat dit verschil klinisch relevant is: bij FLACS is er een 5,93 keer zo groot risico op een voorste kapselruptuur dan bij reguliere phaco-emulsificatie. Hierbij moet wel opgemerkt worden dat het gaat om een complicatie die weinig voorkomt (1,08% in de FLACS groep en 0,12% in de reguliere phaco-emulsificatie groep.
Achterste kapselrupturen lijken vaker voor te komen bij FLACS dan bij reguliere phaco-emulsificatie: er lijkt een 2,99 keer zo hoog risico op een achterste kapselruptuur bij FLACS dan bij reguliere phaco-emulsificatie. De bewijskracht hiervoor is echter laag. Ook hierbij geldt weer dat het relatief weinig voorkomt: 0,75% in de FLACS groep en 0,27% in de reguliere phaco-emulsificatiegroep. Voor de uitkomstmaat postoperatief klinisch significant macula oedeem is het niet duidelijk bij welke interventie dit vaker voorkomt; de bewijskracht hiervoor is zeer laag: er is veel onzekerheid rondom het gevonden resultaat.
De werkgroep is van mening dat de hogere incidentie complicaties (voorste en achterste kapselrupturen) mogelijk (deels) te verklaren is doordat het een nieuwe techniek betreft, waardoor er bij eerste gepubliceerde cohortonderzoeken op dit onderwerpen mogelijk vaker sprake is van complicaties.
Als complicaties die geen onderdeel uitmaakten van de analyse kan nog genoemd worden dat in de FLACS groep van de Franse FEMCAT study een conversie van FLACS naar conventionele phaco-emulsificatie nodig was in 9% van de ogen ten gevolge van technische laser failures, onvoldoende pupil dilatatie of problemen met de dockingprocedure van de laser. Dit beloop kan tot een vermindering in patiënttevredenheid leiden (Schweitzer, 2020).
Enkele case series tonen mogelijke voordelen van FLACS bij subgroepen patiënten met een ondiepe voorste oogkamer of Fuchse endotheeldystrofie of bij toepassing van FLACS bij patiënten met premium IOLs (Fan, 2018; Mencucci, 2019; Vasavada, 2019; Yong, 2018; Zhu, 2018). Er zijn aanwijzingen dat de toepassing van FLACS bij sommige van deze categorieën voordelen kan opleveren, met name op het gebied van energieverbruik bij phacoemulsificatie (cumulatieve dissipated energy), endotheelcelverlies, en centrale dikte. Echter, deze studies zijn niet opgenomen in de literatuuranalyse omdat er geen vergelijking is gemaakt met reguliere phaco-emulsificatie in een gerandomiseerde gecontroleerde trial of geen van de relevante uitkomstmaten rapporteerden en daardoor niet aan de PICO voldeden.
In patiëntengroepen waar conventionele phaco-emulsificatie kan leiden tot een verhoogde kans op complicaties (bijvoorbeeld bij de behandeling van capsular contraction syndrome) (Gerten, 2016; Ibarz, 2017; Recalde, 2020) kan de keuze voor FLACS gerechtvaardigd zijn ondanks de lagere kosten-effectiviteit (Chee, 2021)
De toepassing van FLACS bij premium IOL implantaties kan voordelen bieden omdat de sizing en centrering van de capsulotomie nauwkeuriger kan zijn met een FLACS procedure, maar in de literatuur zijn er onvoldoende aanwijzingen dat dit leidt tot verbetering van de visuele uitkomsten in vergelijking met conventionele phaco-emulsificatie.
Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)
Soms kan bij patiënten de indruk ontstaan dat een nieuwere techniek (soms benoemd als gerobotiseerde staaroperatie) per definitie tot een beter behandelresultaat leidt. De bijbetaling die aan de patiënt wordt gevraagd voor deze techniek kan ook het gevoel geven dat er wordt betaald voor een beter resultaat. Uit de huidige analyse blijkt echter dat FLACS niet superieur is ten opzichte van conventionele phaco-emulsificatie. Het is daarom van belang de patiënt adequaat te informeren en vervolgens op basis van de bestaande evidence een shared decision te nemen.
Kosten (middelenbeslag)
De FLACS procedure is veel kostbaarder dan de conventionele phaco-emulsificatie. Dit zit met name in de investering van het apparaat en de gebruikte disposables (interfaces), maar ook deels in de bewerkelijkheid en de extra benodigde proceduretijd. De Franse FEMCAT-study (Schweitzer, 2020) en de Britse FACT-study (Day, 2020a en Day, 2020b) toonden aan dat FLACS duurder is en minder effectief en daardoor leidt tot een lagere kosten-effectiviteit in vergelijking met reguliere phaco-emulsificatie. In Nederland zijn er met betrekking tot de kosten-effectiviteit geen studies naar FLACS uitgevoerd maar de verwachting is niet dat deze uitkomst substantieel zal verschillen van de FEMCAT-studie. Verschuivingen in dat opzicht zijn slechts te verwachten als de aanschaf- en procedurekosten zullen verminderen.
Voor toepassing van FLACS is een financiële investering in laserapparatuur vereist waarvoor binnen de reguliere DBC vergoedingenstructuur geen mogelijkheden zijn om deze meerkosten bij de patiënt binnen de DBC in rekening te brengen. Momenteel worden de meerkosten vaak in rekening gebracht onder het implanteren van een premium lens.
Aanvaardbaarheid, haalbaarheid en implementatie
Gezien de lagere kosteneffectiviteit en het feit dat de FLACS technologie niet tot een verbeterde veiligheid (vermindering complicaties) en effectiviteit (postoperatieve visuele en refractieve resultaten) leidt, ligt implementatie van FLACS binnen de reguliere cataractchirurgie in Nederland niet in de rede.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Toepassing van FLACS in reguliere cataractchirurgie leidt niet tot betere visuele uitkomsten in vergelijking met conventionele phaco-emulsificatie en heeft een lagere kosteneffectiviteit.
Toepassing van FLACS in reguliere cataractchirurgie leidt niet tot een lagere incidentie van complicaties (anterieure en posterieure kapselrupturen, CME) in vergelijking met conventionele phaco-emulsificatie en mogelijk zelfs tot een hogere incidentie, alhoewel de totale incidentie laag is.
Onderbouwing
Reeds decennialang is de phaco-emulsificatie de standaardbehandeling voor cataract. Sinds enkele jaren wordt (femtosecond) lasertechnologie toegepast bij cataractchirurgie met als doel diverse stappen van de chirurgie verder te verbeteren. Het is onduidelijk wat de voor- en nadelen van femtosecondlaser-assisted cataract surgery (FLACS) zijn vergeleken met de conventionele phaco-emulsificatie met betrekking tot effectiviteit, veiligheid en kosteneffectiviteit.
1. Afwijkingen van doelrefractie
|
Redelijk GRADE |
Er is waarschijnlijk geen verschil tussen FLACS en reguliere phaco-emulsificatie in afwijkingen van de doelrefractie 1 tot 3 maanden postoperatief.
Bronnen: (Day, 2016; Filkorn,2012; Mastropasqua, 2014b; Yu, 2015; Day, 2020; Krarup, 2019; Roberts, 2019 en Schweitzer, 2020. |
2. Verte-gecorrigeerde visus
|
Redelijk GRADE |
Er is waarschijnlijk geen verschil tussen FLACS en reguliere phaco-emulsificatie in verte-gecorrigeerde visus 1 tot 3 maanden postoperatief.
Bronnen: (Day, 2016, Filkorn,2012; Mastropasqua, 2014a, Mastropasqua, 2014b; Schargus, 2015; Yu, 2015; Wang, 2019; Titiyal, 2016; Day, 2020; Krarup, 2019 en Schweitzer, 2020) |
3. Aberraties
|
Zeer laag GRADE |
Het is onduidelijk of er een verschil is in aberraties 4 tot 6 weken postoperatief tussen FLACS en reguliere phaco-emulsificatie.
Bronnen: (Day, 2016; Mastropasqua, 2014; Nagy, 2014) |
4. Verlies van endotheelcellen (> 3 maanden)
|
Laag GRADE |
Er lijkt geen verschil in endotheelcelverlies 3 maanden postoperatief tussen FLACS en reguliere phaco-emulsificatie.
Bronnen: (Day, 2016; Schargus, 2015; Chen, 2016; Conrad-Hengerer, 2013; Day, 2020; Krarup, 2019 en Schweitzer, 2020) |
5. Voorste kapselruptuur
|
Laag GRADE |
FLACS resulteert mogelijk in meer voorste kapselrupturen dan reguliere phaco-emusificatie.
Bronnen: (Day, 2016; Conrad-Hengerer, 2013; Conrad-Hengerer, 2014; Conrad-Hengerer, 2015; Kovacs, 2014; Kranitz, 2012; Nagy, 2011; Nagy, 2014; Reddy, 2013; Schargus, 2015; Yu, 2015; Popovic, 2016; Ewe, 2016; Wang 2019; Abell, 2015; Roberts, 2019; Ang, 2019; Berk, 2018; Day, 2020; Krarup, 2019; Manning, 2016; en Schweitzer, 2020) |
6. Achterste kapselruptuur
|
Laag GRADE |
FLACS resulteert mogelijk in meer achterste kapselrupturen dan reguliere phaco-emulsificatie.
Bronnen: (Day, 2016; Conrad-Hengerer, 2013; Conrad-Hengerer, 2014; Conrad-Hengerer, 2015; Kovacs, 2014; Kranitz, 2012; Nagy, 2011; Nagy, 2014; Reddy, 2013; Schargus, 2015; Yu, 2015; Popovic, 2016; Bali, 2012; Chen, 2015; Ewe, 2016; Khandekar, 2015; Wang 2019; Abell, 2015; Titiyal, 2016; Ang, 2019; Berk, 2018; Day, 2020; Krarup, 2019; Manning, 2016; Roberts, 2019 en Schweitzer, 2020) |
7. Postoperatief klinisch significant macula oedeem
|
Zeer laag GRADE |
Het is onduidelijk of er een verschil is in het optreden van klinisch significant macula oedeem na 6 weken postoperatief tussen FLACS en reguliere phaco-emulsificatie.
Bronnen: (Day, 2016; Conrad-Hengerer, 2013; Conrad-Hengerer, 2014; Conrad-Hengerer, 2015; Kovacs, 2014; Kranitz, 2012; Nagy, 2011; Nagy, 2014; Schargus, 2015; Yu, 2015; Popovic, 2016; Ewe, 2016 en Schweitzer, 2020) |
Beschrijving studies
Systematische reviews
Day (2016) is een systematische Cochrane review waarin 13 RCT’s werden geïncludeerd met patiënten > 18 jaar die een cataractoperatie ondergingen aan één of beide ogen en de vergelijking werd gemaakt tussen 1) FLACS en 2) reguliere phaco-emulsificatie. Er werd gezocht tot mei 2016 en er werd een GRADE-beoordeling uitgevoerd. Voor de uitkomstmaten voorste kapselruptuur, afwijkingen van doelrefractie, verte-gecorrigeerde visus, achterste kapselruptuur en macula oedeem werd een meta-analyse uitgevoerd (Conrad-Hengerer, 2013; Conrad-Hengerer, 2014; Conrad-Hengerer, 2015; Filkorn,2012; Kovacs, 2014; Kranitz, 2012; Mastropasqua, 2014a, Mastropasqua, 2014b; Nagy, 2011; Nagy, 2014; Reddy, 2013; Schargus, 2015 en Yu, 2015). In de individuele studies werd gecontroleerd of er sprake was van klinisch significant macula oedeem. Voor aberraties werd geen meta-analyse uitgevoerd maar benoemd dat de studie dit had gemeten (Mastropasqua, 2014a en Nagy, 2014). Resultaten van aberraties werden uit deze individuele studies gehaald.
Chen (2016) is een systematische review waarin RCT’s en cohortstudies werden geïncludeerd met patiënten met leeftijds-gerelateerde cataract zonder andere oculaire comorbiditeiten zoals amblyopie, glaucoom, diabetische retinopathie of maculadegeneratie) die een cataractoperatie ondergingen en de vergelijking werd gemaakt tussen 1) FLACS en 2) reguliere phaco-emulsificatie en die de uitkomstmaat verlies van endotheelcellen rapporteerden. De kwaliteit van de geïncludeerde studies werd beoordeeld aan de hand van de Newcastle-Ottawa Quality Assessment Scale (NOS). Verlies van endotheelcellen gemeten na 3 maanden werd gerapporteerd door één RCT (Conrad-Hengerer, 2013).
Popovic (2016) is een systematische review waarin RCT’s en cohortstudies (prospectief en retrospectief) werden geïncludeerd met patiënten die een cataractoperatie ondergingen aan één of beide ogen en de vergelijking werd gemaakt tussen 1) FLACS en 2) reguliere phaco-emulsificatie met een minimum van 5 ogen per studie-arm. Er werd gezocht tot maart 2016. De kwaliteit van de geïncludeerde studies werd beoordeeld aan de hand van de NOS. Voor de uitkomstmaat achterste kapselruptuur werden vier cohorten geïncludeerd (Bali, 2012; Chen, 2015; Ewe, 2016 en Khandekar, 2015).
Wang (2019) is een systematische review waarin cohortstudies (prospectief en retrospectief) werden geïncludeerd met patiënten die een cataractoperatie ondergingen aan één of beide ogen en de vergelijking werd gemaakt tussen 1) FLACS en 2) reguliere phaco-emulsificatie en complicaties werden gerapporteerd. Er werd niet beschreven tot welke datum er werd gezocht. Er werden twee cohorten (Abell, 2015 en Titiyal, 2016) en één RCT (Roberts, 2019) (aanvullend aan Day, 2016 en Popovic, 2016) geïncludeerd die complicaties (voorste kapselruptuur, achterste kapselruptuur en klinisch significant macula oedeem) beschreven. De kwaliteit van de geïncludeerde studies werd beoordeeld aan de hand van de NOS. Abell (2015) beschrijft dat patiënt karakteristieken gelijk waren tussen de groepen en dat de procedures tussen mei 2012 en november 2013 werden uitgevoerd.
RCT’s
Day (2020) was een multicenter RCT uit het Verenigd Koninkrijk waarin bij patiënten > 18 jaar die voor één of beide ogen in aanmerking kwamen voor een cataractoperatie de vergelijking werd gemaakt tussen 1) FLACS (N=392 patiënten, gemiddelde leeftijd 68±10 jaar) en 2) reguliere phaco-emulsificatie (N=393 patiënten, gemiddelde leeftijd 68±10 jaar). Exclusiecriteria waren onder andere ernstige cornea troebeling, cornea abnormaliteiten, cornea oedeem, Descemetocele met belemmerende cornea ruptuur of gebrekkige iris dilatatie. De volgende voor de werkgroep relevante uitkomsten werden gerapporteerd: voorste kapselruptuur, afwijkingen van doelrefractie na 3 maanden (in % dat binnen +/- 0.5 dioptrie uitkwam), verte-gecorrigeerde visus na 3 maanden, achterste kapselruptuur, postoperatief macula oedeem (zonder dat gedefinieerd werd dat dit om klinisch significant macula oedeem ging en daarom voor deze analyse niet meegenomen) en verlies van endotheelcellen na 3 maanden. De loss-to-follow up was 19,4% in de FLACS groep en 9,9% in de reguliere phaco-emulsificatiegroep. Patiënten waren niet geblindeerd voor de interventie, outcome assessors wel.
Krarup (2019) was een single-center RCT uit Denemarken waarin bij patiënten > 18 jaar die voor beide ogen in aanmerking kwamen voor een cataractoperatie de vergelijking werd gemaakt tussen 1) FLACS (N=108 patiënten, 108 ogen) en 2) reguliere phaco-emulsificatie (N=108 patiënten, 108 ogen). Er werd gerandomiseerd binnen de patiënt, één oog werd behandeld met FLACS en het andere oog met phaco-emulsificatie. Exclusiecriteria waren onder andere ernstig droge ogen, cornea littekens, keratoconus, uveïtis en visueel significante maculopathie. De volgende voor de werkgroep relevante uitkomsten werden gerapporteerd: voorste kapselruptuur, afwijkingen van doelrefractie (mean absolute error) na 40 dagen, verte-gecorrigeerde visus na 40 dagen, achterste kapselruptuur en verlies van endotheelcellen na 6 maanden. Een beperking van de studie was dat patiëntkarakteristieken niet werden gepresenteerd. Patiënten waren niet geblindeerd voor de interventie, outcome assessors wel.
Schweitzer (2020) was een multicenter RCT uit Frankrijk waarin bij patiënten > 22 jaar die voor één of beide ogen in aanmerking kwamen voor een cataractoperatie de vergelijking werd gemaakt tussen 1) FLACS (N=454 patiënten, 704 ogen, gemiddelde leeftijd 72,4±8,6 jaar) en 2) reguliere phaco-emulsificatie (N=453 patiënten, 685 ogen, gemiddelde leeftijd 72,1±8,7 jaar). Exclusiecriteria waren onder andere gebrekkige iris-dilatatie en cornea-astigmatisme van 1-5 dioptrieën. De volgende voor de werkgroep relevante uitkomsten werden gerapporteerd: voorste kapselruptuur, afwijkingen van doelrefractie na 3 maanden (mean absolute error van het sferische equivalent van de manifeste refractie), verte-gecorrigeerde visus na 3 maanden, achterste kapselruptuur, postoperatief klinisch significant cystoïd macula oedeem en verlies van endotheelcellen na 3 maanden. De loss-to-follow up was met 10% gelijk in beide groepen. Patiënten en outcome assessors waren geblindeerd.
Observationele studies
Ang (2019) beschreef een retrospectief single-center cohort uit de Filipijnen waarvoor patiënten > 18 jaar die een cataractoperatie hadden ondergaan in de periode van januari 2011 tot september 2015 en tenminste één maand follow-up hadden werden geïncludeerd. Exclusiecriteria waren cornea littekens, keratoconus, amblyopie, glaucoom, netvliesproblemen en schade aan de nervus opticus. De vergelijking werd gemaakt tussen 1) FLACS (N=296 patiënten, gemiddelde leeftijd 67,5±10,3 jaar) en 2) phaco-emulsificatie (N=439 patiënten, gemiddelde leeftijd 65,2±10,9 jaar). De volgende voor de werkgroep relevante uitkomsten werden gerapporteerd: voorste kapselruptuur en achterste kapselruptuur.
Berk (2018) beschreef een singlecenter retrospectief cohort uit Canada waarvoor patiënten die een cataractoperatie hadden ondergaan bij één van de vijf ervaren chirurgen uit de kliniek in de periode van juli 2012 tot juli 2015 werden geïncludeerd. Exclusiecriteria waren significante oculaire comorbiditeit die de visus of refractieve uitkomst beïnvloedt. De vergelijking werd gemaakt tussen 1) FLACS (N=995 patiënten, gemiddelde leeftijd 66,8±10,2 jaar) en 2) phaco-emulsificatie (N=883 patiënten, gemiddelde leeftijd 67,1±10,4 jaar). De volgende voor de werkgroep relevante uitkomsten werden gerapporteerd: voorste kapselruptuur en achterste kapselruptuur.
Manning (2016) was een multicenter case-control studie uit Europa waarvoor patiënten die een cataractoperatie hadden ondergaan bij een ervaren chirurg (≥ 50 FLACS operaties uitgevoerd) werden geïncludeerd. Er werd gematcht op pre-operatieve verte-gecorrigeerde visus, leeftijd (< 2 jaar verschil), vergelijkbare hoeveelheid oculaire comorbiditeiten en een vergelijkbaar aantal chirurgische moeilijkheden. De vergelijking werd gemaakt tussen 1) FLACS (N=2814 patiënten, gemiddelde leeftijd 66,4±10,2 jaar) en 2) phaco-emulsificatie (N=4987 patiënten, gemiddelde leeftijd 67,5±9,9 jaar). De volgende voor de werkgroep relevante uitkomsten werden gerapporteerd: voorste en achterste kapselruptuur werden gepresenteerd.
Resultaten
1. Afwijkingen van doelrefractie (4 tot 6 weken na operatie)
Afwijkingen van doelrefractie werden in zeven studies onderzocht. Zes studies rapporteerden de mean absolute error (Filkorn,2012; Krarup, 2019; Mastropasqua, 2014b; Roberts, 2019; Schweitzer, 2020 en Yu, 2015) en één studie rapporteerde de proportie van het aantal ogen waarbij het behaalde sferische equivalent binnen de 0,5 dioptrie uitkwam (Day, 2020). Day (2020) vond op drie maanden geen verschil tussen de FLACS-groep (250/352 ogen,71%) en de reguliere phaco-emulsificatie-groep (224/316,71%). Het gemiddelde verschil in afwijkingen van doelrefractie, in mean absolute error, tussen de FLACS groep en de reguliere phaco-emulsificatie groep was MD= -0,02; 95%BI= (-0,09, 0,06); p=0,67; ntotaal=2206), met een random effect model en een matige heterogeniteit (I2 56%) (figuur 1); geen verschil in afwijkingen van doelfractie tussen beide groepen.
Figuur 1 Uitkomstmaat afwijkingen van doelrefractie (mean absolute error)
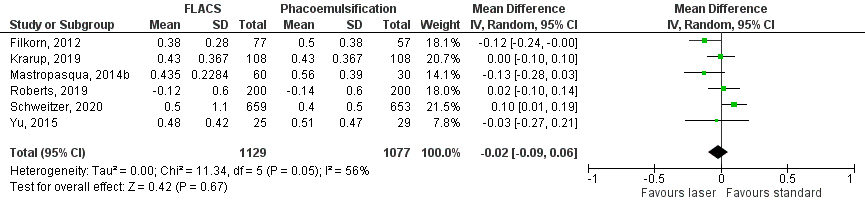
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval; FLACS: femtosecond laser-assisted cataract surgery
2. Verte-gecorrigeerde visus (4 tot 6 weken): 1 tot 3 mo
Verte-gecorrigeerde visus werd in 10 studies onderzocht. Negen studies rapporteerden verte-gecorrigeerde visus uitgedrukt in een gemiddelde op de logMAR schaal (Day, 2020; Filkorn, 2012; Krarup, 2019; Mastropasqua, 2014a, Mastropasqua, 2014b; Schargus, 2015; Schweitzer, 2020; Titiyal, 2016 en Yu, 2015) en één studie rapporteerde het percentage van beide groepen op verschillende Snellen afkapwaarden (Roberts, 2019). Roberts (2019) rapporteerde dat er geen verschil was tussen de FLACS-groep en de reguliere phaco-emulsificatie groep na 1 en na 3 maanden. Het gemiddelde logMAR verschil in verte-gecorrigeerde visus tussen de FLACS-groep en de reguliere phaco-emulsificatie groep was MD= 0,00; 95%BI= (-0,01, 0,01); p=0,85; ntotaal=2781), met een random effect model en een lage heterogeniteit (I2 0%) (figuur 2); geen verschil in verte-gecorrigeerde visus tussen beide groepen.
Figuur 2 Verte-gecorrigeerde visus
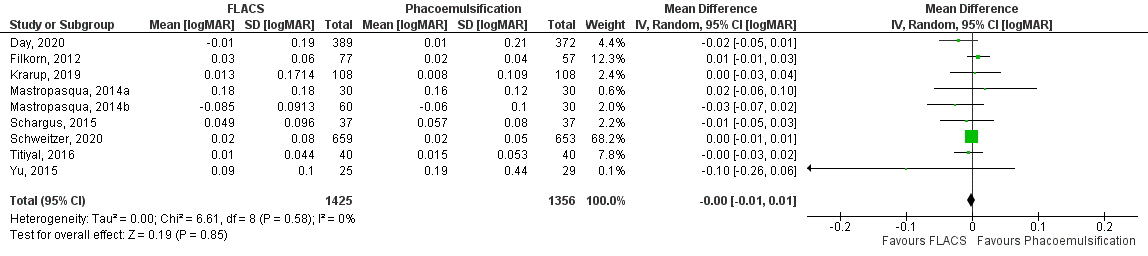
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval; FLACS: femtosecond laser-assisted cataract surgery
3. Aberraties (4 tot 6 weken na operatie)
De uitkomstmaat aberraties werd niet in de meta-analyse van Day (2016) opgenomen. Er werd alleen vermeld dat Mastropasqua (2014a) sferische aberraties onderzocht en Nagy (2014) lage-orde, hoge-orde en totale corneale aberraties onderzocht. Mastropasqua (2014a) rapporteerde dat er geen verschil was in sferische aberraties tussen de groepen postoperatief. Nagy (2014) rapporteerde dat lage orde (p=0,072), hoge-orde (0,078) en totale corneale aberraties (p=0,065) niet significant verschillend waren tussen de groepen postoperatief.
4. Verlies van endotheelcellen (> 3 maanden)
Verlies van endotheelcellen werd in vijf studies onderzocht. In vier studies werd verlies van endotheelcellen uitgedrukt in een verschilscore tussen pre-op en post-op (Conrad-Hengerer, 2013; Day, 2020; Krarup, 2019 en Schargus, 2015). In één studie werden alleen de pre-op en post-op waarden gepresenteerd waardoor de SD van de verschilscore niet berekend kon worden (Schweitzer, 2020). Het gemiddelde verschil in verlies van endotheelcellen tussen de FLACS groep en de reguliere phaco-emulsificatie groep was MD= -52,15; 95%BI= (-161,34;57,04); p=0,35; ntotaal=1197), met een random effect model en een hoge heterogeniteit (I2 71%) (figuur 3); geen verschil in verlies van endotheelcellen tussen beide groepen.
Figuur 3 Uitkomstmaat verlies van endotheelcellen
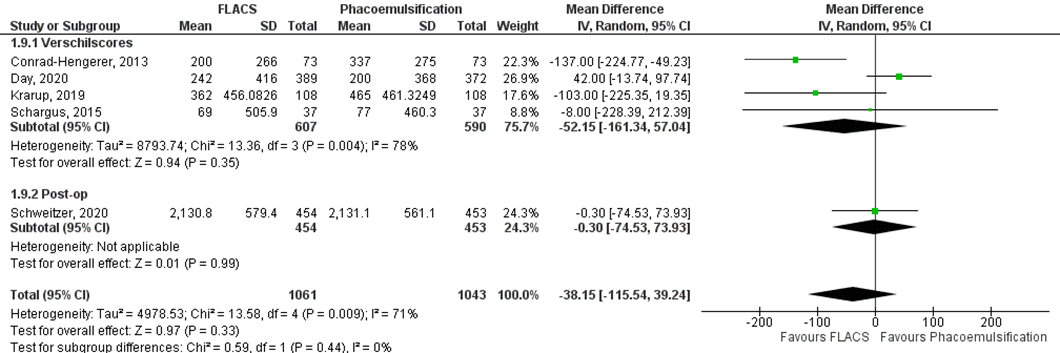
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval; FLACS: femtosecond laser-assisted cataract surgery
5. Voorste kapselruptuur
RCT’s
De hoogste bewijskracht komt voort uit RCT’s. Achterste kapselruptuur werd in 13 RCT’s onderzocht (Conrad-Hengerer, 2013; Conrad-Hengerer, 2014; Conrad-Hengerer, 2015; Day, 2020; Kovacs, 2014; Kranitz, 2012; Krarup, 2019; Nagy, 2011; Nagy, 2014; Reddy, 2013; Schargus, 2015; Schweitzer, 2020 en Yu, 2015). De gepoolde resultaten laten zien dat de incidentie van voorste kapselruptuur 0,67% (11/1636) was in de FLACS groep en 0,41% (7/1703) in de reguliere phaco-emulsificatie groep (figuur 4). Het gemiddelde relatieve risico (RR) van de gepoolde RCT’s voor voorste kapselruptuur in de FLACS groep versus de phaco-emulsificatiegroep was RR: 1,55 (95% BI= (0,61, 3,96); p=0,36; ntotaal=3339), met een random effect model en een lage heterogeniteit (I2 0%). Echter, de RCT’s waren niet gepowered op deze weinig voorkomende complicatie. Daarom is de analyse ook uitgevoerd voor observationeel onderzoek.
Figuur 4 Uitkomstmaat voorste kapselruptuur (alleen RCT’s)
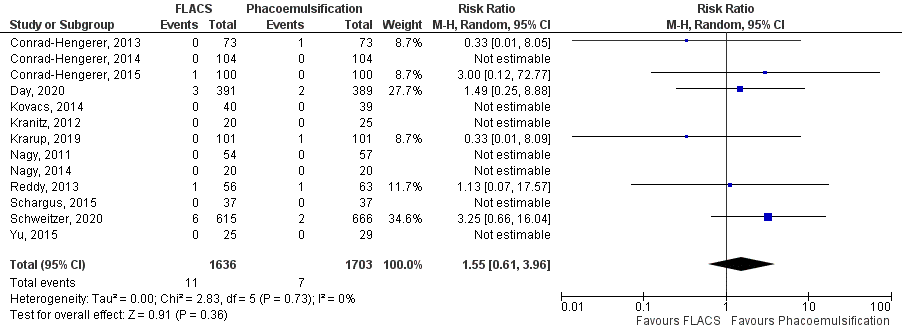
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval; FLACS: femtosecond laser-assisted cataract surgery
Cohorten
Vanwege het feit dat RCT’s niet gepowerd zijn op de weinig voorkomende complicatie voorste kapselruptuur is de uitkomstmaat ook in cohorten onderzocht. Voorste kapselruptuur werd in 6 cohorten onderzocht (Abell, 2015; Ang, 2019; Berk, 2018; Ewe, 2016; Manning, 2016 en Roberts, 2019). De gepoolde resultaten laten zien dat de incidentie van voorste kapselruptuur 1,08% (77/7145) was in de FLACS groep en 0,12% (11/9625) in de reguliere phaco-emulsificatie groep (figuur 5). Het gemiddelde relatieve risico (RR) van de gepoolde cohorten voor voorste kapselruptuur in de FLACS groep versus de phaco-emulsificatiegroep was RR: 5,93 (95% BI= (2,90, 12,13); p<0,00001; ntotaal=16770), met een random effect model en een lage heterogeniteit (I2 17%); minder voorste kapselrupturen in de reguliere phaco-emulsificatie groep. Vanwege het feit dat de complicatie relatief weinig voorkomt is het absolute risicoverschil klein, RD: 0,01 (95% BI=0,00, 0,01); p=0,006.
Figuur 5 Uitkomstmaat voorste kapselruptuur (alleen cohorten)
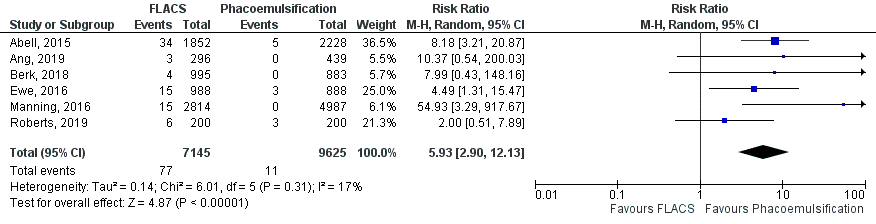
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval; FLACS: femtosecond laser-assisted cataract surgery
Bij observationeel onderzoek kan er sprake zijn van selectiebias waardoor de resultaten beïnvloed worden: met andere woorden, patiënten met een verhoogd risico op een voorste kapselruptuur zouden kunnen zijn toegewezen aan één specifieke groep. De werkgroep geeft aan dat bijvoorbeeld pseudoexfoliatie en trauma in het oog confounders zijn. Voor deze factoren van confounding is niet gecorrigeerd binnen de bovenstaande cohorten. Echter, patiënten met een verhoogd risico op een voorste kapselruptruur werden juist toegewezen aan de phaco-emulsificatie groep. Het effect (meer voorste kapselrupturen) zou dus eerder groter zijn wanneer alle patiënten gerandomiseerd zouden zijn.
6. Achterste kapselruptuur
RCT’s
De hoogste bewijskracht komt voort uit RCT’s. Achterste kapselruptuur werd in 13 RCT’s onderzocht (Conrad-Hengerer, 2013; Conrad-Hengerer, 2014; Conrad-Hengerer, 2015; Day, 2020; Kovacs, 2014; Kranitz, 2012; Krarup, 2019; Nagy, 2011; Nagy, 2014; Reddy, 2013; Schargus, 2015; Schweitzer, 2020 en Yu, 2015). De gepoolde resultaten laten zien dat de incidentie van achterste kapselruptuur 0,58% (10/1736) was in de FLACS groep en 0,81% (14/1725) in de reguliere phaco-emulsificatie groep (figuur 6). Het gemiddelde relatieve risico (RR) van de gepoolde RCT’s voor achterste kapselruptuur in de FLACS groep versus de phaco-emulsificatiegroep was RR: 0,74 (95% BI= (0,34, 1,64); p=0,47; ntotaal=3461), met een random effect model en een lage heterogeniteit (I2 0%). Echter, de RCT’s waren niet gepowered op deze weinig voorkomende complicatie. Daarom is de analyse ook uitgevoerd voor observationeel onderzoek.
Figuur 6 Uitkomstmaat achterste kapselruptuur (alleen RCT’s)
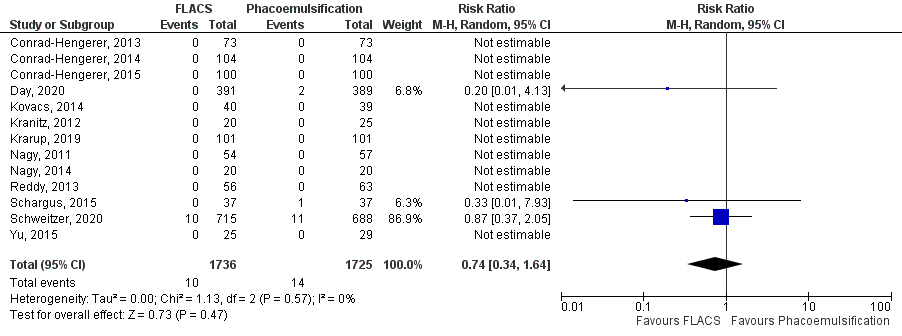
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval; FLACS: femtosecond laser-assisted cataract surgery
Cohorten
Vanwege het feit dat RCT’s niet gepowerd zijn op de weinig voorkomende complicatie achterste kapselruptuur is de uitkomstmaat ook in cohorten onderzocht. Achterste kapselruptuur werd in 10 cohorten onderzocht (Abell, 2015; Ang, 2019; Bali, 2012; Berk, 2018; Chen, 2015; Ewe, 2016; Khandekar, 2015; Manning, 2016; Roberts, 2019 en Titiyal, 2016). De gepoolde resultaten laten zien dat de incidentie van achterste kapselruptuur 0,75% (58/7695) was in de FLACS groep en 0,27% (31/11295) in de reguliere phaco-emulsificatie groep (figuur 7). Het gemiddelde relatieve risico (RR) van de gepoolde cohorten voor achterste kapselruptuur in de FLACS groep versus de phaco-emulsificatiegroep was RR: 2,99 (95% BI= (1,73, 5,17); p=0<0,0001; ntotaal=18990), met een random effect model en een lage heterogeniteit (I2 23%); minder achterste kapselrupturen in de reguliere phaco-emulsificatie groep. Vanwege het feit dat de complicatie relatief weinig voorkomt is het absolute risicoverschil klein, RD: 0,00 (95% BI=0,00, 0,01); p=0,02.
Figuur 7 Uitkomstmaat achterste kapsel ruptuur (alleen cohorten)
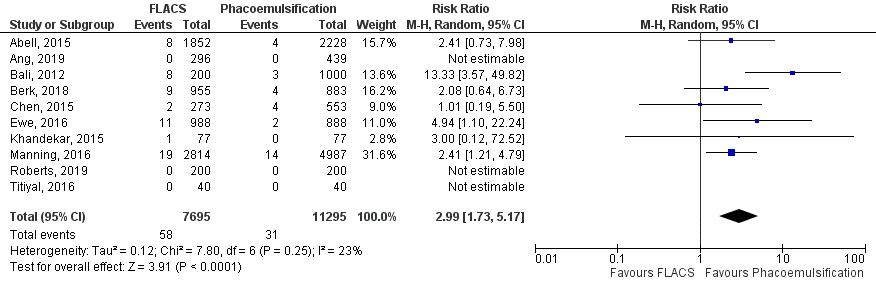
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval; FLACS: femtosecond laser-assisted cataract surgery
Bij observationeel onderzoek kan er sprake zijn van selectiebias waardoor de resultaten beïnvloed worden: met andere woorden, patiënten met een verhoogd risico op een achterste kapselruptuur zouden kunnen zijn toegewezen aan één specifieke groep. De werkgroep geeft aan dat bijvoorbeeld pseudoexfoliatie en trauma in het oog confounders zijn. Voor deze factoren van confounding is niet gecorrigeerd binnen de bovenstaande cohorten. Echter, patiënten met een verhoogd risico op een achterste kapselruptuur werden juist toegewezen aan de phaco-emulsificatie groep. Het effect (meer achterste kapselrupturen) zou dus eerder groter zijn wanneer alle patiënten gerandomiseerd zouden zijn.
7. Postoperatief klinisch significant macula oedeem (6 weken)
Klinisch significant macula oedeem werd in 11 studies onderzocht (Conrad-Hengerer, 2013; Conrad-Hengerer, 2014; Conrad-Hengerer, 2015; Ewe, 2016; Kovacs, 2014; Kranitz, 2012; Nagy, 2011; Nagy, 2014; Schargus, 2015; Schweitzer, 2020 en Yu, 2015). De gepoolde resultaten laten zien dat de incidentie van postoperatief klinisch significant macula oedeem 1,57% (34/2161) was in de FLACS groep en 1,74% (36/2064) in de reguliere phaco-emulsificatie groep (figuur 8). Het gemiddelde relatieve risico (RR) van de gepoolde studies voor postoperatief klinisch significant macula oedeem in de FLACS versus de phaco-emulsificatie groep was RR: 0,88 (95%BI= (0,46, 1,68); p= 0,70; ntotaal =4225), met een random effect model en een lage heterogeniteit (I2 15%); geen verschil in postoperatief klinisch significant macula oedeem tussen beide groepen.
Figuur 8 Uitkomstmaat klinisch significant macula oedeem
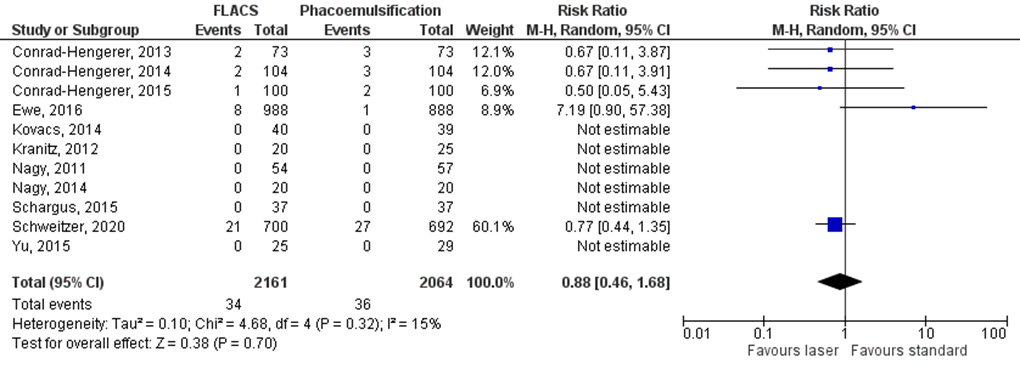
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval; FLACS: femtosecond laser-assisted cataract surgery
Bewijskracht van de literatuur
1. Afwijkingen van doelrefractie (4 tot 6 weken na operatie)
De bewijskracht voor de uitkomstmaat afwijkingen van doelrefractie is met 1 niveau verlaagd vanwege beperkingen in de onderzoeksopzet, waaronder hoge loss to follow-up, onduidelijk of de outcome assessor was geblindeerd en patiënt karakteristieken niet beschreven (-1, risk of bias). Er wordt niet afgetrokken voor inconsistentie, publicatiebias, imprecisie of indirectheid. Vanwege het studiedesign is het startpunt GRADE ‘hoog’, de uiteindelijke bewijskracht komt uit op GRADE ‘redelijk’.
2. Verte-gecorrigeerde visus (4 tot 6 weken): 1 tot 3 mo
De bewijskracht voor de uitkomstmaat verte-gecorrigeerde visus is met 1 niveau verlaagd vanwege beperkingen in de onderzoeksopzet, waaronder hoge loss to follow-up, patiënten en outcome assessor niet geblindeerd en patiënt karakteristieken niet beschreven (-1, risk of bias). Er wordt niet afgetrokken voor inconsistentie, publicatiebias, imprecisie of indirectheid. Vanwege het studiedesign is het startpunt GRADE ‘hoog’, de uiteindelijke bewijskracht komt uit op GRADE ‘redelijk’.
3. Aberraties (4 tot 6 weken na operatie)
De bewijskracht voor de uitkomstmaat aberraties is met 3 niveaus verlaagd vanwege beperkingen in de onderzoeksopzet, waaronder patiënten en outcome assessor niet geblindeerd en onduidelijkheid over de randomisatieprocedure (-1, risk of bias) en het geringe aantal patiënten (-2, imprecisie). Er wordt niet afgetrokken voor inconsistentie, publicatiebias of indirectheid. Vanwege het studiedesign is het startpunt GRADE ‘hoog’, de uiteindelijke bewijskracht komt uit op GRADE ‘zeer laag’.
4. Verlies van endotheelcellen (> 3 maanden)
De bewijskracht voor de uitkomstmaat verlies van endotheelcellen is met 1 niveau verlaagd vanwege beperkingen in de onderzoeksopzet, waaronder hoge loss to follow-up, onduidelijk of de outcome assessor was geblindeerd en patiënt karakteristieken niet beschreven (-1, risk of bias) en vanwege tegenstrijdige resultaten (-1, inconsistentie). Er wordt niet afgetrokken voor publicatiebias, imprecisie of indirectheid. Vanwege het studiedesign is het startpunt GRADE ‘hoog’, de uiteindelijke bewijskracht komt uit op GRADE ‘laag’.
5. Voorste kapselruptuur
Alleen RCT’s
De bewijskracht voor de uitkomstmaat voorste kapsel ruptuur, gebaseerd op alleen RCT’s, is met 2 niveaus verlaagd vanwege beperkingen in de onderzoeksopzet, waaronder hoge loss to follow-up, onduidelijk of de outcome assessor was geblindeerd en patiënt karakteristieken niet beschreven (-1, risk of bias) en het geringe aantal patiënten (-1, imprecisie, RCT’s zijn namelijk niet gepowerd op weinig voorkomende complicaties). Er wordt niet afgetrokken voor inconsistentie, publicatiebias of indirectheid. Vanwege het studiedesign is het startpunt GRADE ‘hoog’, de uiteindelijke bewijskracht komt uit op GRADE ‘laag’.
Alleen cohorten
De bewijskracht voor de uitkomstmaat voorste kapselruptuur, gebaseerd op alleen cohorten, is niet verlaagd voor risk of bias omdat dit al gedisconteerd zit in het starten op een laag niveau bij observationeel onderzoek. Er wordt ook niet afgetrokken voor inconsistentie, publicatiebias, imprecisie of indirectheid. Vanwege het studiedesign (observationeel onderzoek) is het startpunt GRADE ‘laag’, de uiteindelijke bewijskracht komt uit op GRADE ‘laag’.
6. Achterste kapselruptuur
Alleen RCT’s
De bewijskracht voor de uitkomstmaat achterste kapselruptuur, gebaseerd op alleen RCT’s, is met 2 niveaus verlaagd vanwege beperkingen in de onderzoeksopzet, waaronder hoge loss to follow-up, onduidelijk of de outcome assessor was geblindeerd en patiënt karakteristieken niet beschreven (-1, risk of bias) en het gering aantal patiënten (-1, imprecisie, RCT’s zijn namelijk niet gepowerd op weinig voorkomende complicaties). Er wordt niet afgetrokken voor inconsistentie, publicatiebias of indirectheid. Vanwege het studiedesign is het startpunt GRADE ‘hoog’, de uiteindelijke bewijskracht komt uit op GRADE ‘laag’.
Alleen cohorten
De bewijskracht voor de uitkomstmaat achterste kapselruptuur, gebaseerd op alleen cohorten, is niet verlaagd voor risk of bias omdat dit al gedisconteerd zit in het starten op een laag niveau bij observationeel onderzoek. Er wordt ook niet afgetrokken voor inconsistentie, publicatiebias, imprecisie of indirectheid. Vanwege het studiedesign (observationeel onderzoek) is het startpunt GRADE ‘laag’, de uiteindelijke bewijskracht komt uit op GRADE ‘laag’.
7. Postoperatief klinisch significant macula oedeem (6 weken)
De bewijskracht voor de uitkomstmaat postoperatief klinisch significant macula oedeem is niet verlaagd voor risk of bias omdat dit al gedisconteerd zit in het starten op een laag niveau bij observationeel onderzoek. De bewijskracht wordt met 1 niveau verlaagd vanwege de overlap van het betrouwbaarheidsinterval met de grenzen van klinische relevantie. Er wordt niet afgetrokken voor inconsistentie, publicatiebias of indirectheid. Vanwege het studiedesign (observationeel onderzoek) is het startpunt GRADE ‘laag’, de uiteindelijke bewijskracht komt uit op GRADE ‘zeer laag’.
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag:
Wat zijn de voor- en nadelen van femtosecond laser ten opzichte van reguliere phaco-emulsificatie bij cataractchirurgie?
P: patiënten (> 18 jaar) met een indicatie voor cataractchirurgie;
I: femtosecond laser-assisted cataract surgery (FLACS);
C: reguliere phaco-emulsificatie;
O: afwijkingen van doelrefractie, visus, aberraties, hoornvliesendotheelcel verlies, voorste kapselruptuur, achterste kapselruptuur, postoperatief klinisch significant cystoïd macula-oedeem.
Relevante uitkomstmaten
De werkgroep achtte afwijkingen van doelrefractie en visus voor de besluitvorming cruciale uitkomstmaten; aberraties, voorste kapselruptuur, achterste kapselruptuur, postoperatief klinisch significant cystoïd macula oedeem en verlies van endotheelcellen voor de besluitvorming belangrijke uitkomstmaten.
De werkgroep definieerde de uitkomstmaten als volgt: afwijkingen van de doelrefractie: het aantal dioptrieën afwijking van de beoogde refractie of de proportie van het aantal ogen waarbij de behaalde sferische equivalent niet binnen de 0,5 dioptrie of 1,0 dioptrie uitkwam, gemeten minimaal 4 weken na de operatie; visus als best-gecorrigeerde visus uitgedrukt op een logMAR schaal, gemeten minimaal 4 weken na de operatie; de hogere orde aberraties (µm); verlies van endotheelcellen in aantal per mm2, gemeten minimaal 3 maanden na de operatie, minimaal 3 metingen per meetmoment.
Voor kapselrupturen definieerde de werkgroep niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities. Voor postoperatief klinisch significant cystoïd macula oedeem werd gedefinieerd dat er sprake moest zijn van macula oedeem (gedetecteerd middels OCT of FAG) èn een vermindering van de verwachte visus (< 0,2 logMAR dan verwacht) na de cataractoperatie.
De werkgroep definieerde voor afwijkingen van de doelrefractie een verschil van 0,5 dioptrie tussen de groepen als een klinisch (patiënt) relevant verschil. Voor visus een verschil van 0,1 logMAR (1 Snellen lijn) (Kessel, 2016). Voor aberraties en verlies van endotheelcellen is het niet duidelijk wanneer dit als klinisch relevant wordt bevonden, een range van 5 tot 10% zou hiervoor kunnen worden aangehouden. Voor voorste kapselruptuur, achterste kapselruptuur en postoperatief klinisch significant cystoïd macula oedeem werd een risk ratio van < 0,80 en > 1,25 als een klinisch (patiënt-) relevant verschil gezien.
Zoeken en selecteren (Methode)
In de databases Medline (via OVID) en Embase (via Embase.com) is op 6 februari 2020 met relevante zoektermen gezocht naar systematische reviews, gerandomiseerd gecontroleerd onderzoek (RCT’s) en observationeel onderzoek. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 324 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria: systematische review (gezocht in ten minste twee relevante databases, risk of bias beoordeling aanwezig en de resultaten van individuele studies voldoende gepresenteerd) of RCT of observationeel onderzoek waarin een vergelijking is gemaakt tussen femtosecond laser-assisted cataract surgery (FLACS) en reguliere phaco-emulsificatie bij > 200 (100 per arm) patiënten. Daarnaast moest tenminste één van de bovengenoemde uitkomstmaten zijn gerapporteerd. Op basis van titel en abstract werden in eerste instantie 32 studies voorgeselecteerd. Eén artikel werd toegevoegd door snowballing na de searchdatum (Day, 2020). Na raadpleging van de volledige tekst, werden vervolgens 16 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording) en 16 studies definitief geselecteerd. Voor de uitkomstmaten afwijkingen van doelrefractie, visus, aberraties, en verlies van endotheelcellen werden alleen resultaten uit RCT’s geïncludeerd indien deze aanwezig waren omdat RCT’s op een hoge bewijskracht starten. Voor complicaties (voorste kapselruptuur, achterste kapselruptuur en postoperatief klinisch significant cystoïd macula oedeem) werden resultaten uit observationeel onderzoek ook meegenomen vanwege het beperkte aantal cases.
Resultaten
Achtentwintig onderzoeken zijn opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidencetabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk-of-biastabellen.
- Abell, R. G., Darian-Smith, E., Kan, J. B., Allen, P. L., Ewe, S. Y., & Vote, B. J. (2015). Femtosecond laser–assisted cataract surgery versus standard phacoemulsification cataract surgery: outcomes and safety in more than 4000 cases at a single center. Journal of Cataract & Refractive Surgery, 41(1), 47-52.
- Ang, R. E. T., Quinto, M. M. S., Cruz, E. M., Rivera, M. C. R., & Martinez, G. H. A. (2018). Comparison of clinical outcomes between femtosecond laser-assisted versus conventional phacoemulsification. Eye and Vision, 5(1), 8.
- Bali, S. J., Hodge, C., Lawless, M., Roberts, T. V., & Sutton, G. (2012). Early experience with the femtosecond laser for cataract surgery. Ophthalmology, 119(5), 891-899.
- Berk, T. A., Schlenker, M. B., Campos-Möller, X., Pereira, A. M., & Ahmed, I. I. K. (2018). Visual and Refractive Outcomes in Manual versus Femtosecond Laser–Assisted Cataract Surgery: A Single-Center Retrospective Cohort Analysis of 1838 Eyes. Ophthalmology, 125(8), 1172-1180.
- Chee SP, Yang Y, Wong MH. Randomised Controlled Trial comparing Femtosecond Laser-Assisted and Conventional Phacoemulsification on Dense Cataracts. Am J Ophthalmol. 2021 Mar 1:S0002-9394(20)30682-6
- Chen, X., Chen, K., He, J., & Yao, K. (2016). Comparing the curative effects between femtosecond laser-assisted cataract surgery and conventional phacoemulsification surgery: a meta-analysis. PLoS One, 11(3), e0152088.
- Chen, X., Xiao, W., Ye, S., Chen, W., & Liu, Y. (2015). Efficacy and safety of femtosecond laser-assisted cataract surgery versus conventional phacoemulsification for cataract: a meta-analysis of randomized controlled trials. Scientific reports, 5, 13123.
- Conrad-Hengerer, I., Al Juburi, M., Schultz, T., Hengerer, F. H., & Dick, H. B. (2013). Corneal endothelial cell loss and corneal thickness in conventional compared with femtosecond laser–assisted cataract surgery: three-month follow-up. Journal of Cataract & Refractive Surgery, 39(9), 1307-1313.
- Conrad-Hengerer, I., Al Sheikh, M., Hengerer, F. H., Schultz, T., & Dick, H. B. (2015). Comparison of visual recovery and refractive stability between femtosecond laser–assisted cataract surgery and standard phacoemulsification: six-month follow-up. Journal of Cataract & Refractive Surgery, 41(7), 1356-1364.
- Conrad-Hengerer, I., Hengerer, F. H., Al Juburi, M., Schultz, T., & Dick, H. B. (2014). Femtosecond laser-induced macular changes and anterior segment inflammation in cataract surgery. Journal of refractive surgery, 30(4), 222-226.
- Day, A. C., Burr, J. M., Bennett, K., Bunce, C., Doré, C. J., Rubin, G. S.,... & FACT trial group. (2020). Femtosecond laser-assisted cataract surgery compared with phacoemulsification cataract surgery (FACT): a randomised non-inferiority trial. Ophthalmology. (Day, 2020a)
- Day, A. C., Burr, J. M., Bennett, K., Doré, C. J., Bunce, C., Hunter, R.,... & Wilkins, M. R. (2020). Femtosecond laser-assisted cataract surgery compared with phacoemulsification cataract surgery (FACT): a randomised non-inferiority trial, 1 year outcomes. Journal of Cataract & Refractive Surgery. (Day, 2020b)
- Day, A. C., Gore, D. M., Bunce, C., & Evans, J. R. (2016). Laser‐assisted cataract surgery versus standard ultrasound phacoemulsification cataract surgery. Cochrane Database of Systematic Reviews, (7).
- Ewe, S. Y., Abell, R. G., Oakley, C. L., Lim, C. H., Allen, P. L., McPherson, Z. E.,... & Vote, B. J. (2016). A comparative cohort study of visual outcomes in femtosecond laser-assisted versus phacoemulsification cataract surgery. Ophthalmology, 123(1), 178-182.
- Fan W, Yan H, Zhang G. Femtosecond laser-assisted cataract surgery in Fuchs endothelial corneal dystrophy: Long-term outcomes. J Cataract Refract Surg. 2018 Jul;44(7):864-870.
- Filkorn, T., Kovács, I., Takács, Á., Horváth, É., Knorz, M. C., & Nagy, Z. Z. (2012). Comparison of IOL power calculation and refractive outcome after laser refractive cataract surgery with a femtosecond laser versus conventional phacoemulsification. Journal of refractive surgery, 28(8), 540-544.
- Gerten G., Schultz M., Oberheide U. Treating capsule contraction syndrome with a femtosecond laser. J Cataract Refract Surg. 2016;42:1255–1261.
- Ibarz M., Rodriguez-Prats J.L. Femtosecond laser assisted capsulotomy for treatment of bilateral anterior capsule contraction. J Cataract Refract Surg. 2017;43:289–292.
- Kessel, L., Andresen, J., Tendal, B., Erngaard, D., Flesner, P., & Hjortdal, J. (2016). Toric intraocular lenses in the correction of astigmatism during cataract surgery: a systematic review and meta-analysis. Ophthalmology, 123(2), 275-286.
- Khandekar, R., Behrens, A., Towerki, A. E. A., May, W., Motowa, S., Tailor, K., & Souru, C. (2015). Determinants of visual outcomes in femtosecond laser assisted cataract surgery and phacoemulsification: a nested case control study. Middle East African journal of ophthalmology, 22(3), 356.
- Kovács, I., Kránitz, K., Sándor, G. L., Knorz, M. C., Donnenfeld, E. D., Nuijts, R. M., & Nagy, Z. Z. (2014). The effect of femtosecond laser capsulotomy on the development of posterior capsule opacification. Journal of refractive surgery, 30(3), 154-158.
- Kránitz, K., Miháltz, K., Sándor, G. L., Takacs, A., Knorz, M. C., & Nagy, Z. Z. (2012). Intraocular lens tilt and decentration measured by Scheimpflug camera following manual or femtosecond laser–created continuous circular capsulotomy. Journal of Refractive Surgery, 28(4), 259-263.
- Krarup, T., Ejstrup, R., Mortensen, A., La Cour, M., & Holm, L. M. (2019). Comparison of refractive predictability and endothelial cell loss in femtosecond laser-assisted cataract surgery and conventional phaco surgery: prospective randomised trial with 6 months of follow-up. BMJ Open Ophthalmology, 4(1), e000233.
- Krarup, T., Morten Holm, L., la Cour, M., & Kjaerbo, H. (2014). Endothelial cell loss and refractive predictability in femtosecond laser‐assisted cataract surgery compared with conventional cataract surgery. Acta ophthalmologica, 92(7), 617-622.
- Manning, S., Barry, P., Henry, Y., Rosen, P., Stenevi, U., Young, D., & Lundström, M. (2016). Femtosecond laser–assisted cataract surgery versus standard phacoemulsification cataract surgery: study from the European Registry of Quality Outcomes for Cataract and Refractive Surgery. Journal of Cataract & Refractive Surgery, 42(12), 1779-1790.
- Mastropasqua, L., Toto, L., Mastropasqua, A., Vecchiarino, L., Mastropasqua, R., Pedrotti, E., & Di Nicola, M. (2014). Femtosecond laser versus manual clear corneal incision in cataract surgery. Journal of refractive surgery, 30(1), 27-33. (Mastropasqua, 2014a).
- Mastropasqua, L., Toto, L., Mattei, P. A., Vecchiarino, L., Mastropasqua, A., Navarra, R.,... & Nubile, M. (2014). Optical coherence tomography and 3-dimensional confocal structured imaging system–guided femtosecond laser capsulotomy versus manual continuous curvilinear capsulorhexis. Journal of Cataract & Refractive Surgery, 40(12), 2035-2043. (Mastropasqua, 2014b).
- Mencucci R, De Vitto C, Cennamo M, Vignapiano R, Buzzi M, Favuzza E. Femtosecond laser-assisted cataract surgery in eyes with shallow anterior chamber depth: comparison with conventional phacoemulsification. J Cataract Refract Surg. 2020 Dec;46(12):1604-1610.
- Nagy, Z. Z., Dunai, Á., Kránitz, K., Takács, Á. I., Sándor, G. L., Hécz, R., & Knorz, M. C. (2014). Evaluation of femtosecond laser-assisted and manual clear corneal incisions and their effect on surgically induced astigmatism and higher-order aberrations. Journal of Refractive Surgery, 30(8), 522-525.
- Nagy, Z. Z., Kránitz, K., Takacs, A. I., Miháltz, K., Kovács, I., & Knorz, M. C. (2011). Comparison of intraocular lens decentration parameters after femtosecond and manual capsulotomies. Journal of refractive surgery, 27(8), 564-569.
- Popovic, M., Campos-Möller, X., Schlenker, M. B., & Ahmed, I. I. K. (2016). Efficacy and safety of femtosecond laser-assisted cataract surgery compared with manual cataract surgery: a meta-analysis of 14 567 eyes. Ophthalmology, 123(10), 2113-2126.
- Recalde PL, Larco C, Torres D, Larco P Jr. Femtosecond laser assisted capsulotomy in the treatment of capsule contraction case report. Am J Ophthalmol Case Rep. 2020 Aug 23;20:100893.
- Reddy, K. P., Kandulla, J., & Auffarth, G. U. (2013). Effectiveness and safety of femtosecond laser–assisted lens fragmentation and anterior capsulotomy versus the manual technique in cataract surgery. Journal of Cataract & Refractive Surgery, 39(9), 1297-1306.
- Roberts, H. W., Wagh, V. K., Sullivan, D. L., Hidzheva, P., Detesan, D. I., Heemraz, B. S.,... & O'Brart, D. P. (2019). A randomized controlled trial comparing femtosecond laser–assisted cataract surgery versus conventional phacoemulsification surgery. Journal of Cataract & Refractive Surgery, 45(1), 11-20.
- Schargus, M., Suckert, N., Schultz, T., Kakkassery, V., & Dick, H. B. (2015). Femtosecond laser-assisted cataract surgery without OVD: a prospective intraindividual comparison. Journal of Refractive Surgery, 31(3), 146-152.
- Schweitzer, C., Brezin, A., Cochener, B., Monnet, D., Germain, C., Roseng, S.,... & Pisella, P. J. (2020). Femtosecond laser-assisted versus phacoemulsification cataract surgery (FEMCAT): a multicentre participant-masked randomised superiority and cost-effectiveness trial. The Lancet, 395(10219), 212-224.
- Titiyal, J. S., Kaur, M., Singh, A., Arora, T., & Sharma, N. (2016). Comparative evaluation of femtosecond laser-assisted cataract surgery and conventional phacoemulsification in white cataract. Clinical Ophthalmology (Auckland, NZ), 10, 1357.
- Vasavada VA, Vasavada S, Vasavada AR, Vasavada V, Srivastava S. Comparative evaluation of femtosecond laser-assisted cataract surgery and conventional phacoemulsification in eyes with a shallow anterior chamber. J Cataract Refract Surg. 2019 May;45(5):547-552.
- Wang, J., Su, F., Wang, Y., Chen, Y., Chen, Q., & Li, F. (2019). Intra and post-operative complications observed with femtosecond laser-assisted cataract surgery versus conventional phacoemulsification surgery: a systematic review and meta-analysis. BMC ophthalmology, 19(1), 1-8.
- Yong WWD, Chai HC, Shen L, Manotosh R, Anna Tan WT. Comparing Outcomes of Phacoemulsification With Femtosecond Laser-Assisted Cataract Surgery in Patients With Fuchs Endothelial Dystrophy. Am J Ophthalmol. 2018 Dec;196:173-180.
- Yu, A. Y., Ni, L. Y., Wang, Q. M., Huang, F., Zhu, S. Q., Zheng, L. Y., & Su, Y. F. (2015). Preliminary clinical investigation of cataract surgery with a noncontact femtosecond laser system. Lasers in surgery and medicine, 47(9), 698-703.
- Zhu DC, Shah P, Feuer WJ, Shi W, Koo EH. Outcomes of conventional phacoemulsification versus femtosecond laser-assisted cataract surgery in eyes with Fuchs endothelial corneal dystrophy. J Cataract Refract Surg. 2018 May;44(5):534-540.
- Zhu, Y., Chen, X., Chen, P., Xu, W., Shentu, X., Yu, Y., & Yao, K. (2019). Lens capsule-related complications of femtosecond laser–assisted capsulotomy versus manual capsulorhexis for white cataracts. Journal of Cataract & Refractive Surgery, 45(3), 337-342.
Risk of bias tabel
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Day, 2016 |
Yes |
Yes |
Yes |
Yes |
No |
Yes |
Yes |
Yes |
Yes |
|
Popovitch, 2016 |
yes |
yes |
yes |
yes |
No |
yes |
Yes |
Yes |
Yes |
|
Wang, 2019 |
yes |
Yes, no date reported |
Yes but limited |
Yes, but limited |
No |
Yes |
Yes |
Yes |
No, not of individual studies |
|
Chen, 2016 |
Yes |
Yes |
Yes |
Yes |
No |
Yes |
Yes |
Yes |
No, not of individual studies |
|
Study reference
(first author, publication year) |
Describe method of randomisation1 |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome accessors to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Schweitzer, 2020 |
Permuted-block randomisation (block size of 2 or 4 for unilateral cases and 2 or 6 for bilateral cases, allocation 1:1) stratified on centres and type of cataract surgery (unilateral or bilateral) was done within the 5 days before surgery with a centralised web-based system |
A research assistant generated the randomisation sequence and patients were automatically allocated by the software. |
Unlikely
Participants were masked to the surgical treatment allocation until the last follow-up visit at 12 months after surgery, and a sham laser procedure was set up in the operating room for participants randomly assigned to the PCS arm. |
Unlikely
All medical and non-medical staff involved in the study were specifically trained in the participant randomisation and masking processes from the screening visit up to the last follow-up visit, including on the day of surgery in the operating room in the ambulatory surgery setting. |
Unlikely
All outcome assessors and the trained technicians who examined patients were also masked to the surgical treatment allocation |
unlikely
No difference score presented for endothelial cell loss |
unlikely
Loss to FU in 10%, equal in both groups |
Unlikely
modified intention-to-treat (mITT; primary analysis) and as-treated (secondary) analyses.
NOTE: pt number differ between outcome measures…
|
|
Day, 2020 |
PCS. Randomization was performed on the day of surgery using a web-based, online, sealed envelopebased system that used treatment center, surgeon, and 1 or both eyes eligible as minimization stratifiers. |
Unlikely |
Likely
Because of the nature of the intervention, surgeon and participant masking were not possible. |
Unlikely
Because of the nature of the intervention, surgeon and participant masking were not possible. |
Unlikely
All trial follow-ups were performed by an optometrist masked to the trial intervention. |
Unlikely |
Likely, Loss to FU (19.4%) in Intervention vs 9.9% in controlgroup |
All primary and secondary analyses were conducted following the intention-to-treat principle retaining patients in the group to which they were randomly allocated irrespective of the treatment received. |
|
Krarup, 2019 |
Randomisations were block randomisations performed by one clinician (TK) blinded from the operating order of the eyes. All randomisations were noted on a randomisation sheet. On surgery day, the surgeon would open the randomisation sheet and see what operation had to be performed. The other eye would receive the treatment not given to the randomised eye |
Unlikely |
Likely |
Unlikely |
Unlikely; blinded observer (as validation studies suggest), and blinded optometrist refraction performed at day 40 and day 180, as well as the use of the patients as their own control: |
Likely, no pt characteristics reported |
Unlikely |
No ITT analyses, pt with one eye operated |
|
Study reference
(first author, year of publication) |
Bias due to a non-representative or ill-defined sample of patients?1
(unlikely/likely/unclear) |
Bias due to insufficiently long, or incomplete follow-up, or differences in follow-up between treatment groups?2
(unlikely/likely/unclear) |
Bias due to ill-defined or inadequately measured outcome ?3
(unlikely/likely/unclear) |
Bias due to inadequate adjustment for all important prognostic factors?4
(unlikely/likely/unclear) |
|
Manning, 2016 |
Unlikely |
Unlikely |
Unlikely |
Unlikely |
|
Berk, 2018 |
Unlikely |
Unlikely |
Unlikely |
Unlikely |
|
Zhu, 2019 |
Unlikely |
Unlikely |
Unlikely |
Unlikely |
|
Ang, 2018 |
Unlikely |
Unlikely |
Unlikely |
Unlikely |
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Abell, 2013 |
Ook in Popovic, case-control studie. Outcomes niet beschreven of geen cases |
|
Abell, 2013 |
Prospectief cohort: complicaties niet beschreven of geen cases |
|
Abell, 2014 |
Case-series |
|
Ali, 2017 |
Systematische review, voldoet aan PICO maar includeert geen andere vergelijkende studies met >65 pt per arm dan Chen, 2016; Day, 2016; Popovic, 2016 of Wang, 2019 |
|
Chen, 2015 |
Systematische review, in Popovic, voldoet aan PICO maar includeert geen andere vergelijkende studies met >65 pt per arm dan Chen, 2016; Day, 2016; Popovic, 2016 of Wang, 2019 |
|
Dzhaber, 2020 |
RCT < 100 ogen per arm (67/67) |
|
Hida, 2017 |
RCT, outcomes: Alleen endotheel cell verlies gemeten maar geen getallen vermeld. |
|
Ibrahim, 2018 |
PICO voldoet niet. Outcomes niet beschreven |
|
Levitz, 2015 |
Letter to the editor |
|
Lundstrom, 2017 |
Case-series |
|
Ranjini, 2017 |
Case-control, geen specificatie van complicaties beschreven |
|
Shao, 2018 |
PICO voldoet niet, outcomes alleen op droge ogen |
|
Qian, 2016 |
Systematische review, voldoet aan PICO maar includeert geen andere vergelijkende studies met >65 pt per arm dan Chen, 2016; Day, 2016; Popovic, 2016 of Wang, 2019 |
|
Ye, 2017 |
Systematische review, voldoet aan PICO maar includeert geen andere vergelijkende studies met >65 pt per arm dan Chen, 2016; Day, 2016; Popovic, 2016 of Wang, 2019 |
|
Yesilirmak, 2018 |
Prospectief cohort, vergelijking cornea attendings en fellows |
|
Yu, 2016 |
Prospectief cohort, kleine groepen |
Beoordelingsdatum en geldigheid
Publicatiedatum : 15-12-2021
Beoordeeld op geldigheid : 09-11-2021
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Doel en doelgroep
Doel
Een richtlijn is in wezen de beschrijving van de actuele stand van de kennis, technieken en gerelateerde zaken rond het onderwerp van de richtlijn. Daarnaast heeft een richtlijn tot doel de beroepsbeoefenaars aanbevelingen te geven die de kwaliteit van hun werk mede op het gewenste niveau kunnen houden. Er is dus ook sprake van een beschrijving van kwalitatieve normen voor de beroepsgroep. Iedere arts is gehouden om primair te handelen in het belang van de patiënten daarbij zorg te dragen voor diens veiligheid in relatie tot het medische handelen. De Richtlijn Cataract stelt dan ook normen vast voor goede praktijkvoering, stelt standaarden voor patiëntenzorg en veiligheid en biedt een referentiepunt voor de beoordeling van de resultaten waaraan cataractchirurgie van hoge kwaliteit moet voldoen. De aanbevelingen, normen en standaarden zijn getoetst aan de resultaten van gedegen wetenschappelijk onderzoek, gepubliceerd in de wetenschappelijke literatuur. Indien zekere vraagstellingen niet goed beantwoord konden worden op basis van literatuuronderzoek, werden de meningen van erkende experts gehoord door de richtlijnwerkgroep en bij consensus verwerkt in de aanbevelingen.
Doelgroep
Deze richtlijn is geschreven voor met name oogartsen maar ook andere leden van de beroepsgroepen die direct betrokken zijn bij de zorg met cataract.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2018 een werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met cataract.
Werkgroep
- Drs. B.A.E. (Bert) van der Pol, oogarts niet praktiserend, (voorzitter) NOG
- Dr. M.C. (Marjolijn) Bartels, oogarts, Deventer Ziekenhuis, NOG
- Drs. M.M.M.J. (Margot) Dellaert, oogarts, Treant Zorggroep, NOG
- Drs. Y.P. (Ype) Henry, oogarts, VU medisch centrum, NOG
- Dr. L.V. (Long) Ly, oogarts, Bergman Clinics, NOG
- Drs. R.C.M. (Marit) Maatman, oogarts, Alrijne Ziekenhuis, NOG
- Dr. N.J. (Nic) Reus, oogarts, Amphia Ziekenhuis, NOG
- Dr. N. (Nienke) Visser, oogarts, Maastricht Universitair Medisch Centrum, NOG
- Prof. Dr. R.M.M.A. (Rudy) Nuijts, oogarts, Maastricht Universitair Medisch Centrum, NOG
Met ondersteuning van
- Dr. A.C.J. (Astrid) Balemans, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. J. (Josefien) Buddeke, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- M. (Mitchel) Griekspoor MSc, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Klankbordgroep
- H.J. (Anneke) Jansen Molenaar, Adviseur Oogzorg bij de Oogvereniging
- D. (Dana) Kamsteeg-Koerts, Optometrist, Oogziekenhuis Rotterdam
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenwerkzaamheden |
Gemelde belangen |
Actie |
|
Van der Pol |
Niet praktiserend |
Geen |
Geen |
Geen actie |
|
Dellaert |
Oogarts |
Medisch manager, onkostenvergoeding |
Geen |
Geen actie |
|
Bartels |
Zelfstandig ondernemer, via B.V. verbonden aan Verenigde Specialisten Deventer en zo aan Deventer Ziekenhuis |
Voorzitter subcommissie Richtlijnen NOG |
Deelname aan ZonMw studie IBSCS / DBSCS via UMC Maastricht (site - investigator)
Contactpersoon namens cornea werkgroep bij hoornvliespatiënten vereniging.
|
Geen trekker van de modules over ontstekings- en infectieprofylaxe bij reguliere cataractchirurgie. |
|
Henry |
Oogarts; staflid
|
Lid van de steering group van EUREQUO (ESCRS); Secretaris van NIOIC (NOG); Voorzitter van WTO (NOG) |
Geen |
Geen actie |
|
Ly |
Oogarts bij Bergman Clinics |
Geen |
Geen |
Geen actie |
|
Maatman |
Oogarts, Alrijne Ziekenhuis
|
NOG bestuur (secretaris), betaald. Tot 2016/2017 advies Bayer / Eylea, betaald
|
Geen |
Geen trekker module ontstekingsprofylaxe reguliere cataractchirurgie. |
|
Reus |
Oogarts in het Amphia Ziekenhuis, Breda/Oosterhout
|
Bestuurslid Nederlandse Intraoculaire Implant Club (NIOIC) (onbetaald) Bestuurslid European Society of Cataract and Refractive Surgeons (ESCRS) (onbetaald)
|
Bestuurslid Nederlandse Intraoculaire Implant Club (NIOIC) (onbetaald)
1.Principal Investigator van Investigator-Initiated Trial waarvoor subsidie van Alcon (unresticted grant). Het onderwerp is de helderheid van ogen na een staaroperatie. Er wordt onderzoek gedaan naar de hoeveelheid lichtverstrooiing in de ogen na een cataractoperatie en redenen waarom er meer strooilicht in het oog overblijft na een cataractoperatie dan wordt verwacht. 2.Site-Investigator van studie naar bilaterale cataractchirurgie geïnitieerd door prof. R. Nuijts, oogarts (Universiteitskliniek voor Oogheelkunde Maastricht) waarvoor subsidie van ZonMW (unresticted grant). |
Geen trekker van modules met betrekking tot infectieprofylaxe bij reguliere cataractchirurgie en IOLs. |
|
Visser |
Oogarts, aandachtsgebieden cornea- en cataract chirurgie. Werkgever: University Eye Clinic Maastricht, MUMC+
|
Young ophthalmology committee ESCRS (onbetaald)
|
EPICAT study: Effectiveness of Periocular drug Injection in CATaract surgery (gefinancierd door ESCRS, het gaat hierbij om een restricted grant, de ESCRS heeft op voorhand akkoord gegeven voor de specifieke opzet, uitvoering, en terugkoppeling van de EPICAT studie) |
Geen actie |
|
Nuijts |
Prof.dr. RMMA Nuijts, hoogleraar Corneatransplantatie en Refractiechirurgie; MUMC Maastricht
|
- Voorzitter Nederlandse IntraOculaire Implant Club, NIOIC (onbetaald) |
Abbott: NL 56878.068.16/METC162029 A randomised, subject-masked evaluation of visual function after bilateral implantation of two types of presbyopia-correcting IOLs: the Symfony-study. Period: 01-12-2016 - 01-12-2018
Alcon: VERION versus conventional, manual ink-marking in toric IOL implantation. Period: 2015 - 2016
Alcon: ILJ466-P003 Post-Market Investigation of the Clareon IOL. Period: 2018 - 2028
Alcon: The ACRYSOF IQ PanOptix Presbyopia Correcting intraocular lens (IOL) Model TFNT00. Period: 01-12-2015 - 01-12-2017
CHIESI: NL 54419.000.15/CCMO15.0538 Multinational, multicentre, prospective, open-label, uncontrolled clinical trial to assess the efficacy and safety of Autologous Cultivated Limbal Stem Cells Transplantation (ACLSCT) for restoration of corneal epithelium in patients with limbal stem cell deficiency due to ocular burns. Period: 01-12-2016 - 01-12-2018
ESCRS: European Cornea and Cell Transplantation Registry (ECCTR), European Union Third Health Programme 2014-2020 and the European Society of Cataract and Refractive Surgeons. Period: 01-04-2016 - 2019
ESCRS: The ESCRS PREMED study: PREvention of Macular EDema after cataract surgery. Period: 2012 - 2016
InSciTE: EyeScite: smart biomedical solutions for better eyesight. |
Geen trekker van de modules met betrekking tot infectie- en onstekingsprofylaxe en IOLs bij reguliere cataractchirurgie. |
|
Kamsteeg-Koerts (klankbordgroep) |
Optometrist, Oogziekenhuis Rotterdam |
- Per 25 november 2019 lid OVN ledenraad met een aanstelling voor 3 jaar - Lid OVN commissie Beroepsbelangen |
Geen
|
Geen actie |
|
Jansen-Molenaar |
Adviseur Oogzorg bij de Oogvereniging |
Geen |
Geen |
Geen actie |
Inbreng patiëntenperspectief
Een afgevaardigde van de Oogvereniging nam zitting in de klankbordgroep. Daarnaast werden de Oogvereniging en de Patiëntenfederatie uitgenodigd om deel te nemen aan de schriftelijke knelpuntenanalyse. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de betrokken patiëntenverenigingen en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Methode ontwikkeling
Evidence based
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten met cataract. De werkgroep beoordeelde de aanbeveling(en) uit de eerdere richtlijnmodule cataract (2013) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door het Nederlands Oogheelkundig Gezelschap (NOG), de Nederlandse Vereniging voor Klinische Geriatrie (NVKG), het Nederlands Huisartsen Genootschap (NHG), de Oogvereniging, Verenso en de Landelijke Vereniging van Operatieassistenten (LVO) via een schriftelijke knelpuntenanalyse. Een verslag hiervan is opgenomen in de bijlagen.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming) en belangrijk (maar niet cruciaal). Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur en de beoordeling van de risk-of-bias van de individuele studies is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet een-op-een vergelijkbaar met het minimale klinisch relevante verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden die meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello, 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs, de belangrijkste overwegingen en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE-gradering HOOG) zal niet altijd van toepassing zijn onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Algemene informatie
|
Richtlijn: Cataract |
|
|
Uitgangsvraag: Is er een meerwaarde van de femtosecond laser boven reguliere phaco-emulsificatie bij cataractchirurgie? |
|
|
Database(s): Medline, Embase |
Datum: 06-02-2020 |
|
Periode: vanaf 2010 |
Talen: Engels |
|
Literatuurspecialist: Miriam van der Maten |
|
|
Toelichting en opmerkingen: Voor deze uitgangsvraag is gezocht op de P (cataract), de I (femtosecond laser) en de C (conventional cataract surgery). Op deze manier worden studies gevonden die beide opties bij patiënten met cataract met elkaar vergelijken. Alle opgegeven sleutel artikelen worden gevonden met de zoekopdracht. |
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SRs |
9 |
18 |
15 |
|
RCTs |
157 |
80 |
165 |
|
Observationele studies |
106 |
165 |
144 |
|
Totaal |
272 |
263 |
324 |
|
Database |
Zoektermen |
|
Embase
|
#11 #8 OR #9 OR #10 272 #10 #4 AND #7 NOT (#8 OR #9) 106 #9 #4 AND #6 NOT #8 157 #8 #4 AND #5 9 #7 'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) 5121860 #6 'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti 2978900 #5 'meta analysis'/de OR cochrane:ab OR embase:ab OR psycinfo:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de 480880 #4 #1 AND #2 AND #3 AND [english]/lim AND [2010-2020]/py NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) 485 #3 'cataract extraction'/exp OR 'pseudophakia'/exp OR catarectom*:ti,ab,kw OR capsulorhexis:ti,ab,kw OR phacoemulsification:ti,ab,kw OR phakoemulsification:ti,ab,kw OR 'phaco emulsification':ti,ab,kw OR 'phako emulsification':ti,ab,kw OR 'lens emulsification':ti,ab,kw OR pseudo*phaki*:ti,ab,kw 53722 #2 'ophthalmic femtosecond laser'/exp OR femtosecond:ti,ab,kw OR flacs:ti,ab,kw OR 'laser cataract surgery':ti,ab,kw 10347 #1 'cataract'/exp OR cataract*:ti,ab,kw OR ((lens* NEAR/2 (opacit* OR clouding)):ti,ab,kw) OR (('posterior capsule' NEAR/2 opacification):ti,ab,kw) 91050 |
|
Medline (OVID)
|
1 exp Cataract/ or cataract*.ti,ab,kf. or (lens* adj2 (opacit* or clouding)).ti,ab,kf. or ('posterior capsule' adj2 opacification).ti,ab,kf. (63028) 2 (femtosecond or flacs or 'laser cataract surgery').ti,ab,kf. (15753) 3 exp Cataract Extraction/ or exp Pseudophakia/ or catarectom*.ti,ab,kf. or capsulorhexis.ti,ab,kf. or phacoemulsification.ti,ab,kf. or phakoemulsification.ti,ab,kf. or phaco-emulsification.ti,ab,kf. or phako-emulsification.ti,ab,kf. or 'lens emulsification'.ti,ab,kf. or pseudo*phaki*.ti,ab,kf. (38021) 4 1 and 2 and 3 (539) 5 limit 4 to (english language and yr="2010 -Current") (481) 6 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (431143) 7 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1945815) 8 Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or (cohort adj (study or studies)).tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ [Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies] (3359717) 9 5 and 6 (18) 10 (5 and 7) not 9 (80) 11 (5 and 8) not (9 or 10) (165) 12 9 or 10 or 11 (263) |
