Indicatiestelling voor BCD
Uitgangsvraag
Met welke indicatie kan een patiënt een goede kandidaat voor een BCD zijn?
Aanbeveling
Zorg voor het stellen van een juiste indicatie voor een BCD en doe dit in samenwerking met, in elk geval onder supervisie van, de klinisch fysicus-audioloog (KFA) en de KNO-arts.
Bespreek met de patiënt dat het plaatsen van een BCD een veilige en kortdurende operatieve ingreep is met een minimale kans op complicaties.
Overwegingen
Totstandkoming van de aanbevelingen
Per module is de beschikbare wetenschappelijke literatuur systematisch in kaart gebracht. Deze literatuur is samengevat en beoordeeld volgens het Grades of Recommendation Assessment, Development and Evaluation (GRADE) systeem (zie tabblad Verantwoording).
Behandeling met een BCD is een relatief zeldzame ingreep die ook wordt toegepast bij een kwetsbare patiëntenpopulatie (verstandelijk beperkten, ouderen, kinderen). Om deze reden zijn grote, gerandomiseerde interventiestudies in deze setting praktisch niet haalbaar en zijn de conclusies in de module ‘Indicatiestelling voor BCD’ niet gegradeerd. Soms wordt de behandeling toegepast als er (grote) communicatieve nood is en er géén alternatieven zijn, de conventioneel indicatie. Gezien de objectiviteit van de metingen en duidelijke verschillen tussen het horen mét en zonder hulp van BCD is het toch mogelijk om sterke aanbevelingen te doen. Dit wordt onderbouwd in de overwegingen.
Indicatie overstijgende factoren
Aangezien een BCD voor langere termijn gedragen wordt, via een operatief geplaatst implantaat, zijn ook de hiermee samenhangende factoren meegenomen. Denk hierbij aan de stabiliteit, veiligheid en risico’s. Aangezien deze factoren implantaat specifiek en niet indicatie specifiek zijn, worden deze in de algemene inleiding kort nader beschreven. De operatietechniek gerelateerde factoren komen in de module ‘Operatietechnieken BCD bij volwassenen’ nader aan de orde. Ook wordt in de module ‘Informatieverstrekking aan de patiënt bij BCD’ de informatie relevant voor de patiënt in het voorlichtingsgesprek nader gespecificeerd. Indien deze factoren relevant zijn in de afweging van diverse alternatieven bij een specifiek type gehoorverlies, worden deze waar mogelijk gewogen ten opzichte van de meerwaarde voor die groep.
Stabiliteit - implantaat verlies
Huidige generatie implants en abutments geven minder en met name minder ernstige huidreacties en hebben een lager percentage implantaat verlies. De langste beschreven follow-up duur van dit type implantaten is 5 jaar. Concluderend is met de huidige generatie implantaten, abutments en chirurgische techniek in een gezonde volwassen populatie te spreken van implantaat verlies van 3 tot 4% (den Besten, 2015). Voor meer details hieromtrent zie de module ‘Operatietechniek BCD bij volwassenen’.
Veiligheid
Huidcomplicaties direct na BCD-operaties zijn relatief zeldzaam; Deze omvatten over het algemeen aanhoudende bloeding of hematoomvorming, onvoldoende wondgenezing, persisterende pijn of huiddehiscentie. De eerder beschreven necrose van het vroeger gebruikte huidtransplantaat (Tjellström, 2006; Shirazi, 2006; Wazen, 2011) komt tegenwoordig zelden meer voor. De lineaire incisie techniek verminderde niet alleen deze huidnecrose maar vooral ook overige huidreacties (De Wolf, 2008).
De huidreacties zijn een punt van aandacht. De plaats waar het percutane abutment de huid doorkruist, blijft een mogelijke ingang voor micro-organismen, die ontsteking kunnen veroorzaken. De (tot op heden) meest gebruikte manier om de ernst hiervan te classificeren is de Holgers classificatie (Holgers, 1988; Holgers, 1989):
- 0 = géén irritatie;
- 1.= licht roodheid;
- 2. = roodheid en vochtigheid;
- 3. = granulatieweefsel
- 4. = uitgebreide zachte weefselreactie die verwijdering van de steun of implantaat vereist.
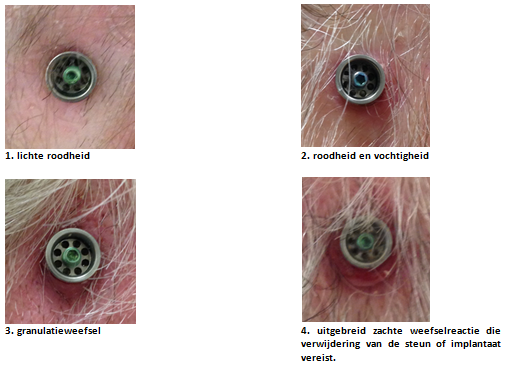
Figuur 1. Holgers classificatie
Holgers 0 en 1 worden beschouwd als licht en zijn derhalve geen indicatie voor medische behandeling. Holgers klasse 2 wordt behandeld met lokale steroïden gecombineerd met antibiotische zalf. Holgers klasse 3 wordt niet alleen lokaal maar ook systemisch behandeld met antibiotica. Soms is het vervangen van het huidige abutment voor een langer abutment nodig. Soms is een beperkte operatie nodig om de huid rondom het abutment te reviseren (opnieuw- uit te dunnen). Holgers graad 4 resulteert tot verwijdering van het abutment of (soms) in implantaatverlies. Dit komt zeer zelden voor.
De recente geïntroduceerde IPS-score lijkt voor de toekomst de aangewezen classificatie (Kruyt, 2017), dit gezien de huidige ontwikkelingen waarbij de geluidsprocessoren ook transcutaan gebruikt kunnen worden en het feit dat ook postoperatieve pijn wordt meegenomen. Echter de meerwaarde zit met name in het gestandaardiseerde behandeladvies, welke op basis van IPS-score wordt gegeven en in de eerdere classificatie ontbrak.
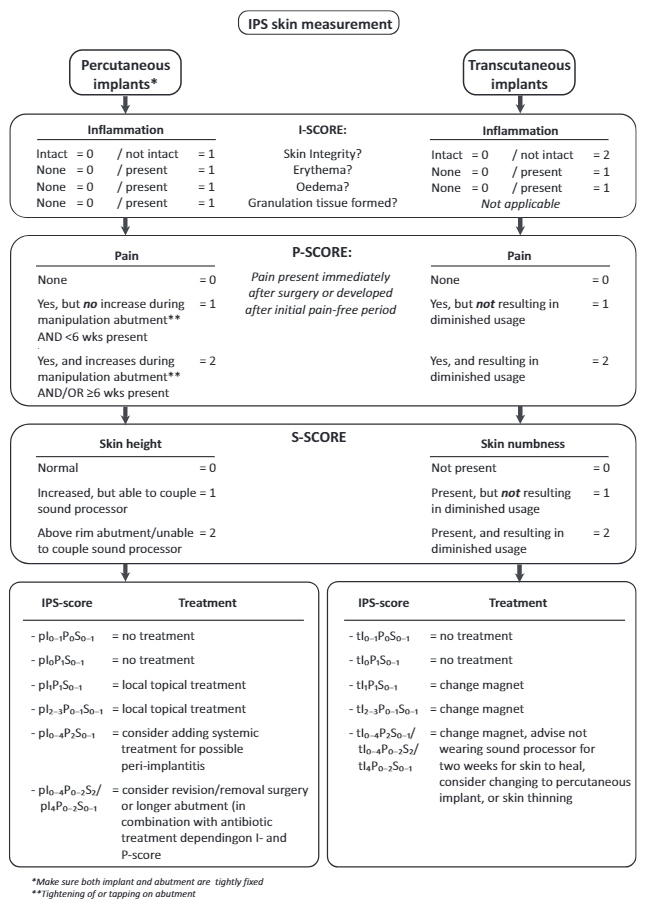
Figuur 2: Flowchart van de IPS-score en behandelingsadvies (Kruyt, 2017)
Uit retrospectieve gegevens is bekend dat de incidentie van ernstige huidreacties (Holgers 2 of hoger) kan variëren tussen 16,1% en 38,1% (Kiringoda, 2013), waarbij deze opmerkelijk lager is in bepaalde centra. Bij 4,6% van alle follow-up bezoeken in eerder genoemde referentiestudie, werd een lichte huidreactie waargenomen (Dun, 2012). Dit verschil tussen deze twee studies is opmerkelijk. Dit verschil kan onder andere te maken hebben met het aantal geplande follow-up bezoeken tussen de verschillende centra en de gebruikte chirurgische techniek. In geval van een Holgers klasse 3 of 4 is een revisie operatie vaak noodzakelijk. Ook bij overgroei van het huidweefsel over de abutment zou chirurgisch ingrijpen nodig kunnen zijn. De incidentie van revisiechirurgie varieert sterk: de beschreven waarden variëren tussen 2,4% en 34,5% (Kiringoda, 2013; Dun, 2012). De introductie van nieuwere typen implantaten (wijdere diameter al dan niet met coating) in combinatie met een andere vorm abutments (al dan niet met coating) en tevens huidbesparende operatie technieken hebben niet alleen het percentage implantaatverlies verminderd maar ook de huidreacties.
In een studie met een follow-up van 5 jaar, met vernieuwd type implantaat, laat een implantaatverlies zien van 4% en slechts 2.5% ernstige huidreacties bij volwassenen (den Besten, 2016). Een adequate studie bij kinderen met dit type implantaat met langdurige follow-up is nog niet verricht. Er zijn aanwijzingen dat ook bij kinderen het gebruik van dit meest recente type implantaat en chirurgische techniek, niet alleen het implantaatverlies maar ook ernstige huidreacties zijn verminderd.
Concluderend is met de huidige generatie implantaten, abutments en chirurgische techniek in een gezonde volwassen populatie te spreken van een kans op ernstige huidreacties van 2 tot 3%.
Overall risico’s
Concluderend kan worden gesteld dat de percutane toepassing van een BCD stabiel en veilig is en dat er relatief weinig complicaties zijn. Belangrijk blijft het geven van duidelijke instructies ten behoeve van nette/hygiënische verzorging van (de huid rond) het implantaat.
Van de ontwikkelingen in zowel de implantaten (wijder en soms met coating) als in de chirurgische technieken wordt beschreven dat er voordelen zijn wat betreft de esthetiek/het cosmetische resultaat, de stabiliteit van het implantaat en de complicaties. Dit maakt dat we inschatten dat de huidige praktijk beter is wat betreft stabiliteit en complicaties dan de lange termijn cijfers van de oudere implantaten laten zien. Extra aandacht is nodig voor kinderen en patiënten met diabetes mellitus type II, patiënten die roken en voor patiënten met bestraling in de voorgeschiedenis.
Audiologische meet- en evaluatietechnieken
Bij evaluatie van gehoorverlies en bijbehorende behandelstrategieën wordt een aantal meet- en evaluatietechnieken vaak gebruikt. De meest gebruikte technieken zullen hieronder kort worden toegelicht.
Metingen
Pure Tone Average (PTA)
Toonaudiometrie wordt bekend verondersteld (zie eventueel hoofdstuk 8.3.2 in het online Leerboek Audiologie: www.audiologieboek.nl). Om een audiogram kort te beschrijven kan een gemiddeld gehoorverlies worden weergegeven. PTA is een internationaal veel gebruikte afkorting voor het pure tone average, het gemiddeld gehoorverlies van 500, 1000, 2000 en 4000 Hz. Als wordt afgeweken hiervan wordt het verder uitgeschreven.
Speech Reception Threshold (SRT)
Het geluidsniveau waarbij 50% goed wordt verstaan, wordt de drempel voor spraakverstaan genoemd (in het Engels: Speech Reception Threshold - SRT). Deze kan in het spraakaudiogram worden bepaald, maar ook in aanwezigheid van rumoer. Reinier Plomp heeft een heden ten dage nog steeds veel gebruikte test ontwikkeld die gebruik maakt van een adaptieve methode. Als eerste wordt de drempel bepaald voor 50% spraakverstaan in stilte, vervolgens wordt bij een vast ruisniveau de drempel bepaald voor het 50% spraakverstaan, waartoe de intensiteit van het spraakmateriaal adaptief wordt gevarieerd. Dit wordt ook wel een SRT-test genoemd, zie eventueel hoofdstuk 8.3.7.2 in het Audiologieboek: www.audiologieboek.nl.
Bij sommige uitgangsvragen is gebruik gemaakt van de verbetering in SRT, indien die niet beschikbaar was (bijvoorbeeld bij kinderen), is de verbetering in PTA genomen.
Vragenlijsten
Abbreviated Profile of Hearing Aid Benefit (APHAB)
Deze vragenlijst bestaat uit 4 domeinen met elk 6 vragen, waarbij patiënten aangaven hoeveel last zij van hun gehoorproblemen hadden in verschillende situaties (communicatie in stilte, in ruis en in een galmende kamer, alsmede als storend ervaren omgevingsgeluid). Per domein werd een percentage berekend, waarbij een hoger percentage meer beperking aangeeft. Dit werd gebruikt om zelf gerapporteerd auditief functioneren te meten (Cox & Alexander, 1995).
IOI-HA
Korte vragenlijst met 7 items waarmee klinisch effect, tevredenheid en gehoor gerelateerde kwaliteit van leven in kaart wordt gebracht met een 5-punts schaal, waarbij geldt dat een hogere score beter is (Cox, 2002).
Speech Spatial and Qualities (SSQ)
Speech Spatial and Qualities of hearing scale questionnaire, een disability-specific vragenlijst, met situaties waarin gehoorproblemen worden aangegeven die met een 10-punt schaal (altijd tot nooit), waarbij een hoger score beter is (Gatehouse & Nobel, 2004).
Glasgow Hearing Aid Benefit Profile (GHABP)
Glasgow Hearing Aid Benefit Profile, een vragenlijst naar meerwaarde van een hoortoestel (Gatehouse, 1999).
Nobel Biocare-vragenlijst
Een lijst met 17 vragen naar hoeveelheid dagelijks gebruik, gebruiksgemak, vermogen om geluiden te lokaliseren en aan/afwezigheid complicaties (Badran, 2006).
Glasgow Childrens Benefit Inventory (GCBI)
Een lijst met 24 vragen over een specifieke interventie (Kubba, 2004; McDermott, 2009).
Onderbouwing
In deze uitgangsvraag wordt nagegaan in welke gevallen een patiënt een goede BCD-kandidaat is. Dit is opgesplitst naar 4 deelvragen, waarin type gehoorverlies varieert en/of het gehoorverlies één- of tweezijdig is. Per module wordt beschreven of er alternatieve revalidatie mogelijk is, aangezien in die gevallen de alternatieven in elk geval besproken en soms geprobeerd moeten zijn. Het blijft daarbij van belang dat de lezer zich realiseert dat deze alternatieven geen onderdeel vormen van deze richtlijn.
BCD-revalidatie kent zowel audiologische als medische aspecten en voor een goede samenwerking moeten deze beide worden belicht. De werkgroep is dan ook van mening dat een goede samenwerking tussen een KNO-arts en een klinisch fysicus-audioloog (KFA) een voorwaarde is voor een optimale indicatiestelling en streeft ernaar om in deze uitgangsvraag richtlijn handvatten te geven voor een juiste indicatie. Zie module ‘Kwaliteitseisen audiologische zorg bij BCD’.
In totaal worden op deze manier vier verschillende soorten gehoorverliezen beschreven waarvoor een BCD mogelijk geïndiceerd kan zijn, waaronder de conventionele indicatie welke evident is. Voor elk van deze indicaties is een aparte module uitgewerkt.
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar studies die uitkomsten van behandeling met BCD vergelijken met de ongeholpen situatie. Bij het zoeken in de literatuur werd gezocht naar studies die de resultaten van een BCD bij één van de typen gehoorverlies (zie de module ‘Indicatiestelling voor BCD’) vergeleken. Voor de deelvragen is dezelfde zoekopdracht gebruikt. De resultaten van deze zoekopdracht zijn vervolgens onderverdeeld naar indicatie. Omdat de literatuur per type gehoorverlies is samengevat was het noodzakelijk dat resultaten werden gepresenteerd over groepen patiënten met een uniforme indicatie.
De volgende zoekvraag is gebruikt:
P (welke patiëntcategorie) uni/bilaterale slechthorende patiënten (inclusief single sided deafness (SSD)/severe to profound unilateral sensorineural hearing loss);
I (welke interventie) BCD (inclusief middenoorimplantaten);
C (welke comparison) andere audiologisch technische revalidatie-technieken als luchtgeleidingstoestellen, (bi)cros hoortoestel, cochleaire implantatie, expectatief (geen interventie);
O (welke uitkomstmaten) spraakverstaan in stilte, spraakverstaan in rumoer, verbeterde lokalisatie van geluid, verbeterd auditief functioneren op basis van vragenlijst, verbetering kwaliteit van leven op basis van vragenlijst, adverse events, duur van de ingreep, esthetiek (litteken/doof gevoel huid), huidreacties volgens Holgers, revisie operaties, necrose huid/infecties.
Relevante uitkomstmaten
De werkgroep achtte spraakverstaan in stilte, spraakverstaan in rumoer, kwaliteit van leven (op basis van een vragenlijst) en auditief functioneren (op basis van een vragenlijst) kritieke uitkomstmaten voor besluitvorming.
De zoekresultaten staan per indicatie weergegeven.
- Badran, Bunstone, Ayra, et al. Patient satisfaction with the bone-anchored hearing aid, a 14 year experience, Oto neurotol. 2006;27:659-66.
- Besten CA den, Stalfors J, Wigren S, et al. Stability, Survival, and Tolerability of an Auditory Osseointegrated Implant for Bone Conduction Hearing: Long-Term Follow-Up of a Randomized Controlled Trial. Otol Neurotol. 2016;37(8):1077-83.
- Besten CA den, Nelissen RC, Peer PG, et al. A Retrospective Cohort Study on the Influence of Comorbidity on Soft Tissue Reactions, Revision Surgery, and Implant Loss in Bone-anchored Hearing Implants. Otol Neurotol. 2015;36(5):812-8.
- Cox RM, Alexander GC. The abbreviated profile of hearing aid benefit. Ear Hear. 1995;16:176186. doi: 10.1097/00003446-199504000-00005.
- Cox, R, Stephens D, Kramer S.E. Translations of the International Outcome Inventory for Hearing Aids (IOI-HA): Traducciones del Inventario Internacional de Resultados para Auxiliares Auditivos (IOI-HA). International Journal of Audiology 2002; 41:326.
- Dun CAJ, Faber HT, de Wolf MJF, et al. Assessment of more than 1,000 implanted percutaneous bone conduction devices: skin reactions and implant survival. Otol Neurotol. 2012;33(2):1928.
- Gatehouse, S. Glasgow Hearing Aid Benefit Profile : Derivation and Validation of a Client-centered, Outcome Measure for Hearing Aid Services. J Am Acad Audiol. 1999;10:80-103.
- Gatehouse S, Noble W. The Speech, Spatial and Qualities of Hearing Scale (SSQ). Int J Audiol. 2004;43(2):85-99.
- Granström G. Osseointegration in Irradiated Cancer Patients: An Analysis with Respect to Implant Failures. Journal of Oral and Maxillofacial Surgery. 2005;63(5):57985.
- Holgers KM, Tjellström A, Bjursten LM, et al. Soft tissue reactions around percutaneous implants: a clinical study of soft tissue conditions around skin-penetrating titanium implants for bone-anchored hearing aids. Am J Otol. 1988;9(1):569.
- Holgers KM, Bjursten LM, Thomsen P, et al. Experience with percutaneous titanium implants in the head and neck: a clinical and histological study. J Invest Surg. 1989;2(1):716.
- Horstink L, Faber HT, de Wolf MJF, et al. Titanium fixtures for bone-conduction devices and the influence of type 2 diabetes mellitus. Otol Neurotol. 2012;33(6):10137.
- Kiringoda R, Lustig LR. A meta-analysis of the complications associated with osseointegrated hearing aids. Otol Neurotol. 2013;34:7904.
- Kruyt I, Nelissen RC, Johansson ML, et al. The IPS-scale: A new soft tissue assessment scale for percutaneous and transcutaneous implants for bone conduction devices. Clin. Otolarynology. 2017
- Kubba H1, Swan IR, Gatehouse S. The Glasgow Children's Benefit Inventory: a new instrument for assessing health-related benefit after an intervention. Ann Otol Rhinol Laryngol. 2004;113(12):980-6.
- McDermott AL, Williams J, Kuo M, et al. Quality of Life in Children Fitted With a Bone-Anchored Hearing Aid. Otol Neurotol. 2009;30(3):3449.
- Nelissen RC, Mylanus EAM, Kunst HPM, et al. A new bone-anchored hearing implant: short-term retrospective data on implant survival and subjective benefit. Eur Arch Otorhinolaryngol. 2013;270(12):301925.
- Sennerby L, Meredith N. Implant stability measurements using resonance frequency analysis: biological and biomechanical aspects and clinical implications. Periodontol 2000. 2008;47:5166.
- Shirazi MA, Marzo SJ, Leonetti JP. Perioperative complications with the bone-anchored hearing aid. Otolaryngol Head Neck Surg. 2006;134:2369.
- Tjellström A, Granström G. How we do it: Frequency of skin necrosis after BAHA surgery. Clin Otolaryngol. 2006;31:21620.
- Wazen JJ, Wycherly B, Daugherty J. Complications of bone-anchored hearing devices. Adv Otorhinolaryngol. 2011;71:6372.
- Wolf MJF de, Hol MKS, Huygen PLM, et al. Clinical outcome of the simplified surgical technique for BAHA implantation. Otol Neurotol. 2008;29:11008.
Beoordelingsdatum en geldigheid
Publicatiedatum : 25-09-2018
Beoordeeld op geldigheid : 01-12-2018
Uiterlijk in 2021 bepaalt het bestuur van de NVKNO of modules in deze richtlijn nog actueel zijn. Zo nodig wordt een nieuwe werkgroep geïnstalleerd om de richtlijn te herzien. De geldigheid van de modules komen eerder te vervallen indien nieuwe ontwikkelingen aanleiding geven een herzieningstraject te starten. Bij enkele modules is de verwachting dat dit eerder dan na 3 jaar zal zijn en dus worden deze modules eerder op actualiteit beoordeeld.
De NVKNO is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
Het doel van deze richtlijn is het verkrijgen van duidelijkheid over de gewenste gang van zaken bij indicatiestelling, diagnostiek en behandeling met Bone conduction devices (BCD). Daarnaast wordt in deze richtlijn een kader geschetst voor de gewenste organisatie van zorg omtrent behandeling met BCD en de minimale informatievoorziening aan de patiënt. Dit alles moet bijdragen aan een meer eenduidig beleid bij het aanbieden van behandeling met BCD.
Doelgroep
Deze richtlijn is geschreven voor allen die betrokken zijn bij gehoorrevalidatie middels BCD. Dit betreft medisch specialisten (KNO-artsen, klinisch fysici-audiologen), maar ook alle andere betrokken zorgverleners en patiënten.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in november 2015 een werkgroep ingesteld, bestaande uit KNO-artsen en klinisch fysici-audiologen. De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep werkte gedurende 3 jaar aan de totstandkoming van de richtlijn. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
Werkgroep
- Dr. M.K.S. Hol, KNO-arts, Radboudumc , Nijmegen (voorzitter); NVKNO
- Ir. M.S. Toll, Klinisch fysicus-audioloog, Erasmus MC, Rotterdam (vicevoorzitter); NVKF
- Ir. T.T. Prinzen, Klinisch fysicus-audioloog, Pento Audiologisch Centrum, Amersfoort; NVKF
- Dr. ir. A.J. Bosman, Klinisch fysicus- audioloog, Radboudumc, Nijmegen; NVKF
- Drs. A.J.M. van der Rijt, KNO-arts, Amphia Ziekenhuis, Breda; NVKNO
- Dr. A. Frima-van Aarem, KNO-arts, Meander Medisch Centrum, Amersfoort; NVKNO
- Prof. dr. R.J. Stokroos, KNO-arts, UMC Utrecht, Utrecht; NVKNO
- Dr. S.J.H. Bom, KNO-arts, Deventer Ziekenhuis, Deventer; NVKNO
Met ondersteuning van:
- S. van Dijk MSc, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten;
- D. Leereveld MSc, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten;
- M.E. Wessels MSc, Literatuurspecialist, Kennisinstituut van de Federatie Medisch Specialisten;
- D.P. Gutierrez, Projectsecretaresse, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of ze in de laatste vijf jaar directe financiële (betrekking commercieel bedrijf, persoonlijke financiële belangen, onderzoek financiering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en oordeel over het omgaan met eventuele belangen vindt u hieronder. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van Medisch Specialisten.
|
Achternaam |
Functie |
Nevenfuncties |
Persoonlijke financiele belangen |
Persoonlijke relaties |
Reputatiemanagement |
Extern gefinancierd onderzoek |
Kennisvalorisatie |
Overige belangen |
Getekend |
Oordeel |
|
Frima-vanaarem |
KNO-arts, plaatsvervangend opleider |
nvt |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 1-10-2015 |
geen belemmeringen |
|
Bosman |
Klinisch fysicus-audioloog |
AudTutor - audiologie onderwijs en onderzoek. Dit zijn betaalde werkzaamheden |
geen |
geen |
geen |
Baha onderzoek. Ik ben momenteel betrokken bij de evaluatie van de Cochlear Baha SP-5 en P-5 toestellen en ontvang hiervoor een vergoeding. |
geen |
geen |
ja, 15-09-2015 |
deelname aan commissie, terugtrekken als onderwerpen van onderzoeken aan bod komen |
|
Hol (vz) |
KNO-arts |
Co-promotor 2 promovendi onderzoeks trials, research gelden uitbetaald aan Radboudumc voor zowel cochlear als oticon. Advisory board member oticon aangaande project BCI tijdelijke functie, start 2015. |
Advisory board, zie nevenfuncties |
geen |
geen |
geen |
geen |
geen |
ja, 29-09-2015 |
deelname aan commissie, met uitzondering van uitspraken over BCI. Nieuwe vragen vanuit Oticon, bespreken met werkgroep |
|
Barneveld, van |
Directeur |
Voorzitter richtlijn advies en autorisatiecommissie in de jeugd en gezondheidzorg Gezondheidsraadcommissie (Medicalisering) |
geen |
geen |
Werkzaam bij het Kennisinstituut van Medisch Specialisten. Dit instituut is een zelfstandig onderdeel van de Federatie Medisch Specialisten. Het instituut houdt zich onder andere bezig met Richtlijnontwikkeling in de 2e lijns curatieve zorg. |
geen |
geen |
geen |
ja, 14-12-2015 |
geen belemmeringen |
|
Leereveld |
adviseur Kennisinstituut van Medisch Specialisten |
nvt |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 7-12-2015 |
geen belemmeringen |
|
Prinzen |
Klinisch fysicus-audioloog 1 fte |
nvt |
geen |
geen |
geen |
geen |
geen |
geen |
ja,31-08-2015 |
geen belemmeringen |
|
Bom |
KNO-arts, full time |
plv. B-opleider lid werkgroep richtlijn perceptieve slechthorendheid secretaris regionale KNO-vereniging Rijn-Ijssel penningmeester vakgroep KNO-heekunde DZ en vertegenwoordiger vakgroep in stafmaatschap lid Capaciteitscommissie Ondersteuning Specialisten DZ |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 25-9-2015 |
geen belemmeringen |
|
Stokroos |
KNO -arts, 1.0 fte |
geen |
geen |
geen |
1.lid medische adviesraad neurofibromatose vereniging nederland |
als hoogleraar otologie/neurotologie heb ik diverse research activiteiten met financieringsbronnen zoals genoemd. Nadrukkelijk is er geen relatie tussen de uitkomsten van deze onderzoekingen en de financiering. Een en ander is onafhankelijk geborgd en gemonitord via CTCM (clinical trial center maastricht) |
geen patenten. Kennis en research op gebied van periabutment implantitis en chirurgische innovaties |
geen |
ja, 7-12-2015 |
geen belemmeringen |
|
Toll (vice- vz) |
Klinisch fysicus - audioloog |
bestuurslid (penningmeester) NVA (Nederlandse vereniging voor Audiologie) |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 5-10-2015 |
geen belemmeringen |
|
van Rijt |
KNO -arts, plaatsvervangend opleider |
participatie onderzoek gefinancierd door Cochlear, geen principal investigator (financiering via maatschap) |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 14-12-2015 |
geen belemmeringen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door tijdens de invitational conference, die werd gehouden in februari 2016 input te vragen van patiëntenvertegenwoordigers vanuit verschillende verenigingen. Tijdens de oriënterende zoekactie werd gezocht op literatuur naar patiëntenperspectief (zie Strategie voor zoeken en selecteren van literatuur). Er is daarnaast een module patiënteninformatie opgenomen in de richtlijn waarin wordt beschreven welke informatie een patiënt moet krijgen wanneer behandeling met BCD wordt overwogen of uitgevoerd. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de betrokken patiëntenorganisaties.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de belangrijkste aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is als aparte module opgenomen en zal later als aanverwant product worden toegevoegd. De richtlijn leent zich niet voor het ontwikkelen van indicatoren, omdat de aanbevelingen te weinig aanknopingspunten bieden om specifiek meetbare indicatoren voor op te stellen. Daarom is in de werkgroep besloten geen officiële indicatorenset te ontwikkelen bij de richtlijn.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen volgens het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is, en op de richtlijn voor richtlijnen voor de beoordeling van de kwaliteit van richtlijnen (http://www.zorginstituutnederland.nl).
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens zijn er knelpunten aangedragen door verschillende veldpartijen tijdens de invitational conference. Een verslag van deze bijeenkomst is opgenomen als aanverwant product.
De werkgroep stelde een long list met knelpunten op en prioriteerde de knelpunten op basis van: (1) klinische relevantie, (2) de beschikbaarheid van evidence van hoge kwaliteit, (3) en de te verwachten impact op de kwaliteit van zorg, patiëntveiligheid en (macro)kosten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk en onbelangrijk. Tevens definieerde de werkgroep voor de kritieke en belangrijke uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Er zijn twee oriënterende literatuursearches uitgevoerd naar bestaande buitenlandse richtlijnen, systematische reviews, en literatuur over patiëntenvoorkeuren (patiëntenperspectief). De resultaten hiervan zijn verwerkt in de overwegingen bij de verschillende uitgangsvragen. Vervolgens werd indien mogelijk voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module van de desbetreffende uitgangsvraag.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of bias tabellen.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij geen van de uitgangsvragen was er sprake van een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies om de resultaten ook kwantitatief samen te vatten in een meta-analyse.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen
Volgens de geldende afspraken binnen het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit, is ook in deze richtlijn gekozen om de kracht van het wetenschappelijk bewijs te bepalen volgende de GRADE-methode. GRADE staat voor Grading Recommendations Assessment, Development and Evaluation (Schünemann, 2013).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van vertrouwen in de literatuurconclusie (zie http://www.guidelinedevelopment.org/handbook/).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Het gebruik van de GRADE-methode impliceert dat enkel behandelingen getest met een RCT voldoende evident (voldoende krachtig van bewijs) zijn. Echter, als de nieuwe behandeling objectief gezien (dus met harde data in de hand) beter is dan de bestaande behandelingen, dan is een RCT niet nodig. Dit is duidelijk doordat zintuiglijke behandelingen bij oorheelkundige (maar ook bijv. bij oogheelkundige patiënten), eenvoudigweg als controle op en van zichzelf gebruik maken door apparatuur wel/niet aan te sluiten.
Behandeling met een BCD is een relatief zeldzame ingreep die ook wordt toegepast bij een kwetsbare patiëntenpopulatie (verstandelijk beperkten, ouderen, kinderen). Om deze reden zijn grote, gerandomiseerde interventiestudies in deze setting praktisch niet haalbaar en zijn de conclusies in de module ‘Indicatiestelling voor BCD’ niet gegradeerd. Soms wordt de behandeling toegepast als er (grote) communicatieve nood is en er géén alternatieven zijn, de conventioneel indicatie. Gezien de objectiviteit van de metingen en duidelijke verschillen tussen het horen mét en zonder hulp van BCD is het toch mogelijk om sterke aanbevelingen te doen. Dit wordt onderbouwd in de overwegingen.
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008), en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Bij interventievragen verwijst de conclusie niet naar één of meer artikelen, maar wordt getrokken op basis van alle studies samen (body of evidence). Hierbij maakten de werkgroepleden de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje Overwegingen.
Overwegingen
Om te komen tot een aanbeveling in deze richtlijn zijn, naast weging van de kwaliteit van het wetenschappelijke bewijs volgens GRADE, met name andere aspecten belangrijk en worden deze evengoed meegewogen in de overwegingen. Hierbij kan gedacht worden aan de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patiënt values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje Overwegingen.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de Kennislacunes beschreven (onder aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Leeswijzer
Onderstaande conceptrichtlijntekst wordt na het doorlopen van de commentaar- en autorisatiefase opgenomen in de Richtlijnendatabase (http://www.richtlijnendatabase.nl). Verwijzingen naar tabbladen zijn in de huidige versie van de richtlijntekst terug te vinden in de aanverwante producten.
Literatuur
Brouwers MC, Kho ME, Browman GP, Burgers JS, et al.; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;14;182(18):E839-42. Review. PubMed PMID: 20603348.
Medisch Specialistische Richtlijnen 2.0. Adviescommissie Richtlijnen van de Raad Kwaliteit. Beschikbaar via: https://www.demedischspecialist.nl/onderwerp/raad-kwaliteit. 2012.
Richtlijn voor Richtlijnen (2012; herziene versie). Regieraad Kwaliteit van Zorg Beschikbaar via: http://www.zorginstituutnederland.nl. 2012.
Schünemann H, Brożek J, Guyatt G, et al. Editors. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html. 2013.
Schünemann HJ, Oxman AD, Brozek J, et al.;GRADE Working Group. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;17;336(7653):1106-10. PubMed PMID: 18483053.
