Operatietechnieken BCD bij volwassenen
Uitgangsvraag
Welke operatietechniek is het meest effectief en geeft de minste kans op bijwerkingen bij volwassenen met een indicatie voor een percutane BCD?
Aanbeveling
Gebruik bij het plaatsen van een percutaan implantaat ten behoeve van een BCD de lineaire incisie techniek, waarbij de huid niet uitgedund hoeft te worden (volwassenen) middels 1-fase chirurgie. Voor kinderen zie de module ‘Operatietechniek BCD bij kinderen’.
Gebruik bij voorkeur een lokale anesthesie techniek in een gecontroleerde setting (Klasse 1 of 2 operatie kamer –OK-).
Kies eventueel voor een gehele narcose om medische redenen, op verzoek van de patiënt of bij kinderen. Zie ook de module ‘Operatietechniek BCD bij kinderen’ ten aanzien van kinderen.
Registreer per-operatief in het elektronisch patiëntendossier (EPD) het implantaat (LOT nummer, artikelnummer van implantaatsysteem, naam leverancier, lengte implantaat en abutment, type, bodem boorschacht en andere bijzonderheden) alsmede de gebruikte operatie techniek.
Vervolg patiënten bij voorkeur jaarlijks poliklinisch, evalueer de status van het implantaat en omliggende huid en tevens of het aandraaien van het abutment nodig is (zie de module ‘Nacontrole na een BCD operatie’).
Registreer alle complicaties, doch in elk geval ten aanzien van huid- en implantaatverlies. Rapporteer de huidreacties in elk geval volgens de Holgersclassificatie en eventueel volgens IPS schaal (zie de module ‘Indicatiestelling voor BCD’ voor IPS en ‘Nacontrole na een BCD operatie’ voor nazorg).
Stel onderzoek in naar de oorzaak van het implantaatverlies. Denk hierbij aan operatieomstandigheden, nazorg/hygiëne en/of door het implantaat naar de betreffende firma terug te sturen met het verzoek om een verslag van hun bevindingen te ontvangen.
Overwegingen
Voor het plaatsen van een percutaan implantaat ten behoeve van een BCD zijn verschillende operatieve technieken ontwikkeld in de loop der jaren. De lineaire incisie heeft om verschillende redenen uiteindelijk de voorkeur gekregen. Dit is met name gelegen in een samenvatting van de bevindingen uit het artikel van de Berg (van de Berg, 2010). Hierin zijn weliswaar niet alle verschillen statistisch significant, feit blijft dat er meer ernstige huidreacties zijn gezien in de eerste 2 jaar na de operatie, wanneer andere technieken dan de lineaire incisie gebruikt werden. De werkgroep is van mening dat de lineaire incisie de aanbevolen techniek genoemd mag worden met de minste kans op complicaties, heroperaties en ongemak.
De belangrijkste keuze die de chirurg anno 2018 nog moet maken is of de huid rondom het abutment wel of niet uitgedund moet worden bij de lineaire incisietechniek. Er zijn aanwijzingen in literatuur dat de ingreep hiermee nog korter duurt en dat de cosmetische uitkomst beter is indien gekozen wordt voor het intact laten van de volledige huiddikte (den Besten, 2016). Dit wordt als logisch gevolg gezien van de eerder geschetste overwegingen waaruit de lineaire incisie techniek de aanbevolen techniek blijkt; i.e. een minder groot wondoppervlak geeft naar verhouding ook minder gevoelsstoornissen rondom het implantaat en minder littekenweefsel. Als er minder chirurgische handelingen worden verricht is de snijtijd automatisch korter, hetgeen niet direct hoeft te leiden tot kortere duur van de gehele ingreep. Een kortere ingreep faciliteert wel nog meer het plaatsen van een BCD onder lokale anesthesie. Er is vooralsnog geen bewijs dat het al of niet uitdunnen van de huid op langere termijn aanleiding is voor een toe- of afname van peri-abutment huidreacties volgens Holgers, het gehoorresultaat of implantaatverlies. Daarnaast blijft het van belang te realiseren dat de afname in huidreacties niet alleen door een verbeterde chirurgische techniek komt, maar mogelijk ook door de veranderde vorm van de abutments (den Besten, 2016). Hierbij is de hoek tussen huid en abutment dusdanig veranderd, dat dit tot verminderde huidreacties heeft geleid. De huid blijft in de loop der jaren wel hoger worden (hypertrofie), dit kan tot op zekere hoogte (dan wel lengte van abutment) worden verholpen door een langer abutment te plaatsen. Wanneer de huid echter geheel over het abutment heen groeit is revisie van de huid de aangewezen therapie. Hiervoor is een her-operatie onder plaatselijke verdoving noodzakelijk, om middels een punch de huid weer rondom het abutment sluitend te laten vallen.
Alvorens meer kwalitatief goede studies zijn gedaan en ook de langere follow-up duur daarvan bekend is, wordt de trend om gebruik te maken van nog meer minimaal invasieve chirurgische technieken, zoals een variant van de punch only techniek, bijvoorbeeld MIPS (minimally invasive Ponto surgery – waarbij door het werken door een canule geen direct zicht is) ontraden in opleidingssetting (Johansson en Holmberg, 2015). In een gecontroleerde studiesetting of uitgevoerd door een ervaren chirurg is deze techniek te overwegen, om antwoord te kunnen krijgen op genoemde vraag (zie kennislacune). Het is daarbij belangrijk uitkomsten te registreren en evalueren.
Onderbouwing
Het plaatsen van een implantaat en abutment in de schedel heeft in de loop der jaren een evolutie doorgemaakt die gericht is op het minimaliseren van de reactie van de huid rond het implantaat, het vlot laten genezen van de chirurgische wond en het minimaliseren van pijnklachten of gevoelsverlies rond de abutment. Daarnaast is de cosmetiek van de peri-abutment regio een belangrijk aandachtspunt.
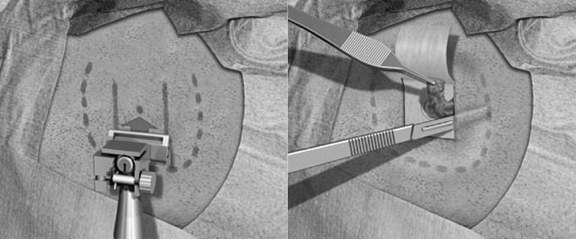
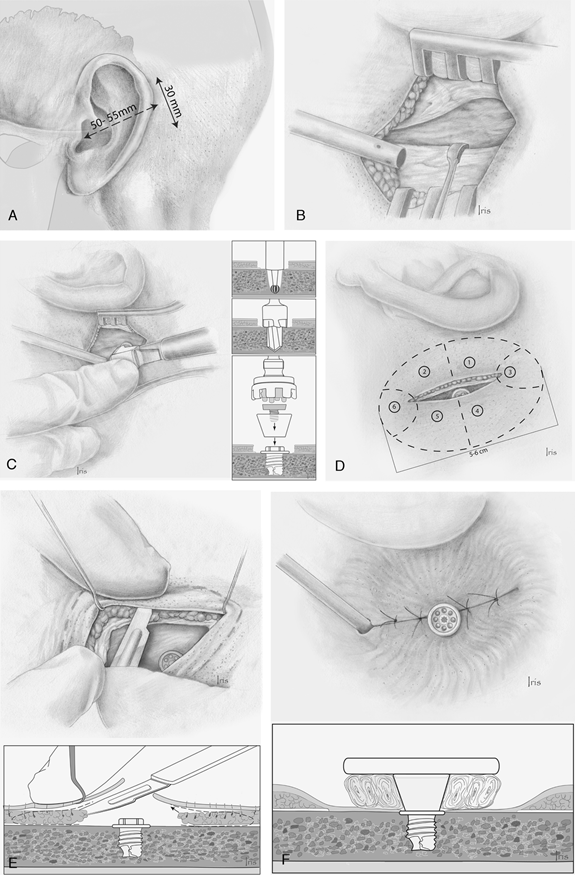
Initieel werd bij het plaatsen van een bone implant de huid rondom het abutment zo dun mogelijk gemaakt, teneinde weefselbewegingen en reacties te minimaliseren. Hiertoe werd aanvankelijk een vrij huid transplantaat, later middels een dermatoom verkregen gebruikt.(zie figuur 1). Enige tijd later evolueerde deze techniek naar onder meer de U-flap, met name om huidnecrose te verminderen (zie figuur 2) (De Wolf, 2008). De lineaire incisie techniek met huiduitdunning (figuur 3) ontstond vervolgens als logische volgende stap ter optimalisatie en was decennialang de techniek van voorkeur. In afgelopen jaren is veel onderzoek geweest naar de meest optimale chirurgische techniek in combinatie met de nieuwste typen bone implants en abutments. Dit heeft erin geresulteerd dat thans veel operateurs een huidsparende chirurgische techniek (dus zonder huiduitdunning) toepassen.
Figuur 1 Dermatoom techniek
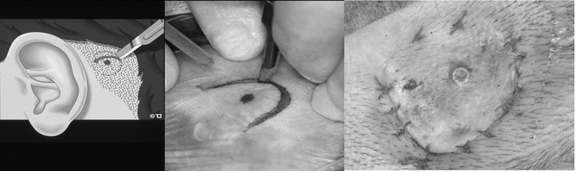
Figuur 2 U-Flap techniek
Figuur 3 Lineaire incisie techniek (de Wolf, 2008)
Aangezien er in de praktijk nog veel variatie blijkt te zijn in de toegepaste operatietechnieken bij het plaatsen van een implantaat wordt in deze richtlijn een overzicht gegeven van de beschikbare literatuur en praktijkervaring. Er is gekozen een vergelijking te maken tussen verschillende incisietechnieken die in de afgelopen jaren het meeste zijn gehanteerd: de dermatoom techniek, de U-flap techniek en de lineaire incisie (zie de module ‘Operatietechniek BCD bij volwassenen’). Daarnaast komt de vraag aan bod of volgens de huidige stand van de wetenschap en ervaringen in de praktijk gebruik dient te worden gemaakt van huiduitdunning of juist van een huidbesparende techniek. Dit alles teneinde aanbevelingen te kunnen doen over de operatietechniek(en) van voorkeur (zie de module ‘Operatietechnieken BCD bij volwassenen’).
Zoekvraag 1
Spraakverstaan
|
Redelijk GRADE |
Er lijkt geen verschil te zijn in spraakverstaan tussen de verschillende incisievormen (met en zonder huiduitdunning) bij volwassenen met een indicatie voor percutane BCD.
Bron (Den Besten, 2016) |
Duur van de ingreep
|
Hoog GRADE |
De duur van de ingreep lijkt korter te zijn bij de incisievorm waarbij geen gebruik wordt gemaakt van huiduitdunning in vergelijking met de incisievorm waarbij wel gebruik wordt gemaakt van huiduitdunning bij volwassen met een indicatie voor percutane BCD.
Bronnen (Hultcrantz, 2011; Brant, 2013; Wilson, 2013; Gordon, 2014; Dumon, 2015; Martinez, 2015; Den Besten, 2016) |
Esthetiek (litteken/gevoelsverlies)
|
Laag GRADE |
De esthetiek lijkt beter te zijn (mooier litteken, minder gevoelsverlies ) zijn bij de incisievorm waarbij geen gebruik wordt gemaakt van huiduitdunning in vergelijking met de incisievorm waarbij wel gebruik wordt gemaakt van huiduitdunning bij volwassen met een indicatie voor percutane BCD.
Bronnen (Hultcrantz, 2011; Hultcrantz, 2014; Hogsbro, 2015; Den Besten, 2016) |
Huidreacties
|
Hoog GRADE |
Er lijkt geen verschil te zijn in huidreacties volgens Holgers tussen de verschillende incisievormen (met en zonder huiduitdunning) bij beschreven type implantaten en abutments, bij volwassenen met een indicatie voor percutane BCD.
Bronnen (Hultcrantz, 2011; Brant, 2013; Wilson, 2013; Gordon, 2014; Hultcrantz, 2014; Dumon, 2015; Hogsbro, 2015; Martinez,2015; Den Besten, 2016) |
Mislukte osseointegratie
|
- GRADE |
Er zijn geen vergelijkende studies gevonden die het effect van de incisievorm (met of zonder huiduitdunning) op mislukte osseointegratie hebben onderzocht bij volwassenen met een indicatie voor percutane BCD.
Bron (Verheij, 2016) |
Zoekvraag 2
Spraakverstaan
|
- GRADE |
Er zijn geen vergelijkende studies gevonden die het effect van de operatietechniek op spraakverstaan hebben onderzocht bij volwassenen met een indicatie voor percutane BCD. |
Duur van de ingreep
|
- GRADE |
Er zijn geen vergelijkende studies gevonden die het effect van de operatietechniek op duur van de ingreep hebben onderzocht bij volwassenen met een indicatie voor percutane BCD. |
Esthetiek (litteken/gevoelsverlies)
|
- GRADE |
Er zijn geen vergelijkende studies gevonden die het effect van de operatietechniek op esthetiek (litteken/gevoelsverlies) hebben onderzocht bij volwassenen met een indicatie voor percutane BCD. |
Huidreacties
|
Zeer laag GRADE |
De ernst van huidreacties lijkt af te hangen van de operatietechniek. De lineaire incisie techniek lijkt tot minder huidreacties te leiden dan de u-flap en dermatoom techniek.
Bronnen (Van De Berg, 2010; Mudry, 2009; Stalfors, 2008) |
Loss of fixture of mislukte osseointegratie
|
Zeer laag GRADE |
Er lijkt geen verschil te zijn in het voorkomen van loss of fixture of mislukte osseointegratie tussen de verschillende operatietechnieken.
Bron (Stalfors, 2008) |
Zoekvraag 1
Beschrijving studies
Er werd één systematische review geïncludeerd die het effect heeft onderzocht van de operatietechniek op huidcomplicaties bij volwassen personen met een indicatie voor een BCD (Mohamad, 2016). In deze review zijn verschillende operatietechnieken bekeken. Voor deze uitgangsvraag zijn alleen de studies meegenomen uit de review die een van de drie vergelijkingen uit de pico bevatten. Er bleven toen nog twee studies over uit de review hieronder worden beschreven (Van de Berg, 2010; Stalfors, 2008). Daarnaast is er één retrospectieve studie geïncludeerd die het effect van de operatietechniek op de uitkomst loss of fixture of mislukte osseointegratie heeft onderzocht (Muldry, 2008). Voor de uitwerking in de tekst is gebruik gemaakt van de informatie uit de drie losse studies.
In de studie van van de Berg (2010) zijn er vier verschillende operatietechnieken vergeleken: (1) FTSG (Full Thickness Skin Graft), (2) U-skin flap, (3) dermatoom, (4) longitudinal (lineair). 143 patiënten zijn geïncludeerd in de leeftijd van 8 tot 85 jaar oud. De follow-up tijd liep tussen de 3 en 147 maanden. In de studie van Stalfors (2008) is de U-flap techniek vergeleken met de dermatoom techniek. 75 patiënten werden geïncludeerd met een leeftijd tussen de 2 en 88 jaar oud (gemiddelde leeftijd was 46 jaar). De follow up tijd lag tussen de 28 en 74 maanden. In de studie van Muldry (2008) werden 113 personen in twee groepen gedeeld. 62 patiënten kregen de skin flap techniek zonder huiduitdunning en 51 patiënten kregen de lineaire incisie techniek. De gemiddelde leeftijd was 53,6 jaar. De follow up tijd was 3 maanden.
Resultaten
Spraakverstaan
De uitkomstmaat spraakverstaan was geen onderzochte uitkomstmaat.
Duur van de ingreep
De uitkomstmaat duur van de ingreep was geen onderzochte uitkomstmaat.
Esthetiek (litteken/gevoelsverlies)
De uitkomstmaat esthetiek was geen onderzochte uitkomstmaat.
Huidreacties
In de studie van Stalfors (2008) is gekeken naar het voorkomen van huidreacties en de gradering van deze huidreacties. De U-shape graft techniek en dermatoom techniek werden in deze studie met elkaar vergeleken. Uit deze studie blijkt dat de U-shape graft groep 19.6% meer episodes had van huidreacties maar dit verschil was niet significant (p=0.14).
In de studie van Mudry (2009) is de uitkomstmaat huidreacties gemeten aan de hand van de mate waarin er sprake was van necrose van de huid. In de skin-flap techniek was er in 6.5% van de patiënten sprake van necrose en in de lineaire incisie groep 1.9%. Het verschil was echter niet significant (p=0.125).
In de studie van van De Berg (2010) zijn huidreacties gemeten door het aantal huidcomplicaties te meten en door deze complicaties te graderen aan de hand van de Holgers classificatie (Holgers, 1988). Het aantal ernstige huidcomplicaties was voor deze uitgangsvraag relevante vergelijkingen niet significant.
Loss of fixture of mislukte osseointegratie
Tabel 1 Studie van van de Berg, 2010 - Reoperations
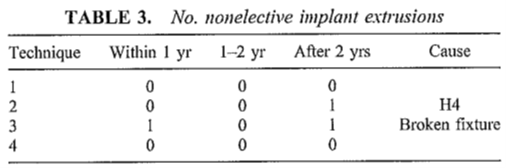
Bewijskracht van de literatuur
Voor de uitkomstmaten spraakverstaan, duur van de ingreep en esthetiek is geen literatuur gevonden en is het dus niet mogelijk om de literatuur te graderen. De bewijskracht voor de uitkomstmaten huidreacties en loss of fixture/mislukte osseointegratie is met 3 niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias); extrapoleerbaarheid door verschillende vergelijkingen (bias ten gunste van indirectheid); het geringe aantal patiënten (imprecisie).
Zoekvraag 2
Beschrijving studies
Er werd één systematische review geïncludeerd die het verschil in effectiviteit en bijwerkingen heeft onderzocht van de incisievorm (lineaire incisie standaard met tissue reduction of tissue preservation) bij volwassen personen met een indicatie voor een percutane BCD (Verheij, 2016). In deze review zijn 18 artikelen geïncludeerd. Slechts in 10 van deze artikelen wordt er een vergelijking gemaakt tussen de incisievorm met en zonder huiduitdunning. En één van deze 10 artikelen ging over kinderen. Uiteindelijk zijn dan ook 9 artikelen meegenomen voor deze module: (1) Brant, 2013; (2) Den Besten, 2016; (3) Dumon, 2015; (4) Gordon, 2014; (5) Hogsbro, 2015, (6); Hultcrantz, 2014; (7) Hultcrantz, 2011; (8) Martinez, 2015; (9) Wilson, 2013. Voor de uitwerking in de tekst is gebruik gemaakt van de review, aangevuld met informatie uit de individuele studies die in de negen onderliggende artikelen zijn besproken. Voor uitgebreide informatie over het aantal patiënten, leeftijd, geslacht, follow up tijd en uitkomsten zie de evidencetabel.
Resultaten
Spraakverstaan
Er is binnen de review van Verheij (2016) slechts één studie die het effect van de incisievorm op het spraakverstaan heeft onderzocht (Den Besten, 2016). Uit deze studie bleken geen significante verschillen in spraakverstaan tussen de beide incisievormen (met en zonder huiduitdunning).
Duur van de ingreep
Zes studies (Brant, 2013; Den Besten, 2016; Dumon, 2015; Gordon, 2014; Hultcrantz, 2011; Martinez, 2015; Wilson, 2013) hebben het verschil in de duur van de ingreep tussen de verschillende incisievormen (met en zonder huiduitdunning) onderzocht. In vijf van deze studies bleek dat de operatieduur significant lager was bij de incisievorm waarbij geen gebruik wordt gemaakt van huiduitdunning. In de studie van Brant (2016) was de operatieduur wat lager in de groep zonder huiduitdunning maar dit verschil was niet statistisch significant.
Esthetiek (litteken/gevoelsverlies)
Twee studies beschrijven het effect van de incisievorm (met en zonder huiduitdunning op de esthetiek van het operatiegebied (het litteken) (Dumon, 2015; Hultcrantz, 2011). Deze studies geven aan dat er bij de incisievorm zonder huiduitdunning het operatiegebied er aanzienlijk beter uit zag in vergelijking met de incisievorm met huiduitdunning. Zo groeide bijvoorbeeld het haar weer terug na een incisie zonder huiduitdunning maar bleef het litteken kaal na een incisie met huiduitdunning. In vier studies (Den Besten, 2016; Hogsbro, 2015; Hultcrantz, 2014; Hultcrantz, 2011) is gevoelsverlies onderzocht als uitkomstmaat. Hier kwamen tegenstrijdige resultaten uit. In een van de studies werd er geen statistisch significant verschil gevonden (Den Besten, 2016). In de andere drie studies kwam gevoelsverlies vaker voor in de controlegroep (met huiduitdunning). In één van deze studies was dit verschil significant (Hogsbro, 2015), in de andere twee studies (Hultcrantz, 2014; Hultcrantz, 2011) werd er significantieniveau weergegeven.
Huidreacties
Alle negen studies hebben huidreacties meegenomen als onderzochte uitkomstmaat. Al deze studies gebruikten ook de classificatie van Holgers om de ernst van de huidreacties te meten. De studies gebruikten verschillende manieren om deze scores te rapporteren. Bijvoorbeeld in de studie van Gordon (2014) is de Holgers score bij het eerste en laatste follow up bezoek vergeleken voor beide incisievormen terwijl Den Besten (2016) de maximale Holgers score bij elke patiënt heeft vergeleken tussen de groep met en zonder huiduitdunning. De ernst van de huidreacties bleek in geen van de studies statistisch significant te verschillen tussen de incisievormen met en zonder huiduitdunning.
Mislukte osseointegratie
Twee studies beschrijven heroperaties: Den Besten (2016) en Dumon (2014). Echter, deze heroperaties zijn het gevolg van trauma of overtollig weefsel en betreffen dus geen mislukte osseointegratie. Er kan dan ook geconstateerd worden dat er geen literatuur beschikbaar is over het verschil in mislukte osseointegratie bij de incisievormen met en zonder huiduitdunning.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat spraakverstaan is met één niveau verlaagd gezien het geringe aantal patiënten (imprecisie) en er slechts één studie is die deze uitkomstmaat heeft onderzocht. De bewijskracht voor de uitkomstmaat esthetiek is met twee niveaus verlaagd gezien onnauwkeurige data (geen significantieniveau gerapporteerd) en het geringe aantal patiënten (imprecisie).
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvragen:
1) Welke operatietechniek (dermatoom techniek, een U-flap of lineaire incisie met huiduitdunning) is het meest effectief en geeft de minste kans op bijwerkingen bij volwassenen met een indicatie voor een percutane BCD?
P (welke patiëntcategorie) volwassen patiënten met een indicatie voor een percutane BCD;
I (welke interventie) (Nijmeegse) lineaire incisie met huiduitdunning Hultkrans;
C (welke comparison) dermatoom techniek;
O (welke uitkomstmaten) spraakverstaan, duur van de ingreep, esthetiek (litteken/doof/gevoel huid), huidreacties volgens Holgers, revisie operaties, necrose huid/infecties.
2) Welke incisievorm (lineaire incisie standaard met tissue reduction (id est huiduitdunning) of tissue preservation (zonder huiduitdunning)) is het meest effectief en geeft de minste kans op bijwerkingen bij volwassenen?
P: volwassen patiënten met een indicatie voor een percutane BCD;
I: lineaire incisie standaard met tissue reduction;
C: lineaire incisie met tissue preservation;
O: spraakverstaan, duur van de ingreep, esthetiek, pijn, gevoelsverlies huid), huidreacties volgens Holgers, revisie operaties, necrose huid/infecties.
Relevante uitkomstmaten
De werkgroep achtte spraakverstaan, duur van de ingreep, esthetiek (litteken/gevoelsverlies huid), huidreacties volgens Holgers (Holgers, 1988), revisie operaties en necrose huid/infecties voor de besluitvorming kritieke uitkomstmaten.
De werkgroep prioriteerde de uitkomstmaten als volgt:
- operatieduur;
- cosmetiek litteken;
- pijnklachten;
- huidreactie volgens Holgers.
Revisie interventies: revisieoperaties vanwege onvoldoende osseointegratie. Revisieoperaties die zijn uitgevoerd vanwege huidreacties worden beschreven onder de uitkomstmaat huidreacties.
Spraakverstaan is indien beschikbaar meegenomen, aangezien gesuggereerd wordt dat het persisteren van vetweefsel (subcutis) rond het abutment (al dan niet in combinatie met een langer abutment) voor demping van het geluid zou kunnen zorgen en daarmee effect op het spraakverstaan.
Zoeken en selecteren (Methode)
In de databases Medline (OVID), Embase en Cochrane is vanaf 1990 tot en met juli 2016 met relevante zoektermen gezocht naar studies over de effecten van verschillende operatietechnieken bij BCD’s. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 112 treffers op. Er is besloten om te kijken naar systematische reviews van RCT’s en observationele studies en individuele RCT’s en observationele studies. Op basis van titel en abstract werden in eerste instantie 28 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 17 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording), en 11 studies definitief geselecteerd. Het gaat om 2 systematische reviews: Mohamed (2016); Verheij (2016). En 9 individuele studies met verschillend design (RCT of observationeel): Van der Pouw (1999); Mudry (2009); van de Berg (2010); Den Besten (2016); Hultcrantz (2014); Hultcrantz (2011); Hogsbro (2015); Brant (2013); Dumon (2016). De evidence-tabellen hiervan en beoordeling van individuele studiekwaliteit zijn weergegeven aan het einde van deze module.
- Berg R van de, Stokroos RJ, Hof JR, et al. Bone-anchored hearing aid: a comparison of surgical techniques. Otol Neurotol. 2010; 31(1):129-35.
- Besten CA den, Bosman AJ, Nelissen RC, et al. Controlled Clinical Trial on Bone-anchored Hearing Implants and a Surgical Technique With Soft-tissue Preservation. Otol Neurotol. 2016;37(5):504-12.
- Brant JA, Gudis D, Ruckenstein MJ. Results of Baha implantation using a small horizontal incision. Am J Otolaryngol. 2013;34(6):641-5.
- Dumon T, Medina M, Sperling NM. Punch and Drill: Implantation of Bone Anchored Hearing Device Through a Minimal Skin Punch Incision Versus Implantation With Dermatome and Soft Tissue Reduction. Ann Otol Rhinol Laryngol. 2016;125(3):199-206.
- Gordon SA, Coelho DH. Minimally Invasive Surgery for Osseointegrated Auditory Implants: A Comparison of Linear versus Punch Techniques. Otolaryngol Head Neck Surg. 2015;152(6):1089-93.
- Hogsbro M, Agger A, Johansen LV. Bone-anchored Hearing Implant Surgery: Randomized Trial of Dermatome Versus Linear Incision Without Soft Tissue Reduction--Clinical Measures. Otol Neurotol. 2015;36(5):805-11.
- Holgers KM, Tjellström A, Bjursten LM, et al. Soft tissue reactions around percutaneous implants: a clinical study of soft tissue conditions around skin-penetrating titanium implants for bone-anchored hearing aids. Am J Otol. 1988;9(1):569.
- Hultcrantz M. Outcome of the bone-anchored hearing aid procedure without skin thinning: a prospective clinical trial. Otol Neurotol. 2011;32(7):1134-9.
- Hultcrantz M, Lanis A. A five-year follow-up on the osseointegration of bone-anchored hearing device implantation without tissue reduction. Otol Neurotol. 2014;35(8):1480-5.
- Johansson en Holmberg. Design and clinical evaluation of MIPS A new perspective on tissue preservation. White Pap. Oticon Medical, Askim, Sweden, 2015, Rep. No. M524252.
- Martinez P, Lopez F, Gomez JR. Cutaneous complications in osseointegrated implants: comparison between classic and tissue preservation techniques. Acta Otorrinolaringol Esp. 2015;66(3):148-53.
- Mudry A. Bone-anchored hearing aids (BAHA): skin healing process for skin flap technique versus linear incision technique in the first three months after the implantation. Rev Laryngol Otol Rhinol (Bord). 2009;130(4-5):281-4.
- Stalfors J, Tjellstrom A. Skin reactions after BAHA surgery: a comparison between the U-graft technique and the BAHA dermatome. Otol Neurotol. 2008;29:11091114.
- Verheij E, Bezdjian A, Grolman W, et al. A Systematic Review on Complications of Tissue Preservation Surgical Techniques in Percutaneous Bone Conduction Hearing Devices. Otol Neurotol. 2016;3:3.
- Wilson DF, Kim HH. A minimally invasive technique for the implantation of bone-anchored hearing devices. Otolaryngol Head Neck Surg. 2013;149(3):473-7.
- Wolf MJF de, Hol MKS, Huygen PLM, et al. Clinical outcome of the simplified surgical technique for BAHA implantation. Otol Neurotol 2008;29:11008.
|
Zoekvraag 1 Individuele studies |
|||||||
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison/control (C)
|
Follow-up |
Outcome measures and effect size |
Comments |
|
Van de Berg, 2010 |
Type of study: Retrospective case study
Setting: Patients who received a BAHA at Maastricht University Medical Center (tertiary referral center) between nov 1996 and Jan 2007.
Country: Netherlands
Source of funding: Unknown |
Inclusion criteria: Patients who received a BAHA at Maastricht University Medical Center, the Netherlands between nov 1996 and Jan 2007 were included unless they met the exclusion criteria.
Exclusion criteria: Follow up of less than 3 months, the absence of a sufficient surgical record, a bilateral implant, and/or an extruded BAHA that required a new fitting.
N total at baseline: 143
Important characteristics: Age and sex: between 8-85 years old, 50% men.
Groups comparable at baseline? yes |
1=A free retroauricular “full-thickness”skin graft. |
2= A pedicled parieto-occipital epidermal “split-skin” graft. 3= A dermatome-pedicled parieto-occipital dermal graft. 4= Two local epidermal skin flaps. |
Length of follow-up: Between 3-147 months.
Loss-to-follow-up: 7 lost to follow up 12 stopped using their BAHA for several reasons |
Skin Complications Maximum of 4 major complications observed in techniques 1,2,4. Maximum of 3 major complications observed in technique 3 (non significant).
Skin revisions 1= 4 within 1 yr, 3 within 1-2 yr, 5 after 2 yrs 2= 6 within 1 yr, 6 within 1-2 yr, 2 after 2 yrs 3= 5 within 1 yr, 0 within 1-2 yr, 3 after 2 yrs 4= 2 within 1 yr, 1 within 1-2 yr, 0 after 2 yrs.
Reoperations 1= 1 within 1 yr, 0 within 1-2 yr, 1 after 2 yrs 2= 2 within 1 yr, 4 within 1-2 yr, 4 after 2 yrs 3= 3 within 1 yr, 0 within 1-2 yr, 3 after 2 yrs 4= 0 within 1 yr, 0 within 1-2 yr, 1 after 2 yrs. |
The outcome ‘complications’ is divided in two categories: 1 Major: Holgers class 3 &4, implant extrusion, abscess, flap necrosis. 2 Minor: Holgers 1 &2, wound dehiscence, pain & epidermal inclusion cyst. |
|
Mudry, 2009 |
Type of study: Retrospective cohort study
Setting: Patients receiving BAHA implantations.
Country: unknown
Source of funding: Unknown |
Inclusion criteria: Patients who received a BAHA between jan 2004 and December 2006.
Exclusion criteria: Not specified
N total at baseline: 113
Important characteristics: Age and sex: mean age 53.6 years. 59 females. 49 men.
Groups comparable at baseline? yes |
62 patients received skin flap technique using a flap of full thickness being prepared with a blade. |
51 implantations with the linear incision technique. |
Length of follow-up: 3 months
Loss-to-follow-up: 0 |
Necrosis 6.5% in skin flap technique and 1,9% in linear incision group (p=12,5%) |
|
|
Stalfors, 2008 |
Type of study: Retrospective cohort study
Setting: Patients receiving BAHA implantations between 2001 and 2004
Country: Sweden
Source of funding: Unknown |
Inclusion criteria: Patients who received a BAHA between march 2001 and November 2004.
Exclusion criteria: Patients from other parts of Sweden than the clinic, charts not found,
N total at baseline: 75
Important characteristics: Age and sex: 42 women, 33 men (male-to-female ratio for Ushape graft 24:26, male-to-female ratio for dermatome 9:16)
Age between 2-88 yrs, mean age 46 (mean age for U-shape graft 44yrs and for dermatome 59 yrs)
Groups comparable at baseline? yes |
45 patients U-shape graft technique |
25 dermatome
(4 patients had had a BAHA implant for between 4 and 19 years and had lost their implant and requested a new one, and 1 received free graft) |
Length of follow-up: Between 28-74 months Routine follow up was performed after 3 months. Subsequent follow ups were made after another 3 months and every 6 to 12 months.
Total of 373 observations
Loss-to-follow-up: 0 |
Skin reactions According to Holgers
Grading skin reactions U-shape graft group: 91,4% revealed a Grade 0 skin reaction.
Dermatome 95% revealed a Grade 0 skin reaction.
Frequency skin reactions U-shape graft group: 64% no adverse skin reaction (95% confidence interval 49-78%). (=29 patients), 15 patients had one episode, 1 patient experienced 2 episodes.
Dermatome group: 21 patients (84%, 95% confidence interval 64-95%) of the 25 patients experienced no skin reaction, 3 patients experienced a single episode, 1 patient had 2 episodes.
U-shape graft group 19,6% more skin reaction episodes compared to dermatome group p. 0.14. |
|
Risk of bias table for intervention studies (observational: non-randomized clinical trials, cohort and case-control studies) bij zoekvraag 1
|
Vraagstelling 1 Individuele studies |
||||
|
Study reference
(first author, year of publication) |
Bias due to a non-representative or ill-defined sample of patients?1
(unlikely/likely/unclear) |
Bias due to insufficiently long, orincomplete follow-up, or differences in follow-up between treatment groups?2
(unlikely/likely/unclear) |
Bias due to ill-defined or inadequately measured outcome ?3
(unlikely/likely/unclear) |
Bias due to inadequate adjustment for all important prognostic factors?4
(unlikely/likely/unclear) |
|
Van De Berg, 2010 |
Unlikely |
Likely, follow-up varies between 3-147 months |
Unlikely |
Unlikely |
|
Mudry, 2008 |
Unlikely |
Likely, only 3 months |
Unlikely |
Unlikely |
|
Stalfors |
Unlikely |
Likely, only 3 months |
Unlikely |
Unlikely |
- Failure to develop and apply appropriate eligibility criteria: a) case-control study: under- or over-matching in case-control studies; b) cohort study: selection of exposed and unexposed from different populations.
- 2 Bias is likely if: the percentage of patients lost to follow-up is large; or differs between treatment groups; or the reasons for loss to follow-up differ between treatment groups; or length of follow-up differs between treatment groups or is too short. The risk of bias is unclear if: the number of patients lost to follow-up; or the reasons why, are not reported.
- Flawed measurement, or differences in measurement of outcome in treatment and control group; bias may also result from a lack of blinding of those assessing outcomes (detection or information bias). If a study has hard (objective) outcome measures, like death, blinding of outcome assessment is not necessary. If a study has soft (subjective) outcome measures, like the assessment of an X-ray, blinding of outcome assessment is necessary.
- Failure to adequately measure all known prognostic factors and/or failure to adequately adjust for these factors in multivariate statistical analysis.
Zoekvraag 2
Table of quality assessment for systematic reviews of RCTs and observational studies bij zoekvraag 2
Based on AMSTAR checklist (Shea et al.; 2007, BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher et al 2009, PLoS Med 6:
e1000097; doi:10.1371/journal.pmed1000097)
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Verheij, 2016 |
Yes |
Yes |
No, only for included studies |
Yes |
Not applicable |
yes |
yes |
yes |
no |
- Research question (PICO) and inclusion criteria should be appropriate and predefined.
- Search period and strategy should be described; at least Medline searched; for pharmacological questions at least Medline + EMBASE searched.
- Potentially relevant studies that are excluded at final selection (after reading the full text) should be referenced with reason.
- Characteristics of individual studies relevant to research question (PICO), including potential confounders, should be reported.
- Results should be adequately controlled for potential confounders by multivariate analysis (not applicable for RCTs).
- Quality of individual studies should be assessed using a quality scoring tool or checklist (Jadad score, Newcastle-Ottawa scale, risk of bias table etcetera.)
- Clinical and statistical heterogeneity should be assessed; clinical: enough similarities in patient characteristics, intervention and definition of outcome measure to allow pooling? For pooled data: assessment of statistical heterogeneity using appropriate statistical tests (bijvoorbeeld Chi-square, I2)?
- An assessment of publication bias should include a combination of graphical aids (bijvoorbeeld funnel plot, other available tests) and/or statistical tests (bijvoorbeeld Egger regression test, Hedges-Olken). Note: If no test values or funnel plot included, score “no”. Score “yes” if mentions that publication bias could not be assessed because there were fewer than 10 included studies.
- Sources of support (including commercial co-authorship) should be reported in both the systematic review and the included studies. Note: To get a “yes,” source of funding or support must be indicated for the systematic review AND for each of the included studies.
Exclusietabel bij zoekvraag 1
|
|
Vraagstelling 1 |
|
Auteur en jaartal |
Redenen van exclusie |
|
Allis, 2014 |
Er wordt geen vergelijking gemaakt tussen verschillende technieken, maar tussen verschillende schroeflengtes bij de lineaire incisie. |
|
Faber, 2009 |
Er worden geen vergelijkingen gemaakt. |
|
Hobson, 2010 |
Er worden geen vergelijkingen gemaakt. |
|
Mierzwinski, 2015 |
Patiënten zijn Kinderen. |
|
Pouw, van der, 1999 |
Niet de juiste vergelijking. |
|
Ray 2012 |
Sheffield techniek is S vormig, geen lineaire incisie. Niet in vooraf beschreven vergelijkingen. |
|
Rompaey, Van, 2011 |
Geen vergelijking. |
|
Strijbos, 2016 |
Geen vergelijking tussen technieken. |
|
Wilkinson, 2009 |
Geen vergelijking, wel beschrijving resultaten lineaire incisie met uitdunning. |
|
Wolf, de, 2008 |
Geen vergelijking. |
Exclusietabel bij zoekvraag 2
|
Vraagstelling 2 |
|
|
Auteur en jaartal |
Redenen van exclusie |
|
Gordon, 2015 |
Zit in review Verheij 2016 en beschrijft geen aanvullende maten. |
|
Iseri, 2015 |
Er wordt geen vergelijking gemaakt tussen verschillende technieken. Er worden wel resultaten beschreven van tissue perservation. |
|
Kiringoda, 2013 |
Er wordt geen vergelijking gemaakt tussen verschillende technieken |
|
Lanis, 2013 |
Gaat uitsluitend over kinderen |
|
Martinez, 2015 |
Zit in review Verheij 2016 en beschrijft geen aanvullende maten. |
|
Mowinckel, 2016 |
Geen vergelijking tussen technieken. |
|
Snyder, 2003 |
Geen vergelijking |
Beoordelingsdatum en geldigheid
Publicatiedatum : 25-09-2018
Beoordeeld op geldigheid : 01-12-2018
Uiterlijk in 2021 bepaalt het bestuur van de NVKNO of modules in deze richtlijn nog actueel zijn. Zo nodig wordt een nieuwe werkgroep geïnstalleerd om de richtlijn te herzien. De geldigheid van de modules komen eerder te vervallen indien nieuwe ontwikkelingen aanleiding geven een herzieningstraject te starten. Bij enkele modules is de verwachting dat dit eerder dan na 3 jaar zal zijn en dus worden deze modules eerder op actualiteit beoordeeld.
De NVKNO is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
Het doel van deze richtlijn is het verkrijgen van duidelijkheid over de gewenste gang van zaken bij indicatiestelling, diagnostiek en behandeling met Bone conduction devices (BCD). Daarnaast wordt in deze richtlijn een kader geschetst voor de gewenste organisatie van zorg omtrent behandeling met BCD en de minimale informatievoorziening aan de patiënt. Dit alles moet bijdragen aan een meer eenduidig beleid bij het aanbieden van behandeling met BCD.
Doelgroep
Deze richtlijn is geschreven voor allen die betrokken zijn bij gehoorrevalidatie middels BCD. Dit betreft medisch specialisten (KNO-artsen, klinisch fysici-audiologen), maar ook alle andere betrokken zorgverleners en patiënten.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in november 2015 een werkgroep ingesteld, bestaande uit KNO-artsen en klinisch fysici-audiologen. De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep werkte gedurende 3 jaar aan de totstandkoming van de richtlijn. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
Werkgroep
- Dr. M.K.S. Hol, KNO-arts, Radboudumc , Nijmegen (voorzitter); NVKNO
- Ir. M.S. Toll, Klinisch fysicus-audioloog, Erasmus MC, Rotterdam (vicevoorzitter); NVKF
- Ir. T.T. Prinzen, Klinisch fysicus-audioloog, Pento Audiologisch Centrum, Amersfoort; NVKF
- Dr. ir. A.J. Bosman, Klinisch fysicus- audioloog, Radboudumc, Nijmegen; NVKF
- Drs. A.J.M. van der Rijt, KNO-arts, Amphia Ziekenhuis, Breda; NVKNO
- Dr. A. Frima-van Aarem, KNO-arts, Meander Medisch Centrum, Amersfoort; NVKNO
- Prof. dr. R.J. Stokroos, KNO-arts, UMC Utrecht, Utrecht; NVKNO
- Dr. S.J.H. Bom, KNO-arts, Deventer Ziekenhuis, Deventer; NVKNO
Met ondersteuning van:
- S. van Dijk MSc, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten;
- D. Leereveld MSc, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten;
- M.E. Wessels MSc, Literatuurspecialist, Kennisinstituut van de Federatie Medisch Specialisten;
- D.P. Gutierrez, Projectsecretaresse, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of ze in de laatste vijf jaar directe financiële (betrekking commercieel bedrijf, persoonlijke financiële belangen, onderzoek financiering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en oordeel over het omgaan met eventuele belangen vindt u hieronder. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van Medisch Specialisten.
|
Achternaam |
Functie |
Nevenfuncties |
Persoonlijke financiele belangen |
Persoonlijke relaties |
Reputatiemanagement |
Extern gefinancierd onderzoek |
Kennisvalorisatie |
Overige belangen |
Getekend |
Oordeel |
|
Frima-vanaarem |
KNO-arts, plaatsvervangend opleider |
nvt |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 1-10-2015 |
geen belemmeringen |
|
Bosman |
Klinisch fysicus-audioloog |
AudTutor - audiologie onderwijs en onderzoek. Dit zijn betaalde werkzaamheden |
geen |
geen |
geen |
Baha onderzoek. Ik ben momenteel betrokken bij de evaluatie van de Cochlear Baha SP-5 en P-5 toestellen en ontvang hiervoor een vergoeding. |
geen |
geen |
ja, 15-09-2015 |
deelname aan commissie, terugtrekken als onderwerpen van onderzoeken aan bod komen |
|
Hol (vz) |
KNO-arts |
Co-promotor 2 promovendi onderzoeks trials, research gelden uitbetaald aan Radboudumc voor zowel cochlear als oticon. Advisory board member oticon aangaande project BCI tijdelijke functie, start 2015. |
Advisory board, zie nevenfuncties |
geen |
geen |
geen |
geen |
geen |
ja, 29-09-2015 |
deelname aan commissie, met uitzondering van uitspraken over BCI. Nieuwe vragen vanuit Oticon, bespreken met werkgroep |
|
Barneveld, van |
Directeur |
Voorzitter richtlijn advies en autorisatiecommissie in de jeugd en gezondheidzorg Gezondheidsraadcommissie (Medicalisering) |
geen |
geen |
Werkzaam bij het Kennisinstituut van Medisch Specialisten. Dit instituut is een zelfstandig onderdeel van de Federatie Medisch Specialisten. Het instituut houdt zich onder andere bezig met Richtlijnontwikkeling in de 2e lijns curatieve zorg. |
geen |
geen |
geen |
ja, 14-12-2015 |
geen belemmeringen |
|
Leereveld |
adviseur Kennisinstituut van Medisch Specialisten |
nvt |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 7-12-2015 |
geen belemmeringen |
|
Prinzen |
Klinisch fysicus-audioloog 1 fte |
nvt |
geen |
geen |
geen |
geen |
geen |
geen |
ja,31-08-2015 |
geen belemmeringen |
|
Bom |
KNO-arts, full time |
plv. B-opleider lid werkgroep richtlijn perceptieve slechthorendheid secretaris regionale KNO-vereniging Rijn-Ijssel penningmeester vakgroep KNO-heekunde DZ en vertegenwoordiger vakgroep in stafmaatschap lid Capaciteitscommissie Ondersteuning Specialisten DZ |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 25-9-2015 |
geen belemmeringen |
|
Stokroos |
KNO -arts, 1.0 fte |
geen |
geen |
geen |
1.lid medische adviesraad neurofibromatose vereniging nederland |
als hoogleraar otologie/neurotologie heb ik diverse research activiteiten met financieringsbronnen zoals genoemd. Nadrukkelijk is er geen relatie tussen de uitkomsten van deze onderzoekingen en de financiering. Een en ander is onafhankelijk geborgd en gemonitord via CTCM (clinical trial center maastricht) |
geen patenten. Kennis en research op gebied van periabutment implantitis en chirurgische innovaties |
geen |
ja, 7-12-2015 |
geen belemmeringen |
|
Toll (vice- vz) |
Klinisch fysicus - audioloog |
bestuurslid (penningmeester) NVA (Nederlandse vereniging voor Audiologie) |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 5-10-2015 |
geen belemmeringen |
|
van Rijt |
KNO -arts, plaatsvervangend opleider |
participatie onderzoek gefinancierd door Cochlear, geen principal investigator (financiering via maatschap) |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 14-12-2015 |
geen belemmeringen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door tijdens de invitational conference, die werd gehouden in februari 2016 input te vragen van patiëntenvertegenwoordigers vanuit verschillende verenigingen. Tijdens de oriënterende zoekactie werd gezocht op literatuur naar patiëntenperspectief (zie Strategie voor zoeken en selecteren van literatuur). Er is daarnaast een module patiënteninformatie opgenomen in de richtlijn waarin wordt beschreven welke informatie een patiënt moet krijgen wanneer behandeling met BCD wordt overwogen of uitgevoerd. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de betrokken patiëntenorganisaties.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de belangrijkste aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is als aparte module opgenomen en zal later als aanverwant product worden toegevoegd. De richtlijn leent zich niet voor het ontwikkelen van indicatoren, omdat de aanbevelingen te weinig aanknopingspunten bieden om specifiek meetbare indicatoren voor op te stellen. Daarom is in de werkgroep besloten geen officiële indicatorenset te ontwikkelen bij de richtlijn.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen volgens het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is, en op de richtlijn voor richtlijnen voor de beoordeling van de kwaliteit van richtlijnen (http://www.zorginstituutnederland.nl).
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens zijn er knelpunten aangedragen door verschillende veldpartijen tijdens de invitational conference. Een verslag van deze bijeenkomst is opgenomen als aanverwant product.
De werkgroep stelde een long list met knelpunten op en prioriteerde de knelpunten op basis van: (1) klinische relevantie, (2) de beschikbaarheid van evidence van hoge kwaliteit, (3) en de te verwachten impact op de kwaliteit van zorg, patiëntveiligheid en (macro)kosten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk en onbelangrijk. Tevens definieerde de werkgroep voor de kritieke en belangrijke uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Er zijn twee oriënterende literatuursearches uitgevoerd naar bestaande buitenlandse richtlijnen, systematische reviews, en literatuur over patiëntenvoorkeuren (patiëntenperspectief). De resultaten hiervan zijn verwerkt in de overwegingen bij de verschillende uitgangsvragen. Vervolgens werd indien mogelijk voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module van de desbetreffende uitgangsvraag.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of bias tabellen.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij geen van de uitgangsvragen was er sprake van een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies om de resultaten ook kwantitatief samen te vatten in een meta-analyse.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen
Volgens de geldende afspraken binnen het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit, is ook in deze richtlijn gekozen om de kracht van het wetenschappelijk bewijs te bepalen volgende de GRADE-methode. GRADE staat voor Grading Recommendations Assessment, Development and Evaluation (Schünemann, 2013).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van vertrouwen in de literatuurconclusie (zie http://www.guidelinedevelopment.org/handbook/).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Het gebruik van de GRADE-methode impliceert dat enkel behandelingen getest met een RCT voldoende evident (voldoende krachtig van bewijs) zijn. Echter, als de nieuwe behandeling objectief gezien (dus met harde data in de hand) beter is dan de bestaande behandelingen, dan is een RCT niet nodig. Dit is duidelijk doordat zintuiglijke behandelingen bij oorheelkundige (maar ook bijv. bij oogheelkundige patiënten), eenvoudigweg als controle op en van zichzelf gebruik maken door apparatuur wel/niet aan te sluiten.
Behandeling met een BCD is een relatief zeldzame ingreep die ook wordt toegepast bij een kwetsbare patiëntenpopulatie (verstandelijk beperkten, ouderen, kinderen). Om deze reden zijn grote, gerandomiseerde interventiestudies in deze setting praktisch niet haalbaar en zijn de conclusies in de module ‘Indicatiestelling voor BCD’ niet gegradeerd. Soms wordt de behandeling toegepast als er (grote) communicatieve nood is en er géén alternatieven zijn, de conventioneel indicatie. Gezien de objectiviteit van de metingen en duidelijke verschillen tussen het horen mét en zonder hulp van BCD is het toch mogelijk om sterke aanbevelingen te doen. Dit wordt onderbouwd in de overwegingen.
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008), en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Bij interventievragen verwijst de conclusie niet naar één of meer artikelen, maar wordt getrokken op basis van alle studies samen (body of evidence). Hierbij maakten de werkgroepleden de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje Overwegingen.
Overwegingen
Om te komen tot een aanbeveling in deze richtlijn zijn, naast weging van de kwaliteit van het wetenschappelijke bewijs volgens GRADE, met name andere aspecten belangrijk en worden deze evengoed meegewogen in de overwegingen. Hierbij kan gedacht worden aan de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patiënt values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje Overwegingen.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de Kennislacunes beschreven (onder aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Leeswijzer
Onderstaande conceptrichtlijntekst wordt na het doorlopen van de commentaar- en autorisatiefase opgenomen in de Richtlijnendatabase (http://www.richtlijnendatabase.nl). Verwijzingen naar tabbladen zijn in de huidige versie van de richtlijntekst terug te vinden in de aanverwante producten.
Literatuur
Brouwers MC, Kho ME, Browman GP, Burgers JS, et al.; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;14;182(18):E839-42. Review. PubMed PMID: 20603348.
Medisch Specialistische Richtlijnen 2.0. Adviescommissie Richtlijnen van de Raad Kwaliteit. Beschikbaar via: https://www.demedischspecialist.nl/onderwerp/raad-kwaliteit. 2012.
Richtlijn voor Richtlijnen (2012; herziene versie). Regieraad Kwaliteit van Zorg Beschikbaar via: http://www.zorginstituutnederland.nl. 2012.
Schünemann H, Brożek J, Guyatt G, et al. Editors. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html. 2013.
Schünemann HJ, Oxman AD, Brozek J, et al.;GRADE Working Group. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;17;336(7653):1106-10. PubMed PMID: 18483053.
Zoekverantwoording
|
Uitgangsvragen: 1) Welke operatietechniek (een (Nijmeegse) lineaire incisie met huiduitdunning, dermatoom techniek of een U–flap) is het meest effectief en geeft de minste kans op bijwerkingen bij volwassenen met een indicatie voor een percutane Bone conduction device?; 2) Welke incisievorm (lineaire incisie standaard met tissue reduction (i.e. huiduitdunning) of tissue preservation (zonder huiduitdunning)) is het meest effectief en geeft de minste kans op bijwerkingen bij volwassenen? |
|
|
Database(s): Medline, Embase |
Datum: 11-07-2016 |
|
Periode: 1990-heden |
Talen: E N D |
|
Database |
Zoektermen |
Totaal |
|
Medline 1990-juli 2016 Engels, |
1 hearing loss/ or hearing loss, conductive/ or hearing loss, mixed conductive-sensorineural/ or hearing loss, unilateral/ or Hearing Loss, Bilateral/ or (hearing adj3 (loss* or disorder* or impairment*)).ti,ab. or "Ear"/ab or Hearing Disorders/ (61283) 2 "Bone Conduction"/ or (bone adj3 conduction).ti,ab. or "Osseointegration"/ or (osseointegrat* or osseo-integrat*).ti,ab. (15802) 3 "Hearing Aids"/ or "hearing aid*".ti,ab. or "correction of hearing impairment"/ or communication methods, total/ (10928) 4 2 and 3 (740) 5 (("bone conduction" or "bone anchored" or "bone vibrat*") adj3 (device* or aid* or implant* or prosthes* or hearing or transducer*)).ti,ab. (1087) 6 (bcd or tbcd or pbcd).ti,ab. (874) 7 (baha* or ponto or bci).ti,ab. (5072) 8 6 or 7 (5942) 9 1 and 8 (350) 10 4 or 5 or 9 (1393) 11 limit 10 to (yr="1990 -Current" and (dutch or english or german)) (1134) 12 "Otologic Surgical Procedures"/mt, is or "Prosthesis Implantation"/ or (surg* or operati*).ti,ab. or hearing loss/su or hearing loss, conductive/su or hearing loss, mixed conductive-sensorineural/su or hearing loss, unilateral/su or Hearing Loss, Bilateral/su (1984571) 13 ("linear incision*" or Hultcrantz* or Nijmegen*).ti,ab. (1955) 14 (tissue* adj3 (reduction* or preservation*)).ti,ab. (5529) 15 "Surgical Flaps"/ or ((skin or epidermal) adj2 graft*).ti,ab. or dermatome*.ti,ab. or (skin adj3 (envelop* or flap*)).ti,ab. (69237) 16 12 or 13 or 14 or 15 (2027943) 17 11 and 16 (664) 18 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (290915) 19 17 and 18 (27) 20 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1594894) 21 17 and 20 (74) 22 Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw,kw. or (cohort adj (study or studies)).tw,kw. or Cohort analy$.tw,kw. or (Follow up adj (study or studies)).tw,kw. or (observational adj (study or studies)).tw,kw. or Longitudinal.tw,kw. or Retrospective.tw,kw. or Prospective.tw,kw. or Cross sectional.tw,kw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ or comparative study.pt. [Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies] (3795676) 23 17 and 22 (348) 24 19 or 21 or 23 (391) 43 19 or 21 (97) 44 remove duplicates from 43 (95) 45 24 not 43 (294) 46 remove duplicates from 45 (292) |
402 |
