Lithium bij bipolaire stoornis
Uit de Cochranereview van 2001 over lithium als onderhoudsbehandeling bleek dat er onvoldoende data waren over specifieke bijwerkingen om een meta-analyse te doen. Een uitzondering hierop was hypothyreoïdie, wat voorkwam bij 5% van de patiënten die lithium gebruiken, en bij geen van de patiënten met placebo (Burgess e.a., 2001).
In een meta-analyse uit 2012 werd lithium geassocieerd met een verhoogd risico op endocriene bijwerkingen zoals hypothyreoïdie en hyperparathyreoïdie, en een verhoogd risico op een verminderd urineconcentrerend vermogen van de nieren (McKnight e.a., 2012).
Preparaten
De voorkeurspreparaten zijn Camcolit 400 mg en Priadel (beide lithiumcarbonaat; 10,8 mmol lithium per tablet van 400 mg; piekspiegel (Tmax) 2-3 uur na inname). De generieke lithiumcarbonaatpreparaten (tabletten van 100, 200, 300 of 400 mg) hebben niet de voorkeur, omdat zij vaker een vieze smaak hebben omdat de tabletten niet gecoat zijn (en daardoor meer aanleiding geven tot verminderde therapietrouw) en omdat de diverse doseringssterkten aanleiding kunnen geven tot vergissingen (en daardoor tot intoxicaties of ineffectiviteit).
Regelmatige bepaling van de lithiumspiegel is onontbeerlijk vanwege de grote interindividuele en intra-individuele verschillen in farmacokinetiek (de halfwaardetijd (T1/2) is 12-48 uur bij normale nierfunctie) en het smalle therapeutische venster.
De standaarddosering is bij voorkeur eenmaal daags (vanwege betere therapietrouw) in de avond (vanwege meting na 12 uur in de ochtend). Een nadeel hiervan is dat de piekspiegel vanwege het circadiane ritme van de lithiumklaring valt op het moment van laagste klaring van de nier. Lithiumcitraat (Litarex) is het enige lithiumpreparaat met vertraagde afgifte en kan voor patiënten met bijwerkingen op Priadel of Camcolit een goed alternatief zijn. Lithiumcitraat is in Nederland niet meer geregistreerd, maar kan met een artsenverklaring uit het buitenland worden geïmporteerd (houd rekening met een potentieel lange levertijd).
Periodieke controles
Bij aanvang van behandeling met lithium zijn de somatische controles, zoals beschreven in de vorige submodule aangevuld met op indicatie schildklierantistoffen (thyroïdperoxidase: TPO) en bijschildklierfunctie (parathyreoïdhormoon: PTH).
Creatinine (inclusief een schatting van de GFR: de glomerular filtration rate, oftewel glomerulusfiltratiesnelheid) worden elke 3-6 maanden gecontroleerd, calcium, thyroïdstimulerend hormoon (TSH), en gewicht na zes maanden en daarna minimaal elk jaar. Op indicatie worden de controles frequenter herhaald, bijvoorbeeld bij nierfunctiestoornissen.
Lithiumspiegels
De lithiumspiegels worden minstens elke 3-6 maanden bepaald, of 5-7 dagen na iedere dosisaanpassing, en op klinische indicatie, zoals na starten, stoppen of dosiswijziging van potentieel interacterende medicatie.
- Een lithiumspiegel is altijd een dalspiegel (12 (+/– 1) uur na inname).
- Een lithiumserumspiegel wordt in het algemeen bepaald na bereiken van steady state. Steady state wordt bereikt na 5 × de halfwaardetijd (T1/2 = 12-48 uur). Als vuistregel kan lithium bepaald worden 5-7 dagen na instellen en idem na elke dosisverandering.
- Bij de acute manie kan de spiegel al na 3 dagen worden bepaald om te voorkomen dat er te hoog wordt gedoseerd (dit is nog geen steadystatespiegel). Bij een te hoge spiegel dient men de dosis te verlagen, bij een te lage spiegel dient men de huidige dosis vooralsnog te handhaven tot een steady-statespiegel bekend is en vervolgens de dosis bij te stellen.
De aanbevolen bloedspiegels zijn oorspronkelijk gebaseerd op een tweemaaldaagse inname. Het is echter onduidelijk of dit consequenties heeft voor aan te houden bloedspiegels. De richtlijncommissie adviseert daarom de aanbevolen bloedspiegels te hanteren ongeacht de doseerfrequentie, en de dosis aan te passen op geleide van bijwerkingen en gebleken effectiviteit bij de individuele patiënt.
Instellen op lithium gebeurt bij voorkeur via de titratiemethode (geleidelijk verhogen van de spiegel volgens herhaalde bloedspiegelmetingen), en niet via een testdosis-schattingsmethode (Geeraerts & Sienaert, 2013). Er zijn aanwijzingen dat het langdurig handhaven van lithiumspiegels boven de 1,0 mmol/l tot nierfunctiestoornissen kan leiden. Ook hypertensie en een hogere leeftijd zijn bijkomende risicofactoren voor nierfunctiestoornissen.
Nierfunctie
Als de geschatte glomerulaire filtratiesnelheid (GFR), bepaald met de CKD-EPI formule uit 2009 (standaard gerapporteerd door vrijwel alle laboratoria) buiten het referentiegebied komt of een dalende trend vertoont, wordt minstens tweemaal per jaar de GFR herhaald en wordt tenminste jaarlijks een kwalitatief urineonderzoek gedaan. Dat bestaat uit een urine sediment inclusief eiwitbepaling om te screenen op andere oorzaken van verminderde nierfunctie (het sediment is normaal bij lithium nefropathie) en ochtendurineosmolariteit (om een globale indruk te krijgen van het concentrerend vermogen van de nieren).
Een patiënt wordt besproken met, en eventueel verwezen naar een internist, internist-ouderengeneeskunde, internist-nefroloog of klinisch geriater bij de volgende afwijkingen:
- een geschatte glomerulusfiltratiesnelheid (GFR) onder de 60 ml/min;
- een daling van de GFR van meer dan 5 ml/min per jaar;
- bij een vermoeden van diabetes insipidus (productie van meer dan 3 liter urine per 24 uur of anderszins onverklaarde polydipsie).
Voor uitgebreide bespreking van renale bijwerkingen bij chronisch lithiumgebruik (renale diabetes insipidus, chronische nierinsufficiëntie) wordt verwezen naar de Richtlijn renale bijwerkingen chronisch lithiumgebruik (De Beus & Rookmaaker, 2013, zie www.nefrovisie.nl/richtlijnen-indicatoren) van de Nederlandse federatie voor Nefrologie. Deze richtlijn voor internisten wordt naar verwachting in 2025-2026 geactualiseerd.
Arginine vasopressine (AVP) resistentie (renale diabetes insipidus)
Van de langdurige gebruikers van lithium heeft tot 17% polyurie (urineproductie van meer dan 3 l per dag)(Gitlin & Bauer 2023) en 59% een verminderd concentrerend vermogen (urineosmolariteit < 800 mosmol/kg) (Tabibzadeh 2022). De diagnose renale diabetes insipidus wordt definitief gesteld met de DDAVP-test (dorstproef, gevolgd door door DDAVP = 1-deamino-8-D-arginine-vasopressine) (De Beus & Rookmaaker, 2013). De positie van het bepalen van copeptin, een split-product van arginine-vasopressive (AVP; ook wel ‘vasopressine’ of ‘antidiuretisch hormoon’ [ADH] genoemd), is nog niet duidelijk.
Deze diagnostiek valt buiten de competentie van de psychiatrie en wordt uitgevoerd binnen de nefrologie.
Om renale diabetes insipidus te voorkomen, is het verstandig de laagst effectieve dosis lithium te gebruiken, al ontbreken er klinische trials die dit bewijzen. Vooral als AVP-resistentie door lithium nog maar relatief kort (enkele jaren) bestaat, kan er een plaats zijn voor het gebruik van amiloride. Dit diureticum remt de opname van lithium in de zogenaamde hoofdcellen van de tubuli, die verantwoordelijk zijn voor het concentreren van de urine. Urine concentrerend vermogen kan in deze vroege fase deels herstellen.
Manifeste polyurie door lithium geïnduceerde AVP resistentie kan doorgaans goed behandeld worden met thiazide diuretica, zoals hydrochlorothiazide. Dit middel verlaagt het volume-aanbod aan de verzamelbuizen, die door lithium verminderd functioneel zijn. Hierdoor wordt er minder terugresorptie van water in dit aangedane segment gevraagd en neemt de 24-uurs urineproductie af. Dit kan gunstige effecten hebben op de kwaliteit van leven en de slaapkwaliteit verbeteren. Bij instellen op (een combinatie van) diuretica (uitgezonderd monotherapie met amiloride) wordt aanbevolen om de lithiumdosis vooraf met een kwart tot een derde te verminderen, en deze te vervolgen, om op geleide hiervan de lithiumdosis bij te stellen. Ook moet men alert zijn op het ontstaan van hyperkaliëmie bij gebruik van amiloride en op hypokaliemie bij gebruik van thiazide diuretica. Daarom moet het kalium binnen enkele weken na de start van een diureticum worden gecontroleerd. Dan wordt ook de (12-uurs) lithiumspiegel bepaald, die immers kan veranderen bij gebruik van een diureticum. Aangezien diuretica ook na langere tijd afwijkende kaliumwaarden kan veroorzaken, moet bij gebruik van een diureticum het kalium eenmaal per jaar worden gecontroleerd. De behandeling van lithium-gerelateerde renale diabetes insipidus met een diureticum vindt bij voorkeur plaats in samenwerking met een internist, internist-ouderengeneeskunde, internist-nefroloog of klinisch geriater.
Daarnaast kan een eiwit- en zoutbeperkt dieet de polyurie doen afnemen. Omdat lithium net als natrium proximaal wordt teruggeresorbeerd zal in geval van verhoogde terugresorptie van natrium ook de terugresorptie van lithium toenemen. Daardoor zal bij een natriumbeperkt dieet er meer lithium terugresorptie vanuit de nier optreden en dus de spiegel kunnen stijgen. Hiermee moet dus bij voorbaat rekening gehouden worden.
Chronische nierinsufficiëntie
Een klinisch relevante afname van de nierfunctie komt voor bij naar schatting 26% van langdurige gebruikers (Schoretsanitis e.a., 2021). Als door het gebruik van lithium nierinsufficiëntie ontstaat, moet het staken van lithium overwogen worden. Echter moeten ook andere oorzaken van een fnemende nierfunctie worden uitgesloten. Hierbij moet de gebleken effectiviteit van de lithiumprofylaxe, en het al dan niet beschikbaarheid van alternatieven voor deze patiënt, worden afgewogen tegen het risico van verdere achteruitgang van de nierfunctie en de daarmee geassocieerde cardiovasculaire risico’s. De leeftijd van de patiënt speelt daarbij ook een rol: hoe ouder de patiënt is (d.w.z. kortere levensverwachting), des te kleiner is de uiteindelijke kans op terminaal nierfalen en dialyse. Dit overleg moet plaatsvinden in samenspraak met patiënt, naaste, internist-nefroloog en psychiater.
Als de klaring een enigszins arbitrair gekozen waarde van 40 ml/min dreigt te naderen, wordt geadviseerd om het staken van lithium te overwegen. Daarbij moet worden bedacht dat hoe lager de GFR inmiddels is, hoe kleiner de kans is op reversibiliteit na staken. Bij een snel progressieve daling van de nierfunctie (bijvoorbeeld verlies van > 5 ml/jaar) moet al bij een klaring van boven de 40 ml/min het staken van lithium overwogen worden. Het is raadzaam om bij een afnemende nierfunctie tijdig te overleggen met een internist-nefroloog.
Schildklierfunctie
Bij een afwijkende waarde van thyroïdstimulerend hormoon (TSH) wordt vrij T4 (FT4 ) bepaald. Als ook het vrij T4 afwijkend is, wordt de patiënt verwezen naar een internist; anders volgt weer controle na drie maanden. Andere oorzaken van verlaagde schildklierindices dan lithium moeten worden nagegaan, eventueel in overleg met een internist Suppletie met levothyroxine is geïndiceerd bij hypothyreoïdie en bij subklinische hypothyreoïdie met een tsh > 10 mU/l (met of zonder tpo-antistoffen). Suppletie met levothyroxine kan overwogen worden bij:
- subklinische hypothyreoïdie met een tsh 5-10 mU/l en tevens tpoantistoffen;
- en/of een verhoogd risico voor hart- en vaatziekten;
- en/of bij zwangerschap;
- en/of indien er cognitieve of stemmingsverschijnselen zijn.
Bij patiënten jonger dan 60 jaar zonder cardiale comorbiditeit kan gestart worden met de volledige substitutiedosis van 1,6 mcg levothyroxine per kg lichaamsgewicht (Van Lieshout e.a., 2013). Dit komt voor een volwassene van 65 kg neer op 100 mcg. Een veilige maximale startdosis lijkt 150 mcg levothyroxine. Na 6 weken worden TSH en vrije T4 gecontroleerd en wordt het effect besproken met de patiënt, evenals eventuele bijwerkingen, mogelijke cardiale klachten, en vragen over de medicatie. De dosis levothyroxine kan verhoogd worden met 12,5 tot 25 mcg met intervallen van 6 weken indien er nog klachten zijn en/of als het tsh nog verhoogd is. De mate van ophoging hangt af van de ernst van de klachten en het tsh en het vrije T4 . Bij patiënten jonger dan 60 jaar met cardiale comorbiditeit, actueel of in de voorgeschiedenis, en patiënten ouder dan 60 jaar, wordt de dosering altijd stapsgewijs verhoogd. Er wordt gestart met 12,5 tot 25 mcg levothyroxine; de hoogte van startdosering hangt af van de leeftijd van de patiënt, de ernst van de cardiale comorbiditeit en de duur van de hypothyreoïdie. De dosering kan na minstens 2 weken steeds verhoogd worden met 12,5 mcg levothyroxine tot een dagdosering van 50 mcg. Na 6 weken worden TSH en vrije T4 gecontroleerd en wordt het effect besproken met de patiënten evenals eventuele bijwerkingen, in het bijzonder mogelijke cardiale klachten en vragen over de medicatie. De dosis levothyroxine kan vervolgens verhoogd worden met 12,5 mcg met intervallen van 6 weken tot de patiënt klachtenvrij is, dan wel zich zo optimaal mogelijk voelt en het TSH en vrije T4 normaal zijn.
Voor beide groepen geldt: maak afspraken met de preferente apotheker over het afleveren van steeds hetzelfde geneesmiddelmerk levothyroxine, vanwege mogelijke verschillen in resorptie. Instrueer de patiënt om de tabletten eenmaal daags in te nemen, steeds op hetzelfde tijdstip en op een lege maag met steeds dezelfde tijdsduur voor de maaltijd, bij voorkeur een halfuur. Pas de dosering levothyroxine aan op geleide van de klachten van de patiënt en streef daarbij naar een normale tsh en een normale vrije T4 , met in achtneming van het feit dat het tsh en het vrije T4 sneller verbeteren dan de klachten. Een kleine verhoging van de dosering met 12,5 mcg levothyroxine, ook al zijn TSH en vrije T4 al normaal, kan ervoor zorgen dat de patiënt zich beter voelt. Controleer het TSH en het vrije T4 pas 6 weken na elke doseringsverandering, aangezien het TSH dan pas is gestabiliseerd.
Bijschildklierfunctie
McKnight e.a. (2012) vonden in hun meta-analyse een 10% hogere waarde van parathyreoïdhormoon (PTH) en calcium bij chronisch lithiumgebruikers ten opzichte van controles.
Een te laag calcium (gecorrigeerde waarden onder 2,15) wordt vaak veroorzaakt door vitamine D-tekort. Maar er zijn ook andere oorzaken, zoals nierinsufficiëntie en magnesiumtekort, waarbij overleg met een internist geïndiceerd is.
Voor correctie moet calcium altijd in combinatie met albumine bepaald worden, of in geïoniseerde vorm. Vervolgens wordt voor de normaalwaarde de volgende correctie toegepast:
((44 – gemeten albumine) × 0,02) + gemeten calcium.
Bij een verhoogd calcium kan er vooral bij ouderen relatief vaak sprake zal zijn van osteogeen gemetastaseerde maligniteiten. De overige oorzaken zoals hyperparathyreoïdie zijn bij ouderen zeldzamer.
Vanwege de vaak voorkomende neuropsychiatrische uitingen van hypercalciëmie en de dehydratie die daarvan het gevolg is, moet bij alle waarden boven de bovengrens van normaal over deze patiënten overleg gepleegd worden met een internist.
Het pathologische beeld bij lithiumgeassocieerde hyperparathyreoïdie is meestal bijschildklieradenoom (2/3) en soms bijschildklierhyperplasie (1/3) (McHenry & Lee, 1996).
Voor aanvang van behandeling met lithium wordt geadviseerd preexistente hypercalciëmie en hyperparathyreoïdie uit te sluiten, daarna wordt geadviseerd serum-calcium en PTH tweemaal per jaar te controleren (De Beus & Rookmaaker, 2013).
Lithiumintoxicatie
Een lithiumintoxicatie is een ernstige en potentieel levensbedreigende toestand waarbij onmiddellijk ingrijpen noodzakelijk is. Een acute intoxicatie kan het gevolg zijn van een eenmalige inname van een hoge dosis bij een lithiumnaïeve patiënt, of een auto-intoxicatie (tentamen suicidii) bij een patiënt die lithium gebruikt.
Geleidelijke oftewel chronische intoxicatie komt veel vaker voor dan acute intoxicatie. Chronische intoxicatie kan verschillende oorzaken hebben. De meest voorkomende oorzaak is een (geleidelijke) achteruitgang in nierfunctie. Daarnaast kunnen er andere oorzaken zijn: te hoge dosering/of vergissing in dosering; een verstoorde water- en zoutbalans (bijvoorbeeld door overschakelen op een zoutarm dieet, door natriumverlies bij hevig transpireren (verblijf in de tropen!), bij hoge koorts, bij braken of diarree), te weinig eten en drinken, diureticagebruik, of gebruik van NSAID’s. Een chronische intoxicatie is ernstiger omdat het kan leiden tot irreversibele symptomen (cerebrale toxiciteit).
Intoxicatieverschijnselen treden meestal op bij bloedspiegels boven 1,5-2,0 mmol/l, maar kunnen ook bij lagere en zelfs bij therapeutische spiegels voorkomen. De therapeutische breedte is vastgesteld op populatieniveau. Voor iedere individuele patiënt wordt een specifieke optimale spiegel vastgesteld. Als die spiegel stijgt of daalt, kan dat gevolgen hebben voor de effectiviteit of de toxiciteit van de lithium.
De symptomen van een lithiumintoxicatie kunnen verward worden met algeheel ziek zijn. Dat kan ertoe leiden dat een intoxicatie niet vroegtijdig herkend wordt, wat een risico kan geven op ontstaan van een chronische intoxicatie met irreversibele schade. Daarom moeten zowel de behandelaar als de patiënt en diens naastbetrokkenen goed op de hoogte zijn van (beginnende) intoxicatieverschijnselen. Vroege intoxicatieverschijnselen zijn:
- verminderde eetlust, misselijkheid, braken, diarree;
- spierzwakte, grove tremor (handen!), spierschokjes, ataxie, dysartrie;
- slaperigheid, sufheid en traagheid;
- afname polsfrequentie, ecg-veranderingen (verkleining qrs-complex, afvlakking T-toppen);
- breed gangspoor (cave verwarring met dronkenschap).
Late intoxicatieverschijnselen zijn:
- opwinding (cave verwarring met manie!);
- hypertonie en fasciculaties van de spieren, hyperreflexie, nystagmus;
- insulten;
- bewustzijnsdaling tot (sub)coma;
- oligurie tot anurie;
- EEG-afwijkingen.
De behandeling van een intoxicatie bestaat uit het onmiddellijk staken van lithium en alle interacterende medicatie. Bij een vermoeden van een intoxicatie kan de patiënt ingestuurd worden naar een algemeen ziekenhuis voor verdere diagnostiek en behandeling (www.toxicologie.org), alwaar indien nog mogelijk (< 1 uur na inname) de maag gespoeld kan worden bij recente auto-intoxicatie (geen kool bij lithium-mono-intoxicatie, wel bij vermoeden van een acute intoxicatie met meerdere middelen). Verder kan er somatisch onderzoek verricht worden en controle van de lithiumspiegel en van de water- en elektrolytenbalans.
Bij lichte of beginnende intoxicatieverschijnselen door water- en zouttekort kunnen verschijnselen worden bestreden met stoppen van het lithium en het innemen van water en zout (bouillon drinken).
Bij ernstige verschijnselen en/of bloedspiegel > 2,0 mmol/l kan ziekenhuisopname, infuusbehandeling en zelfs hemodialyse nodig zijn. Lithiumspiegels kunnen na het staken van hemodialyse opnieuw stijgen door vrijkomen van intracellulair lithium en doorgaande opname vanuit de darm bij inname van grote hoeveelheden ineens (ook bij een chronische intoxicatie), dus de behandeling mag niet te snel gestaakt worden. Staak de hemodialyse indien 6-8 uur na de laatste hemodialyse de spiegel < 1,0 mmol/l bedraagt.
Na langere lithiumintoxicaties hoeft de bloedspiegel niet de spiegel in het centrale zenuwstelsel te weerspiegelen.
Interacties
Lithiumspiegels worden beïnvloed door gelijktijdig gebruik van middelen die interfereren met opname en klaring van lithium. In de praktijk is het verstandig om te anticiperen op de spiegelverhogende of -verlagende effecten van interacterende medicatie zoals diuretica, ACE-remmers en NSAID's.
Als praktische leidraad wordt vaak geadviseerd de lithiumdosering 30-50% aan te passen alvorens een medicament te starten waarvan bekend is dat het de lithiumspiegel kan beïnvloeden. Hierna dient zowel de lithiumspiegel als de nierfunctie na 5-7 dagen gecontroleerd te worden.
Bij het staken van medicatie die een effect heeft op de lithiumspiegel moet geanticipeerd worden op het omgekeerde effect op de lithiumspiegel. Hier wordt niet standaard op bewaakt met de huidige medicatiebewakingssystemen. Staken van potentieel interacterende medicatie vereist dus extra oplettendheid.
De kans op het serotoninesyndroom is toegenomen bij combinatie met SSRI's of monoamineoxidaseremmers (MAO-remmers). Carbamazepine kan de neurotoxiciteit van lithium verhogen.
Perioperatieve aanbevelingen
Lithium is geen absolute contra-indicatie bij spoedeisende operaties. Om (vooral bij operaties met risico op hemodynamische instabiliteit) een postoperatieve lithiumintoxicatie te vermijden, gelden (afgezien van kleine ingrepen onder lokale anesthesie) de volgende aanbevelingen.
- Vooraf de schildklierfunctie, en de natrium-, kalium- en creatinineconcentratie controleren.
- Vanwege frequent voorkomende polydipsie bij lithium en voor het handhaven van een goede postoperatieve vochtbalans voorafgaande aan de operatie: meet de vochtintake.
- De lithiuminname 72 uur voorafgaande aan electieve operaties staken en de volumestatus en elektrolytenhuishouding perioperatief bewaken.
- Zodra de water- en zouthuishouding stabiel is en de patiënt weer kan drinken, de lithiuminname in de oorspronkelijke dosis hervatten, met een spiegelcontrole na 5-7 dagen. Daarbij is het dan van belang dat de patiënt ook de voor hem gebruikelijke hoeveelheid vocht aangeboden krijgt (eventueel per infuus).
- Schakel een consultatieve psychiatrische dienst in voor bewaking van de lithiumtherapie tijdens ziekenhuisopname.
- In overleg met de anesthesioloog kan bijvoorbeeld de lithiumdosis 30-50% gereduceerd worden (eventueel met tijdelijk gebruik van een antipsychoticum). Dit is vaak al effectief en het geeft minder kans op psychiatrische ontregeling.
Kinderen en adolescenten
Lithium mag in Nederland voorgeschreven worden vanaf de leeftijd van 12 jaar (www.cbg-meb.nl). Lithium wordt door jongeren over het algemeen goed verdragen. Bij adolescenten zijn dezelfde somatische controles nodig als bij volwassenen.
De farmacokinetiek van lithium laat ten opzichte van volwassenen bij adolescenten wel enkele verschillen zien waarmee rekening gehouden dient te worden. Door een onderzoek van Findling e.a. (2010) werd duidelijk dat de eliminatiehalfwaardetijd van lithium bij adolescenten korter is door een verhoogde klaring door de nieren. Dit heeft tot gevolg dat er bij adolescenten vaker een hogere dosering lithium noodzakelijk is om een lithiumspiegel te bereiken binnen de therapeutische breedte.
De farmacokinetiek wordt beïnvloed door het gewicht. Verdeel daarom afhankelijk van het gewicht de doses over meerdere tijdstippen per dag (2-3) in de eerste weken. Vervolgens kan dan overgegaan worden op een eenmalige dosis, om de therapietrouw te vergroten. Adolescenten verdragen vaker zonder noemenswaardige bijwerkingen een hoge lithiumspiegel; het is van belang jongeren expliciet informatie te geven over het risico op lithiumintoxicatie bij hoge temperaturen (vakanties) en in combinatie met alcoholgebruik.
Ouderen
De aanbevolen therapeutische bloedspiegels zijn bij ouderen niet lager dan bij jongere volwassenen. Wel wordt een therapeutische lithiumspiegel vaak al bereikt met een 25-50% lagere dagdosis dan bij jongere volwassenen (Sajatovic e.a., 2005). Door een verminderde nierfunctie kan de eliminatiehalfwaardetijd van lithium toenemen (36-48 uur, tegenover circa 24 uur bij jongere volwassenen). Het kan tot 10 dagen duren voordat een stabielespiegel wordt bereikt (Licht e.a., 2003). Een lithiumspiegel van 0,4-0,6 mmol/l kan voldoende zijn, maar soms is 0,8 mmol/l pas effectief.
De lithiumspiegel zal bij ouderen sneller stijgen bij uitdroging door transpiratie, braken, diarree of onvoldoende vochtinname postoperatief, maar ook door comedicatie van bijvoorbeeld diuretica met ace-remmers en nsaid’s. Somatische comorbiditeit kan intoxicatieverschijnselen maskeren. Net als bij jongere volwassenen is het klinische beeld en niet de lithiumspiegel bepalend voor het vaststellen van een lithiumintoxicatie. De bloedspiegel en liquorspiegel van lithium correleren bij ouderen in tegenstelling tot bij jongere volwassenen niet altijd.
Verder zijn ouderen kwetsbaarder voor bijwerkingen als gevolg van veranderde farmacokinetiek en -dynamiek en interacties met andere medicijnen. Bij ouderen komen vaker nierfunctiestoornissen voor als gevolg van supratherapeutische lithiumspiegels, intoxicaties, andere medicatie (vooral diuretia en ace-remmers), somatische comorbiditeit (vooral diabetes mellitus en hypertensie) en een leeftijdgerelateerde afgenomen nierfunctie (Rej e.a., 2012).
Het wordt aanbevolen om het bloed minstens elke 3-6 maanden te controleren op: lithiumspiegel, calcium, creatinine, glomerulusfiltratiesnelheid (GFR) en schildklierfunctie. Bij ouderen kan de creatinineklaring een betrouwbaarder maat zijn voor de nierfunctie dan het serum-creatininegehalte, omdat deze maat rekening houdt met de leeftijdsgebonden spiermassa-afname.
Zwangerschap
Bij lithiumgebruik tijdens de zwangerschap is er een geringe kans op een ernstige congenitale hartafwijking (ebsteinanomalie). Hoewel men de kans hierop aanvankelijk als veel hoger schatte dan in de algemene populatie (20× hoger: kans van 0,1-0,2%), is er discussie ontstaan of de kans op een ebsteinanomalie bij lithiumzwangerschappen inderdaad verhoogd is (Cohen e.a, 1994; McKnight e.a., 2012). Aan de zwangere wordt rond de 18e week een structurele echo naar vooral cardiale congenitale aandoeningen aangeboden.
Als lithium wordt doorgebruikt tijdens de zwangerschap, wordt geadviseerd om al tijdens de periode van het zwanger proberen te worden (en tijdens de zwangerschap) over te gaan op een lithiumpreparaat met een gereguleerde afgifte: Priadel of Camcolit in een doseringsschema van 3-4 giften per dag en met bij voorkeur een 12 uursbloedspiegel van 0,5-0,7 mmol/l. Aangenomen wordt dat vooral de pieken in spiegels teratogeen zouden zijn, maar dit is niet wetenschappelijk onderzocht.
Tijdens de zwangerschap dient de bloedspiegel vaker bepaald te worden. Geadviseerd wordt om tot week 32, 1× per 3 weken de lithiumspiegel te bepalen, daarna tot week 36: 1× per 2 weken en vanaf week 36: 1× per week. Tegen het einde van de zwangerschap keert de lithiumklaring weer terug naar het niveau van voor de zwangerschap; bij ongewijzigde dosis bestaat daardoor het risico op intoxicatie (er is minder lithiuminname nodig voor eenzelfde bloedspiegel).
Vanwege een verhoogd risico op schildklierpathologie wordt de schildklierfunctie (TSH, vrij T4 (FT4 )) bepaald in de 3e, 6e en 9e maand. Bij de start van de weeën wordt geadviseerd om lithium te staken. Bij een geplande inleiding wordt geadviseerd lithium bij voorkeur 24 tot 48 uur van tevoren te staken. Direct na de partus wordt lithium weer hervat in dezelfde (of zelfs iets hogere) dosering als voor de zwangerschap (en met het oorspronkelijke lithiumpreparaat), en daarna verder gedoseerd op geleide van de bloedspiegel.
Controleer de lithiumspiegels op dag 2, 5 en 12 (in verband met veranderingen in waterhuishouding na de bevalling), met op dag 12 tevens controle van de schildklierfunctie vanwege een verhoogd risico op postpartumthyroïditis. Geadviseerd wordt om in het navelstrengbloed de lithiumspiegel en TSH te bepalen en op indicatie vrij T4 (FT4 ) en TSH-receptorstimulerende antistoffen (thyroïdstimulerende immunoglobulinen: TSI).
Onderbouwing
- Gitlin M, Bauer M. Key questions on the long term renal effects of lithium: a review of pertinent data. Int J Bipolar Disord. 2023 Nov 16;11(1):35. doi: 10.1186/s40345-023-00316-5. PMID: 37971552; PMCID: PMC10654310.
- Schoretsanitis G, Filippis R, Brady B, Homan P, Suppes T, Kane JM. Prevalence of impaired kidney function in patients with long-term lithium treatment: a systemic review and meta-analysis. Bipolar Disord. 2021;24:264–74.
- Tabibzadeh N, Vidal-Petiot E, Cheddani L, Haymann JP, Lefevre G, Etain B, Bellivier F, Marlinge E, Delavest M, Vrtovsnik F, Flamant M. Chronic Lithium Therapy and Urine-Concentrating Ability in Individuals With Bipolar Disorder: Association Between Daily Dose and Resistance to Vasopressin and Polyuria. Kidney Int Rep. 2022 Apr 15;7(7):1557-1564. doi: 10.1016/j.ekir.2022.04.008. PMID: 35812274; PMCID: PMC9263256.
Beoordelingsdatum en geldigheid
Publicatiedatum : 24-03-2026
Beoordeeld op geldigheid : 24-03-2026
Uiterlijk in 2020 bepaalt het netwerk kwaliteitsontwikkeling ggz in samenspraak met de betrokken partijen of deze richtlijn nog actueel is. Zo nodig wordt een nieuwe werkgroep geïnstalleerd om de richtlijn te herzien. De geldigheid van de richtlijn komt eerder te vervallen wanneer nieuwe ontwikkelingen ertoe aanleiding geven om een vervroegd herzieningstraject te starten.
Algemene gegevens
Als onderdeel van de modulaire richtlijnherziening in 2025 is enkel het onderdeel ‘Nierfunctie’ herzien.
Deze richtlijn is ontwikkeld door de richtlijnwerkgroep Bipolaire stoornissen, op initiatief van de Nederlandse Vereniging voor Psychiatrie (NVvP). Het is een multidisciplinaire richtlijn die aanwijzingen geeft voor screening, diagnostiek en behandeling van bipolaire stoornissen. De ontwikkeling is gefinancierd vanuit het gealloceerde budget van de Nederlandse Vereniging voor Psychiatrie (NVvP) van de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). Methodologisch en organisatorisch is de richtlijnontwikkeling ondersteund door het Trimbos-instituut.
Verantwoording overige tekst
Deze richtlijn is ontwikkeld door de richtlijnwerkgroep Bipolaire stoornissen, op initiatief van de Nederlandse Vereniging voor Psychiatrie (NVvP) en de beroepsvereniging Verpleegkundigen en Verzorgenden Nederland (v&vn). Het is een multidisciplinaire richtlijn die aanwijzingen geeft voor screening, diagnostiek en behandeling van bipolaire stoornissen. De ontwikkeling is gefinancierd vanuit het gealloceerde budget van de Nederlandse Vereniging voor Psychiatrie (NVvP) van de Stichting Kwaliteitsgelden Medisch Specialisten (skms). Methodologisch en organisatorisch is de richtlijnontwikkeling ondersteund door het Trimbos-instituut. De ontwikkeling vond plaats in nauwe samenwerking met het Britse National Collaborative Centre for Mental Health (nccmh), het uitvoeringsorgaan van National Institute for Health and Clinical Excellence (nice) voor onderwerpen in de geestelijke gezondheidszorg (ggz) (vanaf hier gebruiken we ‘nice’ om nccmh aan te duiden). Nice ontwikkelde gelijktijdig de Britse richtlijn Bipolar disorder (nice, 2014). Zowel voor de afbakening van de richtlijn als voor de uitgangsvragen van de richtlijn heeft de Nederlandse richtlijnwerkgroep grotendeels de keuzen gevolgd die gemaakt zijn door nice. Dit was noodzakelijk om een nauwe samenwerking tussen beide partijen mogelijk te maken. In een toekomstige update van deze Nederlandse richtlijn kan worden besloten of de afbakening en uitgangsvragen aangepast dienen te worden voor de Nederlandse situatie.
Doel en doelgroep
Als onderdeel van de modulaire richtlijnherziening in 2025 is enkel het onderdeel ‘Nierfunctie’ herzien.
Doel
Deze richtlijn is ontwikkeld als hulpmiddel. De richtlijn geeft aanbevelingen en handelingsinstructies voor de screening, diagnostiek en behandeling van zowel kinderen als adolescenten, volwassenen en ouderen met een bipolaire stoornis. De aanbevelingen zijn bedoeld ter ondersteuning van de praktijkvoering van alle professionals die betrokken zijn bij de zorgverlening voor deze patiënten. De richtlijn geeft een overzicht van goed (‘optimaal’) handelen in lijn met de resultaten van wetenschappelijk onderzoek en overige overwegingen, als waarborg voor kwalitatief hoogwaardige zorg. De richtlijn kan tevens richting geven aan de onderzoeksagenda voor wetenschappelijk onderzoek naar bipolaire stoornissen.
De multidisciplinaire ontwikkelprocedure is bedoeld om de multidisciplinaire samenwerking in de dagelijkse praktijk te bevorderen. Daarnaast kan deze richtlijn vertaald worden naar monodisciplinaire richtlijnen van afzonderlijke beroepsgroepen. De richtlijn is dan te beschouwen als een moederrichtlijn voor de richtlijnen van die beroepsgroepen, waarin men aanknopingspunten kan vinden voor lokale zorgprogramma’s en protocollen. Het opstellen van lokale zorgprogramma’s en protocollen op basis van deze richtlijn wordt door de richtlijnwerkgroep aangemoedigd, aangezien de implementatie van de in deze richtlijn beschreven behandeling optimale zorg kan bevorderen.
Indien de aanbevelingen uit deze richtlijn in de concrete situatie niet aansluiten bij de wensen of behoeften van de patiënt met een bipolaire stoornis, kan beredeneerd worden afgeweken van de richtlijn, tenzij de wensen of behoeften van de patiënt naar de mening van de behandelaar hem of haar kunnen schaden, dan wel geen nut hebben. In alle gevallen komt een behandeling tot stand op basis van gezamenlijke besluitvorming door de optimaal geïnformeerde patiënt, naaste en behandelaar(s).
Afbakening
Deze richtlijn betreft de diagnostiek en behandeling van kinderen en adolescenten (12 tot 23 jaar), volwassenen en ouderen (60 jaar of ouder) bij wie er sprake is van (of er een vermoeden is van) een bipolaire stemmingsstoornis. In de richtlijn is gezocht naar oorspronkelijke onderzoeken zonder begindatum, en tot en met november 2024. In sommige gevallen zijn gepubliceerde aanvullende reviews van recenter datum geraadpleegd. Nog niet gepubliceerde onderzoeken zijn niet meegenomen.
Doelgroep
De ontwikkeling van de multidisciplinaire richtlijnen voor de ggz geschiedt primair vanuit een inhoudelijke invalshoek ten behoeve van de verbetering van de kwaliteit van de zorgverlening. De gebruikers van de richtlijn zijn doorgaans allen professioneel betrokken bij de zorg voor patiënten met een bipolaire stoornis of voor patiënten bij wie men die aandoening vermoedt.
In de werkgroep waren ook patiënten- en familieverenigingen vertegenwoordigd, waarmee het perspectief van de patiënten met een bipolaire stoornis en hun naasten in de richtlijn een plaats heeft gekregen. Daardoor kunnen ook niet-professionele zorgverleners en/of belangenverenigingen tot de gebruikers van de richtlijn kan behoren.
Verantwoording overige tekst
Doel
Deze richtlijn is ontwikkeld als hulpmiddel. De richtlijn geeft aanbevelingen en handelingsinstructies voor de screening, diagnostiek en behandeling van zowel kinderen als adolescenten, volwassenen en ouderen met een bipolaire stoornis. De aanbevelingen zijn bedoeld ter ondersteuning van de praktijkvoering van alle professionals die betrokken zijn bij de zorgverlening voor deze groepen patiënten. De richtlijn geeft een overzicht van goed (‘optimaal’) handelen volgens de resultaten van wetenschappelijk onderzoek en overige overwegingen, als waarborg voor kwalitatief hoogwaardige
zorg. De richtlijn kan tevens richting geven aan de onderzoeksagenda voor wetenschappelijk onderzoek naar bipolaire stoornissen.
Het doel is een leidraad bieden voor screening, diagnostiek en behandeling van een bipolaire stoornis. De multidisciplinaire ontwikkelprocedure was bedoeld om de multidisciplinaire samenwerking in de dagelijkse praktijk te bevorderen. Daarnaast kan deze richtlijn vertaald worden naar monodisciplinaire richtlijnen van afzonderlijke beroepsgroepen. De richtlijn is dan te beschouwen als een moederrichtlijn voor de richtlijnen van die beroepsgroepen, waarin men aanknopingspunten kan vinden voor lokale zorgprogramma’s en protocollen. Het opstellen van lokale zorgprogramma’s en protocollen op basis van deze richtlijn moedigt de richtlijnwerkgroep aan, omdat dat bevorderlijk is voor de implementatie van de in deze richtlijn beschreven optimale zorg.
Indien de aanbevelingen uit deze richtlijn in de concrete situatie niet aansluiten bij de wensen of behoeften van de patiënt met een bipolaire stoornis, moet het in principe mogelijk zijn beredeneerd af te wijken van de richtlijn, tenzij de wensen of behoeften van de patiënt naar de mening van de behandelaar hem of haar kunnen schaden, dan wel geen nut hebben.
Afbakening
Deze richtlijn betreft de diagnostiek en behandeling van jeugdigen (12 tot 23 jaar), volwassenen en ouderen (60 jaar of ouder) bij wie er sprake is van (of er een vermoeden is van) een bipolaire stoornis. In de richtlijn is gezocht naar oorspronkelijke onderzoeken zonder begindatum, en tot en met maart 2014. In sommige gevallen zijn gepubliceerde aanvullende reviews van recenter datum geraadpleegd. Nog niet gepubliceerde onderzoeken zijn niet meegenomen (wel onderzoeken ‘in press’). Zie voor meer informatie over de afbakening van de richtlijn de aanverwanten
Doelgroep
De ontwikkeling van de multidisciplinaire richtlijnen voor de ggz geschiedt primair vanuit een inhoudelijke invalshoek ten behoeve van de verbetering van de kwaliteit van de zorgverlening. De gebruikers van de richtlijn zijn doorgaans allen professioneel betrokken bij de zorg voor patiënten met een bipolaire stoornis of voor patiënten bij wie men die aandoening vermoedt.
In de werkgroep waren ook patiënten- en familieverenigingen vertegenwoordigd, waarmee het perspectief van de patiënten met een bipolaire stoornis en diens betrokkenen in de richtlijn een plaats gekregen heeft. Daardoor kunnen ook niet-professionele zorgverleners en/of belangenverenigingen tot de gebruikers van de richtlijn kan behoren.
Samenstelling werkgroep
Als onderdeel van de modulaire richtlijnherziening in 2025 is enkel het onderdeel ‘Nierfunctie’ herzien.
Samenstelling werkgroep
De Multidisciplinaire richtlijn bipolaire stoornissen is ontwikkeld door de richtlijnwerkgroep Bipolaire stoornissen bij volwassenen, in opdracht van de Nederlandse Vereniging voor Psychiatrie (NVvP). De richtlijnwerkgroep, onder voorzitterschap van prof. dr. Ralph Kupka, emeritus hoogleraar bipolaire stoornissen, bestond uit psychiaters, psychologen, verpleegkundig specialisten, belangenbehartigers en ervaringsdeskundigen, allen door de (beroeps)verenigingen uitgenodigd en op persoonlijke titel aan het project verbonden.
Voorafgaande aan het ontwikkeltraject zijn kennismakingsgesprekken gevoerd met kandidaat-leden voor de werkgroep. Uit deze groep belangstellenden zijn de huidige werkgroepleden geselecteerd. Naast de richtlijnwerkgroep is een aantal experts benaderd om adviseur te worden. Deze adviseurs konden op individuele basis worden gevraagd om op verzoek van een werkgroeplid mee te denken over een specifieke uitgangsvraag. De richtlijnwerkgroep is methodologisch en organisatorisch ondersteund door het technische team van het Trimbos-instituut. Dit technische team bestond uit een projectleider, twee literatuur reviewers, een informatiespecialist, en een project assistent. De tabellen Leden werkgroep, Leden adviesgroep en Methodologische ondersteuning geven een overzicht van de samenstelling van de richtlijnwerkgroep, de klankbordgroep en het ondersteunende technische team.
Leden Werkgroep
|
|
Naam |
Organisatie |
Beroepsvereniging |
|
1. |
Prof. dr. Ralph Kupka (voorzitter) |
Amsterdam UMC; Altrecht; GGZ inGeest; Dimence |
Psychiater, NVvP |
|
2. |
dr. Manja Koenders (vicevoorzitter) |
Leiden University Faculty of Social Sciences |
Psycholoog, NIP |
|
3. |
Prof. dr. Manon Hillegers |
afd. K&J Psychiatrie Erasmus MC |
Psychiater, NVvP |
|
3. |
dr. Annemieke Dols |
UMC Utrecht |
Psychiater, NVvP |
|
4. |
dr. Imke Hanssen |
Radboud Universiteit Nijmegen |
Psycholoog, NIP |
|
5. |
dr. Bart Geerling |
Dimence |
verpleegkundig specialist, V&VN |
|
6. |
drs. Henk Mathijssen |
Plusminus |
Plusminus |
|
7. |
Elisabeth Bakker-Timmerman |
Plusminus, KenBiS |
Plusminus |
Leden adviesgroep
|
|
Naam |
Organisatie |
Beroep |
|
1. |
prof. dr. Marc Vervloet* |
Radboud UMC |
Hoogleraar nefrologie |
|
2. |
Dr. Miranda Kurver |
NHG |
Huisarts en senior wetenschappelijk medewerker richtlijnontwikkeling |
|
3. |
dr. Ingeborg Wilting |
UMC Utrecht |
klinisch farmacoloog |
|
4. |
dr. Benno Haarman |
UMC Groningen |
Psychiater |
|
5. |
dr. Rob Havermans |
Mondriaan, PsyQ |
Psychiater |
|
6. |
dr. Debbie Zittema |
GGZ Ingeest |
Psychiater en klinisch farmacoloog |
|
7. |
Bianca van Nieuwendijk |
GGZ Ingeest |
Verpleegkundig specialist |
|
8. |
Mischa van Bendegem |
Mediant |
Verpleegkundig specialist |
|
9. |
Dr. Bram Dierckx |
Erasmus MC |
Psychiater |
|
10. |
Dr. Esther Mesman |
Erasmus MC |
GZ-psycholoog |
|
11. |
Dr. Max de Leeuw |
LUMC |
Psychiater |
|
12. |
Dolf Snel |
|
Naastenperspectief |
|
13. |
Suzanne Demacker |
Altrecht |
GZ-psycholoog |
|
14. |
Dr. Melis Orhan |
Universiteit Leiden |
GZ-psycholoog |
|
15. |
Theo Hoedemaker |
Plusminus |
Naastenperspectief |
|
16. |
JRP van der Veen |
Plusminus |
ervaringsdeskundige |
|
17. |
Bernadette Wigchert |
Plusminus |
ervaringsdeskundige |
|
18. |
Mirthe Knot-Ploeg |
Plusminus |
ervaringsdeskundige |
*Marc Vervloet is namens de NIV gemandateerd om advies te verlenen op module 9 Somatische Aspecten.
Methodologische ondersteuning
|
Naam |
Ondersteuning |
|
Eva Becking |
Projectleider, Trimbos-instituut |
|
Anne van Jaarsveld |
Reviewer, Trimbos-instituut |
|
Matthijs Oud |
Reviewer, Trimbos-instituut |
|
Rikie Deurenberg |
Informatiespecialist, namens Trimbos-instituut |
|
Joyce Huls |
Projectassistent, Trimbos-instituut |
In totaal kwam de Werkgroep Bipolaire Stoornissen voorafgaand aan de commentaarfase acht keer bijeen in de periode van januari 2024 tot maart 2025. In deze periode werden de stappen van de methodiek voor evidence-based richtlijnontwikkeling (EBRO) doorlopen. De informatiespecialist verrichtte in overleg met de werkgroepleden op systematische wijze literatuuronderzoek en de reviewers maakten per uitgangsvraag een selectie in de gevonden onderzoeken (zie voor informatie over de zoekstrategie en de selectiecriteria: het reviewprotocol). De reviewers beoordeelden de kwaliteit en inhoud van de aldus verkregen literatuur en verwerkten deze per uitgangsvraag in evidentie-tabellen, GRADE-profielen, beschrijvingen van de wetenschappelijke onderbouwing en wetenschappelijke (gewogen) conclusies (per module beschreven onder “Onderbouwing”). Leden van de Werkgroep gingen op basis van de gevonden literatuur met elkaar in discussie over praktijkoverwegingen (per module beschreven onder “Overwegingen”) en aanbevelingen (per module beschreven onder “Aanbevelingen”). De werkgroepleden schreven samen met het technisch team van het Trimbos-instituut de concepttekst, welke ter becommentariëring openbaar is gemaakt. De ontvangen commentaren worden verwerkt in een commentaartabel, die tijdens een werkgroep bijeenkomst wordt besproken. Na het doorvoeren van op deze bijeenkomst voorgestelde wijzigingen wordt de definitieve richtlijn aan de opdrachtgever aangeboden.
Verantwoording overige tekst
De Multidisciplinaire richtlijn bipolaire stoornissen is ontwikkeld door de richtlijnwerkgroep Bipolaire stoornissen bij volwassenen, in opdracht van de Nederlandse Vereniging voor Psychiatrie (NVvP) en de beroepsvereniging Verpleegkundigen en Verzorgenden Nederland (v&vn). De richtlijnwerkgroep, onder voorzitterschap van prof.dr. Ralph Kupka, hoogleraar bipolaire stoornissen, bestond uit psychiaters, psychologen, verpleegkundigen, belangenbehartigers en ervaringsdeskundigen, allen door de beroepsverenigingen uitgenodigd en op persoonlijke titel aan het project verbonden.
Voorafgaande aan het ontwikkeltraject zijn kennismakingsgesprekken gevoerd met verscheidene kandidaat-leden voor de werkgroep. Uit deze groep belangstellenden zijn de huidige werkgroepleden geselecteerd. Naast de richtlijnwerkgroep is een adviesgroep samengesteld, die is gevraagd voorafgaand aan de commentaarfase schriftelijk te reageren op de conceptteksten. Leden van de adviesgroep kon tevens worden gevraagd om tijdens een werkgroepbijeenkomst mee te denken over een specifieke uitgangsvraag. De richtlijnwerkgroep is methodologisch en organisatorisch ondersteund door het technische team van het Trimbos-instituut. Dit technische team bestond uit een projectleider, een informatiespecialist, twee literatuurreviewers, een gezondheidseconoom, een notulist en een projectassistent.
In totaal kwam de richtlijnwerkgroep voorafgaand aan de commentaarfase 9 keer bijeen in een periode van 17 maanden (november 2012 - maart 2014). In deze periode werden, in samenwerking met nice, de stappen van de methodiek voor evidence-based richtlijnontwikkeling (ebro) doorlopen.
De informatiespecialisten van nice en van het Trimbos-instituut verrichtten in overleg met de werkgroepleden op systematische wijze literatuuronderzoek en maakten een selectie in de gevonden onderzoeken. De reviewers van nice en van het Trimbos-instituut beoordeelden de kwaliteit en inhoud van de aldus verkregen literatuur en verwerkten deze in evidencetabellen, beschrijvingen van de wetenschappelijke onderbouwing en wetenschappelijke (gewogen) conclusies.
Tabel 1. Leden werkgroep

Leden van de richtlijnwerkgroep gingen op basis van de gevonden literatuur met elkaar in discussie over praktijkoverwegingen en aanbevelingen. De werkgroepleden schreven samen met het technische team van het Trimbosinstituut de conceptrichtlijntekst, die ter becommentariëring openbaar is gemaakt. De ontvangen commentaren zijn verwerkt in een commentaartabel, die tijdens een werkgroepbijeenkomst is besproken. Na het doorvoeren van op deze bijeenkomst voorgestelde wijzigingen is de definitieve richtlijn aangeboden aan de opdrachtgever (Nederlandse Vereniging voor Psychiatrie (NVvP) en Verpleegkundigen & Verzorgenden Nederland (V&VN)). Hierop volgden autorisatie door de beroepsverenigingen, druk en verspreiding.
Tabel 2. Leden adviesgroep
Belangenverklaringen
Als onderdeel van de modulaire richtlijnherziening in 2025 is enkel het onderdeel ‘Nierfunctie’ herzien.
|
Naam werkgroeplid |
Functie |
Nevenwerkzaamheden |
Belangen |
|
Ralph Kupka |
Hoogleraar Bipolaire stoornissen Psychiater |
Bestuurslid Akwa-GGZ Voorzitter bestuur KenBis Bestuurslid ISBD |
nvt |
|
Manja Koenders |
GZ-psycholoog i.o. specialist Universitair docent |
Docent Rino-groep Zzp supervisor |
nvt |
|
Manon Hillegers |
Hoogleraar en afdelingshoofd kinder/jeugd psychiatrie |
Bestuurslid BOPP-west ESCAP bestuurslid ISBD taskforce member |
nvt |
|
Annemieke Dols |
Psychiater |
Onderwijs en nascholing faciliteren |
nvt |
|
Bart Geerling |
Verpleegkundig specialist/hoofd Onderzoeker |
Voorzitter herziening zorgstandaard |
nvt |
|
Imke Hanssen |
Psycholoog i.o. tot GZ-psycholoog Post-doc onderzoeker |
Lid wetenschapscommissie Vereniging voor Mindfulness-Based Trainers Nederland Bestuurslid van de sectie Mindfulness-Based Cognitieve GedragsTherapie (MB-CGT) van de Vereniging voor Cognitieve Gedragstherapieën (VGCt) |
nvt |
|
Henk Matthijsen |
Voorzitter Plusminus |
Lid RvT GGZ Transparant |
nvt |
|
Elisabeth Bakker Timmerman |
Lid Plusminus Gepensioneerd ergotherapeut |
Bestuurslid KenBis Lid familieraad Parnassia
|
nvt |
Methode ontwikkeling
Evidence based
Implementatie
Recent onderzoek laat zien dat er bij richtlijntrajecten voornamelijk aandacht is voor de ontwikkeling van de richtlijn. Planmatige opgezette en onderbouwde invoering komt maar heel beperkt van de grond. Hierop dient gericht te worden aangestuurd door financiers, zodat hier al bij de start geld voor beschikbaar is. De Regieraad voor richtlijntrajecten (de Regieraad Kwaliteit van Zorg te Den Haag) onderschrijft dan ook een programmatische aanpak van de ontwikkeling, invoering én evaluatie van richtlijnen inclusief (financiële en organisatorische) middelen, om het gebruik van de richtlijnen te stimuleren, te monitoren en te evalueren (Fleuren e.a., 2010). Tno, het cbo en het Trimbos-instituut besloten deze opdracht samen uit te voeren, met als doel de complementaire inzichten en expertise te vertalen in een gemeenschappelijke visie op richtlijnen. Dit heeft geresulteerd in een praktisch instrument voor een analyse van richtlijntrajecten: Kwaliteit Richtlijnontwikkeling, Invoering en Evaluatie (krie).
Werkwijze
Als onderdeel van de modulaire richtlijnherziening in 2025 is enkel het onderdeel ‘Nierfunctie’ herzien.
Werkwijze
EBRO-methode voor wetenschappelijke onderbouwing
Deze multidisciplinaire richtlijn is herzien volgens de methodiek van evidence-based richtlijnontwikkeling (EBRO). Hierbij werd de GRADE-methodiek toegepast. Er zijn ook hoofdstukken overgenomen vanuit de vorige versie van de MDR Bipolaire stoornis (2015). Hierin zijn conclusies gebaseerd op de ‘levels of evidence’ (voor informatie over deze werkwijze, raadpleeg de verantwoording van de betreffende hoofdstukken).
GRADE-methodiek
Sinds de introductie van de GRADE-methodiek in 2004 werd dit wereldwijd al snel de methode van voorkeur om wetenschappelijk bewijs te graderen ten behoeve van richtlijnontwikkeling (Guyatt et al., 2008), inclusief deze richtlijn. De GRADE-methodiek gaat er van uit dat de zekerheid van het wetenschappelijk bewijs uit randomized controlled trials (RCT’s) in beginsel hoog is vanwege de, mits goed uitgevoerd, kleine kans op vertekening (bias). In geval van observationele (niet gerandomiseerde) studies is de uitgangspositie van de zekerheid van bewijs laag. De zekerheid van het bewijs per uitkomstmaat wordt, behalve door de methodologische kwaliteit van de individuele onderzoeken, ook bepaald door andere factoren, zoals de mate van consistentie van de gevonden resultaten uit de verschillende onderzoeken en de precisie van de gevonden uitkomst (zie tabel 1.1). Bij observationeel onderzoek kan het bewijs in bepaalde gevallen omhoog worden gegradeerd.
Tabel 1.1 GRADE: Factoren voor downgraden en upgraden 1
⇓ |
We downgraden de zekerheid van bewijs van studies met een hoge uitgangspositie (RCT’s), bij: |
⇑ |
We upgraden de zekerheid van bewijs van observationele studies bij: |
|
|
||
|
|
||
|
|
||
|
|
||
|
|
||
1 De zekerheid van het bewijs (zeer laag, laag, matig en hoog) verwijst naar de mate van vertrouwen dat men heeft in de schatting van het effect van een behandelinBij de beoordeling van het wetenschappelijke bewijs ten aanzien van bovenstaande factoren werd uitgegaan van ‘Grade guidelines’, zoals ook te raadplegen in het ‘Grade handbook’ (Guyatt et al., 2013; Handbook for grading the quality of evidence and the strength of recommendations using the GRADE approach).
Legenda GRADE
Na vaststelling van het niveau van bewijs wordt dit in de bijbehorende conclusies als volgt verwoord:
|
Zekerheid |
Symbolen |
|
Signaalwoorden |
|
Hoog |
⊕⊕⊕⊕ |
“Het is aangetoond dat…” |
geeft, heeft (een effect), resulteert in |
|
Redelijk |
⊕⊕⊕◯ |
“Het is aannemelijk...” |
waarschijnlijk |
|
Laag |
⊕⊕◯◯ |
“Er zijn aanwijzingen…” |
zou kunnen, lijkt, suggereert |
|
Zeer laag |
⊕◯◯◯ |
“Het is onzeker, maar er zijn aanwijzingen dat…” |
onzeker |
Van bewijs naar aanbevelingen: Overwegingen
Naast het wetenschappelijk bewijs bepalen enkele andere factoren mede of een instrument of behandeling wordt aanbevolen. In de teksten van de vorige richtlijn-versies werd dit onder “Overige Overwegingen” beschreven.
Mee te wegen factoren om te bepalen of een instrument of behandeling wordt aanbevolen:
|
1. Kwaliteit van bewijs Hoe hoger de algehele kwaliteit van het bewijs, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. |
|
2. Balans tussen gewenste en ongewenste effecten Hoe groter het verschil is tussen de gewenste en ongewenste effecten, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. Hoe kleiner dit verschil of hoe meer onzekerheid over de grootte van het verschil, des te waarschijnlijker wordt het formuleren van een conditionele aanbeveling. Toelichting:
|
|
3. Patiëntenperspectief Hoe groter de uniformiteit in waarden en voorkeuren van patiënten bij het afwegen van de voor- en nadelen van een interventie, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. |
|
4. Professioneel perspectief Hoe groter de uniformiteit in waarden en voorkeuren van professionals ten aanzien van de toepasbaarheid van een interventie, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. Toelichting:
|
|
5. Middelenbeslag Hoe minder middelen er worden gebruikt (m.a.w. hoe lager de kosten van een interventie zijn vergeleken met de beschouwde alternatieven en andere kosten gerelateerd aan de interventie), des te waarschijnlijker wordt het formuleren van een sterke aanbeveling. Hoe meer onzekerheid over het middelenbeslag, des te waarschijnlijker wordt een conditionele aanbeveling. |
|
6. Organisatie van zorg Hoe meer onzekerheid of de geëvalueerde interventie daadwerkelijk op landelijke schaal toepasbaar is, des te waarschijnlijker wordt het formuleren van een conditionele aanbeveling. Toelichting:
|
Formulering van aanbevelingen
Afhankelijk van deze factoren kun je een instrument of behandeling wel of niet aanbevelen. We maken daarbij onderscheid tussen zwakke en sterke aanbevelingen. In het geval van een sterke aanbeveling zou je behandeling X voor alle patiënten met Y willen aanbevelen. Bij een zwakke aanbeveling is dit bijvoorbeeld afhankelijk van de voorkeuren van de patiënt in kwestie. Het is belangrijk in deze sectie expliciet te vermelden op grond waarvan een behandeling wel of niet wordt aanbevolen en ook waarom die aanbeveling zwak of sterk zou moeten zijn.
Voor de formulering van ‘sterke’ (onvoorwaardelijke) en ‘zwakke’ (voorwaardelijke) aanbevelingen is de volgende indeling aangehouden (zie tabel 1.2):
Tabel 1.2 GRADE Voorkeursformulering sterke / zwakke aanbevelingen
|
Gradering aanbeveling |
Betekenis |
Voorkeursformulering* |
|
STERK VOOR |
De voordelen zijn groter dan de nadelen voor bijna alle patiënten. Alle of nagenoeg alle geïnformeerde patiënten zullen waarschijnlijk deze optie kiezen. |
We bevelen [interventie] aan. |
|
ZWAK VOOR |
De voordelen zijn groter dan de nadelen voor een meerderheid van de patiënten, maar niet voor iedereen. De meerderheid van geïnformeerde patiënten zal waarschijnlijk deze optie kiezen. |
Overweeg [interventie], bespreek de voor- en nadelen). |
|
ZWAK TEGEN |
De nadelen zijn groter dan de voordelen voor een meerderheid van de patiënten, maar niet voor iedereen. De meerderheid van geïnformeerde patiënten zal waarschijnlijk deze optie kiezen. |
Wees terughoudend met [interventie], bespreek de voor- en nadelen). |
|
STERK TEGEN |
De nadelen zijn groter dan de voordelen voor bijna alle patiënten. Alle of nagenoeg alle geïnformeerde patiënten zullen waarschijnlijk deze optie kiezen. |
We bevelen [interventie] niet aan. |
* Het gaat hier om voorkeursaanbevelingen, deze kunnen in een enkel geval afwijken. Voor bepaalde hoofdstukken is GRADE niet toegepast (bijv. Organisatie van zorg) daar zijn uit praktisch oogpunt ook de aanbevelingen niet volgens GRADE.
Zoekstrategie
Om de uitgangsvragen te kunnen beantwoorden, is door de informatiespecialist en reviewers van het Trimbos-instituut, in overleg met de werkgroepleden, op systematische wijze literatuuronderzoek verricht en is een selectie gemaakt binnen de gevonden onderzoeken volgens vooraf vastgestelde selectiecriteria. Er is gezocht naar meta-analyses, systematische reviews en oorspronkelijke onderzoeken. In de literatuursearches is gezocht naar literatuur in de Engelse en Nederlandse taal. Voor het zoeken naar publicaties is gebruikgemaakt van Medline en Psychological Information Database (Psycinfo).
Selectiestrategie
Bij de selectie van artikelen zijn de volgende criteria gehanteerd:
- Geeft het onderwerp van het gevonden onderzoek voldoende antwoord op de uitgangsvraag: worden de binnen GRADE vastgestelde kritische en belangrijke uitkomstmaten in het onderzoek geëvalueerd? (zie voor meer informatie over GRADE verderop in deze paragraaf);
- Sluit de doelgroep van het gevonden onderzoek voldoende aan bij de doelgroep van de richtlijn;
- Is er sprake van een meta-analyse, systematic-review, randomised controlled trial (RCT), cohort onderzoek, cross-sectioneel onderzoek, patiëntcontrole onderzoek of wetenschappelijke verantwoord kwalitatief onderzoek? Bij een longitudinaal onderzoek: Is er sprake van een voldoende lange follow-up periode?;
- Zie voor meer informatie over de zoekstrategie de bijlagen per hoofdstuk en voor meer informatie over de selectiecriteria per uitgangsvraag de reviewprotocollen in de bijlagen per hoofdstuk.
Leeswijzer
Met kinderen en adolescenten bedoelen we kinderen van 8 tot 12 jaar en adolescenten van 12 tot 18 jaar. Met jongvolwassenen bedoelen we volwassenen van 18 tot 25 jaar. Met volwassenen bedoelen we mensen van 25 tot 60 jaar. Met ouderen bedoelen we oudere volwassenen van 60 jaar en ouder.
Verantwoording overige tekst
De richtlijn is ontwikkeld volgens de methodiek van de evidence-based richtlijnontwikkeling (ebro).
Samenvatting literatuur per module
Deze multidisciplinaire richtlijn is een herziening van de Richtlijn bipolaire stoornissen (Nolen e.a., 2008). Bepaalde modules in deze nieuwe richtlijn zijn overgenomen uit de richtlijn uit 2008 en de inhoud is geactualiseerd. Dit geldt voor de modules: Organisatie van zorg, Zelfmanagement bevorderen, Somatische aspecten en Kinderwens, zwangerschap, bevalling en kraambedperiode. In deze modules is voor de wetenschappelijke onderbouwing de methode gebruikt uit de richtlijn van 2008, die afwijkt van de methode in de rest van de nieuwe richtlijn uit 2015. In deze modules is relevante literatuur beschrijvend samengevat (er is geen meta-analyse gemaakt) en zijn de zoekstrategie, de selectiecriteria en de beoordelingscriteria naar aanleiding waarvan onderzoeken zijn geïncludeerd en meegewogen in de conclusies en aanbevelingen, niet expliciet beschreven. Wel is zo veel mogelijk aangegeven op welk onderzoek of welke onderzoeken de conclusies en aanbevelingen gebaseerd zijn.
Tabel 3 Methodologische ondersteuning
De werkgroep heeft tijdens het ontwikkelingsproces besloten een specifieke module over ouderen toe te voegen. Deze module bevat een overzicht van eventuele benodigde aanpassingen in de diagnostiek en behandeling van ouderen. Voor dit onderwerp is geen systematische literatuurreview (inclusief systematische search, selectie en beoordeling van onderzoeken) uitgevoerd. De opbouw van deze module verschilt derhalve van de modules waarvoor een specifieke literatuurreview is gemaakt. Per submodule wordt inleidende informatie gegeven, waarin waar mogelijk een (niet-systematische) wetenschappelijke onderbouwing en praktijkoverwegingen zijn opgenomen. Deze inleidende informatie wordt, indien van toepassing, gevolgd door aanbevelingen voor de klinische praktijk. Tabel 4 vat samen welke methoden per module zijn toegepast voor het vaststellen van de wetenschappelijke evidence.
Tabel 4. Methoden voor vaststellen evidence per module
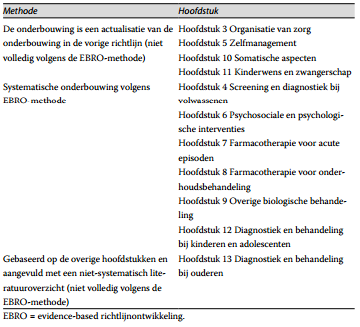
Onderschrift: hoofdstuk kan vertaald worden naar module.
Zoekstrategie
Om de klinische uitgangsvragen te kunnen beantwoorden, is door de informatiespecialisten van nice, in overleg met de werkgroepleden op systematische wijze literatuuronderzoek verricht en is een selectie gemaakt binnen de gevonden onderzoeken volgens vooraf vastgestelde selectiecriteria. Er is gezocht naar bestaande (buitenlandse) evidence-based richtlijnen voor de zorg voor volwassenen met een bipolaire stoornis, systematische reviews en oorspronkelijke onderzoeken. In de literatuursearches is gezocht naar literatuur in de Engelse, Nederlandse, Franse en Duitse taalgebieden. Voor het zoeken naar publicaties is gebruikgemaakt van de volgende informatiebronnen.
- Allied and Complementary Medicine (amed).
- Applied Social Services Index and Abstracts (assia).
- Australian Education Index (aei).
- British Education Index (bei).
- Cochrane Central Register of Controlled Trials (central).
- Cochrane Database of Absracts of Reviews of Effects (dare).
- Cochrane Database of Systematic Reviews (cdsr).
- Cumulative Index to Nursing and Allied Health Literature (cinahl).
- Education Resources in Curriculum (eric).
- Excerpta Medica database (Embase).
- Health Management Information Consortium (hmic).
- Health Technology Assessment (hta) database.
- International Bibliography of Social Science (ibss).
- medline; medline In-Process.
- Psycbooks.
- Psycextra.
- Psychological Information Database (Psycinfo).
- Social Services Abstracts.
- Sociological Abstracts.
Selectiestrategie
Bij de selectie van artikelen zijn de volgende criteria gehanteerd.
- Geeft het gevonden onderzoek voldoende antwoord op de uitgangsvraag (evalueert het onderzoek de essentiële en belangrijke uitkomstmaten volgens grade (Grading of Recommendations Assessment, Development and Evaluation)? Zie voor meer informatie over grade verderop in deze module, onder Beoordeling van de kwaliteit van het bewijs (met tabel 5).
- Sluit de doelgroep van het gevonden onderzoek voldoende aan bij de doelgroep van de richtlijn (kinderen, adolescenten, volwassenen, en volwassenen ouder dan 60 jaar met een van de bipolaire-stemmingsstoornissen, of bij wie men een van die stoornissen vermoedt)? (Literatuur gezocht over kinderen vanaf 12 jaar.)
- Is de bestudeerde groep voldoende groot? (Aantal wisselt per uitgangsvraag.)
- Is er sprake van een randomised controlled trial (rct), een cohortonderzoek, een crosssectioneel onderzoek, een patiënt-controleonderzoek of een wetenschappelijk verantwoord kwalitatief onderzoek (waaronder gedegen observationeel onderzoek en caseseries)?
- Bij een longitudinaal onderzoek: is er sprake van een voldoende lange follow-upperiode?
- Zie voor meer informatie over de zoekstrategie het bijbehorende aanverwant en voor meer informatie over de selectiecriteria per uitgangsvraag de reviewprotocollen in de aanverwanten.
Tabel 5. GRADE-factoren voor downgraden en upgraden. Het niveau van de kwaliteit van het bewijs (zeer laag, laag, matig en hoog) geeft weer welke mate van vertrouwen men heeft in de schatting van het effect van een behandeling
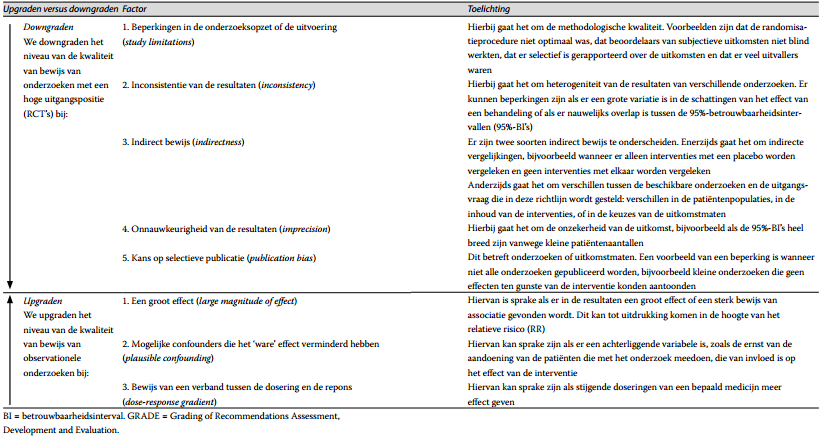
Extrapolatie
In deze richtlijn is extrapolatie toegepast wanneer de richtlijnwerkgroep de klinische uitgangsvraag belangrijk achtte, maar er geen primaire data over adolescenten of volwassenen met een bipolaire stoornis beschikbaar waren of deze onvoldoende werden geacht. Per klinische uitgangsvraag heeft de richtlijnwerkgroep besloten of geëxtrapoleerd kon worden vanuit literatuur over volwassenen met een bipolaire stoornis en vanuit literatuur over een populatie met schizofrenie. Wanneer werd besloten om te extrapoleren, hield de werkgroep in de gaten of de extrapolatiepopulatie op bepaalde algemene kenmerken overeenkwam met de populatie in de richtlijn (zoals op leeftijd, sekse, ernst van de stoornis) en dat andere aspecten van het probleem (zoals bijwerkingen) en uitkomsten (zoals verbeterde toegang tot diensten) gelijk waren. Extrapolatie werd alleen toegepast wanneer de kwaliteit van de data gelijkwaardig was. Modules waarin extrapolatie is toegepast zijn: Organisatie van zorg, Diagnostiek en behandeling van kinderen en adolescenten en Diagnostiek en behandeling van ouderen.
Beoordeling van de kwaliteit van het bewijs
Onderzoeken werden door twee personen beoordeeld op het risico op bias met behulp van de Cochrane Collaboration Risico van Bias Assessment Tool (Higgins e.a., 2008). Verschil in beoordeling werd met een derde persoon besproken en opgelost door middel van consensus. Elk onderzoek werd beoordeeld op:
- randomisatie en toewijzing;
- blindering van de deelnemers, beoordelaars, en therapeuten;
- gehanteerde methode om met uitval van deelnemers om te gaan;
- of alle uitkomsten zijn gerapporteerd.
Risico op bias kon worden beoordeeld als hoog (serieuze kans op beïnvloeding van het resultaat), laag (waarschijnlijk geen invloed op het resultaat), of onduidelijk.
Voor het bewijs over interventies is daarna het bewijs van de onderzoeken per uitkomstmaat gegradeerd met behulp van Grading of Recommendations Assessment, Development and Evaluation (grade). De kwaliteit van het bewijs kent daarbij vier niveaus: zeer laag, laag, matig en hoog. Het onderzoeksdesign bepaalt de uitgangspositie van de kwaliteit van bewijs. Gerandomiseerde gecontroleerde onderzoeken (rct’s) hebben over het algemeen meer bewijskracht dan observationele onderzoeken. Daarom is hun uitgangspositie hoog, terwijl de uitgangspositie van observationele onderzoeken laag is. De kwaliteit van het bewijs per uitkomstmaat wordt, behalve door de methodologische kwaliteit van de individuele onderzoeken, ook bepaald door andere factoren, zoals de mate van consistentie van de gevonden resultaten uit de verschillende onderzoeken, en de precisie van de gevonden uitkomst (zie tabel 5). Grade is niet toegepast bij vragen over screening en diagnostiek. De belangrijkste reden hiervoor is dat grade momenteel nog vooral geschikt is voor interventieonderzoeken.
Samenvatten van de resultaten
Van elk onderzoeksartikel is een samenvatting gemaakt in een zogeheten evidencetabel, waarin de belangrijkste kenmerken van individuele onderzoeken zijn opgenomen (bij een rct zijn dat bijvoorbeeld het doel van het onderzoek, het onderzoeksdesign, de patiëntkenmerken, de interventies, de uitkomstmaten en de resultaten). De resultaten van onderzoeken naar organisatie van zorg, screening en diagnostiek, somatische aspecten, diagnostiek en behandeling ouderen, en kinderwens en zwangerschap zijn op beschrijvende wijze samengevat (een narratieve review). Bij de uitgangsvragen over interventies was het oorspronkelijke doel om voor elke uitkomstmaat een meta-analyse uit te voeren, om de omvang van het klinisch effect van de interventie samen te vatten. De data uit oorspronkelijke onderzoeken worden hiervoor verwerkt in een forest plot, die een grafische weergave van de meta-analyse geeft (zie figuur 1 voor een voorbeeld van een forest plot).
Figuur 1. Voorbeeld van een forest plot met toelichting
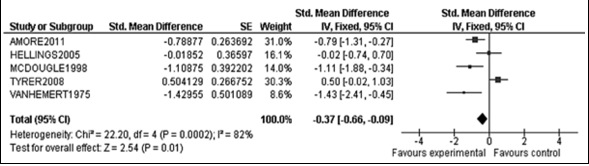
Wanneer er onvoldoende data beschikbaar waren om een meta-analyse uit te voeren, stelden de reviewers een narratieve (beschrijvende) review van het beschikbare bewijs op. Bij de interventieonderzoeken is de waardering van de kwaliteit van het bewijs met behulp van de grade-methodiek in deze narratieve reviews opgenomen. De kwaliteitsbeoordeling en een samenvattende beschrijving van de verschillende onderzoeken worden voor elke uitgangsvraag beschreven onder het kopje ‘Literatuuronderzoek’.
Uitgangsvragen
Deze richtlijn is ontwikkeld op geleide van uitgangsvragen die gebaseerd zijn op knelpunten die de disciplines ervaren bij screening, diagnostiek en behandeling van volwassenen met een bipolaire stoornis. Deze uitgangsvragen zijn vastgesteld door nice, op basis van een knelpuntenanalyse uitgevoerd in Groot-Brittannië. Om nauwe samenwerking met nice mogelijk te maken, heeft de Nederlandse richtlijnwerkgroep deze Britse uitgangsvragen grotendeels overgenomen voor de huidige richtlijn. Om aan te sluiten bij de bestaande monodiscipliniare Richtlijn bipolaire stoornissen (Nolen e.a., 2008), heeft de Nederlandse werkgroep daarnaast drie eigen uitgangsvragen geformuleerd: over zwangerschap bij bipolaire stoornissen, zelfmanagement, en organisatie van zorg. De werkgroep heeft tijdens het ontwikkelingsproces besloten om ook een overzicht te geven van eventuele benodigde aanpassingen in de diagnostiek en behandeling van kinderen en adolescenten, en van ouderen. Dit is respectievelijk opgenomen in hoofdstuk 12, Diagnostiek en behandeling bij kinderen en adolescenten, en hoofdstuk 13, Diagnostiek en behandeling bij ouderen. Dit is een aanvulling op de uitgangsvragen van nice. De richtlijn is geen leerboek waarin zo veel mogelijk beschikbare kennis over een onderwerp wordt opgenomen, maar een document met praktische aanbevelingen over knelpunten uit de praktijk. Dat betekent dat praktijkproblemen zo veel mogelijk uitgangspunt zijn van de teksten in de richtlijn. Dat betekent ook dat de wijze waarop die praktijkproblemen worden opgelost, meer aandacht krijgt dan de vraag welke discipline de problemen dient aan te pakken of op te lossen. De richtlijn is een document waarin staat hoe optimale screening, diagnostiek en behandeling er inhoudelijk uitzien. Indien mogelijk wordt ook beschreven in welke vorm een interventie het beste aangeboden kan worden. Daarnaast worden in een apart hoofdstuk aanbevelingen gedaan voor de organisatie van zorg. In deze richtlijn worden de ‘klinische uitgangsvragen’ behandeld in de verschillende hoofdstukken.
Aanbevelingen
Aanbevelingen kunnen gegradeerd worden als sterk of zwak (voorwaardelijk). Wanneer de kwaliteit van het bewijs voor de positieve en negatieve effecten van een interventie hoog is, kan dit leiden tot een sterke aanbeveling, en omgekeerd: wanneer de bewijskracht laag tot zeer laag is, kan dit een zwakke aanbeveling opleveren. Een zwakke aanbeveling geeft meer ruimte om af te wijken en aandacht te schenken aan alternatieven die passen bij de behoeften van de patiënt, terwijl bij een sterke aanbeveling die ruimte beperkt is.
Echter, de kracht van het wetenschappelijke bewijs is niet de enige factor die de sterkte van de aanbevelingen bepaalt. De aanbevelingen zijn gebaseerd op enerzijds wetenschappelijk bewijs, en anderzijds op overige overwegingen, zoals: praktijkervaringen van de werkgroepleden, ervaringen en voorkeuren van patiënten met een bipolaire stoornis en familie, kosten, beschikbaarheid (in verschillende echelons) en organisatorische aspecten. Deze laatste zijn opgenomen onder het kopje ‘Overige overwegingen’ (zie tabel 6).
Tabel 6. Bepaling van sterkte van aanbeveling volgens GRADE
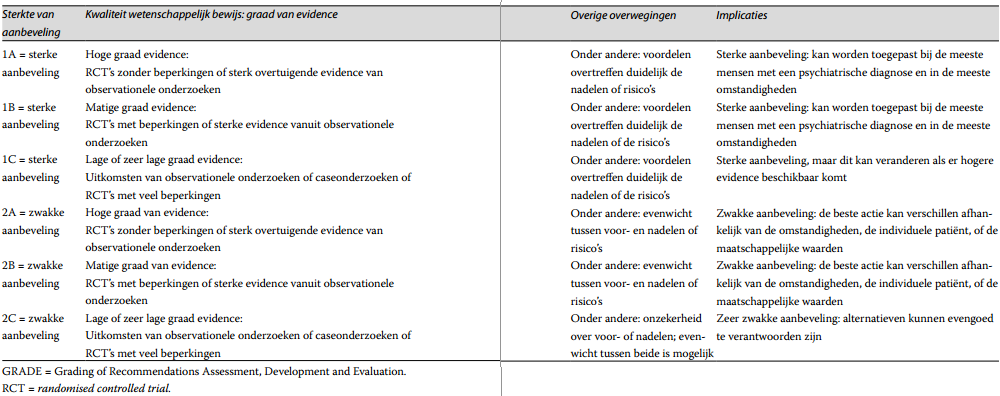
Methode health economics
Het doel van health economics is om bij te dragen aan de ontwikkeling van richtlijnen: door bewijs te leveren over de kosteneffectiviteit van interventies voor volwassenen met een bipolaire stoornis. Dit is bereikt door:
systematische literatuursearch naar bestaand economisch bewijs; beslissingsanalytisch economisch modelleren.
Systematische literatuursearches naar economisch bewijs zijn uitgevoerd voor alle gebieden die aan bod komen in de richtlijn. Het economisch modelleren (modelleren is het op grond van modellen nabootsen van de werkelijkheid met, in dit geval, als doel om de kosten en effecten van interventies te voorspellen) heeft plaatsgevonden op gebieden waarop belangrijke implicaties voor de benodigde middelen werden verwacht, waarop de huidige mate van onzekerheid over de kosteneffectiviteit significant was, en van een economische analyse werd verwacht dat deze de onzekerheid zou kunnen verminderen.
Deze economische modellering vond plaats volgens The guidelines manual (nice, 2012). De rationale voor prioritering van bepaalde klinische uitgangsvragen voor het economisch modelleren was beschreven in een economisch plan, opgesteld in overeenstemming met nice, de richtlijnwerkgroep, de gezondheidseconoom en andere leden van het technische team. Op basis hiervan is een economisch model ontwikkeld om de kosteneffectiviteit te bepalen van medicatie bij volwassenen met een bipolaire stoornis in een acute depressieve episode.
Zoekstrategie
Er is een systematische literatuurzoekstrategie uitgevoerd om al het relevante bewijs op te sporen. De zoekstrategieën zijn beperkt tot economische onderzoeken en health technology assessment reports, en zijn uitgevoerd in de volgende databanken:
- EconLit (the American Economic Association’s electronic bibliography);
- Health Technology Assessment- (hta-) database;
- Embase;
- medline; medline In-Process;
- nhs Economic Evaluation Database (nhseed);
- Psycinfo.
Daarnaast werden Google en Google Scholar doorzocht op onderzoeken die mogelijk waren gemist door de elektronische databanken. Verder werd literatuur in eerdere richtlijnen gecontroleerd. Enig relevant bewijs vanuit de klinische literatuursearch werd in deze periode aan de gezondheidseconoom beschikbaar gesteld. De zoektermen voor de economische searches zijn te vinden onder Aanverwanten.
Selectiestrategie
De volgende selectiecriteria zijn toegepast om vanuit de resultaten van economische searches onderzoeken te selecteren voor nadere evaluatie.
- Er zijn alleen onderzoeken geïncludeerd van Organisation for Economic Co-operation en ontwikkelde landen (Organisation for Economic Co-operation and Development (oecd), omdat het doel van de review was om economische informatie op te sporen die toepasbaar is op de Nederlandse en Britse context.
- Selectiecriteria voor soorten klinische condities, gebruikers van zorg en interventies die worden beoordeeld waren identiek aan die in de klinische literatuurreviews.
- Een voorwaarde voor inclusie van onderzoeken was dat deze voldoende details beschreven over methoden en resultaten en dat de gegevens en de resultaten van het onderzoeken extraheerbaar waren. Dit om het mogelijk te maken om de methodologische kwaliteit van het onderzoeken te beoordelen. Posterpresentaties en abstracts werden geëxcludeerd.
- Zowel volledige economische evaluaties die twee of meer opties vergeleken en die kosten en consequenties beoordeelden, zijn meegenomen, als eenvoudige kostenanalyses.
- Economische onderzoeken zijn meegenomen wanneer ze gegevens over klinische effectiviteit gebruikten vanuit een rct, een cohortonderzoek, een systematische review en meta-analyse, of klinische onderzoeken.
Beoordelingsstrategie
Alle economische artikelen die voldeden aan de inclusiecriteria, zijn beoordeeld op hun toepasbaarheid en kwaliteit met behulp van de methodologische checklist voor economische evaluaties van nice, die is opgenomen in de aanverwanten van deze richtlijn. De methodologische checklist voor economische evaluaties werd ook toegepast op het economische model dat specifiek voor deze richtlijn is ontwikkeld. Onderzoeken die volledig of gedeeltelijk voldeden aan de criteria voor toepasbaarheid en kwaliteit zoals beschreven in de methodologische checklist, werden nader beschouwd tijdens het proces van richtlijnontwikkeling, samen met de resultaten van het economisch model. Ook de ingevulde methodologische checklists voor alle economische evaluaties die voor deze richtlijn zijn bestudeerd, zijn opgenomen in de aanverwanten.
Beschrijving van de resultaten en conclusies
Het economische bewijs dat is geëvalueerd voor deze richtlijn, is weergegeven in de verschillende modulen, volgend op het relevante klinische bewijs. Methoden en resultaten van de economische modellering zijn opgenomen als aanverwant. Kenmerken en resultaten van alle geëvalueerde onderzoeken zijn samengevat in economische bewijsprofielen, samen met bijbehorende klinische bewijsprofielen volgens grade.
