Manie
Uitgangsvraag
Wat is de effectiviteit en wat zijn de bijwerkingen van farmacologische interventies voor acute manie, hypomanie en gemengde episoden bij volwassenen met een bipolaire stoornis?
Aanbeveling
Algemene aanbevelingen over de behandeling van acute manie
- Een manie moet zo snel mogelijk worden behandeld met medicatie, ondersteunende en beschermende interventies, en begeleiding van naasten.
- Bij het beoordelen van de ernst van een manie en de noodzaak tot ingrijpen moeten de observaties en het oordeel van naasten worden meegewogen.
- Behandeling van een ernstige manie moet klinisch plaatsvinden, desnoods onvrijwillig, ook gegeven de grote belasting van naasten. Echter, als het toestandsbeeld van de patiënt, de thuissituatie en draagkracht van de naasten een adequate intensieve outreachende ambulante behandeling mogelijk maken, heeft dat de voorkeur.
- De patiënt en de naasten moeten vanaf het begin worden ingelicht over de fasering van de behandeling (acute behandeling – vervolgbehandeling – onderhoudsbehandeling - deprescribing (van m.n. ingrijpmedicatie in de acute fase)), de duur daarvan en de implicaties voor de verdere behandeling, zodat zij weten wat zij kunnen verwachten wanneer welke afwegingen zullen worden gemaakt.
- Bij de keuze van de medicamenteuze behandelstrategie moet gebruik worden gemaakt van eerdere ervaringen (ook van eerstegraads familieleden), bijwerkingen, het profiel (zie overwegingen) van de patiënt, en diens voorkeur.
- Aansluitend aan de acute behandeling wordt geëvalueerd hoe de manische episode is verlopen en wat effectieve en minder effectieve interventies (medicatie, bejegening, separatie, etc.) waren, en wordt in een crisis-signaleringsplan opgenomen hoe een eventuele volgende episode zo spoedig mogelijk gesignaleerd en behandeld kan worden.
- Tegen het einde van de voortgezette behandeling moet in overleg met de patiënt en naasten, en het profiel van de patiënt meewegend, een besluit worden genomen over het starten c.q. voortzetten van een preventieve medicamenteuze onderhoudsbehandeling.
- Bij een klinische opname worden de volgende verpleegkundige interventies aangeraden: het bieden van structuur, grenzen stellen, het waarborgen van medicatie-inname en het verzamelen en verstrekken van informatie over de toestand van de patient (Daggenvoorde e.a., 2015; Goossens e.a., 2022).
Specifieke aanbevelingen over de farmacotherapie van acute manie
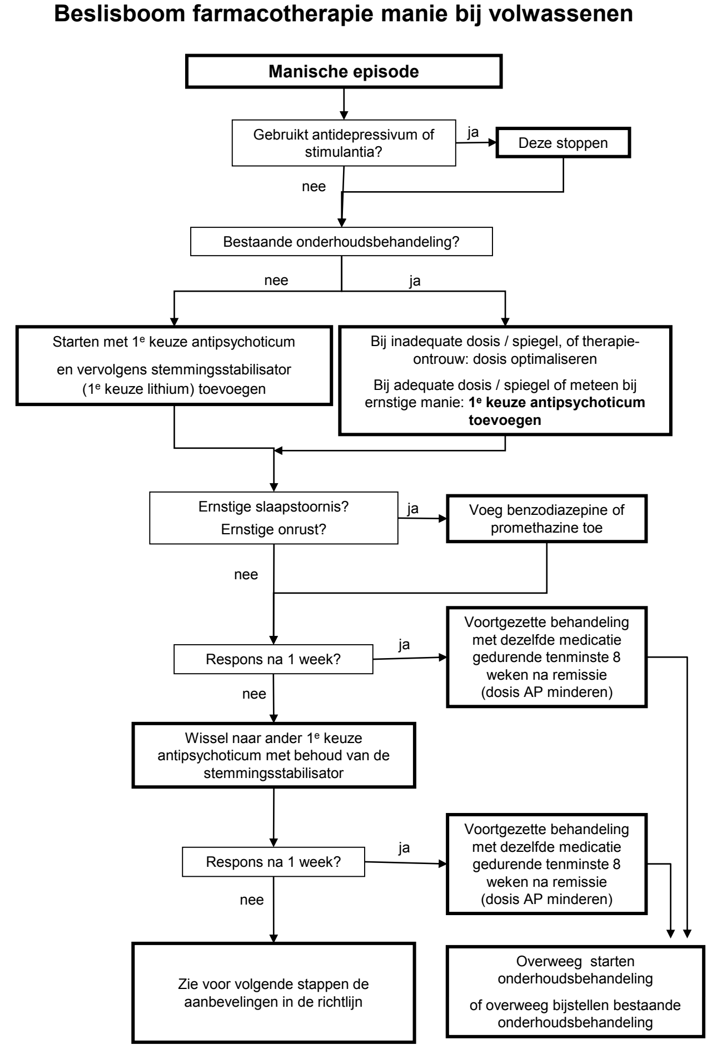
Zie ook beslisboom 6.1 Behandeling manische episode bij volwassenen.
- Indien de manische patiënt een antidepressivum of stimulantia gebruikt, al dan niet in combinatie met onderhoudsmedicatie, wordt dit direct geheel gestaakt, waarbij men alert is op eventuele onttrekkingsverschijnselen, vooral bij antidepressiva met een korte halfwaardetijd; in geval van comorbide ADHD kunnen stimulantie na volledige remissie van de manie in de onderhoudsfase worden hervat.
- Beoordeel of er nog andere medicatie wordt gebruikt die tot manie kan leiden (zoals corticosteroiden, sommige antibiotica) en stop deze indien mogelijk.
- Indien de manische patiënt nog geen onderhoudsmedicatie gebruikt is de medicatie van eerste keuze een antipsychoticum (in alfabetische volgorde: aripiprazol, cariprazine, haloperidol, olanzapine, paliperidon, quetiapine, risperidon); hieraan wordt al in de acute fase zo spoedig mogelijk een stemmingsstabilisator toegevoegd; dat is bij voorkeur lithium of als tweede keuze valproïnezuur (behalve bij vrouwen en mannen in de vruchtbare leeftijd) of als derde keuze carbamazepine (behalve bij vrouwen in de vruchtbare leeftijd).
- Bij een lichte tot matig ernstige manie kan overwogen worden om in de acute fase te behandelen met lithium of valproïnezuur als monotherapie.
- Indien er sprake is van therapieontrouw of het staken van de bestaande onderhoudsmedicatie, of als deze te laag gedoseerd is, moet de onderhoudsmedicatie worden hervat, c.q. de dosis worden geoptimaliseerd; bij onvoldoende respons na een week moet hieraan worden toegevoegd een eerdergenoemd antipsychoticum van eerste keuze; bij ernstige manie wordt meteen een antipsychoticum toegevoegd.
- Indien de manische patiënt al onderhoudsmedicatie met een stemmingsstabilisator gebruikt in een adequate dosering voor acute manie, wordt hieraan een van de eerdergenoemde antipsychotica van eerste keuze toegevoegd.
- Bij de keuze van het antipsychoticum wordt rekening gehouden met het werkingsprofiel (uitsluitend antimanisch, of ook antidepressief) en bijwerkingenprofiel van het middel en het profiel van de patiënt, met name het vóórkomen van depressieve episoden.
- Indien bij een ernstige manie medicatie wordt geweigerd en in overeenstemming met de regelgeving tot dwangbehandeling wordt overgegaan, is van de eerder genoemde antipsychotica een kortwerkende intramusculair toedieningsvorm beschikbaar van aripiprazol, haloperidol en olanzapine.
- Als het gekozen antipsychoticum niet goed wordt verdragen komt een van de andere antipsychotica, mede op geleide van het bijwerkingenprofiel, in aanmerking.
- Een manische episode met gemengde (depressieve) kenmerken wordt behandeld als een manie.
- Slaapstoornissen en onrust kunnen tijdelijk worden behandeld met toevoegen van een benzodiazepine (zoals lorazepam) of promethazine; dit moet zo spoedig als mogelijk weer worden afgebouwd.
- Indien de genoemde antipsychotica niet effectief blijken te zijn, moet behandeling met clozapine overwogen worden (Delgado et al., 2020).
- Indien een ernstige manische episode binnen een acceptabele periode onvoldoende reageert op medicamenteuze behandeling, moet elektroconvulsietherapie (ECT) overwogen worden (zie hoofdstuk Overige biologische behandeling).
- Bij het beoordelen van de effectiviteit van de gekozen behandelstrategie en -middelen moeten duidelijke termijnen worden aangehouden (zie ook beslisboom 6.1 Behandeling manische episode bij volwassenen).
- bij een adequate dosering moet na één week tenminste een beginnende respons zichtbaar zijn;
- bij onvoldoende respons na één week met een adequate dosering moet met een ander antipsychoticum worden behandeld.
- De acute behandeling van een manische episode wordt na symptomatische remissie in alle gevallen gevolgd door een voortgezette behandeling gedurende minstens 8 weken.
- Tijdens deze voortgezette behandeling worden dezelfde middelen gebruikt als in de acute fase, maar wordt de dosering van het antipsychoticum geleidelijk verminderd op geleide van het klinische beeld en eventuele bijwerkingen; bij een combinatie met een stemmingsstabilisator wordt deze (eventueel in aangepaste dosering op geleide van het beeld) altijd voortgezet tot het einde van de voortgezette behandeling, anticiperend op een mogelijke onderhoudsbehandeling met de stemmingsstabilisator.
- Bij de keuze van medicatie moet in acht genomen worden of het desbetreffende middel voor deze toepassing in Nederland is geregistreerd, of dat het een off-label voorschrift betreft van een middel dat voor een andere toepassing is geregistreerd (zie tabel 6.5 Medicatie die in Nederland geregistreerd is voor toepassing bij bipolaire stoornissen). Raadpleeg voor actuele informatie over de beschikbaarheid van medicatie in Nederland www.cbg-med.nl.
- Voor specifieke aanbevelingen over de behandeling van manie bij kinderen en bij oudere volwassenen wordt verwezen naar de desbetreffende hoofdstukken.
Beslisboom 6.1 Behandeling manische episode bij volwassenen
|
Categorie |
Geneesmiddel |
|
Stemmingsstabilisatoren |
Carbamazepine, Lamotrigine, Lithium, Topiramaat, Valproïnezuur, Verapamil |
|
Atypische antipsychotica |
Aripiprazol, Cariprazine, Olanzapine, Quetiapine, Risperidon |
|
Typische antipsychotica |
Haloperidol |
|
Antidepressiva (SSRI/SNRI) |
Fluoxetine, Venlafaxine |
Overwegingen
Behandelstrategie
- De ernst van een manische episode kan bij een kortdurend (crisis-) contact worden onderschat; het is daarom van belang om de observaties en het oordeel van naasten zwaar mee te wegen. Een (aanvankelijk) hypomanische toestand kan in ernst beperkt lijken en ook blijven, maar kan ook een voorbode zijn van een ernstige manie.
- Bij het bepalen van de behandelstrategie en de keuze van de medicatie wordt het profiel van de patiënt meegewogen, zoals leeftijd, geslacht, levensfase, somatische gezondheid, lichaamsgewicht, eerdere beloop, postpartum manie, eerdere respons op (anti-manische) medicatie, middelengebruik, comorbide psychiatrische aandoeningen, familiaire belasting en eventuele vastgelegde afspraken in een zelfbeschikkingsovereenkomst.
- Bij de keuze van de middelen voor de behandeling van een acute manie is het van belang om al vanaf het begin een indicatie en voorkeur voor het starten of voortzetten van een onderhoudsbehandeling mee te wegen.
- Uit een recente netwerkmeta-analyse blijkt dat de combinatie van een antipsychoticum en een stemmingsstabilisator bij acute manie effectiever is dan monotherapie met een van beide. Vanwege het acute karakter van het beeld en de noodzaak om snel in te grijpen wordt aangeraden om eerst te starten met een antipsychoticum en vervolgens, als de toestand van de patiënt een gesprek en besluit hierover mogelijk maakt, een stemmingsstabilisator toe te voegen. Dit geldt met name bij een eerste manische episode of indien de patiënt nog geen stemmingsstabilisator gebruikt.
- Bij de keuze voor een stemmingsstabilisator heeft lithium de voorkeur vanwege de superieure effectiviteit; valproïnezuur is bovendien gecontra-indiceerd bij vrouwen in de vruchtbare leeftijd en waarschijnlijk ook bij mannen met een kinderwens; carbamazepine is ook gecontra-indiceerd bij vrouwen in de vruchtbare leeftijd, en kan bovendien leiden tot veel interacties met andere medicatie; lamotrigine is niet effectief bij acute manie maar hoeft in de meeste gevallen niet te worden afgebouwd indien de patiënt dit al gebruikt, tenzij (in zeldzame gevallen) er sterke aanwijzingen zijn dat de behandeling met lamotrigine heeft bijgedragen aan de huidige manische episode.
- Indien de patiënt al onderhoudsmedicatie gebruikt en er sprake is van een adequate dosering en goede therapietrouw, is het van belang om de effectiviteit hiervan bij elke nieuwe episode te heroverwegen opdat een mogelijk onwerkzame behandeling niet wordt voortgezet.
- Bij therapieontrouw, of het staken van een eerder effectieve onderhoudsmedicatie, of bij te lage dosering, is het van belang om samen met patiënt en naasten de balans tussen effectiviteit en ongewenste effecten opnieuw te beoordelen; indien deze gunstig uitvalt wordt geadviseerd om het gebruik van de stemmingsstabilisator te hervatten.
- Bij een manische episode met gemengde (depressieve) kenmerken is het inschatten van suïcidaliteit van belang.
- Een hypomanische episode hoeft in het algemeen slechts medicamenteus behandeld te worden conform de richtlijn voor acute manie, als die een voorbode lijkt te vormen van een manie (bijvoorbeeld een hypomanie bij een patiënt met een bipolaire-I-stoornis) of op verzoek van de patiënt als die (b.v. in de werksituatie) veel hinder ondervindt van aanhoudende verschijnselen.
- Na symptomatische remissie van de manie is de duur van voortgezette behandeling tenminste 8 weken. Maar er zijn ook aanwijzingen dat pas na 6 maanden van aanhoudende remissie van symptomatisch herstel gesproken kan worden (Tohen e.a., 2009).
- Waar de aanbevelingen over de keuze van effectieve medicatie vooral berust op wetenschappelijke evidentie, zijn de voorgestelde behandelstrategieën vooral gebaseerd op consensus vanuit de klinische praktijk.
- Tijdens de voortgezette behandeling nadat de manie in remissie is kan gestart worden met psychologische behandeling gericht op verwerking van het beleven van de manische episode overwogen worden (zie hoofdstuk Psychologische en psychosociale interventies).
- Bij de keuze van een middel worden eerdere ervaringen van de patiënt m.b.t. effect en bijwerkingen meegewogen. Raadpleeg voor een overzicht van mogelijke bijwerkingen en interacties met andere geneesmiddelen www.farmacotherapeutischkompas.nl.
Balans tussen gewenste en ongewenste effecten
- Bij een acute manie weegt effectiviteit zwaarder dan eventuele bijwerkingen, gegeven de ernst van de toestand en de relatief korte duur van de behandeling.
- Bij een ernstige manie heeft het de voorkeur om medicamenteuze behandeling in het begin voldoende hoog te doseren en pas in tweede instantie op geleide van eventuele bijwerkingen de doseringen te verlagen; dit geldt ook voor combinatiebehandelingen.
- Lagere doseringen worden over het algemeen beter verdragen dan hoge doseringen, wat de therapietrouw kan bevorderen, maar zijn mogelijk minder effectief.
- Combinatietherapie is effectiever dan monotherapie, geeft meestal geen significant grotere kans op bijwerkingen, en leidt daardoor gemiddeld niet tot meer uitval.
Kwaliteit van het bewijs
- De kwaliteit van het bewijs varieert van laag tot redelijk. De voornaamste reden voor afwaarderen betreft de kans op vertekening (o.a. wegens onvolledige beschrijving van het randomisatie proces en reporting bias; bovendien hadden veel patiënten in de studies al medicatie voor randomisatie). Er zijn meerdere recente meta-analyses opgenomen in deze onderbouwing, met daarin trials bij een omvangrijke patiëntenpopulatie.
- Niet alle in wetenschappelijke studies gebruikte middelen zijn verkrijgbaar in Nederland (zoals asenapine, ziprasidon, valnoctamide), en tamoxifen is niet geregistreerd voor psychiatrische toepassingen; deze middelen zijn daarom niet in deze richtlijn meegenomen. Raadpleeg voor een actueel overzicht van de beschikbaarheid van medicatie in Nederland www.cbg-med.nl.
Patiëntenperspectief
- Bij de communicatie tussen behandelaar, patiënt en naasten is het van belang om een goede balans te vinden tussen het bewaren van vertrouwelijkheid en het bevorderen van een optimale uitwisseling van informatie, om effectief te kunnen (be)handelen zonder de onderlinge (werk-) relaties te schaden.
- Alle besluiten over medicamenteuze behandeling moeten in overleg met de patiënt en naasten worden genomen. Hierbij wordt rekening gehouden met een vaak beperkt ziekte-inzicht en daardoor beperkte motivatie voor behandeling bij de manische patiënt.
Naastenperspectief
- Zeker bij een manische episode dienen naasten steeds bij de behandeling betrokken te worden, zowel in de ambulante als de klinische setting.
- Naasten hebben vooral in de thuissituatie goed zicht op de toestand van de manische patiënt; hun beoordeling daarvan moet worden meegewogen in het te voeren beleid.
- Naasten moeten ook vanuit de behandelaars ondersteuning krijgen in de omgang met de manische patiënt en de daaruit voortkomende problemen op korte en lange termijn, zowel emotioneel (zoals trauma, hechting, schaamte) als praktisch (zoals schulden, schade, echtscheiding).
- Als in het gezin van de manische patiënt ook kinderen zijn moet er zowel in de acute fase als nadien aandacht zijn voor het effect van het manische gedrag of een (onvrijwillige) opname op het kind en op de ouder-kind relatie.
- Een manische episode kan voor naasten zeer belastend zijn door het ontremde, vijandige, seksueel ontremde en soms gevaarlijke gedrag, en het verlies van contact met de patiënt. Het gebrek aan inzicht bij de patiënt kan overleg over diens situatie en de te nemen maatregelen in de weg staan, waardoor het onmogelijk wordt om daarover overeenstemming te bereiken.
- Naasten kunnen in een conflict van belangen terecht komen als zij tegen de wens van de manische patiënt om professionele hulp willen vragen. Dit kan ook voorkomen in een lopende behandeling bij een dreigende manische ontregeling. Het wordt aanbevolen om een dergelijke situatie al in het begin van de behandeling met de patiënt en naasten te bespreken en daarover afspraken te maken.
Het professionele perspectief
- De behandeling van een acuut manische patiënt, en de daarbij te nemen beslissingen, soms tegen de wil van de patiënt in, kunnen belastend zijn voor de professionals die bij de behandeling betrokken zijn; intervisie is daarbij belangrijk.
- Na remissie van de manie moet aandacht besteed worden aan een eventueel verstoorde behandelrelatie door het ingrijpen in de acuut manische fase.
Middelenbeslag
- Bij een acute manie is het niet zinvol om de kosten van de medicatie bij de keuze te betrekken, ook omdat er geen grote prijsverschillen zijn. Vanwege de ernst van de symptomen en de relatief korte duur van de behandeling met deze extra medicatie weegt de effectiviteit in deze fase zwaarder dan de directe kosten. Bij een eventuele opname worden de kosten vooral bepaald door de duur van de opname.
Organisatie van zorg
- Vanwege de mogelijk ernstige gevolgen van het manische handelen voor de patiënt en zijn omgeving, en de belasting van de naasten, vindt de behandeling van ernstige acute manie meestal in een klinische setting plaats tenzij de toestand van de patiënt en de thuissituatie ambulante behandeling haalbaar maken. Dit zal mede afhankelijk zijn van de beschikbaarheid van outreachende GGZ-voorzieningen zoals FACT en intensieve thuisbehandeling.
- Bij een klinische opname moet de eventuele ambulante behandelaar bij de behandeling betrokken worden.
Onderbouwing
Farmacotherapie van bipolaire stoornissen.
Farmacotherapie is een essentieel onderdeel van de multidisciplinaire behandeling van de bipolaire stoornis. Dat geldt zowel voor de acute fasen van manie en depressie, eventueel bij een rapid-cycling beloop, zoals in dit hoofdstuk aan bod komt, als voor preventieve onderhoudsbehandeling, besproken in hoofdstuk Farmacotherapie voor onderhoudsbehandeling. Farmacotherapie staat daarom nooit op zichzelf, maar is altijd ingebed in een multidisciplinaire behandeling.
Bij medicamenteuze en andere behandeling van acute episoden van een bipolaire stoornis kan het gaan om patiënten die sterk van elkaar verschillen. Patiënten kunnen bij de arts komen met een eerste manische episode, al dan niet voorafgegaan door één of meer depressieve episoden of ook wel (onopgemerkte) hypomanieën. Anderen hebben al een diagnose bipolaire stoornis en krijgen een recidief episode ondanks een (al dan niet adequaat uitgevoerde) onderhoudsbehandeling. Weer anderen zijn om uiteenlopende redenen gestopt met de onderhoudsbehandeling en worden geconfronteerd met een recidief. Bij de keuze voor een bepaalde medicatie moet men altijd rekening houden met deze individuele aspecten. Daarom is het noodzakelijk om informatie te hebben over eerdere medicamenteuze behandelingen (duur, dosering, effectiviteit, verdraagbaarheid) en ervaringen bij eventuele eerstegraads familieleden met een bipolaire stoornis. Daarnaast speelt de voorkeur van de patiënt een belangrijke rol bij de keuze van medicatie.
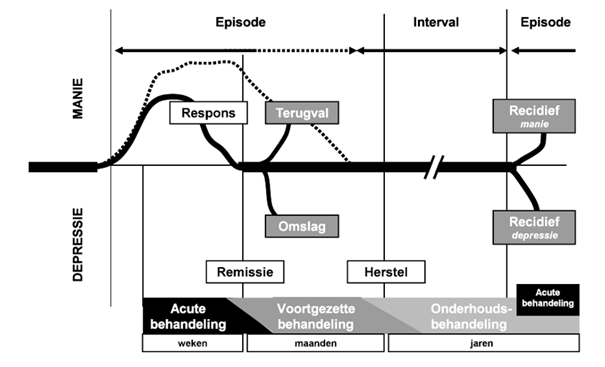
De acute behandeling leidt in geval van een gunstige respons tot remissie van de (meeste) symptomen, die vaak pas later wordt gevolgd door herstel (zie figuur 6.1 Fasering van de farmacotherapie van bipolaire stoornissen). Om het resultaat van de acute behandeling te bestendigen en terugval (relaps) te voorkomen, gaat de behandeling na remissie gedurende enige tijd over in een voortgezette behandeling. Dit is dus een integraal onderdeel van de behandeling van de huidige episode. De duur van deze voortgezette behandelfase is niet precies te definiëren, en is waarschijnlijk wat korter voor de manie dan voor de depressie, maar vanwege een brede expertconsensus (Tohen e.a., 2009) is voorgesteld om hiervoor een periode van minstens acht weken aan te houden waarin de patiënt (vrijwel) geen symptomen van manie, hypomanie of depressie meer vertoont. De fasering van de behandeling is schematisch weergegeven in figuur 6.1 Fasering van de farmacotherapie van bipolaire stoornissen.
Figuur 6.1 Fasering van de farmacotherapie van bipolaire stoornissen
Getoond is de acute manie; voor depressie geldt dezelfde terminologie. De stippellijn geeft het veronderstelde onbehandelde (‘natuurlijke’) beloop van de episode weer.
Overigens is deze duur arbitrair en gaan de behandelfasen in de praktijk geleidelijk in elkaar over. Bij de individuele patiënt wordt dit mede bepaald door de ernst van de episode, de psychosociale gevolgen, de mate van symptomatische remissie dan wel persisterende restsymptomen, en de ervaringen bij eerdere episoden.
Verder betekent symptomatisch herstel nog niet dat er ook een volledig herstel van psychosociaal functioneren is opgetreden: vaak neemt dit functionele herstel meer tijd in beslag. De term herstel heeft hier betrekking op herstel van de huidige episode, niet herstel van de bipolaire stoornis, ervan uitgaande dat bij de meeste patiënten de kwetsbaarheid hiervoor van blijvende aard is. Bovendien wordt het begrip ‘herstel’ in de psychiatrie ook in een veel ruimere betekenis gebruikt.
Tijdens de voortgezette behandeling weegt men opnieuw de balans tussen effectiviteit en eventuele bijwerkingen van de toegepaste medicatie af, en worden indien nodig doseringen aangepast. In de loop van de voortgezette behandeling wordt er een besluit genomen over de (indicatie voor) onderhoudsbehandeling (zie hoofdstuk Farmacotherapie voor onderhoudsbehandeling). Het is van belang om de patiënt en diens naasten vanaf het begin goed in te lichten over deze fasering van de behandeling, opdat zij weten wat zij kunnen verwachten en welke afwegingen op welk moment worden gemaakt.
Bij de farmacotherapie kan men onderscheid maken tussen een farmacotherapeutische strategie (het doel; de timing, fasering en duur van de behandeling; de achtereenvolgende stappen afhankelijk van respons dan wel non-respons) en de keuze van de middelen (type medicatie en specifieke middelen als monotherapie of combinatietherapie). De wetenschappelijke evidentie betreft vooral de effectiviteit van specifieke medicatie, terwijl de behandelstrategieën en de (volgorde van) keuze van de middelen vooral berusten op consensus vanuit de klinische praktijk. Een dergelijke consensus is mede vastgelegd in andere internationale richtlijnen voor de behandeling van bipolaire stoornissen.
Veel evidentie is gebaseerd op onderzoek met patiënten met een bipolaire-I-stoornis. Dit geldt per definitie voor de behandeling van manie. Bij sommige onderzoeken naar de behandeling van de bipolaire depressie werden zowel patiënten met een bipolaire-I-stoornis als met een bipolaire-II-stoornis onderzocht, en in een enkel onderzoek alleen patiënten met een bipolaire-II-stoornis.
Voor de term stemmingsstabilisator (mood stabilizer) bestaat geen eenduidige definitie, maar toch wordt deze zowel in de praktijk als in de wetenschappelijke literatuur veel gebruikt voor middelen die effectief zijn in de acute fase (manie en/of depressie) en tevens preventief werkzaam zijn in de onderhoudsfase zonder een stemmingsomslag te induceren. Er is echter geen enkel middel waarvan men op voorhand mag verwachten dat het al deze effecten in alle fasen van de stoornis bij het merendeel van de patiënten teweegbrengt. Meestal wordt de term stemmingsstabilisator gebruikt voor lithium, valproïnezuur, carbamazepine en lamotrigine, en soms ook voor sommige atypische antipsychotica die in de onderhoudsfase worden toegepast (zie hoofdstuk Farmacotherapie voor onderhoudsbehandeling).
In module Farmacotherapie acute episoden wordt eerst de behandeling van de manie besproken (module Manie, zie aldaar), en vervolgens de behandeling van de bipolaire depressie (module Bipolaire depressie, zie onderstaande). Niet zelden lopen de symptomen van manie en depressie door elkaar (episoden met gemengde kenmerken), of wisselen episoden elkaar snel af (module Rapid cycling, zie aldaar). Dit kan zowel de behandelstrategie als de keuze van de middelen beïnvloeden. Manische episoden met gemengde (namelijk depressieve) kenmerken worden in grote lijnen behandeld als een manie. Over de behandeling van depressieve episoden met gemengde (namelijk manische) kenmerken is veel minder bekend. De behandeling van manische en depressieve stemmingsepisoden bij een rapid cycling beloop wordt apart besproken. Aan de aanbevelingen zijn beslisbomen toegevoegd. Deze beslisbomen berusten in hoge mate op klinische consensus, bij gebrek aan wetenschappelijk onderzoek naar dergelijke behandelalgoritmen.
Farmacotherapie van acute manie
De behandeling van de patiënt met een manie vergt naast kennis van de medicamenteuze behandelstrategieën en -middelen een combinatie van tact, doortastendheid en goede timing. Hulp en inzet van anderen (zowel naasten als andere hulpverleners zoals een crisisdienst) zijn vaak onontbeerlijk. Vooral in het beginstadium van een manische decompensatie is de informatie van anderen die de patiënt de hele dag meemaken, van groot belang om de ernst van de situatie juist te kunnen inschatten.
Het doel van de behandeling is een snelle vermindering van de manische symptomen en beperking van de schade die de manische patiënt zichzelf (en anderen) kan toebrengen. Bij de ernstige manie is daarvoor vaak een al dan niet vrijwillige klinische opname noodzakelijk. Een manie, zeker indien deze gepaard gaat met een (soms gedwongen) opname, is zowel voor de patiënt als diens naasten een zeer ingrijpende en soms zelfs traumatische gebeurtenis. De begeleiding van de acuut manische patiënt vergt bovendien veel van medewerkers van een opnameafdeling. Naast effectieve farmacotherapie is een goede begeleiding van alle betrokken partijen dan ook van groot belang.
De grens tussen hypomanie en manie is soms moeilijk aan te geven en wordt per definitie bepaald door de ernst van de manische symptomen en de gevolgen daarvan voor het gedrag van de patiënt. Ook hierbij zijn de observaties van naasten van belang. Een hypomanische toestand kan in ernst beperkt blijven (dit blijkt pas achteraf) of een voorbode zijn van een (ernstige) manie.
|
⊕⊕ΟΟ
|
Een combinatietherapie van stemmingsstabilisatoren (MS) en antipsychotica (AP) geeft mogelijk een effectievere respons dan een monotherapie van MS of AP, na drie en na zes weken. Tajika2022 |
|
⊕⊕ΟΟ
|
Een combinatietherapie van stemmingsstabilisatoren (MS) en antipsychotica (AP) is mogelijk effectiever in het verminderen van manische symptomen dan een monotherapie van MS of AP, na één, drie, en zes* weken. *MS+AP Combinatietherapie lijkt na 6 weken effectiever dan MS-monotherapie, maar niet effectiever dan AP-monotherapie. Tajika2022 |
|
⊕⊕ΟΟ
|
Een combinatietherapie van stemmingsstabilisatoren (MS) en antipsychotica (AP) is mogelijk niet effectiever in het tegengaan van drop-out dan een monotherapie van MS of AP, na drie en na zes weken. Tajika2022 |
|
⊕⊕ΟΟ
|
Een combinatietherapie van stemmingsstabilisatoren (MS) en antipsychotica (AP) leidt mogelijk tot meer bijwerkingen dan een monotherapie van MS of AP, na drie* en na zes weken. *Bijwerkingen na drie weken zijn alleen gemeten voor de vergelijking MS+AP met MS-monotherapie. Tajika2022 |
|
⊕⊕⊕Ο
|
Aripiprazol, Carbamazepine, cariprazine, haloperidol, lithium, olanzapine, paliperidon, quetiapine, risperidon, en valproaat (in alfabetische volgorde) hebben waarschijnlijk een effectievere behandelrespons dan placebo. Kishi2022 |
|
⊕⊕ΟΟ
|
Asenapine en ziprasidon hebben mogelijk een effectievere behandelrespons dan placebo. Kishi2022 |
|
⊕⊕⊕Ο
|
aripripazol, Carbamazepine, cariprazine, valproaat*, haloperidol, lithium, olanzapine, paliperidon, quetiapine, en risperidon (in alfabetische volgorde) zijn waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo. Hong2022, Kishi2022 *Alleen aangetoond door Hong2022 |
|
⊕⊕ΟΟ
|
Lamotrigine en oxcarbazepine zijn mogelijk niet effectiever in het verminderen van manische symptomen dan placebo. Kishi2022, Hong2022 |
|
⊕⊕⊕Ο
|
Topiramaat en verapamil zijn waarschijnlijk niet effectiever in het verminderen van manische symptomen dan placebo. Kishi2022, Hong2022 |
|
⊕⊕ΟΟ
|
lamotrigine, oxcarbazepine, topiramaat en verapamil hebben mogelijk niet een effectievere behandelrespons dan placebo. Kishi2022 |
|
⊕⊕⊕Ο
|
Asenapine, haloperidol en lithium behandeling resulteren waarschijnlijk in meer uitval wegens bijwerkingen dan placebo. Kishi2022 |
Farmacologische behandeling – Kishi (2022)
In een goed uitgevoerde netwerk meta-analyse (Kishi et al., 2022) werd de effectiviteit van farmacologische interventies voor bipolaire manie bij volwassenen onderzocht. In totaal werden 72 RCTs opgenomen in de meta-analyse, waarin 23 verschillende farmaca werden vergeleken met placebo. De volgende farmaca werden geïncludeerd (aantal studies/aantal patiënten): aripiprazol (9/1205), asenapine0F0F* (3/620), brexpiprazole* (2/321), carbamazepine (6/305), cariprazine (3/612), chlorpromazine (1/10), endoxifen (2/55), eslicarbazepine* (2/148), haloperidol (10/1023), lamotrigine (3/173), licarbazepine* (1/324), lithium (20/965), olanzapine (14/1565), oxcarbazepine* (1/30), paliperidon (2/542), quetiapine (5/630), risperidon (7/676), tamoxifen* (2/43), topiramaat (4/659), valnoctamide* (1/71), valproaat (14/981), verapamil (1/17), ziprasidon* (3/458), en placebo (48/5009).
De studie omvatte in totaal 16442 patiënten met een gemiddelde leeftijd van 40 jaar, en de studieduur was gemiddeld 4 weken. In 38 studies werden patiënten met gemixte episoden opgenomen, en in 35 studies werden patiënten met psychose geïncludeerd.
De primaire uitkomsten waren behandelrespons (effectiviteit) en all-cause discontinuation (acceptatie). De definitie van behandelrespons die werd gebruikt is meer dan 50% verbetering in de manie score. Als toevoeging daarop werd de behandelrespons gemeten na 7-10 dagen, 3 weken, 4-6 weken, en 8-12 weken om aan te tonen hoelang de anti-manische effecten aanhouden. Daarnaast werden verbeteringen in manie symptomen gemeten als secundaire uitkomstmaat.
De auteurs hebben met behulp van de CINeMA applicatie de heterogeniteit, inconsistentie en kwaliteit van de meta-analyse beoordeeld. De heterogeniteit was laag tot laag-gemiddeld voor de meeste uitkomsten. Slechts in 0-20% van de gevallen was bewijs voor inconsistentie. De geïncludeerde RCTs hadden een matige kans op vertekening en werden beoordeeld als studies van lage kwaliteit. Zie tabel 6.2 onder Evidence- en Risk of Biastabellen voor een overzicht van de resultaten met bijhorende GRADE’ing.
* De met een asterisk aangeduide middelen zijn niet beschikbaar dan wel niet geregistreerd in Nederland en worden niet meegenomen in deze wetenschappelijke onderbouwing.
Farmacologische behandeling – Hong (2022)
In een Bayesian netwerk meta-analyse (Hong et al., 2022) werd de effectiviteit van farmacotherapie voor acute manie onderzocht. In totaal werden 87 RCTs, met een totaal van 18724 patiënten met manie, geïncludeerd in de analyse. De helft van de patiënten was vrouw en de gemiddelde leeftijd was 35 jaar. Patiënten hadden een gemiddelde manie score van 29.7 bij baseline. Studies met patiënten met een dubbele diagnose (bipolaire stoornis in combinatie met een andere stoornis) werden geëxcludeerd.
Het grootste deel van de studies (64%) werd uitgevoerd in Noord-Amerika. Er werden 24 actieve farmaca behandelingen vergeleken met placebo: tamoxifen, risperidon, carbamazepine, haloperidol, ziprasidon1F1F*, cariprazine, olanzapine, quetiapine, aripiprazol, lithium, paliperidon, asenapine*, valproaat, verapamil, licarbazepine*, lamotrigine, topiramaat, oxcarbazepine, allopurinol*, melatonine, valnoctamide*, eslicarbazepine*, endoxifen*, en brexpiprazol*. De primaire uitkomstmaten waren veranderingen in manie scores, gemeten met behulp van verschillende meetinstrumenten (YMRS, MRS, MAS, en MSRS). De follow-up duur van de studies varieerde van vier tot 26 weken met een mediaan van acht weken.
De auteurs beoordeelden de kwaliteit van de studie aan de hand van GRADE en CINeMA. Beide instrumenten toonden aan dat de studies over het algemeen van hoge kwaliteit zijn. Zie tabel 6.3 onder Evidence- en Risk of Biastabellen voor een overzicht van de resultaten met bijhorende GRADE’ing. De met een asterisk aangeduide middelen zijn niet beschikbaar dan wel niet geregistreerd in Nederland en worden niet meegenomen in deze wetenschappelijke onderbouwing.
* De met een asterisk aangeduide middelen zijn niet beschikbaar dan wel niet geregistreerd in Nederland en worden daarom niet meegenomen in deze wetenschappelijke onderbouwing.
Tabel 6.1. Overzicht van effectiviteit van farmacologische middelen in vergelijking met placebo in het behandelen van manie. Middelen die niet beschikbaar of niet geregistreerd zijn in Nederland zijn niet opgenomen in de tabel. (bron: Hong 2022 en Kishi 2022)
|
Farmacotherapie effectiever dan placebo: |
|
|
|
|
Farmacotherapie niet effectiever dan placebo: |
|
|
|
Mood Stabilizers and Antipsychotics combination therapy – Tajika (2022)
In de goed uitgevoerde meta-analyse (Tajika et al., 2022) werd de tijd tot behandeleffect van combinatietherapie vergeleken met monotherapie met AP dan wel SS voor de behandeling van acute manie. Alle geïncludeerde patiënten hadden een diagnose van bipolaire manie. Zowel patiënten met een bipolaire stoornis als een schizo-affectieve stoornis werden geïncludeerd. Er was geen leeftijdsbeperking voor de inclusie van patiënten.
Zeventien RCTs vergeleken stemmingsstabilisatoren met combinatietherapie, en acht RCTs vergeleken antipsychotica met combinatietherapie. Drie stemmingsstabilisatoren werden geïncludeerd: lithium, valproaat, en carbamazepine. Antipsychotica omvatten: amisulpride, aripiprazol, asenapine*, chlorpromazine, clozapine, flupentixol, fluphenazine, haloperidol, levomepromazine, olanzapine, paliperidon, perazine, perphenazine, prochlorperazine quetiapine, risperidon, sulpiride, ziprasidon*, zotepine, en zuclopenthixol. De primaire uitkomstmaten waren response, manische symptomen, en drop-out (door bijwerkingen), gemeten na één, drie en zes weken. Voor respons werd de definitie gebruikt zoals beschreven per studie. Secundaire uitkomsten waren remissie en bijwerkingen. Remissie werd gedefinieerd als de afwezigheid van manische symptomen (volgens DSM-IV).
De kwaliteit van de resultaten is door de auteurs beoordeeld aan de hand van Cochrane Risk of bias tool. De geïncludeerde studies varieerden van een lage tot matige kans op vertekening.
Zie tabel 6.4 onder Evidence- en Risk of Biastabellen voor een overzicht van de resultaten met bijhorende GRADE’ing.
Review protocol
|
Topic |
Interventions/ epidemiology |
|
Review question(s) |
Wat is de effectiviteit en wat zijn de bijwerkingen van farmacologische interventies voor acute manie, hypomanie en gemengde episoden bij volwassenen met een bipolaire stoornis? |
|
Criteria for considering studies for the review |
|
|
Volwassen patiënten met een bipolaire stoornis met acute manie, hypomanie of gemengde episoden. |
|
Alle (goedgekeurde) orale medicatie: Antipsychotica Lithium Anticonvulsiva (valproinezuur; carbamazepine; oxcarbazepine; lamotrigine) Benzodiazepinen |
|
Placebo Actieve controle met andere farmacotherapie |
|
Symptomatisch herstel Functioneel herstel
|
|
Kwaliteit van leven Werkherstel Voorkomen nieuwe episoden Bijwerkingen |
|
Dagen/weken/Maanden
|
|
Systematic reviews/ meta-analyses (van RCTs) |
|
In klinische setting |
|
Search strategy |
Databases searched: CINAHL, Pubmed, PsycInfo Date limiters: database inspectie van 2010 tot 2024. Other limiters, e.g. design, language, age: volwassenen (18+) |
|
The review strategy |
De wetenschappelijke onderbouwing wordt zoveel mogelijk gebaseerd op bestaande systematic reviews met meta-analyse. Vanwege de breedte van de uitgangsvraag worden maximaal 5 SRs geïncludeerd die, in overleg met de werkgroep, zoveel mogelijk de PICO dekken (en/of nieuwe relevante inzichten opleveren, denk aan nieuwe interventies). Bij hoge uitzondering zal er nog een search gedaan worden naar (aanvullende) RCTs.
|
- Daggenvoorde, T., Geerling, B., & Goossens, P. J. (2015). A qualitative study of nursing care for hospitalized patients with acute mania. Archives of psychiatric nursing, 29(3), 186-191.
- Delgado A, Velosa J, Zhang J, Dursun SM, Kapczinski F, de Azevedo Cardoso T. Clozapine in bipolar disorder: A systematic review and meta-analysis. J Psychiatr Res. 2020 Jun;125:21-27. doi: 10.1016/j.jpsychires.2020.02.026. Epub 2020 Feb 27. PMID: 32182485.
- Goossens, P. J., de Velde Harsenhorst, R., van Lankeren, J. E., Testerink, A. E., & Daggenvoorde, T. H. (2022). Nursing care for patients with acute mania: Exploring experiential knowledge and developing a standard of good care—Results of the Delphi study. Journal of the American Psychiatric Nurses Association, 28(5), 366-381.
- Hong, Y., Huang, W., Cao, D., Xu, J., Wei, H., Zhang, J., & Wang, L. (2022). A cumulative Bayesian network meta-analysis on the comparative efficacy of pharmacotherapies for mania over the last 40 years. Psychopharmacology, 239(10), 3367–3375. https://doi.org/https://dx.doi.org/10.1007/s00213-022-06230-5
- Kishi, T., Ikuta, T., Matsuda, Y., Sakuma, K., Okuya, M., Nomura, I., Hatano, M., & Iwata, N. (2022). Pharmacological treatment for bipolar mania: a systematic review and network meta-analysis of double-blind randomized controlled trials. Molecular Psychiatry, 27(2), 1136–1144. https://doi.org/https://dx.doi.org/10.1038/s41380-021-01334-4
- Tajika, A., Hori, H., Iga, J., Koshikawa, Y., Ogata, H., Ogawa, Y., Watanabe, K., Kato, T., Matsuo, K., & Kato, M. (2022). Mood stabilizers and antipsychotics for acute mania: Systematic review and meta-analysis of augmentation therapy vs monotherapy from the perspective of time to the onset of treatment effects. International Journal of Neuropsychopharmacology, 25(10), 839–852. https://doi.org/https://dx.doi.org/10.1093/ijnp/pyac050
- Tohen, M., Frank, E., Bowden, C.L., Colom, F., Ghaemi, S.N., Yatham, L.N., e.a. (2009). The International Society for Bipolar disorders (ISBD) Task Force report on the nomenclature of course and outcome in bipolar disorders. Bipolar Disorders, 11, 453-473.
Tabel 6.2: Effectiviteit van verschillende soorten farmacotherapie in de behandeling van acute bipolaire manie. Weergegeven in aflopende mate van effectiviteit.
|
Studie |
Uitkomsten |
Relatief effect |
Aantal deelnemers |
Zekerheid van het bewijs |
|
Opmerkingen |
|
|
Behandelrespons |
|
|
|
|
|
||
|
Kishi |
Behandel respons |
SMD: 1.91 (1.41 tot 2.58) |
305 (6 RCT) |
⨁⨁◯◯ |
|
Carbamazepine heeft mogelijk een effectievere behandelrespons dan placebo. |
|
|
Kishi |
Behandel respons |
SMD: 1.69 (1.41 tot 2.02) |
7 (676) |
⨁⨁⨁◯ |
|
Risperidon heeft waarschijnlijk een effectievere behandelrespons dan placebo. |
|
|
Kishi |
Behandel respons |
SMD: 1.64 (1.43 tot 1.88) |
1023 (10 RCT) |
⨁⨁⨁◯ |
|
Haloperidol heeft waarschijnlijk een effectievere behandelrespons dan placebo. |
|
|
Kishi |
Behandel respons |
SMD: 1.59 (1.40 tot 1.80) |
1565 (14 RCT) |
⨁⨁⨁◯ |
|
Olanzapine heeft waarschijnlijk een effectievere behandelrespons dan placebo. |
|
|
Kishi |
Behandel respons |
SMD: 1.56 (1.26 tot 1.92) |
612 (3 RCT) |
⨁⨁⨁◯ |
|
Cariprazine heeft waarschijnlijk een effectievere behandelrespons dan placebo. |
|
|
Kishi |
Behandel respons |
SMD: 1.55 (1.32 tot 1.83) |
630 (5 RCT) |
⨁⨁⨁◯ |
|
Quetiapine heeft waarschijnlijk een effectievere behandelrespons dan placebo. |
|
|
Kishi |
Behandel respons |
SMD: 1.53 (1.33 tot 1.76) |
1205 (9 RCT) |
⨁⨁⨁◯ |
|
Aripiprazol heeft waarschijnlijk een effectievere behandelrespons dan placebo. |
|
|
Kishi |
Behandel respons |
SMD: 1.42 (1.19 tot 1.71) |
981 (14 RCT) |
⨁⨁⨁◯ |
|
Valproaat heeft waarschijnlijk een effectievere behandelrespons dan placebo. |
|
|
Kishi |
Behandel respons |
SMD: 1.45 (1.28 tot 1.65) |
965 (20 RCT) |
⨁⨁⨁◯ |
|
Lithium heeft waarschijnlijk een effectievere behandelrespons dan placebo. |
|
|
Kishi |
Behandel respons |
SMD: 1.39 (1.10 tot 1.76) |
542 (2 RCT) |
⨁⨁⨁◯ |
|
Paliperidon heeft waarschijnlijk een effectievere behandelrespons dan placebo. |
|
|
Kishi |
Behandel respons |
SMD: 1.35 (1.06 tot 1.72) |
458 (3 RCT) |
⨁⨁◯◯ |
|
Ziprasidon heeft mogelijk een effectievere behandelrespons dan placebo. |
|
|
Kishi |
Behandel respons |
SMD: 1.28 (1.05 tot 1.56) |
(620) (3 RCT) |
⨁⨁◯◯ |
|
Asenapine heeft mogelijk een effectievere behandelrespons dan placebo. |
|
|
Kishi |
Behandel respons |
SMD: 1.02 (0.84 tot 1.24) |
|
|
|
Er is geen bewijs dat lithium een effectievere behandelrespons heeft dan valproaat. |
|
|
Manische symptomen |
|||||||
|
Kishi |
Manische symptomen |
SMD: -0.61 (-0.75 tot -0.47)
|
1023 (10 RCT) |
⨁⨁⨁◯ |
|
Haloperidol is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo. |
|
|
Kishi |
Manische symptomen |
SMD: -0.60 (-0.77 tot -0.43)
|
7 (676) |
⨁⨁⨁◯ |
|
Risperidon is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo |
|
|
Kishi |
Manische symptomen |
SMD: -0.58 (-0.84 tot -0.32)
|
305 (6 RCT) |
⨁⨁⨁◯ |
|
Carbamazepine is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo |
|
|
Kishi |
Manische symptomen |
SMD: -0.49 (-0.61 tot -0.37) |
1565 (14 RCT) |
⨁⨁⨁◯ |
|
Olanzapine is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo |
|
|
Kishi |
Manische symptomen |
SMD: -0.50 (-0.71 tot -0.29) |
612 (3 RCT) |
⨁⨁⨁◯ |
|
Cariprazine is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo |
|
|
Kishi |
Manische symptomen |
SMD: -0.36 (-0.50tot -0.22) |
1205 (9 RCT) |
⨁⨁⨁◯ |
|
Aripiprazol is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo |
|
|
Kishi |
Manische symptomen |
SMD: -0.38 (-0.54 tot -0.21) |
630 (5 RCT) |
⨁⨁⨁◯ |
|
Quetiapine is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo |
|
|
Kishi |
Manische symptomen |
SMD: -0.38 (-0.62 tot -0.13) |
542 (2 RCT) |
⨁⨁⨁◯ |
|
Paliperidon is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo |
|
|
Kishi |
Manische symptomen |
SMD: -0.35 (-0.48 tot -0.22) |
965 (20 RCT) |
⨁⨁⨁◯ |
|
Lithium is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo |
|
|
Kishi |
Manische symptomen |
SMD: -0.22 (-0.37 tot -0.06) |
981 (14 RCT) |
⨁⨁⨁◯ |
|
Valproaat is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo |
|
|
Tolerantie |
|||||||
|
Kishi |
Uitval wegens bijwerkingen |
RR: 1.90 (1.12 tot 3.22) |
14629 (52 RCT) |
⨁⨁⨁◯ |
|
Asenapine resulteert waarschijnlijk in meer uitval wegens bijwerkingen dan placebo. |
|
|
Kishi |
Uitval wegens bijwerkingen |
RR: 1.79 (1.09 tot 2.94) |
14629 (52 RCT) |
⨁⨁⨁◯ |
|
lithium resulteert waarschijnlijk in meer uitval wegens bijwerkingen dan placebo. |
|
|
Kishi |
Uitval wegens bijwerkingen |
RR: 1.87 (1.26 tot 2.78) |
14629 (52 RCT) |
⨁⨁⨁◯ |
|
haloperidol resulteert waarschijnlijk in meer uitval wegens bijwerkingen dan placebo. |
|
|
Kishi |
Uitval wegens bijwerkingen |
RR: 0.64 (0.47 tot 0.89) |
11968 (42 RCT) |
⨁⨁⨁◯ |
|
olanzapine resulteert waarschijnlijk in minder uitval wegens bijwerkingen dan placebo. |
|
| a. Geïncludeerde studies hebben gematigde kans op vertekening. b. Onnauwkeurigheid: < 300 patiënten. c. Het betrouwbaarheidsinterval doorkruist het punt van geen klinisch relevant verschil. | |||||||
Tabel 6.3: Effectiviteit van verschillende soorten farmacotherapie in de behandeling van acute bipolaire manie. Weergegeven in aflopende mate van effectiviteit.
|
Studie |
Uitkomsten |
Relatief effect |
Aantal deelnemers |
Zekerheid van het bewijs |
|
Opmerkingen |
|
|
Hong |
Manische symptomen |
SMD: -6.6 (-8.4 tot -3.7)
|
1032 (4 RCT) |
⨁⨁⨁◯ |
|
Risperidon is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo. |
|
|
Hong |
Manische symptomen |
SMD: -5.3 (-6.9 tot -3.8) |
(10 RCT) |
⨁⨁⨁◯ |
|
Carbamazepine is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo. |
|
|
Hong |
Manische symptomen |
SMD: -5.2 (-7.2 tot -3.1) |
1122 (4 RCT) |
⨁⨁⨁◯ |
|
Cariprazine is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo. |
|
|
Hong |
Manische symptomen |
SMD: -5.0 (-6.3 tot -3.6) |
(13 RCT) |
⨁⨁⨁◯ |
|
Olanzapine is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo. |
|
|
Hong |
Manische symptomen |
SMD: -4.3 (-5.8 tot -2.8) |
9 RCT |
⨁⨁⨁◯ |
|
Quetiapine is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo. |
|
|
Hong |
Manische symptomen |
SMD: -4.3 (-5.6 tot -3.0) |
11 RCT |
⨁⨁⨁◯ |
|
Aripripazole is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo. |
|
|
Hong |
Manische symptomen |
SMD: -4.1 (-5.3 tot -2.8) |
21 RCT |
⨁⨁⨁◯ |
|
Lithium is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo. |
|
|
Hong |
Manische symptomen |
SMD: -4.1 (-6.6 tot -1.5) |
955 (2 RCT) |
⨁⨁⨁◯ |
|
paliperidon is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo. |
|
|
Hong |
Manische symptomen |
SMD: -2.8 (-4.3 tot -1.4) |
16 RCT |
⨁⨁⨁◯ |
|
Valproaat is waarschijnlijk effectiever in het verminderen van manische symptomen dan placebo. |
|
| a. Onnauwkeurigheid: <300 patiënten. b. Geïncludeerde studies hebben gematigde kans op vertekening. c. Verdenkingen van heterogeniteit. D. Lage kans op reporting bias. | |||||||
Tabel 6.4: Behandeleffect voor combinatietherapie versus stemmingsstabilisatoren (MS) en antipsychotica (AP) monotherapie, na één, drie en zes weken.
|
|
Studie |
Uitkomsten |
Relatief effect |
Aantal deelnemers |
Zekerheid van het bewijs |
|
Opmerkingen |
|
|
|
Respons |
|
|
|
|
|
|
|
|
|
Tajika |
Respons |
OR: 1.59 (1.28 tot 1.99)
|
2341 (10 RCT) |
⨁⨁◯◯ |
|
MS+AP combinatie therapie heeft mogelijk een effectievere response dan MS monotherapie na 6 weken |
|
|
|
Tajika |
Respons |
OR: 1.45 (1.17 tot 1.80) |
2921 (13 RCT) |
⨁⨁◯◯ |
|
MS+AP combinatie therapie heeft mogelijk een effectievere response dan MS monotherapie na 3 weken |
|
|
|
Tajika |
Respons |
OR: 1.73 (1.25 tot 2.40) |
609 (4 RCT) |
⨁⨁◯◯ |
|
MS+AP combinatie therapie heeft mogelijk een effectievere response dan AP monotherapie na 3 weken |
|
|
|
Tajika |
Respons |
OR: 1.74 (1.11 tot 2.73) |
395 (2 RCT) |
|
MS+AP combinatie therapie heeft mogelijk een effectievere response dan AP monotherapie na 6 weken |
||
|
|
Drop-out wegens bijwerkingen |
|||||||
|
|
Tajika |
Drop-out |
OR: 1.56 (0.90 tot 2.71) |
1254 (6 RCT) |
⨁⨁◯◯ |
|
MS+AP combinatie therapie is mogelijk niet effectiever in het tegengaan van drop-out dan MS monotherapie na 3 weken |
|
|
|
Tajika |
Drop-out |
OR: 1.61 (0.97 tot 2.67) |
2391 (11 RCT) |
⨁⨁◯◯ |
|
MS+AP combinatie therapie is mogelijk niet effectiever in het tegengaan van drop-out dan MS monotherapie na 6 weken |
|
|
|
Tajika |
Drop-out |
OR: 2.19 (0.48 tot 10.09) |
232 (3 RCT) |
⨁◯◯◯ |
|
MS+AP combinatie therapie is mogelijk niet effectiever in het tegengaan van drop-out dan AP monotherapie na 3 weken, maar het bewijs is onzeker. |
|
|
|
Tajika |
Drop-out |
OR: 0.47 (0.17 tot 1.27) |
356 (1 RCT) |
⨁⨁◯◯ |
|
MS+AP combinatie therapie is mogelijk niet effectiever in het tegengaan van drop-out dan AP monotherapie na 6 weken |
|
|
|
Manische symptomen |
|||||||
|
|
Tajika |
Manische symptomen |
SMD: -0.25 (-0.38 tot -0.12) |
2506 (12 RCT) |
⨁⨁◯◯ |
|
MS+AP combinatie therapie is mogelijk effectiever in het verminderen van manische symptomen dan MS monotherapie na 1 week |
|
|
|
Tajika |
Manische symptomen |
SMD: -0.26 (-0.38 tot -0.15) |
2985 (15 RCT) |
⨁⨁◯◯ |
|
MS+AP combinatie therapie is mogelijk effectiever in het verminderen van manische symptomen dan MS monotherapie na 3 weken |
|
|
|
Tajika |
Manische symptomen |
SMD: -0.30 (-0.41 tot -0.19) |
2324 (11 RCT) |
⨁⨁◯◯ |
|
MS+AP combinatie therapie is mogelijk effectiever in het verminderen van manische symptomen dan MS monotherapie na 6 weken |
|
|
|
Tajika |
Manische symptomen |
SMD: -0.23 (-0.39 tot -0.07) |
589 (4 RCT) |
⨁⨁◯◯ |
|
MS+AP combinatie therapie is mogelijk effectiever in het verminderen van manische symptomen dan AP monotherapie na 1 week |
|
|
|
Tajika |
Manische symptomen |
SMD: -0.40 (-0.64 tot -0.16) |
(574) (4 RCT) |
⨁⨁◯◯ |
|
MS+AP combinatie therapie is mogelijk effectiever in het verminderen van manische symptomen dan AP monotherapie na 3 weken |
|
|
|
Tajika |
Manische symptomen |
SMD: -0.20 (-0.86 tot 0.46) |
36 (1 RCT) |
⨁◯◯◯ |
|
Het effect van MS+AP combinatie therapie in het verminderen van manische symptomen in vergelijking met AP monotherapie na 6 weken is zeer onzeker. |
|
|
Secundaire uitkomsten |
||||||||
|
|
Tajika |
Remissie |
OR: 1.43 (1.11 tot 1.83) |
N.R. |
⨁⨁◯◯ |
|
MS+AP combinatie therapie is mogelijk effectiever in het vergroten van remissie dan MS monotherapie na 3 weken |
|
|
|
Tajika |
Remissie |
OR: 1.48 (1.17 tot 1.86) |
N.R. |
⨁⨁◯◯ |
|
MS+AP combinatie therapie is mogelijk effectiever in het vergroten van remissie dan MS monotherapie na 6 weken |
|
|
|
Tajika |
Remissie |
OR: 1.71 (1.21 tot 2.42) |
(4 RCT) |
⨁⨁◯◯ |
|
MS+AP combinatie therapie is mogelijk effectiever in het vergroten van remissie dan AP monotherapie na 3 weken |
|
|
|
Tajika |
Remissie |
OR: 1.73 (1.12 tot 2.67) |
(2 RCT) |
⨁⨁◯◯ |
|
MS+AP combinatie therapie is mogelijk effectiever in het vergroten van remissie dan AP monotherapie na 6 weken |
|
|
|
Tajika |
bijwerkingen |
OR: 2.17 (1.54 tot 3.07) |
(4 RCT) |
⨁⨁◯◯ |
|
MS+AP combinatie therapie leidt mogelijk tot meer bijwerkingen dan MS monotherapie na 3 weken |
|
|
|
Tajika |
bijwerkingen |
OR: 1.49 (1.09 tot 2.03) |
(6 RCT) |
⨁⨁◯◯ |
|
MS+AP combinatie therapie leidt mogelijk tot meer bijwerkingen dan MS monotherapie na 6 weken |
|
|
|
Tajika |
bijwerkingen |
OR: 1.84 (1.23 tot 2.75) |
(2 RCT) |
⨁⨁◯◯ |
|
MS+AP combinatie therapie leidt mogelijk tot meer bijwerkingen dan AP monotherapie na 6 weken |
|
| a. Onnauwkeurigheid: betrouwbaarheidsinterval laat geen duidelijk klinisch relevant resultaat zien. b. Inconsistentie: Substantiële heterogeniteit (I2 > 50%). c. Onnauwkeurigheid: <300 patiënten. d. Studiebeperkingen: onduidelijke/ontbrekende beschrijving van randomisatie proces. N.R.=Niet gerapporteerd. | ||||||||
Beoordelingsdatum en geldigheid
Publicatiedatum : 24-03-2026
Beoordeeld op geldigheid : 24-03-2026
Algemene gegevens
Deze richtlijn is ontwikkeld door de richtlijnwerkgroep Bipolaire stoornissen, op initiatief van de Nederlandse Vereniging voor Psychiatrie (NVvP). Het is een multidisciplinaire richtlijn die aanwijzingen geeft voor screening, diagnostiek en behandeling van bipolaire stoornissen. De ontwikkeling is gefinancierd vanuit het gealloceerde budget van de Nederlandse Vereniging voor Psychiatrie (NVvP) van de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). Methodologisch en organisatorisch is de richtlijnontwikkeling ondersteund door het Trimbos-instituut.
Doel en doelgroep
Doel
Deze richtlijn is ontwikkeld als hulpmiddel. De richtlijn geeft aanbevelingen en handelingsinstructies voor de screening, diagnostiek en behandeling van zowel kinderen als adolescenten, volwassenen en ouderen met een bipolaire stoornis. De aanbevelingen zijn bedoeld ter ondersteuning van de praktijkvoering van alle professionals die betrokken zijn bij de zorgverlening voor deze patiënten. De richtlijn geeft een overzicht van goed (‘optimaal’) handelen in lijn met de resultaten van wetenschappelijk onderzoek en overige overwegingen, als waarborg voor kwalitatief hoogwaardige zorg. De richtlijn kan tevens richting geven aan de onderzoeksagenda voor wetenschappelijk onderzoek naar bipolaire stoornissen.
De multidisciplinaire ontwikkelprocedure is bedoeld om de multidisciplinaire samenwerking in de dagelijkse praktijk te bevorderen. Daarnaast kan deze richtlijn vertaald worden naar monodisciplinaire richtlijnen van afzonderlijke beroepsgroepen. De richtlijn is dan te beschouwen als een moederrichtlijn voor de richtlijnen van die beroepsgroepen, waarin men aanknopingspunten kan vinden voor lokale zorgprogramma’s en protocollen. Het opstellen van lokale zorgprogramma’s en protocollen op basis van deze richtlijn wordt door de richtlijnwerkgroep aangemoedigd, aangezien de implementatie van de in deze richtlijn beschreven behandeling optimale zorg kan bevorderen.
Indien de aanbevelingen uit deze richtlijn in de concrete situatie niet aansluiten bij de wensen of behoeften van de patiënt met een bipolaire stoornis, kan beredeneerd worden afgeweken van de richtlijn, tenzij de wensen of behoeften van de patiënt naar de mening van de behandelaar hem of haar kunnen schaden, dan wel geen nut hebben. In alle gevallen komt een behandeling tot stand op basis van gezamenlijke besluitvorming door de optimaal geïnformeerde patiënt, naaste en behandelaar(s).
Afbakening
Deze richtlijn betreft de diagnostiek en behandeling van kinderen en adolescenten (12 tot 23 jaar), volwassenen en ouderen (60 jaar of ouder) bij wie er sprake is van (of er een vermoeden is van) een bipolaire stemmingsstoornis. In de richtlijn is gezocht naar oorspronkelijke onderzoeken zonder begindatum, en tot en met november 2024. In sommige gevallen zijn gepubliceerde aanvullende reviews van recenter datum geraadpleegd. Nog niet gepubliceerde onderzoeken zijn niet meegenomen.
Doelgroep
De ontwikkeling van de multidisciplinaire richtlijnen voor de ggz geschiedt primair vanuit een inhoudelijke invalshoek ten behoeve van de verbetering van de kwaliteit van de zorgverlening. De gebruikers van de richtlijn zijn doorgaans allen professioneel betrokken bij de zorg voor patiënten met een bipolaire stoornis of voor patiënten bij wie men die aandoening vermoedt.
In de werkgroep waren ook patiënten- en familieverenigingen vertegenwoordigd, waarmee het perspectief van de patiënten met een bipolaire stoornis en hun naasten in de richtlijn een plaats heeft gekregen. Daardoor kunnen ook niet-professionele zorgverleners en/of belangenverenigingen tot de gebruikers van de richtlijn kan behoren.
Samenstelling werkgroep
De Multidisciplinaire richtlijn bipolaire stoornissen is ontwikkeld door de richtlijnwerkgroep Bipolaire stoornissen bij volwassenen, in opdracht van de Nederlandse Vereniging voor Psychiatrie (NVvP). De richtlijnwerkgroep, onder voorzitterschap van prof. dr. Ralph Kupka, emeritus hoogleraar bipolaire stoornissen, bestond uit psychiaters, psychologen, verpleegkundig specialisten, belangenbehartigers en ervaringsdeskundigen, allen door de (beroeps)verenigingen uitgenodigd en op persoonlijke titel aan het project verbonden.
Voorafgaande aan het ontwikkeltraject zijn kennismakingsgesprekken gevoerd met kandidaat-leden voor de werkgroep. Uit deze groep belangstellenden zijn de huidige werkgroepleden geselecteerd. Naast de richtlijnwerkgroep is een aantal experts benaderd om adviseur te worden. Deze adviseurs konden op individuele basis worden gevraagd om op verzoek van een werkgroeplid mee te denken over een specifieke uitgangsvraag. De richtlijnwerkgroep is methodologisch en organisatorisch ondersteund door het technische team van het Trimbos-instituut. Dit technische team bestond uit een projectleider, twee literatuur reviewers, een informatiespecialist, en een project assistent. De tabellen Leden werkgroep, Leden adviesgroep en Methodologische ondersteuning geven een overzicht van de samenstelling van de richtlijnwerkgroep, de klankbordgroep en het ondersteunende technische team.
Leden Werkgroep
|
|
Naam |
Organisatie |
Beroepsvereniging |
|
1. |
Prof. dr. Ralph Kupka (voorzitter) |
Amsterdam UMC; Altrecht; GGZ inGeest; Dimence |
Psychiater, NVvP |
|
2. |
dr. Manja Koenders (vicevoorzitter) |
Leiden University Faculty of Social Sciences |
Psycholoog, NIP |
|
3. |
Prof. dr. Manon Hillegers |
afd. K&J Psychiatrie Erasmus MC |
Psychiater, NVvP |
|
3. |
dr. Annemieke Dols |
UMC Utrecht |
Psychiater, NVvP |
|
4. |
dr. Imke Hanssen |
Radboud Universiteit Nijmegen |
Psycholoog, NIP |
|
5. |
dr. Bart Geerling |
Dimence |
verpleegkundig specialist, V&VN |
|
6. |
drs. Henk Mathijssen |
Plusminus |
Plusminus |
|
7. |
Elisabeth Bakker-Timmerman |
Plusminus, KenBiS |
Plusminus |
Leden adviesgroep
|
|
Naam |
Organisatie |
Beroep |
|
1. |
prof. dr. Marc Vervloet* |
Radboud UMC |
Hoogleraar nefrologie |
|
2. |
Dr. Miranda Kurver |
NHG |
Huisarts en senior wetenschappelijk medewerker richtlijnontwikkeling |
|
3. |
dr. Ingeborg Wilting |
UMC Utrecht |
klinisch farmacoloog |
|
4. |
dr. Benno Haarman |
UMC Groningen |
Psychiater |
|
5. |
dr. Rob Havermans |
Mondriaan, PsyQ |
Psychiater |
|
6. |
dr. Debbie Zittema |
GGZ Ingeest |
Psychiater en klinisch farmacoloog |
|
7. |
Bianca van Nieuwendijk |
GGZ Ingeest |
Verpleegkundig specialist |
|
8. |
Mischa van Bendegem |
Mediant |
Verpleegkundig specialist |
|
9. |
Dr. Bram Dierckx |
Erasmus MC |
Psychiater |
|
10. |
Dr. Esther Mesman |
Erasmus MC |
GZ-psycholoog |
|
11. |
Dr. Max de Leeuw |
LUMC |
Psychiater |
|
12. |
Dolf Snel |
|
Naastenperspectief |
|
13. |
Suzanne Demacker |
Altrecht |
GZ-psycholoog |
|
14. |
Dr. Melis Orhan |
Universiteit Leiden |
GZ-psycholoog |
|
15. |
Theo Hoedemaker |
Plusminus |
Naastenperspectief |
|
16. |
JRP van der Veen |
Plusminus |
ervaringsdeskundige |
|
17. |
Bernadette Wigchert |
Plusminus |
ervaringsdeskundige |
|
18. |
Mirthe Knot-Ploeg |
Plusminus |
ervaringsdeskundige |
*Marc Vervloet is namens de NIV gemandateerd om advies te verlenen op module 9 Somatische Aspecten.
Methodologische ondersteuning
|
Naam |
Ondersteuning |
|
Eva Becking |
Projectleider, Trimbos-instituut |
|
Anne van Jaarsveld |
Reviewer, Trimbos-instituut |
|
Matthijs Oud |
Reviewer, Trimbos-instituut |
|
Rikie Deurenberg |
Informatiespecialist, namens Trimbos-instituut |
|
Joyce Huls |
Projectassistent, Trimbos-instituut |
In totaal kwam de Werkgroep Bipolaire Stoornissen voorafgaand aan de commentaarfase acht keer bijeen in de periode van januari 2024 tot maart 2025. In deze periode werden de stappen van de methodiek voor evidence-based richtlijnontwikkeling (EBRO) doorlopen. De informatiespecialist verrichtte in overleg met de werkgroepleden op systematische wijze literatuuronderzoek en de reviewers maakten per uitgangsvraag een selectie in de gevonden onderzoeken (zie voor informatie over de zoekstrategie en de selectiecriteria: het reviewprotocol). De reviewers beoordeelden de kwaliteit en inhoud van de aldus verkregen literatuur en verwerkten deze per uitgangsvraag in evidentie-tabellen, GRADE-profielen, beschrijvingen van de wetenschappelijke onderbouwing en wetenschappelijke (gewogen) conclusies (per module beschreven onder “Onderbouwing”). Leden van de Werkgroep gingen op basis van de gevonden literatuur met elkaar in discussie over praktijkoverwegingen (per module beschreven onder “Overwegingen”) en aanbevelingen (per module beschreven onder “Aanbevelingen”). De werkgroepleden schreven samen met het technisch team van het Trimbos-instituut de concepttekst, welke ter becommentariëring openbaar is gemaakt. De ontvangen commentaren worden verwerkt in een commentaartabel, die tijdens een werkgroep bijeenkomst wordt besproken. Na het doorvoeren van op deze bijeenkomst voorgestelde wijzigingen wordt de definitieve richtlijn aan de opdrachtgever aangeboden.
Belangenverklaringen
|
Naam werkgroeplid |
Functie |
Nevenwerkzaamheden |
Belangen |
|
Ralph Kupka |
Hoogleraar Bipolaire stoornissen Psychiater |
Bestuurslid Akwa-GGZ Voorzitter bestuur KenBis Bestuurslid ISBD |
nvt |
|
Manja Koenders |
GZ-psycholoog i.o. specialist Universitair docent |
Docent Rino-groep Zzp supervisor |
nvt |
|
Manon Hillegers |
Hoogleraar en afdelingshoofd kinder/jeugd psychiatrie |
Bestuurslid BOPP-west ESCAP bestuurslid ISBD taskforce member |
nvt |
|
Annemieke Dols |
Psychiater |
Onderwijs en nascholing faciliteren |
nvt |
|
Bart Geerling |
Verpleegkundig specialist/hoofd Onderzoeker |
Voorzitter herziening zorgstandaard |
nvt |
|
Imke Hanssen |
Psycholoog i.o. tot GZ-psycholoog Post-doc onderzoeker |
Lid wetenschapscommissie Vereniging voor Mindfulness-Based Trainers Nederland Bestuurslid van de sectie Mindfulness-Based Cognitieve GedragsTherapie (MB-CGT) van de Vereniging voor Cognitieve Gedragstherapieën (VGCt) |
nvt |
|
Henk Matthijsen |
Voorzitter Plusminus |
Lid RvT GGZ Transparant |
nvt |
|
Elisabeth Bakker Timmerman |
Lid Plusminus Gepensioneerd ergotherapeut |
Bestuurslid KenBis Lid familieraad Parnassia
|
nvt |
Methode ontwikkeling
Evidence based
Werkwijze
EBRO-methode voor wetenschappelijke onderbouwing
Deze multidisciplinaire richtlijn is herzien volgens de methodiek van evidence-based richtlijnontwikkeling (EBRO). Hierbij werd de GRADE-methodiek toegepast. Er zijn ook hoofdstukken overgenomen vanuit de vorige versie van de MDR Bipolaire stoornis (2015). Hierin zijn conclusies gebaseerd op de ‘levels of evidence’ (voor informatie over deze werkwijze, raadpleeg de verantwoording van de betreffende hoofdstukken).
GRADE-methodiek
Sinds de introductie van de GRADE-methodiek in 2004 werd dit wereldwijd al snel de methode van voorkeur om wetenschappelijk bewijs te graderen ten behoeve van richtlijnontwikkeling (Guyatt et al., 2008), inclusief deze richtlijn. De GRADE-methodiek gaat er van uit dat de zekerheid van het wetenschappelijk bewijs uit randomized controlled trials (RCT’s) in beginsel hoog is vanwege de, mits goed uitgevoerd, kleine kans op vertekening (bias). In geval van observationele (niet gerandomiseerde) studies is de uitgangspositie van de zekerheid van bewijs laag. De zekerheid van het bewijs per uitkomstmaat wordt, behalve door de methodologische kwaliteit van de individuele onderzoeken, ook bepaald door andere factoren, zoals de mate van consistentie van de gevonden resultaten uit de verschillende onderzoeken en de precisie van de gevonden uitkomst (zie tabel 1.1). Bij observationeel onderzoek kan het bewijs in bepaalde gevallen omhoog worden gegradeerd.
Tabel 1.1 GRADE: Factoren voor downgraden en upgraden 1
⇓ |
We downgraden de zekerheid van bewijs van studies met een hoge uitgangspositie (RCT’s), bij: |
⇑ |
We upgraden de zekerheid van bewijs van observationele studies bij: |
|
|
||
|
|
||
|
|
||
|
|
||
|
|
||
1 De zekerheid van het bewijs (zeer laag, laag, matig en hoog) verwijst naar de mate van vertrouwen dat men heeft in de schatting van het effect van een behandelinBij de beoordeling van het wetenschappelijke bewijs ten aanzien van bovenstaande factoren werd uitgegaan van ‘Grade guidelines’, zoals ook te raadplegen in het ‘Grade handbook’ (Guyatt et al., 2013; Handbook for grading the quality of evidence and the strength of recommendations using the GRADE approach).
Legenda GRADE
Na vaststelling van het niveau van bewijs wordt dit in de bijbehorende conclusies als volgt verwoord:
|
Zekerheid |
Symbolen |
|
Signaalwoorden |
|
Hoog |
⊕⊕⊕⊕ |
“Het is aangetoond dat…” |
geeft, heeft (een effect), resulteert in |
|
Redelijk |
⊕⊕⊕◯ |
“Het is aannemelijk...” |
waarschijnlijk |
|
Laag |
⊕⊕◯◯ |
“Er zijn aanwijzingen…” |
zou kunnen, lijkt, suggereert |
|
Zeer laag |
⊕◯◯◯ |
“Het is onzeker, maar er zijn aanwijzingen dat…” |
onzeker |
Van bewijs naar aanbevelingen: Overwegingen
Naast het wetenschappelijk bewijs bepalen enkele andere factoren mede of een instrument of behandeling wordt aanbevolen. In de teksten van de vorige richtlijn-versies werd dit onder “Overige Overwegingen” beschreven.
Mee te wegen factoren om te bepalen of een instrument of behandeling wordt aanbevolen:
|
1. Kwaliteit van bewijs Hoe hoger de algehele kwaliteit van het bewijs, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. |
|
2. Balans tussen gewenste en ongewenste effecten Hoe groter het verschil is tussen de gewenste en ongewenste effecten, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. Hoe kleiner dit verschil of hoe meer onzekerheid over de grootte van het verschil, des te waarschijnlijker wordt het formuleren van een conditionele aanbeveling. Toelichting:
|
|
3. Patiëntenperspectief Hoe groter de uniformiteit in waarden en voorkeuren van patiënten bij het afwegen van de voor- en nadelen van een interventie, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. |
|
4. Professioneel perspectief Hoe groter de uniformiteit in waarden en voorkeuren van professionals ten aanzien van de toepasbaarheid van een interventie, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. Toelichting:
|
|
5. Middelenbeslag Hoe minder middelen er worden gebruikt (m.a.w. hoe lager de kosten van een interventie zijn vergeleken met de beschouwde alternatieven en andere kosten gerelateerd aan de interventie), des te waarschijnlijker wordt het formuleren van een sterke aanbeveling. Hoe meer onzekerheid over het middelenbeslag, des te waarschijnlijker wordt een conditionele aanbeveling. |
|
6. Organisatie van zorg Hoe meer onzekerheid of de geëvalueerde interventie daadwerkelijk op landelijke schaal toepasbaar is, des te waarschijnlijker wordt het formuleren van een conditionele aanbeveling. Toelichting:
|
Formulering van aanbevelingen
Afhankelijk van deze factoren kun je een instrument of behandeling wel of niet aanbevelen. We maken daarbij onderscheid tussen zwakke en sterke aanbevelingen. In het geval van een sterke aanbeveling zou je behandeling X voor alle patiënten met Y willen aanbevelen. Bij een zwakke aanbeveling is dit bijvoorbeeld afhankelijk van de voorkeuren van de patiënt in kwestie. Het is belangrijk in deze sectie expliciet te vermelden op grond waarvan een behandeling wel of niet wordt aanbevolen en ook waarom die aanbeveling zwak of sterk zou moeten zijn.
Voor de formulering van ‘sterke’ (onvoorwaardelijke) en ‘zwakke’ (voorwaardelijke) aanbevelingen is de volgende indeling aangehouden (zie tabel 1.2):
Tabel 1.2 GRADE Voorkeursformulering sterke / zwakke aanbevelingen
|
Gradering aanbeveling |
Betekenis |
Voorkeursformulering* |
|
STERK VOOR |
De voordelen zijn groter dan de nadelen voor bijna alle patiënten. Alle of nagenoeg alle geïnformeerde patiënten zullen waarschijnlijk deze optie kiezen. |
We bevelen [interventie] aan. |
|
ZWAK VOOR |
De voordelen zijn groter dan de nadelen voor een meerderheid van de patiënten, maar niet voor iedereen. De meerderheid van geïnformeerde patiënten zal waarschijnlijk deze optie kiezen. |
Overweeg [interventie], bespreek de voor- en nadelen). |
|
ZWAK TEGEN |
De nadelen zijn groter dan de voordelen voor een meerderheid van de patiënten, maar niet voor iedereen. De meerderheid van geïnformeerde patiënten zal waarschijnlijk deze optie kiezen. |
Wees terughoudend met [interventie], bespreek de voor- en nadelen). |
|
STERK TEGEN |
De nadelen zijn groter dan de voordelen voor bijna alle patiënten. Alle of nagenoeg alle geïnformeerde patiënten zullen waarschijnlijk deze optie kiezen. |
We bevelen [interventie] niet aan. |
* Het gaat hier om voorkeursaanbevelingen, deze kunnen in een enkel geval afwijken. Voor bepaalde hoofdstukken is GRADE niet toegepast (bijv. Organisatie van zorg) daar zijn uit praktisch oogpunt ook de aanbevelingen niet volgens GRADE.
Zoekstrategie
Om de uitgangsvragen te kunnen beantwoorden, is door de informatiespecialist en reviewers van het Trimbos-instituut, in overleg met de werkgroepleden, op systematische wijze literatuuronderzoek verricht en is een selectie gemaakt binnen de gevonden onderzoeken volgens vooraf vastgestelde selectiecriteria. Er is gezocht naar meta-analyses, systematische reviews en oorspronkelijke onderzoeken. In de literatuursearches is gezocht naar literatuur in de Engelse en Nederlandse taal. Voor het zoeken naar publicaties is gebruikgemaakt van Medline en Psychological Information Database (Psycinfo).
Selectiestrategie
Bij de selectie van artikelen zijn de volgende criteria gehanteerd:
- Geeft het onderwerp van het gevonden onderzoek voldoende antwoord op de uitgangsvraag: worden de binnen GRADE vastgestelde kritische en belangrijke uitkomstmaten in het onderzoek geëvalueerd? (zie voor meer informatie over GRADE verderop in deze paragraaf);
- Sluit de doelgroep van het gevonden onderzoek voldoende aan bij de doelgroep van de richtlijn;
- Is er sprake van een meta-analyse, systematic-review, randomised controlled trial (RCT), cohort onderzoek, cross-sectioneel onderzoek, patiëntcontrole onderzoek of wetenschappelijke verantwoord kwalitatief onderzoek? Bij een longitudinaal onderzoek: Is er sprake van een voldoende lange follow-up periode?;
- Zie voor meer informatie over de zoekstrategie de bijlagen per hoofdstuk en voor meer informatie over de selectiecriteria per uitgangsvraag de reviewprotocollen in de bijlagen per hoofdstuk.
Leeswijzer
Met kinderen en adolescenten bedoelen we kinderen van 8 tot 12 jaar en adolescenten van 12 tot 18 jaar. Met jongvolwassenen bedoelen we volwassenen van 18 tot 25 jaar. Met volwassenen bedoelen we mensen van 25 tot 60 jaar. Met ouderen bedoelen we oudere volwassenen van 60 jaar en ouder.
Zoekverantwoording
Op 15 mei 2024 is er een search uitgevoerd in PsychInfo en Medline databases. De specifieke zoektermen zijn in het review protocol opgenomen. De search leverde 229 referenties op. Na beoordeling op titel en abstract bleven er 16 referenties over voor selectie op basis van de volledige teksten: Cipriani2011; Kishi2022; Yildiz2011; Hong2022; Yildiz2015; Muralidharan2013; Bartoli2021; Tajika2022; Glue2015; Ogawa2014; McKnight2019; Pinto2020; Vita2013; Palacios2019; Fountoulakis2022; Haenen2024. De voornaamste exclusieredenen waren onjuiste populatie of onjuiste interventie. Na een uitgebreide tweede selectie bleven drie studies over die zijn opgenomen in dit hoofdstuk: Kishi2022; Tajika2022; Hong2022. N.a.v. suggestie tijdens commentaarfase is Delgado2020 geraadpleegd voor een aanbeveling over clozapine gebruik.