Cardiologische bijwerkingen van biologicals
Uitgangsvraag
Hoe kunnen cardiovasculaire bijwerkingen van biologicals, zoals hartfalen en dyslipidemie, worden voorkomen en, indien deze optreden, worden behandeld?
Aanbeveling
Bij IMID patiënten met hartfalen NYHA klasse III-IV is terughoudendheid bij het geven van TNFα-blokkers geïndiceerd.
Andere biologicals kunnen aan IMID patiënten worden gegeven zonder dat daarbij rekening hoeft te worden gehouden met een eventueel verhoogd cardiovasculair risico. Er zijn geen specifieke voorzorgsmaatregelen geïndiceerd.
Bij gebruik van biologicals hoeven geen specifieke (extra) maatregelen te worden genomen betreffende het lipidenspectrum; een uitzondering vormt mogelijk Tocilizumab.
Overwegingen
De literatuur over (nieuw ontstaan of vergeren van bestaand) hartfalen bij IMID is beperkt en is met name gebaseerd op RA patiënten. Overtuigende bewijzen dat gebruik van TNFα-blokkers hartfalen induceert of verergert zijn niet voorhanden. Toch heeft de werkgroep gemeend een standpunt in te moeten nemen dat in overeenstemming is met 1B-teksten en overige richtlijnen. Bij patiënten met hartfalen met een NYHA klasse III-IV (tabel) is terughoudendheid geïndiceerd, waarbij dus voor het starten met een TNFα-blokker op basis van anamnese een oordeel over de cardiale situatie van de patiënt moet worden verkregen.
TABEL 1: NYHA classificatie hartfalen
- Klasse I: Patiënten zonder beperking van fysieke activiteit. Normale activiteit veroorzaakt geen klachten.
- Klasse II: Patiënten met een geringe beperking van fysieke activiteit. Geen klachten in rust, maar wel bij matige fysieke activiteit.
- Klasse III: Patiënten met een duidelijke beperking van de fysieke activiteit. Geringe inspanning geeft al klachten.
- Klasse IV: Patiënten met ernstige beperkingen in de fysieke activiteit. Klachten zijn ook in rust aanwezig.
Voor andere biologicals zijn er geen aanwijzingen dat deze de hartfunctie beïnvloeden. Ook hiervoor geldt dat deze conclusie is gebaseerd op beperkte informatie (zeker voor de nieuwere middelen) en dat informatie over bijwerkingen over het algemeen korte follow-up betreft. Dit geldt eveneens voor de invloed van biologicals op het lipidenspectrum. Met name studies met langere follow-up en optreden van cardiovasculaire events zijn in deze van essentieel belang, maar ontbreken.
Onderbouwing
Achtergrond
IMID patiënten hebben een, in vergelijking tot de algemene populatie, tot twee keer verhoogd risico op atherosclerotische aandoeningen en hartfalen. Factoren als systemische inflammatie en medicatiegebruik, waaronder het gebruik van TNFα-blokkers, lijken een rol te spelen, maar de precieze oorzaak van het hartfalen is verre van duidelijk. Zo wordt van TNFα verondersteld dat dit cytokine een belangrijke pathofysiologische rol speelt in de ontwikkeling van hartfalen. De behandeling van patiënten met hartfalen met een TNFα-blokker leidde echter niet tot een verbetering van de myocardfunctie. Bij hogere doseringen anti-TNFα was er zelfs sprake van een trend naar verslechtering van het hartfalen (Danila et al 2008). De vraag is dan ook in hoeverre biologicals, TNF-blokkers in het bijzonder, veilig bij patiënten met hartfalen kunnen worden toegediend.
Daarnaast komt premature atherosclerose bij IMID patiënten vaker voor (Nurmohamed 2007; Popa et al, 2006; van Leuven et al, 2007; Mehta et al, 2009). In het kader van preventie is er toenemende aandacht voor (traditionele) cardiovasculaire risicofactoren, en eventuele correctie daarvan. In het kader van het gebruik van biologicals is van belang in hoeverre het gebruik van deze middelen van invloed is op de traditionele cardiovasculaire risicofactoren, in het bijzonder de hyperlipidemie.
Conclusies
|
Niveau 3 |
Het gebruik van TNFα-blokkers leidt niet tot de novo hartfalen, of verergering van bestaand hartfalen bij RA en Crohn patiënten. Patiënten ouder dan 65 jaar en patiënten met klasse III en IV vormen hierop mogelijk een uitzondering.
B Wolfe en Michaud 2004 C Cole et al, 2007; Curtis et al, 2007; Setoguchi et al, 2008; Bernatsky et al, 2005; Carmona et al, 2007; Listing et al, 2008 |
|
Niveau 4 |
Er zijn geen aanwijzingen dat gebruik van rituximab, anakinra, tocilizumab of abatacept een verhoogd risico geeft op de ontwikkeling of progressie van hartfalen bij patiënten met IMID, maar data hierover zijn zeer beperkt.
C Cohen et al, 2002; Fleischmann et al, 2006; Kremer et al, 2006; Cohen et al, 2006; Weinblatt et al, 2007 |
|
Niveau 3 |
Er zijn aanwijzingen dat het gebruik van TNFα-blokkers en van Tocilizumab een tijdelijke, geringe verandering geeft van het lipidenspectrum bij de patiënten die met deze middelen worden behandeld. De klinische consequenties hiervan zijn onduidelijk. Van andere biologicals zijn de effecten op het lipidenspectrum onvoldoende onderzocht.
B Nurmohammed 2007 |
Samenvatting literatuur
Hartfalen
TNFα-blokkers
TNFα heeft een negatief inotrope invloed op het myocard, remt remodelling, en speelt als zodanig een rol in de pathogenese van hartfalen. De effecten van TNFα zijn echter complex. Zo is de invloed op het myocard mogelijk afhankelijk van de expositieduur aan TNFα en de gelijktijdige invloed van andere cytokines als IL-1β en IL-10.
Er zijn diverse case reports verschenen van patiënten met RA, IBD, artritis psoriatica of JCA die tijdens het gebruik van TNFα-blokkers hartfalen ontwikkelden of waarbij verergering van bestaand hartfalen optrad. Bij de helft van de patiënten (n=19) met nieuw ontstaan hartfalen was geen risicofactor aanwezig, hetgeen suggereert dat het gebruik van TNFα-blokkers mogelijk een oorzakelijke rol speelt (Kwon et al, 2003). In RCTs is echter geen verhoogd voorkomen van hartfalen gevonden tijdens het gebruik van TNFα-blokkers (Danila et al 2008). Ook in observationele studies is geen verhoogd risico gevonden. In de National Databank for Rheumatic Diseases werden 13.171 patiënten met RA geëvalueerd. Hartfalen werd geconstateerd bij 3.1% van de infliximab en etanercept gebruikers, terwijl dat percentage op 3.8% lag bij patiënten die geen TNFα-blokkers gebruikten. Ook na correctie voor belangrijke covariabelen werd geen verschil in incidentie van hartfalen tussen beide groepen aangetoond (Wolfe & Michaud, 2004). Hartfalen kwam niet voor bij met anti-TNFα behandelde patiënten jonger dan 50 jaar. In een kleine case-control studie werd het optreden van hartfalen in een groep van 103 RA patiënten, behandeld met etanercept, infliximab of adalimumab vergeleken met RA patiënten zonder TNFα-blokkers en niet-RA patiënten. Ook in deze studie werd geen verschil in optreden van hartfalen tussen de groepen gevonden (Cole et al, 2007).
In een studie met relatief jonge RA en Crohn patiënten (≤50 jaar) werd gedurende de follow-up van 18 maanden bij 9 (0.2%) van de in totaal 2.121 RA en 1.897 Crohn patiënten hartfalen geconstateerd. Het RR bij RA was niet-significant verhoogd (4.3) bij RA patiënten (Curtis et al, 2007). Bij oudere RA patiënten is het risico op hartfalen bij gebruik van TNFα-blokkers mogelijk wel verhoogd. In een RA cohort van patiënten ouder 65 jaar (1.002 behandeld met, 5.593 zonder TNFα-blokkers) werd een verhoogd risico op ziekenhuisopname ten gevolge van hartfalen gevonden (hazard ratio 1.7, 95% CI:1-07-2.69) (Setoguchi et al, 2008). In een grote cohort studie, met 41.885 RA patiënten, werd de incidentie van ziekenhuisopnames ten gevolge van hartfalen onderzocht. De incidentie van hartfalen bedroeg 1.0/100 patiëntjaren. Patiënten behandeld met infliximab en etanercept hadden een lager risico op hartfalen dan de patiënten behandeld zonder DMARDs (RR 0.5, 95% CI:0.2-0.9) en patiënten behandeld met MTX (RR 0.8, 95% CI 0.6-1.0) (Bernatsky et al, 2005).
Recent werden mortaliteitsgegevens uit de BIOBADASER database gepubliceerd, een nationaal Spaans cohort van RA patiënten behandeld met biologicals waarbij de mortaliteit van patiënten behandeld met TNFα-blokkers werd vergeleken met de mortaliteit van RA patiënten afkomstig uit de EMECAR database, welke niet werden behandeld met TNFα-blokkers. Zowel de mortaliteit t.g.v. alle doodsoorzaken als de cardiovasculaire sterfte was lager in de groep RA patiënten behandeld met anti-TNF. Ook incidentie van hartfalen, voor leeftijd gestratificeerd, was lager in deze groep (0.4 (95% betrouwbaarheidinterval 0.2-0.9/100 patiëntjaren) versus 1.9 (1.3-2.7)/100 patiëntjaren (Carmona et al, 2007). Uit de Duitse RABBIT database kwamen soortgelijke gegevens naar voren. Optreden van hartfalen in RA patiënten in een tijdsspanne van 3 jaar was 2.2% en 0.4% bij patiënten respectievelijk met en zonder cardiovasculaire ziekte op het moment van starten van een behandeling met een TNFα-blokker. Dit cohort besloeg 2.757 patiënten. Het gebruik van anti-TNF middelen was eerder geassocieerd met een lager, dan een hoger risico op hartfalen (HR 0.7, 95% CI: 0.27-1.84) (Listing et al, 2008). In een subanalyse van 98 patiënten met bekend hartfalen werd geen associatie gevonden tussen verergering van hartfalen en gebruik van TNFα-blokkers.
Samenvattend zijn geen harde data voorhanden die een verhoogd risico op het nieuw ontstaan of verergering van bestaand hartfalen aantonen bij IMID patiënten door gebruik van TNFα-blokkers (Danila et al, 2008). Wellicht moet een uitzondering worden gemaakt voor patiënten ouder dan 65 jaar en voor patiënten met klasse III en IV hartfalen, omdat die in studies geëxcludeerd waren. Men moet zich echter realiseren dat de data waarop deze conclusies zijn gebaseerd berusten op studies waarin zeer verschillende definities van hartfalen werden gehanteerd en dat bij een groot aantal studies patiënten met hartfalen tevoren werden geëxcludeerd.
Door onder andere de ACR wordt hartfalen NYHA klasse III-IV, ongeacht de leeftijd, als een contra-indicatie voor het gebruik van TNFα-blokkers beschouwd (Saag et al, 2008). Dit is gebaseerd op een tweetal gerandomiseerde, gecontroleerde studies bij niet-RA patiënten. In de RENEWAL studie werd het effect van etanercept op ziekenhuisopname door hartfalen en mortaliteit in patiënten met NYHA klasse II-IV chronisch hartfalen met een ejectiefractie van ≤ 0.30 beoordeeld. Enig effect op beide uitkomstmaten kon niet worden aangetoond (Mann et al, 2004). In een andere studie werd toevoegen van infliximab in verschillende doseringen bij patiënten met NYHA klasse III-IV hartfalen en een ejectiefractie ≤ 0.35 onderzocht. De ejectiefractie in de patiënten behandeld met 5 mg/kg infliximab verbeterde. Het gecombineerde risico van overlijden als gevolge van elke oorzaak en opname als gevolg van hartfalen was significant verhoogd in patiënten behandeld met 10 mg/kg infliximab (Chung et al, 2003).
In de recent gepubliceerde richtlijnen voor de behandeling van inflammatoire darmziekten wordt eveneens hartfalen NYHA klasse III-IV als contra-indicatie voor het gebruik van TNFα-blokkers beschouwd (CBO-IBD, 2008).
Andere biologicals
Over de andere biologicals zijn zeer beperkt data verschenen in relatie met hartfalen. In de RCTs met anakinra, tot op heden gepubliceerd, is geen hartfalen vermeld in de met anakinra behandelde RA patiënten (Cohen et al, 2004; Fleischmann et al, 2006). Dat geldt evenzeer voor abatacept (Kremer et al, 2006; Weinblatt et al, 2007) en rituximab (Cohen et al, 2006).
Hyperlipidemie
TNFα-blokkers
Patiënten met systemische reumatische ziekten hebben een verhoogd cardiovasculair risico, wat onder ander wordt veroorzaakt door de aanwezigheid van dyslipidemie, deels gerelateerd aan ziekteactiviteit. Inflammatie leidt tot lagere totaal cholesterol maar vooral ook verlaagde HDL-cholesterol spiegels.
Het gebruik van TNFα-blokkers heeft op het lipidenprofiel mogelijk een gunstig effect, al is de literatuur hierin niet eenduidig. In een eerste, kleine studie naar de effecten van TNFα-blokkers vonden Cauza et al in 15 patiënten met RA een ongunstige, pro-atherogene verschuiving in het lipidenprofiel na gebruik van infliximab (Cauza et al, 2002). In een grotere studie, met 69 RA patiënten, werd een stijging van totaal cholesterol en HDL cholesterol gezien na 2 weken behandeling met infliximab (Vis et al, 2005), waarbij het atherogene profiel gelijk bleef. Soortgelijke resultaten in patiënten met RA, werden beschreven tijdens behandeling met infliximab en etanercept (Seriolo et al, 2006; Spanakis et al, 2006) en met adalimumab (Popa et al, 2009). Daarentegen werd in andere studies na 1 jaar behandeling geen verschil op het lipidenspectrum gevonden tijdens gebruik van TNFα-blokkers en werd zelfs een verslechtering gerapporteerd na 2 jaar infliximab gebruik (Dahlqvist et al, 2006; Kiortsis et al, 2006). In een studie met 80 RA patiënten werd tijdens een studieduur van 48 weken aanvankelijk een verbetering van het lipidenprofiel gevonden, maar aan het einde van de studie was dit effect weer verdwenen (Peters et al, 2007). Het effect van TNFα-blokkers op het lipidenprofiel lijkt derhalve vooral passagere en klinisch weinig relevant.
Andere biologicals
Over de effecten van andere biologicals is slechts zeer beperkte informatie voorhanden. In een ongecontroleerde studie met 5 RA patiënten, behandeld met rituximab, werd het lipidenprofiel tot 16 weken na behandeling bepaald. Totaal cholesterol daalde 3-11% en HDL-Cholesterol steeg 14-35% bij de patiënten (Kerekes et al, 2009). Gebruik van tocilizumab leidt tot geringe stijging in totaal cholesterol (gemiddeld 0.8 mmol/l), HDL cholesterol (0.1 mmol/l) en LDL cholesterol (0.5 mmol/l), welke gerelateerd is aan daling van de CRP waarden (Genovese et al, 2008; Emery et al, 2008). De lange termijn klinische consequenties hiervan zijn nog niet duidelijk.
Verantwoording
Autorisatiedatum en geldigheid
Laatst beoordeeld : 01-01-2011
Laatst geautoriseerd : 01-01-2011
Geplande herbeoordeling : 01-01-2014
De Nederlandse Vereniging voor Reumatologie is als houder van deze richtlijn de eerstverantwoordelijke voor de actualiteit van deze richtlijn. Uiterlijk in 2013 bepaalt de NVR of deze richtlijn nog actueel is. Zo nodig wordt een nieuwe werkgroep geïnstalleerd om de richtlijn te herzien. De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De andere aan deze richtlijn deelnemende beroepsverenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid ten aanzien van het bewaken van de actualiteit van de aanbevelingen in de richtlijn. Hen wordt verzocht relevante ontwikkelingen binnen hun vakgebied kenbaar te maken aan de eerstverantwoordelijke.
Algemene gegevens
Met ondersteuning van de afdeling Ondersteuning Professionele Kwaliteit van de Orde van Medisch Specialisten. De richtlijnontwikkeling werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (= SKMS).
Doel en doelgroep
Deze richtlijn geeft een leidraad voor de dagelijkse praktijk van het gebruik van Biologicals. De richtlijn heeft een algemeen karakter, kan gebruikt worden om beroepsspecifieke richtlijnen te formuleren en biedt aanknopingspunten voor bijvoorbeeld lokale (instituuts- of regiogebonden) protocollen en/of zorgafspraken.
De richtlijn is primair geschreven voor medisch specialisten die patiënten met chronische ontstekingsziekten (IMID = Immune Mediated Inflammatory Disorders) behandelen met biologicals, alsmede voor deze patiënten zelf en hun overige behandelaars.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2009 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die met biologicals te maken hebben.
Bij het samenstellen van de werkgroep is rekening gehouden met geografische spreiding en evenredige vertegenwoordiging van verschillende verenigingen, ‘scholen’ en academische achtergrond. De werkgroepleden zijn door de wetenschappelijke verenigingen gemandateerd voor deelname en de samenstelling van de werkgroep is goedgekeurd door alle deelnemende wetenschappelijke verenigingen. De werkgroepleden zijn gezamenlijk verantwoordelijk voor de tekst.
- Dr. D.L. Baeten, reumatoloog, Academisch Medisch Centrum, Amsterdam
- Dr. M. Bijl, reumatoloog, Universitair Medisch Centrum Groningen
- Prof. dr. J.W.J. Bijlsma, reumatoloog, Universitair Medisch Centrum Utrecht (voorzitter)
- Dr. A.A. van Bodegraven, maag-, darm-, leverarts, VU Medisch Centrum, Amsterdam
- Dr. P.L.A. van Daele, internist-klinisch immunoloog, Erasmus Medisch Centrum, Rotterdam
- Prof. dr. M. Drent, longarts, Academisch Ziekenhuis Maastricht
- Mevr. drs. G.J. Geven, Reumapatiëntenbond, Amersfoort
- Mevr. drs. J.W. Hagemeijer, senior adviseur, Orde van medisch Specialisten, Utrecht
- Dr. T.L.Th.A. Jansen, reumatoloog, Medisch Centrum Leeuwarden
- Prof. dr. M.A.F.J. van de Laar, reumatoloog, Medisch Spectrum Twente, Enschede
- Prof. dr. R.B.M. Landewé, reumatoloog, Academisch Ziekenhuis Maastricht
- Prof. dr. W.F. Lems, reumatoloog, VU medisch centrum, Amsterdam
- Dr. M.T. Nurmohamed, reumatoloog, Jan van Breemen Instituut, Amsterdam
- Dr. E. Prens, dermatoloog, Erasmus Medisch Centrum, Rotterdam
- Mevr. drs. M.M.J.H. Scholte-Voshaar, Reumapatiëntenbond, Amersfoort
- Mevr. drs. M. Wessels, informatiespecialist, Orde van Medisch Specialisten, Utrecht
Belangenverklaringen
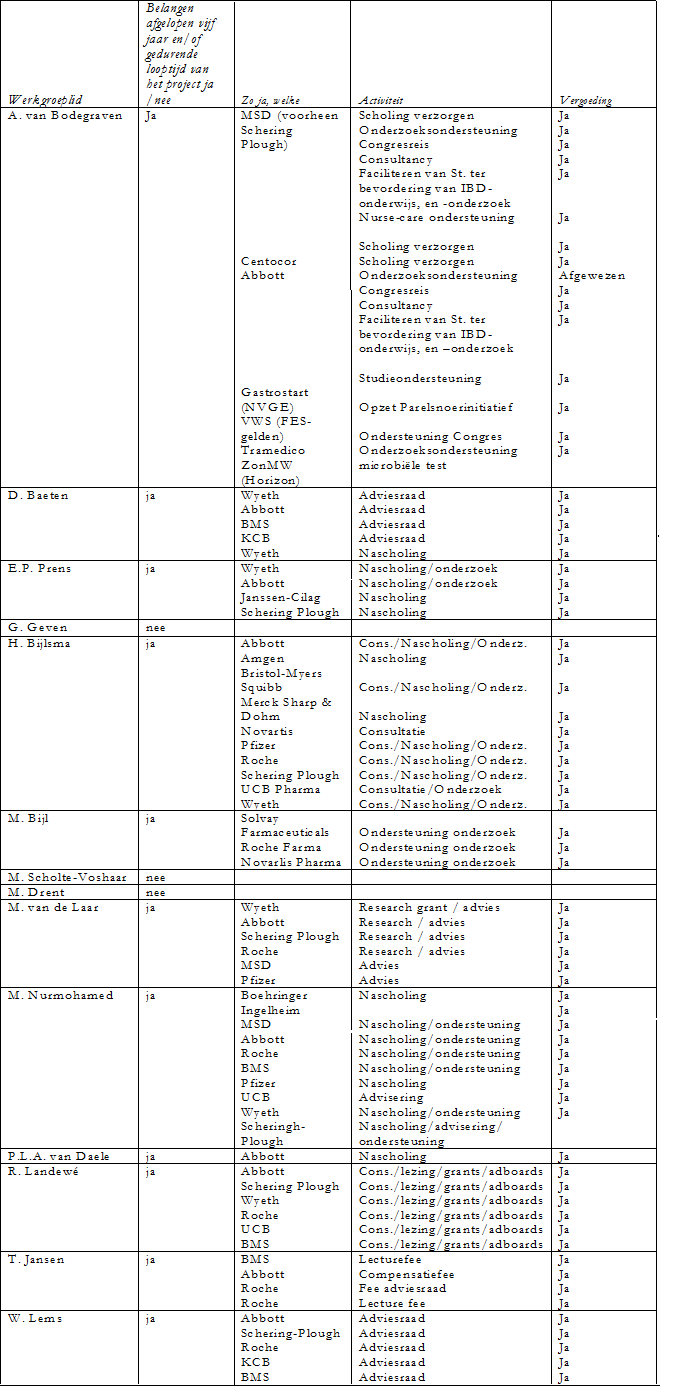
De werkgroepleden is gevraagd om aan te geven of er sprake is van een mogelijke belangenverstrengeling met commerciële bedrijven. Een overzicht hiervan is hieronder weergegeven. De verklaringen van werkgroepleden over mogelijke financiële belangenverstrengeling ligt ter inzage bij de afdeling Ondersteuning Professionele Kwaliteit van de Orde van Medisch Specialisten. Uit de ingevulde belangenverklaringen blijkt dat de werkgroepleden banden met de farmaceutische industrie hebben en dat deze banden gezien het onderwerp belangrijk zijn. Er wordt geconcludeerd dat deze banden geen invloed hebben gehad bij het totstandkomen van de richtlijn.
Inbreng patiëntenperspectief
Gedurende de ontwikkeling van de richtlijn is nadrukkelijk aandacht besteed aan het in kaart brengen van het patiëntenperspectief. In de werkgroep hebben twee patiëntenvertegenwoordigers zitting genomen en zij brachten het perspectief van de patiënten naar voren tijdens de bespreking van de teksten en de formulering van de aanbevelingen. Daarnaast is halverwege het traject een focusgroep georganiseerd waaraan 9 patiënten hebben deelgenomen. De uitgangsvragen zijn voorgelegd aan de leden van de focusgroep en hen is gevraagd naar hun ervaringen en overwegingen die zij van belang achten bij het formuleren van de aanbevelingen. Hiervan is een verslag gemaakt en aan de leden voorgelegd ter verifiëring en eventuele aanvulling. De leden van het schrijverscollectief hebben gebruikgemaakt van de inhoud van deze documentatie voor de formulering van overwegingen vanuit patiëntenperspectief. Een verslag hiervan is hieronder te vinden.
Patiëntenperspectief – verslag focusgroep
In totaal hebben 9 patiënten hun medewerking verleend aan het in kaart brengen van het patiëntenperspectief. Twee mannelijke patiënten met Sarcoidose met Remicade (via infuuskliniek (1 X p.m.) of Humira zelf injecteren (1X p.w.), één mannelijke patiënt met Psoriasis Enbrel zelf injecteren (1X p.w.), twee vrouwen met RA (Enbrel en Rituximab), één mannelijke patiënt met RA (Enbrel), twee vrouwelijke patiënten met Ziekte van Crohn (Humira en Remicade).
Drie personen waren aanwezig bij de focusgroepbijeenkomst die gehouden is op 12 november 2009. De overige 5 personen waren niet in staat om aanwezig te zijn en hebben op digitale wijze hun input geleverd door per uitgangsvraag hun ervaringen terug te koppelen.
Naast het bespreken van de ervaringen is ook gevraagd naar overwegingen die vanuit het perspectief van de patiënt van belang zijn en die naar hun idee meegewogen dienen te worden bij de formulering van de aanbevelingen.
Uit de besprekingen is naar voren gekomen dat de patiënten de geformuleerde uitgangsvragen complex vinden. De patiënten hebben aangegeven dat het maken van een patiëntenversie van de richtlijn belangrijk is omdat nog veel onduidelijk is over het gebruik van biologicals. Door het ontwikkelen van een patiëntenversie van de richtlijn ontvangen de patiënten een instrument waarmee zij ook kunnen bijdragen aan het goed en verantwoord gebruik van biologicals. Hierbij is als voorwaarde gesteld dat de patiëntenversie toegankelijk geschreven moet worden.
Alle deelnemers waren lid van een patiëntenvereniging en ervaren dit als zeer plezierig. Het geeft onder meer de mogelijkheid tot het uitwisselen van informatie met lotgenoten.
VOORAFGAANDE AAN DE BEHANDELING MET BIOLOGICALS: |
Overweging vanuit het patiëntenperspectief bij UV 1: - Patiënten geven aan dat de aanloop naar de behandeling met biologicals overwegend een langdurig proces is geweest. Er wordt overgegaan tot biologicals als alle andere behandelingsvormen niet blijken te helpen of te veel bijwerkingen veroorzaken. - Patiënten vinden het belangrijk dat alle aspecten die van belang zijn bij de behandeling van biologicals worden onderzocht, maar hebben geen zicht op welke aspecten dit dan moeten zijn. Zij geven aan dat het echter belangrijk is dat zij door de specialist of door de verpleegkundige deelgenoot worden gemaakt van het afwegingsproces door informatie te ontvangen zodat zij zelf actief kunnen meewerken aan het zorgproces. |
Overweging vanuit het patiëntenperspectief bij UV 2: - Patiënten vinden het belangrijk dat de arts door wie zij worden behandeld deskundig is, zodat zij erop kunnen vertrouwen in goede handen te zijn. - De (voorschrijvende) medisch specialist dient de regie in handen te houden en daarbij is het overleg met de andere betrokken professionals belangrijk. - Het is belangrijk dat de professionals communicatief zijn en duidelijk uitleg kunnen geven op niveau van de leek. Daarnaast is het wenselijk dat de medisch specialist toegankelijk en laagdrempelig is bij vragen; te weten via de telefoon of email. - Als het niet goed gaat met de patiёnt is het belangrijk dat de medisch specialist confronterend en direct is door aan te geven dat het helemaal niet goed gaat, dat de patiënt zich overvraagt of dat bijvoorbeeld gestopt moet worden met werken. Het is daarbij belangrijk dat de patiënt geen ruimte wordt gegeven om te marchanderen. - De partner is samen met de patiënt ziek en hiermee een essentiёle schakel die duidelijk betrokken behoort te worden in het zorgproces. |
BIJWERKINGEN VAN BIOLOGICALS: |
Overweging vanuit het patiëntenperspectief bij UV 3: - Patiënten vinden het belangrijk dat zij duidelijke en volledige (zowel schriftelijke als mondelinge) informatie ontvangen over de bijwerkingen die zich kunnen voordoen bij een behandeling met biologicals. - Patiënten vinden het belangrijk dat, als zij bijwerkingen ervaren, duidelijk is tot wie zij zich moeten richten, dus tot de huisarts of de medisch specialist. - Patiënten vinden het belangrijk dat, als zij bijwerkingen ervaren, hier serieus naar wordt gekeken en deskundig op wordt geacteerd. - Patiënten vinden het belangrijk dat zij instructies ontvangen wat zij zelf kunnen doen om bepaalde bijwerkingen te voorkomen. |
Overweging vanuit het patiëntenperspectief bij UV 4: - Patiënten vinden het belangrijk dat zij informatie ontvangen over de het risico op kanker bij biologicals. - Patiënten vinden het belangrijk dat zij actief worden gevolgd op het mogelijk ontstaan van kanker. |
ZWANGERSCHAP EN BIOLOGICALS: |
Overweging vanuit het patiëntenperspectief bij UV 5: Op basis van de focusgroep zijn geen overwegingen aan te dragen. |
BIOLOGICALS EN (OPERATIEVE) INGREPEN: |
Overweging vanuit het patiëntenperspectief bij UV 6: - Patiënten vinden het belangrijk dat de voorschrijvend specialist betrokken is bij het besluitvormingsproces van een operatie. Daarbij is het essentieel dat er direct contact is tussen de betrokken specialisten. - Patiënten vinden het belangrijk dat zij in bezit zijn van een ‘kaartje’ waarop staat dat zij biologicals gebruiken en dat met de specialist contact opgenomen moet worden in geval van tandheelkundige of operatieve ingrepen. - Patiënten vinden het belangrijk dat zij informatie ontvangen over de stappen die gezet moeten worden bij het staken of doorgaan van biologicals bij een operatie. Hierdoor zijn zij in staat zelf actief mee te werken en hebben meer het gevoel controle te hebben over hun behandeling met biologicals. |
FOLLOW-UP VAN DE BEHANDELING MET BIOLOGICALS: |
Overweging vanuit het patiëntenperspectief bij UV 7: - Patiënten vinden het belangrijk dat zij regelmatig (om de 3 tot 6 mnd) door de medisch specialist worden onderzocht waarbij de werking van de biologicals in kaart wordt gebracht. - Patiënten vinden het belangrijk dat zij worden geinformeerd over de uitslag van de periodieke controle zodat zij deelgenoot zijn van het zorgproces. - Patiënten geven aan geconfronteerd te worden met een veelheid aan informatiestromen die regelmatig tegenstrijdig zijn. Zij vinden het belangrijk dat hier meer regie over gevoerd gaat worden. - Patiënten vinden het belangrijk dat professionels aangeven wanneer men geen duidelijkheid ten aanzien van bepaalde vraagstukken kunnen geven omdat nog zoveel onbekend is bij de behandeling van biologicals. - Patiënten vinden het belangrijk regelmatig contact te hebben met de (specialistisch) verpleegkundige zodat zij eventuele vragen kan beantwoorden. |
BIOLOGICALS EN VACCINATIE: |
Overweging vanuit het patiëntenperspectief bij UV 8: - Patiënten vinden het belangrijk dat zij (tijdig) informatie ontvangen over welke vaccinaties zij toegediend kunnen krijgen. - Patiënten vinden het belangrijk dat zij informatie ontvangen bij welke verschijnselen, nadat zij een vaccinatie hebben ontvangen, zij contact op moeten nemen met de medisch speicalist. |
DE BEHANDELING MET BIOLOGICALS: |
Overweging vanuit het patiëntenperspectief bij UV 9: - Patiënten vinden het belangrijk dat de arts door wie zij worden behandeld deskundig is en over de meest recente inzichten beschikt zodat zij erop kunnen vertrouwen in goede handen te zijn. - De (voorschrijvende) medisch specialist dient de regie in handen te houden en daarbij is het overleg met de andere betrokken professionals belangrijk. - Het is belangrijk dat de professionals communicatief zijn en duidelijk uitleg kunnen geven op niveau van de leek. Daarnaast is het wenselijk dat de medisch specialist toegankelijk en laagdrempelig is bij vragen; te weten via de telefoon of email. - Als het niet goed gaat met de patiёnt is het belangrijk dat de medisch specialist confronterend en direct is door aan te geven dat het helemaal niet goed gaat, dat de patient zich overvraagt of dat bijvoorbeeld gestopt moet worden met werken. Het is daarbij belangrijk dat de patiënt geen ruimte wordt gegeven om te marchanderen. |
LANGDURIG VERBLIJF ELDERS: |
Overweging vanuit het patiëntenperspectief bij UV 10: - Patiënten vinden het belangrijk dat zij informatie ontvangen over: - hoe zij de biologicals het beste naar het buitenland kunnen vervoeren; - naar welke gebieden zij kunnen reizen; - de mogelijkheden om in het buitenland een infuus met biologicals te ontvangen.
|
Methode ontwikkeling
Evidence based
Implementatie
Tijdens de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de uitvoerbaarheid van de aanbevelingen. Daarbij is gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. De richtlijn is verspreid onder alle relevante beroepsgroepen en instellingen. Een samenvatting van de richtlijn is gepubliceerd in het Nederlands Tijdschrift voor Geneeskunde en in tijdschriften van de deelnemende wetenschappelijke verenigingen.
Werkwijze
De werkgroep heeft een jaar aan de totstandkoming van de richtlijn gewerkt. Binnen de werkgroep was een schrijverscollectief ingesteld. De leden van het schrijverscollectief zochten systematisch naar literatuur en beoordeelden kwaliteit en inhoud ervan. Vervolgens schreven zij een concepttekst waarin de literatuur werd verwerkt. Tijdens vergaderingen lichtten zij hun teksten toe aan de overige leden van de werkgroep. De conceptrichtlijn is in februari 2010 schriftelijk aan alle betrokken wetenschappelijke verenigingen aangeboden en gevraagd de richtlijn aan hun leden voor te leggen. Daarnaast is de richtlijn ook naar wetenschappelijke verenigingen gestuurd die niet in de werkgroep hebben geparticipeerd, te weten oogartsen, neurologen, gynaecologen en tandartsen. De ontvangen commentaren zijn, waar relevant bevonden, verwerkt in de definitieve richtlijn.
Wetenschappelijke onderbouwing
De onderbouwing van de richtlijn is mede gebaseerd op bewijs uit gepubliceerd wetenschappelijk onderzoek. Relevante artikelen werden gezocht met systematische zoekacties. Er werd gezocht tussen 1998 en 2009 in Medline en Embase. Voor de oriënterende search werd ook gezocht in de Cochrane Library en werd specifiek gezocht naar al bestaande richtlijnen in online raadpleegbare (inter)nationale guideline clearinghouses.
Hierbij werd de taal gelimiteerd tot Nederlands, Engels, Duits en Frans. Daarnaast werden artikelen geëxtraheerd uit referentielijsten van opgevraagde literatuur. Dit leverde bij enkele uitgangsvragen nog aanvullende artikelen op.
Doordat de uitgangsvragen niet gericht waren op het beoordelen van de effectiviteit van de interventies maar veelal gingen over bijwerkingen, complicaties en diagnostiek bleek een beperking tot systematische reviews en RCTs vaak niet zinvol. De searches zijn verricht in mei en juni 2009. Voor alle uitgangsvragen is gebruik gemaakt van een uniforme formulering van de patiëntencategorie en de interventie.
Voor de gehanteerde zoektermen wordt verwezen naar Appendix 1. Op verzoek zijn de volledige zoekstrategieën beschikbaar. Daarnaast werden artikelen geëxtraheerd uit referentielijsten van opgevraagde literatuur en zijn enkele relevante publicaties tot 1 november 2009 meegenomen. Lopend onderzoek is buiten beschouwing gelaten. Abstracts van congressen van de afgelopen 2 jaar (november 2007 tot 1 november 2009) zijn meegenomen bij de selectie van de literatuur. Relevante informatie vanuit deze abstract wordt uitgewerkt bij de overige overwegingen. Onder samenvatting van de literatuur / conclusies worden alleen gepubliceerde onderzoeken / richtlijnen uitgewerkt.
De geselecteerde artikelen zijn beoordeeld op kwaliteit van het onderzoek en gegradeerd naar mate van bewijs. Hierbij is de standaardindeling gebruikt: zie tabel 1. Na selectie bleven de artikelen over die als onderbouwing bij de verschillende conclusies staan vermeld. De beoordeling van de verschillende artikelen is opgenomen onder het kopje ‘samenvatting van de literatuur’. Het wetenschappelijk bewijs is vervolgens kort samengevat in een ‘conclusie’. De belangrijkste literatuur waarop deze conclusie is gebaseerd staat bij de conclusie vermeld, inclusief de mate van bewijs (zie tabel 2).
Voor het formuleren van een aanbeveling zijn, naast het wetenschappelijk bewijs, vaak nog andere aspecten van belang, bijvoorbeeld patiëntenvoorkeuren, kosten, beschikbaarheid of organisatorische aspecten. Deze aspecten worden, voor zover niet wetenschappelijk onderzocht, vermeld onder het kopje ‘overwegingen’. In de overige overwegingen spelen de ervaring en de mening van de werkgroepleden een belangrijke rol. De ‘aanbeveling’ is het resultaat van de combinatie van het beschikbare bewijs en de overige overwegingen.
Voor een aantal uitgangsvragen zijn evidencetabellen gemaakt en deze zijn te raadplegen in Appendix 3.
Tabel 1: Indeling van methodologische kwaliteit van individuele studies
|
|
Interventie |
Diagnostische accuratesse onderzoek |
Schade of bijwerkingen, etiologie, prognose* |
|
A1 |
Systematische review van ten minste twee onafhankelijk van elkaar uitgevoerde onderzoeken van A2-niveau |
||
|
A2 |
Gerandomiseerd dubbelblind vergelijkend klinisch onderzoek van goede kwaliteit van voldoende omvang |
Onderzoek ten opzichte van een referentietest (een ‘gouden standaard’) met tevoren gedefinieerde afkapwaarden en onafhankelijke beoordeling van de resultaten van test en gouden standaard, betreffende een voldoende grote serie van opeenvolgende patiënten die allen de index- en referentietest hebben gehad |
Prospectief cohortonderzoek van voldoende omvang en follow-up, waarbij adequaat gecontroleerd is voor ‘confounding’ en selectieve follow-up voldoende is uitgesloten |
|
B |
Vergelijkend onderzoek, maar niet met alle kenmerken als genoemd onder A2 (hieronder valt ook patiënt-controleonderzoek, cohort-onderzoek) |
Onderzoek ten opzichte van een referentietest, maar niet met alle kenmerken die onder A2 zijn genoemd |
Prospectief cohortonderzoek, maar niet met alle kenmerken als genoemd onder A2 of retrospectief cohortonderzoek of patiënt-controleonderzoek |
|
C |
Niet-vergelijkend onderzoek |
||
|
D |
Mening van deskundigen |
||
* Deze classificatie is alleen van toepassing in situaties waarin om ethische of andere redenen gecontroleerde trials niet mogelijk zijn. Zijn die wel mogelijk dan geldt de classificatie voor interventies.
Tabel 2: Niveau van bewijs van de conclusie
|
Conclusie gebaseerd op |
|
|
1 |
Onderzoek van niveau A1 of ten minste twee onafhankelijk van elkaar uitgevoerde onderzoeken van niveau A2 |
|
2 |
Eén onderzoek van niveau A2 of ten minste twee onafhankelijk van elkaar uitgevoerde onderzoeken van niveau B |
|
3 |
Eén onderzoek van niveau B of C |
|
4 |
Mening van deskundigen |
Deze (concept)richtlijn is opgesteld aan de hand van het Appraisal of Guidelines for Research & Evaluation (AGREE) instrument. Dit instrument is in een Europees verband opgesteld om de procedurele kwaliteit van richtlijnen te kunnen beoordelen. Door de aspecten van AGREE te verwerken in de inleiding van de richtlijn, wordt duidelijk aan welke kwaliteitseisen is voldaan.
Zoekverantwoording
Zoekacties zijn opvraagbaar. Neem hiervoor contact op met de Richtlijnendatabase.
