Expectatief beleid bij BPPD
Uitgangsvraag
Kan bij patiënten met BPPD volstaan worden met een expectatief beleid?
Aanbeveling
Behandelen van BPPD verdient de voorkeur boven het afwachten van het natuurlijk beloop.
Overwegingen
- Voordeel: De symptomen verdwijnen bij 35-50 procent van de patiënten na ongeveer 1 maand zonder interventie.
- Nadeel: Langer last van symptomen dan bij behandeling waardoor de patiënt een groter valrisico heeft of niet in staat is tot werken.
- Kosten: indirect kosten vanwege een vertraagde genezing in vergelijking met andere behandelingen.
- Afweging: Een afwachtend beleid als behandeling voor posterieur kanaal BPPD heeft als voordeel dat de patiënt geen manoeuvres of vestibulaire revalidatie hoeft te ondergaan. Niet behandelen heeft echter als nadeel dat de klachten langer persisteren met mogelijke gevolgen voor kwaliteit van leven, vallen en arbeidsverzuim..
- Waarde oordeel: de werkgroep heeft een voorkeur voor een behandelingsinterventie in plaats van het natuurlijk beloop af te wachten, vooral omdat de klachten dan sneller verdwijnen.
- Rol van de voorkeur van de patiënt: substantieel gezien de gezamenlijke beslissing over de behandeling.
- Exclusiecriteria: geen
Onderbouwing
|
Niveau 2
|
De symptomen verdwijnen bij 35-50 procent van de patiënten na ongeveer 1 maand zonder interventie.
|
Observation may be defined as a “watchful waiting” or the withholding of specific therapeutic interventions for a given disease. Observation is often considered when the disease course is self-limited and/or felt to be benign with limited sequelae occurring from the withholding of therapy. In BPPV, observation implies that therapeutic interventions such as vestibular rehabilitation and/or PRMs will be withheld, anticipating a natural and spontaneous improvement of the symptoms of BPPV. Under a course of observation, patients may still be instructed to avoid provocative positions and activities where the risk of injury (ie, falls) may be increased until symptoms resolve spontaneously or until they are reassessed for symptom resolution.
To consider observation as an option in the management of BPPV, the clinician must determine the natural history of the BPPV. It has been presumed that the natural history of BPPV is one of eventual resolution in most patients. It should be noted, however, that an often quoted study by Blakley, (Blakley, et al., 1994) which reported high rates of spontaneous resolution of BPPV, relied on subjective symptom reporting, rather than objective testing with a Dix-Hallpike maneuver, as the outcome measure for resolution. It is believed that a significant fraction of patients reporting subjective improvement actually have reduction in symptoms secondary to avoiding provocative (vertigo-producing) positions rather than actual cure (Woodworth, et al., 2004). More recent RCTs have utilized objective testing with the Dix-Hallpike maneuver as an additional outcome measure to assess for objective resolution of BPPV. Notably, to observe proper blinding, most RCTs also use a sham positional maneuver in the control group, which theoretically may affect the natural history of BPPV.
In several studies, the spontaneous rate of symptomatic resolution of BPPV ranges from 15 to 86 percent. The reported rate of spontaneous improvement based on objective positional testing (ie, conversion to a negative Dix- Hallpike maneuver) ranges from 35 percent to 50 percent (Woodworth, et al., 2004). As demonstrated in Table 4.1, the natural history of posterior canal BPPV varies widely across studies at a 1-month and a 3-month follow-up interval. Further variability in the spontaneous resolution rate arises from differences in duration of symptoms prior to actual diagnoses of BPPV as well as differences in duration of follow-up (Hilton, et al., 2004) (Froehling, et al., 2000) (Lynn, et al., 1995) (Sekine, et al., 2006). Longitudinal follow-up studies of untreated BPPV patients are lacking, but one study of completely untreated patients determined a mean time interval from onset of symptoms to spontaneous resolution of BPPV of 39 _ 47 days (Imai, et al., 2005). As would be expected, spontaneous symptom resolution rates increase with increasing duration of follow-up among observed patients.
Tabel 4.1: Symptoom reductie rates voor observatie alleen van BPPD
|
Referentie |
Genezen n/m |
% genezen |
Placebo behandeling of pure observatie |
Tijd tot assessment |
|
Von Brevern, 2007 |
22/26 |
84.6% |
Placebo |
4 weken |
|
Sakine 2006 |
48/60 |
80.0% |
Observatie |
1 maand |
|
Imai 2005 |
45/70 |
64.0 |
Observatie |
1 maand |
|
Simhadri 2003 |
3/15 |
20 |
Observatie |
4 weken |
|
Yimtae 2003 |
7/20 |
35.0 |
Observatie |
1 maand |
|
Sherman 2001 |
11/22 |
50.0 |
Placebo |
3 maanden |
|
Asawavichianginda 2000 |
18/22 |
81.8 |
Observatie |
3 maanden |
|
Steenerson 1996 |
17/40 |
42.5 |
Observatie |
3 maanden |
|
Lynn 1995 |
3/15 |
20.0 |
Placebo |
1 maand |
|
Blakley 1994 |
19/22 |
86.4 |
Observatie |
1 maand |
Eindpunt: herstel van vertigo symptomen op het tijdstip van assessment.
Although observation of posterior canal BPPV is an option for management, clinicians should also be aware that other treatments such as the PRM have been shown to offer patients faster resolution of BPPV symptoms. A meta-analysis of nine separate trials examining the efficacy of the PRM for BPPV treatment demonstrated consistent improvement in the treatment group, with up to 4.1 times greater rates of symptom resolution (95% confidence interval, 3.1- 5.2) in the PRM groups vs the control groups at initial assessments within 1 month. Studies with follow-up at beyond 1 month still demonstrated an improvement rate of nearly three times that of controls (Woodworth, et al., 2004). Other longer-term follow-up data also suggest that patients treated with a PRM had lower rates of relapse of BPPV at 6 months and 1 year posttreatment (Simhadri, et al., 2003).
Observation as an option for the management of posterior canal BPPV offers the potential benefits of avoiding repositioning maneuvers or vestibular rehabilitation, which in turn may provoke symptoms and discomfort. There may also be a cost savings from decreased rates of referral for vestibular rehabilitation or PRMs. From a potential harms perspective, patients who elect for the observation option should be informed about a typically longer duration of symptoms compared with a treatment maneuver and potentially higher recurrence rates. Appropriate precautions for the risks associated with BPPV symptoms should be taken during the watchful waiting period.
The natural history of lateral canal BPPV is less well defined than that of posterior canal BPPV. Several authors have commented that lateral canal BPPV may be prone to more rapid spontaneous resolution than posterior canal BPPV (Moon, et al., 2006) (Sekine, et al., 2006). In one study, the mean time between the onset of vertigo in lateral canal BPPV to spontaneous resolution was 16 _ 19 days (Imai, et al., 2005). Although repositioning maneuvers have shown success in lateral canal BPPV, overall high quality comparative data regarding treatment vs observation such as RCTs are limited in this subtype of BPPV (Casani, et al., 2002) (Sekine, et al., 2006) (Fife, et al., 2006). Thus, observation of lateral canal BPPV remains an option for management. Future RCTs need to be dedicated to the interventional management of lateral canal BPPV.
- Blakley, B.W. (1994). A randomized, controlled assessment of the canalith repositioning maneuver. Otolaryngol Head Neck Surg, 110, 391-6.
- Casani, A.P., Vannucci, G., Fattori, B., et al. (2002). The treatment of horizontal canal positional vertigo: our experience in 66 cases. Laryngoscope, 112, 172-8.
- Fife, T.D. (1998). Recognition and management of horizontal canal benign positional vertigo. Am J Otol, 19, 345-51.
- Froehling, D.A., Bowen, J.M., Mohr, D.N., et al. (2000). The canalith repositioning procedure for the treatment of benign paroxysmal positional vertigo: a randomized controlled trial. Mayo Clin Proc, 75, 695-700.
- Hilton, M., Pinder, D. (2004). The Epley (canalith repositioning) manoeuvre for benign paroxysmal positional vertigo. Cochrane Database Syst Rev, 0, CD003162-.
- Imai, T., Ito, M., Takeda, N., et al. (2005). Natural course of the remission of vertigo in patients with benign paroxysmal positional vertigo. Neurology, 64, 920-1.
- Lynn, S., Pool, A., Rose, D., et al. (1995). Randomized trial of the canalith repositioning procedure. Otolaryngol Head Neck Surg, 113, 712-20.
- Moon, S.Y., Kim, J.S., Kim, B.K., et al. (2006). Clinical characteristics of benign paroxysmal positional vertigo in Korea: a multicenter study. J Korean Med Sci, 21, 539-43.
- Sekine, K., Imai, T., Sato, G., et al. (2006). Natural history of benign paroxysmal positional vertigo and efficacy of Epley and Lempert maneuvers. Otolaryngol Head Neck Surg, 135, 529-33.
- Simhadri, S., Panda, N., Raghunathan, M. (2003). Efficacy of particle repositioning maneuver in BPPV: a prospective study. Am J Otolaryngol, 24, 355-60.
- Woodworth, B.A., Gillespie, M.B., Lambert, P.R. (2004). The canalith repositioning procedure for benign positional vertigo: a meta-analysis. Laryngoscope, 114, 1143-6.
Beoordelingsdatum en geldigheid
Publicatiedatum : 20-08-2013
Beoordeeld op geldigheid : 01-02-2020
De tekst van deze module is opgesteld tijdens de richtlijnontwikkeling in 2010 door de oorspronkelijke richtlijnwerkgroep (zie Samenstelling werkgroep). De module is opnieuw beoordeeld en nog actueel bevonden door de werkgroep samengesteld voor de richtlijnherziening in 2019 (zie samenstelling huidige werkgroep). Uiterlijk in 2024 bepaalt het bestuur van de Nederlandse Vereniging voor Keel-Neus-Oorheelkunde en Heelkunde van het Hoofd-Halsgebied of de richtlijnmodule nog actueel is.
Algemene gegevens
Met ondersteuning van de Orde van Medisch Specialisten. De richtlijnontwikkeling werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
De richtlijn betreft een adaptatie van:
Clinical practice guideline: Benigne Paroxysmale Positionele Duizeligheid.
De Amerikaanse richtlijn van de Academy of Otolaryngology-Head and Neck surgery foundation ‘Clinical practice guideline: Benign paroxysmal positional vertigo’ (Bhattacharayya, et al., 2008) vormde het uitgangspunt van de onderhavige richtlijn. Daarnaast werd de Amerikaanse richtlijn van de Academy of neurology, gericht op de behandeling van BPPD, gebruikt ter aanvulling (Fife, et al., 2008), alsmede de discussies en richtlijnen van de Standaardisatie commissie van de Barany Society (Reykjavik, et al., 2010, www.baranysociety.nl).
Doel en doelgroep
De primaire doelstellingen van deze richtlijn zijn:
- De kwaliteit van de zorg te verbeteren door middel van een accurate en snelle diagnose van BPPD.
- Voorkomen van onnodig gebruik van medicijnen.
- Doelgericht gebruik van aanvullend onderzoek.
- Stimuleren van het gebruik van repositiemanoeuvres als therapie voor BPPD.
Secundaire doelstellingen zijn: beperking van de kosten van diagnose en behandeling van BPPD, vermindering van het aantal artsenbezoeken, en verbetering van de kwaliteit van leven. Het grote aantal patiënten met BPPD en de verscheidenheid aan diagnostische en therapeutische interventies voor BPPD maakt dit een geschikt onderwerp voor een evidence-based richtlijn.
De Amerikaanse richtlijn van de Academy of Otolaryngology-Head and Neck surgery foundation ‘Clinical practice guideline: Benign paroxysmal positional vertigo’ (Bhattacharayya, et al., 2008) vormde het uitgangspunt van de onderhavige richtlijn. Daarnaast werd de Amerikaanse richtlijn van de Academy of neurology, gericht op de behandeling van BPPD, gebruikt ter aanvulling (Fife, et al., 2008), alsmede de discussies en richtlijnen van de Standaardisatie commissie van de Barany Society (Reykjavik, et al., 2010, www.baranysociety.nl)). Onze doelstelling was om deze multidisciplinaire richtlijn te adapteren aan de Nederlandse situatie met behulp van Nederlandse input, waarbij de aanbevelingen rekening houden met wetenschappelijk bewijs en zich richten op harm-benefit balans, en expert consensus om de gaten in wetenschappelijk bewijs op te vullen. Deze specifieke aanbevelingen kunnen dan gebruikt worden om indicatoren te ontwikkelen en te gebruiken voor kwaliteitsverbetering.
Deze richtlijn is opgesteld voor KNO-artsen en neurologen die in hun klinische praktijk in aanraking komen met BPPD. De richtlijn is toepasbaar in iedere setting waar BPPD gediagnosticeerd en behandeld wordt.
Samenstelling werkgroep
Voor het ontwikkelen van de module is in 2018 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met BPPD.
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep is verantwoordelijk voor de integrale tekst van deze module.
Samenstelling huidige werkgroep:
- Dr. Tj.D. (Tjasse) Bruintjes, KNO-arts, Gelre Ziekenhuizen, Apeldoorn, NVKNO (voorzitter)
- Dr. R.B. (Roeland) van Leeuwen, neuroloog, Gelre ziekenhuizen, Apeldoorn, NVN
- Dr. R. (Raymond) van de Berg, KNO-arts/vestibuloloog, Maastricht UMC+, Maastricht, NVKNO
- Dr. M. (Marloes) Thoomes-de Graaf, fysiotherapeut/manueel therapeut/klinisch epidemioloog, Fysio-Experts, Hazerswoude, KNGF en NVMT
- R.A.K. (Sandra) Rutgers, arts, MPH en voorzitter Commissie Ménière Stichting Hoormij, Houten, Stichting Hoormij
Met ondersteuning van:
- D. (Dieuwke) Leereveld, MSc., senior adviseur Kennisinstituut van de Federatie Medisch Specialisten
- Drs. M. (Monique) Wessels, informatiespecialist Kennisinstituut van de Federatie Medisch Specialisten
Samenstelling oorspronkelijke werkgroep (2010):
- dr. Tj.D. Bruintjes (voorzitter), KNO-arts, Gelre ziekenhuizen, Apeldoorn
- prof. dr. H. Kingma, klinisch fysicus/vestibuloloog, Maastricht Universitair Medisch Centrum en Technische Universiteit Eindhoven
- dr. D.J.M. Mateijsen, KNO-arts, Catharina ziekenhuis, Eindhoven
- dr. R.B. van Leeuwen, neuroloog, Gelre ziekenhuizen, Apeldoorn
- dr. ir. T van Barneveld klinisch epidemioloog, Orde van Medisch specialisten (adviseur)
- dr. M.L. Molag, Orde van Medisch specialisten (adviseur)
Belangenverklaringen
De werkgroepleden hebben onafhankelijk gehandeld en waren vrij van financiële of zakelijke belangen betreffende het onderwerp van de richtlijn.
Methode ontwikkeling
Evidence based
Werkwijze
De Amerikaanse richtlijn van de Academy of Otolaryngology-Head and Neck surgery foundation ‘Clinical practice guideline: Benign paroxysmal positional vertigo’ (Bhattacharayya, et al., 2008) vormde het uitgangspunt van de onderhavige richtlijn. Daarnaast werd de Amerikaanse richtlijn van de Academy of neurology gebruikt (Fife, et al., 2008). Dit betekent dat de Nederlandse richtlijncommissie de studies, de beoordeling & gradering ervan en de begeleidende tekst heeft overgenomen. Studies, relevant voor dit onderwerp, die nadien werden gepubliceerd konden in de richtlijncommissie worden ingebracht. De literatuur werd bovendien geupdate door te zoeken in Medline naar nieuw verschenen systematische reviews en RCTs met als onderwerp BPPD in de periode van 2008 t/m 2010.
De richtlijncommissie is voor elke aanbeveling in de Amerikaanse richtlijn nagegaan welke overwegingen naast het wetenschappelijk bewijs zijn gebruikt en of de door de commissie aangedragen studies de aanbeveling zouden kunnen veranderen. Wanneer er consensus was over deze overwegingen en door de commissie aangedragen studies geen ander inzicht opleverden, zijn de aanbevelingen overgenomen. Indien de commissie andere overwegingen (ook) van belang achtte of meende dat de door haar aangedragen studies een (iets) ander licht wierpen op de in de Amerikaanse richtlijn vermelde aanbeveling, zijn de aanbevelingen gemodificeerd.
De gradering van de studies in de Amerikaanse richtlijn wijkt af van wat hier te lande gangbaar is. Vanuit het oogpunt van uniformiteit achtte de Nederlandse commissie het wenselijk de classificatie van bewijs c.q. gradering te converteren naar de Nederlandse classificatie. De Amerikaanse classificatie is hieronder afgebeeld in tabel. De corresponderende “Nederlandse” classificatie is in tabel 1.2 opgenomen.
Tabel 1.1: gradering van de studies in de Amerikaanse richtlijn
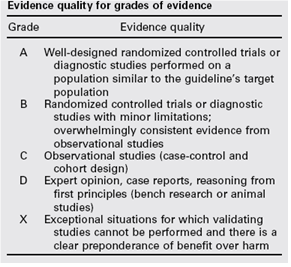
Tabel 1.2 Relatie tussen Evidence quality for grades of evidence en niveau van conclusie op basis van kwaliteit van bewijs conform Classificatieschema van CBO.
|
Evidence Quality - symbool |
Evidence Quality – omschrijving |
Niveau van conclusie – symbool |
Niveau van conclusie omschrijving |
|
A
|
Well-designed randomized controlled trials or diagnostic studies performed on a population similar to the guideline’s target population |
1 |
Meerdere gerandomiseerde dubbelblinde vergelijkende klinisch onderzoeken van goede kwaliteit van voldoende omvang, of
Meerdere onderzoeken ten opzichte van een referentietest (een ‘gouden standaard’) met tevoren gedefinieerde afkapwaarden en onafhankelijke beoordeling van de resultaten van test en gouden standaard, betreffende een voldoende grote serie van opeenvolgende patiënten die allen de index- en referentietest hebben gehad |
|
B |
Randomized controlled trials or diagnostic studies with minor limitations; overwhelmingly consistent evidence from observational studies |
2 |
Meerdere vergelijkende onderzoeken, maar niet met alle kenmerken als genoemd onder 1 (hieronder valt ook patiënt-controle onderzoek, cohort-onderzoek), of
Meerdere onderzoeken ten opzichte van een referentietest, maar niet met alle kenmerken die onder 1 zijn genoemd. |
|
C |
Observational studies (case-control and cohort design) |
||
|
D |
Expert opinion, case reports, reasoning from first principles (bench research or animal studies) |
3 en 4 |
Niet vergelijkend onderzoek of mening van deskundigen |
In de Amerikaanse richtlijn worden ook de aanbevelingen gegradeerd in termen van ‘strong recommendation’, ‘recommendation’, ‘option’. Hier te lande is graderen van aanbevelingen niet gebruikelijk. Om deze reden zijn in de Nederlandse richtlijn de aanbevelingen niet gegradeerd.
De literatuurzoekstrategie die de Amerikaanse richtlijncommissie heeft gevolgd, staat in bijlage 1 beschreven. Voor het opstellen van de aanbevelingen heeft de Amerikaanse richtlijncommissie gebruik gemaakt van de GuideLine Implementability Appraisal (GLIA) tool. Dit instrument dient om de helderheid van de aanbevelingen te verbeteren en potentiële belemmeringen voor de implementatie te voorspellen. In bijlage 3 wordt een aantal criteria beschreven. Ook de Nederlandse richtlijncommissie heeft deze criteria gehanteerd.
