Pijnmeting bij pijn bij kanker
Uitgangsvraag
Welke meetinstrumenten zijn het meest geschikt bij de diagnostiek en behandeling van patiënten met pijn bij kanker?
Aanbeveling
- Gebruik bij voorkeur de Numerical Rating Scale en als tweede keus de Visual Analogue Scale of Verbal Rating Scale voor het meten van pijn bij patiënten met kanker (IC).
- Onderneem actie, volgens de beschreven interventies in deze richtlijn, indien de pijnintensiteitsscore ≥4 is (op een 11-punts schaal) en de patiënt hiermee instemt, en evalueer het effect hiervan met een pijnscore (ID).
- Meet pijn regelmatig. Het aantal keer is afhankelijk van de plaats waar de patiënt verblijft:
- Ziekenhuis: Meet bij opgenomen patiënten pijn eenmaal daags. Meet pijn bij elke poliklinisch bezoek.
- Verpleeghuis/hospice: Meet bij patiënten met pijn en/of pijnmedicatie de pijn minimaal eenmaal per dag. Meet pijn bij patiënten zonder pijn minimaal eenmaal per week.
- Thuis: Stimuleer patiënten met pijn om dagelijks een pijndagboek bij te houden.
Leg alle pijnscores vast in het (elektronisch) patiëntendossier (ID).
- Streef bij de behandeling van pijn naar een afname van de pijnscore met minimaal twee punten of 30% en bij voorkeur naar een pijnintensiteitsscore van <4 (op 11-punts pijnschaal) (ID).
- Informeer altijd bij de patiënt of de aangegeven pijnintensiteit voor hem acceptabel is (ID).
- Gebruik gedragsobservatieschalen bij patiënten met cognitieve beperkingen die hun pijn niet aan kunnen geven met een Numeric Rating Scale, Visual Analogue Scale of Verbal Rating Scale (IC).
- Gebruik de DN4 of de PainDetect om te screenen of een patiënt neuropatische pijn heeft (IC).
- Gebruik de Brief Pain Inventory of de McGill Pain Questionnaire om de invloed van pijn op het dagelijks functioneren uit te vragen (IC).
- Neem naast het gebruik van meetinstrumenten een multidimensionele pijnanamnese af (ID).
Overwegingen
Unidimensionele pijnmetingen
In 2009 is in het kader van het VMS Veiligheidsprogramma het thema pijn beschreven voor in het ziekenhuis opgenomen patiënten. Dit betreft echter veelal postoperatieve patiënten. In het programma wordt de 11-punts pijnschaal (NRS) gebruikt en een afkapwaarde van ≥4 voorgesteld waarboven tot actie dient te worden overgegaan. Om eenduidig te zijn, stelt de werkgroep voor om ook bij de patiënten met kanker en pijn een afkapwaarde van ≥4 te hanteren en om onderstaand stroomschema te gebruiken (zie figuur 1 Stroomschema Herkenning van pijn). Deze figuur over de herkenning van pijn is ook van toepassing op pijn bij kanker.
Figuur 1. Stroomschema Herkenning van pijn
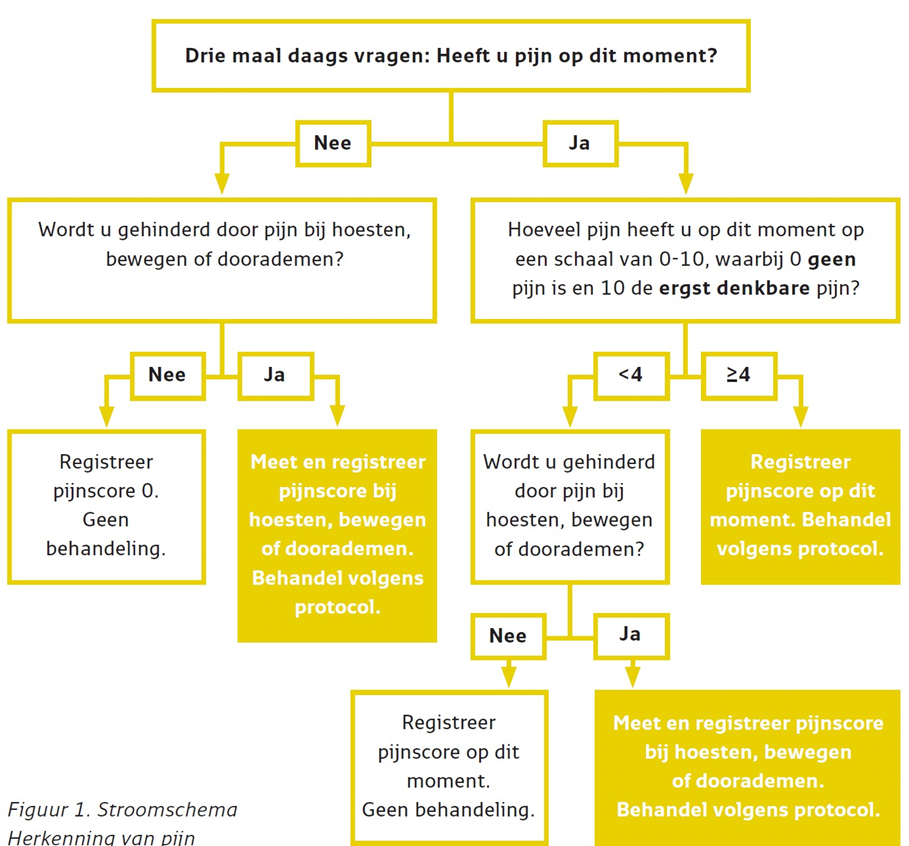
Bron: VMS Veiligheidsprogramma het thema pijn
De populatie zoals door VMS voorgesteld betreft veelal postoperatieve patiënten. In het programma wordt drie keer per dag naar de pijn op dat moment gevraagd. In de verpleegkundige praktijk is dit niet altijd haalbaar en bij patiënten met stabiele pijn niet altijd noodzakelijk. Voor opgenomen patiënten met kanker stelt de werkgroep voor om twee tot drie keer daags pijn te meten. Bij elk polikliniek bezoek moet er naar pijn gevraagd worden en dient dit in het patiëntendossier vastgelegd te worden. In verpleeghuizen, hospices en dergelijke dient bij patiënten die bekend zijn met pijn, of die pijnmedicatie gebruiken dagelijks eenmalig naar pijn gevraagd te worden. Indien er geen pijn gemeld wordt door de bewoner, kan de meting wekelijks gedaan worden. In de thuissituatie kan het dagelijks gebruik van een zogenaamd pijndagboek gestimuleerd worden waarin de patiënt zelf de mate van pijn noteert (zie ook uitgangsvraag Educatie en voorlichting).
Multidimensioneel: de invloed van pijn op dagelijks functioneren
Omdat pijn veelal niet op zichzelf staat maar beïnvloedt wordt door andere symptomen is de werkgroep van mening dat naast pijn er ook altijd gevraagd moet worden naar de invloed van pijn op het dagelijks functioneren en naar alle dimensies van pijn (zie de module Multidimensionele benadering van pijn). Hiertoe kan de landelijke Pijnanamnese gebruikt worden (zie appendix bij de richtlijn). Deze praktische, goed bruikbare Nederlandstalige vragenlijst is ontwikkeld door V&VN.
Pijnverpleegkundigen en heeft een acceptabele validiteit (Oldenmenger, 2006). De vragenlijst is gestoeld op vragen uit de BPI en de McGill questionnaire, omvat in totaal 15 vragen over diverse aspecten van pijn en geeft de patiënt en de hulpverlener meer inzicht in de ervaren pijn en de invloed van pijn.
Specifiek voor wetenschappelijk onderzoek wordt regelmatig gebruik gemaakt van de zeven vragen uit de BPI over zogenaamde interference: de invloed van ervaren pijn op bijvoorbeeld. slapen, stemming, omgang met anderen en algemene activiteiten.
Doorbraakpijn
Voor doorbraakpijn zijn er tot nu toe geen aparte Nederlandstalige gevalideerde en gepubliceerde vragenlijsten beschikbaar.
Neuropatische pijn
Andere vragenlijsten naast de DN4, zijn de PainDETECT en de LANSS. De PainDETECT bevat 62 items en is recent vertaald, gevalideerd en gepubliceerd (zie appendix aan het eind van deze module) (Timmerman, 2013). De vragenlijst is nog niet gevalideerd voor oncologische patiënten. De LANSS is een vragenlijst die wel in de praktijk gebruikt wordt, maar waarvan de Nederlandse vertaling nog niet gevalideerd en gepubliceerd is (Bennet, 2001). De werkgroep is van mening dat voor het screenen van neuropatische pijn zowel de DN4 als de PainDETECT kunnen worden gebruikt.
Specifieke groepen
Voor het beoordelen van pijn bij patiënten met bijvoorbeeld uitingsbeperkingen, of bij de groep fragiele ouderen met milde cognitieve stoornissen, is het afnemen van een NRS of VAS veelal wel mogelijk. Bij patiënten waarbij dit niet mogelijk is moet vooral gekeken worden naar pijngedrag. Specifieke meetinstrumenten voor het observeren en interpreteren van pijngedrag kunnen hiervoor worden gebruikt, zoals beschreven in de Verenso Richtlijn Pijn (Verenso, 2011).
De pijnschalen en meetinstrumenten die in deze richtlijnmodule zijn opgenomen:
- DN4 (Doleur Neuropatique - 4)
- BPI (Brief Pain Inventory)
- MPQ (McGill Pain Questionnaire)
- Landelijke pijnanamnese verpleegkundigen
- PainDETECT
- DN4 (Doleur Neuropatique - 4)


- BPI (Brief Pain Inventory)
Korte Pijn Inventarisatie (BPI Short Version – Dutch language)
- Tijdens ons leven hebben de meesten van ons af en toe pijn gehad (zoals lichte hoofdpijn, verstuikin- gen en kiespijn). Heeft u vandaag pijn gehad, anders dan deze allerdaagse soorten pijn?
O Ja O Nee
- Arceer op de afbeelding de gebieden waar u pijn heeft. Plaats een ‘X’ in het gebied waar u de meeste pijn voelt.
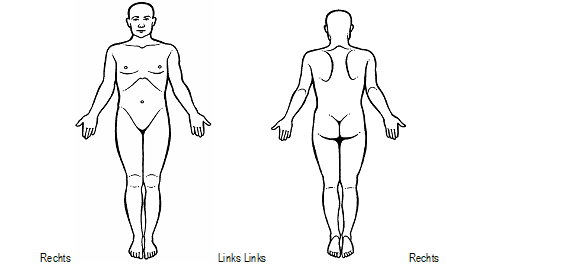
Als u uw pijn uitdrukt in een cijfer tussen 0 en 10:
0 1 2 3 4 5 6 7 8 9 10
0 = geen pijn
10 = ergste pijn die u zich kunt voorstellen
Hoeveel pijn,
- Heeft u als uw pijn op zijn ergst is?
0 1 2 3 4 5 6 7 8 9 10
- Heeft u als uw pijn het minst erg is?
0 1 2 3 4 5 6 7 8 9 10
- Heeft u de afgelopen 24-uur gemiddeld gehad?
0 1 2 3 4 5 6 7 8 9 10
- Heeft u op dit moment?
0 1 2 3 4 5 6 7 8 9 10
- Wat voor behandelingen/medicijnen krijgt u voor uw pijn? _
- Hoeveel verlichting hebben pijnbehandelingen of medicijnen u in de afgelopen 24 uur gegeven? Kunt u dit in een percentage tussen 0 en 100 aangeven met 0% is geen verlichting en 100% is volledige verlichting.
|
Geen 0% |
10% |
20% |
30% |
40% |
50% |
60% |
70% |
80% |
90% |
100% Volledige |
|
verlichting |
|
|
|
|
|
|
|
|
|
verlichting |
- Geef het ene nummer dat het beste omschrijft hoe de pijn in de afgelopen 24-uur belemmerend heeft ge- werkt op uw:
A. Algemene activiteit
|
Geen 0 belemmering
B. Stemming |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 Volledige belemmering |
|
Geen 0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 Volledige |
|
belemmering |
|
|
|
|
|
|
|
|
|
belemmering |
|
C. Loopvermogen |
|
|
|
|
|
|
|
|
|
|
|
Geen 0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 Volledige |
|
belemmering |
|
|
|
|
|
|
|
|
|
belemmering |
|
D. Normale werkzaamheden (hieronder valt zowel werk buitenshuis als huishoudelijk werk) |
||||||||||
|
Geen 0 1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 Volledige |
|
|
belemmering |
|
|
|
|
|
|
|
|
belemmering |
|
|
E. Relaties met andere |
mensen |
|
|
|
|
|
|
|
|
|
|
Geen 0 1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 Volledige |
|
|
belemmering |
|
|
|
|
|
|
|
|
belemmering |
|
|
F. Slaap |
|
|
|
|
|
|
|
|
|
|
|
Geen 0 1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 Volledige |
|
|
belemmering |
|
|
|
|
|
|
|
|
belemmering |
|
|
G. Plezier in het leven |
|
|
|
|
|
|
|
|
|
|
|
Geen 0 1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 Volledige |
|
|
belemmering |
|
|
|
|
|
|
|
|
belemmering |
|
- MPQ (McGill Pain Questionnaire)
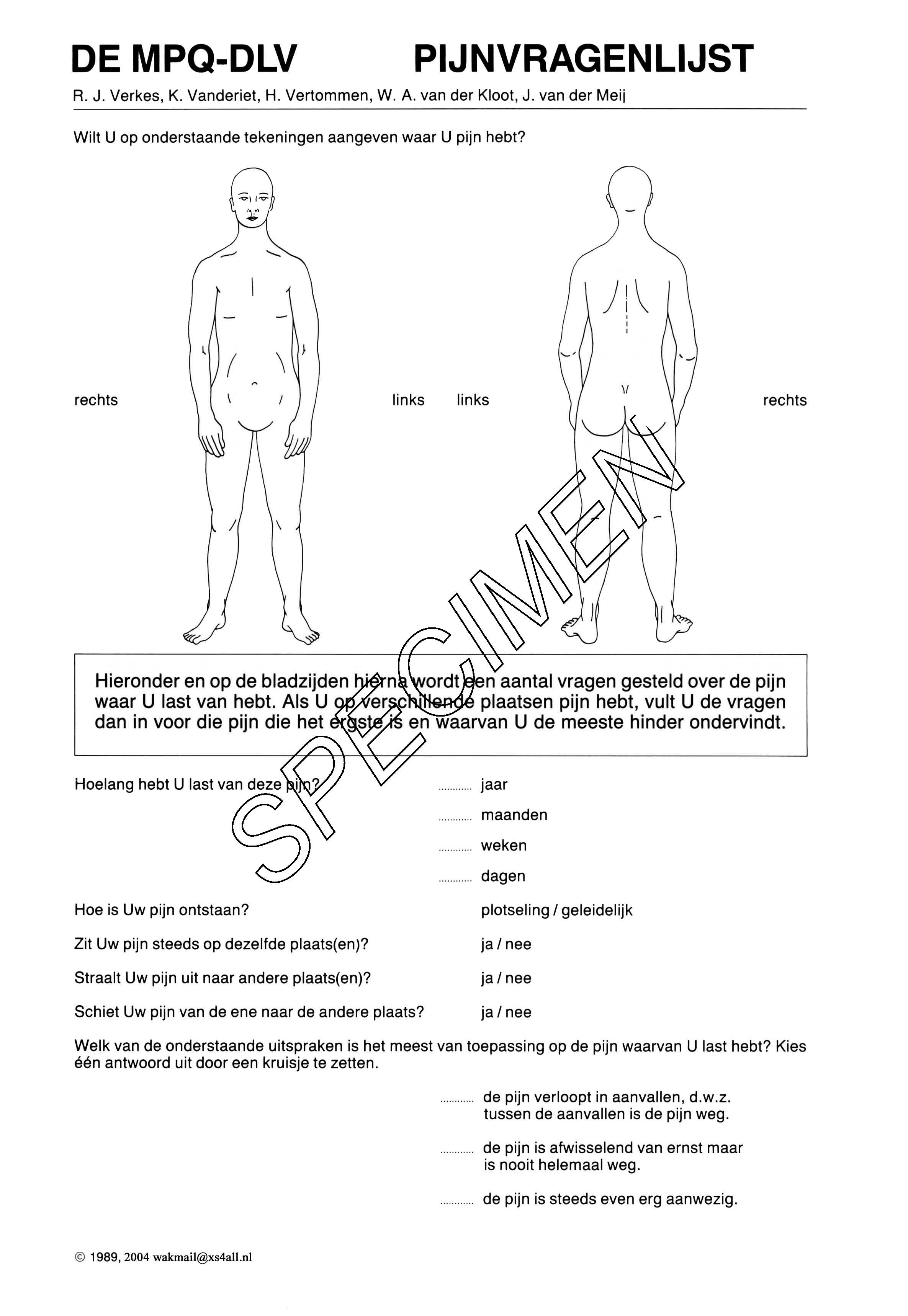


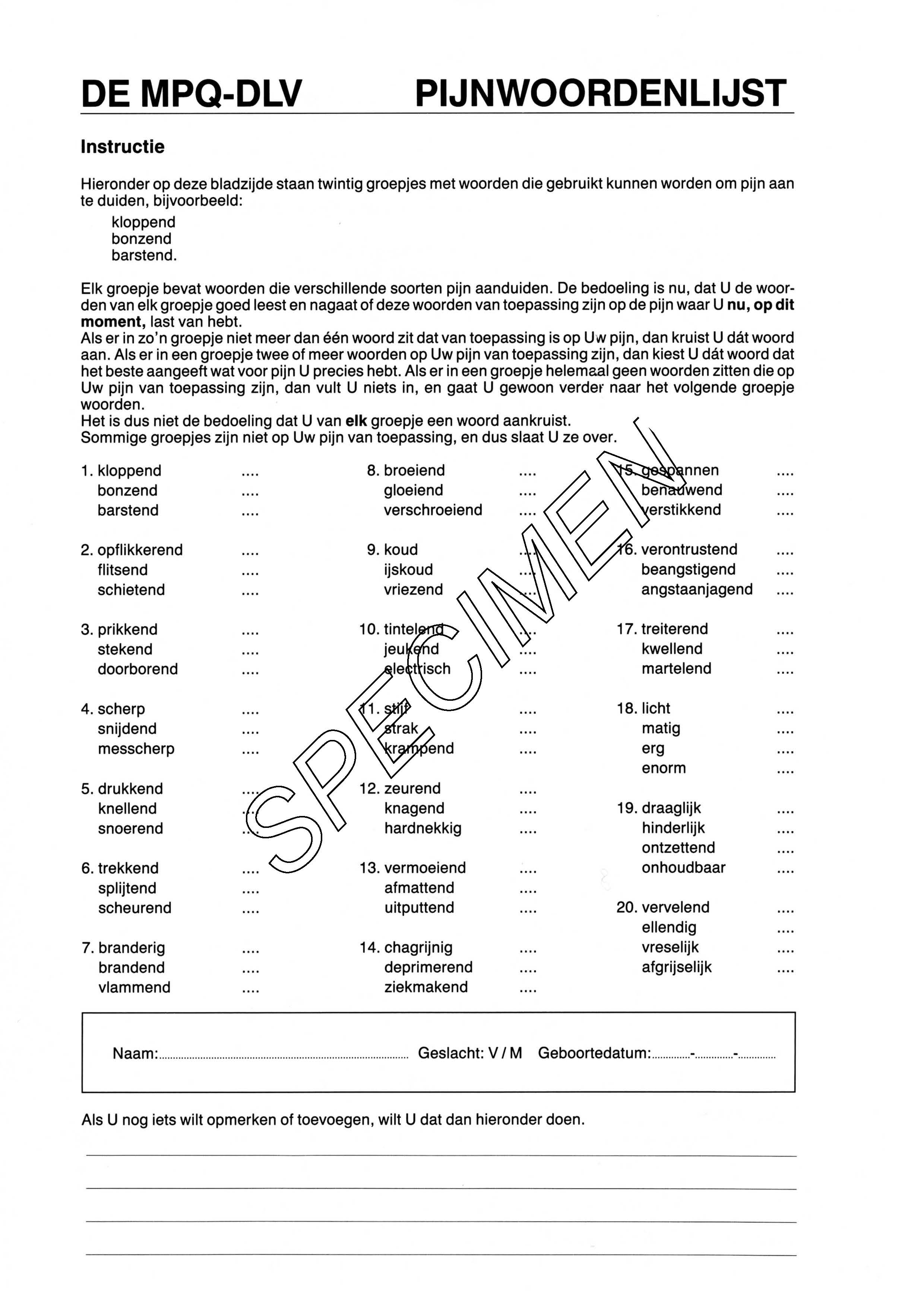
- Landelijke pijnanamnese verpleegkundigen
Pijnanamnese
BETREFT PATIËNT: M / V
Naam verpleegkundige:
Afdeling:
Instelling:
Datum:
Probleem
1. WAAR HEEFT U PIJN? (op tekening aangeven, indien van toepassing op meerdere plaatsen)

2. SINDS WANNEER HEEFT U DEZE PIJN? ………dagen ………weken ………maanden jaren
3. HOE IS UW PIJN ONTSTAAN? 0 geleidelijk 0 plotseling
4. WELK VERLOOP HEEFT UW PIJN? 0 De pijn is steeds even erg aanwezig
0 De pijn verloopt in aanvallen, d.w.z. tussen de aanvallen is de pijn weg
0 De pijn is wisselend van ernst maar is nooit helemaal weg
|
5. HOE ZOU U DE PIJN DIE U VOELT |
1 |
2 |
3 |
|
HET BESTE KUNNEN OMSCHRIJVEN? |
0 opflikkerend 0 flitsend 0 schietend |
0 prikkelend 0 stekend 0 doorborend |
0 drukkend 0 knellend 0 snoerend |
|
4 |
5 |
6 |
|
|
0 branderig |
0 scherp |
0 zeurend |
|
|
0 brandend |
0 snijdend |
0 knagend |
|
|
0 vlammend |
0 messcherp |
0 hardnekkig |
|
0 anders,nl……………………………………………………………..
6. ALS U UW PIJN UITDRUKT IN EEN CIJFER TUSSEN 0 EN 10, a. heeft u op dit moment? .......
WAARBIJ 0 BETEKENT GEEN PIJN EN 10 BETEKENT b. had u gemiddeld de afgelopen week? .......
DE ERGSTE PIJN DIE U ZICH KUNT VOORSTELLEN, c. heeft u als uw pijn het minst erg is? .......
HOEVEEL PIJN d. heeft u als uw pijn op zijn ergst is? ........
e. vindt u draaglijk? ........
Etiologie (oorzaak + samenhangende factoren)
7. WAARDOOR DENKT U DAT UW PIJN ……………………………………………………………………………..
WORDT VEROORZAAKT? ……………………………………………………………………………..
|
8. WAARDOOR WORDT UW PIJN ERGER? |
0 Lichamelijke verzorging |
0 Behandelingen |
|
(meerdere antwoorden mogelijk) |
0 Bepaalde stemmingen |
0 Anders, nl …………….. |
|
|
0 Bepaalde houdingen en bewegingen |
|
9. WAARDOOR KUNT U ZELF DE PIJN VERLICHTEN? .........................................................................................………………
(Behalve medicijnen in nemen?) …………………………………………………………………. ……………
Symptomen
10. BELEMMERDE DE PIJN U DE AFGELOPEN WEEK BIJ HET
-
- inslapen 0 nee 0 beetje 0 tamelijk 0 veel
- doorslapen 0 nee 0 beetje 0 tamelijk 0 veel
- werd u de afgelopen week ’s morgens wakker met pijn? 0 nee 0 beetje 0 tamelijk 0 veel
11. Belemmerde de pijn u de afgelopen week
-
- bij normale houding en beweging 0 nee 0 beetje 0 tamelijk 0 veel
- bij normale eetgewoonten 0 nee 0 beetje 0 tamelijk 0 veel
- bij normale bezigheden en/of 0 nee 0 beetje 0 tamelijk 0 veel werkzaamheden?
- in contacten met anderen 0 nee 0 beetje 0 tamelijk 0 veel
12. WAS U DE AFGELOPEN WEEK DOOR UW PIJN
|
a. gespannen |
0 nee |
0 beetje |
0 tamelijk |
0 |
veel |
|
b. somber |
0 nee |
0 beetje |
0 tamelijk |
0 |
veel |
|
c. zenuwachtig |
0 nee |
0 beetje |
0 tamelijk |
0 |
veel |
|
d. boos |
0 nee |
0 beetje |
0 tamelijk |
0 |
veel |
|
e. minder geconcentreerd |
0 nee |
0 beetje |
0 tamelijk |
0 |
veel |
|
f. angstig |
0 nee |
0 beetje |
0 tamelijk |
0 |
veel |
|
g. futloos |
0 nee |
0 beetje |
0 tamelijk |
0 |
veel |
|
h. anders, nl……………. |
|
0 beetje |
0 tamelijk |
0 |
veel |
13. KUNT U ZELF AANGEVEN WELKE MEDICIJNEN U 0 nee 0 ja
TEGEN DE PIJN GEBRUIKT MET TIJDEN EN DOSERINGEN? ………………………………………………………………………………..
………………………………………………………………………………..
………………………………………………………………………………..
………………………………………………………………………………..
………………………………………………………………………………..
………………………………………………………………………………..
………………………………………………………………………………..
………………………………………………………………………………..
………………………………………………………………………………..
………………………………………………………………………………..
14. HAD U DE AFGELOPEN WEEK LAST VAN BIJWERKINGEN VAN DE PIJNBEHANDELING, ZOALS:
|
Hoofdpijn |
0 nee |
0 beetje |
0 tamelijk |
0 |
veel |
|
Verwardheid |
0 nee |
0 beetje |
0 tamelijk |
0 |
veel |
|
Sufheid |
0 nee |
0 beetje |
0 tamelijk |
0 |
veel |
|
Duizeligheid |
0 nee |
0 beetje |
0 tamelijk |
0 |
veel |
|
Droge mond |
0 nee |
0 beetje |
0 tamelijk |
0 |
veel |
|
Jeuk |
0 nee |
0 beetje |
0 tamelijk |
0 |
veel |
|
Misselijkheid/ braken |
0 nee |
0 beetje |
0 tamelijk |
0 |
veel |
|
Maagpijn |
0 nee |
0 beetje |
0 tamelijk |
0 |
veel |
|
Obstipatie |
0 nee |
0 beetje |
0 tamelijk |
0 |
veel |
|
Anders, nl.………………………………. |
|
0 beetje |
0 tamelijk |
0 |
veel |
15. Opmerkingen: ……………………………………………………………..
……………………………………………………………..
……..………………………………………………………
……………………………………………………………..
……………………………………………………………..
- PainDETECT
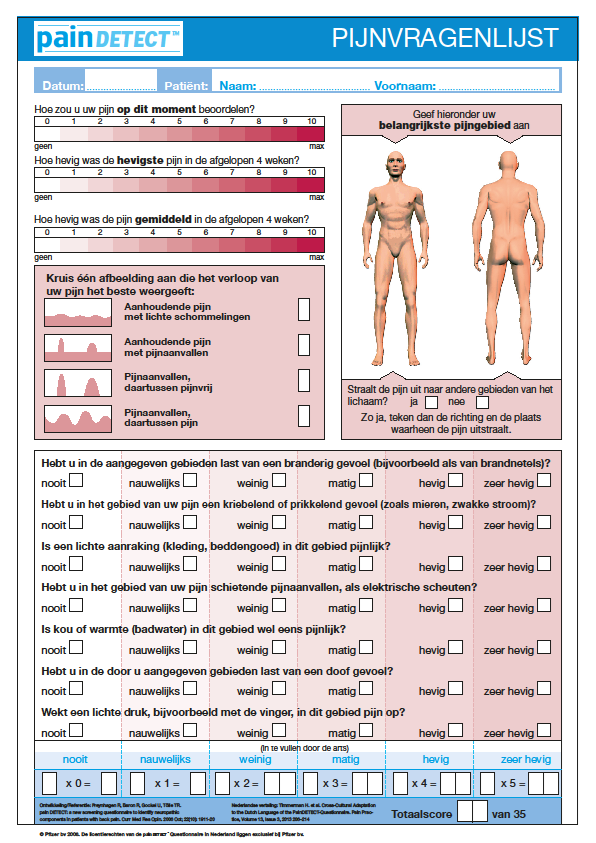
Onderbouwing
Bij het beoordelen van pijn bij patiënten met kanker, en vervolgens bij het behandelen van de klacht en het begeleiden van de patiënt, is het van belang de aard van de pijn goed in kaart te brengen en het beloop van ervaren pijn in de loop van de tijd te vervolgen. Hiertoe kunnen specifieke pijnvragenlijsten gebruikt worden als meetinstrument voor signalering, screening en monitoring. Het doel van de uitgangsvraag is te komen tot meer uniformiteit in hoe pijn uitgevraagd, gemeten en vervolgd wordt, om zo tot een effectieve, integrale pijnbehandeling te komen. Hierbij zijn enkel in de Nederlandse taal beschikbare en gevalideerde meetinstrumenten in beschouwing genomen.
Voor het meten van pijn bij patiënten met pijn bij kanker zijn zowel de Visual Analogue Scale, de Numeric Rating Scale en de Verbal Rating Scale valide en betrouwbaar. De Numeric Rating Scale is in de praktijk het best bruikbaar (geen beoordeling).
(Jensen, 2003; Hjermstad, 2011)
Het is aannemelijk dat het gebruik van multidimensionele vragenlijsten inzicht geeft in welke mate de patiënt met pijn bij kanker in zijn dagelijks functioneren door de pijn beperkt wordt (geen beoordeling).
(Jensen, 2003)
Het is aannemelijk dat een pijnintensiteit <5 aangeeft dat de pijn voor de patiënt met pijn bij kanker voldoende onder controle is (geen beoordeling).
(Oldenmenger, 2013)
Voor het meten van doorbraakpijn bij patiënten met pijn bij kanker is de NRS het meest bruikbaar (geen beoordeling).
(Hjermstad, 2011; Brunelli, 2010)
Voor het identificeren van neuropatische pijn bij patiënten met pijn bij kanker is de DN4 bruikbaar (geen beoordeling).
(Van Seventer, 2013)
Het is aannemelijk dat dokters de intensiteit van pijn bij patiënten met pijn bij kanker onderschatten en dat de inschatting van verpleegkundigen het meest overeenkomst met die van de patiënt (geen beoordeling).
(Jensen 20013)
Beschrijving van de studies
Bij de beantwoording van de uitgangsvraag werd net als bij de vorige richtlijn de systematische review van Jensen uit 2003 als uitgangspunt gebruikt, aangevuld door een systematische review van Hjermstad uit 2011, een review van Oldenmenger (2013) en een studie van Van Seventer (2013). De review van Jensen gaf een uitgebreide beschrijving van de literatuur betreffende de validiteit en betrouwbaarheid van verschillende meetinstrumenten voor pijn bij kanker. De meer recente studie van Hjermstad onderzocht eveneens de validiteit en betrouwbaarheid van de meetinstrumenten, zowel in een bredere patiëntengroepen dan Jensen als in een subanalyse voor studies met patiënten met kanker en pijn. Oldenmenger gaf een overzicht van recente literatuur betreffende de overgangen (afkapwaarden) tussen milde en matige pijn en tussen matige en ernstige pijn. De studie van Van Seventer betrof een validatiestudie voor het gebruik van de DN4, een diagnostisch meetinstrument voor neuropatische pijn (zie appendix aan het eind van deze module). Alle uitspraken hieronder komen voort uit Jensen en/of Hjermstad, tenzij anders vermeld.
Literatuur
Voor de pijnmeting bij patiënten met kanker wordt onderscheid gemaakt tussen unidimensionele en multidimensionele pijnvragenlijsten. Bij unidimensionele metingen wordt uitsluitend gevraagd naar de intensiteit van de pijn. Bij multidimensionele metingen wordt ook aandacht besteed aan de psychologische, sociale en functionele dimensies van pijn, ofwel, wat betekent het hebben van pijn voor de patiënt. Dit kan met behulp van een specifieke pijnanamnese of door middel van aanvullende vragen.
Unidimensionele metingen
Bij de unidimensionele metingen wordt gebruikt gemaakt van verschillende schalen (zie appendix aan het eind van deze module):
- Visual Analogue Scale (VAS). De standaard VAS is een lijn van 10 centimeter, met aan de uiteinden ‘geen pijn' en ‘ergst denkbare pijn';
- Numerical Rating Scale (NRS). De NRS is een schaal van 0 (geen pijn) tot 10 (ergst denkbare pijn);
- Verbal Rating Scale (VRS). In de VRS zijn verschillende schalen beschikbaar, van een vier woorden schaal (geen, licht, matig, ernstig) tot een zes punts-schaal (geen, heel licht, licht, nogal, ernstig, heel ernstig). Deze laatste schaal is vertaald en gevalideerd in diverse talen, inclusief het Nederlands.
Beide reviews concludeerden dat alle drie de schalen valide, betrouwbaar en bruikbaar zijn gebleken. De VAS is de meest abstracte schaal en blijkt in de dagelijkse praktijk het moeilijkste te hanteren. De VRS is de minst gevoelige schaal maar is gemakkelijk in gebruik. Bij patiënten met verminderde cognitieve vermogens is een 4-punts VRS de meest optimale keuze. De NRS is gevoelig voor verandering en wordt goed geaccepteerd door patiënten. In onderzoeken waarbij deze schalen onderling vergeleken zijn, komt naar voren dat de schalen in gelijke mate valide en betrouwbaar zijn. Tevens wordt aangegeven dat in de praktijk de NRS de meest bruikbare keuze is.
De betekenis van de uitkomsten van de NRS en de VAS zijn ook onderzocht. Hierbij is onderzocht in welke mate de pijnintensiteit zoals aangegeven door de patiënt zijn dagelijks functioneren beïnvloedt. Meestal wordt de indeling milde pijn (NRS-score 1 tot en met 3-4), matige pijn (score 4-5 tot en met 6) en ernstige pijn (score 7 tot en met 10) gehanteerd (Serin, 1995). Oldenmenger concludeert dat de literatuur geen eenduidigheid geeft over de overgangen tussen milde en matige pijn en tussen matige en ernstige pijn (Oldenmenger, 2013). De studie concludeert dat bewezen is dat een pijncijfer van 5 en meer een grote invloed heeft op het dagelijks functioneren. Ter evaluatie van een behandeling kan hiernaast ook gebruik gemaakt worden van de klinisch relevante afname van pijn, wat een vermindering in pijnintensiteit van twee punten (op een 0 tot 10 schaal) inhoudt en/of een afname van pijnintensiteit van 30% (Jensen, 2003; Farrar, 2001).
Multidimensionele meting
Voor de multidimensionele meting van pijn kan gebruik gemaakt worden van specifieke multidimensionele pijnvragenlijsten, zoals de Brief Pain Inventory (BPI) of de McGill Pain Questionnaire (MPQ) (zie appendix aan het eind van deze module). De BPI wordt momenteel het meest gebruikt en is een simpel en makkelijk instrument dat informatie geeft over de intensiteit van de pijn op een 0 tot 10 schaal, op vier wijzen gemeten; op dit moment, de minst, de ergste en de gemiddelde pijn. De BPI geeft tevens de ingenomen pijnmedicatie, de locatie van de pijn, de invloed van pijn op het dagelijks functioneren (=interferentie) met behulp van zeven vragen en de mate waarin door de interventie de pijn is afgenomen (0 tot 100%) aan. De MPQ is een lange (78 items) vragenlijst die samengestelde metingen van vier dimensies van pijn beschrijft, namelijk sensorisch, affectief, evaluatief en overig. Er is een verkorte (short-form) MPQ ontwikkeld welke 15 items bevat. De associatie tussen de unidimensionele pijnmeting met bijvoorbeeld een NRS en de MPQ is matig. Gebruik van de MPQ geeft meer inzicht in de diversie dimensies van pijn. Overige vragenlijsten zoals de Rotterdamse Symptom CheckList (RSCL) of de SF-36 zijn nog uitgebreider, maar niet pijn-specifiek genoeg.
Pijndifferentiatie
Zoals in Algemene inleiding beschreven wordt onderscheid gemaakt tussen nociceptieve en neuropathische pijn. Dit onderscheid heeft grote consequenties voor de behandeling.
Om neuropatische pijn te kunnen onderscheiden is de DN4 vragenlijst (Douleur Neuropathique) (Bouhassira, 2005) ontwikkeld (zie appendix aan het eind van deze module). De DN4 is vertaald in het Nederlands en gevalideerd bij niet-oncologische patiënten en bestaat uit tien items (zeven voor de patiënt, drie voor de arts) (Van Seventer, 2013). Bij een afkapwaarde van >4 is er hoogst waarschijnlijk sprake van neuropatische pijn.
Een derde aparte entiteit is doorbraakpijn, waaraan aparte aandacht dient te worden besteedt. Doorbraakpijn wordt gedefinieerd als een voorbijgaande exacerbatie van pijn die spontaan optreedt, of optreedt in relatie met een specifieke voorspelbare of onvoorspelbare factor, ondanks relatief stabiele en voldoende gereguleerde achtergrondpijn (Davies, 2009). Voor doorbraakpijn zijn geen aparte gevalideerde vragenlijsten beschikbaar in het Nederlands. Brunelli (2010) toonde dat voor het meten van doorbraakpijn de NRS het meest bruikbaar is (Hjermstad, 2011; Brunelli, 2010).
Pijnmetingen door derden
Bij voorkeur wordt de mate van pijn door de patiënt zelf gescoord. Indien dit niet mogelijk is, bijvoorbeeld bij patiënten die te suf zijn, is het mogelijk de pijn door anderen te laten scoren. Artsen blijken pijn van patiënten met kanker te onderschatten terwijl naasten de pijn overschatten. De inschatting door verpleegkundigen komt het meest overeen met die van de patiënt (Jensen, 2003).
Voor dit onderdeel van de herziening van de richtlijn is geen nieuwe systematische literatuuranalyse volgens de GRADE methodiek uitgevoerd. De literatuur is daarom niet systematisch beoordeeld. Wel werd aan de hand van nieuw verschenen systematische reviews, meta-analyses andere relevante literatuur nagegaan of nieuwe bevindingen of inzichten aanleiding geven de aanbevelingen uit de vorige versie van de richtlijn uit 2008 te herzien. Hiervoor werd een literatuursearch uitgevoerd naar studies die zijn verschenen na de literatuursearch van de vorige versie van de richtlijn. In de databases Medline (OVID), Embase and Cochrane is met relevante zoektermen gezocht naar systematische reviews, randomized controlled trials en ander vergelijkend onderzoek. De literatuurzoekactie leverde 541 treffers op.
Bij de rapportage van de bevindingen zijn alleen die (meet)instrumenten besproken die beschikbaar zijn in Nederland en zijn gevalideerd in de Nederlandse taal.
- Bennett M. The LANSS Pain Scale: the Leeds assessment of neuropathic symptoms and signs. Pain 2001;92(1- 2):147-57.
- Brunelli C, Zecca E, Martini C, et al. Comparison of numerical and verbal rating scales to measure pain exacerbations in patients with chronic cancer pain. Health Qual Life Outcomes 2010;8:42.
- Grond S, Zech D, Diefenbach C, et al. Assessment of cancer pain: a prospective evaluation in 2266 cancer patients referred to a pain service. Pain 1996;64(1):107-14.
- Hjermstad MJ, Fayers PM, Haugen DF, et al. Studies comparing Numerical Rating Scales, Verbal Rating Scales, and Visual Analogue Scales for assessment of pain intensity in adults: a systematic literature review. [Review]. Journal of Pain & Symptom Management 2011;41(6):1073-93.
- Jensen MP. The validity and reliability of pain measures in adults with cancer. J Pain. 2003;4(1):2-21.
- Oldenmenger WH, de Raaf PJ, de KC, et al. Cut points on 0-10 numeric rating scales for symptoms included in the Edmonton Symptom Assessment Scale in cancer patients: a systematic review. [Review]. Journal of Pain & Symptom Management 2013;45(6):1083-93.
- Oldenmenger WH, Stronks DL, et al. Naar een landelijke, uniforme verpleegkundige pijnanamnese. Nederlands Tijdschrift voor Pijn en Pijnbestrijding 2006;25:6-12. PMID: 14622723
- Serlin RC, Mendoza TR, Nakamura Y, et al. When is cancer pain mild, moderate of severe? Grading pain severity by its interference with function. Pain 1995;61:277-284.
- Timmerman H, Wolff AP, Schreyer T, et al. Cross-cultural adaptation to the Dutch language of the PainDETECT- Questionnaire. Pain Pract 2013;13(3):206-14.
- Van Seventer R, Vos C, Giezeman M, et al. Validation of the Dutch version of the DN4 diagnostic questionnaire for neuropathic pain. Pain Pract 2013;13(5):390-8.
- Verenso Multidisciplinaire Richtlijn Pijn. 2011. www.verenso.nl/assets/Uploads/Downloads/Richtlijnen/VERRichtlijnPijnDeel2web.pdf
- Bouhassira D, Attal N, Alchaar H, Boureau F, Brochet B, Bruxelle J, Cunin G, Fermanian J, Ginies P, Grun-Overdyking A, Jafari-Schluep H, Lantéri-Minet M, Laurent B, Mick G, Serrie A, Valade D, Vicaut E. Comparison of pain syndromes associated with nervous or somatic lesions and development of a new neuropathic pain diagnostic questionnaire (DN4). Pain. 2005;114: 29-36.
Beoordelingsdatum en geldigheid
Publicatiedatum : 04-02-2020
Beoordeeld op geldigheid : 01-11-2023
Actualisatie
Deze richtlijn is goedgekeurd op 6 december 2019. De Nederlandse Vereniging voor Anesthesiologie (NVA) bewaakt samen met betrokken verenigingen de houdbaarheid van deze (modules van de) richtlijn. Zo nodig zal de richtlijn tussentijds op onderdelen worden bijgesteld. De geldigheidstermijn van de richtlijn is maximaal 5 jaar na vaststelling. Indien de richtlijn dan nog actueel wordt bevonden, wordt de geldigheidsduur van de richtlijn verlengd.
Houderschap richtlijn
De houder van de richtlijn (NVA) moet kunnen aantonen dat de richtlijn zorgvuldig en met de vereiste deskundigheid tot stand is gekomen.
IKNL draagt zorg voor het beheer en de ontsluiting van de richtlijn.
Juridische betekenis van richtlijnen
Een richtlijn is een kwaliteitsstandaard. Een kwaliteitsstandaard beschrijft wat goede zorg is, ongeacht de financieringsbron (Zorgverzekeringswet (Zvw), Wet langdurige zorg (Wlz), Wet maatschappelijke ondersteuning (Wmo), aanvullende verzekering of eigen betaling door de cliënt/patiënt). Opname van een kwaliteitsstandaard in het Register van Zorginstituut Nederland betekent dus niet noodzakelijkerwijs dat de in de kwaliteitsstandaard beschreven zorg verzekerde zorg is.
De richtlijn bevat aanbevelingen van algemene aard. Het is mogelijk dat deze aanbevelingen in een individueel geval niet van toepassing zijn. Er kunnen zich feiten of omstandigheden voordoen waardoor het wenselijk is dat in het belang van de patiënt van de richtlijn wordt afgeweken. Wanneer van de richtlijn wordt afgeweken, dient dit beargumenteerd gedocumenteerd te worden. De toepassing van de richtlijnen in de praktijk is de verantwoordelijkheid van de behandelende arts.
Algemene gegevens
Autoriserende/instemmende en bij de werkgroep betrokken verenigingen:
- Nederlandse Internisten Vereniging
- Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose
- Nederlandse Vereniging voor Anesthesiologie
- Nederlandse Vereniging voor Klinische Geriatrie
- Nederlandse Vereniging voor Neurologie
- Vereniging voor Specialisten Ouderengeneeskunde
- Verpleegkundigen en Verzorgenden Nederland
- Nederlandse Vereniging van Ziekenhuisapothekers
- Nederlandse vereniging voor professionele palliatieve zorg
Financiering
Deze richtlijn c.q. module is gefinancierd door IKNL. De inhoud van de richtlijn c.q. module is niet beïnvloed door de financierende instantie.
Procesbegeleiding
IKNL (Integraal Kankercentrum Nederland) is het kennis- en kwaliteitsinstituut voor professionals en bestuurders in de oncologische en palliatieve zorg dat zich richt op het continu verbeteren van de oncologische en palliatieve zorg.
IKNL benadert preventie, diagnose, behandeling, nazorg en palliatieve zorg als een keten waarin de patiënt centraal staat. Om kwalitatief goede zorg te waarborgen ontwikkelt IKNL producten en diensten ter verbetering van de oncologische zorg, de nazorg en de palliatieve zorg, zowel voor de inhoud als de organisatie van de zorg binnen en tussen instellingen. Daarnaast draagt IKNL nationaal en internationaal bij aan de beleidsvorming op het gebied van oncologische en palliatieve zorg.
IKNL rekent het (begeleiden van) ontwikkelen, implementeren en evalueren van multidisciplinaire, evidence-based richtlijnen voor de oncologische en palliatieve zorg tot een van haar primaire taken. IKNL werkt hierbij conform de daarvoor geldende (inter)nationale kwaliteitscriteria. Bij ontwikkeling gaat het in toenemende mate om onderhoud (modulaire revisies) van reeds bestaande richtlijnen.
Doel en doelgroep
Doel
Een richtlijn geeft aanbevelingen ter ondersteuning van de belangrijkste knelpunten uit de dagelijkse praktijk. Deze richtlijn is zoveel mogelijk gebaseerd op wetenschappelijk onderzoek en consensus. De richtlijn 'Pijn’ geeft aanbevelingen over begeleiding en behandeling van patiënten met pijn bij kanker (zowel in de curatieve als de palliatieve fase) en beoogt hiermee de kwaliteit van de zorgverlening te verbeteren.
Hoewel de evidentie alleen is verzameld voor de diagnostiek en behandeling van pijn bij patiënten met kanker zijn de aanbevelingen ook grotendeels van toepassing voor patiënten met andere levensbedreigende aandoeningen.
Doelgroep
Deze richtlijn is bestemd voor alle professionals die betrokken zijn bij de zorg voor patiënten met pijn zoals huisartsen, specialisten ouderengeneeskunde, medisch specialisten, apothekers, verpleegkundigen, verzorgenden, verpleegkundig specialisten, physician assistants, fysiotherapeuten, medisch maatschappelijk werkers, geestelijk verzorgers, GZ- en klinisch psychologen.
Indien in de richtlijn wordt gesproken over zorgverleners rondom de patiënt met pijn, worden, afhankelijk van de specifieke situatie van de patiënt, alle bovengenoemde professionals bedoeld.
De richtlijn is ook relevant voor zorgverleners van andere disciplines en vrijwilligers die werkzaam zijn in de palliatieve fase. De multidimensionele benadering van de patiënt in de palliatieve fase vergt immers een gezamenlijke, interdisciplinaire verantwoordelijkheid, zoals ook in het Kwaliteitskader palliatieve zorg Nederland is beschreven.
Samenstelling werkgroep
Alle werkgroepleden en klankbordleden zijn afgevaardigd namens wetenschappelijke, beroeps- en patiëntenverenigingen en hebben daarmee het mandaat voor hun inbreng. Bij de samenstelling van de werkgroep is geprobeerd rekening te houden met landelijke spreiding, inbreng van betrokkenen uit zowel academische als algemene ziekenhuizen/instellingen en vertegenwoordiging van de verschillende verenigingen/disciplines.
Het patiëntenperspectief is vertegenwoordigd door Patiëntenfederatie Nederland.
Bij de uitvoering van het evidence-based literatuuronderzoek is de kaderopleiding Palliatieve Zorg en een literatuuronderzoeker van IKNL en de voorzitter van de richtlijnwerkgroep betrokken geweest.
Werkgroepleden
- Mw. prof. dr. M.H.J. van den Beuken-van Everdingen, internist, NIV
- Dhr. dr. M.J.M.M. Giezeman †, anesthesioloog, NVA
- Dhr. dr. A. de Graeff (voorzitter), internist-oncoloog en hospice-arts, Palliactief
- Mw. drs. H. Klaren, klinisch geriater, NVKG
- Mw. B. Kramp, verpleegkundig specialist, V&VN
- Dhr. drs. M. Martens, specialist ouderengeneeskunde en consulent palliatieve zorg, Verenso
- Mw. drs. M.J. Oortman, huisarts, SCEN-arts, palliatief consulent en hospice-arts, NHG
- Dhr. drs. P. Oosterhof, poliklinisch apotheker, NVZA
- Mw. prof.dr. A.K.L. Reyners, internist, NIV
- Mw. M. Schielke, verpleegkundig pijnspecialist, V&VN
- Mw. drs. M.C. Sieders, huisarts (waarnemend), SCEN-arts, palliatief consulent, NHG
- Dhr. dr. M.F.M. Wagemans, anesthesioloog, NVA
Klankbordleden
- Dhr. prof. dr. K.C.P. Vissers, anesthesioloog, NVA
- Mw. drs. L. Bellersen, cardioloog, NVVC
- Mw. drs. B.A. Brouwer, neuroloog/pijnspecialist NVN/pijnspecialist
- Mw. M. Geerts, verpleegkundig specialist, V&VN
- Dhr. drs. S.M. de Hosson, longarts, NVALT
- Mw. drs. S. Visser, apotheker, KNMP
- Mw. drs. R. Lammers, beleidsmedewerker, Patiëntenfederatie Nederland
Ondersteuning
- Mw. T.T.M. Bluemink-Holkenborg, secretaresse, IKNL
- Mw. drs. M.G. Gilsing, adviseur (richtlijnen) palliatieve zorg, IKNL
- Mw. dr. O.L. van der Hel, literatuuronderzoeker, IKNL
- Prof.dr. J Kleijnen, epidemioloog, literatuuronderzoeker MUMC Maastricht/York
- Mw. L.K. Liu, secretaresse, IKNL
- Dhr. dr. R. Vernooij (i.s.m. de kaderopleiding Palliatieve Zorg), literatuuronderzoeker, IKNL
Belangenverklaringen
Om de beïnvloeding van de richtlijnontwikkeling of formulering van de aanbevelingen door conflicterende belangen te minimaliseren zijn de leden van werkgroep gemandateerd door de wetenschappelijke en beroepsverenigingen.
Alle leden van de richtlijnwerkgroep hebben verklaard onafhankelijk gehandeld te hebben bij het opstellen van de richtlijn. Een onafhankelijkheidsverklaring ‘Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling' zoals vastgesteld door onder meer de KNAW, KNMG, Gezondheidsraad, CBO, NHG en Orde van Medisch Specialisten is door de werkgroepleden bij aanvang en bij afronding van het traject ingevuld. De bevindingen zijn schriftelijk vastgelegd in de belangenverklaring en opvraagbaar via info@iknl.nl.
Inbreng patiëntenperspectief
De input van patiëntvertegenwoordigers is nodig voor de ontwikkeling van kwalitatief goede richtlijnen. Goede zorg voldoet immers aan de wensen en eisen van zowel zorgverlener als patiënt. Patiëntenfederatie Nederland is in het gehele richtlijntraject meegenomen en heeft plaats gehad in de klankbordgroep (zie ook de Samenstelling van de werkgroep).
Tijdens de landelijke consultatiefase heeft Patiëntenfederatie Nederland commentaar gegeven op de conceptrichtlijn en patiënten/naasten geraadpleegd via een referentenpanel voor onderzoeksaanvragen op het gebied van palliatieve zorg. Ook heeft de Patiëntenfederatie Nederland - naast NFK, nog andere patiëntenorganisaties benaderd voor het leveren van commentaar.
Patiëntenfederatie Nederland heeft tot slot de richtlijn goedgekeurd.
Patiënteninformatie gebaseerd op de richtlijn is opgesteld en gepubliceerd op de daarvoor relevante sites (o.a. zie link https://www.kanker.nl/gevolgen-van-kanker/pijn/wat-is/pijn-bij-kanker#show-menu).
Methode ontwikkeling
Evidence based
Implementatie
Bevorderen van het toepassen van de richtlijn in de praktijk begint met een brede bekendmaking en verspreiding van de richtlijn.
Bij verdere implementatie gaat het om gerichte interventies om te bevorderen dat professionals de nieuwe kennis en kunde opnemen in hun routines van de zorgpraktijk, inclusief borging daarvan.
Als onderdeel van elke richtlijn stelt IKNL samen met de richtlijnwerkgroep een implementatieplan op en ondersteunt een aantal basis-activiteiten voor de implementatie. De verantwoordelijkheid voor verdere implementatie-activiteiten ligt bij de eigenaar van de richtlijn (en het veld).
Activiteiten en interventies voor verspreiding en implementatie kunnen zowel op landelijk als regionaal niveau plaatsvinden. Deze kunnen eventueel ook op maat gemaakt worden per instelling of specialisme.
Het implementatieplan bij deze richtlijn is een belangrijk hulpmiddel om effectief de aanbevelingen uit deze richtlijn te implementeren voor en door de verschillende disciplines.
Werkwijze
In de huidige richtlijn zijn de NVA-richtlijn van 2015 en de richtlijn 'Pijn' van Pallialine samengevoegd. Daarbij zijn de onderdelen van de NVA-richtlijn, die in 2015 niet zijn herzien (en waarbij de teksten van de NVA-versie van 2008 onveranderd zijn gehandhaafd) grotendeels evidence-based (op basis van aanvullend literatuuronderzoek) aangepast en aangevuld met evidence-based en consensus-based teksten over de diagnostiek en behandeling van pijn bij patiënten met gevorderde stadia van COPD of hartfalen. De onderdelen van de NVA-richtlijn die in 2015 zijn herzien zijn onveranderd overgenomen (zie ook de Algemene inleiding).
De bedoeling is om te komen tot een integrale en actuele richtlijn over de diagnostiek en behandeling van pijn bij zowel patiënten met kanker (in de curatieve én de palliatieve fase) als bij patiënten met COPD of hartfalen.
Voor de evidence-based (herzieningen van) modules zijn de aanbevelingen voorzien van een gradering met cijfers en letters om de verhouding tussen de sterkte van de aanbeveling en de kwaliteit van de evidence weer te geven (zie onderstaande tabel). Deze werkwijze is gebaseerd op de methodiek zoals voorgesteld door de GRADE working group (zie http://www.gradeworkinggroup.org).
|
Gradering van aanbevelingen |
|
|
Sterkte van de aanbeveling |
Cijfer |
|
Sterke aanbeveling |
1 |
|
Zwakke aanbeveling |
2 |
|
Kwaliteit van de evidence |
Letter |
|
Hoog |
A |
|
Matig |
B |
|
Laag |
C |
|
Zeer laag |
D |
De richtlijnteksten die gebaseerd zijn op uitgangsvragen, zijn opgebouwd volgens het volgende vaste stramien: uitgangsvraag en aanbevelingen, literatuur, conclusies, overwegingen en referenties. De evidence tabellen staan bij de desbetreffende modules. De antwoorden op de uitgangsvragen (derhalve de aanbevelingen in deze richtlijn) zijn voor zover mogelijk gebaseerd op gepubliceerd wetenschappelijk onderzoek.
De uitgangsvragen zijn óf evidence-based (via de GRADE methodiek) óf consensus-based (zonder systematisch literatuuronderzoek) uitgewerkt.
De GRADE-methodiek
Selectie
Naast de selectie van studies op relevantie werd tevens geselecteerd op bewijskracht. Hiervoor werd gebruik gemaakt van de volgende hiërarchische indeling van studiedesigns gebaseerd op bewijskracht:
- Gerandomiseerde gecontroleerde studies (RCT's)
- Niet gerandomiseerde gecontroleerde studies (CCT's)
Waar deze niet voorhanden waren werd verder gezocht naar vergelijkend cohortonderzoek.
Critical appraisal
De kwaliteit van bewijs wordt weergegeven in vier categorieën: hoog, matig, laag en zeer laag. RCT's starten hoog en observationele studies starten laag. Vijf factoren verlagen de kwaliteit van de evidentie (beperkingen in onderzoeksopzet, inconsistentie, indirectheid, imprecisie, publicatie bias) en drie factoren kunnen de kwaliteit van de evidentie verhogen (sterke associatie, dosis-respons relatie, plausibele (residuele) confounding) (zie tabel 1).
Tabel 1. GRADE-methodiek voor het graderen van bewijs
|
Quality of evidence |
Study design |
Lower if * |
Higher if * |
|
High (4) |
Randomized trial |
Study limitations -1 Serious -2 Very serious Inconsistency -1 Serious -2 Very serious Indirectness -1 Serious -2 Very serious Imprecision -1 Serious -2 Very serious Publication bias -1 Likely -2 Very likely |
Large effect + 1 Large + 2 Very large Dose response + 1 Evidence of a gradient All plausible confounding + 1 Would reduce a demonstrated effect, or + 1 Would suggest a spurious effect when results show no effect |
|
Moderate (3) |
|
||
|
Low (2)
|
Observational study |
||
|
Very low (1) |
|
Algehele kwaliteit van bewijs
Omdat het beoordelen van de kwaliteit van bewijs in de GRADE-benadering per uitkomstmaat geschiedt, is er behoefte aan het bepalen van de algehele kwaliteit van bewijs. Zowel voor als na het literatuuronderzoek wordt door de richtlijnwerkgroep bepaald welke uitkomstmaten cruciaal, belangrijk en niet belangrijk zijn.
Het niveau van de algehele kwaliteit van bewijs wordt in principe bepaald door de cruciale uitkomstmaat met de laagste kwaliteit van bewijs. Als echter de kwaliteit van het bewijs verschilt tussen de verschillende cruciale uitkomstmaten zijn er twee opties:
- De uitkomstmaten wijzen in verschillende richtingen (zowel gewenst als ongewenste effecten) of de balans tussen gewenste en ongewenste effecten is onduidelijk, dan bepaalt de laagste kwaliteit van bewijs van de cruciale uitkomstmaten de algehele kwaliteit van bewijs;
- De uitkomstmaten in dezelfde richting wijzen (richting gewenst of richting ongewenst effecten), dan bepaalt de hoogste kwaliteit van bewijs van de cruciale uitkomstmaat dat op zichzelf voldoende is om de interventie aan te bevelen de algehele kwaliteit van bewijs.
Tabel 2. Formulering conclusies op basis van kwaliteit van bewijs per uitkomstmaat
|
Kwaliteit van bewijs |
Interpretatie |
Formulering conclusie |
|
Hoog |
Er is veel vertrouwen dat het werkelijk effect dicht in de buurt ligt van de schatting van het effect. |
Er is bewijs van hoge kwaliteit dat...
(Referenties) |
|
Matig |
Er is matig vertrouwen in de schatting van het effect: het werkelijk effect ligt waarschijnlijk dicht bij de schatting van het effect, maar er is een mogelijkheid dat het hier substantieel van afwijkt. |
Er is bewijs van matige kwaliteit dat...
(Referenties) |
|
Laag |
Er is beperkt vertrouwen in de schatting van het effect: het werkelijke effect kan substantieel verschillend zijn van de schatting van het effect. |
Er is bewijs van lage kwaliteit dat....
(Referenties) |
|
Zeer laag |
Er is weinig vertrouwen in de schatting van het effect: het werkelijke effect wijkt waarschijnlijk substantieel af van de schatting van het effect. |
Er is bewijs van zeer lage kwaliteit dat....
(Referenties) |
|
Formulering algehele kwaliteit van bewijs: hoog/matig/laag/zeer laag |
||
Methode voor het formuleren van ‘Overwegingen’
Naast de evidence uit de literatuur (conclusies) zijn er andere overwegingen die meespelen bij het formuleren van de aanbeveling. Deze aspecten worden besproken onder het kopje ‘Overwegingen' in de richtlijntekst. Hierin worden de conclusies (op basis van de literatuur) geplaatst in de context van de dagelijkse praktijk en vindt een afweging plaats van de voor- en nadelen van de verschillende beleidsopties. De uiteindelijk geformuleerde aanbeveling is het resultaat van de conclusie(s) in combinatie met deze overwegingen.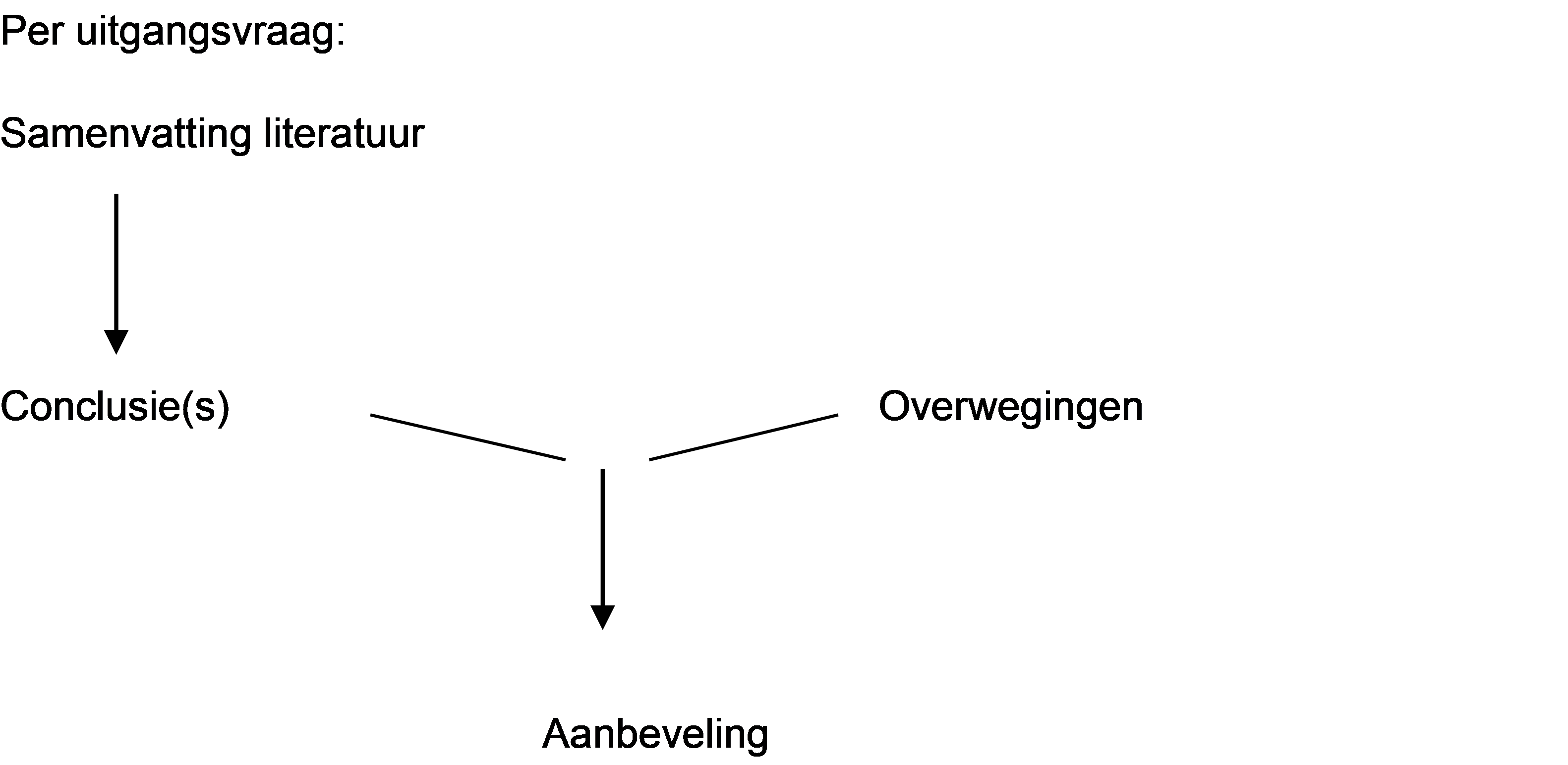
Figuur 1. Van bewijs naar aanbeveling
Bij het schrijven van de overwegingen zijn onderstaande zaken in acht genomen.
- Kwaliteit van het bewijs
Hoe hoger de algehele kwaliteit van het bewijs, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. - Balans van gewenste en ongewenste effecten
Hoe groter het verschil is tussen de gewenste en ongewenste effecten, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. Hoe kleiner dit verschil of hoe meer onzekerheid over de grootte van het verschil, des te waarschijnlijker wordt het formuleren van een conditionele aanbeveling.
Toelichting: - Patiëntenperspectief
Hoe groter de uniformiteit in waarden en voorkeuren van patiënten bij het afwegen van de voor- en nadelen van een interventie, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. - Professioneel perspectief
Hoe groter de uniformiteit in waarden en voorkeuren van professionals ten aanzien van de toepasbaarheid van een interventie, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling.
Toelichting:
- Kennis en ervaring met technieken/therapieën.
- Risico’s die professional loopt bij het toepassen van de interventie.
- Verwachte tijdbesparing.
- Verlies aan tijd door het invoeren van de interventie.
N.B.: de hierna volgende factoren (5, 6 en 7) alleen evalueren als een positief geformuleerde aanbeveling wordt overwogen! Een positief geformuleerde aanbeveling is een aanbeveling waarbij een bepaalde interventie wel ‘dient’ plaats te vinden (sterk) of wel ‘kan worden overwogen’ (zwak/conditioneel). Als dat daarentegen juist niet het geval is, is sprake van een negatief geformuleerde aanbeveling.
- Middelenbeslag
Hoe minder middelen er worden gebruikt (m.a.w. hoe lager de kosten van een interventie zijn vergeleken met de beschouwde alternatieven en andere kosten gerelateerd aan de interventie), des te waarschijnlijker wordt het formuleren van een sterke aanbeveling. Hoe meer onzekerheid over het middelenbeslag, des te waarschijnlijker wordt een conditionele aanbeveling. - Organisatie van zorg
Hoe meer onzekerheid of de geëvalueerde interventie daadwerkelijk op landelijke schaal toepasbaar is, des te waarschijnlijker wordt het formuleren van een conditionele aanbeveling.
Toelichting: - Maatschappelijk perspectief
(Juridische overwegingen/ethische overwegingen/industriële belangen/vergoeding door verzekeraars/politieke en strategische consequenties)
Hoe groter de onzekerheid hierover is, des te waarschijnlijker wordt het formuleren van een conditionele aanbeveling.
Toelichting:
- Indien twee behandelingen even effectief zijn waarvan één behandeling wordt vergoed, zal deze laatste behandeling mogelijk de voorkeur hebben.
Methode voor het formuleren van aanbevelingen
GRADE kent twee soorten aanbevelingen: sterke aanbevelingen of conditionele (zwakke) aanbevelingen. De sterkte van aanbevelingen reflecteert de mate van vertrouwen waarin – voor de groep patiënten waarvoor de aanbevelingen zijn bedoeld - de gewenste effecten opwegen tegen de ongewenste effecten.
Formulering:
- Sterke aanbevelingen: Doe/geef etc. (of er dient…. te worden gegeven/gedaan)
- Zwakke/conditionele aanbevelingen: Overweeg….. te geven/te doen.
Consensus-based methodiek
Naast de evidence-based uitwerking (GRADE) zijn er ook uitgangsvragen via de consensus-based methodiek uitgewerkt. Hierbij zijn de richtlijnteksten ook gebaseerd op evidence, maar is er geen systematisch literatuuronderzoek gedaan en zijn de gevonden studies niet methodologisch beoordeeld.
