Chirurgie bij pijn bij kanker
Uitgangsvraag
Wat is het effect van chirurgie op pijn bij patiënten met kanker?
Aanbeveling
- Bespreek bij pijn ten gevolge van primaire tumoren (of een lokaal recidief daarvan) is het raadzaam multidisciplinair of een operatieve ingreep zinvol en/of oncologisch wenselijk is, al dan niet in combinatie met chemotherapie en/of radiotherapie. Een operatieve ingreep kan zowel met een curatieve als met een palliatieve intentie worden verricht.
- Overweeg een percutane radiofrequente ablatie bij patiënten met pijnlijke botmetastasen die niet reageren op eerdere behandelingen, waaronder radiotherapie. Dit dient bij voorkeur te geschieden in een gespecialiseerd centrum.
- Voor de behandeling van pijnlijke wervelmetastasen: zie de richtlijn Wervelmetastasen (2015).
- Verricht een stabiliserende osteosynthes bij patiënten met pijnlijke fracturen in lange pijpbeenderen ten gevolge van kanker is een stabiliserende osteosynthese aangewezen. Overweeg een profylactische osteosynthese bij patiënten met pijnlijke niet-gefractureerde botlaesies met een geschat hoog risico op een fractuur. Voorwaarde voor beide indicaties is dat er een levensverwachting is van langer dan een maand.
- Overweeg een operatieve ingreep bij patiënten met pijnlijke metastasen in huid of subcutis.
Overwegingen
Primaire tumor
In het algemeen moet bij een chirurgische ingreep bij patiënten met kanker en pijn een afweging worden gemaakt van de voor- en nadelen van chirurgie in relatie tot de kansen op een zinvol effect (curatie of palliatie), de belasting en de gevolgen van de ingreep en de mogelijke alternatieven (radiotherapie, chemotherapie of een combinatie hiervan). Bij pijn ten gevolge van primaire tumoren die ingroeien in omliggend weefsel en/of organen, is meestal een combinatiebehandeling met chemotherapie en radiotherapie aangewezen om de kans op lokale controle zo groot mogelijk te maken. Enkele voorbeelden zijn het locally advanced mammacarcinoom en rectumcarcinoom. Tevens is een verschuiving gaande naar zo mogelijk ‘orgaansparende’ behandelingen, met als doel de morbiditeit van de diverse behandelingen zo veel mogelijk te beperken (bijvoorbeeld ‘locally advanced’ hoofd-halstumoren (Lefebvre, 2006) en cervixtumoren (Eifel, 2006)). Een andere benadering is bijvoorbeeld de geïsoleerde regionale perfusie met tumornecrosefactor-alfa (TNF-α) bij wekedelentumoren in extremiteiten, waarbij mogelijk een amputatie van een ledemaat kan worden voorkomen (Eggermont, 1996; Grunhagen, 2006). Vanwege het multidisciplinaire karakter van de behandelingen is het wenselijk dat de keuze tot behandelen in een multidisciplinaire setting wordt gemaakt.
Metastasen
Botmetastasen in wervels
Omdat bij pijn ten gevolge van wervelmetastasen uit prospectief gerandomiseerde onderzoeken blijkt dat uitwendige radiotherapie een zinvolle afname van pijn kan bewerkstelligen (Van der Linden, 2005), is de werkgroep van mening dat over het algemeen een laminectomie of uitgebreidere chirurgie alleen meerwaarde heeft boven radiotherapie en te overwegen is bij (De Graeff, 2006):
- patiënten met neurologische uitval (met name bij instabiliteit van de wervel en/of compressie van het myelum door een wervelfragment) en/of een ingezakte wervel, een goede prognose (minimaal drie tot zes maanden) en een goede performancestatus;
- patiënten met neurologische uitval die tijdens radiotherapie en voldoende hoge doses dexamethason een verslechterend neurologisch beeld laten zien;
- patiënten met pijn die eerder zijn behandeld met in opzet curatieve of palliatieve radiotherapie die tot het maximum gegeven is vanwege bereikte radiatietolerantie van het myelum.
Uit de praktijk blijkt dat slechts een klein deel van de patiënten in aanmerking komt voor een uitgebreide operatieve ingreep. Een dergelijke ingreep moet alleen worden verricht door een (orthopedisch of neuro)chirurg met ervaring op dit gebied.
Botmetastasen in lange pijpbeenderen (femur, humerus)
Het is moeilijk bij pijnlijke ‘impending lesions’ in lange pijpbeenderen een reële inschatting te maken van het korte termijnrisico op het ontwikkelen van een pathologische fractuur. Hoewel een praktische overweging zou zijn om alle impending lesions te opereren, is dit in de praktijk niet haalbaar en niet wenselijk in een patiëntengroep met een over het algemeen beperkte levensverwachting. Een profylactische osteosynthese gaat immers gepaard met een zeker percentage postoperatieve morbiditeit en ook mortaliteit. In de literatuur is een groot aantal risicofactoren voor fracturering bekend, veelal gebaseerd op retrospectieve gegevens van patiënten met al gefractureerde botmetastasen (Van der Linden, 2004). Voor femurmetastasen blijkt vooralsnog uit prospectief onderzoek de mate van axiale corticale aantasting (>30 mm) de meest objectieve voorspellende risicofactor voor het ontstaan van een pathologische fractuur (Van der Linden, 2003; Van der Linden, 2004). De werkgroep is daarom van mening dat bij een laag risico kortdurende radiotherapie kan worden gegeven voor pijn. Bij een hoog risico moet profylactische osteosynthese worden overwogen. Indien de patiënt inoperabel is ten gevolge van comorbiditeit, is radiotherapie met een hogere dosis aangewezen om remineralisatie te induceren (Koswig, 1999). Ook een concomitante systemische behandeling met bisfosfonaten is te overwegen bij patiënten met botmetastasen ten gevolge van een mammacarcinoom, prostaatcarcinoom of de ziekte van Kahler.
Onderbouwing
Achtergrond
Het verrichten van een operatieve ingreep kan bij patiënten met kanker en pijn een verbetering geven van de aanwezige pijnklachten of zelfs leiden tot het verdwijnen ervan. Een onderverdeling valt te maken tussen ingrepen met betrekking tot de primaire tumor (of een lokaal recidief daarvan) en eventuele metastasen.
Primaire tumor
In de praktijk blijkt er een aantal indicaties te onderscheiden, waarbij de behandeling van de primaire tumor (of een lokaal recidief daarvan) zowel curatief als palliatief van opzet kan zijn:
- resectie van primaire tumoren (of een lokaal recidief daarvan) die lokale pijn veroorzaken. Te denken valt aan bijvoorbeeld wekedelentumoren of botsarcomen, hoofdhalstumoren, intra-abdominale of retroperitoneale tumoren zoals gastro-intestinale tumoren, het niercelcarcinoom of gynaecologische tumoren;
- aanleggen van een ontlastend stoma bij obstructie van een orgaan ten gevolge van tumoringroei, bijvoorbeeld bij darmtumoren (colostoma) of blaastumoren (urostoma);
- aanleggen van een bypass ter bevordering van de darmpassage, bijvoorbeeld bij obstructie van de darm ten gevolge van tumoringroei.
Metastasen
Operatieve ingrepen die in de Nederlandse ziekenhuizen momenteel worden verricht bij metastasen voor de behandeling van pijn, zijn onder te verdelen naar de lokalisatie in het lichaam:
- botmetastasen in wervels;
- botmetastasen in lange pijpbeenderen (femur, humerus);
- metastasen in huid of subcutis.
Conclusies / Summary of Findings
Algemeen
Primaire tumor
Er zijn aanwijzingen dat een operatieve ingreep, bijvoorbeeld resectie van de primaire tumor (of een lokaal recidief daarvan), afname van pijn kan bewerkstelligen bij colorectale carcinomen en het prostaatcarcinoom (niveau 3).
(C: Kamat 2003, Verrees 1996, Yeung 1993)
De werkgroep is van mening dat het aanleggen van een (uro- of colo-) stoma of gastro-intestinale bypass afname van pijn kan bewerkstelligen (niveau 4).
(D: Werkgroep)
Metastasen
Er zijn aanwijzingen dat een percutane radiofrequente ablatie leidt tot afname van pijn bij patiënten met botmetastasen (niveau 3).
(C: Goetz 2004)
Botmetastasen in wervels
Er zijn aanwijzingen dat een laminectomie of een wervelresectie met reconstructie leidt tot afname van rugpijn bij patiënten met wervelmetastasen (niveau 3).
(B: Patchell 2005)
(C: Atanasiu 1993, Bilsky 2000, Colak 2004, Fourney 2001, Fourney 2003, Gerszten 2005, Golaskan 1998, Holman 2005, Jackson 2001, Schoeggl 2002, Wang, 2004)
Botmetastasen in lange pijpbeenderen (femur, humerus)
Er zijn aanwijzingen dat een chirurgische stabilisatie van een pathologische fractuur in femur of humerus een vrijwel directe afname van pijn en herstel van mobiliteit geeft (niveau 3).
(C: Algan 1996, Ampil 2001, Assal 2000, Athwal 2005, Bickels 2005, Dijkstra 1994, Talbot 2005, Ward 2003)
Er zijn aanwijzingen dat een chirurgische stabilisatie van een ‘impending lesion’ in femur of humerus het optreden van een pathologische fractuur voorkomt (niveau 3).
Metastasen in huid of subcutis
De werkgroep is van mening dat bij patiënten met pijnlijke metastasen in huid of subcutis een operatieve ingreep afname van pijn kan geven (niveau 4).
(D: Werkgroep)
(C: Dijkstra 1994)
Samenvatting literatuur
Primaire tumor
Een artikel uit 1996 naar re-resectie voor recidief van rectumcarcinoom vermeldde afname van pijnklachten bij acht van in totaal negen patiënten (Verrees, 1996). Yeung rapporteerde over een totale exenteratie bij recidief en locally advanced colorectale tumoren: 29 van 30 patiënten die met een curatieve intentie werden geopereerd hadden afname van pijn, en 13 van 20 patiënten die met een palliatieve intentie werden geopereerd (Yeung, 1993). Bij 14 patiënten met recidief van prostaatcarcinoom die een totale exenteratie ondergingen, werd in 79% van de gevallen een complete pijnreductie gerapporteerd (Kamat, 2003). Een Cochranereview over chirurgie bij maligne darmobstructie bij gynaecologische en gastro-intestinale tumoren rapporteerde over 24 retrospectieve onderzoeken en één prospectief onderzoek (Feuer, 2000). Alle onderzoeken waren van matige methodologische kwaliteit. Er werd een veelvoud van definities over symptoomcontrole gehanteerd, waaronder ook pijn. Er kon geen eenduidige conclusie worden geformuleerd anders dan de noodzaak tot het ontwikkelen van gevalideerde meetinstrumenten voor symptoomcontrole en het verrichten van gerandomiseerde onderzoeken.
Metastasen
Operatieve ingrepen bij andere, minder vaak voorkomende lokalisaties, bijvoorbeeld uitgebreide botaantasting van het acetabulum of bekken met oncontroleerbare pijn ondanks uitwendige radiotherapie, worden sporadisch uitgevoerd en bij voorkeur in gespecialiseerde centra (Wunder, 2003). In een review uit 2006 (Callstrom, 2006) worden andere gespecialiseerde ingrepen voor pijnlijke botmetastasen besproken, zoals de percutane cryoablatie, waarbij met behulp van argongas snelle koeling tot min 100 °C wordt bereikt, en de percutane radiofrequente ablatie, waarbij met een hoogfrequente bron via een naald een elektrode wordt ingebracht in weefsel, resulterend in hitte en necrose. In een prospectief onderzoek werd met percutane radiofrequente ablatie een respons van 95% gemeld bij patiënten die niet respondeerden op onder meer eerdere radiotherapie (Goetz, 2004).
Botmetastasen in wervels
In de literatuur is één prospectief gerandomiseerd onderzoek verschenen waarin 151 patiënten met klinische en/of radiologische myelumcompressie werden gerandomiseerd tussen chirurgie gevolgd door radiotherapie of radiotherapie alleen (Patchell, 2005). Het betrof meestal een uitgebreide chirurgische ingreep. Inname van analgetica was een secundair eindpunt in dit onderzoek. Naast een significant verbeterde mobiliteit was de mediane morfine-inname significant minder in de gecombineerde arm (0,4 mg (0 tot 60 mg) ten opzichte van 4,8 mg (0 tot 200 mg), p=0,002). Bij dit onderzoek zijn enkele methodologische bedenkingen aan te voeren, onder meer dat dit een geselecteerde groep patiënten betreft. Elf retrospectieve onderzoeken en één prospectief, niet- gerandomiseed onderzoek naar de effectiviteit van de verschillende chirurgische technieken rapporteerden allemaal verbetering van pijn bij het merendeel van de patiënten (Atanasiu, 1993; Bilsky, 2000; Colak, 2004; Fourney, 2001; Fourney, 2003; Gerszten, 2005; Golaskan, 1998; Holman, 2005; Jackson, 2001; Schoeggl, 2002; Wang, 2004).
Zoeken en selecteren
Primaire tumor
Er zijn in de literatuur geen prospectief gerandomiseerde onderzoeken met als primair of secundair eindpunt het effect van een operatieve ingreep op pijn bij patiënten met kanker ten gevolge van de primaire tumor (of een lokaal recidief daarvan). Wel verschenen er diverse retrospectieve onderzoeken.
Metastasen
-
Referenties
- Algan S, Horowitz S. Surgical treatment of pathological hip lesion in patients with metastatic disease. Clin Orthop Relat Res 1996;332:223-31.
- Ampil F, Sadasivan K. Prophylactic and therapeutic fixation of weight-bearing long bones with metastatic cancer. South Med J 2001;94:394-6.
- Assal M, Zanone X. Osteosynthesis of metastatic lesions of the proximal femur with a solid femoral nail and interlocking spiral blade inserted without reaming. J Orthop Trauma 2000;14:394-7.
- Atanasiu J, Badatcheff F. Metastatic lesions of the cervical spine. A retrospective analysis of 20 cases. Spine 1993;18:1279-84.
- Athwal G, Chin P. Coonrad-Morrey total elbow arthorplasty for tumours of the distal humerus and elbow. J Bone Joint Surg Br 2005;87:1369-74.
- Barr J, Barr M. Percutaneous vertebroplasty for pain relief and spinal stabilization. Spine 2000;25:923-8.
- Bickels J, Kollender Y. Function after resection of humeral metastases:analysis of 59 consecutive patients. Clin Orthop Relat Res 2005;437:201-8.
- Bilsky M, Boland P. Single-stage posterolateral transpedicle approach for spondylectomy, epidural decompression, and circumferential fusion of spinal metastases. Spine 2000;25:2240-9.
- Callstrom MR, Charboneau JW, Goetz MP. Image-guided ablation of painful metastatic bone tumors: a new and effective approach to a difficult problem. Skeletal Radiol 2006;35:1-15.
- Cheung G, Chow E. Percutaneous vertebroplasty in patients with intractable pain from osteoporotic or metastatic fractures: A prospective study using quality-of-life assessment. Can Assoc Radiol J 2006;57:13-21.
- Colak A, Kutlay M. Two-staged operation on C2 neoplastic lesions: anterior excision and posterior stabilisation. Neurosurg Rev 2004;27:189-93.
- Dijkstra S, Wiggers T, Geel BN van, et al. Impending and actual pathological fractures in patients with bone metastases of the long bones. A retrospective study of 233 surgically treated fractures. Eur J Surg 1994;160:535-42.
- Eifel PJ. Chemoradiotherapy in the treatment of cervical cancer. Semin Radiat Oncol 2006;16:177-85.
- Eggermont A, Schraffordt Koops H. Isolated limb perfusion with high-dose tumor necrosis factor-alpha in combi- nation with interferon-gamma and melphalan for non-resectable extremity soft tissue sarcomas; a multicentre trial. J Clin Oncol 1996;14:2653-65.
- Feuer D, Broadley K. Surgery for the resolution of symptoms in malignant bowel obstruction in advanced gynaeco-logical and gastrointestinal cancer. Cochrane Database of Systematic Reviews 2000, issue 3, Art.No: CD002764. DOI:10.1002/14651858. CD002764.
- Fourney D, Schomer D. Percutaneous vertebroplasty and kyphoplasty for painful vertebral body fractures in cancer patients. J Neurosurg 2003;98(1 Suppl):21-30.
- Fourney D, Bi-Said D. Use of pedicle screw fixation in the management of malignant spinal disease: experience in 100 consecutive procedures. J Neurosurg 2001;94(1 Suppl):25-37.
- Fourney D, York J. Management of atlantoaxial metastases with posterior occipitocervical stabilization. J Neurosurg 2003;98(2 Suppl):165-70.
- Frankel HL, Hancock DO, Hyslop G, et al. The value of postual reduction in the initial management of closed injuries of the spine with paraplegia and tetraplegia. Paraplegia 1969;7:179-92.
- Gerszten P, Germanwala A. Combination kyphoplasty and spinal radiosurgery: a new treatment paradigm for pathological fractures. J Neurosurg Spine 2005;3:296-301.
- Goetz MP, Callstrom MR, Charboneau JW. Percutaneous image-guided radiofrequency ablation of painful metastases involving bone: a multicenter study. J Clin Oncol 2004;22:300-6.
- Golaskan Z, York J. Transthoracic vertebrectomy for metastatic spinal tumors. J Neurosurg 1998;89:599-609.
- Graeff A de, Taphoorn MJB, Lindeman E, et al. Richtlijn dwarslaesie. In: Graeff A de, Hesselmann GM, Krol RJA, et al (red). Palliatieve zorg: richtlijnen voor de praktijk. Utrecht: VIKC, januari 2006:235-51.
- Grunhagen D, Wilt J de. Technology Insight: utility of TNF-based isolated limb perfusion to avoid amputation of irresectable tumors of the extremities. Nature Clin Practice Oncol 2006;3:94-103.
- Harrington KD. Metastatic disease of the spine. J Bone Joint Surg Am 1986;68:1110-5.
- Holman P, Suki D. Surgical management of metastatic disease if the lumbar spine: experience with 139 patients. J Neurosurg Spine 2005;2:550-63. Jackson R, Loh S. Metastatic renal cell carcinoma of the spine: surgical treatment and results. J Neurosurg 2001;94(1 Suppl):18-24.
- Kamat A, Huang S. Total pelvic exenteration: effective palliation of perineal pain in patients with locally recurrent prostate cancer. J Urol 2003;170:1868-71.
- Kose KC, Cabesoy O, Akan B, et al. Functional results of vertebral augmentation techniques in pathological vertebral fractures of myelomatous patients. J Natl Med Assoc 2006;98:1654-8.
- Koswig S, Budach V. [Remineralization and pain relief in bone metastases after different radiotherapy fractions (10 times 3 Gy vs. 1 time 8 Gy). A prospective study]. Strahlenther Onkol 1999;175:500-8.
- Lefebvre JL. Laryngeal preservation in head and neck cancer: multidisciplinary approach. Lancet Oncol 2006;7:747-55.
- Linden YM van der, Dijkstra PDS, Vonk EJA, et al. Prediction of survival in patients with metastases in the spinal column. Cancer 2005;103:320-8.
- Linden YM van der, Dijkstra PD, Kroon HM, et al. Comparative analysis of risk factors for pathological fracture with femoral metastases. Results based on a randomised trial of radiotherapy. J Bone Joint Surg Br 2004;86B:5665-73.
- Linden YM van der, Kroon HM, Dijkstra PD, et al. Simple radiographic parameter predicts fracturing in metastatic femoral bone lesions: results from a randomized trial. Radiother Oncol 2003;69:21-31.
- Patchell R, Tibbs PA, Regine WF, et al. Direct decompressive surgical resection in the treatment of spinal cord compression caused by metastatic cancer: a randomised trial. Lancet 2005;366:643-8.
- Schoeggl A, Reddy M. Neurological outcome following laminectomy in spinal metastases. Spinal Cord 2002;40:363-6.
- Talbot M, Turcotte R. Function and health status in surgically treated bone metastases. Clin Orthop Relat Res 2005;438:215-20.
- Taylor RS, Taylor RJ. Balloon kyphoplasty and vertebroplasty for vertebral compression fractures: a comparative systematic review of efficacy and safety. Spine 2006;31:2747-55.
- Verrees J, Fernandez-Trigo V. Rectal cancer recurrence after prior resection and radiotherapy: palliation following additional surgery. Int J Colorectal Dis 1996;11:211-6.
- Wang J, Boland P. Single-stage posterolateral transpedicular approach for resection of epidural metastatic spine tumors involving the vertebral body with circumferential reconstruction: results in 140 patients. J Neurosurg Spine 2004;1:287-98.
- Ward W, Holsenbeck S. Metastatic disease of the femur: surgical treatment. Clin Orthop Relat Res 2003; 415(Suppl):S230-44.
- Weill A, Chiras J, Simon JM, et al. Spinal metastases: indications for and results of percutaneous injection of acrylic surgical cement. Radiology 1996;199:241-7.
- Wunder J, Ferguson P. Acetabular metastases: planning for reconstruction and review of results. Clin Orthop Relat Res 2003;415(Suppl):S187-97.
- Yeung R, Moffat F. Pelvic exenteration for recurrent and extensive primary colorectal adenocarcinoma. Cancer 1993;15:1853-8.
Verantwoording
Beoordelingsdatum en geldigheid
Laatst beoordeeld : 01-11-2023
Actualisatie
Deze richtlijn is goedgekeurd op 6 december 2019. De Nederlandse Vereniging voor Anesthesiologie (NVA) bewaakt samen met betrokken verenigingen de houdbaarheid van deze (modules van de) richtlijn. Zo nodig zal de richtlijn tussentijds op onderdelen worden bijgesteld. De geldigheidstermijn van de richtlijn is maximaal 5 jaar na vaststelling. Indien de richtlijn dan nog actueel wordt bevonden, wordt de geldigheidsduur van de richtlijn verlengd.
Houderschap richtlijn
De houder van de richtlijn (NVA) moet kunnen aantonen dat de richtlijn zorgvuldig en met de vereiste deskundigheid tot stand is gekomen.
IKNL draagt zorg voor het beheer en de ontsluiting van de richtlijn.
Juridische betekenis van richtlijnen
Een richtlijn is een kwaliteitsstandaard. Een kwaliteitsstandaard beschrijft wat goede zorg is, ongeacht de financieringsbron (Zorgverzekeringswet (Zvw), Wet langdurige zorg (Wlz), Wet maatschappelijke ondersteuning (Wmo), aanvullende verzekering of eigen betaling door de cliënt/patiënt). Opname van een kwaliteitsstandaard in het Register van Zorginstituut Nederland betekent dus niet noodzakelijkerwijs dat de in de kwaliteitsstandaard beschreven zorg verzekerde zorg is.
De richtlijn bevat aanbevelingen van algemene aard. Het is mogelijk dat deze aanbevelingen in een individueel geval niet van toepassing zijn. Er kunnen zich feiten of omstandigheden voordoen waardoor het wenselijk is dat in het belang van de patiënt van de richtlijn wordt afgeweken. Wanneer van de richtlijn wordt afgeweken, dient dit beargumenteerd gedocumenteerd te worden. De toepassing van de richtlijnen in de praktijk is de verantwoordelijkheid van de behandelende arts.
Algemene gegevens
Autoriserende/instemmende en bij de werkgroep betrokken verenigingen:
- Nederlandse Internisten Vereniging
- Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose
- Nederlandse Vereniging voor Anesthesiologie
- Nederlandse Vereniging voor Klinische Geriatrie
- Nederlandse Vereniging voor Neurologie
- Vereniging voor Specialisten Ouderengeneeskunde
- Verpleegkundigen en Verzorgenden Nederland
- Nederlandse Vereniging van Ziekenhuisapothekers
- Nederlandse vereniging voor professionele palliatieve zorg
Financiering
Deze richtlijn c.q. module is gefinancierd door IKNL. De inhoud van de richtlijn c.q. module is niet beïnvloed door de financierende instantie.
Procesbegeleiding
IKNL (Integraal Kankercentrum Nederland) is het kennis- en kwaliteitsinstituut voor professionals en bestuurders in de oncologische en palliatieve zorg dat zich richt op het continu verbeteren van de oncologische en palliatieve zorg.
IKNL benadert preventie, diagnose, behandeling, nazorg en palliatieve zorg als een keten waarin de patiënt centraal staat. Om kwalitatief goede zorg te waarborgen ontwikkelt IKNL producten en diensten ter verbetering van de oncologische zorg, de nazorg en de palliatieve zorg, zowel voor de inhoud als de organisatie van de zorg binnen en tussen instellingen. Daarnaast draagt IKNL nationaal en internationaal bij aan de beleidsvorming op het gebied van oncologische en palliatieve zorg.
IKNL rekent het (begeleiden van) ontwikkelen, implementeren en evalueren van multidisciplinaire, evidence-based richtlijnen voor de oncologische en palliatieve zorg tot een van haar primaire taken. IKNL werkt hierbij conform de daarvoor geldende (inter)nationale kwaliteitscriteria. Bij ontwikkeling gaat het in toenemende mate om onderhoud (modulaire revisies) van reeds bestaande richtlijnen.
Doel en doelgroep
Doel
Een richtlijn geeft aanbevelingen ter ondersteuning van de belangrijkste knelpunten uit de dagelijkse praktijk. Deze richtlijn is zoveel mogelijk gebaseerd op wetenschappelijk onderzoek en consensus. De richtlijn 'Pijn’ geeft aanbevelingen over begeleiding en behandeling van patiënten met pijn bij kanker (zowel in de curatieve als de palliatieve fase) en beoogt hiermee de kwaliteit van de zorgverlening te verbeteren.
Hoewel de evidentie alleen is verzameld voor de diagnostiek en behandeling van pijn bij patiënten met kanker zijn de aanbevelingen ook grotendeels van toepassing voor patiënten met andere levensbedreigende aandoeningen.
Doelgroep
Deze richtlijn is bestemd voor alle professionals die betrokken zijn bij de zorg voor patiënten met pijn zoals huisartsen, specialisten ouderengeneeskunde, medisch specialisten, apothekers, verpleegkundigen, verzorgenden, verpleegkundig specialisten, physician assistants, fysiotherapeuten, medisch maatschappelijk werkers, geestelijk verzorgers, GZ- en klinisch psychologen.
Indien in de richtlijn wordt gesproken over zorgverleners rondom de patiënt met pijn, worden, afhankelijk van de specifieke situatie van de patiënt, alle bovengenoemde professionals bedoeld.
De richtlijn is ook relevant voor zorgverleners van andere disciplines en vrijwilligers die werkzaam zijn in de palliatieve fase. De multidimensionele benadering van de patiënt in de palliatieve fase vergt immers een gezamenlijke, interdisciplinaire verantwoordelijkheid, zoals ook in het Kwaliteitskader palliatieve zorg Nederland is beschreven.
Samenstelling werkgroep
Alle werkgroepleden en klankbordleden zijn afgevaardigd namens wetenschappelijke, beroeps- en patiëntenverenigingen en hebben daarmee het mandaat voor hun inbreng. Bij de samenstelling van de werkgroep is geprobeerd rekening te houden met landelijke spreiding, inbreng van betrokkenen uit zowel academische als algemene ziekenhuizen/instellingen en vertegenwoordiging van de verschillende verenigingen/disciplines.
Het patiëntenperspectief is vertegenwoordigd door Patiëntenfederatie Nederland.
Bij de uitvoering van het evidence-based literatuuronderzoek is de kaderopleiding Palliatieve Zorg en een literatuuronderzoeker van IKNL en de voorzitter van de richtlijnwerkgroep betrokken geweest.
Werkgroepleden
- Mw. prof. dr. M.H.J. van den Beuken-van Everdingen, internist, NIV
- Dhr. dr. M.J.M.M. Giezeman †, anesthesioloog, NVA
- Dhr. dr. A. de Graeff (voorzitter), internist-oncoloog en hospice-arts, Palliactief
- Mw. drs. H. Klaren, klinisch geriater, NVKG
- Mw. B. Kramp, verpleegkundig specialist, V&VN
- Dhr. drs. M. Martens, specialist ouderengeneeskunde en consulent palliatieve zorg, Verenso
- Mw. drs. M.J. Oortman, huisarts, SCEN-arts, palliatief consulent en hospice-arts, NHG
- Dhr. drs. P. Oosterhof, poliklinisch apotheker, NVZA
- Mw. prof.dr. A.K.L. Reyners, internist, NIV
- Mw. M. Schielke, verpleegkundig pijnspecialist, V&VN
- Mw. drs. M.C. Sieders, huisarts (waarnemend), SCEN-arts, palliatief consulent, NHG
- Dhr. dr. M.F.M. Wagemans, anesthesioloog, NVA
Klankbordleden
- Dhr. prof. dr. K.C.P. Vissers, anesthesioloog, NVA
- Mw. drs. L. Bellersen, cardioloog, NVVC
- Mw. drs. B.A. Brouwer, neuroloog/pijnspecialist NVN/pijnspecialist
- Mw. M. Geerts, verpleegkundig specialist, V&VN
- Dhr. drs. S.M. de Hosson, longarts, NVALT
- Mw. drs. S. Visser, apotheker, KNMP
- Mw. drs. R. Lammers, beleidsmedewerker, Patiëntenfederatie Nederland
Ondersteuning
- Mw. T.T.M. Bluemink-Holkenborg, secretaresse, IKNL
- Mw. drs. M.G. Gilsing, adviseur (richtlijnen) palliatieve zorg, IKNL
- Mw. dr. O.L. van der Hel, literatuuronderzoeker, IKNL
- Prof.dr. J Kleijnen, epidemioloog, literatuuronderzoeker MUMC Maastricht/York
- Mw. L.K. Liu, secretaresse, IKNL
- Dhr. dr. R. Vernooij (i.s.m. de kaderopleiding Palliatieve Zorg), literatuuronderzoeker, IKNL
Belangenverklaringen
Om de beïnvloeding van de richtlijnontwikkeling of formulering van de aanbevelingen door conflicterende belangen te minimaliseren zijn de leden van werkgroep gemandateerd door de wetenschappelijke en beroepsverenigingen.
Alle leden van de richtlijnwerkgroep hebben verklaard onafhankelijk gehandeld te hebben bij het opstellen van de richtlijn. Een onafhankelijkheidsverklaring ‘Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling' zoals vastgesteld door onder meer de KNAW, KNMG, Gezondheidsraad, CBO, NHG en Orde van Medisch Specialisten is door de werkgroepleden bij aanvang en bij afronding van het traject ingevuld. De bevindingen zijn schriftelijk vastgelegd in de belangenverklaring en opvraagbaar via info@iknl.nl.
Inbreng patiëntenperspectief
De input van patiëntvertegenwoordigers is nodig voor de ontwikkeling van kwalitatief goede richtlijnen. Goede zorg voldoet immers aan de wensen en eisen van zowel zorgverlener als patiënt. Patiëntenfederatie Nederland is in het gehele richtlijntraject meegenomen en heeft plaats gehad in de klankbordgroep (zie ook de Samenstelling van de werkgroep).
Tijdens de landelijke consultatiefase heeft Patiëntenfederatie Nederland commentaar gegeven op de conceptrichtlijn en patiënten/naasten geraadpleegd via een referentenpanel voor onderzoeksaanvragen op het gebied van palliatieve zorg. Ook heeft de Patiëntenfederatie Nederland - naast NFK, nog andere patiëntenorganisaties benaderd voor het leveren van commentaar.
Patiëntenfederatie Nederland heeft tot slot de richtlijn goedgekeurd.
Patiënteninformatie gebaseerd op de richtlijn is opgesteld en gepubliceerd op de daarvoor relevante sites (o.a. zie link https://www.kanker.nl/gevolgen-van-kanker/pijn/wat-is/pijn-bij-kanker#show-menu).
Methode ontwikkeling
Evidence based
Implementatie
Bevorderen van het toepassen van de richtlijn in de praktijk begint met een brede bekendmaking en verspreiding van de richtlijn.
Bij verdere implementatie gaat het om gerichte interventies om te bevorderen dat professionals de nieuwe kennis en kunde opnemen in hun routines van de zorgpraktijk, inclusief borging daarvan.
Als onderdeel van elke richtlijn stelt IKNL samen met de richtlijnwerkgroep een implementatieplan op en ondersteunt een aantal basis-activiteiten voor de implementatie. De verantwoordelijkheid voor verdere implementatie-activiteiten ligt bij de eigenaar van de richtlijn (en het veld).
Activiteiten en interventies voor verspreiding en implementatie kunnen zowel op landelijk als regionaal niveau plaatsvinden. Deze kunnen eventueel ook op maat gemaakt worden per instelling of specialisme.
Het implementatieplan bij deze richtlijn is een belangrijk hulpmiddel om effectief de aanbevelingen uit deze richtlijn te implementeren voor en door de verschillende disciplines.
Werkwijze
In de huidige richtlijn zijn de NVA-richtlijn van 2015 en de richtlijn 'Pijn' van Pallialine samengevoegd. Daarbij zijn de onderdelen van de NVA-richtlijn, die in 2015 niet zijn herzien (en waarbij de teksten van de NVA-versie van 2008 onveranderd zijn gehandhaafd) grotendeels evidence-based (op basis van aanvullend literatuuronderzoek) aangepast en aangevuld met evidence-based en consensus-based teksten over de diagnostiek en behandeling van pijn bij patiënten met gevorderde stadia van COPD of hartfalen. De onderdelen van de NVA-richtlijn die in 2015 zijn herzien zijn onveranderd overgenomen (zie ook de Algemene inleiding).
De bedoeling is om te komen tot een integrale en actuele richtlijn over de diagnostiek en behandeling van pijn bij zowel patiënten met kanker (in de curatieve én de palliatieve fase) als bij patiënten met COPD of hartfalen.
Voor de evidence-based (herzieningen van) modules zijn de aanbevelingen voorzien van een gradering met cijfers en letters om de verhouding tussen de sterkte van de aanbeveling en de kwaliteit van de evidence weer te geven (zie onderstaande tabel). Deze werkwijze is gebaseerd op de methodiek zoals voorgesteld door de GRADE working group (zie http://www.gradeworkinggroup.org).
|
Gradering van aanbevelingen |
|
|
Sterkte van de aanbeveling |
Cijfer |
|
Sterke aanbeveling |
1 |
|
Zwakke aanbeveling |
2 |
|
Kwaliteit van de evidence |
Letter |
|
Hoog |
A |
|
Matig |
B |
|
Laag |
C |
|
Zeer laag |
D |
De richtlijnteksten die gebaseerd zijn op uitgangsvragen, zijn opgebouwd volgens het volgende vaste stramien: uitgangsvraag en aanbevelingen, literatuur, conclusies, overwegingen en referenties. De evidence tabellen staan bij de desbetreffende modules. De antwoorden op de uitgangsvragen (derhalve de aanbevelingen in deze richtlijn) zijn voor zover mogelijk gebaseerd op gepubliceerd wetenschappelijk onderzoek.
De uitgangsvragen zijn óf evidence-based (via de GRADE methodiek) óf consensus-based (zonder systematisch literatuuronderzoek) uitgewerkt.
De GRADE-methodiek
Selectie
Naast de selectie van studies op relevantie werd tevens geselecteerd op bewijskracht. Hiervoor werd gebruik gemaakt van de volgende hiërarchische indeling van studiedesigns gebaseerd op bewijskracht:
- Gerandomiseerde gecontroleerde studies (RCT's)
- Niet gerandomiseerde gecontroleerde studies (CCT's)
Waar deze niet voorhanden waren werd verder gezocht naar vergelijkend cohortonderzoek.
Critical appraisal
De kwaliteit van bewijs wordt weergegeven in vier categorieën: hoog, matig, laag en zeer laag. RCT's starten hoog en observationele studies starten laag. Vijf factoren verlagen de kwaliteit van de evidentie (beperkingen in onderzoeksopzet, inconsistentie, indirectheid, imprecisie, publicatie bias) en drie factoren kunnen de kwaliteit van de evidentie verhogen (sterke associatie, dosis-respons relatie, plausibele (residuele) confounding) (zie tabel 1).
Tabel 1. GRADE-methodiek voor het graderen van bewijs
|
Quality of evidence |
Study design |
Lower if * |
Higher if * |
|
High (4) |
Randomized trial |
Study limitations -1 Serious -2 Very serious Inconsistency -1 Serious -2 Very serious Indirectness -1 Serious -2 Very serious Imprecision -1 Serious -2 Very serious Publication bias -1 Likely -2 Very likely |
Large effect + 1 Large + 2 Very large Dose response + 1 Evidence of a gradient All plausible confounding + 1 Would reduce a demonstrated effect, or + 1 Would suggest a spurious effect when results show no effect |
|
Moderate (3) |
|
||
|
Low (2)
|
Observational study |
||
|
Very low (1) |
|
Algehele kwaliteit van bewijs
Omdat het beoordelen van de kwaliteit van bewijs in de GRADE-benadering per uitkomstmaat geschiedt, is er behoefte aan het bepalen van de algehele kwaliteit van bewijs. Zowel voor als na het literatuuronderzoek wordt door de richtlijnwerkgroep bepaald welke uitkomstmaten cruciaal, belangrijk en niet belangrijk zijn.
Het niveau van de algehele kwaliteit van bewijs wordt in principe bepaald door de cruciale uitkomstmaat met de laagste kwaliteit van bewijs. Als echter de kwaliteit van het bewijs verschilt tussen de verschillende cruciale uitkomstmaten zijn er twee opties:
- De uitkomstmaten wijzen in verschillende richtingen (zowel gewenst als ongewenste effecten) of de balans tussen gewenste en ongewenste effecten is onduidelijk, dan bepaalt de laagste kwaliteit van bewijs van de cruciale uitkomstmaten de algehele kwaliteit van bewijs;
- De uitkomstmaten in dezelfde richting wijzen (richting gewenst of richting ongewenst effecten), dan bepaalt de hoogste kwaliteit van bewijs van de cruciale uitkomstmaat dat op zichzelf voldoende is om de interventie aan te bevelen de algehele kwaliteit van bewijs.
Tabel 2. Formulering conclusies op basis van kwaliteit van bewijs per uitkomstmaat
|
Kwaliteit van bewijs |
Interpretatie |
Formulering conclusie |
|
Hoog |
Er is veel vertrouwen dat het werkelijk effect dicht in de buurt ligt van de schatting van het effect. |
Er is bewijs van hoge kwaliteit dat...
(Referenties) |
|
Matig |
Er is matig vertrouwen in de schatting van het effect: het werkelijk effect ligt waarschijnlijk dicht bij de schatting van het effect, maar er is een mogelijkheid dat het hier substantieel van afwijkt. |
Er is bewijs van matige kwaliteit dat...
(Referenties) |
|
Laag |
Er is beperkt vertrouwen in de schatting van het effect: het werkelijke effect kan substantieel verschillend zijn van de schatting van het effect. |
Er is bewijs van lage kwaliteit dat....
(Referenties) |
|
Zeer laag |
Er is weinig vertrouwen in de schatting van het effect: het werkelijke effect wijkt waarschijnlijk substantieel af van de schatting van het effect. |
Er is bewijs van zeer lage kwaliteit dat....
(Referenties) |
|
Formulering algehele kwaliteit van bewijs: hoog/matig/laag/zeer laag |
||
Methode voor het formuleren van ‘Overwegingen’
Naast de evidence uit de literatuur (conclusies) zijn er andere overwegingen die meespelen bij het formuleren van de aanbeveling. Deze aspecten worden besproken onder het kopje ‘Overwegingen' in de richtlijntekst. Hierin worden de conclusies (op basis van de literatuur) geplaatst in de context van de dagelijkse praktijk en vindt een afweging plaats van de voor- en nadelen van de verschillende beleidsopties. De uiteindelijk geformuleerde aanbeveling is het resultaat van de conclusie(s) in combinatie met deze overwegingen.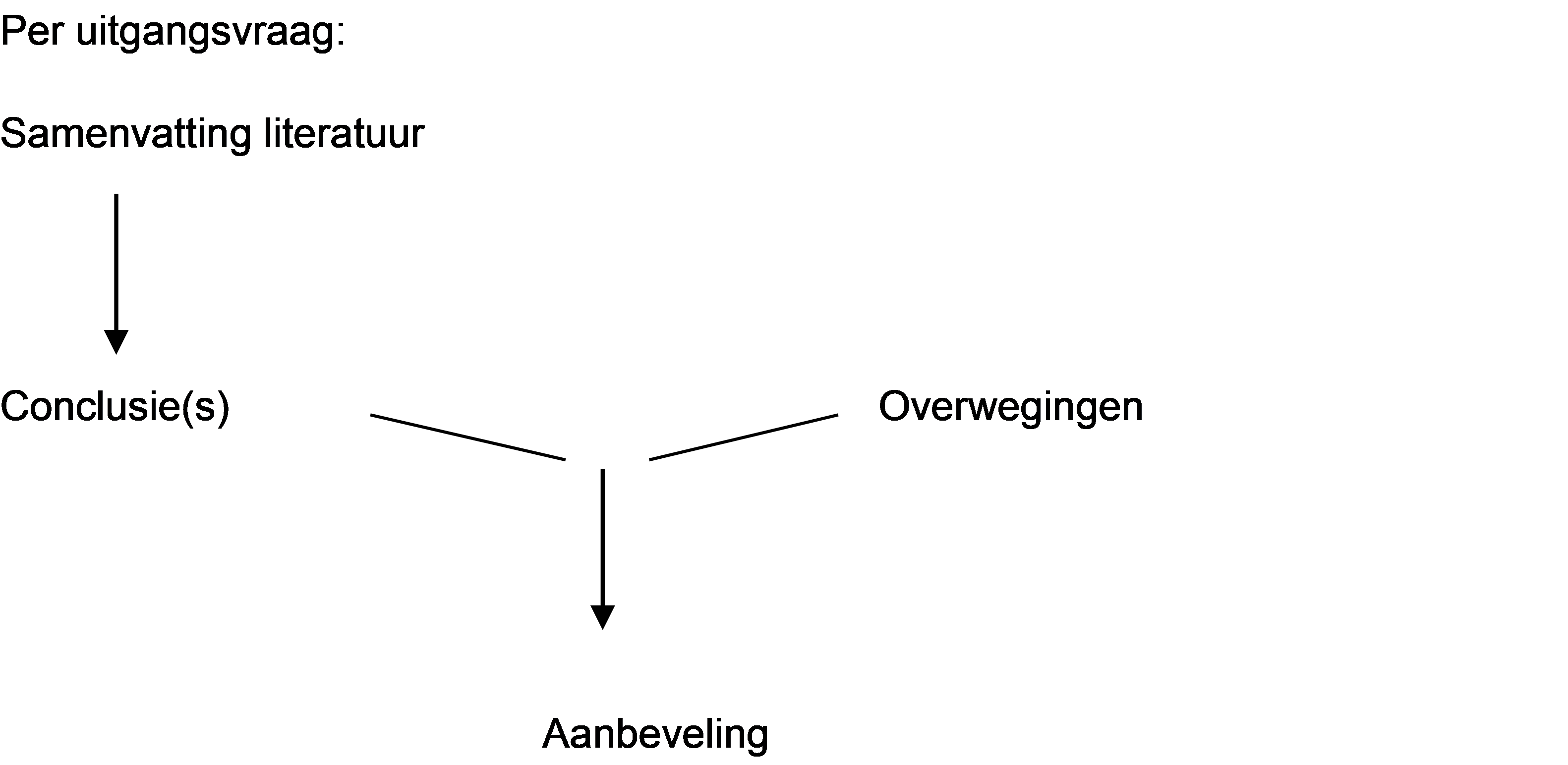
Figuur 1. Van bewijs naar aanbeveling
Bij het schrijven van de overwegingen zijn onderstaande zaken in acht genomen.
- Kwaliteit van het bewijs
Hoe hoger de algehele kwaliteit van het bewijs, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. - Balans van gewenste en ongewenste effecten
Hoe groter het verschil is tussen de gewenste en ongewenste effecten, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. Hoe kleiner dit verschil of hoe meer onzekerheid over de grootte van het verschil, des te waarschijnlijker wordt het formuleren van een conditionele aanbeveling.
Toelichting: - Patiëntenperspectief
Hoe groter de uniformiteit in waarden en voorkeuren van patiënten bij het afwegen van de voor- en nadelen van een interventie, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. - Professioneel perspectief
Hoe groter de uniformiteit in waarden en voorkeuren van professionals ten aanzien van de toepasbaarheid van een interventie, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling.
Toelichting:
- Kennis en ervaring met technieken/therapieën.
- Risico’s die professional loopt bij het toepassen van de interventie.
- Verwachte tijdbesparing.
- Verlies aan tijd door het invoeren van de interventie.
N.B.: de hierna volgende factoren (5, 6 en 7) alleen evalueren als een positief geformuleerde aanbeveling wordt overwogen! Een positief geformuleerde aanbeveling is een aanbeveling waarbij een bepaalde interventie wel ‘dient’ plaats te vinden (sterk) of wel ‘kan worden overwogen’ (zwak/conditioneel). Als dat daarentegen juist niet het geval is, is sprake van een negatief geformuleerde aanbeveling.
- Middelenbeslag
Hoe minder middelen er worden gebruikt (m.a.w. hoe lager de kosten van een interventie zijn vergeleken met de beschouwde alternatieven en andere kosten gerelateerd aan de interventie), des te waarschijnlijker wordt het formuleren van een sterke aanbeveling. Hoe meer onzekerheid over het middelenbeslag, des te waarschijnlijker wordt een conditionele aanbeveling. - Organisatie van zorg
Hoe meer onzekerheid of de geëvalueerde interventie daadwerkelijk op landelijke schaal toepasbaar is, des te waarschijnlijker wordt het formuleren van een conditionele aanbeveling.
Toelichting: - Maatschappelijk perspectief
(Juridische overwegingen/ethische overwegingen/industriële belangen/vergoeding door verzekeraars/politieke en strategische consequenties)
Hoe groter de onzekerheid hierover is, des te waarschijnlijker wordt het formuleren van een conditionele aanbeveling.
Toelichting:
- Indien twee behandelingen even effectief zijn waarvan één behandeling wordt vergoed, zal deze laatste behandeling mogelijk de voorkeur hebben.
Methode voor het formuleren van aanbevelingen
GRADE kent twee soorten aanbevelingen: sterke aanbevelingen of conditionele (zwakke) aanbevelingen. De sterkte van aanbevelingen reflecteert de mate van vertrouwen waarin – voor de groep patiënten waarvoor de aanbevelingen zijn bedoeld - de gewenste effecten opwegen tegen de ongewenste effecten.
Formulering:
- Sterke aanbevelingen: Doe/geef etc. (of er dient…. te worden gegeven/gedaan)
- Zwakke/conditionele aanbevelingen: Overweeg….. te geven/te doen.
Consensus-based methodiek
Naast de evidence-based uitwerking (GRADE) zijn er ook uitgangsvragen via de consensus-based methodiek uitgewerkt. Hierbij zijn de richtlijnteksten ook gebaseerd op evidence, maar is er geen systematisch literatuuronderzoek gedaan en zijn de gevonden studies niet methodologisch beoordeeld.
