Behandeling van hypernasaliteit bij schisis
Uitgangsvraag
Wat is de beste chirurgische behandelstrategie indien er sprake is van velopharyngeale insufficiëntie bij kinderen met een (cheilo-gnatho)palatoschisis?
Aanbeveling
Maak de keuze voor een specifieke operatieve techniek op basis van preoperatief logopedisch onderzoek gecombineerd met een onderzoek zoals nasendoscopie en/of videofluoroscopie (zie module diagnostiek van hypernasaliteit).
Overweeg een intravelaire palatum plastiek met repositionering van de palatale spieren alvorens over te gaan tot een pharynxplastiek indien sprake is van persisterende velopharyngeale disfunctie ondanks eerder gesloten palatum.
Overweeg bij aanhoudende velopharyngeale insufficiëntie ondanks de hernieuwde positionering van palatale spieren, een pharynxplastiek welke gebaseerd is op hernieuwde diagnostiek zoals een naso-endoscopie en/of videofluoroscopie.
Overweeg bij een submuceuze palatoschisis een enkelvoudige palatumplastiek boven een gecombineerde operatie van een palatumplastiek met pharynxplastiek.
Pas vetinjectie alleen toe in het kader van wetenschappelijk onderzoek.
Overwegingen
De meest optimale operatieve methode ter correctie van VPI blijft controversieel door een gemis aan goed gerandomiseerde gecontroleerde, prospectieve studies die verschillende operatieve technieken met elkaar vergelijken. Daarnaast ontbreekt het in de hiervoor en later genoemde studies aan afdoende lengte in klinische follow-up (minimaal drie jaar) om het operatieve resultaat op waarde in de tijd te kunnen schatten. Bovendien bestaat er geen consensus over de objectieve diagnostische middelen om de operatieve technieken goed te vergelijken. Een belangrijk onderdeel van de differentiaal diagnose VPI, bij een eerder gecorrigeerd palatum, zal onder andere ook moeten bestaan uit de gedachte dat de eerder verrichte palatumplastiek met intravelaire veloplastiek niet optimaal genezen is. De herstelde spiersling kan immers dehiscent zijn geraakt of opnieuw verkleefd met de achterand van het palatum durum. Een aanwijzing hiervoor kan een gecompliceerde palatum genezing zijn of verlittekening met verminderde mobiliteit. Er bestaat echter geen onderzoek waarbij een vergelijking is gemaakt tussen een hernieuwde intravelaire veloplastiek en andere spraakverbeterende operaties.
Gezien het beperkte aantal wetenschappelijke studies wil de werkgroep in het hiernavolgende gedeelte ook ter overweging die vergelijkende studies toevoegen waarin andere operatieve technieken of gecombineerde technieken worden beschreven.
Carlisle (2011) voerden en een retrospectieve analyse uit bij 46 patiënten met schisis (palatum schisis nno (80%) submuceuze schisis (20%, inclusief velocardiaal faciaalsyndroom) en VPI waarbij sphincter pharyngoplastiek (SP; n=20) werd vergeleken met sphincter pharyngoplastiek gecombineerd met een verlengingsplastiek volgens Furlow (SP+; n=26). Een uitkomstmaat van deze studie was de kans op revisiechirurgie vanwege aanhoudende hypernasaliteit. De twee groepen waren niet vergelijkbaar in indicatiestelling en verschilden van dien aard dat de SP+ groep bestond uit patiënten met een grotere afstand van velum naar pharynxachterwand, vastgelegd middels nasendoscopie. De resultaten van dit onderzoek lieten zien dat in de groep met SP meer revisie chirurgie noodzakelijk was dan in de groep met SP+ (25% vs 4%).
Een retrospectieve vergelijkende studie door Meek (2003) beschrijft een populatie van 93 patiënten met VPI, waarbij een caudale (n=53) of craniaal (n=40) gesteelde pharynxachterwandlap werd uitgevoerd. De keuze van de steel werd peroperatief gemaakt afhankelijk van de aanwezigheid van vergroot adenoïde en van de grootte van de afstand van velum tot achterwand. Logopedisch lieten alle patiënten een verbetering zien op gebied van articulatie, luchtverlies en hypernasaliteit. De verbetering van de VPI was significant groter indien geopereerd was voor het zesde levensjaar. Er werd geen verschil aangetoond tussen beide technieken. Een belangrijke beperking van deze studie is het grote verschil in fenotypering dat geleid heeft tot de VPI (groep bestaand uit: congenitaal kort palatum, complete CGP schisis tot submuceuze schisis).
Uit beide studies komt naar voren dat de keuze van de plastiek afhankelijk is van het preoperatieve onderzoek en de peroperatieve bevindingen van het velum, de adenoïden en de afstand naar de pharynxachterwand. Middels deze wijze is er zowel met gecombineerde ingrepen als met caudaal en craniaal gesteelde plastieken een goed resultaat te behalen.
Ysunza (2001) onderzochten 203 patiënten waarvan uiteindelijk 72 kinderen werden geïncludeerd met een niet-syndromale submuceuze palatoschisis en VPI. Alle kinderen werden onderworpen aan zowel oraal onderzoek, logopedisch onderzoek, nasendoscopie en videofluoroscopie. Er werd gerandomiseerd in 2 groepen; in de controlegroep werd een standaard minimale incisie palatopharyngoplastiek (MIPP) gedaan (n=37) en in de experimentele groep werd MIPP gecombineerd met een geïndividualiseerde operatie gebaseerd op de preoperatieve diagnostiek (n=35; 32 pharyngeale lap, 3 sphincterplastiek). Bij beide technieken werden dezelfde resultaten gevonden voor complete afsluiting (86 % in groep 1 versus 89% in groep 2) en velopharyngeale afstand. Er werd na operatie bij geen van de patiënten slaapapneu gevonden. Dit komt mede door screening op vergrote tonsillen die anders in eerste tempo operatief werden verwijderd voor overgegaan werd tot een pharynx- of palatumplastiek. Gezien de minimale verschillen tussen de twee operatietechnieken is het advies van de auteurs te kiezen voor de minst invasieve techniek zonder aanvullende pharynxplastiek en residuele VPI te corrigeren in een tweede tempi met een meer geïndividualiseerde pharynxplastiek.
De werkgroep acht het voordeel van gecombineerde operaties aan palatum en pharynx ter correctie van VPI ten opzichte van een enkelvoudige procedure onvoldoende bewezen. Het advies is de operaties te scheiden, waarbij een redo van het palatum als eerste stap wordt geadviseerd.
Keuning (2009) verrichten een observationele longitudinale studie in 130 patiënten met residuele VPI na eerdere operatie aan het palatum waarbij een craniaal gesteelde pharynxachterwandlap werd uitgevoerd. De casemix in deze studie was groot bestaand uit deels unilaterale cheilognathopalatoschisis, deels bilaterale cheilognathopalatoschisis, deels submuceuze of geisoleerde palataloschisis en eveneens syndromale patiënten. Er was in 15 % een revisie chirurgische ingreep nodig en er deden zich weinig complicaties voor. Gezien het feit dat de auteurs overeenkomstige resultaten boekten met de craniaal gesteeld pharynxachterwandlap ten opzichten van eerder beschreven andere technieken, benadrukken zij vooral de operatieve kanten van de techniek. De werkhypothese wordt onderzocht of een ervaren chirurg minder complicaties heeft en dus een beter functioneel resultaat. De auteurs beklemtonen dat de uitkomst van de plastiek vaak moeilijk in te schatten is door onder anderen het concept van buisvorming/krimp en verkorting van de lap in het pharynxgebied. Geadviseerd wordt het rauwe oppervlak van de pharynxlap te bedekken ten einde tubing te verminderen (Keuning, 2009; Rintala and Haapanen, 1995).
Uit de studie komt naar voren dat er geen onderscheid kon worden gemaakt naar ervaring van de operateurs, waarbij de jongste operateur overigens minder complicaties scoorde dan de oudste. Men concludeert dat de individuele technische vaardigheden van de chirurg meer dan de chirurgische ervaring van belang zijn om complicaties te minimaliseren.
Autologe vet injecties (lipofilling)
Een relatief nieuwe interventie ter behandeling van VPI is de autologe vet injectie (lipofilling). In een systemische review (Bishop, 2014) werd de literatuur over pharynxachterwandaugmentaties systematisch onderzocht; van artificiële toevoegingen zoals siliconen en goretex tot biologisch materiaal zoals kraakbeen en lipofilling. Elf onderzoeken over lipofilling werden geïncludeerd waarvan 3 een beschrijving gaven van selectieve augmentatie van de pharynxachterwand en de overige 8 studies een beschrijving van augmentatie van palatum molle/pharynxbogen en pharynxachterwand. Geen van deze 11 studies betrof een vergelijkend onderzoek. Er was geen meta-analyse mogelijk vanwege de sterke heterogeniteit van de populatie. Er waren geen vergelijkbare diagnostische middelen gebruikt noch werden er goede vergelijkende objectieve postoperatieve beoordelingen gegeven. Alle studies gebruikten dezelfde techniek voor het verkrijgen van het vet (Coleman set). De hoeveelheid resterend volume van het geïnjecteerde vet op korte en langere termijn werd niet consistent gerapporteerd, behoudens in de studie door Filip (2011) die een associatie vonden tussen het volume vet geïnjecteerd op MRI aangetoond en vermindering van de velopharyngeale afstand. In deze studie werd echter niet gerapporteerd over de daadwerkelijke klinische verandering van de VPI.
Een voorkeurslocatie voor injectie van vet werd niet aangetoond. Slechts 1 complicatie werd gemeld, namelijk een toename van vet bij toename van gewicht van het kind over een periode van 31 maanden. Dit resulteerde in obstructieve slaap apneu klachten. De conclusie die de auteurs gaven aan de hand van deze systematisch review is dat vet injectie een simpele, relatief goedkope techniek lijkt met weinig complicaties. Er is echter sprake van belangrijke missende informatie over patiëntselectie, volume en locatie van vetinjectie als mede hoeveelheid resorptie van het geinjecteerde vetdepot en het resultaat ten opzichte van andere bestaande operatieve technieken.
De werkgroep acht het gebruik van lipofilling op dit moment dan nog niet bewezen effectief ter behandeling van VPI. De werkgroep is dan ook van mening dat VPI correctie d.m.v. lipofilling alleen toe mag worden gepast indien andere operatieve opties zijn weggevallen.
Algemene overwegingen
In de afwezigheid van bewezen effectieve universele operatieve aanpak van VPI zal men bij de keuze voor een techniek vooral moeten varen op een goede preoperatieve evaluatie van de vorm van VPI, gebaseerd het onderzoek zoals beschreven in de module diagnostiek bij VPI. Van dit pre-operatieve en peroperatieve onderzoek dient verslaglegging te zijn en dient eventueel postoperatief herhaald te worden. Niet alleen ter controle van het behaalde succes of falen van de behandeling, maar ook als registratie en mogelijkheid tot vergelijking. De leeftijd waarop een operatie ter correctie van VPI het best kan plaatsvinden zal in gezamenlijkheid door de behandelaars moeten worden vastgesteld met als leidraad de de instrueerbaarheid ten aanzien van logopedische oefeningen. Deze instrueerbaarheid is te testen tijdens de logopedische spraaktest welke tot de standaard diagnostiek zou moeten behoren voorafgaande aan de operatie.
Gezien de beperkte aangetoonde verschillen tussen pharynxachterwandlap en pharyngosfincterplastiek lijken beide technieken vergelijkbaar ten aanzien van klinische effectiviteit.
Een oorzaak voor de beperkte verschillen tussen de technieken zouden zeer goed veroorzaakt kunnen worden door onder meer de beperkte sample size van de verschillende studies en de diversiteit van aandoeningen van de geincludeerde patiënten leidend tot de VPI. Om een verschil van 20% aan te tonen tussen verschillende technieken binnen een studie met een verwachte uitval van 10% van de onderzoekspopulatie is berekend dat er een groepsgrootte noodzakelijk is van 292 patiënten (Åbyholm, 2005). Om deze aantallen te kunnen bereiken wordt een oproep gedaan zoveel mogelijk identieke studies te starten, wetende dat het inclusieaantal per ziekenhuis laag is.
Onderbouwing
Achtergrond
Het doel van chirurgische behandeling van velopharyngeale insufficiëntie (VPI) is het herstel van een functionele afsluiting tussen nasopharynx en oropharynx zodat normale articulatie en spraak kan volgen. Verschillende procedures voor de secundaire behandeling van velopharyngeale insufficiëntie zijn beschreven, waarbij repositie van de palatummusculatuur naar een meer anatomische positie (verbinding in de mediaan en meer naar posterieur geplaatst) bovenaan zou moeten staan, ook als deze procedure reeds eerder heeft plaatsgevonden.
Aanvullende technieken zijn pharynxachterwandlappen (craniaal of caudaal gesteeld), sfincterpharyngoplastieken (zoals Orticochea), combinatie van verlengen van palatum en een craniale gesteelde pharynxlap (gemodificeerde Honig), verlengingsplastiek van het palatum (Furlow Z-plastiek of uni/-bilaterale buccale lappen) en pharynxachterwandaugmentatie (bijv. vetinjectie therapie of Hynes). Elke behandeloptie kent voor- en nadelen. Het doel van deze uitgangsvraag is te bepalen welke chirurgische behandelstrategie de voorkeur heeft indien er sprake is van velopharyngeale insufficiëntie bij een patiënt met een schisis waarbij een primaire palatumsluiting reeds is uitgevoerd.
Conclusies / Summary of Findings
|
Very low GRADE |
We found very little proof that pharyngeal flap and sphincter pharyngoplasty are equally effective in treating velopharyngeal insufficiency.
Ysunza, 2004; Åbyholm, 2005 |
|
Very low GRADE |
We found very little proof that pharyngeal flap and sphincter pharyngoplasty result in comparable complications in treating velopharyngeal insufficiency.
Ysunza, 2004; Åbyholm, 2005 |
Samenvatting literatuur
Study characteristics
The study by Ysunza (2004) concerned a 7-year prospective study to assess the planning and results of pharyngeal flaps and sphincter pharyngoplasties for correcting velopharyngeal insufficiency. The customized pharyngeal flap and sphincter pharyngoplasty were performed according to findings of videonasopharyngoscopy and multiview videofluoroscopy. The study population consisted of 70 patients with complete unilateral cleft lip and palate with no other medical conditions, which was randomly divided into two groups. Palate repair was performed before 8 months of age in all patients. Age ranged from 4 years and one month to 7 years and 10 months (median: 5 years, 2 months) in the group with a pharyngeal flap, and from 4 years and 5 months to 7 years and 7 months (median: 5 years 4 months) in the group with sphincter pharyngoplasty. Outcomes were evaluated postoperatively and after four months. No loss to follow up was reported.
The study by Åbyholm (2005) is a randomized clinical trial comparing pharyngeal flap and sphincter pharyngoplasty for correcting velopharyngeal insufficiency in 97 patients with a repaired cleft palate with no other medical conditions were randomly divided in two groups. Patients, aged 3 to 25 years old, were evaluated at both three months and one year.
Results
VPI resolution
Whereas Ysunza (2004) reports no significant difference in VPI resolution between the groups, Åbyholm (2005) found a significant difference in favour of pharyngeal flap (P = 0.005). The pooled odds ratio for VPI resolution calculated by Collins (2012) was found to be 2.95 (95% CI: 0.66 - 13.23) in favour of the pharyngeal flap. In figure 2 the forest plot from Collins (2012) is shown. The meta-analysis by Collins (2012) included the selected studies by Ysunza (2004) and Åbyholm (2005). Collinset (2004) pooled the data of the two studies (133 patients) to calculate a pooled odds ratio for VPI resolution. This figure shows the number of patients with resolution of VPI after pharyngeal flap and sphincter pharyngoplasty procedures at follow-up times of 3 to 4 months for the RCTs of Åbyholm and Ysunza. Odds ratio and 95% confidence intervals for each study and for the meta-analysis as a whole are shown.
Figure 2. Pooled odds ratio for VPI resolution (Collins, 2012)
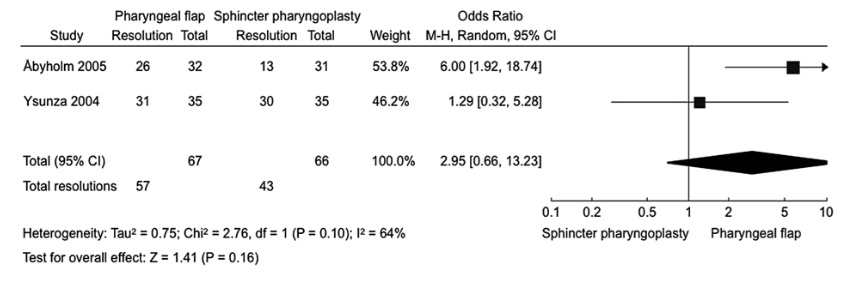
Although Åbyholm (2005) found a high level of clinical improvement for both surgical interventions, at 3 months postsurgery, elimination of hypernasality was found in twice as many patients after flap surgery (significant). At 12 months post-surgery, however, Åbyholm found no statistically significant difference in VPI resolutions between the sphincter and pharyngeal flaps procedures, resp. 78% vs. 83% (P = 0.45).
Postoperative complications
Both studies reported no differences in postoperative complications between the groups. Åbyholm reported low complication rate, low reoperation rate, and no significant differences between the two procedures. In addition, Åbyholm found that both procedures rarely resulted in clinically significant sleep apnea directly after surgery or on long-term incidence. This was assessed by carrying out overnight polysomnograms 1 month prior to surgery, and repeated 4 to 6 weeks and 1 year after surgery.
Grading the evidence
Grading the evidence started at the level of high evidence. Downgrading with three levels was, however, necessary as the sample size needed for statistical significance was not achieved, and due to heterogeneity of results. The number of patients, and for some outcomes like complications the number of events was very low.
Zoeken en selecteren
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende wetenschappelijke vraagstelling:
P: Niet-syndromale (cheilo-gnatho-palato)schisispatiënten met gesloten palatum met velopharyngeale insufficiëntie;
I: Pharyngoplastiek; palatumplastiek; pharynxaugmentatie; vetinjectie therapie;
C: Onderlinge vergelijking chirurgische mogelijkheden;
O: Spraak; aanwezigheid van (open) nasaliteit (gapsize); revisie chirurgie; en postoperatieve complicaties of bijwerkingen (slaap apnoe, dehiscentie/loslaten van lap).
Relevante uitkomstmaten
De werkgroep definieerde niet a priori de uitkomstmaten, maar hanteerde de in de studie gebruikte definities. De werkgroep achtte succespercentage van de ingreep (gedefinieerd als postoperatieve (open)nasaliteit) een voor de besluitvorming kritieke uitkomstmaat, en spraak en complicaties of bijwerkingen voor de besluitvorming belangrijke uitkomstmaten.
Search and study selection (methods)
A systematic search was performed in the databases of Medline (through OVID), Embase and the Cochrane Library between 1980 and April 9, 2014. This search was aimed to identify systematic reviews, RCTs, controlled clinical trials, and observational studies. Detailed search characteristics are shown in the appendix.
Studies that included patients with repaired cleft lip and palate were selected if they compared surgical interventions to correct velopharyngeal insufficiency. Data on effect sizes or primary data had to be available for at least one of the outcomes of interest: speech, hypernasality, hyponasality, adverse effects and/or complications.
Results selection
The initial search identified 315 references. After selection 11 studies were found describing VPI and assessed full-text. Nine studies were excluded because these studies did not meet the inclusion criteria (see appendix). One of these 9 studies was a systematic review/ meta analysis (Collins, 2012). However, in adition to this review two RCT studies were described which do meet the inclusion criteria. The evidence table and risk of bias assessment table are added as an appendix.
Referenties
- Abyholm F, D'Antonio L, Davidson Ward SL, Kjoll L, Saeed M, Shaw W, et al. Pharyngeal flap and sphincterplasty for velopharyngeal insufficiency have equal outcome at 1 year postoperatively: results of a randomized trial. Cleft Palate-Craniofac J 2005 Sep;42(5):501-11
- Bishop A, Hong P, Bezuhly M. Autologous fat grafting for the treatment of velopharyngeal insufficiency: State of the art. J Plast Reconstr Aesthetic Surg 2014;67(1):1-8
- Carlisle MP, Sykes KJ, Singhal VK. Outcomes of sphincter pharyngoplasty and palatal lengthening for velopharyngeal insufficiency: a 10-year experience. Archives of Otolaryngology -- Head & Neck Surgery 2011 Aug;137(8):763-6
- Collins J, Cheung K, Farrokhyar F, Strumas N. Pharyngeal flap versus sphincter pharyngoplasty for the treatment of velopharyngeal insufficiency: a meta-analysis. Journal of Plastic, Reconstructive & Aesthetic Surgery: JPRAS 2012 Jul;65(7):864-8
- Filip C, Matzen M, Aagenæs I, et al. Speech and magnetic resonance imaging results following autologous fat transplantation to the velopharynx in patients with velopharyngeal insufficiency. Cleft Palate Craniofac J 2011;48:708e16.
- Keuning KH, Meijer GJ, van der Bilt A, Koole R. Revisional surgery following the superiorly based posterior pharyngeal wall flap. Historical perspectives and current considerations. International Journal of Oral & Maxillofacial Surgery 2009 Nov;38(11):1137-42
- Meek MF, Coert JH, Hofer SO, Goorhuis-Brouwer SM, Nicolai JP. Short-term and long-term results of speech improvement after surgery for velopharyngeal insufficiency with pharyngeal flaps in patients younger and older than 6 years old: 10-year experience. Ann Plast Surg 2003 Jan;50(1):13-7
- Rintala AE, Haapanen ML. The correlation between training and skill of the surgeon and reoperation rate for persistent cleft palate speech. Br J Oral Maxillofac Surg. 1995 Oct;33(5):295-71; discussion 297-8.
- Ysunza A, Pamplona MC, Mendoza M, Molina F, Martinez P, Garcia-Velasco M, et al. Surgical treatment of submucous cleft palate: a comparative trial of two modalities for palatal closure. Plastic & Reconstructive Surgery 2001 Jan;107(1):9-14
- Ysunza A, Pamplona MC, Molina F, Drucker M, Felemovicius J, Ramirez E, et al. Surgery for speech in cleft palate patients. Int J Pediatr Otorhinolaryngol 2004 Dec;68(12):1499-505
Evidence tabellen
Evidence table for intervention studies (randomized controlled trials and non-randomized observational studies [cohort studies, case-control studies, case series]
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Ysunza, 2004 |
Type of study: randomized clinical trial
Setting: Cleft palate clinic of hospital
Country: Mexico
Source of funding: Not reported |
Inclusion criteria: Complete unilateral cleft lip and palate with no other medical conditions; Palate repair performed before 8 months of age; presence of VPI; age 5 to 10
Exclusion criteria: Hearing disorders
N total at baseline: Intervention: 35 Control: 35
Important prognostic factors2: Age in years range: I: 4y 1m to 7y 10m C:4y 5m to 7y 7m
Groups comparable at baseline? Yes |
I: A customized pharyngeal flap according to findings of videonasopharyngoscopy and multiview videofluoroscopy
|
C: Sphincter pharyngoplasty according to findings of videonasopharyngoscopy and multiview videofluoroscopy |
Length of follow-up: I: 4 months C: 4 months
Loss-to-follow-up: I: 0 C: 0
|
VPI resolution: I: 89% (n=31) C: 85% (n=30) P > 0.05
Velopharyngeal closure patterns Uniformly distributed between the two groups of patients.
Complications: None of the patients presented serious complications concerning the risk of obstruction in the immediate postoperative period.
No complications such as fistulae, dehiscence of the flap (pharyngeal flap) or flaps (sphincter pharyngoplasty), bleeding nor infection were detected in this series of patients. |
The planning of the surgical procedure, in order to match the postoperative structure to the pre- operative velopharyngeal dimensions and movements visualized through VNP and MVVF, seems to be the most important aspect of the surgery for correcting residual VPI after palatal closure. This was done on individual basis in both groups. |
|
Åbyholm, 2005 |
Type of study: randomized clinical trial
Setting: Cleft palate clinic of hospital
Country: US, Norway, UK
Source of funding: National Institute of Dental and Craniofacial Research (US) and NW Regional Health Authority |
Inclusion criteria: Complete unilateral cleft lip and palate with no other medical conditions; already undergone a primary repair of the palate (with or without a cleft lip or alveolus), aged between of 3 and 25 years with apparent VPI diagnosed by an experienced specialist speech pathologist at one of the participating centers
Exclusion criteria: Hearing disorders
N total at baseline: Intervention: 52 Control: 45
Important prognostic factors2: Age in years range (3-7): I: 48% C: 58% Age in years range (8-14): I: 38% C: 31% Age in years range (15-25): I: 14% C: 11%
Groups comparable at baseline? Yes |
I: Pharyngeal flap
|
C: Sphincter pharyngoplasty |
Length of follow-up: I: 12 months C: 12 months
Loss-to-follow-up: I: 0 C: 0
|
VPI resolution: 3 months I: 82% (n=26) C: 42% (n=13) P = 0.005
12 months I: 83% (n=43) C: 78% (n=35) P = 0.45
Complications: low complication rate, low reoperation rate, and no significant differences were detected between the two procedures. Both procedures rarely resulted in clinically significant sleep apnea, and that no difference was found in its long- term incidence. |
|
Notes:
1) Prognostic balance between treatment groups is usually guaranteed in randomized studies, but non-randomized (observational) studies require matching of patients between treatment groups (case-control studies) or multivariate adjustment for prognostic factors (confounders) (cohort studies); the evidence table should contain sufficient details on these procedures
2) Provide data per treatment group on the most important prognostic factors [(potential) confounders]
3) For case-control studies, provide sufficient detail on the procedure used to match cases and controls
4) For cohort studies, provide sufficient detail on the (multivariate) analyses used to adjust for (potential) confounders
Risk of bias table for intervention studies (randomized controlled trials)
|
Study reference
(first author, publication year) |
Describe method of randomisation1 |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Ysunza, 2004 |
Block randomization, unclear |
unclear |
unclear |
unclear |
unlikely |
likely |
unlikely |
Unlikely |
|
Åbyholm, 2005 |
computer-generated random numbers, with allocation concealment through sealed envelopes |
unlikely |
unlikely |
unclear |
unlikely |
unlikely |
likely |
unLikely |
1) Randomisation: generation of allocation sequences have to be unpredictable, for example computer generated random-numbers or drawing lots or envelopes. Examples of inadequate procedures are generation of allocation sequences by alternation, according to case record number, date of birth or date of admission.
2) Allocation concealment: refers to the protection (blinding) of the randomisation process. Concealment of allocation sequences is adequate if patients and enrolling investigators cannot foresee assignment, for example central randomisation (performed at a site remote from trial location) or sequentially numbered, sealed, opaque envelopes. Inadequate procedures are all procedures based on inadequate randomisation procedures or open allocation schedules..
3) Blinding: neither the patient nor the care provider (attending physician) knows which patient is getting the special treatment. Blinding is sometimes impossible, for example when comparing surgical with non-surgical treatments. The outcome assessor records the study results. Blinding of those assessing outcomes prevents that the knowledge of patient assignement influences the proces of outcome assessment (detection or information bias). If a study has hard (objective) outcome measures, like death, blinding of outcome assessment is not necessary. If a study has “soft” (subjective) outcome measures, like the assessment of an X-ray, blinding of outcome assessment is necessary.
4) Results of all predefined outcome measures should be reported; if the protocol is available, then outcomes in the protocol and published report can be compared; if not, then outcomes listed in the methods section of an article can be compared with those whose results are reported.
5) If the percentage of patients lost to follow-up is large, or differs between treatment groups, or the reasons for loss to follow-up differ between treatment groups, bias is likely. If the number of patients lost to follow-up, or the reasons why, are not reported, the risk of bias is unclear
6) Participants included in the analysis are exactly those who were randomized into the trial. If the numbers randomized into each intervention group are not clearly reported, the risk of bias is unclear; an ITT analysis implies that (a) participants are kept in the intervention groups to which they were randomized, regardless of the intervention they actually received, (b) outcome data are measured on all participants, and (c) all randomized participants are included in the analysis.
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 10-10-2016
Beoordeeld op geldigheid : 01-09-2018
De richtlijnwerkgroep heeft als doel de richtlijn periodiek (digitaal) van updates te voorzien.
De NVPC is als houder van deze richtlijn de eerstverantwoordelijke voor de actualiteit van deze richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de eerstverantwoordelijke over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
In samenwerking met:
Nederlandse Vereniging voor Keel-Neus-Oorheelkunde en Heelkunde van het Hoofd-Halsgebied (NVKNO)
Nederlandse Vereniging van Orthodontisten (NVvO)
Nederlandse Vereniging voor Mondziekten, Kaak- en Aangezichtschirurgie (NVMKA)
Nederlandse Vereniging voor Tandheelkunde (NVT)
Vereniging Klinische Genetica Nederland (VKGN)
Nederlands Instituut van Psychologen (NIP)
Nederlandse Vereniging voor Logopedie en Foniatrie (NVLF)
Nederlandse Vereniging voor Schisis en Cranio-Faciale Afwijkingen (NVSCA)
Nederlandse Vereniging van Pedagogen en Onderwijskundigen (NVO)
Met ondersteuning van:
Kennisinstituut van de Federatie Medisch Specialisten
Financiering
De richtlijnontwikkeling werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS) met cofinanciering van de NVKNO, NVvO, NvT en NVMKA.
Doel en doelgroep
Doel
Doel van de richtlijn is het optimaliseren van de zorg voor patiënten met een schisis in Nederland, voor zover mogelijk onderbouwd met wetenschappelijke kennis uit onderzoek. Onder optimaliseren wordt ook verstaan het inzichtelijk maken van de oorzaak van de bestaande praktijkvariatie tussen de verschillende schisisteams en hierbij onderscheid te maken tussen gewenste en ongewenste praktijkvariatie in de behandeling van patiënten met een schisis. Dit resulteert in voorstellen voor een meer uniforme behandeling voor zover dit wetenschappelijk onderbouwd kan worden.
Specifieke aandacht zal worden gegeven aan de volgende onderwerpen:
- terugdringen van ongewenste/ongefundeerde praktijkvariatie in de werkwijze en behandelprotocollen van de Nederlandse schisisteams, zonder daarbij maatwerk, innovatie of onderzoek in de weg te staan;
- het beschikbaar stellen en toegankelijk maken van objectieve / evidence based informatie over de behandeling van schisis aan zorgverleners, patiënten, ouders en andere partijen;
- te bezien in hoeverre de bestaande organisatie van zorg aanpassing behoeft om te kunnen voldoen aan de eisen ten aanzien van “state of the art” behandeling van een kind of volwassene met een schisis en de controle daarop.
De richtlijn biedt op deze wijze een handvat voor een meer uniforme zorg op het gebied van de postnatale behandeling van een kind met een schisis en de implementatie van deze zorg in Nederland.
Doelgroep
De richtlijn is primair bedoeld voor alle zorgverleners die betrokken zijn bij de zorg van een kind met een schisis: huisartsen, verloskundigen, gynaecologen, kinderartsen, keel-, neus- en oorartsen, plastische chirurgen, mond-, kaak- en aangezichtschirurgen, orthodontisten, klinisch genetici, gespecialiseerde verpleegkundigen, logopedisten, (kinder)tandartsen, medisch psychologen, orthopedagogen en maatschappelijk werkers. De secundaire doelgroep betreft de ouders en hun omgeving.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2013 een multidisciplinair samengestelde werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met een schisis en de NVSCA (zie hiervoor de samenstelling van de werkgroep). De werkgroepleden zijn door hun wetenschappelijke verenigingen en de NVSCA gemandateerd voor deelname. De werkgroep werkte gedurende twee jaar aan de totstandkoming van de richtlijn. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
Samenstelling van de werkgroep:
- dr. A.B. Mink van der Molen (voorzitter), plastisch chirurg, Universitair Medisch Centrum Utrecht
- dr. R.J.C. Admiraal, KNO-arts, Radboudumc Nijmegen
- dr. L.N.A. van Adrichem, plastisch chirurg, Erasmus MC Rotterdam
- drs. F.Bierenbroodspot, Mond-, Kaak- en Aangezichtschirurg, Isala, Zwolle
- drs. D. Bitterman, tandarts, Universitair Medisch Centrum Utrecht
- dr. M.J.H. van den Boogaard, Klinisch Geneticus, Universitair Medisch Centrum Utrecht
- drs. J.M. Dijkstra-Putkamer MPA, logopedist, Medisch Centrum Leeuwarden
- dr. M.C.M. van Gemert-Schriks, tandarts-pedodontoloog, Academisch Centrum Tandheelkunde Amsterdam
- Prof.dr. A.M. Kuijpers-Jagtman, orthodontist, Radboudumc Nijmegen
- dr.C.M.Moues-Vink, plastisch chirurg, Medisch Centrum Leeuwarden Friesland
- dr. H.F.N. Swanenburg de Veye, gezondheidszorgpsycholoog, Universitair Medisch Centrum Utrecht/Wilhelmina Kinderziekenhuis
- drs. N. van Tol – Verbeek, orthopedagoog-generalist; Koninklijke Kentalis Deventer / Almelo
- dr. C. Vermeij – Keers, registratieleider, Nederlandse Vereniging voor Schisis en Craniofaciale Afwijkingen
- drs. H. de Wilde, logopedist, Universitair Medisch Centrum Utrecht
Met ondersteuning van:
- P.H. Broos MSc, senior adviseur, Kennisinstituut van Medisch Specialisten
- dr. I.M. Mostovaya, adviseur, Kennisinstituut van Medisch Specialisten
Met dank aan:
- drs. N.G. Janssen, Mond-, kaak- en aangezichtschirurg, Universitair Medisch Centrum Utrecht
Belangenverklaringen
De KNMG-Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Op de richtlijnendatabase in de richtlijn behandeling van patiënten met een schisis vindt u een overzicht van de belangen van alle werkgroepleden en het oordeel over het omgaan met eventuele belangen.
In 2017/2018 hebben we de belangen opnieuw uitgevraagd van de mensen die meegewerkt hebben aan de aanvullende modules: (1) Le Fort I vs. distractie-osteogense en (2) NAM. Een overzicht van de belangen van deze werkgroepleden is zichtbaar in onderstaande tabel.
De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Reputatiemanagement |
Extern gefinancierd onderzoek |
Kennisvalorisatie |
Overige belangen |
|
Admiraal |
Arts |
geen |
nee |
nee |
nee |
nee |
nee |
nee |
|
Bierenbroodspot |
lid werkgroep vanuit de |
nee |
nee |
nee |
nee |
nee |
nee |
nee |
|
Bitterman |
kinderarts in WKZ Utrecht. Op dit moment hoofd poli kindertandheelkunde van WKZ Utrecht |
werkzaam als tandarts in algemene praktijk |
nee |
nee |
nee |
nee |
nee |
nee |
|
De Wilde |
logopedist WKZ Utrecht |
Post HBO cursus Schisis |
nee |
nee |
nee |
nee |
nee |
nee |
|
Dijkstra-Putkamer |
logopedist schisisteam (8 uur p/w) |
voorzitter werkgroep |
nee |
nee |
nee |
nee |
nee |
nee |
|
Kuipers-Jagtman |
Hoogleraar orthodontie; omvang 1,0 fte tot 01-03-2014; daarna 0,6 fte |
Editor-in-Chief Orthodontics and Craniofacial Research, hoofdredacteur scientific impact-factor journal op het gebied van orthodontisch en craniofaciaal onderzoek; 0,2 fte, betaald |
nee |
nee |
Ik was tot 01-01-2014 hoofd van het Centrum voor Schisis en Craniofaciale Afwijkingen van het Radboudumc. |
nee |
nee |
nee |
|
Mink van der Molen |
50% UMCU, 50% St. |
nee |
nee |
nee |
nee |
nee |
nee |
nee |
|
Moues |
Werkgroep lid |
nee |
nee |
nee |
nee |
nee |
nee |
nee |
|
Swanenburg de Veye |
Gezondheidszorgpsycholoog |
geen |
nee |
nee |
nee |
nee |
nee |
nee |
|
Van Adrichem |
Plastisch Chirurg, Erasmus MC Rotterdam (Sophia Kinderziekenhuis), sectorhoofd |
Adviseur Medirisk/VVAA (betaald via Maatschap) |
nee |
nee |
nee |
nee |
nee |
nee |
|
Van den Boogaard |
klinisch geneticus |
nee |
nee |
nee |
nee |
nee |
nee |
nee |
|
Van Gemert – Schriks |
Tandarts-pedodontoloog |
|
geen |
geen |
geen |
nvt |
nvt |
nee |
|
Van Tol-Verbeek |
behandelcoördinator Kentalis |
lid netwerk LZMG |
nee |
nee |
nee |
nee |
nee |
nee |
|
Vermeij – Keers |
registratieleider NVSCA schisis |
wetenschappelijk onderzoeker |
nee |
nee |
nee |
nee |
nee |
nee |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door middel van een focusgroepbijeenkomst. Een geanonimiseerd verslag is als bijlage bij de richtlijn gevoegd. De resultaten van de focusgroepbijeenkomst zijn waar mogelijk verwerkt in de richtlijn. Daarnaast heeft de BOSK de conceptrichtlijn beoordeeld tijdens de commentaarfase en suggesties voor verbetering van de richtlijn gegeven.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren.
De richtlijn wordt opgenomen in de richtlijnendatabase (www.richtlijnendatabase.nl) waarmee hij toegankelijk is voor alle relevante beroepsgroepen en patiënten. Daarnaast wordt er een samenvatting van de richtlijn gepubliceerd in tijdschriften van de deelnemende wetenschappelijke verenigingen. Ook is de richtlijn te downloaden vanaf de websites van betrokken wetenschappelijke verenigingen en de NVSCA.
De werkgroep heeft echter besloten geen nieuwe indicatoren te ontwikkelen bij de huidige richtlijn. De werkgroep beveelt de betrokken wetenschappelijke verenigingen aan om pas over een aantal jaren uitkomstindicatoren te ontwikkelen als de kwaliteitsregistratie van de NVSCA en PROMS ─ volgens bijvoorbeeld ICHOM ─ volledig operationeel zijn. Om dit te bereiken dienen de schisisteams eerst de tijd te krijgen toe te werken naar een uniforme werkwijze zoals beschreven in module Organisatie van zorg en het implementeren van PROMS.
Werkwijze
AGREE II
Deze richtlijn is opgesteld conform de eisen in het rapport ‘Richtlijnen 2.0’ van de adviescommissie Richtlijnen van de Raad kwaliteit van de Orde van Medisch Specialisten. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II) (https://www.agreetrust.org/), dat een internationaal breed geaccepteerd instrument is voor de beoordeling van de kwaliteit van richtlijnen.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens zijn in een invitational conference knelpunten besproken waarbij, naast vertegenwoordigers van de partijen in de werkgroep, vertegenwoordigers van de Nederlands Huisartsen Genootschap (NHG), de Bosk en Achmea aanwezig waren. Een verslag hiervan kunt u vinden in de bijlage bij de richtlijn.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn vervolgens verder uitgewerkt door de leden van de werkgroep en tijdens de werkgroepvergadering vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang als kritiek, belangrijk en onbelangrijk. Tevens definieerde de werkgroep, voor zover mogelijk, wat zij voor een bepaalde uitkomstmaat een klinisch relevant verschil vond, dat wil zeggen wanneer de verbetering in uitkomst een verbetering voor de patiënt is.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar bestaande buitenlandse richtlijnen en naar systematische reviews in Medline (OVID) en Cochrane Library. Vervolgens werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekactie of gebruikte trefwoorden van de zoekactie en de gehanteerde selectiecriteria zijn te vinden in de module van de desbetreffende uitgangsvraag. De gedetailleerde zoekstrategieën zijn vermeld in een bijlage bij de richtijn.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de kolom ‘Beoordeling kwaliteit studie’ van een evidencetabel.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie https://gdt.gradepro.org/app/handbook/handbook.html).
B) Voor vragen over de waarde van diagnostische tests, schade of bijwerkingen, etiologie en prognose
Bij dit type vraagstelling kan GRADE (nog) niet gebruikt worden. De bewijskracht van de conclusie is bepaald volgens de gebruikelijke EBRO-methode (Van Everdingen, 2004).
|
GRADE |
Definitie |
|
Hoog |
het is zeer onwaarschijnlijk dat de literatuurconclusie verandert als er verder onderzoek wordt gedaan; er is veel vertrouwen dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt zoals vermeld in de literatuurconclusie; |
|
Matig |
het is mogelijk dat de conclusie verandert als er verder onderzoek wordt gedaan; er is matig vertrouwen dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt zoals vermeld in de literatuurconclusie. |
|
Laag |
het is waarschijnlijk dat de conclusie verandert als er verder onderzoek wordt gedaan; er is beperkt vertrouwen dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt zoals vermeld in de literatuurconclusie. |
|
Zeer laag |
de conclusie is zeer onzeker; er is weinig vertrouwen dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt zoals vermeld in de literatuurconclusie. |
Formuleren van de conclusies
Bij interventievragen verwijst de conclusie niet naar een of meer artikelen, maar wordt getrokken op basis van alle studies samen (body of evidence). Hierbij maakten de werkgroepleden de balans op voor elke interventie. Bij het opmaken van de balans werden door de werkgroep de gunstige en ongunstige effecten voor de patiënt afgewogen.
Voor vragen over de waarde van diagnostische tests, schade of bijwerkingen, etiologie en prognose is het wetenschappelijke bewijs samengevat in een of meerdere conclusie(s), waarbij het niveau van het meest relevante bewijs is weergegeven. Omwille van de homogeniteit is het niveau van bewijs voor alle conclusies weergegeven als hoog/matig/laag/zeer laag, waarbij EBRO niveau 1 is vertaald naar hoog, 2 naar matig, 3 naar laag en 4 naar zeer laag.
Wanneer er voor een uitgangsvraag geen systematisch literatuuronderzoek werd verricht, is de literatuur niet beoordeeld op kwaliteit en is de kracht van het bewijs niet bepaald.
Overwegingen
Voor een aanbeveling zijn naast het wetenschappelijke bewijs ook andere aspecten belangrijk, zoals de expertise van de werkgroepleden, patiëntenvoorkeuren, kosten, beschikbaarheid van voorzieningen of organisatorische zaken. Deze aspecten worden, voor zover niet wetenschappelijk onderzocht, vermeld onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven een antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen. Bij het formuleren en graderen van de aanbeveling worden minimaal de volgende vier factoren in ogenschouw genomen: algehele kwaliteit van het wetenschappelijke bewijs; balans tussen voor- en nadelen van de interventie; waarden en voorkeuren van professional en patiënten; en beschikbare middelen.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is.
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor autorisatie en door hen geautoriseerd.
Zoekverantwoording
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID)
1966-april 2014
Engels |
1 Cleft Palate/ (17834) 2 ((palato or cheilo-gnatho-palato) adj10 schisis).ti,ab. (7) 3 (cleft adj3 palate*).ti,ab. (15224) 4 "Velopharyngeal Insufficiency"/ (1517) 5 (Velopharyngeal adj3 (Insufficiency or function or dysfunction or incompetence)).ti,ab. (1470) 6 1 or 2 or 3 or 4 or 5 (22988) 7 "Voice Disorders"/ or Articulation Disorders/ or speech intelligibility/ (9226) 8 "Voice Quality"/ (4657) 9 (nasality or hypernasality or nasalance or articulation or (nasal adj3 emission)).ti,ab. (8677) 10 7 or 8 or 9 (19644) 11 6 and 10 (1182) 12 (pharyngoplast* or furlow).ti,ab. (644) 13 Reconstructive Surgical Procedures/ or Otorhinolaryngologic Surgical Procedures/ (37051) 14 ("palatal closure*" or palatoplast*).ti,ab. (873) 15 "Surgical Flaps"/ or "Adipose Tissue"/tr (54234) 16 "intravelar veloplasty".ti,ab. (81) 17 surgery.fs. (1648736) 18 12 or 13 or 14 or 15 or 16 or 17 (1661890) 19 exp "rehabilitation of speech and language disorders"/ (8900) 20 "speech therap*".ti,ab. (2268) 21 19 or 20 (10237) 22 limit 11 to english language (1056) 23 18 or 21 (1670565) 24 22 and 23 (694) 35 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (231161) 36 24 and 35 (6)
|
10 SR |
|
Embase (Elsevier) |
('cleft palate'/exp/mj OR 'palatopharyngeal incompetence'/exp/mj OR (cleft NEAR/3 palate*):ab,ti OR (velopharyngeal NEAR/3 (insufficiency OR function OR dysfunction OR incompetence)):ab,ti) AND (pharyngoplast*:ab,ti OR 'palatal closure':ab,ti OR palatoplast*:ab,ti OR 'intravelar veloplasty':ab,ti OR 'speech therapy':ab,ti OR 'speech therapist':ab,ti OR 'palatoplasty'/exp/mj OR 'speech therapy'/exp/mj) AND [english]/lim AND ('voice disorder'/exp/mj OR 'nasal speech'/exp/mj OR 'hypernasality'/exp/mj OR ('speech disorder'/exp/mj AND [1966-2013]/py) OR nasality:ab,ti OR hypernasality:ab,ti OR nasalance:ab,ti OR articulation:ab,ti OR (nasal NEAR/3 emission):ab,ti OR 'speech'/exp),
AND 'meta analysis'/de OR cochrane:ab OR embase:ab OR psychlit:ab OR cinahl:ab OR medline:ab OR (systematic NEAR/1 (review OR overview)):ab,ti OR (meta NEAR/1 analy*):ab,ti OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de NOT ('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp NOT 'human'/exp) AND
9 referenties , 4 uniek |
|
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID)
1966-april 2014
Engels |
1 Cleft Palate/ (16412) 2 ((palato or cheilo-gnatho-palato) adj10 schisis).ti,ab. (7) 3 (cleft adj3 palate*).ti,ab. (13962) 4 "Velopharyngeal Insufficiency"/ (1328) 5 (Velopharyngeal adj3 (Insufficiency or function or dysfunction or incompetence)).ti,ab. (1268) 6 1 or 2 or 3 or 4 or 5 (21131) 13 "Voice Disorders"/ or Articulation Disorders/ (5860) 14 "Voice Quality"/ (4317) 15 (nasality or hypernasality or nasalance or articulation or (nasal adj3 emission)).ti,ab. (8128) 16 13 or 14 or 15 (16016) 17 6 and 16 (966) 18 (pharyngoplast* or furlow).ti,ab. (531) 19 Reconstructive Surgical Procedures/ or Otorhinolaryngologic Surgical Procedures/ (31823) 20 ("palatal closure*" or palatoplast*).ti,ab. (736) 21 "Surgical Flaps"/ or "Adipose Tissue"/tr (46934) 22 "intravelar veloplasty".ti,ab. (63) 23 surgery.fs. (1553661) 24 18 or 19 or 20 or 21 or 22 or 23 (1564457) 25 exp "rehabilitation of speech and language disorders"/ (8477) 26 "speech therap*".ti,ab. (2136) 27 25 or 26 (9725) 28 limit 17 to english language (846) 29 24 or 27 (1572711) 30 28 and 29 (532) 40 Articulation Disorders/ (1474) 41 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (204692) 42 30 and 41 (5) 43 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1348724) 44 30 and 43 (51) – 49 uniek 45 Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Case control.tw. or (cohort adj (study or studies)).tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective.tw. or prospective.tw. or Cross sectional.tw. or Cross-sectional studies/ [Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies] (1959958) 46 30 and 45 (262) 47 46 not (42 or 44) (226) – 225 uniek
|
310 |
|
Embase (Elsevier) |
'cleft palate'/exp/mj OR 'palatopharyngeal incompetence'/exp/mj OR (cleft NEAR/3 palate*):ab,ti OR (velopharyngeal NEAR/3 (insufficiency OR function OR dysfunction OR incompetence)):ab,ti AND ('voice disorder'/exp/mj OR 'nasal speech'/exp/mj OR 'hypernasality'/exp/mj OR ('speech disorder'/exp/mj AND [1966-2013]/py) OR (nasality:ab,ti OR hypernasality:ab,ti OR nasalance:ab,ti OR articulation:ab,ti OR (nasal NEAR/3 emission):ab,ti AND [1966-2013]/py)) AND (pharyngoplast*:ab,ti OR 'palatal closure':ab,ti OR furlow OR palatoplast*:ab,ti OR 'intravelar veloplasty':ab,ti OR 'speech therapy':ab,ti OR 'speech therapist':ab,ti AND [1966-2013]/py OR 'palatoplasty'/exp/mj OR 'speech therapy'/exp/mj) AND [english]/lim AND [embase]/lim
Filter SR: 1,) 0 uniek Filter RCT: 42, 10 uniek Major clinical studies: 57, 21 uniek
|
