Niet-beademen/-reanimeren beleid bij COPD
Uitgangsvraag
Wanneer en op grond van welke argumenten dienen behandelbeperkingen te worden besproken en vastgelegd bij patiënten met COPD die zijn opgenomen in het ziekenhuis met een longaanval?
Aanbeveling
Bespreek het reanimeer- en beadembeleid bij alle patiënten die worden opgenomen met een COPD-longaanval en leg dit vast in het patiëntendossier.
Bespreek in een stabiele situatie de behandelbeperkingen met de patiënt en naasten, bij voorkeur in de poliklinische setting:
- bespreek de verwachtingen en angst ten aanzien van de toekomst met de patiënt;
- ga na of de gedachten van de patiënt en de naasten overeenkomen met wat redelijkerwijs te verwachten is;
- bespreek de wensen ten aanzien van wel/niet-reanimeren en eventueel beademing;
- leg afspraken over wel/niet-reanimeren en beademing vast op een voor betrokkenen toegankelijke plaats;
- maak gebruik van de patiëntenversie van de richtlijn Palliatieve zorg bij COPD.
Bij gewijzigde klinische situatie zal dit opnieuw beoordeeld en besproken moeten worden.
Betrek bij de besluitvorming over reanimatie / beademing bij een patiënt opgenomen met een COPD-longaanval de volgende factoren:
- de wens van de patiënt en naasten;
- het reanimatiebeleid;
- het non-invasief en invasief beadembeleid;
- de aanwezigheid van negatief voorspellende factoren om een reanimatie te overleven zonder grote schade.
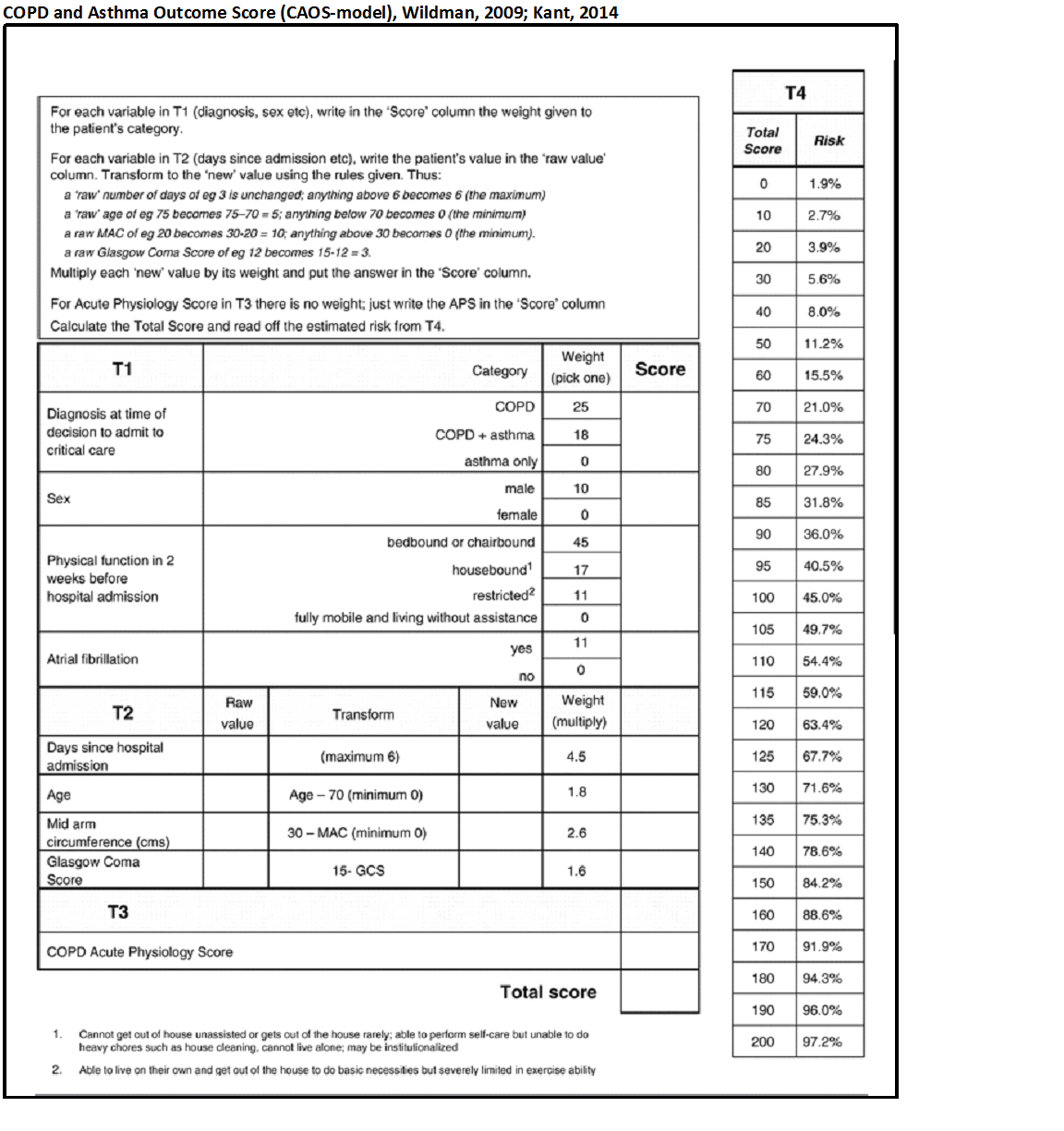
Hierbij kan het COPD and asthma outcome study (CAOS)-model’ als instrument dienen voor de gedachtenvorming over medische zinvolheid van een IC opname, al of niet met invasieve beademing.
De wens tot een terughoudend beleid van patiënt (en/of namens deze zijn naasten) is leidend.
Overwegingen
Indien een patiënt in het ziekenhuis met een COPD-longaanval respiratoir insufficiënt wordt zal een beslissing genomen moeten worden over de inzet van (non-)invasieve beademing. De kans op overleving en de kwaliteit van leven na de beademing zijn factoren die meewegen in deze besluitvorming. Ook de mate van kwetsbaarheid (frailty) bij opname op de IC en ernstige interfererende comorbiditeit in de besluitvorming, van dementie tot cardiaal tot maligniteit, kunnen hierbij een rol spelen. De bovengenoemde review benoemt een aantal parameters die houvast kunnen bieden in de voorspelling van de korte termijn overleving na een IC opname. Echter, voorspellers van kwaliteit van leven worden niet genoemd en zijn ook anderszins niet bekend. Patiënt en zorgverleners vinden kwaliteit van leven na een IC opname minstens zo belangrijk als de uitkomst, maar voorspellers daarvan zijn niet onderzocht. Hoewel in de praktijk de FEV1 vaak wordt gebruikt is uit geen enkele studie gebleken dat er een relatie bestaat tussen deze parameter en de zes maanden overleving na een IC opname. Daarnaast blijken artsen de kans op IC-overleving vaak te somber in te schatten (Wildman, 2009; Kant, 2014).
In studies wordt vaak geen onderscheid gemaakt tussen non-invasieve en invasieve mechanische beademing terwijl deze vraag in de klinische setting relevant is. Bovendien wordt non-invasieve beademing in Nederland veelal ook buiten de muren van de IC succesvol ingezet. Non-invasieve beademing heeft de prognose van patiënten met een longaanval duidelijk verbeterd met een afname van invasieve mechanische beademing en kortere opnameduur (NVALT, 2013). Daarbij gaat het falen van non-invasieve beademing vergeleken met het direct inzetten van invasieve beademing niet gepaard met een hogere mortaliteit.
Bespreken en vastleggen van niet-reanimeren en niet-beademen beleid
Het bespreken en vastleggen van niet-beademen niet-reanimeren beleid kan zowel voor patiënt als arts een beladen en emotioneel gespreksonderwerp zijn. Mede hierdoor wordt dit gesprek vaak te laat gevoerd. Indien een goed geïnformeerde, wilsbekwame patiënt een beperkt behandelbeleid en/of geen reanimatie wenst, is deze wens leidend. Wanneer een arts op medische gronden een beperkend beleid afspreekt is dit leidend, omdat de inschatting wordt gemaakt dat bepaalde behandelingen en/of reanimatie geen reële slagingskans geeft. Het is van belang dat de verwachtingen en angst ten aanzien van de toekomst door de arts met de patiënt worden besproken. De werkgroep stelt hierbij voor de volgende punten in acht te nemen:
- ga na of de gedachten van de patiënt en de naasten overeenkomen met wat redelijkerwijs te verwachten is;
- bespreek de wensen ten aanzien van wel/niet-reanimeren en eventueel beademing;
- leg afspraken over wel/niet-reanimeren en beademing vast op een voor betrokkenen toegankelijke plaats;
- maak gebruik van de patiëntenversie van de richtlijn Palliatieve zorg bij COPD (te bestellen bij www.longfonds.nl)
Goede communicatie is essentieel tussen en binnen de lijnen over al eerder besproken behandelbeperkingen, ook door de huisarts, en nieuwe beperkingen naar aanleiding van de opname.
Mockford (2015) beschreef de grote variabiliteit in argumenten voor een niet-reanimeren beleid in een review. Op basis van negatief voorspellende factoren zal een arts individueel een reanimatiebesluit moeten nemen. Er wordt gesteld dat reanimatie moet beschouwd worden als medisch zinloos handelen indien er geen redelijke kans bestaat op overleving met uitblijven van grote schade.
Field (2014) stelde in een review een relatief simpele proces verbetering voor: het protocollair bespreken van een niet-reanimeren beleid op de spoedeisende hulp, voorafgaand aan de opname van de patiënt. Voor de hand liggend kan er indien een niet-beademen beleid wordt afgesproken ook een niet-reanimeren beleid volgen.
CAOS-model
Een gesprek over de zorg rond het levenseinde zal geïntegreerd moeten worden in de reguliere behandeling van COPD. Dit gesprek kan bijvoorbeeld worden gevoerd naar aanleiding van de uitslag op de BODE-index, zuurstofafhankelijkheid, opname voor een COPD-longaanval of de start van een revalidatieproces (Kant, 2014). Voordat men begint met non-invasieve beademing dient nagedacht te worden welke vorm van behandeling aangewezen is indien de non-invasieve beademing faalt. Dit wordt mede bepaald door de mate waarin de patiënt zijn kwaliteit van leven voorafgaand aan de beademing waardeert. Bij de beslissing om over te gaan tot invasieve beademing zullen de prognose, de kwaliteit van leven in een stabiele situatie vóór de opname en de wensen van de patiënt meegenomen dienen te worden. De COPD and Asthma Outcome Score (CAOS-model) lijkt op dit moment het meest geschikt om de prognose in te schatten (Wildman, 2009) (zie bijlage). Kant (2014) stelde dat indien er sprake is van medisch zinloos handelen de behandelend arts de plicht heeft om, in samenspraak met collega’s en met betrokkenheid van de patiënt en naasten, over te gaan van een curatief-palliatieve behandeling op een louter palliatieve behandeling.
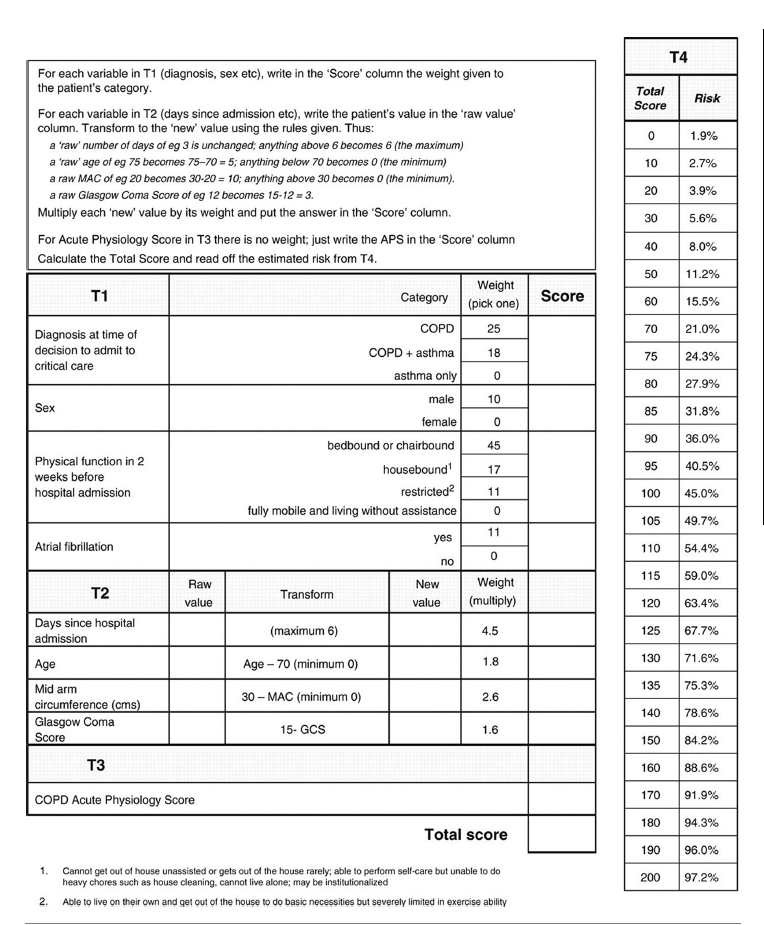
Figuur 1 COPD and Asthma Outcome Score (CAOS-model), Wildman, 2009; Kant, 2014
Onderbouwing
Momenteel is er geen landelijke richtlijn voor het vaststellen van een niet-reanimeerbeleid (NR) niet-beadembeleid (NB) bij patiënten met COPD die in het ziekenhuis zijn opgenomen met een longaanval. De richtlijnen ”Palliatieve zorg voor mensen met COPD (LAN, 2011)” en “Nalaten en staken van behandeling en palliatieve zorg na het staken van behandeling bij volwassen IC patiënten (NVIC, 2009)” bieden hierin enige houvast, maar zijn niet toereikend.
De beslissing om over te gaan tot een vorm van mechanische beademing bij patiënten met een acuut respiratoir falen op basis van een COPD-longaanval wordt beïnvloed door voorspellingen van de kans op overleving en de kwaliteit van leven na de beademing (Kant, 2014). Een goede voorspelling hiervan helpt arts en patiënt bij het maken van een weloverwogen keuze. Het is echter onduidelijke welke factoren goede voorspellers zijn van overleving en kwaliteit van leven na (non)invasieve beademing.
In deze module worden aanbevelingen gedaan over de argumenten welke een rol kunnen spelen bij het bespreken en vastleggen van een behandelbeperking bij patiënten die vanwege een COPD-longaanval zijn opgenomen in het ziekenhuis. Hierbij is ook de timing van het gesprek een belangrijk aspect.
|
|
Er zijn aanwijzingen dat de volgende prognostische variabelen geassocieerd zijn met hogere mortaliteit tot 6 maanden na IC-opname: opnameduur voorafgaand aan IC-opname, IC-opname na een cardiorespiratoir arrest, IC-opname met een lage Glasgow Coma Scale (GCS), de aanwezigheid van ritmestoornissen, lage bi-carbonaat bij IC-opname en een hoge “COPD and Asthma Physiology Score” (CAPS) of APACHE II
Bronnen (Messer, 2012) |
In de review van Messer (2012) worden 28 studies beschreven die voorspellende variabelen van mortaliteit tot zes maanden na IC-opname bij patiënten met een COPD-longaanval onderzochten. Er wordt geconcludeerd dat de volgende zes prognostische variabelen geassocieerd zijn met mortaliteit tot 6 maanden na IC-opname: opnameduur voorafgaand aan IC-opname, IC-opname na een cardiorespiratoir arrest, IC-opname met een lage Glasgow Coma Scale (GCS), de aanwezigheid van ritmestoornissen, laag bi-carbonaat bij IC-opname en een hoge COPD and Asthma Physiology Score (CAPS) of APACHE II. De variabelen leeftijd, geslacht, pulmonale functietesten, BMI waren niet geassocieerd met mortaliteit tot zes maanden na IC-opname. Echter stellen de auteurs dat enkele van deze variabelen wel zijn geassocieerd met een ongunstige uitkomst op langere termijn. Messer beschreef dat in geen van de gevonden studies de resultaten zijn gevalideerd, wat kwantificering van het gevonden effect niet mogelijk maakt.
Messer (2012) maakte in zijn review onder andere gebruik van een studie van Wildman (2009) waarin een predictiemodel wordt gepresenteerd ten aanzien van de kans op overleving en de kwaliteit van leven na de beademing. Dit model, het COPD and Asthma Outcome Score (CAOS)-model, dient ter ondersteuning van de keuze om al dan niet over te gaan tot een vorm van mechanische beademing bij patiënten met een acuut respiratoir falen op basis van een COPD-longaanval. In een prospectieve multicenter cohort studie werden 832 patiënten opgenomen vanwege een COPD-longaanval zes maanden gevolgd. De volgende parameters werden gebruikt om met een logistische regressie en bootstrapping een predictiemodel te ontwikkelen, leeftijd, geslacht, opnameduur, diagnose, fysieke conditie voorafgaand aan opname, mid-upper-arm circumference (MUAC), atriumfibrilleren, CAPS en GCS.
In de bovengenoemde richtlijnen (LAN, 2011; NVIC, 2009) worden bij een literatuursearch geen gevalideerde criteria gevonden waarmee een voorspelling gedaan kan worden over de kans op overlijden <6 maanden. De richtlijnen benoemen wel een aantal voorspellende factoren waarmee de ernst van de ziekte en daarmee de kans op een succesvolle behandeling ingeschat kan worden. Er wordt gesteld dat een FEV1 <30%, slechte bloedgassen, cor pulmonale (met pulmonale hypertensie), MRC dyspnoeschaal score van 5, BMI <21, spiermassaverlies, slechte kwaliteit van leven (CCQ of SGRQ), relevante comorbiditeit factoren zijn die meegewogen moeten worden of beademing en /of reanimatie zinvol is. Hiernaast wordt benoemd dat comorbiditeit en frequente ziekenhuisopnames in verband met longaanvallen zonder herstel ook een rol spelen in deze overweging. De Britse BTS/NICE guideline benoemt leeftijd, FEV1, eerdere IC-opnames, BMI, pulmonale functietesten, mate van zuurstofafhankelijkheid in stabiele status en aanwezigheid van comorbiditeit als factoren om overwegingen te nemen bij het bepalen van het beademingsbeleid. Deze laatste criteria zijn opgesteld vanuit een expert opinion en kunnen derhalve niet leidend zijn in de besluitvorming. De FEV1 wordt vaak in de praktijk gebruikt echter blijkt dit geen voorspeller te zijn voor de halfjaarsoverleving na een IC-opname. Non-invasieve beademing van patiënten met acute respiratoire insufficiëntie met pH<7.35 en paCO2>6.0 Kpa verbetert de mortaliteit (NVALT, 2013).
Bij deze uitgangsvraag is een algemene literatuursearch uitgevoerd. In de databases Medline (OVID), Embase en de Cochrane Library is gezocht naar prognostisch onderzoek van voorspellende variabelen van mortaliteit bij patiënten opgenomen met een COPD-longaanval. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 615 treffers op, en leverde één review en een studie op die direct relevant was voor de beantwoording van de uitgangsvraag. Aangezien bij deze review geen systematische literatuuranalyse werd uitgevoerd worden de resultaten hieronder niet systematisch samengevat. De uitwerking van deze uitgangsvraag is voornamelijk gebaseerd op bovengenoemde review en de richtlijnen palliatieve zorg voor mensen met COPD (LAN, 2011) en de richtlijn nalaten en staken van behandeling en palliatieve zorg na het staken van behandeling bij volwassen IC patiënten (NVIC, 2009). Bij de formulering van de aanbevelingen is gebruik gemaakt van bovengenoemde literatuur en de expert opinion van de werkgroep, zoals beschreven onder het tabblad overwegingen.
- Field RA, Fritz Z, Grova A, et al. Systemic review of interventions to improve appropriate use and outcomes associated with do-not-attempt cardiopulmonary-resuscitation decisions Rescusitation. 2014;85(11)1418-31.
- Kant KM, Djaming RS, Belderbos HMA, et al. Acute respiratoire insufficiëntie door COPD. Ned Tijdschr Geneeskd. 2014;158:ASA5276.
- Longalliantie Nederland. Richtlijn palliatieve zorg voor mensen met COPD. 2011.
- Messer B, Griffiths J, Baudouin SV. The prognostic variables predictive of mortality in patients with an exacerbation of COPD admitted to the ICU: an integrative review. QJM. 2012;105(2):115-26.
- Mockford C, Fritz Z, George R, et al. Do not attempt cardiopulmonary resuscitation (DNACPR) orders; a systemic review of the barriers and fascilitators of decision-making and implementation. Resuscitation. 2015;88:99-113.
- Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose. Richtlijn Non-invasieve beademing tijdens acute respiratoire insufficiëntie bij COPD. 2013.
- NVIC. Richtlijn nalaten en staken van de behandeling en palliatievezorg na het staken van de behandeling bij volwassen IC-patienten. 2009.
- Verenso. Multidisciplinaire Richtlijn Besluitvorming over reanimatie. Anticiperende besluitvorming over reanimatie bij kwetsbare ouderen. Utrecht Verenso 2014.
- Wildman MJ, Sanderson C, Groves J, et al. Predicting mortality for patients with exacerbations of COPD and Asthma in the COPD and Asthma Outcome Study (CAOS). QJM. 2009;102(6):389-99.
Beoordelingsdatum en geldigheid
Publicatiedatum : 13-04-2017
Beoordeeld op geldigheid : 01-01-2017
De richtlijnwerkgroep heeft als doel de richtlijn periodiek (digitaal) van updates te voorzien.
De NVALT en LAN zijn als houder van deze richtlijn de eerstverantwoordelijken voor de actualiteit van deze richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de eerstverantwoordelijken over relevante ontwikkelingen binnen hun vakgebied.
De KNMP heeft als lid van de LAN afgezien van autorisatie om inhoudelijke en procesmatige redenen. Het LAN bestuur, inclusief de overige leden van de LAN, hebben de richtlijn geautoriseerd. KNMP heeft bijgedragen als reviewer.
Algemene gegevens
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor autorisatie en door hen geautoriseerd.
In samenwerking met:
Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose (NVALT)
Long Alliantie Nederland (LAN)
Nederlandse Vereniging voor Intensive Care (NVIC)
Nederlandse Vereniging van Diëtisten (NVD)
Nederlands Instituut van Psychologen (NIP)
Koninklijk Nederlands Genootschap voor Fysiotherapie (KNGF)
Verpleegkundigen & Verzorgenden Nederland (V&VN)
Longfonds
De richtlijnontwikkeling werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel van de richtlijn
In deze richtlijn worden aanbevelingen gedaan over de indicatiestelling van opname, het diagnostisch traject, de medicamenteuze en niet medicamenteuze behandeling tijdens ziekenhuisopname na COPD-longaanval, inclusief criteria voor monitoring en ontslag. Hiermee wordt een bijdrage geleverd aan een meer eenduidige, doelgerichte behandeling van patiënten met een COPD-longaanval in het ziekenhuis.
Beoogde gebruikers van de richtlijn
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen die betrokken zijn bij de zorg voor patiënten met COPD en een longaanval die klinisch moeten worden behandeld. De gebruikers van de richtlijn (en het zorgpad) betreffen dan ook naast de longartsen veel andere medische beroepsgroepen zoals intensivisten, specialisten ouderengeneeskunde, huisartsen, longfunctieanalisten, verpleegkundigen (waaronder verpleegkundig specialisten en longverpleegkundigen), ziekenhuisapothekers, psychologen, fysiotherapeuten, diëtisten en ergotherapeuten.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2014 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten gedurende een ziekenhuisopname na een COPD-longaanval (zie hieronder). De werkgroepleden zijn door hun wetenschappelijke verenigingen gemandateerd voor deelname. De werkgroep werkte gedurende twee jaar aan de totstandkoming van de richtlijn. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
- dr. F.J.J. van den Elshout (voorzitter), longarts, NVALT
- W.J.M. van Litsenburg (vicevoorzitter), verpleegkundig specialist, LAN/V&VN
- prof. Dr. H.A.M. Kerstjens, longarts, NVALT
- drs. P. L. Salomé, huisarts, COPD & Astma Huisartsen Advies Groep NHG
- drs. M.L.J. Scheer, longarts-intensivist, NVIC
- drs. R. van Snippenburg, longarts, NVALT
- dr. M. A. Spruit, fysiotherapeut, KNGF
- M.P.G. Stegers MSc, diëtist, NVD
- P.E.M. Fikkers-Mol MANP, verpleegkundig specialist, V&VN
- dr. J.N. de Voogd, psycholoog, NIP
- dr. S. Holverda, Longfonds (voorheen Astma Fonds)
Met ondersteuning van:
- P.H. Broos MSc, senior adviseur, Kennisinstituut van Medisch Specialisten
- dr. B.H. Stegeman, adviseur, Kennisinstituut van Medisch Specialisten
Met dank aan:
- drs. L. Sekhuis, LAN
Belangenverklaringen
De werkgroepleden hebben schriftelijk verklaard of ze in de laatste vijf jaar een (financieel ondersteunde) betrekking onderhielden met commerciële bedrijven, organisaties of instellingen die in verband staan met het onderwerp van de richtlijn.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Persoonlijke financiele belangen |
Persoonslijke relaties |
Reputatiemanagement |
Extern gefinancierd onderzoek |
Kennisvalorisatie |
Overige belangen |
Getekend |
|
De Voogd |
gezondheidszorg psycholoog CvR UMCG |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
19-nov-15 |
|
Fikkers-Mol |
verpleegkundig specialist ziekenhuis Rijnstaete. |
alg. bestuurslid V&VN Longverpleegkundigen. Hier houd ik me, naast de reguliere bestuurstaken, vooral ook bezig met de scholingen. Hievoor ontvang ik vacatiegeld. |
geen |
geen |
geen |
geen |
geen |
geen |
25-sep-14 |
|
Kerstjens |
hoogleeraar en afdelingshoofd, afd. Longziekten en Tuberculose, Universitair Medisch Centrum Groningen |
tot 29-9-2014 secretaris bestuur Long Alliantie Nederland (onbetaald).Voorzitter Nordelijke CARA Stichting (onbetaald) |
geen PERSOONLIJK fin. Belang; betaling naar UMCG; over afgelopen 5 jaar ad hoc lid adviescommissie /adviseur/spreker voor verschillende farmaceutische bedrijven (Almiral, Astra Zeneca, Boehringer, Chiesi, GlaxoSmithKline, Novartis, Pfizer, Takeda) |
geen PERSOONLIJK fin. Belang; betaling naar UMCG; over afgelopen 5 jaar ad hoc lid adviescommissie /adviseur/spreker voor verschillende farmaceutische bedrijven (Almiral, Astra Zeneca, Boehringer, Chiesi, GlaxoSmithKline, Novartis, Pfizer, Takeda) |
|
over de afgelopen 5 jaar deelname aan onderzoek gefinancierd door overheid, astmafonds/longfonds. AstraZeneca, Boehringer, GlaxoSmithKline, Novartis, Pfizer, Takeda |
geen |
geen |
19-sep-14 |
|
Salomé |
huisarts |
kernlid CAHAG |
geen |
geen |
geen |
geen |
geen |
geen |
2-okt-14 |
|
Scheer |
longarts -intensivist. Volledig werkzaam op de IC in de functie van intensivist |
EMS B instructeur (onbetaald) |
geen |
geen |
geen |
geen |
geen |
geen |
ja 8 jan 2015 |
|
Spruit |
wetenschappelijk adviseur CIRO + te Horn (NL) |
Gastprofessor in Hassels University te Hasselt (B) - betaald |
geen |
geen |
geen |
geen |
werkzaam bij het CIRO+, alwaar longrevalidatie wordt aangeboden als zorgproduct. Verwijzing naar longrevalidatie kan een mogelijk resultaat zijn van de commisie. |
geen |
ja 18 sept 2014 |
|
Stegers |
dietist in CWZ |
geen |
geen |
geen |
ik ben lid van de NVD, maar participerend lid. Vanuit de NVD ook gevraagd voor deze richtlijn. |
2011-2013 meegedaan aan onderzoek Zicht op gewicht via Medizorg B.V. Gegevens zijn verzameld, resultaten moet nog gepresenteerd worden. |
geen |
geen |
25-sep-14 |
|
Van den Elshout |
longarts Rijnstate Ziekenhuis Arnhem (fulltime) voorzitter richtijn commissie |
lid centraal tuchtcollege Den Haag; vacatiegelden komen ten goede aan de maatschap longartsen |
geen |
geen |
geen |
educational Grant GSK voor promovendus |
geen |
geen |
6-okt-14 |
|
Van Litsenburg |
verpleegkundig specialist longgeneeskunde |
Lid kernteam PICASSO |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 3 dec 2014 |
|
Van Snippenburg |
longarts |
vz MCC Diakonessenhuis Utrecht (onbetaald) |
geen |
geen |
lid werkgroep COPD vd NVALT. Lid werkgroep Transmuraal Zorgpad Longaanval LAN. |
in afrondende fase van Liaison studie (in opdracht van Chisi) astma survey studie |
samen met patient een DVD geproduceerd over Bewegen bij COPD voor patieten. Sponsoring door GSK, eenmalig en Swieringa Stichting eenmalig. Auteursrechten van deze DVD liggen bij van der Colk BV. DVD is gratis verstrekt aan zorgverleners tbv patiënten en rechtstreeks aan patiënten. Zolang de voorraad strekt. |
geen |
20-okt-14 |
|
Vercoulen |
Klinisch Psycholoog/sectieleider Medische Psychologie Volwassenen en Ouderen, Radboudumc |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
ja 23 feb 2015 |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door middel van vertegenwoordiging van het Longfonds in de werkgroep. Daarnaast heeft de Longfonds de conceptrichtlijn beoordeeld tijdens de commentaarfase en suggesties voor verbetering van de richtlijn gegeven.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren.
De richtlijn wordt opgenomen in de richtlijnendatabase (www.richtlijnendatabase.nl) waarmee hij toegankelijk is voor alle relevante beroepsgroepen en patiënten. Daarnaast wordt er een samenvatting van de richtlijn gepubliceerd in tijdschriften van de deelnemende wetenschappelijke verenigingen. Ook is de richtlijn te downloaden vanaf de website van betrokken wetenschappelijke verenigingen en de Long Alliantie Nederland.
Werkwijze
AGREE II
Deze richtlijn is opgesteld conform de eisen in het rapport ‘Richtlijnen 2.0’ van de adviescommissie Richtlijnen van de Raad kwaliteit van de Orde van Medisch Specialisten. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II) (www.agreetrust.org), dat een internationaal breed geaccepteerd instrument is voor de beoordeling van de kwaliteit van richtlijnen.
Knelpuntenanalyse
In de eerste fase werden de knelpunten geïnventariseerd. Tevens is gebruikt gemaakt van de knelpuntenanalyse bij de ontwikkeling van het landelijk zorgpad COPD-longaanval met ziekenhuisopname dat parallel aan deze richtlijn is ontwikkeld.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn vervolgens verder uitgewerkt door de leden van de werkgroep en tijdens de werkgroepvergadering vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang als kritiek, belangrijk en onbelangrijk. Tevens definieerde de werkgroep, voor zover mogelijk, wat zij voor een bepaalde uitkomstmaat een klinisch relevant verschil vond, dat wil zeggen wanneer de verbetering in uitkomst een verbetering voor de patiënt is.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar bestaande buitenlandse richtlijnen en naar systematische reviews in Medline (OVID) en Cochrane Library. Vervolgens werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekactie of gebruikte trefwoorden van de zoekactie en de gehanteerde selectiecriteria zijn te vinden in de module van de desbetreffende uitgangsvraag. De gedetailleerde zoekstrategieën zijn vermeld per module.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de kolom ‘Beoordeling kwaliteit studie’ van een evidence-tabel.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidence-tabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor Grading Recommendations Assessment, Development and Evaluation (zie http://gdt.guidelinedevelopment.org/app/handbook/handbook.html).
|
GRADE |
Definitie |
|
Hoog |
|
|
Matig |
|
|
Laag |
|
|
Zeer laag |
|
B) Voor vragen over de waarde van diagnostische tests, schade of bijwerkingen, etiologie en prognose
Bij dit type vraagstelling kan GRADE (nog) niet gebruikt worden. De bewijskracht van de conclusie is bepaald volgens de gebruikelijke EBRO-methode (Van Everdingen, 2004).
Formuleren van de conclusies
Bij interventievragen verwijst de conclusie niet naar een of meer artikelen, maar wordt getrokken op basis van alle studies samen (body of evidence). Hierbij maakten de werkgroepleden de balans op voor elke interventie. Bij het opmaken van de balans werden door de werkgroep de gunstige en ongunstige effecten voor de patiënt afgewogen.
Voor vragen over de waarde van diagnostische tests, schade of bijwerkingen, etiologie en prognose is het wetenschappelijke bewijs samengevat in een of meerdere conclusie(s), waarbij het niveau van het meest relevante bewijs is weergegeven. Omwille van de homogeniteit is het niveau van bewijs voor alle conclusies weergegeven als hoog/matig/laag/zeer laag, waarbij EBRO niveau 1 is vertaald naar hoog, 2 naar matig, 3 naar laag en 4 naar zeer laag.
Wanneer er voor een uitgangsvraag geen systematisch literatuuronderzoek werd verricht, is de literatuur niet beoordeeld op kwaliteit en is de kracht van het bewijs niet bepaald.
Overwegingen
Voor een aanbeveling zijn naast het wetenschappelijke bewijs ook andere aspecten belangrijk, zoals de expertise van de werkgroepleden, patiëntenvoorkeuren, kosten, beschikbaarheid van voorzieningen of organisatorische zaken. Deze aspecten worden, voor zover niet wetenschappelijk onderzocht, vermeld onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven een antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen. Bij het formuleren en graderen van de aanbeveling worden minimaal de volgende vier factoren in ogenschouw genomen: algehele kwaliteit van het wetenschappelijke bewijs; balans tussen voor- en nadelen van de interventie; waarden en voorkeuren van professional en patiënten; en beschikbare middelen.
Indicatorontwikkeling
De werkgroep heeft besloten geen nieuwe indicatoren bij deze richtlijn te ontwikkelen, maar gebruik te maken van de reeds bestaande indicatoren op het gebied van COPD.
Kennislacunes
Tijdens de ontwikkeling van de richtlijn ‘Diagnostiek en Behandeling van een COPD-longaanval in het Ziekenhuis’ is systematisch gezocht naar onderzoeksbevindingen die nuttig konden zijn voor het beantwoorden van de uitgangsvragen. Een deel (of een onderdeel) van de uitgangsvragen is met het resultaat van deze zoekacties te beantwoorden, een groot deel echter niet. Door gebruik te maken van de evidence-based methodiek (EBRO) is duidelijk geworden dat op het terrein van longaanvallen COPD nog lacunes in de beschikbare kennis bestaan. Een inventarisatie hiervan is opgenomen in de bijlage bij de richtlijn.
Literatuur
Atkins D, Best D, Briss PA, et al. Grading quality of evidence and strength of recommendations. BMJ. 2004;328(7454):1490.
Van Everdingen JJE, Burgers JS, Assendelft WJJ, et al. Evidence-based richtlijnontwikkeling. Bohn Stafleu Van Loghum. 2004.
