Mucus evacuerende technieken bij COPD
Uitgangsvraag
Wat is de plaats van mucus evacuerende technieken in de behandeling van patiënten met een COPD-longaanval en sputumproblematiek die zijn opgenomen in het ziekenhuis?
Aanbeveling
Overweeg het toepassen van technieken die sputumevacuatie bevorderen bij patiënten met COPD en sputumproblematiek tijdens een ziekenhuisopname vanwege van een COPD-longaanval. Een voorkeursinterventie kan niet worden aangegeven.
Overwegingen
Een beperkt aantal studies heeft de effecten onderzocht van sputum evacuerende technieken tijdens een COPD-longaanval. Alle interventies werden beschreven als fysiotherapeut-geleide interventies. Vele studies hebben een beperkte steekproefomvang en de interventies en de uitkomstmaten zijn erg verschillend tussen studies. Mede hierdoor zijn de effecten van sputum evacuerende interventies bij patiënten tijdens een ziekenhuisopname voor een COPD-longaanval onduidelijk. Of sputum evacuerende technieken dienen te worden toegepast bij alle patiënten met COPD tijdens een ziekenhuisopname of enkel bij die patiënten met een uitgesproken toename in de hoeveelheid sputum is op dit moment onbekend. Aanvullende evidentie is zeer wenselijk om goede interventie(s) te identificeren bij de juiste doelgroep.
Onderbouwing
Tijdens een longaanval kan een duidelijke toename optreden van klachten zoals kortademigheid, sputum en/of hoesten. Ademhalingstechnieken kunnen mogelijk de kortademigheid verminderen, mede door het evacueren van sputum. Daarnaast kunnen interventies gericht op sputumevacuatie tijdens de ziekenhuisopname positieve invloed hebben op de dyspnoe.
|
Zeer laag GRADE |
Mucus evacuerende interventies bij patiënten opgenomen voor een COPD-longaanval lijken geen verschil te geven ten aanzien van de longfunctie in vergelijking wanneer toegevoegd aan de gangbare behandeling.
Bronnen (Tang, 2010; Goktalay, 2014; Kodric, 2009) |
|
Zeer laag GRADE |
Mucus evacuerende interventies bij patiënten opgenomen voor een COPD-longaanval lijken geen verschil te geven ten aanzien van de opnameduur in het ziekenhuis in vergelijking wanneer toegevoegd aan de gangbare behandeling.
Bronnen (Newton, 1978; Kodric, 2009) |
|
Zeer laag GRADE |
Er zijn zeer voorzichtige aanwijzingen dat mucus evacuerende interventies bij patiënten opgenomen voor een COPD-longaanval een positief effect hebben op het inspanningsvermogen in vergelijking wanneer toegevoegd aan de gangbare behandeling.
Bronnen (Goktalay, 2013) |
Zeer laag GRADE |
Het is onduidelijk of mucus evacuerende interventies effectief zijn ten aanzien van het ophoesten van sputum bij patiënten opgenomen voor een COPD-longaanval in vergelijking wanneer toegevoegd aan de gangbare behandeling.
Bronnen (Kodric, 2009; Bellone, 2002; Newton, 1978; Petersen, 1967; Anthonisen, 1964) |
|
Zeer laag GRADE |
Mucus evacuerende interventies bij patiënten opgenomen voor een COPD-longaanval lijken geen verschil te geven ten aanzien van kwaliteit van leven in vergelijking wanneer toegevoegd aan de gangbare behandeling.
Bronnen (Bosaglu, 2005; Kodric, 2009) |
|
Zeer laag GRADE |
Het is onduidelijk of mucus evacuerende interventies effectief zijn ten aanzien van het verminderen van dyspnoe bij patiënten opgenomen voor een COPD-longaanval in vergelijking wanneer toegevoegd aan de gangbare behandeling.
Bronnen (Goktalay, 2014; Kodric, 2009) |
|
Zeer laag GRADE |
Mucus evacuerende interventies bij patiënten opgenomen voor een COPD-longaanval lijken geen verschil te geven ten aanzien van de noodzaak tot beademen in vergelijking wanneer toegevoegd aan de gangbare behandeling.
Bronnen (Bellone, 2002; Newton, 1978) |
Er werden twee systematische reviews gevonden over patiënten die in het ziekenhuis werden opgenomen omwille van een COPD-longaanval, waarbij het effect van mucus evacuerende interventies werd onderzocht. Uit de literatuurzoekactie kwamen daarnaast nog twee RCTs naar voren die na deze review werden gepubliceerd en aan de inclusiecriteria voldoen. Deze zijn systematisch geanalyseerd en beoordeeld. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidence tabellen. De evidence tabellen en beoordeling van individuele studiekwaliteit zijn opgenomen onder het tabblad Onderbouwing.
Beschrijving studies
In de systematische review van Tang (2010) werd gezocht naar studies die het effect onderzochten van mucus evacuerende interventies, beschreven als chest physiotherapy, sputum clearance techniques, airway clearance techniques en physical therapy, bij patiënten die in het ziekenhuis werden opgenomen met een COPD-longaanval. De zoekstrategie werd in september 2007 uitgevoerd. Op basis van de volgende criteria werden studies geselecteerd: opgenomen in een ziekenhuis als patiënt met een COPD-longaanval en tijdens opnameduur één of meerdere mucus evacuerende technieken gekregen. Uiteindelijk werden er in de review 13 trials in de review geïncludeerd, met in totaal 473 patiënten. De studies met een pre-post design werden geëxcludeerd, zodat er uiteindelijk acht klinische studies met verschillende designs werden meegenomen in de literatuuranalyse.
Verschillende mucus evacuerende interventies werden in de geïncludeerde trials onderzocht, namelijk: houdingsdrainage in verschillende posities, prikkel spirometrie (incentive spirometry), oscillerende positieve expiratoire druk (PEP) via flutter, expiratie met glottis open in laterale positie, intermitterende positieve druk ventilatie (IPPV), PEP met een apart masker, of een combinatie van deze therapieën. Er werden de volgende uitkomsten gemeten, hoeveelheid opgehoest sputum, arteriële bloedgassen, longfunctie, niveau van dyspnoe, inspanningscapaciteit, kwaliteit van leven/functie en opnameduur. Een opdeling van de resultaten op het soort mucus evacuerende interventie was niet mogelijk.
In de review van Osadnik (2012) werd gezocht naar gerandomiseerde studies die de effectiviteit en veiligheid van mucus evacuerende interventies bij patiënten met een COPD-longaanval, stabiele COPD, emfyseem of een chronische bronchitis onderzochten. De zoekstrategie werd in oktober 2011 uitgevoerd. Uiteindelijk werden er vier studies in de review geïncludeerd, die patiënten onderzochten met een COPD-longaanval; Bellone (2002), Newton (1978), Kodric (2009) en Vargas (2005). De studie van Vargas (2005) betrof patiënten die waren opgenomen op de intensive care en valt buiten de inclusiecriteria van deze uitgangsvraag. De werkgroep besloot om de studie van Kodric (2009) apart te includeren en te beschrijven (zie hieronder) voor uitgebreidere analyse van de studie resultaten. De studies van Bellone (2002) en Newton (1978) werden tevens geïncludeerd in de review van Tang (2010).
Aanvullend op de reviews van Tang en Osadnik werd één RCT geïncludeerd welke werd gepubliceerd na het verschijnen van de reviews. In de RCT van Goktalay (2014) werden alle patiënten behandeld met een gestandaardiseerd protocol voor longaanval. De patiënten in de interventiegroep (n=25) kregen aanvullend op dit protocol hoogfrequente borstkas oscillatie therapie. De interventiegroep bestond uit 25 patiënten. Patiënten ondergingen vijf dagen drie keer per dag 20 minuten lang hoogfrequente borstkas oscillatie therapie (20 Hz). Gedurende vijf opnamedagen in het ziekenhuis werden patiënten gevolgd.
De RCT van Kodric (2009) werd in de review van Osadnik al opgenomen maar wordt hier apart beschreven. De interventiegroep (n=30) ontving standaard medische therapie (steroïden, bronchodilatoren en antibiotica volgens GOLD-richtlijnen) aangevuld met mucus evacuerende fysiotherapie (dat wil zeggen expiratie met open glottis in laterale houding. Patiënten ontvingen zeven opeenvolgende dagen twee keer per dag 30 minuten mucus evacuerende fysiotherapie. Na zeven dagen werd in deze groep alleen de standaard medische behandeling voortgezet tot ontslag. De controlegroep (n=29) werd alleen met de standaard medische therapie behandeld.
Resultaten
Falen van behandeling
Deze uitkomstmaat werd in geen van de geïncludeerde studies gerapporteerd.
Terugval
Deze uitkomstmaat werd in geen van de geïncludeerde studies gerapporteerd.
Mortaliteit
Deze uitkomstmaat werd in geen van de geïncludeerde studies gerapporteerd.
Longfunctie (FEV1)
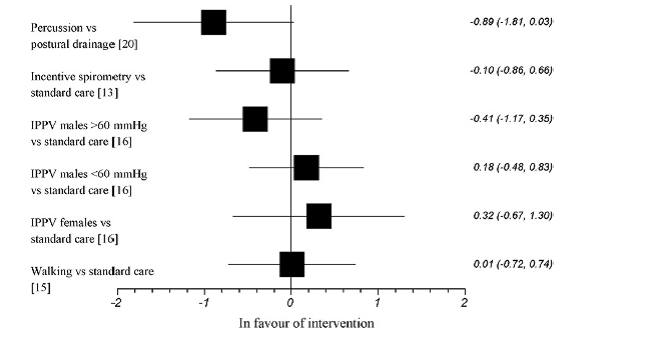
In vier studies uit de review van Tang werd FEV1, genomen als uitkomstmaat. In geen van deze studies werd een significant effect gevonden van een fysiotherapeutische interventie op FEV1 (Basoglu, 2005; Campbell, 1975; Kristen, 1998; Newton, 1978). Resultaten werden in een forest plot weergegeven (zie figuur 1).
Figuur 1 Forest plot voor FEV1. Gestandaardiseerd gemiddeld verschil (95% BI) (Tang, 2010).
In twee aanvullende RCTs werd longfunctie als uitkomstmaat meegenomen. In de RCT van Goktalay werd geen statistisch significant effect gevonden van hoogfrequente borstkas oscillatie therapie op FEV1 (gemiddelden dag 0-dag 3= interventie: 28 (SD 9,0) en 33 (10,5); controle: 30 (SD 8,9) en 33 (SD 11,1); P=0,734; n=50).
In de RCT van Kodric werd geen significant effect gevonden op FEV1 van expiratie met open glottis in laterale houding (gemiddelden opname-ontslag= interventiegroep: 55,6 (SD 27,6) en 64,4 (SD 34,0); controlegroep: 52,3 (SD 18,7) en 57,9 (SD 23,9); P=0,405; n=59).
Opnameduur
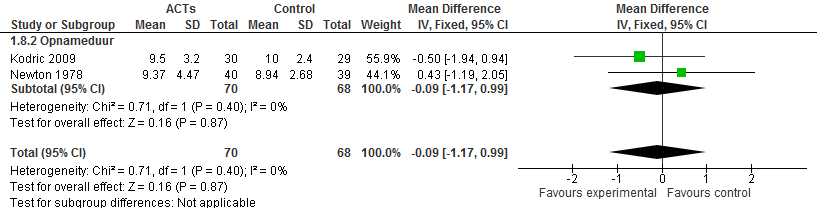
In één relevante studie, zowel geïncludeerd in de review van Tang als in Osadnik werd het effect van IPPV op opnameduur in het ziekenhuis gerapporteerd (niet primaire eindpunt) (Newton, 1978). Er werd geen significant verschil gevonden in opnameduur tussen de interventiegroep (IPPV) en controlegroep. De resultaten werden niet gekwantificeerd weergegeven. In de studie van Kodric werd het effect onderzocht op de opnameduur in het ziekenhuis (Kodric, 2009). Kodric vond geen statistisch significant effect van mucus evacuerende fysiotherapie op opnameduur. Patiënten lagen in de interventiegroep gemiddeld 9,5 dagen (SD 3,2) in het ziekenhuis en de patiënten in de controlegroep 10,0 dagen (SD 2,4). Dit verschil was niet statistisch significant (P=0,530; n=59). Osadnik poolde de resultaten van Kodric en Newton en vond een niet significant verschil in opname duur van -0,09 (95% BI -1,17 tot 0,99) in het voordeel van de interventiegroep (zie figuur 2).
Figuur 2 Forest plot opnameduur, gebaseerd op Osadnik, 2012
Inspanningsvermogen
In de reviews van Tang en Osadnik werd het effect van mucus evacuerende interventies op inspanningsvermogen niet gerapporteerd. In de studie van Goktalay (2013) werd de 6-minuten looptest gemeten als maat voor inspanningsvermogen. In deze studie was er een statistisch significant verschil in de looptest tussen het moment van opname en vijf dagen na opname (interventiegroep: toename van 145 (dag 0) naar 264 (dag 5) meter; controlegroep: toename van 133 (dag 0) naar 208 (dag 5) meter; P=0,000; n=50). Het verschil tussen beide groepen in de gemiddelde verandering van de 6MWD (+120 versus +75m) is groter dan de klinisch relevante verbetering van +30 m (Holland, 2014).
Ophoesten van sputum
In vier studies uit de review van Tang werd het effect van verschillende mucus evacuerende interventies op het ophoesten van sputum in het ziekenhuis onderzocht. Er werd een statistisch significant effect gevonden op het ophoesten van sputum (sputumgewicht) van PEP vergeleken met een gangbare behandeling (gestandaardiseerd gemiddeld verschil 2,54 (95% BI 1,46 tot 3,46; n=27) (Bellone, 2002). Tevens werd een statistisch significant effect gevonden op het ophoesten van sputum van IPPV vergeleken met een gangbare behandeling bij mannen met een partiële druk van zuurstof in het arteriële bloed >60 mmHg (gestandaardiseerd gemiddeld verschil 1,33; 95% BI 0,46 tot 2,12; n wordt niet gerapporteerd) (Newton, 1978). Voor vibratie en een gecombineerde therapie (Anthonisen, 1964; Petersen, 1967) werd geen significant effect gevonden op het ophoesten van sputum. De resultaten van deze laatste twee studies worden in de review niet gekwantificeerd weergegeven.
In de RCT van Kodric werd sputum volume als uitkomstmaat meegenomen. Er was geen statistisch significant verschil tussen de interventiegroep die mucus evacuerende fysiotherapie onderging en de controlegroep die standaardtherapie onderging (interventiegroep= opname: 13,6 (SD 13,6) mL/dag; ontslag; 8,2 (SD 9,4) mL/dag; controlegroep= opname: 19,5 (SD 17,2) mL/dag; ontslag: 6,8 (SD 7,6) mL/dag; P=0,703).
Dyspnoe
In twee studies werd dyspneu als uitkomstmaat meegenomen. In de RCT van Goktalay werd dyspneu gemeten met de Modified Medical Research Council dyspnea scale. Er was geen statistisch significant verschil tussen de interventiegroep (borstkas oscillatie therapie) en de controlegroep (gemiddelden dag 0-dag 5= interventiegroep: 3,32 (SD 0,9) en 3,04 (SD 0,88); controlegroep: 3,36 (SD 0,9) en 3,28 (SD 0,89); P=0,268).
In de RCT van Kodric werd de gemiddelde Borg score gegeven. Er werd een statistisch significant verschil gevonden ten aanzien van expiration with the glottis open in the lateral posture (ELTGOL) op de Borg-score (gemiddelden opname-ontslag= interventiegroep: 5,2 (SD 2,7) en 3,0 (SD 1,8); controlegroep: 4,6 (SD 2,0) en 4,3 (SD 1,5); P=0,004). Ook werd de Medical Research Council (MRC) score meegenomen als een maat voor chronische dyspnoe. Er was geen statistisch significant verschil tussen de interventiegroep en de controlegroep op de MRC-score (gemiddelden opname-ontslag= interventiegroep: 2,9 (SD 1,3) en 3,0 (SD 1,2); controlegroep: 2,5 (SD 1,4) en 2,9 (SD 1,1); P=0,332).
Kwaliteit van leven
In één studie uit de review van Tang werd kwaliteit van leven meegenomen als uitkomstmaat (Bosaglu, 2005). Gerapporteerd werd dat er een significante verbetering was op de St. George Respiratory Questionnaire. In de interventiegroep (Incentive Spirometer) werd een statistisch significante afname van de SGRQ-score tussen baseline (69,1; SD 14.2) en ontslag (44,4 SD 15,0) gerapporteerd. In de controlegroep was geen sprake van een statistisch significante afname. Een vergelijking tussen de groepen werd niet gerapporteerd. Ook de studie van Kodric rapporteerde de uitkomstmaat kwaliteit van leven gemeten met de SGRQ. Er werd geen statistisch significant verschil gevonden tussen de groepen (gem. verschil -2.30, 95%CI -11.80 tot 7.20). Alleen bij de studie van Bosaglu oversteeg de gemiddelde verandering in de interventiegroep het klinisch relevant verschil van -4 punten voor SGRQ-score.
Noodzaak tot beademen
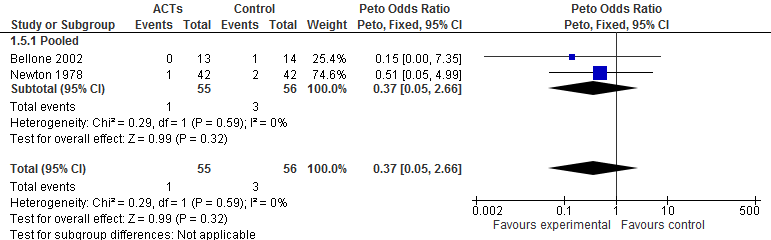
Enkele studies rapporteren over de uitkomstmaat noodzaak tot extra beademing (invasief en non-invasief). Bellone rapporteert over invasieve beademing en vindt een Odds Ratio van 0,33 (BI 95% 0,01 tot 8,83). Newton rapport over non-invasieve beademing en vindt een Odds Ratio van 0,49 (BI 95% 0,04 tot 5,59). Aanvullend hierop werden gepoolde Peto Odds Ratio berekend van 0,37 (BI 95% 0,05 tot 2,66).
Figuur 3 Forest plot noodzaak tot beademen, gebaseerd op Osadnik, 2012
Bijwerkingen
Deze uitkomstmaat werd in geen van de geïncludeerde studies gerapporteerd.
Bewijskracht van de literatuur
De bewijskracht voor alle uitkomstmaten inspanningsvermogen is met drie niveaus verlaagd vanwege beperkingen in de onderzoeksopzet (beperkte blindering), het geringe aantal patiënten (imprecisie) en een verschil in interventies waardoor vergelijking tussen de studies lastig was (indirectheid).
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende vraagstelling:
Wat zijn (on)gunstige effecten van mucus evacuerende technieken bij patiënten met een COPD-longaanval opgenomen in het ziekenhuis met problemen met sputum ten opzichte van standaardtherapie?
P (welke patiëntcategorie) patiënten met een COPD-longaanval opgenomen in het ziekenhuis met problemen met sputum;
I (welke interventie) mucus evacuerende technieken;
C (welke comparison) gebruikelijke zorg;
O (welke uitkomstmaten) falen van behandeling; terugval; mortaliteit; longfunctie (FEV1); opnameduur; inspanningsvermogen; symptomen en kwaliteit van leven; bijwerkingen en noodzaak tot beademen.
Relevante uitkomstmaten
De werkgroep achtte falen van de behandeling, terugval, en opnameduur kritieke uitkomstmaten. Daarnaast zijn inspanningsvermogen, dyspnoe en kwaliteit van leven en noodzaak tot beademen als additionele uitkomstmaten voor besluitvorming benoemd.
De werkgroep definieerde niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities. Ten aanzien van de uitkomstmaat inspanningsvermogen werd op basis van Singh (2014) een klinisch relevante verbetering gedefinieerd als 30 meter afgelegde afstand of meer bij de 6 minute walking test.
Zoeken en selecteren (Methode)
In de databases Medline (OVID), Embase en de Cochrane Library is met relevante zoektermen gezocht naar systematische reviews en gerandomiseerde trials. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 110 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria: systematische review (gezocht in tenminste twee databases met een objectieve en transparante zoekstrategie, data extractie en methodologische beoordeling) of gerandomiseerde trials. In deze trials dienden de behandeling van een fysiotherapeut voor sputum problemen bij patiënten opgenomen in het ziekenhuis vanwege een COPD-longaanval te worden vergeleken met gebruikelijke zorg. Op basis van titel en abstract werden in eerste instantie 34 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 30 studies geëxcludeerd (zie exclusietabel), en vier studies definitief geselecteerd.
Vanwege de heterogeniteit in interventie en uitkomstmaten was het niet mogelijk om de resultaten te poolen. De geïncludeerde studies worden daarom afzonderlijk besproken.
- Anthonisen P, Riis P, Sogaard-Andersen T, et al. The value of lung physiotherapy in the treatment of acute exacerbations in chronic bronchitis. Acta Med Scand. 1964;175:715-9. PMID: 14171977.
- Babu AS, Noone MS, Haneef M, et al. The effects of 'on-call/out of hours' physical therapy in acute exacerbations of chronic obstructive pulmonary disease: a randomized controlled trial. Clin Rehabil. 2010;24(9):802-9. PMID: 20543018.
- Bellone A, Spagnolatti L, Massobrio M, et al. Short-term effects of expiration under positive pressure in patients with acute exacerbation of chronic obstructive pulmonary disease and mild acidosis requiring non-invasive positive pressure ventilation. Intensive Care Med. 2002;28(5):581-5. Epub 2002 Mar 15. PMID: 12029406.
- Campbell AH, O'Connell JM, Wilson F. The effect of chest physiotherapy upon the FEV1 in chronic bronchitis. Med J Aust. 1975;1(2):33-5. PMID: 1128356.
- Cross JL, Elender F, Barton G, et al. Evaluation of the effectiveness of manual chest physiotherapy techniques on quality of life at six months post exacerbation of COPD (MATREX): a randomised controlled equivalence trial. BMC Pulm Med. 2012;12:33. PMID: 22748085
- Goktalay T, Akdemir SE, Alpaydin AO, et al. Does high-frequency chest wall oscillation therapy have any impact on the infective exacerbations of chronic obstructive pulmonary disease? A randomized controlled single-blind study. Clin Rehabil. 2013;27(8):710-8. PMID: 23503735.
- Holland AE, Spruit MA, Troosters T, et al. An official European Respiratory Society/American Thoracic Society technical standard: field walking tests in chronic respiratory disease. Eur Respir J. 2014;44(6):1428-46.
- Kirsten DK, Taube C, Lehnigk B, et al. Exercise training improves recovery in patients with COPD after an acute exacerbation. Respir Med. 1998;92(10):1191-8. PMID: 9926148.
- Kodric M, Garuti G, Colomban M, et al. The effectiveness of a bronchial drainage technique (ELTGOL) in COPD exacerbations. Respirology. 2009;14(3):424-8. PMID: 19192230.
- Newton DA, Bevans HG. Physiotherapy and intermittent positive-pressure ventilation of chronic bronchitis. Br Med J. 1978;2(6151):1525-8. PMID: 365289.
- Petersen ES, Esmann V, Honcke P, et al. A controlled study of the effect of treatment on chronic bronchitis. An evaluation using pulmonary function tests. Acta Med Scand. 1967;182(3):293-305. PMID: 6069924.
- Singh SJ, Puhan MA, Andrianopoulos V, et al. An official systematic review of the European Respiratory Society/American Thoracic Society: measurement properties of field walking tests in chronic respiratory disease. Eur Respir J. 2014;44(6):1447-78.
- Tang CY, Taylor NF, Blackstock FC. Chest physiotherapy for patients admitted to hospital with an acute exacerbation of chronic obstructive pulmonary disease (COPD): a systematic review. Physiotherapy. 2010;96(1):1-13. PMID: 20113757.
- Yohannes AM, Connolly MJ. Early mobilization with walking aids following hospital admission with acute exacerbation of chronic obstructive pulmonary disease. Clin Rehabil. 2003;17(5):465-71. PubMed PMID: 12952150.
Evidence table for intervention studies (randomized controlled trials and non-randomized observational studies [cohort studies, case-control studies, case series])1
This table is also suitable for diagnostic studies (screening studies) that compare the effectiveness of two or more tests. This only applies if the test is included as part of a test-and-treat strategy – otherwise the evidence table for studies of diagnostic test accuracy should be used.
Research question:
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Goktalay, 2013 |
Type of study: RCT
Setting: Stage III-IV COPD patients hospitalized with acute infective exacerbation who had received high-frequency chest wall oscillation therapy
Country: Turkey
Source of funding: Scientific Research Projects Unit, Celal Bayar University (non-commercial) |
Inclusion criteria: - stage 3–4 COPD (GOLD) - hospitalized for infective exacerbations of COPD
Exclusion criteria: - need for invasive mechanical ventilation - bronchiectasis - active lung tuberculosis - chest wall trauma - thoracic or abdominal operation in last 3 months - diagnosis of pulmonary embolism in the last 3 months - diagnosis of myocardial infarction in the last 6 months - thrombocytopenia (<50,000/mm3) plus exacerbation secondary to cardiovascular causes and non-infective exacerbations.
N total at baseline: 50 Intervention: 25 Control: 25
Important prognostic factors2: age ± SD: I: 63.6 ± 8.0 C: 66.5 ± 6.6
Groups were comparable at baseline
|
Treated by acute COPD exacerbation protocol. Received additional high-frequency chest wall oscillation therapy for 20 minutes three times a day for five days. The application and oscillation frequency were standardized at 20 Hz and 10 Hz, respectively.
|
As part of acute COPD exacerbation protocol patients have been treated with bronchodilators, antibiotics, if necessary oxygen and patient education.
|
Length of follow-up: 5 days
Loss-to-follow-up: 0 patients
Incomplete outcome data: 0 patients
|
Exercise capacity 6-minute walk test, median-IQR I: 145 (day 0) to 264 (day 5) m C: 133 (day 0) to 208 (day 5) m P=0.000
Length of stay I: 7 days (range 6-p) C: 7 days (range 6-8), P=0.527
Recurrence Not reported
Physical activity Not reported
Symptom recovery Not reported
Dyspnoea Modified Medical Research Council dyspnea scale, mean (SD) I: 3.32 (0.90) (day 0) to 3.04 (0.88) (day 5) C: 3.36 (0.90) (day 0) to 3.28 (0.89) (day 5) NS difference
Quality of life Not reported
Remaining outcomes measures Blood acidity (pH) I: mean 7.39 (SD 0.03) C: mean 7.40 (SD 0.03) P=0.99
Partial oxygen pressure (PaO2) I: mean 63 (SD 9.11) C: mean 64 (SD 14.06) P=0.72
Oxygen saturation (SpO2) I: mean 90 (SD 4.63) C: mean 90 (SD 5.15) P=0.69 |
|
|
Cross, 2012 |
Type of study: RCT
Setting: patients hospitalised with acute COPD exacerbation
Country: UK
Source of funding: Research grant from the NIHR HTA (non-commercial) |
Inclusion criteria: Patients admitted to hospital with an exacerbation of COPD
Exclusion criteria: - any contraindication to the use of MCP techniques - with no evidence of excess sputum production on auscultation - Osteoporosis, haemoptysis, bronchial hyper-reactivity, respiratory system malignancy, raised intracranial pressure, uncontrolled hypertension (diastolic>110), pulmonary embolism, coagulopathy (platelets <50 and/or INR ≥3), bronchopleural fistula, subcutaneous emphysema and left ventricular failure as primary diagnosis
N total at baseline: 527 Intervention: 261 Control: 266
Important prognostic factors2: age ± SD: I: 69.1 ± 9.9 C: 69.6 ± 9.5
Sex: I: 56% M C: 58% M
Groups were comparable at baseline (no p-values reported) |
Manual chest physiotherapy (MCP) plus advice on airway clearance. Part of the MCP protocol was the Active Cycle of Breathing Technique (ACBT), including breathing control, thoracic expansion exercises and FET.
|
Advice on chest clearance alone
|
Length of follow-up: 6 months
Loss-to-follow-up: Intervention: 72 (28%) Due to: death (n=33), withdrawal (n=8) and non response (n=31)
Control: 78 (29%) Due to: death (n=37), withdrawal (n=6) and non-response (n=35)
Incomplete outcome data: Intervention: 75 (29%) Control: 80 (30%)
|
Exercise capacity Not reported
Length of stay Hospital length of stay in days, mean adjusted difference (95% CI) 1.07 (0.91 to 1.24), P=0.421
Recurrence Not reported
Physical activity Not reported
Symptom recovery Not reported
Dyspnoea Not reported
Quality of life Health-related quality of life with SGRQ score, mean adjusted difference (95% CI) 0.51 (-2.67 to 3.69), P=0.753
|
MCP = Manual chest therapy SGRQ = Saint Georges Respiratory Questionnaire |
|
Babu, 2010 |
Type of study: RCT
Setting: patients hospitalised with acute COPD exacerbation
Country: India
Source of funding: Not reported |
Inclusion criteria: Acute exacerbations of COPD were staged at admission using the Winnipeg Clinical Criteria according to the presence of increased sputum volume, sputum purulence and shortness of breath.
Exclusion criteria: Pulmonary embolism, pulmonary oedema, acute myocardial infarction and acute heart failure
N total at baseline: 38 Intervention: 19 Control: 19
Important prognostic factors2: age ± SD: I: 65 ± 15.9 C: 58 ± 13.3
Sex: I: 74% M C: 68% M
Groups comparable on demographics at baseline. Difference in mean rate pressure product (P=0.003): I: 18680 ± 6241 C: 13227 ±3445
|
Received regular physical therapy and on-call physical therapy services. Physical therapy interventions included positioning, relaxation, breathing control and airway clearance techniques as appropriate. The calls to the therapist on-call were made either by the nursing staff or the resident medical officers.
|
Received the same physical therapy interventions as in the experimental group but only during working hours (i.e. twice a day). No on-call physical therapy services were given. |
Length of follow-up: Admission to discharge
Loss-to-follow-up: 0 patients
Incomplete outcome data: 0 patients
|
Exercise capacity 6-minute walk test, mean (SD) at discharge I: 387.89 (110.1) C: 289.73 (103.2), P=0.004
Length of stay Hospital length of stay in days, mean (SD) I: 4.31 (2.49) C: 5.05 (2.41), P=0.361
Recurrence Not reported
Physical activity Not reported
Symptom recovery Not reported
Dyspnoea Not reported
Quality of life Not reported
Remaining outcomes measures Peak expiratory flow rate (L/min), mean (SD) I: 211.6 (51.1); C: 159.5 (67.8), P=0.01
Median Δ in peak expiratory flow rate 120 (30 to 240) vs 50 (-60 to 170) L/min, P=0.002
Sustained maximal inspiratory rate (cc/s), mean (SD) I: 652.6 (226.9); C: 531.6 (210.9), P=0.09
New York Heart Association functional dyspnoea grading, mean (SD) I: 1.15 (0.95); C: 1.26 (0.65), P=0.695 |
|
|
Kodric, 2009 |
Type of study: RCT
Setting: patients hospitalised with acute COPD exacerbation
Country: Italy
Source of funding: Not reported |
Inclusion criteria: - COPD according to GOLD criteria - Acute exacerbation of COPD defined on the basis of the clinical history, physical examination and CXR and the severity score according to the Anthonisen Criteria
Exclusion criteria: Positive bronchodilator reversibility test or any other chest disease likely to bias results.
N total at baseline: 59 Intervention: 30 Control: 29
Important prognostic factors2: age ± SD: I: 71.3 ± 8.4 C: 69.1 ± 8.3
Sex: I: 67% M C: 72% M
Differences between groups at baseline not tested statistically.
|
Received standard medical therapy and chest physiotherapy (ELTGOL) 30 minutes (after inhaled medications) twice daily for seven consecutive days. After 7 days of treatment, patients were continued on standard medical treatment alone until hospital discharge.
|
Treated with standard medical therapy alone (steroids, bronchodilators and antibiotics) according to the GOLD guidelines.
|
Length of follow-up: 6 months
Loss-to-follow-up: Intervention: 17 (58%) Control: 18 (60%) Due to transport limitations, lack of subjective improvement and no active physiotherapy treatment
Incomplete outcome data: 0 After 1 week and 1 month analysis for overall assessment and quality of life with complete data
|
Exercise capacity Not reported
Length of stay Hospital length of stay in days, mean (SD) I: 9.5 (3.2) C: 10.0 (2.4), P=0.530
Recurrence Not reported
Physical activity Not reported
Symptom recovery Sputum volume (mL/day), mean (SD) Admission I: 19.5 (17.2); C: 13.6 (13.6) Discharge I: 6.8 (7.6); C:8.2 (9.4) P (I vs C) = 0.703
Dyspnoea MRC score (chronic dyspnoea) , mean (SD) Admission I: 2.9 (1.3); C: 3.0 (1.2) Discharge I: 2.5 (1.4); C: 2.9 (1.1) P (I vs C) = 0.332
BORG score (dyspnoea measurement during exercise, 10 steps), mean (SD) Admission I: 5.2 (2.7); C: 4.6 (2.0) Discharge I: 3.0 (1.8); C: 4.3 (2.0) P (I vs C) = 0.004
Quality of life SGRQ score, mean (SD) Admission I: 59.1 (17.3); C: 57.4 (18.7) Discharge I: 54.7 (17.7); C: 54.4 (19.2) P (I vs C) = 0.961
1 month SQRQ score, mean (SD) I: 54.9 (17.3) C: 57.2 (19.8), P=0.775
Remaining outcomes measures FEV, % of predicted, mean (SD) Admission I: 55.6 (27.6); C: 52.3 (18.7) Discharge I: 64.4 (34); C: 57.9 (23.9), P (I vs C) = 0.405 |
Hospitalized patients between March-Sept 2002
MRC = Medical Research Council SGRQ = St George Respiratory Questionnaire |
Notes:
- Prognostic balance between treatment groups is usually guaranteed in randomized studies, but non-randomized (observational) studies require matching of patients between treatment groups (case-control studies) or multivariate adjustment for prognostic factors (confounders) (cohort studies); the evidence table should contain sufficient details on these procedures
- Provide data per treatment group on the most important prognostic factors [(potential) confounders]
- For case-control studies, provide sufficient detail on the procedure used to match cases and controls
- For cohort studies, provide sufficient detail on the (multivariate) analyses used to adjust for (potential) confounders
Evidence table for systematic review of RCTs and observational studies (intervention studies)
Research question: UV10a
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C) |
Follow-up |
Outcome measures and effect size |
Comments |
|
Tang, 2010 |
SR of RCTs, pre-post trials and parallel groups trials
Literature search up to September 2007
13 studies were included in the review. We excluded pre-post studies (n=5).
A: Anthonisen, 1964 B: Basoglu, 2005 C: Bellone, 2002 D: Campbell, 1975 E: Kristen, 1998 F: Newton, 1978 G: Petersen, 1967 H: Yohannes, 2003
Study design: RCT: B, D, G, H, J Non-randomized CT: A, F
Setting and Country: Patients admitted in hospital with AECOPD
Source of funding: Not reported
|
Inclusion criteria SR: - admitted to an acute care hospital as an inpatient with an AECOPD - received ≥ physiotherapy technique during their inpatient stay
Exclusion criteria SR: - patients were intubated and mechanically ventilated - if respiratory mechanics, outcomes and demands for physiotherapy on mechanically ventilated patients are different from self-ventilated patients - if they included patients who were unable to actively participate in physiotherapy interventions
Important patient characteristics at baseline: N, mean age, sex A: 68 patients, 59.5y, 65% M B: 27 patients, 65.5y, 96% M D: 27 patients, 65.0y, 63% M F: 17 patients, 65.5y, %M NA G: 29 patients, 62.3y, 90% M H: 79 patients, 69.5y, 80% M J: 38 patients, 64.0y, 61% M:110 patients, 75y, 54%
Groups comparable at baseline? Not reported |
A: postdural drainage + vibration B: incentive spirometry (5-10 breaths every hour) C: PEP (2 min, 5-7 min/day) D: percussion + postdural drainage E: walking (5 per day) F: combination therapy (3x 10-15 min per day) G: combination therapy H: walking program using gutter framerollator with oxygen/air (3x15 min per day)
|
A: standard care B: standard care C: standard care D: postdural drainage E: standard care F: G: standard care H:
|
End-point of follow-up: Not reported in article.
For how many participants were no complete outcome data available? Not reported
|
Exercise capacity Not reported
Length of stay C: -2.7 days favouring PEP F, H: No differences between groups (no quantitative data reported)
Recurrence Adverse effects C, D: No differences between groups (no quantitative data reported)
Physical activity Not reported
Symptom recovery Lung function B: -0.10 (-0.86 to 0.66) D: -0.89 (-1.81 to 0.03) E: 0.01 (-0.72 to 0.74) F: Males >60 mgHg: -0.41 (-1.17 to 0.35) Males <60 mmHg: 0.18 (-0.48 to 0.83) Females: 0.32 (-0.67 to 1.30)
Sputum expectoration Standardized mean difference (95% CI) C: 2.54 (1.46 to 3.46) F: Males >60 mgHg: 1.33 (0.46 to 2.12) Males <60 mmHg: 0.05 (-0.59 to 0.72) Females: -0.69 (-1.66 to 0.35)
Dyspnoea E: reduction in dyspnoea favouring walking (no quantitative data reported) B, H: No differences between groups (no quantitative data reported)
Quality of life B: significant improvement on St George Respiratory Questionnaire (no quantitative data reported) H: significant improvement in Barthel score (no quantitative data reported) |
No quantitative effect reported of outcomes: Length of stay Adverse effects Perceived level of dyspnoea Quality of life
No meta-analysis performed.
AECOPD: acute exacerbation of COPD |
Risk of bias table for intervention studies (randomized controlled trials)
Research question:
|
Study reference
(first author, publication year) |
Describe method of randomisation1 |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Goktalay, 2013 |
Systematically randomized according to hospitalization date sequentially |
Likely, allocation to date of admission |
Likely, intervention could not be blinded for participants |
Likely, intervention could not be blinded for care providers |
Unlikely, reported that outcome assessors were unaware of allocation. |
Unclear |
Unlikely, no loss to follow-up |
Unlikely |
|
Cross, 2012 |
Randomisation by telephone using a voice-activated, automated system to stratify by site (block size six) |
Unlikely, allocation undertaken by an individual not involved in recruitment |
Likely, intervention could not be blinded for participants |
Likely, intervention could not be blinded for care providers |
Unclear, outcome assessors are not described |
Unlikely |
Likely, high percentage lost to follow-up (I: 28%, C: 29%) |
Unlikely |
|
Babu, 2010 |
Randomisation by computer-generated randomization list (sealed envelopes containing group allocation were opened by the on-call therapist) |
Unlikely |
Likely, this was a non-blinded study |
Likely, this was a non-blinded study |
Likely, this was a non-blinded study |
Unlikely |
Unlikely, no loss to follow-up |
Unlikely |
|
Kodric, 2009 |
Randomization not described |
Unclear, not described |
Likely, this was a non-blinded study |
Likely, this was a non-blinded study |
Unclear, outcome assessors are not described |
Unlikely |
Unlikely |
Unlikely |
- Randomisation: generation of allocation sequences have to be unpredictable, for example computer generated random-numbers or drawing lots or envelopes. Examples of inadequate procedures are generation of allocation sequences by alternation, according to case record number, date of birth or date of admission.
- Allocation concealment: refers to the protection (blinding) of the randomisation process. Concealment of allocation sequences is adequate if patients and enrolling investigators cannot foresee assignment, for example central randomisation (performed at a site remote from trial location) or sequentially numbered, sealed, opaque envelopes. Inadequate procedures are all procedures based on inadequate randomisation procedures or open allocation schedules..
- Blinding: neither the patient nor the care provider (attending physician) knows which patient is getting the special treatment. Blinding is sometimes impossible, for example when comparing surgical with non-surgical treatments. The outcome assessor records the study results. Blinding of those assessing outcomes prevents that the knowledge of patient assignement influences the proces of outcome assessment (detection or information bias). If a study has hard (objective) outcome measures, like death, blinding of outcome assessment is not necessary. If a study has “soft” (subjective) outcome measures, like the assessment of an X-ray, blinding of outcome assessment is necessary.
- Results of all predefined outcome measures should be reported; if the protocol is available, then outcomes in the protocol and published report can be compared; if not, then outcomes listed in the methods section of an article can be compared with those whose results are reported.
- If the percentage of patients lost to follow-up is large, or differs between treatment groups, or the reasons for loss to follow-up differ between treatment groups, bias is likely. If the number of patients lost to follow-up, or the reasons why, are not reported, the risk of bias is unclear
- Participants included in the analysis are exactly those who were randomized into the trial. If the numbers randomized into each intervention group are not clearly reported, the risk of bias is unclear; an ITT analysis implies that (a) participants are kept in the intervention groups to which they were randomized, regardless of the intervention they actually received, (b) outcome data are measured on all participants, and (c) all randomized participants are included in the analysis.
Table of quality assessment for systematic reviews of RCTs and observational studies
Based on AMSTAR checklist (Shea et al.; 2007, BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher et al 2009, PLoS Med 6: e1000097; doi:10.1371/journal.pmed1000097)
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Tang, 2010 |
Yes |
Yes |
Yes |
Yes |
NA |
Yes |
No (no meta-analysis performed) |
No |
No |
- Research question (PICO) and inclusion criteria should be appropriate and predefined
- Search period and strategy should be described; at least Medline searched; for pharmacological questions at least Medline + EMBASE searched
- Potentially relevant studies that are excluded at final selection (after reading the full text) should be referenced with reasons
- Characteristics of individual studies relevant to research question (PICO), including potential confounders, should be reported
- Results should be adequately controlled for potential confounders by multivariate analysis (not applicable for RCTs)
- Quality of individual studies should be assessed using a quality scoring tool or checklist (Jadad score, Newcastle-Ottawa scale, risk of bias table etc.)
- Clinical and statistical heterogeneity should be assessed; clinical: enough similarities in patient characteristics, intervention and definition of outcome measure to allow pooling? For pooled data: assessment of statistical heterogeneity using appropriate statistical tests (e.g. Chi-square, I2)?
- An assessment of publication bias should include a combination of graphical aids (e.g., funnel plot, other available tests) and/or statistical tests (e.g., Egger regression test, Hedges-Olken). Note: If no test values or funnel plot included, score “no”. Score “yes” if mentions that publication bias could not be assessed because there were fewer than 10 included studies.
- Sources of support (including commercial co-authorship) should be reported in both the systematic review and the included studies. Note: To get a “yes,” source of funding or support must be indicated for the systematic review AND for each of the included studies.
Beoordelingsdatum en geldigheid
Publicatiedatum : 13-04-2017
Beoordeeld op geldigheid : 01-01-2017
De richtlijnwerkgroep heeft als doel de richtlijn periodiek (digitaal) van updates te voorzien.
De NVALT en LAN zijn als houder van deze richtlijn de eerstverantwoordelijken voor de actualiteit van deze richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de eerstverantwoordelijken over relevante ontwikkelingen binnen hun vakgebied.
De KNMP heeft als lid van de LAN afgezien van autorisatie om inhoudelijke en procesmatige redenen. Het LAN bestuur, inclusief de overige leden van de LAN, hebben de richtlijn geautoriseerd. KNMP heeft bijgedragen als reviewer.
Algemene gegevens
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor autorisatie en door hen geautoriseerd.
In samenwerking met:
Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose (NVALT)
Long Alliantie Nederland (LAN)
Nederlandse Vereniging voor Intensive Care (NVIC)
Nederlandse Vereniging van Diëtisten (NVD)
Nederlands Instituut van Psychologen (NIP)
Koninklijk Nederlands Genootschap voor Fysiotherapie (KNGF)
Verpleegkundigen & Verzorgenden Nederland (V&VN)
Longfonds
De richtlijnontwikkeling werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel van de richtlijn
In deze richtlijn worden aanbevelingen gedaan over de indicatiestelling van opname, het diagnostisch traject, de medicamenteuze en niet medicamenteuze behandeling tijdens ziekenhuisopname na COPD-longaanval, inclusief criteria voor monitoring en ontslag. Hiermee wordt een bijdrage geleverd aan een meer eenduidige, doelgerichte behandeling van patiënten met een COPD-longaanval in het ziekenhuis.
Beoogde gebruikers van de richtlijn
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen die betrokken zijn bij de zorg voor patiënten met COPD en een longaanval die klinisch moeten worden behandeld. De gebruikers van de richtlijn (en het zorgpad) betreffen dan ook naast de longartsen veel andere medische beroepsgroepen zoals intensivisten, specialisten ouderengeneeskunde, huisartsen, longfunctieanalisten, verpleegkundigen (waaronder verpleegkundig specialisten en longverpleegkundigen), ziekenhuisapothekers, psychologen, fysiotherapeuten, diëtisten en ergotherapeuten.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2014 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten gedurende een ziekenhuisopname na een COPD-longaanval (zie hieronder). De werkgroepleden zijn door hun wetenschappelijke verenigingen gemandateerd voor deelname. De werkgroep werkte gedurende twee jaar aan de totstandkoming van de richtlijn. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
- dr. F.J.J. van den Elshout (voorzitter), longarts, NVALT
- W.J.M. van Litsenburg (vicevoorzitter), verpleegkundig specialist, LAN/V&VN
- prof. Dr. H.A.M. Kerstjens, longarts, NVALT
- drs. P. L. Salomé, huisarts, COPD & Astma Huisartsen Advies Groep NHG
- drs. M.L.J. Scheer, longarts-intensivist, NVIC
- drs. R. van Snippenburg, longarts, NVALT
- dr. M. A. Spruit, fysiotherapeut, KNGF
- M.P.G. Stegers MSc, diëtist, NVD
- P.E.M. Fikkers-Mol MANP, verpleegkundig specialist, V&VN
- dr. J.N. de Voogd, psycholoog, NIP
- dr. S. Holverda, Longfonds (voorheen Astma Fonds)
Met ondersteuning van:
- P.H. Broos MSc, senior adviseur, Kennisinstituut van Medisch Specialisten
- dr. B.H. Stegeman, adviseur, Kennisinstituut van Medisch Specialisten
Met dank aan:
- drs. L. Sekhuis, LAN
Belangenverklaringen
De werkgroepleden hebben schriftelijk verklaard of ze in de laatste vijf jaar een (financieel ondersteunde) betrekking onderhielden met commerciële bedrijven, organisaties of instellingen die in verband staan met het onderwerp van de richtlijn.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Persoonlijke financiele belangen |
Persoonslijke relaties |
Reputatiemanagement |
Extern gefinancierd onderzoek |
Kennisvalorisatie |
Overige belangen |
Getekend |
|
De Voogd |
gezondheidszorg psycholoog CvR UMCG |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
19-nov-15 |
|
Fikkers-Mol |
verpleegkundig specialist ziekenhuis Rijnstaete. |
alg. bestuurslid V&VN Longverpleegkundigen. Hier houd ik me, naast de reguliere bestuurstaken, vooral ook bezig met de scholingen. Hievoor ontvang ik vacatiegeld. |
geen |
geen |
geen |
geen |
geen |
geen |
25-sep-14 |
|
Kerstjens |
hoogleeraar en afdelingshoofd, afd. Longziekten en Tuberculose, Universitair Medisch Centrum Groningen |
tot 29-9-2014 secretaris bestuur Long Alliantie Nederland (onbetaald).Voorzitter Nordelijke CARA Stichting (onbetaald) |
geen PERSOONLIJK fin. Belang; betaling naar UMCG; over afgelopen 5 jaar ad hoc lid adviescommissie /adviseur/spreker voor verschillende farmaceutische bedrijven (Almiral, Astra Zeneca, Boehringer, Chiesi, GlaxoSmithKline, Novartis, Pfizer, Takeda) |
geen PERSOONLIJK fin. Belang; betaling naar UMCG; over afgelopen 5 jaar ad hoc lid adviescommissie /adviseur/spreker voor verschillende farmaceutische bedrijven (Almiral, Astra Zeneca, Boehringer, Chiesi, GlaxoSmithKline, Novartis, Pfizer, Takeda) |
|
over de afgelopen 5 jaar deelname aan onderzoek gefinancierd door overheid, astmafonds/longfonds. AstraZeneca, Boehringer, GlaxoSmithKline, Novartis, Pfizer, Takeda |
geen |
geen |
19-sep-14 |
|
Salomé |
huisarts |
kernlid CAHAG |
geen |
geen |
geen |
geen |
geen |
geen |
2-okt-14 |
|
Scheer |
longarts -intensivist. Volledig werkzaam op de IC in de functie van intensivist |
EMS B instructeur (onbetaald) |
geen |
geen |
geen |
geen |
geen |
geen |
ja 8 jan 2015 |
|
Spruit |
wetenschappelijk adviseur CIRO + te Horn (NL) |
Gastprofessor in Hassels University te Hasselt (B) - betaald |
geen |
geen |
geen |
geen |
werkzaam bij het CIRO+, alwaar longrevalidatie wordt aangeboden als zorgproduct. Verwijzing naar longrevalidatie kan een mogelijk resultaat zijn van de commisie. |
geen |
ja 18 sept 2014 |
|
Stegers |
dietist in CWZ |
geen |
geen |
geen |
ik ben lid van de NVD, maar participerend lid. Vanuit de NVD ook gevraagd voor deze richtlijn. |
2011-2013 meegedaan aan onderzoek Zicht op gewicht via Medizorg B.V. Gegevens zijn verzameld, resultaten moet nog gepresenteerd worden. |
geen |
geen |
25-sep-14 |
|
Van den Elshout |
longarts Rijnstate Ziekenhuis Arnhem (fulltime) voorzitter richtijn commissie |
lid centraal tuchtcollege Den Haag; vacatiegelden komen ten goede aan de maatschap longartsen |
geen |
geen |
geen |
educational Grant GSK voor promovendus |
geen |
geen |
6-okt-14 |
|
Van Litsenburg |
verpleegkundig specialist longgeneeskunde |
Lid kernteam PICASSO |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 3 dec 2014 |
|
Van Snippenburg |
longarts |
vz MCC Diakonessenhuis Utrecht (onbetaald) |
geen |
geen |
lid werkgroep COPD vd NVALT. Lid werkgroep Transmuraal Zorgpad Longaanval LAN. |
in afrondende fase van Liaison studie (in opdracht van Chisi) astma survey studie |
samen met patient een DVD geproduceerd over Bewegen bij COPD voor patieten. Sponsoring door GSK, eenmalig en Swieringa Stichting eenmalig. Auteursrechten van deze DVD liggen bij van der Colk BV. DVD is gratis verstrekt aan zorgverleners tbv patiënten en rechtstreeks aan patiënten. Zolang de voorraad strekt. |
geen |
20-okt-14 |
|
Vercoulen |
Klinisch Psycholoog/sectieleider Medische Psychologie Volwassenen en Ouderen, Radboudumc |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
ja 23 feb 2015 |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door middel van vertegenwoordiging van het Longfonds in de werkgroep. Daarnaast heeft de Longfonds de conceptrichtlijn beoordeeld tijdens de commentaarfase en suggesties voor verbetering van de richtlijn gegeven.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren.
De richtlijn wordt opgenomen in de richtlijnendatabase (www.richtlijnendatabase.nl) waarmee hij toegankelijk is voor alle relevante beroepsgroepen en patiënten. Daarnaast wordt er een samenvatting van de richtlijn gepubliceerd in tijdschriften van de deelnemende wetenschappelijke verenigingen. Ook is de richtlijn te downloaden vanaf de website van betrokken wetenschappelijke verenigingen en de Long Alliantie Nederland.
Werkwijze
AGREE II
Deze richtlijn is opgesteld conform de eisen in het rapport ‘Richtlijnen 2.0’ van de adviescommissie Richtlijnen van de Raad kwaliteit van de Orde van Medisch Specialisten. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II) (www.agreetrust.org), dat een internationaal breed geaccepteerd instrument is voor de beoordeling van de kwaliteit van richtlijnen.
Knelpuntenanalyse
In de eerste fase werden de knelpunten geïnventariseerd. Tevens is gebruikt gemaakt van de knelpuntenanalyse bij de ontwikkeling van het landelijk zorgpad COPD-longaanval met ziekenhuisopname dat parallel aan deze richtlijn is ontwikkeld.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn vervolgens verder uitgewerkt door de leden van de werkgroep en tijdens de werkgroepvergadering vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang als kritiek, belangrijk en onbelangrijk. Tevens definieerde de werkgroep, voor zover mogelijk, wat zij voor een bepaalde uitkomstmaat een klinisch relevant verschil vond, dat wil zeggen wanneer de verbetering in uitkomst een verbetering voor de patiënt is.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar bestaande buitenlandse richtlijnen en naar systematische reviews in Medline (OVID) en Cochrane Library. Vervolgens werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekactie of gebruikte trefwoorden van de zoekactie en de gehanteerde selectiecriteria zijn te vinden in de module van de desbetreffende uitgangsvraag. De gedetailleerde zoekstrategieën zijn vermeld per module.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de kolom ‘Beoordeling kwaliteit studie’ van een evidence-tabel.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidence-tabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor Grading Recommendations Assessment, Development and Evaluation (zie http://gdt.guidelinedevelopment.org/app/handbook/handbook.html).
|
GRADE |
Definitie |
|
Hoog |
|
|
Matig |
|
|
Laag |
|
|
Zeer laag |
|
B) Voor vragen over de waarde van diagnostische tests, schade of bijwerkingen, etiologie en prognose
Bij dit type vraagstelling kan GRADE (nog) niet gebruikt worden. De bewijskracht van de conclusie is bepaald volgens de gebruikelijke EBRO-methode (Van Everdingen, 2004).
Formuleren van de conclusies
Bij interventievragen verwijst de conclusie niet naar een of meer artikelen, maar wordt getrokken op basis van alle studies samen (body of evidence). Hierbij maakten de werkgroepleden de balans op voor elke interventie. Bij het opmaken van de balans werden door de werkgroep de gunstige en ongunstige effecten voor de patiënt afgewogen.
Voor vragen over de waarde van diagnostische tests, schade of bijwerkingen, etiologie en prognose is het wetenschappelijke bewijs samengevat in een of meerdere conclusie(s), waarbij het niveau van het meest relevante bewijs is weergegeven. Omwille van de homogeniteit is het niveau van bewijs voor alle conclusies weergegeven als hoog/matig/laag/zeer laag, waarbij EBRO niveau 1 is vertaald naar hoog, 2 naar matig, 3 naar laag en 4 naar zeer laag.
Wanneer er voor een uitgangsvraag geen systematisch literatuuronderzoek werd verricht, is de literatuur niet beoordeeld op kwaliteit en is de kracht van het bewijs niet bepaald.
Overwegingen
Voor een aanbeveling zijn naast het wetenschappelijke bewijs ook andere aspecten belangrijk, zoals de expertise van de werkgroepleden, patiëntenvoorkeuren, kosten, beschikbaarheid van voorzieningen of organisatorische zaken. Deze aspecten worden, voor zover niet wetenschappelijk onderzocht, vermeld onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven een antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen. Bij het formuleren en graderen van de aanbeveling worden minimaal de volgende vier factoren in ogenschouw genomen: algehele kwaliteit van het wetenschappelijke bewijs; balans tussen voor- en nadelen van de interventie; waarden en voorkeuren van professional en patiënten; en beschikbare middelen.
Indicatorontwikkeling
De werkgroep heeft besloten geen nieuwe indicatoren bij deze richtlijn te ontwikkelen, maar gebruik te maken van de reeds bestaande indicatoren op het gebied van COPD.
Kennislacunes
Tijdens de ontwikkeling van de richtlijn ‘Diagnostiek en Behandeling van een COPD-longaanval in het Ziekenhuis’ is systematisch gezocht naar onderzoeksbevindingen die nuttig konden zijn voor het beantwoorden van de uitgangsvragen. Een deel (of een onderdeel) van de uitgangsvragen is met het resultaat van deze zoekacties te beantwoorden, een groot deel echter niet. Door gebruik te maken van de evidence-based methodiek (EBRO) is duidelijk geworden dat op het terrein van longaanvallen COPD nog lacunes in de beschikbare kennis bestaan. Een inventarisatie hiervan is opgenomen in de bijlage bij de richtlijn.
Literatuur
Atkins D, Best D, Briss PA, et al. Grading quality of evidence and strength of recommendations. BMJ. 2004;328(7454):1490.
Van Everdingen JJE, Burgers JS, Assendelft WJJ, et al. Evidence-based richtlijnontwikkeling. Bohn Stafleu Van Loghum. 2004.
Zoekverantwoording
|
Uitgangsvraag: Wat is de positie van de fysiotherapeut bij sputumevacuatie/ ademhalingstechnieken? |
|
|
Database(s): Medline en Embase |
Datum: 29-12-2015 |
|
Periode: > 2005 |
Talen: Engels |
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID)
|
1 ((exp *Pulmonary Disease, Chronic Obstructive/ or ('chronic obstructive' adj2 (lung or pulmonary or airway)).ab,ti. or copd.ab,ti. or chronic bronchitis.ab,ti. or exp *Emphysema/ or emphysema.ab,ti.) and (exacerbation* or emergenc* or acute).ab,ti.) or aecopd.ab,ti.
2 exp Chest Wall Oscillation/ or exp Breathing Exercises/ or chest wall oscillation*.ab,ti. or airway clearance.ab,ti. or (breathing adj1 exercise*).ab,ti. or percussive ventilation.ab,ti.
1 and 2 and limit to (yr="2005 -Current" and english)
and (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/)
and (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) |
110 |
|
Embase |
'chronic obstructive lung disease'/exp OR 'chronic obstructive' NEAR/2 (lung OR pulmonary OR airway) OR 'copd':ab,ti OR 'chronic bronchitis':ab,ti OR emphysema:ab,ti OR aecopd:ab,ti AND (exacerbat*:ab,ti OR emergenc*.ab,ti OR acute.ab,ti) OR aecopd:ab,ti
AND ('chest wall oscillation'/exp OR 'breathing exercise'/exp OR 'airway clearance':ab,ti OR 'chest wall oscillation':ab,ti OR (breathing NEAR/1 exercise*):ab,ti OR 'percussive ventilation':ab,ti)
AND [english]/lim AND [2005-2015]/py
AND ('meta analysis'/de OR cochrane:ab OR embase:ab OR psychlit:ab OR cinahl:ab OR medline:ab OR (systematic NEAR/1 (review OR overview)):ab,ti OR (meta NEAR/1 analy*):ab,ti OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT ('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp NOT 'human'/exp)
OR ('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it) |
