Bronchusverwijders bij COPD
Uitgangsvraag
Wat is de positie van bronchusverwijders bij de behandeling van patiënten met COPD-longaanval?
Aanbeveling
Geef β2-agonisten of anticholinergica of een combinatie van beide middelen tijdens een opname voor een COPD-longaanval.
Geef bij voorkeur langwerkende bronchusverwijders tijdens een opname voor een COPD-longaanval.
Geef naast de vaste dosering bronchusverwijders in het ziekenhuis, indien extra bronchusverwijders nodig zijn, dezelfde langwerkende middelen in hetzelfde apparaat waarmee de totale dosering doorgaans uitkomt boven de standaard dosering in de stabiele situatie.
Geef tijdens opname voor een COPD-longaanval bij voorkeur de bronchusverwijders via de toedieningsvorm die ook thuis gebruikt wordt, en benut de opname voor goede instructie en begeleiding van inname van de bronchusverwijders. Pas desgewenst de inhalatietherapie aan volgens de richtlijn Goed gebruik inhalatiemedicatie (LAN).
Overwegingen
Wat betreft het gebruik van kortwerkende bronchusverwijders bij de behandeling van een longaanval handhaaft de werkgroep de samenvatting van de literatuur uit de richtlijn Diagnostiek en behandeling van COPD (2010). De richtlijn beschrijft het volgende: Bestaande literatuur over het gebruik van kortwerkende β2-agonisten, anticholinergica of combinatie van beide werd beschreven. McCrory en Brown publiceerden een Cochrane-review waarbij β2-agonisten en anticholinergica toediening bij patiënten met een COPD-longaanval werd bestudeerd (McCrory, 2002). Hierin zijn vier RCTs geïncludeerd waarin ipratropium werd vergeleken met β2-agonisten en vijf RCTs waarin een vergelijking een combinatie van beide middelen versus β2- agonisten alleen werd gemaakt (447 patiënten met een COPD-longaanval, gemiddelde leeftijd 57,6-69,2 jaar, FEV1 dag één longaanval 0,44-0,93 L).
In de review van McCrory (2002) vergeleken vier onderzoeken de effecten van ipratropium versus β2-agonisten. Geconcludeerd werd dat anticholinergica eenzelfde response op FEV1 gaven als β2-agonisten (WMD 0,0 L 95%BI –0,19 tot 0,19 L). In vijf onderzoeken werd een vergelijking gemaakt van de combinatie van beide middelen versus β2-agonisten alleen. De combinatie van beide middelen had geen duidelijk voordeel ten opzichte van β2-agonisten alleen, noch op korte termijn (90 min) (95%BI WMD –0,08 tot 0,12 L) noch op lange termijn (24 uur) (WMD –0,05 L 95%BI –0,14 tot 0,05 L) (McCrory, 2002). Er werd geen verschil in PaO2 gevonden tussen beide interventies (McCrory, 2002). Concluderend hebben anticholinergica en β2-agonisten een vergelijkbaar effect op luchtwegverwijding bij patiënten met een COPD-longaanval. Er is geen bewijs dat een combinatie van β2-agonisten en ipratropium een beter effect heeft bij een COPD-longaanval dan een van beide middelen alleen.
In veel ziekenhuizen wordt traditioneel bij patiënten opgenomen voor een COPD-longaanval verneveld met kortwerkende bronchusverwijders. Zoals te zien uit de literatuur ontbreekt de goede onderbouwing voor verneveling tijdens opname voor een COPD-longaanval. In reviews is geen meerwaarde van verneveling in stabiele toestand of bij verslechtering zonder opname gevonden. Overigens geven veel patiënten wel aan dat zij een verneveling plezierig vinden. Het is onduidelijk of dit te maken heeft met de genomen rust en tijd voor de verneveling of met het verschil tussen de ideale onderzoeks-setting versus “real life” is onduidelijk.
Het is irrationeel tijdens opname van langwerkende bronchusverwijders over te stappen op kortwerkende. Immers, is bekend dat in de stabiele fase het effect van de langwerkende doorgaans groter is dan dat van de kortwerkende. Bovendien houdt het effect langer aan. Beiden zijn belangrijk in de acute situatie, waarin het effect toch al geringer is en het merkbare effect korter.
De reden om kortwerkende luchtwegverwijders in plaats van langwerkende te geven is waarschijnlijk historisch gegroeid. Ten eerste kunnen de meeste langwerkende niet verneveld worden. Ten tweede gold voor de kortwerkende β2-agonisten dat ze sneller werkten dan de eerst verkrijgbare langwerkende β2-agonist (sameterol). Voor andere langwerkende β2-agonisten geldt dat niet of in mindere mate, en ook voor de anticholinergica is de situatie anders (tiotropium ruwweg zelfde inwerkingstredingstijd; glycopyrronium kortere tijd).
Met het oog op het voortzetten van bronchusverwijdende behandeling in de thuissituatie (niet per vernevelaar) kan de opname benut worden om het inhaleren te oefenen onder moeilijke omstandigheden, techniek zo nodig te verbeteren, en het vertrouwen van patiënten te vergroten dat ze problemen wellicht ook thuis kunnen oplossen. Vernevelaars zouden enkel de voorkeur hebben bij een duidelijk groter bronchus verwijdend effect of effect op dyspnoe, waarvoor geen bewijs is gevonden. Bij presentatie op de spoedeisende hulp kan eenmalig verneveling overwogen worden.
Is er een probleem om extra langwerkenden te geven tijdens een longaanval, boven aanbevolen doseringen? Met langwerkende is er de facto vaak terughoudendheid om hoger te doseren dan de maximale dosering die voor de stabiele situatie gedefinieerd is. Soms wordt die maximum dosering niet eens gehaald (formoterol bijvoorbeeld heeft een maximale dosering van 96 microgram). Die terughoudendheid lijkt er met vernevelingen in de acute situatie niet te zijn. Met verneveling is de totale dosering van bronchusverwijder die in het lichaam komt (hoewel niet noodzakelijkerwijs in de long) doorgaans aanzienlijk groter dan met droog poeder of dosisaerosol met voorzetkamer. Bovendien wordt tijdens opname ook bij een patiënt met forse obstructie de verneveling frequent herhaald, beiden ondanks het risico op bijwerkingen. Het geven van extra langwerkende bronchusverwijders kan in het ziekenhuis derhalve een goed en te verkiezen alternatief zijn voor vernevelingen, met een vergelijkbaar risico op bijwerkingen.
Onderbouwing
Kortwerkende β2-agonisten, anticholinergica of een combinatie van beide worden gebruikt in de behandeling van een COPD-longaanval (GOLD, 2016; ATS/ERS, 2004; NVALT, 2010). Er zijn nog onvoldoende publicaties over de effectiviteit van langwerkende β2-agonisten bij patiënten met een COPD-longaanval. Tevens is het niet bekend wat de gewenste toedieningsvorm is.
Vergelijking 1: Langwerkende versus kortwerkende bronchusverwijder
|
Zeer laag GRADE |
Het effect van de langwerkende bronchusverwijder indacaterol in een droog poeder inhalator na vijf dagen op longfunctie is mogelijk groter vergeleken met de kortwerkende bronchusverwijder salbutamol in een vernevelaar.
Bronnen (Segreti, 2013) |
Vergelijking 2: Inhalatiemethode van bronchusverwijder
|
Zeer laag GRADE |
Het effect van een bronchusverwijder op de longfunctie van patiënten opgenomen met een COPD-longaanval is mogelijk niet verschillend bij toediening via een MDI spacer of via een vernevelaar.
Bronnen (Mazhar, 2007; Berry, 1989; Turner, 1988) |
|
Zeer laag GRADE |
Het effect van een bronchusverwijder op de dyspneu van patiënten opgenomen met een COPD-longaanval is mogelijk niet verschillend bij toediening via een MDI spacer of via een vernevelaar ..
Bronnen (Berry, 1989; Turner, 1988) |
Vergelijking 1: Langwerkende versus kortwerkende bronchusverwijder
Beschrijving studies
Segreti (2013) onderzocht de effecten van een langwerkende β2-agonist indacaterol eenmaal daags in patiënten met COPD die zich met een longaanval op de eerste hulp presenteerden. 29 patiënten met een longaanval in de afgelopen vier dagen die opgenomen diende te worden, waren geïncludeerd. Patiënten kregen eenmaal daags 300 µg indacaterol maleate in een Breezhaler inhalator (droog poeder inhalatie) of drie maal daags 1250 µg salbutamol in een vernevelaar. Alle patiënten ontvingen ook driemaal daags 500 µg ipratropium bromide aerosol, tweemaal daags 20 mg methylprednisolon intraveneus en eenmaal daags 500 mg levoflexacin oraal. 19 patiënten waren naar indacaterol gerandomiseerd en tien patiënten kregen salbutamol. De onderzochte vergelijking betreft een langwerkende bronchusverwijder in een droog poeder inhalator versus een kortwerkende bronchusverwijder in vernevelaar. Dit is een scheve vergelijking; echter, een vernevelaar met salbutamol is een onderdeel van reguliere zorg en zal daarom hier beschreven worden.
Resultaten
1. Longfunctie
In de trial van Segreti (2013) werd de FEV1 gemeten en de resultaten alleen in een grafiek weergegeven (zie figuur 1). De vergelijkende statistiek tussen de armen werd niet gegeven.
Figuur 1 Invloed van een vijfdaagse behandeling met salbutamol (A&C) of indacaterol (B&D) op FEV1, FVC, PEF en FEV1/FVC ratio uitgedrukt in liters of % voorspeld op dag 1 en dag 5 (Segreti (2013)).

Uit de grafiek of in de tekst is niet goed af te leiden wat het effect van indacaterol in droog poeder inhalator in vergelijking met verneveling van salbutamol op longfunctie is. Beiden laten een toename zien, waarbij die op indacaterol iets groter oogt.
2. Dyspneu
Deze uitkomstmaat werd niet in Segreti (2013) gerapporteerd.
3. Falen van behandeling
Deze uitkomstmaat werd niet in Segreti (2013) gerapporteerd.
4. Terugval
Deze uitkomstmaat werd niet in Segreti (2013) gerapporteerd.
5. Mortaliteit
Deze uitkomstmaat werd niet in Segreti (2013) gerapporteerd.
Vergelijking 2: Inhalatiemethode van bronchusverwijder
Beschrijving studies
Mazhar (2007) evalueerde de depositie in de longen bij gebruik van een MDI spacer of een vernevelaar in patiënten met een acute longaanval opgenomen in het ziekenhuis. Patiënten met een longaanval als gevolg van astma of COPD zonder symptomen van acute respiratoir falen werden geïncludeerd. Alleen de data van patiënten met COPD worden hier verder beschreven. In totaal werden 11 patiënten met COPD gerekruteerd en allen hebben de studie voltooid. Alle patiënten kregen terbutaline als β2-agonist voorgeschreven. Op dag twee en dag vier werd de terbutaline dosis vervangen door de studiedosis van salbutamol gegeven via verschillende inhalatiemethoden; dosisaerosol of vernevelaar. De methode van inhalatie op dag twee of vier was gerandomiseerd, zodat alle patiënten tijdens de studieperiode via beide inhalatiemethoden salbutamol kregen. Bij dosisaerosol salbutamol werd vijfmaal 100 µg doses geïnhaleerd met een MDI verbonden met een groot volume spacer. Voor verneveling van salbutamol werd 5 mg in 2,5 ml verder opgelost in 4 ml zoutoplossing en gegeven een Portaneb vernevelaar. Gebruik van andere medicijnen was niet beschreven.
Berry (1989) vergeleek de effectiviteit van twee inhalatiemethoden (MDI-spacer of vernevelaar) van albuterol in opgenomen patiënten met een COPD-longaanval. Auteurs hebben een gerandomiseerd gecontroleerde cross-over trial gebruikt. In totaal deden 20 patiënten mee aan de studie. Patiënten kregen eerst albuterol of een placebo via een MDI-spacer en vijf minuten later gevolgd door albuterol of placebo (in wisselende volgorde) via een vernevelaar. Vier uur later werd het proces herhaald en omgedraaid. Via de MDI-spacer werd 0,36 mg albuterol gegeven en via de vernevelaar 2,5 mg. Als placebo werd 2,5 ml fysiologisch zoutoplossing gegeven. Standaard behandeling bestond uit intraveneus aminophylline, intraveneus corticosteroïden, en geïnhaleerde of orale sympathomimetica. Geïnhaleerd bronchusverwijder therapie en orale β-adrenergetische agonisten werden vier uur voor het starten van de studie gestopt en gedurende acht uur was het niet toegestaan om sympathomimetica toe te dienen die niet in het protocol stonden beschreven.
Turner (1988) evalueerde of het gebruik van een MDI spacer een effectief alternatief is voor verneveling in de behandeling van acute luchtwegobstructie op de spoedeisende hulp. Patiënten die zich presenteerden met een longaanval kwamen in aanmerking voor de studie. Patiënten werden geclassificeerd als patiënten met COPD op basis van 10 of meer pakjaren roken en symptomen die begonnen op 30 jarige of latere leeftijd. De trial includeerden ook astma patiënten die voor deze vraag buiten beschouwing werden gelaten. 10 patiënten werden naar een MDI spacer gerandomiseerd en ontvingen metaproterenol in drie pufs (650 µg per puf). 12 patiënten kregen 15 mg metaproterenol opgelost met normale zoutoplossing tot een volume van 2,5 mL in een vernevelaar. Elke patiënt ontving drie behandelingen met de vernevelaar en drie behandelingen met de MDI spacer. Patiënten kregen extra zuurstof en intraveneus steroïden van de spoedeisende hulp arts die niet betrokken was bij de studie. Intraveneus en oraal theophylline werd voor en tijdens de studie stopgezet.
Resultaten
1. Longfunctie
In de trial van Mazhar (2007) werd longfunctie, bepaald met FEV1, vlak voor toediening van salbutamol gemeten en 60 min erna. De longfunctie was in beide groepen vergelijkbaar vooraf. Vlak voor toediening via een dosis aerosol met voorzetkamer was de voorspelde FEV1 27,2% (SD 12,5) en vlak voor verneveling 24,1% (SD 9,7). 60 minuten na inhalatie van salbutamol via dosisaerosol met voorzetkamer was FEV1 met 2,6% (SD 3,3) toegenomen en bij verneveling met 4,3% (SD 4,8).
In de cross-over trial van Berry (1989) was de verandering in FEV1 één uur na behandeling bij gebruik van de MDI-spacer 103 mL (SD 167) en bij gebruik van de vernevelaar 139 mL (SD 149). Dit resultaat was niet statistisch significant verschillend.
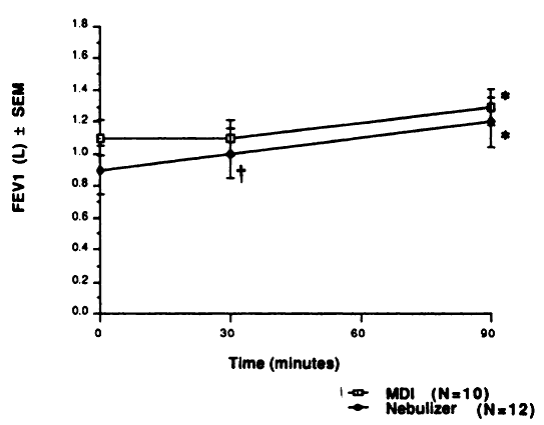
In de trial van Turner, 1988 werd de resultaten van FEV1 alleen in een grafiek weergegeven (zie figuur 2). De vergelijkende statistiek tussen de armen werd niet gegeven, alleen ten opzichte van baseline.
Figuur 2 Effect op FEV1 van een behandeling met metaproterenol via een MDI-spacer of via een vernevelaar op baseline, 30 minuten en 90 minuten na behandeling. * = significant verschillend van baseline (p≤0,005); † = significant verschillende van baseline (p≤0,05) (Turner, 1988).
2. Dyspneu
Deze uitkomstmaat was niet in de trial van Mazhar (2007) gerapporteerd.
In de trial van Berry (1989) was dyspneu met behulp van de Borg-score geëvalueerd. De verandering in Borg score 1 uur na behandeling was -1,08 (SD 2,01) bij gebruik van albuterol via de MDI-spacer en -0,73 (SD 1,75) via een vernevelaar. Dit resultaat was niet statistisch significant verschillend bevonden.
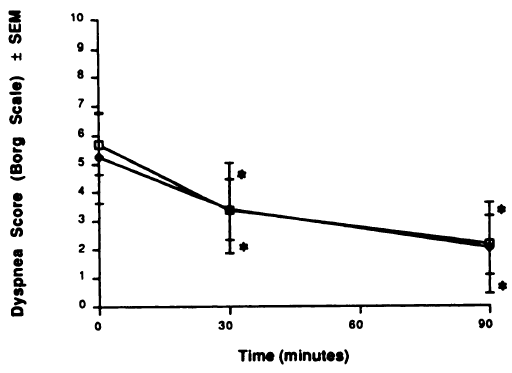
Ook de data over dyspneu in de trial van Turner, 1988 werd alleen in een grafiek weergegeven (zie figuur 3). De vergelijkende statistiek tussen de armen werd niet gegeven, alleen ten opzichte van baseline.
Figuur 3 Effect op dyspneu van een behandeling met metaproterenol via een MDI-spacer of via een vernevelaar op baseline, 30 minuten en 90 minuten na behandeling. * = significant verschillend van baseline (p≤0,005); † = significant verschillende van baseline (p≤0,05) (Turner, 1988).
Higgins, 1987 rapporteerde geen data over het mogelijke effect op dyspneu.
3. Falen van behandeling
Deze uitkomstmaat was niet in één van de trials gerapporteerd.
4. Terugval
Deze uitkomstmaat was niet in één van de trials gerapporteerd.
5. Mortaliteit
Deze uitkomstmaat was niet in één van de trials gerapporteerd.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat longfunctie en dyspneu zijn met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet; het geringe aantal patiënten (imprecisie).
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende twee wetenschappelijke vraagstellingen:
1. Wat is de rol van langwerkende bronchusverwijders bij de behandeling van een COPD-longaanval?
P (welke patiëntcategorie) patiënten met een COPD-longaanval die worden opgenomen in het ziekenhuis;
I (welke interventie) langwerkende bronchusverwijders;
C (welke comparison) kortwerkende bronchusverwijders of placebo;
O (welke uitkomstmaten)
1. FEV1;
2. dyspnoe;
3. falen van behandeling;
4. terugval;
5. mortaliteit.
2. Is er verschil in effect van behandeling tussen verschillende toedieningswijze van bronchusverwijders bij een COPD-longaanval?
P (welke patiëntcategorie) patiënten met een COPD-longaanval die worden opgenomen in het ziekenhuis;
I (welke interventie) verneveling, dosis aerosol of droog poeder;
C (welke comparison) verneveling, dosis aerosol of droog poeder;
O (welke uitkomstmaten)
1. FEV1;
2. dyspnoe;
3. falen van behandeling;
4. terugval;
5. mortaliteit.
Relevante uitkomstmaten
De werkgroep achtte longfunctie (FEV1) een voor de besluitvorming kritieke uitkomstmaat; en dyspnoe en het falen van behandeling voor de besluitvorming belangrijke uitkomstmaten.
De werkgroep definieerde de uitkomstmaten als volgt:
- Het falen van behandeling wordt gedefinieerd als noodzaak tot intensiveren van farmacologische behandeling nog tijdens de fase van studiemedicatie. In de meeste studies voldeden opname op IC, of overlijden ook aan de definitie van falen van behandeling.
- Terugval wordt gedefinieerd als behandeling of ziekenhuisopname voor een COPD-longaanval na voltooiing van de fase met studiemedicatie, maar binnen 30 dagen. In een aantal studies voldeed ook presentatie op de spoedeisende hulp als terugval.
Per uitkomstmaat: de werkgroep definieerde 100 mL in FEV1 als een klinisch relevant verschil.
Zoeken en selecteren (Methode)
In de databases Medline (OVID), Embase en de Cochrane Library is met relevante zoektermen gezocht naar systematische reviews en gerandomiseerde trials. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 295 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria: systematische review (gezocht in tenminste twee databases met een objectieve en transparante zoekstrategie, data extractie en methodologische beoordeling), gerandomiseerde trial van patiënten opgenomen met een COPD-longaanval onder behandeling van een langwerkende bronchusverwijder vergeleken met een kortwerkende bronchusverwijder of placebo of gerandomiseerde trials van patiënten opgenomen met een COPD-longaanval onder behandeling van een bronchusverwijder toegediend via één van de volgende opties: vernevelaar, dosisaërosol of droog poederinhalator. Op basis van titel en abstract werden in eerste instantie 16 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 14 studies geëxcludeerd (zie exclusietabel) en twee studies definitief geselecteerd. Daarnaast bleken twee andere relevante studies (Mazhar, 2007; Turner, 1988) niet gevonden te worden vanwege incorrecte of incomplete indexering. Deze studies zijn alsnog geïncludeerd.
Vier onderzoeken zijn opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidence-tabellen. De evidence-tabellen en beoordeling van individuele studiekwaliteit zijn opgenomen onder het tabblad Onderbouwing.
- American Thoracic Society (ATS), European Respiratory Society (ETS). Standards for the Diagnosis and Management of Patients with COPD (2004).
- Berry RB, Shinto RA, Wong FH, et al. Nebulizer vs spacer for bronchodilator delivery in patients hospitalized for acute exacerbations of COPD. Chest. 1989;96(6):1241-6.
- Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global Strategy for Diagnosis, Management, and Prevention of COPD 2016.
- Mazhar SH, Ismail NE, Newton DA, et al. Relative lung deposition of salbutamol following inhalation from a spacer and a Sidestream jet nebulizer following an acute exacerbation. Br J Clin Pharmacol. 2008;65(3):334-7.
- McCrory DC, Brown CD. Anti-cholinergic bronchodilators versus beta2-sympathomimetic agents for acute exacerbations of chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2002;(4):CD003900.
- Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose (NVALT). Richtlijn Diagnostiek en behandeling van COPD Actualisatie, maart 2010.
- Segreti A, Fiori E, Calzetta L, et al. The effect of indacaterol during an acute exacerbation of COPD. Pulm Pharmacol Ther. 2013;26(6):630-4.
- Turner JR, Corkery KJ, Eckman D, et al. Equivalence of continuous flow nebulizer and metered-dose inhaler with reservoir bag for treatment of acute airflow obstruction. Chest. 1988;93(3):476-81.
Evidence table for intervention studies (randomized controlled trials and non-randomized observational studies [cohort studies, case-control studies, case series])1
This table is also suitable for diagnostic studies (screening studies) that compare the effectiveness of two or more tests. This only applies if the test is included as part of a test-and-treat strategy – otherwise the evidence table for studies of diagnostic test accuracy should be used.
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Vergelijking 1: Langwerkende versus kortwerkende bronchusverwijder |
|||||||
|
Segreti, 2013 |
Type of study: RCT
Setting: Patients presenting at the emergency department
Country: Italy
Source of funding: Not reported |
Inclusion criteria:
Exclusion criteria:
N total at baseline: Intervention: 19 Control:10
Important prognostic factors2: Age ± SD: I: 75 (1) C:76 (3)
Sex: I: 47% M C: 80% M
Groups comparable at baseline? Yes for age, but not for sex |
Inhaled indacaterol maleate 300 µg once a day using Breezhaler device
|
Salbutamol nebulizer 1250 µg three times a day
|
Length of follow-up: 5 days
Loss-to-follow-up: Intervention: N=0 (0%) Control: N=0 (0%)
Incomplete outcome data: Intervention: N=0 (0%) Control: N=0 (0%)
|
1. Treatment failure Not reported
2. Relapse Not reported
3. Mortality Not reported
4. FEV1 Reported in a graph.
5. Dyspnoea Not reported |
All patients also received therapy with ipratropium bromide aerosol 500 g three times a day, intravenous methylprednisolone 20 mg twice a day and oral levofloxacin 500 mg once a day.
This was a non-blinded, randomized, controlled pilot trial. |
|
Vergelijking 2: Inhalatiemethode van bronchusverwijder |
|||||||
|
Mazhar, 2007 |
Type of study: Cross-over trial
Setting: Patients hospitalized following an acute exacerbation of asthma or COPD.
Only data from COPD patients will be described.
Country: United Kingdom
Source of funding: Not reported |
Inclusion criteria:
N total at baseline: 11 COPD patients
Important prognostic factors2: Age ± SD: 63 (9)
Sex: 55% M
Percentage predicted FEV1 on admission: 19.2 (6.6) |
Salbutamol – inhaler
Five separate 100 µg doses inhaled from a MDI attached to a Volumatic large volume spacer |
Salbutamol – nebulized
5 mg in 2.5 ml, diluted to 4ml with normal saline for nebulization, and nebulized to spluttering using a Sidestream chamber driven by a Portaneb compressor (NEB) |
Length of follow-up: 4 days
Loss-to-follow-up: Intervention: N=0 (0%) Control: N=0 (0%)
Incomplete outcome data: Intervention: N=0 (0%) Control: N=0 (0%)
|
1. Treatment failure Not reported
2. Relapse Not reported
3. Mortality Not reported
4. FEV1 Mean percentage predicted (SD)
Predose I: 27.2 (12.5) C: 24.1 (9.7) Increase 60 min postdose I: 2.6 (3.3) C: 4.3 (4.8)
5. Dyspnoea Not reported |
All patients received as their β2-agonist terbutaline. On the second and fourth day the terbutaline was replaced with the study dose.
Use of other medication was not reported. |
|
Berry, 1989 |
Type of study: Randomized controlled crossover trial
Setting: Emergency rooms at medical wards
Country: Unknown
Source of funding: Commercial |
Inclusion criteria:
Exclusion criteria:
N total at baseline: 20 patients
Important prognostic factors2: Age ± SD: 61 (7)
Sex: 100% M
FEV1 at admission in L (SD): 0.71 (0.26)
|
Albuterol
|
Placebo (MDI-spacer or nebulizer)
|
Length of follow-up: 1 hour after treatment
Loss-to-follow-up: 0 (0%)
Incomplete outcome data: 0 (0%)
|
1. Treatment failure Not reported
2. Relapse Not reported
3. Mortality Not reported
4. FEV1 Change in ml, mean (SD)
MDI-spacer: 103 (167) Nebulizer: 139 (149) Not statistically significant
5. Dyspnoea Measured with the Borg score (range from 0 to 10)
MDI-spacer: -1.08 (2.01) Nebulizer: -0.73 (1.75) Not statistically significant |
Patients received first four puffs via the MDI-spacer (active drug or placebo) followed after five minutes with the nebulizer (active drug or placebo). After four hours the process was repeated and switched.
Standard therapy included intravenous aminophylline, intravenous corticosteroids, and inhaled or oral sympathomimetics. Such therapy was left tot the discretion of the primary-care physicians. Inhaled bronchodilator therapy and oral β-adrenergic agonists were withheld for 4 h before starting the study, and for the next 8 h, no nonprotocol sympathomimetics were allowed. |
|
Turner, 1988 |
Type of study: Randomized controlled trial
Setting: Emergency room of a general hospital
Country: United Stated of America
Source of funding: Not stated |
Inclusion criteria:
Exclusion criteria:
N total at baseline*: Intervention: 10 Control: 12
Important prognostic factors2: Age ± SD: I: 55 (4) C: 57 (3)
Sex: I: 70% M C: 69% M
FEV1 in L I: 1.1 (0.1) C: 0.9 (0.1)
Groups comparable at baseline? Yes |
Metaproterenol in MDI with InspiEase (three puff of 650 µg) and nebuliser with normal saline solution
Each subject received three treatments with the nebulizer and three with the MDI and InspirEase at 30-minute intervals.
|
Nebuliser with 15 mg metaproterenol diluted with normal saline solution to a volume of 2.5 mL and placebo MDI with InspiEase
Each subject received three treatments with the nebulizer and three with the MDI and InspirEase at 30-minute intervals.
|
Length of follow-up: 90 minutes
Loss-to-follow-up: 0 (0%)
Incomplete outcome data: 0 (0%)
|
1. Treatment failure Not reported
2. Relapse Not reported
3. Mortality Not reported
4. FEV1 Data reported in graph and with the following sentence in the results section:
“The FEV1 improved significantly at 30 minutes only in the patients treated with metaproterenol by wet nebulizer and in both treatment groups at 90 minutes.”
5. Dyspnoea Data reported in graph and with the following sentence in the results section:
“[..], the dyspnea score improved significantly at 30 and 90 minutes in both treatment groups.” |
Patients were categorized as having COPD based on 10 or more pack-years of smoking and onset of symptoms at 30 years or older.
Patients were given supplemental oxygen and intravenous steroids at the discretion of the emergency room physician who was not involved in the study. Intravenous and oral theophylline were withheld before and during the study period.
*Data from COP patients were reported; data from asthma patients was not taken into account. |
Notes:
- Prognostic balance between treatment groups is usually guaranteed in randomized studies, but non-randomized (observational) studies require matching of patients between treatment groups (case-control studies) or multivariate adjustment for prognostic factors (confounders) (cohort studies); the evidence table should contain sufficient details on these procedures
- Provide data per treatment group on the most important prognostic factors [(potential) confounders]
- For case-control studies, provide sufficient detail on the procedure used to match cases and controls
- For cohort studies, provide sufficient detail on the (multivariate) analyses used to adjust for (potential) confounders
Risk of bias table for intervention studies (randomized controlled trials)
|
Study reference
(first author, publication year) |
Describe method of randomisation1 |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Segreti, 2013 |
After consenting to participate in the study, consecutive eligible patients were randomly allocated to one of the two treatment groups (A and B) using the sequential randomization scheme ABA. |
Likely |
Likely |
Likely |
Likely |
Unlikely |
Unlikely |
Unlikely |
|
Mazhar, 2007 |
The inhalation method to be used on the study days was randomized. |
Likely |
Likely |
Likely |
Likely |
Unlikely |
Unlikely |
Unlikely |
|
Berry, 1989 |
The order with which active drug was given by MDI-spacer (first or second treatment block) was randomized. |
Unlikely |
Unlikely |
Unclear |
Unclear |
Unlikely |
Unlikely |
Unlikely |
|
Turner, 1988 |
Patients were randomized in double-blind fashion. |
Unclear |
Unlikely |
Unlikely |
Unclear |
Unlikely |
Unlikely |
Likely |
|
Higgins, 1987 |
The order of the session was randomized and the nature of treatment double blind. |
Unlikely |
Unlikely |
Unlikely |
Unlikely |
Unlikely |
unlikely |
Unlikely |
- Randomisation: generation of allocation sequences have to be unpredictable, for example computer generated random-numbers or drawing lots or envelopes. Examples of inadequate procedures are generation of allocation sequences by alternation, according to case record number, date of birth or date of admission.
- Allocation concealment: refers to the protection (blinding) of the randomisation process. Concealment of allocation sequences is adequate if patients and enrolling investigators cannot foresee assignment, for example central randomisation (performed at a site remote from trial location) or sequentially numbered, sealed, opaque envelopes. Inadequate procedures are all procedures based on inadequate randomisation procedures or open allocation schedules..
- Blinding: neither the patient nor the care provider (attending physician) knows which patient is getting the special treatment. Blinding is sometimes impossible, for example when comparing surgical with non-surgical treatments. The outcome assessor records the study results. Blinding of those assessing outcomes prevents that the knowledge of patient assignement influences the proces of outcome assessment (detection or information bias). If a study has hard (objective) outcome measures, like death, blinding of outcome assessment is not necessary. If a study has “soft” (subjective) outcome measures, like the assessment of an X-ray, blinding of outcome assessment is necessary.
- Results of all predefined outcome measures should be reported; if the protocol is available, then outcomes in the protocol and published report can be compared; if not, then outcomes listed in the methods section of an article can be compared with those whose results are reported.
- If the percentage of patients lost to follow-up is large, or differs between treatment groups, or the reasons for loss to follow-up differ between treatment groups, bias is likely. If the number of patients lost to follow-up, or the reasons why, are not reported, the risk of bias is unclear
- Participants included in the analysis are exactly those who were randomized into the trial. If the numbers randomized into each intervention group are not clearly reported, the risk of bias is unclear; an ITT analysis implies that (a) participants are kept in the intervention groups to which they were randomized, regardless of the intervention they actually received, (b) outcome data are measured on all participants, and (c) all randomized participants are included in the analysis.
Beoordelingsdatum en geldigheid
Publicatiedatum : 13-04-2017
Beoordeeld op geldigheid : 01-01-2017
De richtlijnwerkgroep heeft als doel de richtlijn periodiek (digitaal) van updates te voorzien.
De NVALT en LAN zijn als houder van deze richtlijn de eerstverantwoordelijken voor de actualiteit van deze richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de eerstverantwoordelijken over relevante ontwikkelingen binnen hun vakgebied.
De KNMP heeft als lid van de LAN afgezien van autorisatie om inhoudelijke en procesmatige redenen. Het LAN bestuur, inclusief de overige leden van de LAN, hebben de richtlijn geautoriseerd. KNMP heeft bijgedragen als reviewer.
Algemene gegevens
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor autorisatie en door hen geautoriseerd.
In samenwerking met:
Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose (NVALT)
Long Alliantie Nederland (LAN)
Nederlandse Vereniging voor Intensive Care (NVIC)
Nederlandse Vereniging van Diëtisten (NVD)
Nederlands Instituut van Psychologen (NIP)
Koninklijk Nederlands Genootschap voor Fysiotherapie (KNGF)
Verpleegkundigen & Verzorgenden Nederland (V&VN)
Longfonds
De richtlijnontwikkeling werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel van de richtlijn
In deze richtlijn worden aanbevelingen gedaan over de indicatiestelling van opname, het diagnostisch traject, de medicamenteuze en niet medicamenteuze behandeling tijdens ziekenhuisopname na COPD-longaanval, inclusief criteria voor monitoring en ontslag. Hiermee wordt een bijdrage geleverd aan een meer eenduidige, doelgerichte behandeling van patiënten met een COPD-longaanval in het ziekenhuis.
Beoogde gebruikers van de richtlijn
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen die betrokken zijn bij de zorg voor patiënten met COPD en een longaanval die klinisch moeten worden behandeld. De gebruikers van de richtlijn (en het zorgpad) betreffen dan ook naast de longartsen veel andere medische beroepsgroepen zoals intensivisten, specialisten ouderengeneeskunde, huisartsen, longfunctieanalisten, verpleegkundigen (waaronder verpleegkundig specialisten en longverpleegkundigen), ziekenhuisapothekers, psychologen, fysiotherapeuten, diëtisten en ergotherapeuten.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2014 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten gedurende een ziekenhuisopname na een COPD-longaanval (zie hieronder). De werkgroepleden zijn door hun wetenschappelijke verenigingen gemandateerd voor deelname. De werkgroep werkte gedurende twee jaar aan de totstandkoming van de richtlijn. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
- dr. F.J.J. van den Elshout (voorzitter), longarts, NVALT
- W.J.M. van Litsenburg (vicevoorzitter), verpleegkundig specialist, LAN/V&VN
- prof. Dr. H.A.M. Kerstjens, longarts, NVALT
- drs. P. L. Salomé, huisarts, COPD & Astma Huisartsen Advies Groep NHG
- drs. M.L.J. Scheer, longarts-intensivist, NVIC
- drs. R. van Snippenburg, longarts, NVALT
- dr. M. A. Spruit, fysiotherapeut, KNGF
- M.P.G. Stegers MSc, diëtist, NVD
- P.E.M. Fikkers-Mol MANP, verpleegkundig specialist, V&VN
- dr. J.N. de Voogd, psycholoog, NIP
- dr. S. Holverda, Longfonds (voorheen Astma Fonds)
Met ondersteuning van:
- P.H. Broos MSc, senior adviseur, Kennisinstituut van Medisch Specialisten
- dr. B.H. Stegeman, adviseur, Kennisinstituut van Medisch Specialisten
Met dank aan:
- drs. L. Sekhuis, LAN
Belangenverklaringen
De werkgroepleden hebben schriftelijk verklaard of ze in de laatste vijf jaar een (financieel ondersteunde) betrekking onderhielden met commerciële bedrijven, organisaties of instellingen die in verband staan met het onderwerp van de richtlijn.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Persoonlijke financiele belangen |
Persoonslijke relaties |
Reputatiemanagement |
Extern gefinancierd onderzoek |
Kennisvalorisatie |
Overige belangen |
Getekend |
|
De Voogd |
gezondheidszorg psycholoog CvR UMCG |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
19-nov-15 |
|
Fikkers-Mol |
verpleegkundig specialist ziekenhuis Rijnstaete. |
alg. bestuurslid V&VN Longverpleegkundigen. Hier houd ik me, naast de reguliere bestuurstaken, vooral ook bezig met de scholingen. Hievoor ontvang ik vacatiegeld. |
geen |
geen |
geen |
geen |
geen |
geen |
25-sep-14 |
|
Kerstjens |
hoogleeraar en afdelingshoofd, afd. Longziekten en Tuberculose, Universitair Medisch Centrum Groningen |
tot 29-9-2014 secretaris bestuur Long Alliantie Nederland (onbetaald).Voorzitter Nordelijke CARA Stichting (onbetaald) |
geen PERSOONLIJK fin. Belang; betaling naar UMCG; over afgelopen 5 jaar ad hoc lid adviescommissie /adviseur/spreker voor verschillende farmaceutische bedrijven (Almiral, Astra Zeneca, Boehringer, Chiesi, GlaxoSmithKline, Novartis, Pfizer, Takeda) |
geen PERSOONLIJK fin. Belang; betaling naar UMCG; over afgelopen 5 jaar ad hoc lid adviescommissie /adviseur/spreker voor verschillende farmaceutische bedrijven (Almiral, Astra Zeneca, Boehringer, Chiesi, GlaxoSmithKline, Novartis, Pfizer, Takeda) |
|
over de afgelopen 5 jaar deelname aan onderzoek gefinancierd door overheid, astmafonds/longfonds. AstraZeneca, Boehringer, GlaxoSmithKline, Novartis, Pfizer, Takeda |
geen |
geen |
19-sep-14 |
|
Salomé |
huisarts |
kernlid CAHAG |
geen |
geen |
geen |
geen |
geen |
geen |
2-okt-14 |
|
Scheer |
longarts -intensivist. Volledig werkzaam op de IC in de functie van intensivist |
EMS B instructeur (onbetaald) |
geen |
geen |
geen |
geen |
geen |
geen |
ja 8 jan 2015 |
|
Spruit |
wetenschappelijk adviseur CIRO + te Horn (NL) |
Gastprofessor in Hassels University te Hasselt (B) - betaald |
geen |
geen |
geen |
geen |
werkzaam bij het CIRO+, alwaar longrevalidatie wordt aangeboden als zorgproduct. Verwijzing naar longrevalidatie kan een mogelijk resultaat zijn van de commisie. |
geen |
ja 18 sept 2014 |
|
Stegers |
dietist in CWZ |
geen |
geen |
geen |
ik ben lid van de NVD, maar participerend lid. Vanuit de NVD ook gevraagd voor deze richtlijn. |
2011-2013 meegedaan aan onderzoek Zicht op gewicht via Medizorg B.V. Gegevens zijn verzameld, resultaten moet nog gepresenteerd worden. |
geen |
geen |
25-sep-14 |
|
Van den Elshout |
longarts Rijnstate Ziekenhuis Arnhem (fulltime) voorzitter richtijn commissie |
lid centraal tuchtcollege Den Haag; vacatiegelden komen ten goede aan de maatschap longartsen |
geen |
geen |
geen |
educational Grant GSK voor promovendus |
geen |
geen |
6-okt-14 |
|
Van Litsenburg |
verpleegkundig specialist longgeneeskunde |
Lid kernteam PICASSO |
geen |
geen |
geen |
geen |
geen |
geen |
ja, 3 dec 2014 |
|
Van Snippenburg |
longarts |
vz MCC Diakonessenhuis Utrecht (onbetaald) |
geen |
geen |
lid werkgroep COPD vd NVALT. Lid werkgroep Transmuraal Zorgpad Longaanval LAN. |
in afrondende fase van Liaison studie (in opdracht van Chisi) astma survey studie |
samen met patient een DVD geproduceerd over Bewegen bij COPD voor patieten. Sponsoring door GSK, eenmalig en Swieringa Stichting eenmalig. Auteursrechten van deze DVD liggen bij van der Colk BV. DVD is gratis verstrekt aan zorgverleners tbv patiënten en rechtstreeks aan patiënten. Zolang de voorraad strekt. |
geen |
20-okt-14 |
|
Vercoulen |
Klinisch Psycholoog/sectieleider Medische Psychologie Volwassenen en Ouderen, Radboudumc |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
ja 23 feb 2015 |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door middel van vertegenwoordiging van het Longfonds in de werkgroep. Daarnaast heeft de Longfonds de conceptrichtlijn beoordeeld tijdens de commentaarfase en suggesties voor verbetering van de richtlijn gegeven.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren.
De richtlijn wordt opgenomen in de richtlijnendatabase (www.richtlijnendatabase.nl) waarmee hij toegankelijk is voor alle relevante beroepsgroepen en patiënten. Daarnaast wordt er een samenvatting van de richtlijn gepubliceerd in tijdschriften van de deelnemende wetenschappelijke verenigingen. Ook is de richtlijn te downloaden vanaf de website van betrokken wetenschappelijke verenigingen en de Long Alliantie Nederland.
Werkwijze
AGREE II
Deze richtlijn is opgesteld conform de eisen in het rapport ‘Richtlijnen 2.0’ van de adviescommissie Richtlijnen van de Raad kwaliteit van de Orde van Medisch Specialisten. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II) (www.agreetrust.org), dat een internationaal breed geaccepteerd instrument is voor de beoordeling van de kwaliteit van richtlijnen.
Knelpuntenanalyse
In de eerste fase werden de knelpunten geïnventariseerd. Tevens is gebruikt gemaakt van de knelpuntenanalyse bij de ontwikkeling van het landelijk zorgpad COPD-longaanval met ziekenhuisopname dat parallel aan deze richtlijn is ontwikkeld.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn vervolgens verder uitgewerkt door de leden van de werkgroep en tijdens de werkgroepvergadering vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang als kritiek, belangrijk en onbelangrijk. Tevens definieerde de werkgroep, voor zover mogelijk, wat zij voor een bepaalde uitkomstmaat een klinisch relevant verschil vond, dat wil zeggen wanneer de verbetering in uitkomst een verbetering voor de patiënt is.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar bestaande buitenlandse richtlijnen en naar systematische reviews in Medline (OVID) en Cochrane Library. Vervolgens werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekactie of gebruikte trefwoorden van de zoekactie en de gehanteerde selectiecriteria zijn te vinden in de module van de desbetreffende uitgangsvraag. De gedetailleerde zoekstrategieën zijn vermeld per module.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de kolom ‘Beoordeling kwaliteit studie’ van een evidence-tabel.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidence-tabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor Grading Recommendations Assessment, Development and Evaluation (zie http://gdt.guidelinedevelopment.org/app/handbook/handbook.html).
|
GRADE |
Definitie |
|
Hoog |
|
|
Matig |
|
|
Laag |
|
|
Zeer laag |
|
B) Voor vragen over de waarde van diagnostische tests, schade of bijwerkingen, etiologie en prognose
Bij dit type vraagstelling kan GRADE (nog) niet gebruikt worden. De bewijskracht van de conclusie is bepaald volgens de gebruikelijke EBRO-methode (Van Everdingen, 2004).
Formuleren van de conclusies
Bij interventievragen verwijst de conclusie niet naar een of meer artikelen, maar wordt getrokken op basis van alle studies samen (body of evidence). Hierbij maakten de werkgroepleden de balans op voor elke interventie. Bij het opmaken van de balans werden door de werkgroep de gunstige en ongunstige effecten voor de patiënt afgewogen.
Voor vragen over de waarde van diagnostische tests, schade of bijwerkingen, etiologie en prognose is het wetenschappelijke bewijs samengevat in een of meerdere conclusie(s), waarbij het niveau van het meest relevante bewijs is weergegeven. Omwille van de homogeniteit is het niveau van bewijs voor alle conclusies weergegeven als hoog/matig/laag/zeer laag, waarbij EBRO niveau 1 is vertaald naar hoog, 2 naar matig, 3 naar laag en 4 naar zeer laag.
Wanneer er voor een uitgangsvraag geen systematisch literatuuronderzoek werd verricht, is de literatuur niet beoordeeld op kwaliteit en is de kracht van het bewijs niet bepaald.
Overwegingen
Voor een aanbeveling zijn naast het wetenschappelijke bewijs ook andere aspecten belangrijk, zoals de expertise van de werkgroepleden, patiëntenvoorkeuren, kosten, beschikbaarheid van voorzieningen of organisatorische zaken. Deze aspecten worden, voor zover niet wetenschappelijk onderzocht, vermeld onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven een antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen. Bij het formuleren en graderen van de aanbeveling worden minimaal de volgende vier factoren in ogenschouw genomen: algehele kwaliteit van het wetenschappelijke bewijs; balans tussen voor- en nadelen van de interventie; waarden en voorkeuren van professional en patiënten; en beschikbare middelen.
Indicatorontwikkeling
De werkgroep heeft besloten geen nieuwe indicatoren bij deze richtlijn te ontwikkelen, maar gebruik te maken van de reeds bestaande indicatoren op het gebied van COPD.
Kennislacunes
Tijdens de ontwikkeling van de richtlijn ‘Diagnostiek en Behandeling van een COPD-longaanval in het Ziekenhuis’ is systematisch gezocht naar onderzoeksbevindingen die nuttig konden zijn voor het beantwoorden van de uitgangsvragen. Een deel (of een onderdeel) van de uitgangsvragen is met het resultaat van deze zoekacties te beantwoorden, een groot deel echter niet. Door gebruik te maken van de evidence-based methodiek (EBRO) is duidelijk geworden dat op het terrein van longaanvallen COPD nog lacunes in de beschikbare kennis bestaan. Een inventarisatie hiervan is opgenomen in de bijlage bij de richtlijn.
Literatuur
Atkins D, Best D, Briss PA, et al. Grading quality of evidence and strength of recommendations. BMJ. 2004;328(7454):1490.
Van Everdingen JJE, Burgers JS, Assendelft WJJ, et al. Evidence-based richtlijnontwikkeling. Bohn Stafleu Van Loghum. 2004.
Zoekverantwoording
|
Uitgangsvraag: AANVULLENDE SEARCH - Wat is de positie van bronchusverwijders bij de behandeling van patiënten met een exacerbatie van COPD? |
|
|
Database(s): Medline en Embase |
Datum: 19-02-2016 |
|
Periode: Geen beperking |
Talen: Engels en Nederlands |
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID) 1946 – februari 2016
|
((exp *Pulmonary Disease, Chronic Obstructive/ or ('chronic obstructive' adj2 (lung or pulmonary or airway)).ab,ti. or copd.ab,ti. or chronic bronchitis.ab,ti. or exp *Emphysema/ or emphysema.ab,ti.) and (exacerbation* or emergenc* or acute).ab,ti.) or aecopd.ab,ti.
AND exp *Hospitalization/ or hospitalis*.ab,ti. or hospitaliz*.ab,ti. or hospital admission*.ab,ti.
AND exp Cholinergic Antagonists/ or anticholinergic*.ab,ti. or Muscarinic Antagonists/ or muscarin*.ab,ti. or exp Adrenergic beta-Antagonists/ or LABA.ab,ti. or saba.ab,ti. or lama.ab,ti. or sama.ab,ti.
limit to (dutch or english)
AND ((meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/))
OR (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/))
=0 (na ontdubbeling met eerdere search dd 07-12-15) |
4 |
|
Embase |
'chronic obstructive lung disease'/exp OR 'chronic obstructive' NEAR/2 (lung OR pulmonary OR airway) OR 'copd':ab,ti OR 'chronic bronchitis':ab,ti OR emphysema:ab,ti OR aecopd:ab,ti AND (exacerbation* OR emergenc* OR acute):ab,ti OR aecopd:ab,ti
AND ('hospitalization'/exp/mj OR hospitalis*:ab,ti OR hospitaliz*:ab,ti)
AND ('cholinergic receptor blocking agent'/exp OR anticholinergic*:ab,ti OR 'muscarinic agent'/exp OR muscarin*:ab,ti OR 'beta adrenergic receptor stimulating agent'/exp OR laba:ab,ti OR saba:ab,ti OR lama:ab,ti OR sama:ab,ti)
AND ([dutch]/lim OR [english]/lim) AND [embase]/lim
AND (('meta analysis'/de OR cochrane:ab OR embase:ab OR psychlit:ab OR cinahl:ab OR medline:ab OR (systematic NEAR/1 (review OR overview)):ab,ti OR (meta NEAR/1 analy*):ab,ti OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT ('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp NOT 'human'/exp)
OR ('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it))
= 4 (na ontdubbeling met eerdere search dd 07-12-15) |
