Magnesiumsulfaat bij acuut astma bij kinderen
Uitgangsvraag
Is behandeling met magnesiumsulfaat (verschillende doses, al dan niet met herhaling) geïndiceerd voor kinderen met een status astmaticus op de SEH?
Aanbeveling
Een behandeling met intraveneus magnesiumsulfaat kan worden overwogen bij kinderen met een status astmaticus die onvoldoende verbeteren (Qureshi-score ≥ 10 na drie keer vernevelen) met luchtwegverwijding alleen.
Behandeling met intraveneus magnesiumsulfaat mag bij een ernstig bedreigde patiënt geen uitstel van behandeling met systemische steroïden en/of intraveneus salbutamol betekenen.
De aanbevolen dosering van intraveneus magnesiumsulfaat, als toevoeging aan (continue) salbutamol inhalatie, voor behandeling van status astmaticus bij kinderen is 40 mg/kg/dosis, in 10-15min (max. 2 g/dosis) en kan zonodig herhaald worden (conform Kinderformularium).
Overwegingen
De kwaliteit van het bewijs was in het algemeen laag tot zeer laag. Dat maakt de kans op een andere uitkomst dan het gevonden bewijs voor de individuele patiënt groter.
Vanuit professioneel perspectief kan een extra medicament in de praktijk met een acuut benauwd kind dat niet voldoende opknapt met luchtwegverwijding en orale steroïden een belangrijk verschil maken. Wel vergt toediening van MgSO4 een intraveneuze toegang. Werkzaamheid van MgSO4 per verneveling was geen onderdeel van deze uitgangsvraag. De afweging bij de individuele patiënt kan gezien het acute karakter (rug tegen de muur) zo zijn dat alle rescue-medicatie wordt ingezet. Dit maakt een proefbehandeling in elk geval aanvaardbaar, ook omdat geen ernstige bijwerkingen in de literatuur zijn gerapporteerd bij gebruikelijke doseringen en inloopsnelheden. Indien behandeling met MgSO4 i.v. effectief is, kan mogelijk overplaatsing naar een IC worden voorkómen.
De te verwachten gunstige effecten zijn op grond van het gevonden bewijs in het algemeen klein.
Op basis van de evidence, en de lage kwaliteit daarvan, is het lastig een goede afweging te maken tussen gewenste en ongewenste effecten van MgSO4 i.v. Een strikte aanbeveling vóór inzet van MgSO4 kan daarom niet onderbouwd worden. De werkgroep is van mening dat behandeling met MgSO4 overwogen kan worden bij kinderen met een status astmaticus die onvoldoende reageren (blijvend hoge astmascore) op salbutamol inhalatie, als toevoeging aan (continue) salbutamol inhalatie. De werkgroep is van mening dat een eventuele behandeling met MgSO4 geen uitstel van behandeling met intraveneus salbutamol mag betekenen, indien deze laatste behandeling geïndiceerd is (zie de module Salbutamol i.v.).
Er zijn vooralsnog geen aanwijzingen voor responders versus non-responders op Magnesiumsulfaat i.v. bij status astmaticus. De werkgroep (expert opinion) neemt aan dat de mate van bronchoconstrictie en mogelijk ook een gedeeltelijke ventilatie-perfusie mismatch het meest bepalend is voor het al dan niet werkzaam zijn van magnesiumsulfaat i.v. Dit maakt dat de succeskans bij toediening niet vooraf kan worden vastgesteld en eerdere ervaring bij een patiënt in een vergelijkbare situatie niet dezelfde uitkomst hoeft te geven.
Op klinische gronden is het raadzaam om alvast (orale) systemische corticosteroïden te geven ruim voor het moment dat magnesiumsulfaat i.v. of salbutamol i.v. wordt overwogen bij patiënten die onvoldoende verbeteren op een eerste luchtwegverwijding. Een vroege gift van systemische steroïden voorkomt mogelijk ingrijpende vervolgstappen.
Voor adviezen m.b.t. dosering van Magnesiumsulfaat i.v. vond de werkgroep in de gevonden literatuur geen redenen om af te wijken van die in het Kinderformularium.
Onderbouwing
De vorige richtlijn acuut astma, opvang in het eerste uur in 2012, gaf magnesiumsulfaat (MgSO4) een plek bij de behandeling van acuut astma dat niet voldoende reageert op behandeling met geïnhaleerde luchtwegverwijding. Sindsdien is er meer ervaring opgedaan bij patiënten met status astmaticus in de praktijk. Er lijken daarbij wisselende resultaten: sommige patiënten lijken te reageren, anderen niet. Dit roept vragen op t.a.v. de indicatie (ook op jonge leeftijd), timing, plaatsbepaling, toedieningswijze en dosering (inclusief herhaling) van MgSO4.
|
|
Het is niet bekend of behandeling van kinderen met een status astmaticus op de SEH met intraveneus MgSO4 geassocieerd is minder noodzaak tot beademing of minder gebruik van intraveneus salbutamol. Het is niet bekend uit de literatuur wat het optimale doseringsregime van MgSO4 i.v. is bij kinderen met een status astmaticus. |
|
⨁◯◯◯ ZEER LAAG |
Er is geen eenduidig bewijs over het effect van intraveneus MgSO4 op symptomen/ astmascore bij kinderen met een status astmaticus op de SEH. Gürkan, 1999; Ciarallo, 2000; Devi, 1997; Scarfone, 2000; Pruikkonen, 2018 (1, 5, 8, 19, 20) |
|
⨁⨁◯◯ LAAG |
Er lijkt geen verschil in de kans op ziekenhuisopname bij gebruik van MgSO4 in vergelijking met geen gebruik van MgSO4 door kinderen met een status astmaticus op de SEH. Ciarallo, 1996; Scarfone, 2000 (2, 19) |
|
⨁◯◯◯ ZEER LAAG |
Er is mogelijk een (statistisch significant) verschil in opnameduur bij gebruik van MgSO4 in vergelijking met geen gebruik van MgSO4 door kinderen met een status astmaticus op de SEH. De werkgroep acht dit verschil niet klinisch relevant. Devi, 1997(5) |
|
⨁◯◯◯ ZEER LAAG |
Er lijkt geen verschil in gebruik van systemische steroïden bij gebruik van MgSO4 in vergelijking met geen gebruik van MgSO4 door jonge kinderen met een status astmaticus op de SEH. Pruikkonen, 2018(20) |
|
⨁◯◯◯ ZEER LAAG |
Er is geen eenduidig bewijs over het optreden van bijwerkingen bij gebruik van MgSO4 in vergelijking met geen gebruik van MgSO4 door kinderen met een status astmaticus op de SEH. Ernstige bijwerkingen werden niet gerapporteerd. Ciarallo, 1996; Devi, 1997; Egelund, 2013; Gürkan, 1999(2, 5, 6, 8) |
|
Algehele kwaliteit van bewijs: ZEER LAAG |
Zes van de geïncludeerde studies waren dubbelblinde RCT’s;(1, 2, 5, 8, 19, 20) nog eens 3 studies waren niet-geblindeerde RCT’s;(3, 10, 17) de laatste studie was een prospectief vergelijkend cohortonderzoek.(6) In het onderzoek van Singhi et al. werd niet-geblindeerd intraveneuze behandeling met MgSO4 (50 mg/kg) vergeleken met intraveneus terbutaline bij 100 kinderen met acuut ernstig astma; daarbij werd gekeken naar de CAS (Clinical Asthma Score) en bijwerkingen.(17) Irazuzta et al. vergeleken niet-geblindeerd intraveneus MgSO4 in een continue infuus (50 mg/kg/uur 4 uur, max. 8000 mg/uur) met een MgSO4-bolus (50 mg/kg) bij 38 kinderen met astma op de SEH.(10) In de dubbelblinde RCT van Gürkan et al. werd bij 20 kinderen met een acute astma-exacerbatie het gebruik van MgSO4 (40 mg/kg, max. 2g) vergeleken met placebo, waarbij werd gekeken naar de astmascore en bijwerkingen.(8) In het onderzoek van Egelund et al. werd prospectief behandeling met MgSO4 (oplaaddosis 75 mg/kg bij kinderen <30 kg of 50 mg/kg bij kinderen ≥30 kg 30-45 minuten, daarna 40 mg/kg/uur 4 uur) vergeleken met geen MgSO4 bij 57 kinderen met status astmaticus, waarbij gekeken werd naar bijwerkingen.(6) Devi et al. bestudeerden in een dubbelblinde placebogecontroleerde RCT de werking van MgSO4 (100 mg/kg in 35 min. i.v.) bij 47 kinderen met acuut ernstig astma, waarbij gekeken werd naar de astmascore, opnameduur en bijwerkingen.(5) In de niet-geblindeerde RCT van Daengsuwan et al. werd intraveneus MgSO4 (50 mg/kg 20 minuten) vergeleken met verneveld MgSO4 (3 maal 2,5 ml in 6% oplossing elke 20 minuten) bij 28 kinderen met ernstig astma, waarbij werd gekeken naar de Asthma Severity Score, bijwerkingen en opnameduur.(3) Ciarallo et al. publiceerden 2 artikelen over 31 en 30 kinderen met een acute astma exacerbatie, waarbij intraveneus MgSO4 in 25 mg/kg in de ene studie en 40 mg/kg in de andere studie werd vergeleken met placebo; gekeken werd naar ziekenhuisopname, opnameduur, astmascore (modified Wood-Downes clinical asthma score) en bijwerkingen.(1, 2) Scarfone et al. voerden een dubbelblind placebogecontroleerde RCT uit bij 54 kinderen met een matige tot ernstige astma-exacerbatie op de SEH. Zij vergeleken intraveneus MgSO4 (75 mg/kg, max. 2,5 g) met placebo (na behandeling met salbutamol verneveling en prednisolon); gekeken werd naar verbetering van klinische astmascores, ziekenhuisopname en tijd tot ontslag.(19) Pruikkonen et al. publiceerden een dubbelblind placebogecontroleerde RCT over 61 kinderen in de leeftijd van 6 maanden tot 4 jaar met acuut ernstig piepen. Hierin werd MgSO4 i.v. (40 mg/kg, max. 2g, 20 minuten) vergeleken met placebo. Als uitkomstmaten werden symptomen, zuurstofbehoefte, ICU-behandeling, opnameduur, heropname en behandeling met systemische steroïden bestudeerd. (20)
Een tabel met studiekarakteristieken is opgenomen in de evidence tabellen.
Kwaliteit van bewijs
Een GRADE Evidence Profile is weergegeven in de evidence tabellen.
Voor de uitkomstmaten gebruik prednisolon, noodzaak tot beademing en salbutamol i.v. werden geen resultaten gevonden. Hiervan kon uiteraard de kwaliteit van bewijs niet bepaald worden. Voor alle overige uitkomstmaten was de kwaliteit van bewijs laag tot zeer laag, vanwege de volgende factoren:
- Voor de uitkomstmaat bijwerkingen was alleen bewijs beschikbaar uit observationeel onderzoek.
- Bij de uitkomstmaten ernst symptomen en opnameduur is er sprake van indirect bewijs, omdat de patiëntenpopulatie in deze onderzoeken slecht vergelijkbaar is met de patiëntenpopulatie Nederlandse kinderen met een astma-exacerbatie; de kinderen in de studies hadden over het algemeen een milder ziektebeeld. Voor de uitkomstmaat ernst symptomen geldt bovendien dat onder andere vergeleken is met een behandeling die in Nederland niet meer wordt toegepast (terbutaline); dit impliceert eveneens indirect bewijs.
- Er is sprake van grote onnauwkeurigheid (imprecisie) van de resultaten bij alle uitkomstmaten, vanwege een beperkt aantal patiënten in de studies, en een nog beperkter aantal patiënten dat een bepaalde uitkomst (bijv. ziekenhuisopname) bereikt.
Effecten
Voor de uitkomstmaten noodzaak tot beademing en gebruik salbutamol i.v. zijn geen resultaten beschikbaar. Voor de overige uitkomstmaten worden onderstaand de resultaten beschreven:
- Symptomen/astmascore: de resultaten van de geïncludeerde studies zijn beperkt kwantitatief beschikbaar. Devi et al. rapporteerden astmascores, waarbij gebruik werd gemaakt van een gemodificeerde pulmonary index score, gebaseerd op ademhalingsfrequentie, wheezing, gebruik hulpademhalingsspieren en mate van dyspnoe. Zij vonden bij gebruik van MgSO4 na 1 uur een astmascore van 9 en bij placebo een astmascore van 10. De auteurs rapporteren dat dit een statistisch significant verschil is, maar dit wordt door de auteurs van deze richtlijn geen relevant verschil geacht.(5) Cirarallo et al. maakten gebruik van een gemodificeerde score voor de ernst van astma (modified Wood-Downes clinical asthma score), die na 95 minuten in de groep met MgSO4 gemiddeld 1,4 was en bij placebo 2,5.(1) In de studie van Gürkan ten slotte werd na 90 minuten de astmascore (vitale waarden, cyanose, inspiratoir ademgeluid, gebruik hulpademhalingsspieren, expiratoire wheezing en cerebrale functie) bepaald; bij gebruik van MgSO4 was deze gemiddeld 2,5, in de placebogroep 5,5, waarbij een lagere score een gunstiger resultaat betekent.(8) Uit het onderzoek van Scarfone et al. bleek geen statistisch significant verschil tussen MgSO4 en placebo voor wat betreft verbetering klinische astmascores.(19) Pruikkonen et al. vonden eveneens geen statistisch significant verschil in symptomen (gerapporteerd als verandering in RDAI (respiratory distress assessment instrument) bij jonge kinderen met acuut ernstig piepen.(20)
- Ziekenhuisopname: In het onderzoek van Ciarallo et al. werden in de MgSO4-groep 11/15 kinderen (73,3%) opgenomen en in de placebogroep 16/16 (100%). Het relatief risico (RR) was 0,73 (95%BI: 0,54-1,00).(2) De NNT was 4 (95%BI: 2 tot 20). Dat betekent dat 4 kinderen met MgSO4 behandeld moeten worden om één ziekenhuisopname te voorkomen. In het onderzoek van Scarfone et al. werden 11/24 (46%) van de kinderen uit de MgSO4-groep opgenomen in het ziekenhuis en in de placebogroep 16/30 (53%); dit verschil was niet statistisch significant.(19) Het geaggregeerde relatief risico op opname voor deze twee studies was 0,81 (95%BI: 0,58 tot 1,13).
- Opnameduur: In het onderzoek van Devi et al. werd een verschil in opnameduur gevonden tussen de MgSO4-groep (gem. 13,6 uur (sd 6,8)) en de placebogroep (gem. 18,9 uur (sd 7,7)) van 5,3 uur korter (95%BI: 1 uur korter tot 9,5 uur korter).(5)
- Gebruik prednisolon: In het onderzoek van Pruikkonen et al. kreeg 10% van de kinderen in de MgSO4-groep behandeling met systemische steroïden, in vergelijking met 23% in de placebogroep. Het verschil van 13,3% was niet statistisch significant (95%BI: -33,2 tot 5,5).(20)
- Bijwerkingen: In de geïncludeerde onderzoeken werd gevonden dat kinderen bij gebruik van MgSO4 geen ernstige of relevante bijwerkingen hadden.(2, 5, 6, 8) Devi et al. rapporteerden geen verschillen tussen MgSO4 en geen behandeling met MgSO4 voor wat betreft bloeddruk, saturatie en hypotensie. Bij kinderen die met MgSO4 werden behandeld, was de hart- en ademhalingsfrequentie wat lager.(5) Ciarallo et al. rapporteerden geen verschillen in bloeddruk en geen verandering in lichaamstemperatuur, duizeligheid, misselijkheid of andere symptomen.(2) Egelund et al. rapporteerden geen verschil tussen behandel- en controlegroep in systolische of diastolische bloeddruk. Hart- en ademhalingsfrequentie waren lager in de MgSO4-groep, maar dit was geen klinisch relevant verschil.(6) Gurkan et al. vonden geen verschil in bloeddruk en hartfrequentie tussen de MgSO4-groep en placebo.(8)
P Kinderen (1-18 jaar) met een status astmaticus op de SEH
I Intraveneuze behandeling met magnesiumsulfaat (verschillende doseringen, inloopsnelheid, herhaling van toediening)
C Geen behandeling met magnesiumsulfaat (of vergelijk met een andere dosering, andere inloopsnelheid, geen herhaling)
O Ernst van de symptomen (astmascore), ziekenhuisopname, noodzaak tot beademing, opnameduur, behoefte salbutamol i.v., duur en dosering prednisolon, bijwerkingen
Systematische review
Voor het beantwoorden van deze vraag is een systematische review van de literatuur uitgevoerd.
Zoekstrategie en selectie van de literatuur
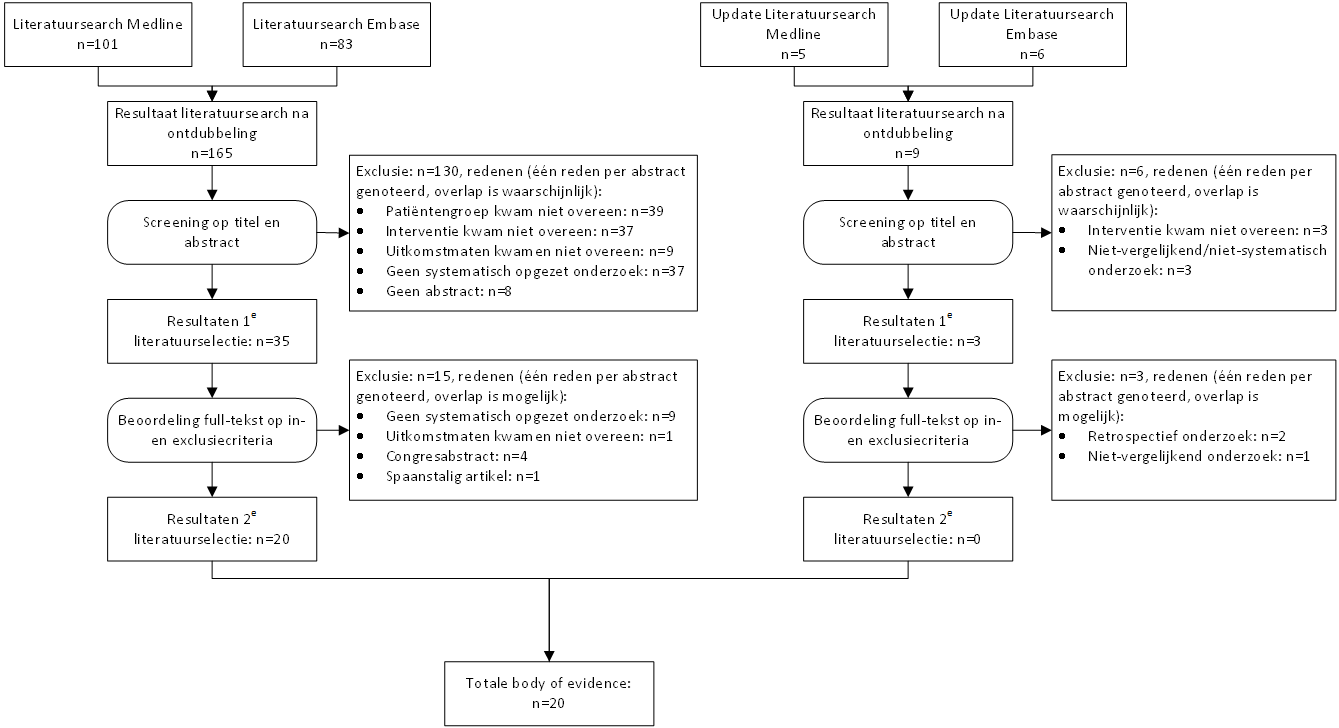
Voor het beantwoorden van deze uitgangsvraag is op 5 april 2019 gezocht in Medline en Embase (search strategie zie de zoekverantwoording). De literatuur is vervolgens geselecteerd op onderwerp (sluit het artikel aan bij de uitgangsvraag?), studiekenmerken (ten minste systematisch opgezet prospectief vergelijkend onderzoek) en artikeleigenschappen (abstract aanwezig, artikel in volledige tekst verkrijgbaar in Nederland, gepubliceerd in Nederlandse, Engelse of Duitse taal). De literatuurselectie is weergegeven in de zoekverantwoording. De eerste ronde literatuurselectie gebeurde op basis van de abstracts, waarna van 35 artikelen de volledige tekst werd bestudeerd. Daarvan bleken 20 artikelen geschikt voor beoordeling van de uitgangsvraag.(1-20) Een aantal van de gevonden artikelen waren systematische reviews;(12-16, 18) alle in deze reviews geïncludeerde studies waren ook in de literatuurselectie opgenomen. Vanwege de beperkte detailbeschrijving van de primaire studies in de review, dan wel de gedateerdheid van de review, is besloten uit te gaan van de primaire studies. Vanwege de grote kans op bias zijn daarbij retrospectieve en niet-vergelijkende studies geëxcludeerd.(4, 7, 10, 11). Bij een update van de search in juni 2020 werden nog eens 9 abstracts geïdentificeerd waarvan na selectie 3 artikelen in volledige tekst werden bestudeerd. Deze studies werden vervolgens geëxcludeerd, vanwege retrospectieve en/of niet-vergelijkende opzet. (21-23)
- Ciarallo L, Brousseau D, Reinert S. Higher-dose intravenous magnesium therapy for children with moderate to severe acute asthma. Arch Pediatr Adolesc Med. 2000;154(10):979-83.
- Ciarallo L, Sauer AH, Shannon MW. Intravenous magnesium therapy for moderate to severe pediatric asthma: results of a randomized, placebo-controlled trial. J Pediatr. 1996;129(6):809-14.
- Daengsuwan T, Watanatham S. A comparative pilot study of the efficacy and safety of nebulized magnesium sulfate and intravenous magnesium sulfate in children with severe acute asthma. Asian Pac J Allergy Immunol. 2017;35(2):108-12.
- DeSanti RL, Agasthya N, Hunter K, Hussain MJ. The effectiveness of magnesium sulfate for status asthmaticus outside the intensive care setting. Pediatr Pulmonol. 2018;53(7):866-71.
- Devi PR, Kumar L, Singhi SC, Prasad R, Singh M. Intravenous magnesium sulfate in acute severe asthma not responding to conventional therapy. Indian Pediatr. 1997;34(5):389-97.
- Egelund TA, Wassil SK, Edwards EM, Linden S, Irazuzta JE. High-dose magnesium sulfate infusion protocol for status asthmaticus: a safety and pharmacokinetics cohort study. Intensive Care Med. 2013;39(1):117-22.
- Glover ML, Machado C, Totapally BR. Magnesium sulfate administered via continuous intravenous infusion in pediatric patients with refractory wheezing. J Crit Care. 2002;17(4):255-8.
- Gurkan F, Haspolat K, Bosnak M, Dikici B, Derman O, Ece A. Intravenous magnesium sulphate in the management of moderate to severe acute asthmatic children nonresponding to conventional therapy. Eur J Emerg Med. 1999;6(3):201-5.
- Irazuzta J, Egelund T, Wassil SK, Hampp C. Feasibility of short-term infusion of magnesium sulfate in pediatric patients with status asthmaticus. Journal Pediatric Pharmacology & Therapeutics. 2012;17(2):150-4.
- Irazuzta JE, Paredes F, Pavlicich V, Dominguez SL. High-Dose Magnesium Sulfate Infusion for Severe Asthma in the Emergency Department: Efficacy Study. Pediatr Crit Care Med. 2016;17(2):e29-33.
- Johnson MD, Zorc JJ, Nelson DS, Casper TC, Cook LJ, Finkelstein Y, et al. Intravenous Magnesium in Asthma Pharmacotherapy: Variability in Use in the PECARN Registry. J Pediatr. 2020;220:165-74.e2.
- Kapuscinski CA, Stauber SD, Hutchinson DJ. Escalation in Therapy Based on Intravenous Magnesium Sulfate Dosing in Pediatric Patients With Asthma Exacerbations. J. 2020;25(4):314-9.
- Kokotajlo S, Degnan L, Meyers R, Siu A, Robinson C. Use of intravenous magnesium sulfate for the treatment of an acute asthma exacerbation in pediatric patients. J. 2014;19(2):91-7.
- Liu X, Yu T, Rower JE, Campbell SC, Sherwin CMT, Johnson MD. Optimizing the use of intravenous magnesium sulfate for acute asthma treatment in children. Pediatr Pulmonol. 2016;51(12):1414-21.
- Mohammed S, Goodacre S. Intravenous and nebulised magnesium sulphate for acute asthma: systematic review and meta-analysis. Emerg Med J. 2007;24(12):823-30.
- Ozdemir A, Dogruel D. Efficacy of Magnesium Sulphate Treatment in Children with Acute Asthma. Medical principles and practice: international journal of the Kuwait University, Health Science Centre. 2020;19.
- Pruikkonen H, Tapiainen T, Kallio M, Dunder T, Pokka T, Uhari M, et al. Intravenous magnesium sulfate for acute wheezing in young children: a randomised double-blind trial. Eur Respir J. 2018;51(2):02.
- Rowe BH, Bretzlaff JA, Bourdon C, Bota GW, Camargo Jr CA. Intravenous magnesium sulfate treatment for acute asthma in the emergency department: A systematic review of the literature. Ann Emerg Med. 2000;36(3):181-90.
- Rowe BH, Bretzlaff JA, Bourdon C, Bota GW, Camargo Jr CA. Magnesium sulfate for treating exacerbations of acute asthma in the emergency department. Cochrane database of systematic reviews (Online). 2000(2):CD001490.
- Scarfone RJ, Loiselle JM, Joffe MD, Mull CC, Stiller S, Thompson K, et al. A randomized trial of magnesium in the emergency department treatment of children with asthma. Ann Emerg Med. 2000;36(6):572-8.
- Shan Z, Rong Y, Yang W, Wang D, Yao P, Xie J, et al. Intravenous and nebulized magnesium sulfate for treating acute asthma in adults and children: a systematic review and meta-analysis. Respir Med. 2013;107(3):321-30.
- Singhi S, Grover S, Bansal A, Chopra K. Randomised comparison of intravenous magnesium sulphate, terbutaline and aminophylline for children with acute severe asthma. Acta Paediatr. 2014;103(12):1301-6.
- Su Z, Li R, Gai Z. Intravenous and Nebulized Magnesium Sulfate for Treating Acute Asthma in Children: A Systematic Review and Meta-Analysis. Pediatr Emerg Care. 2018;34(6):390-5.
Systematische reviews
Deze reviews zijn uiteindelijk niet in de resultaten opgenomen, omdat de hierin beschreven primaire studies die aan de selectiecriteria voldeden alle ook gevonden zijn in de literatuursearch voor deze richtlijn, en in de primaire studies met meer details beschreven zijn.
|
1e Auteur |
Jaartal |
Setting |
Design |
Doel |
Patiënten |
Interventie |
Controle |
Relevante uitkomstmaten |
Resultaten |
Conclusie auteurs |
Risk of bias / kwaliteit bewijs |
Opmerkingen |
|
Su |
2018 |
- |
Systematische review met meta-analyse |
Onderzoeken van de effectiviteit van intraveneus en verneveld MgSO4 bij kinderen met acuut astma op ziekenhuisopname en longfunctie |
V.w.b. studies naar intraveneus MgSO4: 6 studies met 20 tot 143 kinderen per studie, waarvan 4 studies onder kinderen met matig-ernstig astma en 2 met ernstig astma. Leeftijdsgroepen varieerden tussen de studies van 1-18 jaar. Drie v.d. studies werden uitgevoerd in de USA, de overige in Argentinië, Turkije en India |
Verschillende doseringen en schema’s intraveneus MgSO4 |
Saline oplossingen en co-behandelingen met beta-agonisten en corticosteroïden (ook in interventiegroep) |
|
De details van de geïncludeerde studies staan beperkt vermeld; daarom besloten om van de originele studies uitgegaan, die eveneens waren opgenomen in de literatuurselectie |
(Intraveneus MgSO4 is een effectieve behandeling voor kinderen, waarbij het aantal ziekenhuisopnamen wordt verminderd) |
Voor in de systematische review geïncludeerde studies: zie desbetreffende studies Voor systematische review: niet relevant |
Uiteindelijk exclusie en uitgaan van de primaire onderzoeken die in deze studie zijn opgenomen. |
|
Shan |
2013 |
- |
Systematische review met meta-analyse |
Onderzoeken van de effectiviteit van intraveneus en verneveld MgSO4 bij kinderen en volwassenen met acuut astma |
V.w.b. studies naar intraveneus MgSO4 bij kinderen: 5 studies met 20 tot 54 kinderen per studie, waarvan 4 studies onder kinderen met matig-ernstig astma en 1 met ernstig astma. Leeftijdsgroepen varieerden tussen de studies van 1-18 jaar. Drie v.d. studies werden uitgevoerd in de USA, de overige in Turkije en India |
Verschillende doseringen en schema’s intraveneus MgSO4 |
Saline oplossingen en co-behandelingen met beta-agonisten en corticosteroïden (ook in interventiegroep) |
|
De details van de geïncludeerde studies staan beperkt vermeld; daarom besloten om van de originele studies uitgegaan, die eveneens waren opgenomen in de literatuurselectie |
(Het gebruik van intraveneus MgSO4 lijkt effectief bij kinderen met acuut astma, in aanvulling op behandeling met beta-agonisten en systemische steroïden, in het verminderen van het aantal ziekenhuisopnamen) |
Voor in de systematische review geïncludeerde studies: zie desbetreffende studies Voor systematische review: niet relevant |
Uiteindelijk exclusie en uitgaan van de primaire onderzoeken die in deze studie zijn opgenomen. |
|
Liu |
2016 |
- |
Systematische review |
Onderzoeken rationale voor gebruik intraveneus MgSO4 bij kinderen met acuut astma, en voorstel doen voor toekomstig onderzoek |
7 studies met 20 tot 143 kinderen per studie, waarvan 4 studies onder kinderen met matig-ernstig astma en 3 met ernstig astma. Leeftijdsgroepen varieerden tussen de studies van 1-18 jaar |
Verschillende doseringen en schema’s intraveneus MgSO4 |
Saline oplossingen en co-behandelingen met beta-agonisten en corticosteroïden (ook in interventiegroep) |
|
De details van de geïncludeerde studies staan beperkt vermeld; daarom besloten om van de originele studies uitgegaan, die eveneens waren opgenomen in de literatuurselectie |
(Optimale dosisbepaling kan onderzocht worden in farmacokinetische/farmacodynamische modelstudies) |
Voor in de systematische review geïncludeerde studies: zie desbetreffende studies Voor systematische review: niet relevant |
Uiteindelijk exclusie en uitgaan van de primaire onderzoeken die in deze studie zijn opgenomen. |
|
Mohammed |
2007 |
- |
Systematische review met meta-analyse |
Onderzoeken effectiviteit intraveneus en verneveld MgSO4 bij kinderen en volwassenen met acuut astma |
V.w.b. studies naar intraveneus MgSO4 bij kinderen: 5 studies met 20 tot 54 kinderen per studie, waarvan vier studies onder kinderen met matig-ernstig astma en 1 met ernstig astma. Leeftijdsgroepen varieerden tussen de studies van 1-18 jaar |
Verschillende doseringen en schema’s intraveneus MgSO4 |
Saline oplossingen en co-behandelingen met beta-agonisten en corticosteroïden (ook in interventiegroep) |
|
De details van de geïncludeerde studies staan beperkt vermeld; daarom besloten om van de originele studies uitgegaan, die eveneens waren opgenomen in de literatuurselectie |
(Intraveneuze behandeling met MgSO4 lijkt een effectieve behandeling te zijn voor kinderen) |
Voor in de systematische review geïncludeerde studies: zie desbetreffende studies Voor systematische review: niet relevant |
Uiteindelijk exclusie en uitgaan van de primaire onderzoeken die in deze studie zijn opgenomen. |
|
Rowe (Ann Emerg Med) |
2000 |
- |
Systematische review met meta-analyse |
Onderzoeken effectiviteit intraveneus MgSO4 voor de behandeling van acuut astma |
V.w.b. studies naar intraveneus MgSO4 bij kinderen: 2 studies met 31 en 47 kinderen van 6-18 respectievelijk 1-21 jaar |
Verschillende doseringen en schema’s intraveneus MgSO4 |
Saline oplossing en co-behandeling met corticosteroïden (ook in interventiegroep) |
|
De details van de geïncludeerde studies staan beperkt vermeld; daarom besloten om van de originele studies uitgegaan, die eveneens waren opgenomen in de literatuurselectie |
(Geen evidence voor het routine gebruik van intraveneus MgSO4 bij patiënten met acuut astma, maar wel veilig voor patiënten met acuut ernstig astma) |
Voor in de systematische review geïncludeerde studies: zie desbetreffende studies Voor systematische review: niet relevant |
Uiteindelijk exclusie en uitgaan van de primaire onderzoeken die in deze studie zijn opgenomen. |
|
Rowe (Cochrane) |
2000 |
- |
Systematische review met meta-analyse |
Onderzoeken effectiviteit toevoegen intraveneus MgSO4 aan standaard behandeling bij patiënten met acuut astma op de SEH |
V.w.b. studies naar intraveneus MgSO4 bij kinderen: 2 studies met 31 en 47 kinderen van 6-18 respectievelijk 1-21 jaar |
Verschillende doseringen en schema’s intraveneus MgSO4 |
Saline oplossing en co-behandeling met corticosteroïden (ook in interventiegroep) |
|
Besloten om uit te gaan van de originele studies, die eveneens waren opgenomen in de literatuurselectie, aangevuld met studies die na publicatie van deze systematische review zijn uitgevoerd |
(Geen evidence voor het routine gebruik van intraveneus MgSO4 bij patiënten met acuut astma, maar wel veilig voor patiënten met acuut ernstig astma) |
Voor in de systematische review geïncludeerde studies: zie desbetreffende studies Voor systematische review: niet relevant |
Uiteindelijk exclusie en uitgaan van de primaire onderzoeken die in deze studie zijn opgenomen. |
Primaire studies
|
1e Auteur |
Jaartal |
Setting |
Design |
Doel |
Patiënten |
Interventie |
Controle |
Relevante uitkomstmaten |
Resultaten |
Conclusie auteurs |
Risk of bias / kwaliteit bewijs |
Opmerkingen |
||||||||||||||||||||||||||||||||||
|
Singhi |
2014 |
Kinder-SEH opleidingsziekenhuis, India |
Niet geblindeerde RCT |
Vergelijken effectiviteit en veiligheid intraveneus MgSO4, terbutaline en aminofylline op symptomen van acuut ernstig astma bij kinderen die onvoldoende reageerden op standaard behandeling |
100 kinderen van 1-12 jaar met acuut ernstig astma, die niet goed reageerden op de initiële standaard behandeling; de kinderen waren al bekend met astma. Exclusie: koorts, andere longziekten, hartziekten, nierziekten of hypotensie. Initiële behandeling patiënten: zuurstof inhalatie (6L/min), 3 maal verneveling salbutamol (0,15 mg/kg/dosis), budesonide (800 µg/dosis) en ipratropiumbromide (250 µg/dosis) en eenmaal hydrocortison (10mg/kg) Mediane lft 4-5 jaar, 65% jongens |
Intraveneuze behandeling met MgSO4 (50% oplossing van 50 mg/kg in 30 ml 0,18% saline in D5W) gedurende 20 min. |
|
|
|
Toevoegen van eenmalige intraveneuze dosis MgSO4 aan beta-2-agonisten en corticosteroïden leidt tot een snellere oplossing van acuut ernstig astma bij patiënten die niet goed reageren op de standaard behandeling, vergeleken met terbutaline of aminofylline |
|
|
|
|||||||||||||||||||||||||||||||||
|
Irazuzta |
2016 |
SEH van kinderziekenhuis, Paraguay |
Niet-geblindeerde RCT |
Onderzoeken effectiviteit hooggedoseerd intraveneus MgSO4 |
38 kinderen met niet-infectieus astma op de SEH, gem. lft. 10 jaar, 42% jongens Standaard behandeling op de SEH: dexamethason 0,2 mg/kg i.v. en 5 mg salbutamol via vernevelaar elke 20 minuten. Ernstig astma was gedefinieerd als geen verbetering (persisterend astma, incl. respiratoire distress en een Woods-Downes astmascore >2) na 2 uur behandeling. |
Intraveneus MgSO4 50 mg/kg/uur voor 4 uur, max. 8.000 mg/4 uur, in 0,9% saline 10 mg/mL |
Intraveneus MgSO4 50 mg/kg bolus (> 1 uur) |
|
|
Vroege beschikbaarheid van langdurig hooggedoseerd intraveneus MgSO4 verkort verblijf op de SEH en beperkt ziekenhuiskosten |
|
|
|
|||||||||||||||||||||||||||||||||
|
Gürkan |
1999 |
Kinder-SEH, universitair ziekenhuis, Turkije |
Dubbelblinde RCT |
Onderzoeken effectiviteit MgSO4 in terugdringen symptomen matig tot ernstig acuut astma, als beta-agonisten en corticosteroïden onvoldoende blijken |
20 kinderen met een acute astma exacerbatie (PEFRpred < 60% na 3 maal verneveld salbutamol (0,15 mg/kg), met tussenpozen van 20 min. en i.v. methylprednisolon 2 mg/kg), gem. lft. 10,8 jaar (sd 2,8, range 6-16), 55% jongens. Geen koorts, hypotensie, geen andere pulmonale, cardiale of renale aandoeningen |
Intraveneus MgSO4 15% 40 mg/kg (max. 2 g) in 100 ml saline 20 minuten. |
Waarschijnlijk saline oplossing, niet duidelijk vermeld |
|
|
Meer data zijn nodig om routine gebruik MgSO4 te ondersteunen, maar MgSO4 zou gebruikt moeten worden bij levensbedreigende astma voordat tot beademing wordt overgegaan |
|
|
|
|||||||||||||||||||||||||||||||||
|
Egelund |
2013 |
PICU, USA |
Prospectief cohortonderzoek |
Onderzoeken bruikbaarheid en veiligheid continue infuus MgSO4 in doses gebruikelijk bij pre-eclampsie |
57 kinderen met status astmaticus op PICU, gem. lft in behandellgroep 8,9 jaar (sd 4,2) in controlegroep 5,6 jaar (sd 3,8), 67% jongens |
Behandeling met MgSO4: oplaaddosis 75 mg/kg (bij kinderen <30 kg) of 50 mg/kg (bij kinderen ≥30 kg) gedurende 30-45 minuten, gevolgd door continue infusie van 40 mg/kg/uur voor 4 uur (n in deze groep 19) |
Geen behandeling met MgSO4 (n in deze groep 38) |
|
|
Continue infusie MgSO4 is veilig |
|
|
|
|||||||||||||||||||||||||||||||||
|
Devi |
1997 |
Kinder-SEH, opleidingsziekenhuis, India |
Dubbelblinde placebo-gecontroleerde RCT |
Onderzoeken effectiviteit vroege toediening intraveneus MgSO4 aan kinderen met acuut ernstig astma |
47 kinderen met acuut ernstig astma (onvoldoende reactie op 3 maal vernevelen met salbutamol gedurende 1 uur, geen koorts, geen hypotensie). Gem. lft. 6,7 jaar (sd 3,6), 77% jongens |
MgSO4: 0,2 ml/kg 50% in 30 ml oplossing saline in 5% dextrose gedurende 35 minuten + standaardbehandeling (zie controle) |
Placebo + standaardbehandeling (toediening zuurstof, adrenaline, salbutamol verneveling, steroïden, zo nodig aminofylline, isoprotenerol, ventilatie) |
|
|
Toevoegen van MgSO4 aan standaard behandeling helpt om sneller verbetering van tekenen en symptomen van astma te krijgen als op standaard behandeling onvoldoende gereageerd wordt |
|
|
|
|||||||||||||||||||||||||||||||||
|
Daengsuwan |
2017 |
Kinderziekenhuis, Thailand |
Niet geblindeerde RCT |
Vergelijken effectiviteit en veiligheid intraveneus en verneveld MgSO4 |
28 kinderen met persisterend ernstig astma (opgenomen kinderen met astmascore (niet vermeld welke score) >5, respiratoir falen (Wood), of wanneer kinderarts besloten had tot gebruik MgSO4), (geen andere long-, nier- of leverziekte, geen eerdere levensbedreigende aandoening, geen allergie voor MgSO4). Standaardbehandeling: salbutamol verneveling, ipratropium, corticosteroïden, zuurstof) Gem. lft. 5,3 jaar, 50% jongens |
Intraveneus MgSO4 eenmalig 20 minuten 50 mg/kg |
Verneveld MgSO4 3 maal 2,5 mL in 6% oplossing om de 20 minuten |
|
|
MgSO4 is zowel verneveld als intraveneus gunstig en veilig voor gebruik bij kinderen met een ernstige astma-exacerbatie |
|
|
|
|||||||||||||||||||||||||||||||||
|
Ciarallo |
1996 |
Kinder-SEH, USA |
Dubbelblinde placebo-gecontroleerde RCT |
Onderzoeken effectiviteit intraveneus MgSO4 bij kinderen met een matige tot ernstige astma exacerbatie |
31 kinderen met een acute astma exacerbatie (geen koorts, hypotensie, andere long-, nier- of leverziekte, geen theofylline gebruik) Gem. lft. 11,4 jaar (sd 3,5), 55% jongens Standaard behandeling: 3 maal verneveld salbutamol; bij PEFRpred <60%: inclusie in studie. Daarna methylprednisolon i.v. 2 mg/kg (als dit nog niet eerder gegeven was) |
Intraveneus MgSO4 25 mg/kg, max 2g, in 100 mL saline |
Placebo |
|
|
Intraveneus MgSO4 is veilig en effectief voor kinderen met matig tot ernstig astma, die onvoldoende reageren op standaard therapie |
Geen grote tekortkomingen |
|
|
|||||||||||||||||||||||||||||||||
|
Ciarallo |
2000 |
Kinder-SEH, 2 derdelijns ziekenhuizen, SEH |
Dubbelblinde placebo-gecontroleerde RCT |
Onderzoeken effectiviteit hooggedoseerde intraveneuze MgSO4 voor matige tot ernstige astma exacerbaties bij kinderen |
30 kinderen met acute astma exacerbatie, onvoldoende respons op 3 maal beta-agonisten (PEFRpred <70%), (geen koorts, theofylline, of andere aandoening). Behandeling met corticosteroïden Gem. lft 11,5 jaar, 60% jongens |
Intraveneus MgSO4 40 mg/kg (max 2 g) in 100 mL saline |
Placebo |
|
|
Kinderen die met 40 mg/kg intraveneus MgSO4 worden behandeld voor een matige tot ernstige astma exacerbatie laten een sterke verbetering zien in de longfunctie op korte termijn |
Geen grote tekortkomingen |
|
|
|||||||||||||||||||||||||||||||||
|
Scarfone |
2000 |
SEH, kinderziekenhuis, USA |
Dubbelblinde placebogecontroleerde RCT |
Onderzoeken effect magnesium i.v. bij matig tot ernstig zieke kinderen met astma |
54 kinderen met ≥1x piepen in anamnese, met matige tot ernstige astma exacerbatie op SEH (pulmonary index 8-13), geen gebruik corticosteroïden in laatste 72 uur. 28 jongens, gem. lft in Mg-groep: 81 mnd, in placebogroep: 58 mnd (p=0,04) |
Initiële behandeling met salbumatol verneveling; daarna salbutamol verneveling en 1,0 mg/kg (max 125 mg) prednisolon i.v., gevolgd door 75 mg/kg (max. 2,5 g) MgSO4 i.v. in 20 min. Aanvullend O2 bij saturatie ≤92%. Daarna salbutamol verneveling elke 30 min, |
Initiële behandeling met salbumatol verneveling; daarna salbutamol verneveling en 1,0 mg/kg (max 125 mg) prednisolon i.v., gevolgd door placebo (saline) i.v. in 20 min. Aanvullend O2 bij saturatie ≤92%. Daarna salbutamol verneveling elke 30 min, |
|
|
Routinegebruik van MgSO4 i.v. aan kinderen met een ernstige astma-exacerbatie is niet effectief |
Geen grote tekortkomingen |
|
|
|||||||||||||||||||||||||||||||||
|
Pruikkonen |
2018 |
Kinderziekenhuis, Finland |
Dubbelblinde placebogecontroleerde RCT |
Onderzoeken effectiviteit MgSO4 i.v. bij kinderen 6 mnd-4 jr met viral wheeze en ernstig acuut piepen |
61 kinderen met viral wheeze (exclusie kinderen met chronisch astma); gem. lft. 1,8 jr (sd 0,9), 53% jongen; gem. RDAI (respiratory distress assessment instrument) 10,2 bij MgSO4 en 12,0 bij placebo bij baseline (kinderen in MgSO4 groep bij aanvang minder symptomen) |
Salbutamol verneveling, zuurstof bij saturatie ≤92% MgSO4 i.v. 40mg/kg, max 2 g in 20 min. |
Salbutamol verneveling, zuurstof bij saturatie ≤92% Placebo |
|
|
MgSO4 i.v. is niet effectief voor de behandeling van acuut ernstig piepen bij jonge kinderen met viral wheeze |
Geen grote tekortkomingen |
|
|
|||||||||||||||||||||||||||||||||
GRADE Evidence Profile
Auteur(s): Mariska Tuut
Vraagstelling: Intraveneuze behandeling met magnesiumsulfaat compared to Geen intraveneuze behandeling met magnesiumsulfaat in kinderen met een status astmaticus
Setting: SEH, Nederlandse ziekenhuizen
Literatuur:
|
Certainty assessment |
Aantal patiënten |
Effect |
Certainty |
Importantie |
||||||||
|
Aantal studies |
Studieopzet |
Risk of bias |
Inconsistentie |
Indirect bewijs |
Onnauwkeurigheid |
Andere factoren |
intraveneuze behandeling met magnesiumsulfaat |
Geen intraveneuze behandeling met magnesiumsulfaat |
Relatief |
Absoluut |
||
|
Ernst symptomen (astmascore) (follow up: range 60 minuten tot 90 minuten; vastgesteld met: astmascore) |
||||||||||||
|
5 |
gerandomiseerde trials |
niet ernstig a |
niet ernstig |
ernstig b,c |
zeer ernstig d |
niet gevonden |
- Devi, studie met 22 patiënten: astmascore na 1 uur: MgSO4: 9, placebo: 10 (p<0,01), geen sd of 95%BI vermeld - Ciarallo, studie met 30 patiënten: astmascore (modified score) na 95 minuten: MgSO4: 1,4, placebo: 2,5 Gürkan: studie met 20 patiënten: astmascore na 90 minuten: MgSO4: 2,5, placebo: 5,5; Scarfone en Pruikkonen: geen statistisch significant verschil in symptomen |
⨁◯◯◯ |
||||
|
Ziekenhuisopname |
||||||||||||
|
2 |
gerandomiseerde trials |
niet ernstig |
niet ernstig |
niet ernstig |
zeer ernstig d |
niet gevonden |
22/39 (56.4%) |
32/46 (69.6%) |
RR 0.81 |
132 minder per 1.000 |
⨁⨁◯◯ |
|
|
Noodzaak tot beademing - niet gemeten |
||||||||||||
|
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
|
Opnameduur |
||||||||||||
|
1 |
gerandomiseerde trials |
niet ernstig |
niet ernstig f |
ernstig b |
zeer ernstig d |
niet gevonden |
11 |
11 |
- |
MD 5.3 uren minder |
⨁◯◯◯ |
|
|
Behoefte salbutamol i.v. - niet gemeten |
||||||||||||
|
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
|
Gebruik prednisolon (duur en dosering) |
||||||||||||
|
1 |
gerandomiseerde trials |
niet ernstig |
niet ernstig f |
ernstig b |
zeer ernstig d |
niet gevonden |
Niet te berekenen |
133 minder per 1.000 |
⨁◯◯◯ |
|||
|
Bijwerkingen |
||||||||||||
|
4 |
observationele studies g |
niet ernstig |
niet ernstig |
niet ernstig |
zeer ernstig d |
niet gevonden |
- Egelund, cohortstudie met 57 patiënten, 3/19 kinderen (16%) in MgSO4-groep had bijwerkingen (bijv. misselijkheid), geen ernstige bijwerkingen - Devi, dubbelblinde RCT met 47 patiënten: geen ernstige bijwerkingen; 13% had last van warmte, 17% pijn bij infuus, 13% tintelingen bij infuus - Gürkan, dubbelblinde RCT met 20 patiënten: geen 'significante' bijwerkingen - Ciarallo, 1996: dubbelblinde RCT met 31 patiënten: geen relevante bijwerkingen |
⨁◯◯◯ |
||||
CI: Confidence interval; RR: Risk ratio; MD: Mean difference
Explanations
a. Bij 1 van de 5 studies (Gürkan, 1999) is niet duidelijk of adequaat gerandomiseerd is, maar dit is onvoldoende grond om af te waarderen op risk of bias
b. De patiëntenpopulaties in de onderzoeken zijn niet vergelijkbaar met de Nederlandse patiëntenpopulatie van deze richtlijn
c. In één van de geïncludeerde onderzoeken is vergeleken met terbutataline, dat in Nederland niet meer gebruikt wordt
d. Optimal information size wordt niet gehaald, te weinig patiënten om zekere resultaten te geven
e. Geen controlegroep bij deze studie, dat maakt vergelijken met geen behandeling met MgSO4 onmogelijk
f. Inconsistentie is niet mogelijk, wanneer er resultaten van slechts één onderzoek gebruikt zijn
g. 3 kleine RCT's, 2 cohortonderzoeken
Beoordelingsdatum en geldigheid
Publicatiedatum : 02-11-2021
Beoordeeld op geldigheid : 29-09-2021
De Nederlandse Vereniging voor Kindergeneeskunde is eerstverantwoordelijke voor de actualiteit van deze richtlijn. Ook de overige bij de ontwikkeling van deze richtlijn betrokken wetenschappelijke verenigingen en de patiëntenorganisatie monitoren de actualiteit van de richtlijn. Ontwikkelingen binnen het vakgebied kunnen aanleiding zijn om één of meerdere modules van de richtlijn te herzien. Uiterlijk in 2026 bepaalt de richtlijncommissie van de Nederlandse Vereniging voor Kindergeneeskunde of deze richtlijn nog actueel is. Indien gedeeltelijke of totale herziening wenselijk is, dan spant de Nederlandse Vereniging voor Kindergeneeskunde zich ervoor in om dit te realiseren.
Algemene gegevens
De ontwikkeling van deze richtlijn is gefinancierd door de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier had geen invloed op de inhoud van de richtlijn.
Aanleiding
De herziening van de NVK-richtlijnen ‘Astma bij kinderen (2013)’ en ‘Acuut astma bij kinderen, richtlijn voor de opvang in het 1e uur (2012)’ is geprioriteerd door de sectie Kinderlongziekten van de Nederlandse Vereniging voor Kindergeneeskunde. Op basis van die prioritering en advies van de commissie Richtlijnen van de Nederlandse Vereniging voor Kindergeneeskunde is een SKMS-aanvraag gedaan.
Doel en doelgroep
Doel
Het doel van deze richtlijn is het bieden van ondersteuning aan kinderartsen bij het realiseren van een uniform en zoveel mogelijk evidence-based beleid bij kinderen van 1 tot 18 jaar met (verdenking op) astma.
Doelgroep
Deze richtlijn is primair geschreven voor de doelgroep kinderartsen en arts-assistenten (niet) in opleiding tot kinderarts. Kinderlongverpleegkundigen, verpleegkundig specialisten en physician assistants en andere zorgmedewerkers die betrokken zijn bij de zorg voor kinderen met astma in de 2e lijn kunnen eveneens informatie ontlenen aan deze richtlijn.
Samenstelling werkgroep
Voor de ontwikkeling van deze richtlijn is een richtlijnwerkgroep samengesteld. In de werkgroep participeerden gemandateerde vertegenwoordigers van de belangrijkste beroepsverenigingen die te maken hebben met de zorg rondom kinderen met astma. Verschillende secties van de Nederlandse Vereniging voor Kindergeneeskunde waren hierin vertegenwoordigd. Om het patiëntenperspectief te waarborgen, hadden een ouder van een kind met astma en een medewerker van het Longfonds zitting in de werkgroep. De werkgroep is procedureel en methodologisch ondersteund door PROVA en logistiek door het bureau van de Nederlandse Vereniging voor Kindergeneeskunde. De werkgroep bestond uit de volgende personen:
- Dr. Erik-Jonas van de Griendt, kinderarts-pulmonoloog, namens de Sectie Kinderlonggeneeskunde van de Nederlandse Vereniging voor Kindergeneeskunde, voorzitter en projectleider (sinds april 2020)
- Mariska Tuut, epidemioloog/richtlijnmethodoloog, PROVA, secretaris
- Magda Barnhoorn, namens Longfonds (tot april 2020)
- Patrick Bhairosing, namens Longfonds (sinds december 2020)
- Prof. Dr. Patrick Bindels, huisarts, namens het Nederlands Huisartsen Genootschap
- Dr. Annemie Boehmer, kinderarts-pulmonoloog, namens de Sectie Kinderlonggeneeskunde van de Nederlandse Vereniging voor Kindergeneeskunde, voorzitter en projectleider (tot april 2020)
- Viona Boerefijn-Smets, ervaringsdeskundige, namens Longfonds (tot juni 2020)
- Linda Eijking, longverpleegkundige, namens Verpleegkundigen & Verzorgenden Nederland
- Dr. Bart van Ewijk, kinderarts-pulmonoloog, namens de Sectie Kinderlonggeneeskunde van de Nederlandse Vereniging voor Kindergeneeskunde
- Sabien van der Geest-Heisterkamp, kinderarts-intensivist, namens de Sectie Intensive Care Kinderen van de Nederlandse Vereniging voor Kindergeneeskunde
- Xana van Jaarsveld, namens Longfonds (van april 2020 tot december 2020)
- Ursula Kooijman, ervaringsdeskundige, namens Longfonds (sinds augustus 2020)
- Dr. Gerbrich van der Meulen, kinderarts-allergoloog, namens de Sectie Kinderallergologie van de Nederlandse Vereniging voor Kindergeneeskunde
- Niels Rutjes, kinderarts-pulmonoloog, namens de Sectie Kinderlonggeneeskunde van de Nederlandse Vereniging voor Kindergeneeskunde
- Mariël Verwaal, Verpleegkundig Specialist Kinderlongziekten, namens Verpleegkundigen & Verzorgenden Nederland
De klankbordgroep bestond uit gemandateerde vertegenwoordigers van beroepsgroepen, die niet primair de doelgroep zijn van deze richtlijn, maar wel specifieke expertise hebben op het gebied van het onderwerp van de richtlijn. De klankbordgroep is per e-mail benaderd om de conceptteksten van de richtlijn te becommentariëren. De klankbordgroep bestond uit de volgende personen:
- Dr. Mathieu Bolhuis, ziekenhuisapotheker, namens de Nederlandse Vereniging voor Ziekenhuisapothekers
- Dr. Peter Klijn, kinderfysiotherapeut, namens het Koninklijk Nederlands Genootschap voor Fysiotherapie
- Sandra Lever, kinderlongfunctie-analist, namens de Nederlandse Vereniging van Longfunctieanalisten
- Ellen van der Linden, jeugdarts, namens AJN Jeugdartsen Nederland
- Renate Nicolaas, klinisch psycholoog, namens het Nederlands Instituut van Psychologen
- Roselin van der Torren-Klever, jeugdarts, namens AJN Jeugdartsen Nederland
- Jurgen te Rijdt, keel-neus-oorarts, namens de Nederlandse Vereniging voor Keel-Neus-Oorheelkunde en Heelkunde van het Hoofd-Halsgebied
- Dr. Marjo van de Ven, longarts, namens de Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose
- Rene Verbeek, spoedeisende hulp arts, namens de Nederlandse Vereniging van Spoedeisende Hulp Artsen
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden en klankbordgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad (zie onderstaande tabel). Er waren geen beperkingen voor deelname geconstateerd.
|
Naam |
Hoofdfunctie(s) |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
|
|
Erik-Jonas van de Griendt (projectleider sinds april 2020) |
Kinderarts-pulmonoloog:
|
Lid werkgroep Persisterend Ernstig Astma (PSA) van de Sectie kinderlongziekten, NVK (onbetaald) PhD-candidate Post Graduate School UvA Amsterdam (onbetaald) |
Geen persoonlijke financiële belangen te melden |
Geen persoonlijke relaties die kunnen leiden tot belangenverstrengeling te melden |
Geen extern gefinancierd onderzoek te melden |
Niet van toepassing |
Nee |
|
|
Mariska Tuut (richtlijnmethodoloog) |
Eigenaar PROVA (adviesbureau evidence-based richtlijnontwikkeling, richtlijnmethodoloog) |
PhD-candidate CAPRHI Research School, Maastricht University, onbetaald |
geen |
geen |
geen |
geen |
geen |
|
|
Magda Barnhoorn (werkgroep, tot april 2020) |
Projectleider Zorg bij Longfonds |
- |
- |
- |
- |
- |
- |
|
|
Patrick Bhairosing (werkgroep sinds december 2020) |
Projectleider Kinderen en jongeren met longziekten |
- |
- |
- |
- |
- |
- |
|
|
Patrick Bindels (werkgroep) |
Hoogleraar huisartsgeneeskunde, hoofd afdeling huisartsgeneeskunde, Erasmus MC Rotterdam, fulltime |
- |
Geen |
Nee |
- |
Geen |
Nee |
|
|
Annemie Boehmer (projectleider tot april 2020) (kerngroep) |
|
Alles dus onbetaald |
Ik heb betaald advies gegeven aan GlaxoSmithKline en zou nog uitgenodigd kunnen worden voor weer een advies op gebied van biologicals voor ernstig astma |
Nee |
Geen belangenverstrengeling |
Geen |
Geen bekend |
|
|
Viona Boerefijn-Smets (werkgroep tot juni 2020) |
Niet werkzaam, thuisblijfmoeder (in 2013 afgestudeerd aan de Universiteit van Tilburg; master theologie/categoriaal pastoraat) |
|
|
|
n.v.t. |
Nee, in principe niet |
Nee |
|
|
Linda Eijking (werkgroep) |
|
Voorzitter taakgroep Kinderlongverpleegkundigen V&VN (onbetaald) |
Nee |
Nee |
Nee |
Nee |
Nee |
|
|
Bart van Ewijk (werkgroep) |
|
|
Geen |
Nee |
Nee |
Werkzaam in enige astmacentrum in Nederland met klinische opname mogelijkheid |
Nee |
|
|
Sabien van der Geest-Heisterkamp (werkgroep) |
Kinderarts-kinderintensivist LUMC (ICK) |
Instructeur APLS (Riel), onbetaald/onkosten vergoeding |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
|
|
Xana van Jaarsveld (werkgroep van april 2020 tot december 2020) |
Adviseur Zorg, Longfonds |
n.v.t. |
n.v.t |
n.v.t |
n.v.t. |
n.v.t |
geen |
|
|
Ursula Kooijman (werkgroep, sinds augustus 2020) |
Patiëntvertegenwoordiger Longfonds |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
|
|
Gerbrich v.d. Meulen (werkgroep) |
Kinderarts-allergoloog, Martini Ziekenhuis, Groningen |
n.v.t. |
geen |
neen |
Alleen onderzoek mede gefinancierd door Danone. Geen belangenverstrengeling m.b.t. astma richtlijn |
Boegbeeld Speerpunt Martini allergie centrum voor kinderen (geen belangenverstrengeling m.b.t. deze richtlijn) |
neen |
|
|
Niels Rutjes (werkgroep) |
Kinderlongarts, Amsterdam UMC / Emma Kinderziekenhuis |
|
Eenmalige deelname adviseraad mepolizumab GSK |
Geen |
Geen |
Geen |
Geen |
|
|
Mariël Verwaal (werkgroep) |
|
|
Geen persoonlijke financiële belangen |
Nee, geen persoonlijke belangen |
Geen belang |
Geen belang |
Neen |
|
|
Mathieu Bolhuis (klankbordgroep) |
Ziekenhuisapotheker / klinisch farmacoloog UMCG |
n.v.t. |
n.v.t. |
|
n.v.t. |
n.v.t. |
n.v.t. |
|
|
Peter Klijn (klankbordgroep) |
|
|
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
|
|
Sandra Lever (klankbordgroep) |
Longdiagnostisch laborant, ErasmusMC locatie Sophia Kinderziekenhuis |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
|
|
Ellen van der Linden (klankbordgroep) |
Jeugdarts Jeugdgezondheidszorg Zuid-Holland West |
|
- |
- |
- |
- |
- |
|
|
Renate Nicolaas (klankbordgroep) |
Klinisch psycholoog / kinder- en jeugdpsycholoog NIP |
geen |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
geen |
|
|
Jurgen te Rijdt (klankbordgroep) |
|
- |
geen |
geen |
nee |
geen |
Geen belangen |
|
|
Roselin van der Torren-Klever (klankbordgroep) |
Jeugdarts GGDHM |
geen |
geen |
geen |
geen |
geen |
geen |
|
|
Marjo v.d. Ven (klankbordgroep) |
Longarts Rijnstate Arnhem |
geen |
|
nee |
|
n.v.t. |
nee |
|
|
René Verbeek (klankbordgroep) |
SEH-arts KNMG in het Nij Smellinghe Ziekenhuis te Drachten |
|
Niet van toepassing |
Nee |
Niet van toepassing |
Niet van toepassing |
|
|
Methode ontwikkeling
Evidence based
Implementatie
Tijdens de ontwikkeling van de richtlijn is zoveel mogelijk rekening gehouden met de implementatie van de richtlijn en de uitvoerbaarheid van de aanbevelingen. Bij deze richtlijn hoort een implementatieplan, bedoeld om de implementatie van de richtlijn te faciliteren.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van de Federatie Medisch Specialisten.
Knelpunteninventarisatie
Bij de start van het richtlijnontwikkeltraject zijn knelpunten in de zorg voor kinderen met astma geïnventariseerd alle Nederlandse kinderartsen via de Nederlandse Vereniging voor Kindergeneeskunde (NVK) en separaat bij de Sectie Kinderlongziekten van de NVK, de leden van de richtlijnwerkgroep en de klankbordgroep. Dit heeft geleid tot een grote hoeveelheid knelpunten. Door de richtlijnwerkgroep zijn 6 knelpunten geprioriteerd. Vijf daarvan zijn nieuwe knelpunten, die niet eerder in de richtlijn zijn behandeld. Deze vijf nieuwe knelpunten zijn uitgewerkt m.b.v. de GRADE-methodiek (www.gradeworkinggroup.org). Een uitgebreide verantwoording van de werkwijze is vermeld in de betreffende modules. Het zesde geprioriteerde knelpunt betreft een herziening van de belangrijkste delen van de eerdere richtlijn uit 2013; deze was destijds grotendeels gebaseerd op de toentertijd actuele BTS/SIGN-richtlijn. De werkgroep heeft de betreffende tekst getoetst op actualiteit en waar nodig aangepast.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpunteninventarisatie zijn door de kerngroep concept-uitgangsvragen vastgesteld, inclusief een voorstel voor patiëntrelevante uitkomstmaten. Deze uitgangsvragen en uitkomstmaten zijn vervolgens door de richtlijnwerkgroep bediscussieerd en vastgesteld.
Literatuuronderzoek
Het literatuuronderzoek voor de richtlijn is uitgevoerd door de richtlijnmethodoloog van de richtlijnwerkgroep, daarin inhoudelijk bijgestaan door de projectleider. De conceptteksten zijn geschreven door de projectleider en richtlijnmethodoloog. De conceptteksten zijn per e-mail voorbereid en tijdens de werkgroepvergaderingen zorgvuldig bediscussieerd door de richtlijnwerkgroep. Daarbij is telkens expliciet aandacht besteed aan het patiëntenperspectief. De conceptteksten zijn vastgesteld door de richtlijnwerkgroep. Daarna zijn de conceptteksten voorgelegd aan de leden van de klankbordgroep.
Strategie voor zoeken en selecteren van de literatuur
Er werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in Medline en Embase. Voor specifieke verantwoording van het zoek- en selectieproces wordt verwezen naar de inhoudelijke modules.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld en samengevat in tabellen met studiekarakteristieken en ook samengevat in de tekst van de modules. Daarbij is expliciet aandacht besteed aan risk of bias en overige kwaliteitsaspecten van het wetenschappelijk bewijs.
Samenvatten van de literatuur
Een samenvatting van de totale body of evidence werd gemaakt met behulp van de GRADE methodiek (zie www.gradeworkinggroup.org), waarbij GRADE Evidence Profiles werden opgesteld. Voor het statistisch poolen van data werd gebruik gemaakt van RevMan5.
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt, kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje Van bewijs naar aanbeveling.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling.
Commentaarronde
Na verwerking van alle feedback uit de werkgroep en de klankbordgroep is de richtlijn voor commentaar voorgelegd aan de volgende verenigingen/organisaties:
- Nederlandse Vereniging voor Kindergeneeskunde:
- Sectie kinderlongziekten
- Sectie Intensive Care Kinderen
- Sectie Kinderallergologie
- Expertisegroep Algemene Kindergeneeskunde
- Expertisegroep Acute Kindergeneeskunde
- Alle leden Nederlandse Vereniging voor Kindergeneeskunde
- Longfonds
- Stichting Kind en Ziekenhuis
- Verpleegkundigen & Verzorgenden Nederland:
- Afdeling longverpleegkundigen
- Afdeling verpleegkundig specialisten
- Nederlands Huisartsen Genootschap
- Nederlandse Vereniging van Ziekenhuisapothekers
- Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose
- Nederlandse Vereniging van Longfunctieanalisten
- AJN Jeugdartsen Nederland
- Nederlandse Vereniging van Spoedeisende Hulp Artsen
- Lareb
- Kinderformularium
- Zorgverzekeraars Nederland
- Nederlandse Federatie van Universitair Medische Centra
- Nederlandse Vereniging van Ziekenhuizen
- Vereniging Innovatieve Geneesmiddelen
De binnengekomen commentaren zijn verzameld en in concept verwerkt door de projectleider en richtlijnmethodoloog. Dit is voorgelegd aan de richtlijnwerkgroep. De vastgestelde conceptteksten zijn ter autorisatie voorgelegd.
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling beschreven (zie de bijlage ‘Kennislacunes’).
Patiëntenvoorlichtingsmateriaal
Hiervoor verwijst de werkgroep naar www.thuisarts.nl, www.astmakids.nl en www.longfonds.nl/longziekten/astma.
Juridische betekenis
Richtlijnen zijn geen wettelijke voorschriften, maar op wetenschappelijk bewijs gebaseerde inzichten en aanbevelingen waaraan zorgverleners moeten voldoen om kwalitatief goede zorg te verlenen. Na autorisatie van de richtlijn door een beroepsvereniging, wordt de richtlijn gezien als deel van de ‘professionele standaard'.
Aangezien de aanbevelingen hoofdzakelijk gebaseerd zijn op de ‘gemiddelde patiënt', kunnen zorgverleners op basis van hun professionele autonomie waar nodig afwijken van de richtlijn. Afwijken van richtlijnen kan in bepaalde situaties zelfs noodzakelijk zijn. Wanneer van de richtlijn wordt afgeweken, dient dit beargumenteerd en gedocumenteerd te worden.
Zoekverantwoording
Medline
Database: Ovid MEDLINE(R) ALL <1946 to April 05, 2019>
Search Strategy:
--------------------------------------------------------------------------------
1 "asthma zoekacties april 2019".ti. (0)
2 exp Asthma/ (122293)
3 exp Bronchial Spasm/ (4275)
4 asthma$.mp. (170072)
5 wheez$.mp. (12896)
6 bronchospas$.mp. (5295)
7 (bronch$ adj3 spas$).mp. (4619)
8 bronchoconstrict$.mp. (11277)
9 (bronch$ adj3 constrict$).mp. (697)
10 airway$ inflammation$.mp. (13948)
11 or/2-10 (187530)
12 "P voor asthma".ti. (0)
13 (status adj2 asthmatic*).tw. (1357)
14 (status adj2 asthmatic*).kf. (46)
15 "asthma exacerbation".kw. (117)
16 (status adj2 asthmatic*).ti. (921)
17 (child??? or childhood or infant* or p?ediatr* or perinat* or neonat* or newborn* or infan* or boy? or girl? or kid? or schoolage* or juvenil* or adolescen* or toddler?).tw. (2184768)
18 (child??? or childhood or infant* or p?ediatr* or perinat* or neonat* or newborn* or infan* or boy? or girl? or kid? or schoolage* or juvenil* or adolescen* or toddler?).kf. (263466)
19 exp Child/ (1819952)
20 exp infant/ (1092151)
21 "Adolescent"/ (1923475)
22 17 or 18 or 19 or 20 or 21 (4037996)
23 exp Status Asthmaticus/ (1220)
24 11 or 23 (187530)
25 (dutch or english or german or french).la. (26454068)
26 22 and 24 and 25 (61904)
27 exp Magnesium Sulfate/ (4971)
28 (magnesium adj2 sul??ate).tw. (5106)
29 (magnesium adj2 sul??ate).kf. (658)
30 exp Administration, Intravenous/ (139003)
31 intravenous.tw. (269648)
32 intravenous.kf. (5742)
33 or/30-32 (343948)
34 27 or 28 or 29 (7278)
35 26 and 33 and 34 (101)
36 35 (101)
37 limit 36 to yr="1990 -Current" (100)
38 from 37 keep 1-100 (100)
39 exp Albuterol/ (9706)
40 "Adrenergic beta-2 Receptor Agonists"/ (2694)
41 (bronchodilat* or adrenergic beta-agonists or beta-agonist or (beta adj agonist*) or beta2* or beta-2* or albuterol or salbutamol or levalbuterol or levosalbutamol or ventolin* or proventil or ventosol or proair or isoproterenol or metaproterenol or aluprent or terbutaline or brethine or bricanyl or fenoterol or bedoradrine or reproterol or clenbuterol).tw. (107248)
42 (bronchodilat* or adrenergic beta-agonists or beta-agonist or (beta adj agonist*) or beta2* or beta-2* or albuterol or salbutamol or levalbuterol or levosalbutamol or ventolin* or proventil or ventosol or proair or isoproterenol or metaproterenol or aluprent or terbutaline or brethine or bricanyl or fenoterol or bedoradrine or reproterol or clenbuterol).kf. (3688)
43 39 or 40 or 41 or 42 (110434)
44 (bronchodilat* or adrenergic beta-agonists or beta-agonist or (beta adj agonist*) or beta2* or beta-2* or albuterol or salbutamol or levalbuterol or levosalbutamol or ventolin* or proventil or ventosol or proair or isoproterenol or metaproterenol or aluprent or terbutaline or brethine or bricanyl or fenoterol or bedoradrine or reproterol or clenbuterol).ti. (30543)
45 (intraven* or bolus or infus* or inject*).tw. (1154849)
46 (intraven* or bolus or infus* or inject*).kf. (23748)
47 30 or 45 or 46 (1200148)
48 39 or 40 or 42 or 44 (38273)
49 26 and 47 and 48 (228)
50 49 (228)
51 limit 50 to yr="1990 -Current" (145)
52 26 and 34 and 47 (105)=kind +P of status asthmaticus +talen
53 52 (105)
54 limit 53 to yr="1990 -Current" (104)
Embase
Database: Embase <1974 to 2019 April 24>
Search Strategy:
--------------------------------------------------------------------------------
1 exp asthma/ (241412)
2 wheezing/ (24972)
3 chronic lung disease/ (11409)
4 exp bronchospasm/ (25096)
5 exp bronchoconstriction/ (26808)
6 asthma$.mp. (273625)
7 wheez$.mp. (30684)
8 bronchospas$.mp. (27644)
9 (bronch$ adj3 spas$).mp. (597)
10 bronchoconstrict$.mp. (11958)
11 (bronch$ adj3 constrict$).mp. (950)
12 airway$ inflammation$.mp. (22027)
13 or/1-12 (320245)
14 (dutch or english or german or french).la. (29001375)
15 (status adj2 asthmatic*).tw. (1649)
16 (status adj2 asthmatic*).kw. (250)
17 (asthma adj exacerbation).kw. (311)
18 asthmatic state/ (2168)
19 13 or 15 or 16 or 17 or 18 (320245)
20 "filter kind embase".ti. (0)
21 child/ (1571210)
22 exp pediatrics/ (98356)
23 adolescent/ (1419188)
24 (child??? or childhood or infant* or p?ediatr* or perinat* or neonat* or newborn* or infan* or boy? or girl? or kid? or schoolage* or juvenil* or adolescen* or toddler?).tw. (2661698)
25 (child??? or childhood or infant* or p?ediatr* or perinat* or neonat* or newborn* or infan* or boy? or girl? or kid? or schoolage* or juvenil* or adolescen* or toddler?).kw. (434710)
26 or/21-25 (3728105)
27 magnesium sulfate/ (15259)
28 (magnesium adj2 sul??ate).tw. (6889)
29 (magnesium adj2 sul??ate).kw. (1327)
30 27 or 28 or 29 (16377)
31 14 and 19 and 26 and 30 (448)
32 31 (448)
33 limit 32 to yr="1990 -Current" (446)
34 *magnesium sulfate/ (5812)
35 (magnesium adj2 sul??ate).ti. (2881)
36 29 or 34 or 35 (6193)
37 31 and 36 (132) P + kind + I(focus)
Literatuurselectie