Tromboseprofylaxe bij gipsimmobilisatie been
Uitgangsvraag
Is tromboseprofylaxe geïndiceerd bij patiënten met gipsimmobilisatie van het onderbeen voor een geïsoleerd letsel?
Voor de uitwerking van deze uitgangsvraag zijn drie deelvragen geformuleerd:
- Deelvraag 1. Wat is de effectiviteit van behandeling met tromboseprofylaxe bij patiënten met gipsimmobilisatie van het onderbeen voor een geïsoleerd letsel?
- Deelvraag 2. Wat zijn risicofactoren voor het optreden van een trombose bij patiënten met gipsimmobilisatie van het onderbeen?
- Deelvraag 3. Welke predictiemodellen kunnen gebruikt worden voor het voorspellen van trombose bij patiënten met gipsimmobilisatie van het onderbeen?
Aanbeveling
Overweeg om geen farmacologische tromboseprofylaxe aan patiënten met onderbeengips immobilisatie te geven.
Overweeg patiënten met een voorgeschiedenis van VTE, of met een uitgebreid trauma, te behandelen met farmacologische tromboseprofylaxe met LMWH.
Overwegingen
Bewijs effectiviteit LMWH bij gips-immobilisatie
De meest recente Cochrane review beschrijft alle trials die zijn uitgevoerd tot april 2017 (Zee, 2017). Er werden ten opzichte van de eerdere Cochrane (Testroote, 2014) twee nieuwe RCT’s geïncludeerd (Bruntink, 2017 en van Adrichem, 2017). In deze Cochrane werd met lage GRADE bewijslast een positief effect gevonden voor het gebruik van LMWH op de reductie van symptomatische VTE (RR 0,41, 95%BI 0,18 tot 0,94). Van de 8 RCT’s die zijn meegenomen in deze Cochrane was er echter maar 1 die de effectiviteit op het voorkomen van symptomatische VTE heeft onderzocht (van Adrichem, 2017). In de andere 7 trials werd gescreend op asymptomatische DVT, waarbij symptomatische VTE’s werden gedefinieerd als een asymptomatische DVT waarbij de patiënt éen of meer symptomen van pijn, zwelling et cetera aangaf tijdens screening op een DVT. Deze misclassificatie van symptomatische VTE, zorgt er in combinatie met een selectie van patiënten (bias) en hoge aantallen patiënten die lost to follow-up waren voor, dat de bewijskracht van deze Cochrane review Laag is. De studie van Van Adrichem (2017) was als enige groot genoeg voor de effectiviteit op symptomatische VTE, deze weegt dan ook het zwaarst mee bij het gepoolde resultaat.
Figuur 1
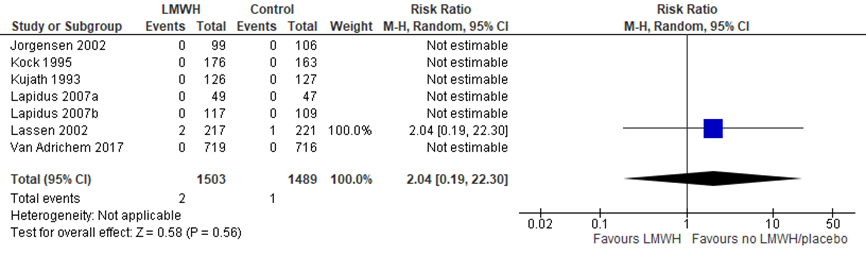
Het risico op VTE is ongeveer 2,0% voor patiënten die worden behandeld met onderbeengips immobilisatie (Nemeth, 2019). Uitgaande van een incidentie van 2,0% en een relatief risico op VTE met LMWH van 0,41, is er absolute risicoreductie te behalen van maximaal -1,18%. Dit geeft een minimaal Number Needed to Treat (NNT) van 85, wat waarschijnlijk hoger ligt doordat de RR van 0,41 is overschat. Door het hoge NNT, lage absolute risico voor VTE, het mogelijk verhoogde risico op complicaties en de LAGE GRADE-classificatie voor effectiviteit van tromboseprofylaxe is de commissie van mening dat tromboseprofylaxe voor alle patiënten met onderbeengips niet wordt aanbevolen.
Selectie hoog risico patiënten
Selectie van patiënten met een hoog risico zorgt ervoor dat de NNT omlaag wordt gebracht. Er zijn aanwijzingen dat er onderscheid kan worden gemaakt tussen laag en hoog-risico patiënten. Een recente systematische review (Horner, 2018) omvatte 15 studies en onderzocht risicofactoren voor VTE bij patiënten met een onderbeengips behandeling. Er werd geconcludeerd dat leeftijd en uitgebreider letseltype de enige risicofactoren zijn die meerdere keren zijn gerapporteerd in afzonderlijke studies.
Tevens wordt gesteld dat er gelimiteerd bewijs is om individuele risicofactoren te gebruiken om tromboseprofylaxe beleid op te bepalen. Derhalve kan als alternatief een risicoscore voor trombose worden gebruikt. In 2016 is een review naar risicoscores voor VTE bij onderbeengips patiënten uitgekomen (Watson, 2016). Er werden 5 modellen gevonden waarvan 2 mogelijk geschikt zijn, echter bij gebrek aan een validatie worden deze niet aangeraden voor gebruik in de praktijk.
In 2015 werd de L-TRiP(cast) score gepubliceerd (Nemeth, 2015), een predictie model, welke specifiek is ontwikkeld om het VTE risico te schatten voor patiënten met onderbeengips. In twee validatiestudies (retrospectieve case-control setting) werd een goede onderscheidende waarde gevonden (AUC van 0,76 (95%CI 0,66 tot 0,86)).
Conclusie
Voor patiënten met een laag risico wordt door het lage absolute risico, de hoge NNT, het mogelijk verhoogde risico op bloedingen (en overige complicaties) en de LAGE Grade bewijslast voor effectiviteit op VTE reductie, geen tromboseprofylaxe geadviseerd.
Voor patiënten met een hoger risico op VTE wordt gesteld dat zij baat zouden kunnen hebben bij farmacologische tromboseprofylaxe. Hoog-risico patiënten kunnen momenteel nog niet door een risicoscore worden geïdentificeerd door gebrek aan prospectieve validatie. Wel staat vast dat patiënten met een voorgeschiedenis van VTE en patiënten met een uitgebreid letsel een verhoogd risico hebben voor VTE.
Mocht tromboseprofylaxe worden overwogen, dan wordt geadviseerd om de door de fabrikant geadviseerde en/of in trials geëvalueerde dosering te gebruiken bij het voorschrijven van farmacologische profylaxe.
Onderbouwing
Een behandeling met onderbeengips is geassocieerd met een verhoogd risico op veneuze trombo-embolieën (VTE); ongeveer 2% ontwikkelt een symptomatische VTE (Nemeth, 2019). Het risico op VTE neemt toe naar mate het letsel zich dichter bij de knie bevindt, er sprake is van een uitgebreid letsel, de mate van immobilisatie toeneemt en wanneer patiënten meerdere risicofactoren hebben voor VTE. Het individuele risico van een patiënt is dus sterk afhankelijk van meerdere factoren. Er is tegenstrijdig bewijs over de effectiviteit van tromboseprofylaxe voor deze groep patiënten. In deze richtlijn wordt een advies uitgebracht of tromboseprofylaxe geïndiceerd is, en voor welke patiënten dit geldt. Momenteel is alleen LMWH een goedgekeurde behandeling. DOAC’s zijn daarom bij deze uitgangsvraag buiten beschouwing gelaten.
Deelvraag 1: effectiviteit LMWH
Symptomatische VTE
|
Laag GRADE |
Het is mogelijk dat het gebruik van LMWH het risico op symptomatische VTE reduceert ten opzichte van placebo bij patiënten met onderbeengips immobilisatie voor een geïsoleerd letsel van het onderbeen.
Bronnen: (Zee, 2017; Bruntink, 2017; Jorgensen, 2002; Kock, 1995; Lapidus, 2007b, Lassen, 2002; van Adrichem, 2017) |
Bloedingen
|
Zeer laag GRADE |
Het is mogelijk dat het gebruik van LMWH het risico op complicaties (waaronder bloedingen) verhoogt ten opzichte van placebo bij patiënten met onderbeengips immobilisatie voor een geïsoleerd letsel van het onderbeen.
Bronnen: (Zee, 2017) |
Deelvraag 2: risicofactoren
|
Redelijk GRADE |
Hogere leeftijd en uitgebreide letsels werden als enige consistent gerapporteerd als risicofactor voor VTE. Het is waarschijnlijk dat deze factoren het risico op VTE bij patiënten met immobilisatie van het onderbeen verhogen.
Bronnen: (Horner, 2019) |
|
Laag GRADE |
Voor andere risicofactoren is het onzeker of er een sterke associatie is met symptomatische VTE.
Bronnen: (Horner, 2019) |
Predictiemodellen
|
- GRADE |
Er zijn geen risicomodellen beschikbaar die het VTE risico voor patiënten met gipsimmobilisatie van het (onder)been voorspellen, welke in een prospectieve setting zijn gevalideerd. |
Deelvraag 1: Wat is de effectiviteit van behandeling met tromboseprofylaxe bij patiënten met gipsimmobilisatie van het onderbeen voor een geïsoleerd letsel?
Voor de beantwoording van deze uitgangsvraag is de Cochrane review van Zee (2017) als uitgangspunt gebruikt. Er werden na de zoekdatum (april 2017) geen recentere studies gevonden die aan de selectiecriteria voldeden. Daarom worden de resultaten van de Cochrane review hier beschreven. Doel van deze review was het beoordelen van de effectiviteit van LMWH voor preventie van veneuze trombo-embolieën bij patiënten met gipsimmobilisatie van het onderbeen voor een geïsoleerd traumatisch letsel. Gipsimmobilisatie voor electieve (niet-traumatische) chirurgie wordt in de Cochrane, en in deze richtlijn, buiten beschouwing gelaten evenals gipsimmobilisatie middels een gipskoker of bovenbeengips. Inclusiecriteria van de review zijn: RCT en gecontroleerde klinische trials (CCT), vergelijking van de effectiviteit van LMWH met placebo voor de preventie van VTE in patiënten met onderbeen immobilisatie in de ambulante setting. Er werden acht studies geïncludeerd (Bruntink, 2017; Jorgensen, 2002; Kock, 1995; Kujath, 1993; Lapidus, 2007a; Lapidus, 2007b; Lassen, 2002; Van Adrichem, 2017).
In totaal werden in de acht geïncludeerde studies 3680 (range 105 tot 1519) patiënten geïncludeerd. De patiënten in de trials hadden onderbeen immobilisatie nodig voor de behandeling van geïsoleerde letsels als voet en enkelfracturen en achillespees rupturen. Alle bovenstaande studies includeerden patiënten prospectief en hadden vergelijkbare exclusiecriteria: zwangerschap, allergie voor heparine of contrastvloeistof, ongecontroleerde hypertensie, contra-indicatie voor antistolling en eerdere VTE. Voor alle studies werd een profylactische LMWH dosering gebruikt, meestal voor de complete duur van immobilisatie. In de studie van Lassen werden patiënten die chirurgie ondergingen voor randomisatie maximaal vier dagen behandeld met LMWH. In de studie van Lapidus (2007) werden alle patiënten vóór randomisatie een week behandeld met LMWH.
In de meeste studies was de primaire uitkomstmaat een gecombineerd eindpunt van zowel symptomatische als asymptomatische DVT (gediagnostiseerd met venografie (Jorgensen, 2002; Lapidus, 2007b; Lassen, 2002) of echografie (Bruntink, 2017; Kock, 1995; Kujath, 1993; Lapidus, 2007a). De studie van van Adrichem was de enige waarin alleen symptomatische VTE’s geregistreerd werden als primaire uitkomst (er werd geen routinematige echo verricht). Voor deze richtlijn worden alleen de symptomatische VTE’s, DVT of longembolie (PE) (of combinatie) gerapporteerd.
Symptomatische VTE
Alle geïncludeerde studies behalve Lapidus 2007a rapporteerden symptomatische VTE (Bruntink, 2017; Jorgensen, 2002; Kock, 1995; Lapidus, 2007b, Lassen, 2002; van Adrichem, 2017). Echter, alle studies met uitzondering van de RCT van van Adrichem, registreerden asymptomatische VTE’s waarbij het hebben van een klacht/symptoom tijdens aanvullend onderzoek de diagnose symptomatische VTE opleverde. Deze “symptomatische VTE’s” representeren volgens de werkgroep niet de werkelijke symptomatische VTE’s waarmee patiënten zich presenteren in de klinische praktijk. Ondanks deze tekortkoming worden alle symptomatische VTE’s voor de huidige analyse bij elkaar gevoegd. In totaal werd symptomatische VTE in 12 van 1469 (0,8%) van de patiënten in de LMWH groep gerapporteerd tegenover 31 van 1455 (2,1%) in de controlegroep (RR 0,41 (0,18 tot 0,94, 6 RCT’s, n=2924).
Figuur 2 uitkomstmaat symptomatische VTE
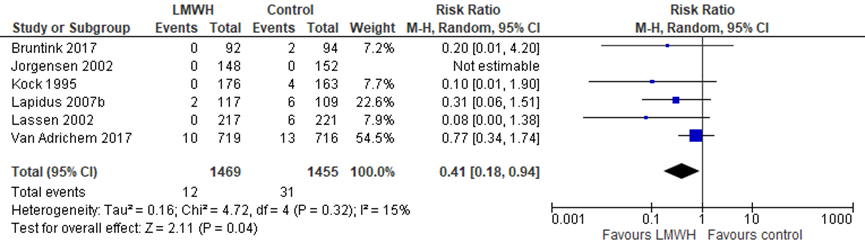
*Voor deze richtlijn zijn de meta-analyses opnieuw uitgevoerd omdat in de Cochrane review een Odds Ratio werd gerapporteerd (met fixed effects model) en in dezen een relatief risico (random effects) de voorkeur heeft
Bloedingen
De uitkomstmaat bloedingen werd in de Cochrane review gevat onder de samengestelde uitkomstmaat “adverse outcomes of treatment”. Voor deze richtlijn is de uitkomstmaat ernstige bloedingen als kritieke uitkomstmaat gedefinieerd, deze data werd daarom separaat uit de Cochrane review gehaald. In de meeste studies werden echter geen gevallen van ernstige bloedingen gerapporteerd (Kock, 1995; Jorgensen, 2002; Kujath, 1993; Lapidus, 2007; van Adrichem, 2017). In de studie van Lassen werden in de LMWH groep 2 en in de placebogroep 1 ernstige bloeding gerapporteerd.
Resultaten voor de samengestelde uitkomstmaat “adverse outcomes of treatment” (gedefinieerd als: bloeding, heparine geïnduceerde trombocytopenie (HIT), allergische reactie en anderen (als beschreven in de studies)) zoals beschreven in de Cochrane review: Lassen (2002) rapporteert dat 14 patiënten in de LMWH groep en 12 in de placebogroep een bloeding hadden (majeur: 2 in de LMWH groep versus 1 in de controlegroep). Ook rapporteert deze studie geen gevallen van heparine geïnduceerde trombocytopenie. Kock (1995) rapporteert vijf patiënten met mineure complicaties (4 kleine lokale hematomen en eenmaal eczeem). Jorgensen rapporteert geen gevallen van HIT, hematoom of ernstige bloeding. Kujath (1993) rapporteert dat er geen gevallen van bijwerkingen werden gezien. Lapidus (2007) rapporteert geen ernstige bloedingen. Van Adrichem (2017) rapporteert geen ernstige bloeding en één klinisch relevante niet-ernstige bloeding in de LMWH groep, tevens ontwikkelen 55 patiënten een mineure bloeding in de LMWH groep in vergelijking met 49 patiënten in de controle groep. Bruntink (2017) rapporteert alleen niet ernstige complicaties: 22 in de LMWH groep met mineure bloedingen zoals hematurie of donkere ontlasting en geen patiënt rapporteerde dergelijke klachten in de controlegroep. Een analyse van gecombineerde bijwerkingen laat een RR van 1,85 zien (95%-CI 0,82 tot 4,20, I² = 55%, 3178 patiënten; 8 studies) (figuur 3).
Figuur 3 Uitkomstmaat adverse outcomes of treatment
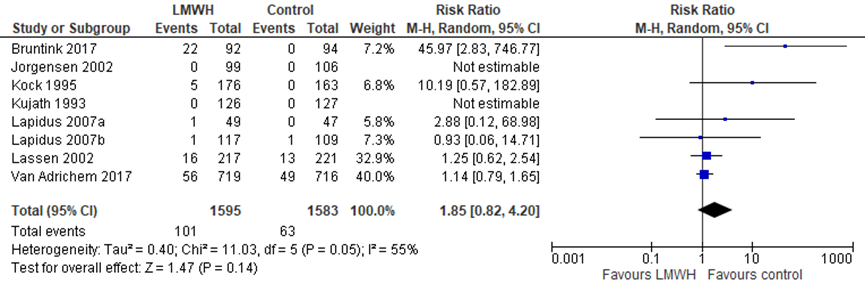
(bron: Zee, 2017)
Bewijskracht van de literatuur
De gradering (GRADE) is overgenomen uit de Cochrane review van Zee (2017). De bewijskracht voor de uitkomstmaat symptomatische VTE is met twee niveaus verlaagd gezien het risico op bias voor 3 van de studies en imprecisie van de gepoolde resultaten.
De bewijskracht voor de uitkomstmaat adverse events is met drie niveaus verlaagd naar zeer laag gezien het risico op bias in 4 van de 8 studies en ernstige imprecisie (klein aantal events) van de gepoolde resultaten.
Deelvraag 2: Wat zijn risicofactoren voor het optreden van een trombose bij patiënten met gipsimmobilisatie van het onderbeen?
De systematische review van Horner (2019) is als uitgangspunt genomen voor het beantwoorden van deze deelvraag (Horner, 2019). Deze systematische review had als doel om individuele risicofactoren van patiënten te identificeren die samenhangen met het optreden van een vorm van VTE na gipsimmobilisatie van het been door een trauma. De search werd gedaan in mei 2017. Inclusiecriteria: alle studies die VTE rapporteren in volwassenen die tijdelijk immobilisatie (gips of brace in poliklinische setting) voor geïsoleerd letsel van het been hebben en waarbij risicofactoren werden gerapporteerd. Onder VTE wordt elke geregistreerde diagnose van asymptomatische of symptomatische DVT, PE of overlijden hierdoor beschouwd. Individuele risicofactoren die door regressie, OR analyse of parametrische testen significant gerelateerd waren aan het optreden van VTE werden geëxtraheerd. Daarnaast werd in elke studie gekeken of een van de risicofactoren die momenteel gebruikt worden in risicostratificatie tools, gerapporteerd werden.
In de bewijs tabel worden de belangrijkste karakteristieken van de geïncludeerde studies weergegeven (zie de evidencetabel voor details).
De auteurs van de review geven aan dat het niet mogelijk was meta-analyse uit te voeren door heterogeniteit tussen de studies, verschillende wijze van rapporteren en het hoge risico op bias. Er werden verschillende risicomaten beschreven uit verschillende studies om risicofactoren te rapporteren.
In totaal werden 15 studies met 80.678 patiënten geïncludeerd. Alle geïncludeerde studies hadden een matig tot hoog risico op bias (beoordeeld met ROBINS-I risk of bias tool).
De studies werden gepubliceerd tussen 1993 en 2017. Vijf waren RCT’s met conservatieve arm, drie waren prospectieve observationele cohort of cross-sectionele studies, een was een case-control studie (39) en zes waren retrospectieve cohortstudies. De mediane prevalentie van alle VTE was 4,8% (range 0,22% tot 23,4%) en de gemiddelde leeftijd lag tussen de 33,8 tot 52,6 jaar. De gemiddelde prevalentie van symptomatische VTE (in studies met interpretabele data, n=77.261) was 2,9%.
De methodologische kwaliteit van de 15 geïncludeerde studies werd beoordeeld met de ROBINS-I framework. Alle studies hadden een matig (7 studies) of hoog (acht studies) risico op bias. In de meeste studies met een hoog risico op bias werd dit met name veroorzaakt door de selectie van participanten in studie: hoog-risico patiënten voor VTE kregen vaak al tromboseprofylaxe of worden op een andere manier behandeld. Dit reduceert het gerapporteerde risico in de populatie.
Leeftijd
Leeftijd als risicofactor werd in twaalf studies beschreven. Elf studies rapporteren een associatie tussen hogere leeftijd en het optreden van VTE (Odds ratios varieerden van 1,05 tot 3,45) en een studie vond geen associatie tussen VTE en hogere leeftijd.
Van de zeven studies die alleen symptomatische VTE als uitkomst namen en leeftijd als risicofactor analyseerden vonden zes studies een positieve associatie en één studie geen associatie.
Type letsel
Type letsel werd in zes studies met multivariate logistische regressie gerelateerd aan een verhoogd risico op VTE waarbij ernstige letsels en fracturen een hoger risico lijken te geven dan weke delen letsels. Eén studie rapporteerde een verhoogt risico op VTE na een achillespeesruptuur in vergelijking met andere type letsels. Verder onderscheidt voor type letsel in relatie tot VTE risico werd niet beschreven.
BMI
Tien studies rapporteerden over BMI als risicofactor voor VTE. Body Mass Index (BMI) werd in vier studies gerapporteerd als individuele risicofactor met Odds Ratio’s van 1,2 tot 17,2. In zes studies werd echter geen associatie gevonden.
Geslacht
Zes studies rapporteerden geen associatie tussen geslacht en VTE.
Gebruik van oestrogeen
Vijf studies rapporteerden geen associatie tussen het gebruik van oestrogeen en VTE en twee studies rapporteren een positieve associatie.
Roken
Zes studies rapporteerden geen associatie tussen roken en VTE.
Overige risicofactoren
Actieve maligniteit: éen studie vond een positieve relatie en éen studie vond geen relatie.
Zwangerschap: in geen van de studies wordt de relatie tussen zwangerschap en VTE onderzocht/beschreven.
Recente ziekenhuisopname: in geen van de studies wordt recente ziekenhuisopname onderzocht/beschreven.
Voorafgaande immobiliteit: in geen van de studies wordt voorafgaande immobiliteit onderzocht/beschreven.
Spataders: twee studies vinden geen relatie en éen studie vindt een positieve relatie.
Familiegeschiedenis VTE: drie studies vinden geen relatie en twee studies vinden een positieve relatie.
Trombofilie: éen studie vindt een positieve associatie en éen studie vindt een negatieve associatie.
Belastbaarheid in gips: twee studies vinden een positieve associatie en éen studie vindt geen associatie.
Voorgeschiedenis van VTE: In de review van Horner (2019) wordt het hebben van een voorgeschiedenis van VTE niet genoemd als risicofactor doordat deze patiënten uit bijna alle studies zijn geëxcludeerd (omdat deze patiënten een hoog risico hebben (Nemeth, 2018).
Predictiemodellen
Er werden twee studies gevonden voor deze deelvraag (Watson, 2016; Nemeth, 2015). In deze twee publicaties worden 6 mogelijke risicomodellen beschreven: vijf in de review van Watson en éen in de studie van Nemeth (2015). Geen van deze studies voldoen echter aan het inclusiecriterium: prospectieve validatie van risicomodel. Bij deze uitgangsvraag zijn daarom geen evidencetabellen opgesteld. De resultaten van de retrospectieve validaties worden volledigheidshalve wel beschreven.
In de review van Watson (2016) (zoekdatum niet gerapporteerd) werden alleen modellen die toepasbaar waren voor patiënten met onderbeen gips geïncludeerd. Van de 34 gevonden risicomodellen waren er vijf toepasbaar op patiënten met onderbeengips. Twee modellen waren specifiek voor patiënten met onderbeengips (Roberts, 2013; Plymouth) en drie waren toepasbaar op alle in het ziekenhuis opgenomen patiënten (Department of Health, Nygaard, 2010; Caprini, 2001). De auteurs geven aan dat geen van deze risicomodellen klinisch gevalideerd zijn binnen patiënten met onderbeengips.
In de studie van Watson (2016) worden de vijf risicomodellen gebruikt om een retrospectieve validatie uit te voeren binnen 721 patiënten met onderbeengips. 21/721 patiënten (2,9%) ontwikkelde symptomatische VTE gerapporteerd (groep 1). Deze cases werden gekoppeld aan 21 van patiënten zonder VTE (controles).
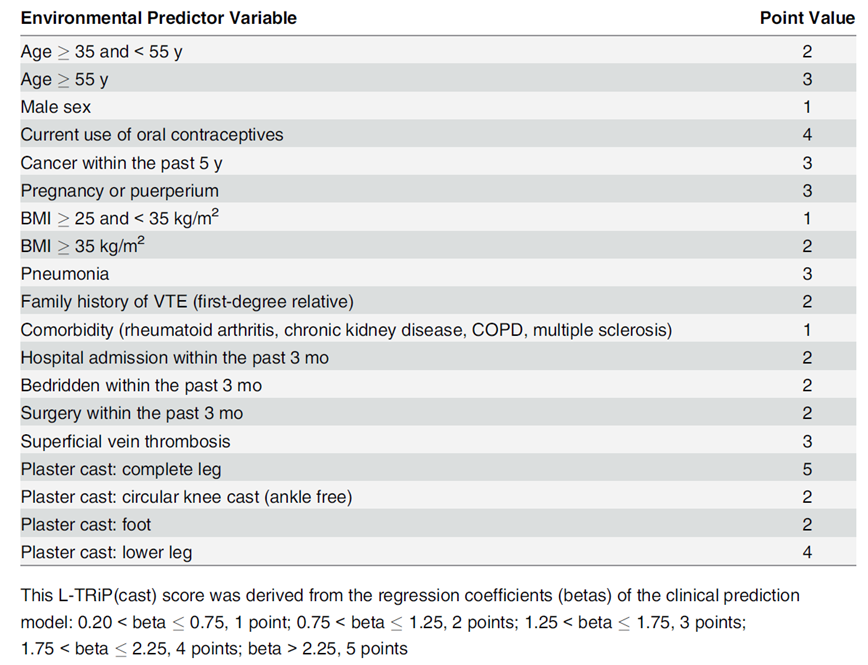
In de studie van Nemeth (2015) wordt een klinisch predictiemodel voor VTE risico, specifiek voor patiënten met onderbeengips ontwikkeld: de L-TRiP(cast) Score (zie figuur 4). Deze score werd opgesteld op basis van gegevens uit een grote population-based case-control studie (MEGA studie, 4,446 cases met VTE en 6,118 controles zonder VTE). Predictie scores werden vervolgens berekend in 230 patiënten met gips immobilisatie (194 cases, 36 controles). De L-TRiP(cast) Score werd met data uit twee andere retrospectieve population based case-controle studies gevalideerd: de THE-VTE studie en de Milan studie.
Figuur 4 L-TRiP(cast) score (bron: Nemeth, 2015)
Resultaten
In de studie van Watson (2016) worden drie risicomodellen (niet specifiek ontwikkeld voor patiënten met onderbeengips) besproken met een sensitiviteit van 100%, maar specificiteit van 0%. De Plymouth had een sensitiviteit van 57,1% en specificiteit van 52,4% (accuraatheid 54,8%). Roberts (2013) had een sensitiviteit van 85,7% en specificiteit van 4,76% (accuraatheid 45,2%).
In de MEGA studie had de L-TRiP(cast) score een Area Under the Curve (AUC) van 0,76 (95% CI 0,66–0,86). Bij de Milan en THE-VTE studie waren de AUC’s 0,95 (95% CI 0,91–0,99) en 0,77 (95% CI 0,58–0,96) respectievelijk. Bij een afkappunt van 10 (59,6% van de patiënten) om patiënten in hoog versus laag risicogroep te stratificeren was de sensitiviteit 65,1% en de specificiteit 72,2%. Tabel 1 toont predicatieve statistieken voor de verschillende risicomodellen.
Tabel 1 diagnostische performance voor de vijf modellen beschreven in Watson, 2015 aangevuld met de resultaten van Nemeth, 2015
|
Risicomodel |
Accuraatheid |
Sensitiviteit |
Specificiteit |
Vals positieven |
Vals negatieven |
Positief voorspellende waarde |
Negatief voorspellende waarde |
AUC (95%-CI) |
|
Plymouth |
54,8 |
57,1 |
52,4 |
45,5 |
45 |
54,5 |
55 |
|
|
Dep. of health |
50 |
100 |
0 |
50 |
n/a |
50 |
n/a |
|
|
Nygaard |
50 |
100 |
0 |
50 |
n/a |
50 |
n/a |
|
|
Caprini |
50 |
100 |
0 |
50 |
n/a |
50 |
n/a |
|
|
Roberts |
45,2 |
85,7 |
4,76 |
52,6 |
75 |
47,4 |
25 |
|
|
L-TRiP(cast) score1 |
|
|
|
|
|
|
|
0,76 (0,66-0,86) |
|
L-TRiP(cast) score2 |
|
|
|
|
|
|
|
0,95 (0,91-0,99) |
|
L-TRiP(cast) score3 |
|
|
|
|
|
|
|
0,77 (0,58–0,96) |
|
L-TRiP(cast)score (overall)* |
65,1% |
72,2% |
|
|
5,7% |
98,8% |
|
|
Bron: Watson (2016) aangevuld met Nemeth (2015). *cut-off waarde van 10 en bij assumptie van 2,5% incidentie. 1) MEGA-study 2)THE-VTE study 3) Milan study
Bewijskracht van de literatuur
Er werden geen studies gevonden die aan de inclusiecriteria voor de systematische literatuuranalyse voldeden (waarin een risicomodel prospectief werd gevalideerd). De bij de samenvatting van de literatuur beschreven studies voldeden niet aan de inclusiecriteria maar worden volledigheidshalve wel beschreven.
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag (vragen):
P: patiënten met gipsimmobilisatie van het onderbeen;
Deelvraag 1: Wat is de effectiviteit van behandeling met tromboseprofylaxe bij patiënten met gipsimmobilisatie van het onderbeen voor een geïsoleerd letsel?
I: tromboseprofylaxe middels een laag-moleculair-gewicht-heparine (LMWH);
C: geen tromboseprofylaxe (placebo);
O: symptomatische VTE, ernstige bloedingen.
Deelvraag 2: Wat zijn risicofactoren voor het optreden van een trombose bij patiënten met gipsimmobilisatie van het onderbeen?
I: risicofactoren;
O: optreden VTE.
Deelvraag 3: Welke predictiemodellen kunnen gebruikt worden voor het voorspellen van trombose bij patiënten met gipsimmobilisatie van het onderbeen?
I: predictiemodel voor optreden VTE;
O: Predictieve statistische maten zoals (maar niet beperkt tot): sensitiviteit, specificiteit, positief voorspellende waarde en negatief voorspellende waarde.
Relevante uitkomstmaten
De werkgroep achtte symptomatische veneuze trombo-embolieën en ernstige bloedingen voor de besluitvorming cruciale uitkomstmaten. Asymptomatische VTE acht de werkgroep niet relevant gezien hier niet actief naar wordt gescreend in de klinische praktijk. Tevens is uit eerder onderzoek is gebleken dat de effectiviteit van tromboseprofylaxe voor asymptomatische trombose en symptomatische trombose niet goed overeenkomt. Studies die de effectiviteit op asymptomatische trombose onderzoeken zijn derhalve nauwelijks relevant.
De werkgroep definieerde niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
Zoeken en selecteren (Methode)
In de databases (Medline (via OVID), Embase (via Embase.com) is 11 januari 2019 met relevante zoektermen gezocht naar studies gepubliceerd na 2000 naar tromboseprofylaxe bij patiënten met gipsimmobilisatie van het onderbeen, gepubliceerd in het Engels. Aangezien deze vraag drie deelvragen omvat is breed gezocht en in de selectie per deelvraag geselecteerd op verdere selectiecriteria. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 157 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria:
- Deelvraag 1: systematische review (met RCT’s) of RCT waarbij tromboseprofylaxe met LMWH bij patiënten met gipsimmobilisatie werd vergeleken met geen tromboseprofylaxe of placebo en waarbij een van de relevante uitkomstmaten wordt gerapporteerd.
- Deelvraag 2: systematische review van Horner (2019) is als uitgangspunt genomen. Aanvullende studies zijn niet toegevoegd aan de systematische literatuuranalyse, deze studies worden wel kort beschreven in de overwegingen en worden genoemd in de exclusietabel.
- Deelvraag 3: systematische review of prospectief onderzoek waarbij een predictiemodel voor VTE bij patiënten met gipsimmobilisatie van het onderbeen wordt beschreven en waarbij een van de relevante uitkomstmaten wordt gerapporteerd.
Op basis van titel en abstract werden in eerste instantie:
- Deelvraag 1: 16 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 15 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording) en een systematische review definitief geselecteerd.
- Deelvraag 2: 8 studies voorgeselecteerd. Na raadpleging van de volledige tekst werd vervolgens 7 studie geëxcludeerd (zie exclusietabel) en1 studies geselecteerd.
- Deelvraag 3: 3 studies voorgeselecteerd. Na raadpleging van de volledige tekst werd 1 studies geëxcludeerd (zie exclusietabel) en een review en een primaire studie geselecteerd.
Resultaten
De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de bewijstabellen.
De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk-of-biastabellen.
- van Adrichem RA, Nemeth B, Algra A, le Cessie S, Rosendaal FR, Schipper IB, Nelissen RGHH, Cannegieter SC; POT-KAST and POT-CAST Group. Thromboprophylaxis after Knee Arthroscopy and Lower-Leg Casting. N Engl J Med. 2017 Feb 9;376(6):515-525. doi: 10.1056/NEJMoa1613303. Epub 2016 Dec 3. PubMed PMID: 27959702.
- Bruntink MM, Groutars YM, Schipper IB, Breederveld RS, Tuinebreijer WE, Derksen RJ, PROTECT Study Group. Nadroparin or fondaparinux versus no thromboprophylaxis in patients immobilised in a below-knee plaster cast (PROTECT): a randomised controlled trial. Injury 2017; 376:936–40. PUBMED: 28279428).
- Caprini Ja, Arcelus JI, Reyna JJ. Effective risk stratification of surgical and nonsurgical patients for venous thromboembolic disease. Semin Hematol 2001;38:12–9 Health D of. Venous thromboembolism (VTE) risk assessment. Dep Heal Publ.
- Horner D, Pandor A, Goodacre S, Clowes M, Hunt BJ. Individual risk factors predictive of venous thromboembolism in patients with temporary lower limb immobilization due to injury: a systematic review. J Thromb Haemost. 2019 Feb;17(2):329-344. doi: 10.1111/jth.14367. Epub 2019 Feb 7. PubMed PMID: 30580466.
- Jorgensen PS,Warming T, Hansen K, Paltved C, Berg HV, Jensen R, et al. Low molecular weight heparin (Innohep) as thromboprophylaxis in outpatients with a plaster cast; a venography controlled study. Thrombosis Research 2002; 105(6):477–80.
- Kock HJ, Schmit-Neuerburg KP, Hanke J, Rudofsky G, Hirche H. Thromboprophylaxis with low-molecular-weight heparin in outpatients with plaster-cast immobilisation of the leg. Lancet 1995 Aug 19;346(8973):459–61.
- Kujath 1993 {published data only} Habscheid W, Spannagel U, Kujath P, Schindler G. Prevention of thrombosis with low molecular weight heparin in ambulatory patients with injury of the lower extremity: an ultrasound study. Vasa Supplementum 1991; 33:222–3.
- Lapidus(a) L, Rosfors S, Ponzer S, Levander C, Elvin A, Elvin G, et al. Prolonged thromboprophylaxis with dalteparin after surgical treatment of Achilles tendon rupture – a randomized, placebo-controlled study. Journal of Bone and Joint Surgery - British Volume 2009;91-B(Suppl 1):165.
- Lapidus(b) LJ, Ponzer S, Elvin A, Levander C, Laerfars G, Rosfors S, et al. Prolonged thromboprophylaxis with Dalteparin during immobilization after ankle fracture surgery: a randomized, placebo-controlled, double-blind study. Acta Orthopaedica 2007;78(4):528–35.
- Lassen MR, Borris LC, Nakov RL. Use of the low-molecular-weight heparin reviparin to prevent deep-vein thrombosis after leg injury requiring immobilization. N Engl J Med. 2002 Sep 5;347(10):726-30.
- Nemeth B, van Adrichem RA, van Hylckama Vlieg A, Bucciarelli P, Martinelli I, Baglin T, Rosendaal FR, le Cessie S, Cannegieter SC. Venous Thrombosis Risk after Cast Immobilization of the Lower Extremity: Derivation and Validation of a Clinical Prediction Score, L-TRiP(cast), in Three Population-Based Case-Control Studies. PLoS Med. 2015 Nov 10;12(11):e1001899; discussion e1001899. doi: 10.1371/journal.pmed.1001899. eCollection 2015 Nov. PubMed PMID: 26554832; PubMed Central PMCID: PMC4640574.
- Nemeth B, Cannegieter SC. Venous thrombosis following lower-leg cast immobilization and knee arthroscopy: From a population-based approach to individualized therapy. Thromb Res. 2019 Feb;174:62-75. doi: 10.1016/j.thromres.2018.11.030. Epub 2018 Dec 10.
- Nemeth B, Timp JF, van Hylckama Vlieg A, Rosendaal FR, Cannegieter SC. High risk of recurrent venous thrombosis in patients with lower-leg cast immobilization. J Thromb Haemost. 2018 Nov;16(11):2218-2222.
- Nokes TJC, Keenan J. Venous thromboembolism risk assessment V2. Plymouth (Derriford Hospital). VTE Prev Engl 2010. http://www.vteprevention-nhsengland. org.uk/k2inv/item/222-plymouth-derriford-hospital (accessed 08.07.15).
- Nygaard A, Nelson AS, Pick A, Danekas PL, Massoomi F, Thielen J, et al. Interrater reliability in the evaluation of a thrombosis risk assessment tool. Hosp Pharm 2010;44:1089–94, doi:http://dx.doi.org/10.1310/hpj4412-1089
- Policy and Guidance n.d. http://webarchive.nationalarchives.gov.uk/20130107105354/ http:/www.dh.gov.uk/en/Publicationsandstatistics/Publications/Publications- PolicyAndGuidance/DH_088215 (accessed 08.07.15).
- Roberts C, Horner D, Coleman G, Maitland L, Curl-Roper T, Smith R, et al. Guidelines in Emergency Medicine Network (GEMNet): guideline for the use of thromboprophylaxis in ambulatory trauma patients requiring temporary limb immobilisation. Emerg Med J 2013;30:968–82.
- Testroote M, Stigter WA, Janssen L, Janzing HM. Low molecular weight heparin for prevention of venous thromboembolism in patients with lower-leg immobilization. Cochrane Database Syst Rev. 2014 Apr 25;(4):CD006681. doi: 10.1002/14651858.CD006681.pub3. Review.
- Watson U, Hickey BA, Jones HM, Perera A. A critical evaluation of venous thromboembolism risk assessment models used in patients with lower limb cast immobilisation. 2016; Foot and Ankle Surgery. 22(3):191-5.
- Zee AA, van Lieshout K, van der Heide M, Janssen L, Janzing HM. Low molecular weight heparin for prevention of venous thromboembolism in patients with lower-limb immobilization. Cochrane Database Syst Rev. 2017 Aug 6;8:CD006681. doi: 10.1002/14651858.CD006681.pub4. Review. PubMed PMID: 28780771.
Deelvraag 1
Research question: UV5 part 1: efficacy LMWH in patients with cast-immobilization
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C) |
Follow-up |
Outcome measures and effect size |
Comments |
|
Zee, 2017
individual study characteristics deduced from Zee, 2018
|
SR and meta-analysis of RCT’s
Literature search up to April 2017
A: Bruntink 2017 B: Jorgensen 2002 C: Kock 1995 D: Kujath 1993 E: Lapidus 2007a F: Lapidus 2007b; G: Lassen 2002 H: Van Adrichem 2017
Study design: All: RCT
Setting and Country: A: Netherlands B: Denmark C: Germany D: Germany E: Sweden F: Sweden G: Denmark H: Netherlands
Source of funding and conflicts of interest: Not stated |
Inclusion criteria SR: RCT, CCT, thromboprophylaxis with LMWH in adults with lower limb immobilization in ambulatory setting. Comparison versus. placebo/no profylaxis
Exclusion criteria SR: comparison oral anticoagulants, UFH or aspirin
8 studies included
Important patient characteristics at baseline: N, (I; C) (randomized) A: 310 (treatment group 154; control group 156) B: 300 (treatment group 148; control group 152) C: 428; D:306, E: 105; treatment group 52; control group 53 F: 272; treatment group 136; control group 136 G: 440; treatment group 217; control group 223 H: 1519; treatment 761; control group 758
Age (mean) A: 47.7 (16.4); control group 44.5 (17.2) B: adult patients > 18 years (range 18 to 93) C: treatment group 34.1 years (18 to 63); control group 33.5 years (18 to 64) D: treatment group 32.9 years (16 to 70); control group 35.6 years (16 to 76) F: treatment group 49 years (sd14); control group 48 years (sd14) G: treatment group 47 years (37 to 55); control group 47 years (37 to 56) H: treatment group 46.5 (16.5); control group 45.6 (16.4)
Groups comparable at baseline? Yes |
Describe intervention:
A: Nadroparin 2850 IE anti-Xa = 0.3 mL, given once daily B: LMWH 3500 IU anti-Xa of tinzaparin (Innohep) once daily C: LMWH 32 mg (certoparin; Mono-Embolex NM) once daily D: LMWH36mg heparin fraction calcium(nadroparin; Fraxiparin) once Daily E: LMWH dalteparin 5000 units sc once daily until removal of the plaster Cast F: LMWH dalteparin 5000 units sc once daily until removal of the plaster Cast G: LMWH once daily SC injection of 2850 IU nadroparin or 2500 IU dalteparin for participants ≤ 100 kg, or a double dose for participants weighing > 100 kg (LMWH (nadroparin or dalteparin) chosen according to preference at the hospital) |
Describe control:
A: no prophylaxis B: no prophylaxis C: no prophylaxis D: no prophylaxis E: placebo F: placebo G: placebo H: no prophylaxis
|
End-point of follow-up: Not stated
For how many participants were no complete outcome data available? A: 124 (62 treatment group, 62 control group). B: 95; treatment group 49; control group 46. C: 5 refused to take part, 32 excluded due to exclusion criteria, data not evaluated from 52: treatment group 21; control group 31 D: 53 excluded post randomization (12 in treatment group interrupted prophylaxis without permission, 14 control group patients received prophylaxis, 18 lost to follow-up, 6 participants operated on before 7th day, and 3 participants had cast removed before 7th day E: 4 (withdrawal of consent treatment group 2, control group 2) and excluded from efficacy analysis F: 75 considered non-evaluable for primary analysis (35 treatment group and 40 in control group), due to: withdrawal of consent (38), technical failure of phlebography (27), refracture or resurgery (4), failure of protocol compliance (3), minor bleeding (1), inconclusive phlebography (1), never received allocated treatment due to DVT before start of treatment (1). Exclusions were evenly divided over the two groups G: 69 excluded from efficacy analysis: 2 received no injections (control group), 2 withdrew consent (treatment group), 4 withdrew because of adverse events (1 treatment, 3 control group), 61 did not have venograms that could be evaluated (31 treatment, 30 control group) H: after randomization, 33 excluded as either failed inclusion or met exclusion criteria, 23 withdrew consent, and 28 lost to follow-up
|
Symptomatic VTE Effect measure: I versus. C A: 0/92 versus. 2/94 B: 0/148 versus. 0/152 C: 0/176 versus. 4/163 F: 2/117 versus. 6/109 G: 0/217 versus. 6/221 H: 10/719 versus. 13/716
Pooled effect (fixed effects model): OR 0.40 (0.21 to 0.76) favoring Heterogeneity (I2): GRADE: low Downgraded by two levels as 3 out of 6 studies showed considerable risk of bias, and imprecision of pooled results
Major bleeding Not reported (data extracted from text): B: 0/99 versus 0/106 C: 0/176 versus. 0/163 D: 0/126 versus. 0/127 E: 0/49 versus. 0/47 F 0/117 versus. 0/109 G: : 2/217 versus. 1/221 H: 0/719 versus. 0/716
Adverse outcomes of treatment Defined as bleeding, heparin induced thrombocytopenia (HIT), allergic reaction, others (definitions of adverse outcomes as reported by study authors): A: 22/92 versus. 0/94 B: 0/99 versus. 0/106 C: 5/176 versus. 0/163 D: 0/126 versus. 0/127 E: 1/49 versus. 0/47 F: 1/117 versus. 13/221 G: 16/217 versus. 13/221 H: 56/719 versus. 49/716
|
|
Table of quality assessment for systematic reviews of RCT’s and observational studies: Deelvraag 1
Based on AMSTAR checklist (Shea, 2007; BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher, 2009; PLoS Med 6: e1000097; doi:10.1371/journal.pmed1000097
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Zee, 2017 |
Yes |
Yes |
Yes |
Yes |
Yes |
Yes |
Yes |
Yes |
Yes |
- Research question (PICO) and inclusion criteria should be appropriate and predefined.
- Search period and strategy should be described; at least Medline searched; for pharmacological questions at least Medline + EMBASE searched.
- Potentially relevant studies that are excluded at final selection (after reading the full text) should be referenced with reasons.
- Characteristics of individual studies relevant to research question (PICO), including potential confounders, should be reported.
- Results should be adequately controlled for potential confounders by multivariate analysis (not applicable for RCT’s).
- Quality of individual studies should be assessed using a quality scoring tool or checklist (Jadad score, Newcastle-Ottawa scale, risk of bias table et cetera).
- Clinical and statistical heterogeneity should be assessed; clinical: enough similarities in patient characteristics, intervention and definition of outcome measure to allow pooling? For pooled data: assessment of statistical heterogeneity using appropriate statistical tests (for exampl Chi-square, I2)?
- An assessment of publication bias should include a combination of graphical aids (for example funnel plot, other available tests) and/or statistical tests (for example Egger regression test, Hedges-Olken). Note: If no test values or funnel plot included, score “no”. Score “yes” if mentions that publication bias could not be assessed because there were fewer than 10 included studies.
- Sources of support (including commercial co-authorship) should be reported in both the systematic review and the included studies. Note: To get a “yes,” source of funding or support must be indicated for the systematic review AND for each of the included studies.
Deelvraag 2
Author, year |
Design, setting |
Inclusion criteria |
Patients, sex, age |
Incidence VTE |
Profylaxis |
Duration follow-up |
Risk factor ascentainment |
Outcome ascentainment |
Statistical analysis |
Overall risk of bias |
|
Gehling, 1998; Germany |
Design:Prospective open-label RCT |
Age >16 years with lower limb injury requiring immobilisation with plaster or bandages (and at least one risk factor for VTE) |
N=287 50.5% male Mean age: 36.3a |
LMWH group: 6.3% Aspirin group: 4.8% |
NR |
NR |
Physician assessment (prospective) |
Clinical assessment, screening sonography and confirmation n phlebography |
NR (appears descriptive |
Moderate |
|
Goel et al., 2009; Canada |
Design:Prospectivedouble-blind RCT |
Adults 18 to 75 years with unilateral displaced fractures below the knee requiring operative intervention |
N=238 62% male Mean age: 40.5a |
LMWH group: 8.7% Control group:12.6% |
No prophylaxis prior to randomisatio n |
Minimum of 3 months following surgery or until the fracture had united. |
Physician assessment (prospective) |
Clinical assessment and bilateral lower leg venography for all patients |
Univariate and multivariate logistic regression |
Moderate |
|
Kock, 1995 |
Design:Prospective open- label RCT |
Adults 18 to 65 years undergoing conservative treatment for below knee injury with cylinder or below knee cast |
N=339 61% male Mean age: 33.8a |
LMWH group: 0% Control group: 4.3% |
No prophylaxis rior to randomisation |
NR (however, duration of casting: LMWH group, 15.2 days; Control group, 18.8 days) |
Physician assessment (prospective) |
Clinical assessment, screening sonography and confirmation n phlebography |
NR (appears descriptive) |
Moderate |
|
Kujath, 1993 Germany |
Design: Prospective open-label RCT Setting: Outpatient |
Age >16 years undergoing conservative treatment for lower limb injury with below knee plaster applied >7days |
N=253 58% male Mean age: 34.3a |
LMWH group: 4.8% Control roup: 16.5% |
No prophylaxis prior to randomisatio n |
NR (however, duration of casting: LMWH group, 15.6 days; Control group, 15.8 days) |
Physician assessment (prospective) |
Compression ultrasound by 2 examiners and confirmation phlebography |
NR (appears descriptive) |
Moderate |
|
Zheng, 2017 China |
Design: Prospective double-blind RCT Setting: Outpatient |
Adults >18 years with any fracture of the lower limb requiring operative treatment |
N=814 62.3% male Mean age: 47.8 |
LMWH group: 1.5% Control group: 3.2% |
No prophylaxis prior to randomisation |
3 months |
Physician assessment (prospective |
Blinded bilateral Doppler compression ultrasound |
Logisticregression |
Moderate |
|
Riou, 2007 France |
Design: Prospective cohort study Setting: Outpatient |
Age >18 years with isolated lower limb injury (below the knee) managed conservatively (immobilisation duration >7 days) |
N=2761 51% male Mean age: 40 |
6.4% |
Antithrombotic prophylaxis was given to 61% patients |
3 months |
Physician assessment (prospective) |
Adjudication committee |
Logistic regression with propensity score analysis |
Moderate |
|
Hanslow, 2006 Australia |
Design: Retrospective cohort study Setting: Outpatient |
Patients who had an operative intervention to the foot or ankle |
N=602 52% male Mean age: 42.9 |
5.3% |
Antithrombot ic prophylaxis was given to 31% patients |
4.4 months |
Collected from clinical records (retrospective ) |
Case note search, including hospital reattendance and diagnostic imaging |
Logistic regression |
Serious |
|
Jameson, 2014 UK |
Design: Retrospective cohort study Setting: Outpatient |
Patients with isolated unilateral closed ankle fracture managed conservatively |
N=14,777 47% male Mean age: 46.4 |
0.22% (PE only) |
No data recorded |
3 months |
NR; assumed collected from clinical records (retrospective ) |
Inpatient mortality or coded diagnosis of pulmonary embolism within 90 days of injury |
Logistic regression |
Serious |
|
Makhdom, 2013 Canada |
Design: Retrospective cohort study Setting: Outpatient until surgery, short day-case stay thereafter |
All patients undergoing Achilles tendon repair |
N=115 86.1% male Mean age 41 |
23.5% |
No peri- or Postoperative profylaxis |
3 months |
Collected from Electronic medical record system (retrospective) |
Case note search, including hospital reattendance and diagnostic imaging |
Non-parametric testing using fishers exact |
Serious |
|
Meek and Tong, 2012 Australia |
Design: Retrospective cohort study Setting:Outpatient |
Age >18 years with acute lower limb injury requiring temporary immobilisation (ED discharge within 24 hours of presentation) |
N=1231 56.3% male Mean age: 37 |
2.9% |
No prophylaxis (excluded if received at any dose) |
NR |
Electronic notes screened for eligibility by one investigator (retrospective ) |
Case note search,including hospital reattendance and diagnostic imaging |
Logistic regression |
Serious |
|
Patel, 2012 USA |
Design:Retrospective cohort study Setting: Mostly outpatient, some with short inpatient stays (<3 days) |
All patients who had Achilles tendon rupture |
N=1172 NR Mean age: 45 |
0.77% |
Nil routine, assumed to be none provided |
3 months |
Collected from electronic medical record system (retrospective ) |
Case note search, including hospital reattendance and diagnostic imaging |
Logistic regression |
Moderate |
|
Wahlsten, 2015 Denmark |
Design: Retrospective cohort study Setting: Inpatient or outpatient |
Age >18 years undergoing an operative procedure for a fracture of the foot, ankle, tibia or patella |
N=57,619 51.4% male Mean age: 52.6a |
1.0% |
Routine perioperative prophylaxis with nil postoperative |
180 days |
Collected from 5 different cross linked registries (retrospective ) |
Case note search, including hospital reattendance and diagnostic imaging |
Multivariate cox regression |
Moderate |
|
Van Adrichem, 2014 The Netherlands |
Design: Case-control study Setting:Mostly outpatient, some with short inpatient stays (<3 days) |
Age 18 to 70 years with a first VTE identified at an anticoagulation clinic (cases) Control group identified by random dialling method (matched for sex and age) |
N= 10,567b Sex: NR Mean age: NR |
NR |
No data recorded |
3 months |
Participant completed questionnaire (prospective collection) |
Case note search, including hospital reattendance and diagnostic imaging |
Logistic regression |
Serious |
|
Ho and Omari, 2017 Australia |
Design: Cross-sectional study Setting: Outpatient |
Age >18 years with fracture to foot/ ankle with conservative management |
N=72 45.8% male Mean age: NR (median: 38) |
11% |
Nil routine, assumed to be none provided |
6 months |
Questionnaire (unclear if physician or patient completed) |
Prospective Compression ultrasound |
Parametric and non-parametric testing with bootstrapping |
Serious |
|
Manafi Rasi, 2012 Iran |
Design: Cross-sectional study Setting: Outpatient |
Age >15 years with stable foot/ ankle fracture or grade 3 sprain (non-surgical Treatment) |
N=95 77.9% male Mean age: 38 |
3% |
NR |
7 to 14 days |
NR |
Compression ultrasound by 2 independent examiners |
NR (appears descriptive) |
Serious |
A data calculated based on mean of means
b Sample included 4418 cases and 6149 controls (of these only 227 cases and 76 controls had lower extremity injuries)
Deelvraag 3
Geen studies geïncludeerd voor systematische literatuuranalyse en derhalve geen evidence tabellen beschikbaar.
Exclusietabel
|
Artikel |
Reden van exclusie |
|
Deelvraag 1: effectiviteit tromboseprofylaxe met LMWH bij gipsimmobilisatie van het onderbeen. |
|
|
Does thromboprophylaxis reduce symptomatic venous thromboembolism in patients with below knee cast treatment for foot and ankle trauma? A systematic review and meta-analysis. 2018; Hickey BA, Watson U, Cleves A, Alikhan R, Pugh N, Nokes L, et al. Foot and Ankle Surgery. 24(1):19-27. |
Exclusie Searchdatum juni 2015 dus ouder dan Cochrane van Zee |
|
Low molecular weight heparin for prevention of venous thromboembolism in patients with lower-limb immobilization. 2017; Zee AAG, van Lieshout K, van der Heide M, Janssen L, Janzing HMJ. Cochrane Database of Systematic Reviews. 2017(8). |
Inclusie |
|
Prevention of venous thromboembolic events with low-molecular-weight heparin in the non-major orthopaedic setting: Meta-analysis of randomized controlled trials. 2014; Chapelle C, Rosencher N, Jacques Zufferey P, Mismetti P, Cucherat M, Laporte S. Arthroscopy - Journal of Arthroscopic and Related Surgery. 30(8):987-96. |
Exclusie, overlap review van Zee en ouder. |
|
Insufficient Evidence for Routine Use of Thromboprophylaxis in Ambulatory Patients with an Isolated Lower Leg Injury Requiring Immobilization: Results of a Meta-Analysis. 2009 |
Exclusie, overlap review van Zee en ouder. |
|
Prevention of venous thromboembolism in patients with immobilization of the lower extremities: A meta-analysis of randomized controlled trials. 2008; Ettema HB, Kollen BJ, Verheyen CCPM, Büller HR. Journal of Thrombosis and Haemostasis. 6(7):1093-8. |
Exclusie, overlap review van Zee en ouder. |
|
Low molecular weight heparin for prevention of venous thromboembolism in patients with lower leg immobilization. 2007; Testroote M, Stigter W, Janzing H, De Visser D. Cochrane Database of Systematic Reviews. (3). |
Exclusie, overlap review van Zee en ouder. |
|
Venous Thromboembolic Prophylaxis in Foot and Ankle Surgery: A Review of Current Literature and Practice. 2017; Weisman MHS, Holmes JR, Irwin TA, Talusan PG. Foot & Ankle Specialist. 10(4):343-51. |
Exclusie, overlap review van Zee en ouder. |
|
Thromboprophylaxis after Knee Arthroscopy and Lower-Leg Casting. 2017; van Adrichem RA, Nemeth B, Algra A, le Cessie S, Rosendaal FR, Schipper IB, et al. New England Journal of Medicine. 376(6):515-25. |
Exclusie studie: zit reeds in Cochrane review van Zee. |
|
Nadroparin or fondaparinux versus no thromboprophylaxis in patients immobilised in a below-knee plaster cast (PROTECT): A randomised controlled trial. 2017; Bruntink MM, Groutars YME, Schipper IB, Breederveld RS, Tuinebreijer WE, Derksen RJ, et al. Injury. 48(4):936-40. |
Exclusie studie: zit reeds in Cochrane review van Zee. |
|
Comparison of Fondaparinux with Low-Molecular-Weight Heparin for Venous Thromboembolism Prevention in Patients Requiring Rigid or Semi-Rigid Immobilization for Isolated Non-Surgical Below-Knee Injury. 2014; Samama CM, Lecoules N, Kierzek G, Claessens YE, Riou B, Rosencher N, et al. Annales Francaises de Medecine d'Urgence. 4(3):153-66. |
Exclusie: niet juiste vergelijking (LMWH versus. fondaparinux) |
|
Comparison of fondaparinux with low molecular weight heparin for venous thromboembolism prevention in patients requiring rigid or semi-rigid immobilization for isolated non-surgical below-knee injury. 2013; Samama CM, Lecoules N, Kierzek G, Claessens YE, Riou B, Rosencher N, et al. Journal of Thrombosis and Haemostasis. 11(10):1833-43. |
Exclusie: niet juiste vergelijking (LMWH versus. fondaparinux) |
|
Thromboprophylaxis in patients with lower limb immobilisation - Review of current status. 2009; Nokes TJC, Keenan J. British Journal of Haematology. 146(4):361-8. |
Exclusie: overlap en ouder dan Cochrane review Zee |
|
Prolonged thromboprophylaxis with dalteparin after surgical treatment of achilles tendon rupture: A randomized, placebo-controlled study. 2007; Lapidus LJ, Rosfors S, Ponzer S, Levander C, Elvin A, Lärfars G, et al. Journal of Orthopaedic Trauma. 21(1):52-7. |
Exclusie studie: zit reeds in Cochrane review van Zee. |
|
Prolonged thromboprophylaxis with Dalteparin during immobilization after ankle fracture surgery: A randomized placebo-controlled, double-blind study. 2007; Lapidus LJ, Ponzer S, Elvin A, Levander C, Lärfars G, Rosfors S, et al. Acta Orthopaedica. 78(4):528-35. |
Exclusie studie: zit reeds in Cochrane review van Zee. |
|
Use of the low-molecular-weight heparin reviparin to prevent deep-vein thrombosis after leg injury requiring immobilization. 2002; Lassen MR, Borris LC, Nakov RL. New England Journal of Medicine. 347(10):726-30. |
Exclusie studie: zit reeds in Cochrane review van Zee. |
|
Low molecular weight heparin (Innohep) as thromboprophylaxis in outpatients with a plaster cast: A venografic controlled study. 2002; Jorgensen PS, Warming T, Hansen K, Paltved C, Vibeke Berg H, Jensen R, et al. Thrombosis Research. 105(6):477-80. |
Exclusie studie: zit reeds in Cochrane review van Zee. |
|
Deelvraag 2: risicofactoren |
|
|
Venous thrombosis following lower-leg cast immobilization and knee arthroscopy: From a population-based approach to individualized therapy. 2019; Nemeth B, Cannegieter SC. Thrombosis Research. 174:62-75. |
Exclusie: overlap met Horner en niet systematische review. |
|
Effect of Early Versus Late Weightbearing in Conservatively Treated Acute Achilles Tendon Rupture: A Meta-Analysis. 2018; El-Akkawi AI, Joanroy R, Barfod KW, Kallemose T, Kristensen SS, Viberg B. Journal of Foot and Ankle Surgery. 57(2):346-52. |
Exclusie: overlap Horner |
|
High incidence of deep venous thrombosis after Achilles tendon rupture: A prospective study. 2009; Nilsson-Helander K, Thurin A, Karlsson J, Eriksson BI. Knee Surgery, Sports Traumatology, Arthroscopy. 17(10):1234-8. |
Exclusie: gepubliceerd in tijdsperiode Horner en deze review wordt als uitgangspunt genomen. |
|
High risk of recurrent venous thrombosis in patients with lower-leg cast immobilization. 2018; Nemeth B, Timp JF, van Hylckama Vlieg A, Rosendaal FR, Cannegieter SC. Journal of Thrombosis and Haemostasis. 16(11):2218-22. |
Exclusie: Horner als uitgangspunt genomen en geen additionele studies toegevoegd. |
|
The impact of risk assessment on the implementation of venous thromboembolism prophylaxis in foot and ankle surgery. 2014; Saragas NP, Ferrao PNF, Saragas E, Jacobson BF. Foot and Ankle Surgery. 20(2):85-9. |
Exclusie: studie naar optreden van VTE bij patiënten met gipsimmobilisatie na operatie, maar niet specifieke analyses naar risicofactoren. Tevens analyse naar asymptomatische VTE en geen van de benoemde uitkomstmaten gerapporteerd. |
|
Symptomatic venous thromboembolism after non-operatively treated foot or ankle injury. 2018; Prince RM, Lubberts B, Buda M, Guss D, DiGiovanni CW. Journal of Orthopaedic Research. |
Exclusie: relevante studie maar gekozen om Horner als uitgangspunt te nemen. |
|
Venous thromboembolism in emergency department patients with rigid immobilization for lower leg injury: Incidence and risk factors. 2012; Meek R, Tong RLK. EMA - Emergency Medicine Australasia. 24(3):277-84. |
Exclusie: zit in review Horner. |
|
Deelvraag 3: predictiemodellen |
|
|
C 11. Venous Thromboembolism Prophylaxis in Outpatient Lower Limb Fractures and Injuries. 2016; Ajwani SH, Shaw A, Naiz O, Bhaskar D, Charalambous CP. Ortopedia, traumatologia, rehabilitacja. 18(3):263-8. |
Exclusie: andere PICO (onderzoeken gebruik van tool en effect op gegeven tromboseprofylaxe) |
Beoordelingsdatum en geldigheid
Publicatiedatum : 06-08-2020
Beoordeeld op geldigheid : 01-09-2020
Deze richtlijn is modulair herzien. Een aantal modules dienen binnen de tijdstermijn van 5 jaar herzien te worden. De NIV is daarom voornemens een deel van de werkgroep in stand te houden. Een nader uitgewerkt onderhoudsplan wordt tijdens de commentaarronde ter consultatie voorgelegd aan de NIV commissie richtlijnen en kwaliteitsmeting.
De NIV is als houder van deze richtlijn de eerstverantwoordelijke voor de actualiteit van deze richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijk verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de eerstverantwoordelijke over relevante ontwikkelingen binnen hun vakgebied.
Omdat deze richtlijn in modulair onderhoud is zullen er de komende tijd regelmatig modules van deze richtlijn worden geüpdatet of waar nodig nieuwe modules worden ontwikkeld en toegevoegd. Er volgen hiervoor nog aparte commentaar- en autorisatiefases. Zie het ‘Overzicht modulair onderhoud’ bij de aanverwante producten van deze module voor een overzicht van de vragen die momenteel uitgewerkt worden.
Algemene gegevens
Deze richtlijnmodule is goedgekeurd door:
- Patiëntenfederatie Nederland
- Harteraad
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van Medisch Specialisten (https://www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
Het doel is de multidisciplinaire nationale richtlijn Antitrombotisch beleid te herzien, waarbij er een duidelijke invulling komt van de gesignaleerde klinische knelpunten. Als voorbeeld wordt de hiaat met betrekking tot het beleid van perioperatief gebruik van antistolling herzien en wordt aandacht gegeven aan de introductie van DOACs.
Doelgroep
Deze richtlijn is geschreven voor patiënten, trombosediensten, en alle leden van de beroepsgroepen die betrokken zijn bij de zorg voor patiënten met antitrombotische therapie.
Samenstelling werkgroep
Kerngroep
- prof. dr. M.V. (Menno) Huisman, internist-vasculaire geneeskunde, LUMC, NIV (voorzitter)
- dr. M.J.H.A. (Marieke) Kruip, internist-hematoloog, ErasmusMC, NIV, NVVH (Nederlandse Vereniging voor Hematologie)
- dr. F.A. (Erik) Klok, internist-vasculaire geneeskunde, LUMC, NIV
- dr. M.A. (Marc) Brouwer, cardioloog, RadboudUMC, NVVC
- dr. H.B. (Harmen) Ettema, orthopedisch chirurg, Isala, NOV
- drs. B. (Banne) Nemeth, aios orthopedie, LUMC, NOV
- dr. A.M. (Arno) Wiersema, vaatchirurg, NVVH
- dr. M.E. (Maarten) Tushuizen, maag-darm-leverarts, LUMC, NVMDL
- dr. J.M. (Jonathan) Coutinho, neuroloog, AMC-UVA, NVN
- drs. A. (Andrew) Oostindjer, huisarts/ Kaderhuisarts HVZ, NHG
Klankbordgroep
- dr. J.J.C.M. (Sjef) van de Leur, arts klinische chemie, Isala, NVKC
- dr. A.W.M.M. (Ankie) Koopman - van Gemert, anesthesioloog, ASZ, NVA
- dr. M.G. (Mariëlle) van Pampus, gynaecoloog, OLVG, NVOG
- drs. R.J. (Repke) Snijder, longarts, Antoniusziekenhuis, NVALT
- drs. R.J. Lely, radioloog, VUMC, NVVR
- dr. C. van Montfrans, dermatoloog, ErasmusMC, NVDV
- dr. R.A. (Richard) Faaij, klinisch geriater, Diakonessenhuis, NVKG
- dr. B. van Minnen, kaakchirurg, UMCG, NVMKA
- mw. A (Annemarie) Auwerda, beleidsadviseur, Harteraad (vanaf maart 2019)
- A.M. (Anne) Kors-Walraven MSc BA, beleidsadviseur, Harteraad (van November 2018 tot maart 2019).
- prof. dr. S (Saskia) Middeldorp, internist vasculaire-geneeskunde, AMC-UVA, NIV
- M.J. (Jacqueline) Krol- van Straaten, internist – nefroloog, Hagaziekenhuis, NIV
- dr. M. (Marcel) Schouten, internist – nefroloog, Tergooi, NIV
- dr. N. (Nakisa) Khorsand, ziekenhuisapotheker, OLVG, NVZA
- dr. M.F. (Margreet) Warlé- van Herwaarden, openbaar apotheker, KNMP
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Achternaam werkgroeplid |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Getekend op |
Acties |
|
Huisman |
Internist vasculaire geneeskunde Leids Universitair Medisch Centrum |
- Voorzitter commissie herziening Antitrombotisch Beleid, onbetaald |
Adviseur farmaceutische bedrijven die (nieuwe) antistollingsmiddelen maken - betaald; gelden gaan naar afdeling Interne Geneeskunde LUMC |
Niet van toepassing |
ZONMW grant Dutch-AF - registry met onderzoek op het gebied van antistolling bij patiënten met atriumfibrilleren; betaald, gelden gaan naar afdeling Interne Geneeskunde LUMC |
Niet van toepassing |
Niet van toepassing |
14-6-2018 |
Deelname in werkgroep als voorzitter in verband met expertise op dit gebied. In verband met adviseur farmaceutische bedrijven: participeert niet bij besluitvorming middelen |
|
Kruip |
Internist-hematoloog Erasmus MC |
Medisch leider trombosedienst Star-SHL, gedetacheerd vanuit het Erasmus MC |
Geen |
Geen |
- Anti-thrombotic standardship S-team introduction (2015-2016) Boehringer-Ingelheim |
Niet van toepassing |
- 2015: bezoek Sheffield trombosekliniek / Bayer / € 500,- (reiskosten) |
26-6-2018 |
In verband met belangen geen participatie besluitvorming keuze middelen |
|
Wiersema |
Vaatchirurg in het Westfriesgasthuis te Hoorn en AUMC, locatie Vumc |
Grant onderzoek ACT en heparine arteriële vaatingrepen Medtronic, geen onderwerp van deze richtlijn |
Geen |
Geen |
Grant onderzoek ACT en heparine arteriële vaatingrepen Medtronic, geen onderwerp van deze richtlijn |
Geen |
Geen |
24-7-2018 |
Geen acties |
|
Ettema |
Orthopedisch chirurg Isala Klinieken, Zwolle |
geen |
geen van bovenstaande |
geen van bovenstaande |
In verleden deelname verschillende RCT waarvan de laatste > 2 jaar gelden |
geen van bovenstaande |
geen |
31-7-2018 |
RCT's >3 jaar geleden, geen actie |
|
Coutinho |
Neuroloog Amsterdam UMC |
geen |
geen |
geen |
RESPECT-CVT studie. Gefinancierd door Boehringer. Ondergetekende zit in het steering Committee van deze studie |
geen |
geen |
31-8-2018 |
geen actie, studie gaat over andere patiëntpopulatie |
|
Warlé-van Herwaarden |
Apotherker, Apotheek Groesbeek |
participeert af en toe in onderzoek (onbetaald) |
geen |
geen |
geen |
geen |
Geen |
3-9-2018 |
Geen acties |
|
Brouwer |
Cardioloog, Radboudumc |
Afgevaardigde van de NVVO bij LSKA (Landelijke Standaard Keten Antistolling), onbetaald |
De research-afdeling cardiologie heeft voor verschillende projecten financiële ondersteuning ontvangen van : Astra Zeneca, BMS-Pfizer, Boehringer Ingelheim, Beyer, Daiichi Sankyo |
nee |
Dutch AF registry |
Niet van toepassing |
Niet van toepassing |
8-11-2017 |
Geen, ander onderwerp |
|
Klok |
Internist Vasculair geneeskundige, LUMC, Leiden |
Adjunct Professor Universiteit van Mainz, Duitsland (onbetaald) |
Geen |
Geen |
Dr. F.A. Klok heeft financiële steun ontvangen voor studies (unrestricted research grants) van Bayer, BMS/Pfizer, Boehringer Ingelheim, Daiichi Sankyo, MSD, Actelion, Trombose Stichting Nederland en de Hartstichting. Dit betroffen allen studies naar diagnostiek van longembolie/DVT of voorkomen van langetermijn effecten (pulmonale hypertensie, lagere kwaliteit van leven et cetera). |
Geen |
Geen |
21-9-2018 |
Geen, gesponsorde studies gaan over diagnostiek. Diagnostiek komt vooralsnog niet aan bod in deze richtlijn. Mocht dit het geval zijn belangen opnieuw bespreken. Geen actie nodig |
|
Alikhil |
* Huisarts, werkzaam in huisartspraktijk Alikhil |
* Huisartsenzorg in volle breedte |
Neen |
Neen |
Neen |
Neen |
Neen |
1-11-2018 |
Geen acties |
|
Tushuizen |
MDL-arts, staflid Leids Universitair Medisch Centrum, Leiden |
MDL-arts; DC-kliniek Almere, Almere, verrichten van endoscopie (betaald) |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
14-12-2018 |
Geen acties |
|
Oostindjer |
Huisarts - eigen praktijk in Oldenzaal. |
Als Kaderhuisarts HVZ: |
Ik heb momenteel geen (financiële) belangen bij welke organisatie dan ook die producten produceert die van belang zijn voor deze richtlijn (antistolling). |
nvt |
nvt |
Ik heb geen belangen die geschaad of bevoordeeld kunnen worden. Enige wat zou kunnen is dat er meer vraag komt naar onderwijs op dit onderwerp welke ik dan zou kunnen verzorgen mogelijk een vorm van “vermarkting”. |
nvt |
19-8-2019 |
|
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiënten perspectief door een search naar het patiënten perspectief. Daarnaast zal bij de richtlijn een zogenaamde ‘option grid’ worden ontwikkeld (keuzehulp voor patiënten en zorgverleners samen) voor het onderwerp continueren antistolling.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten. De werkgroep heeft tevens interne kwaliteitsindicatoren ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken (zie indicatorenontwikkeling).
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen volgens het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II) (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is en op ‘richtlijnen voor richtlijn’ voor de beoordeling van de kwaliteit van richtlijnen (www.zorginstituutnederland.nl).
Doordat delen van de richtlijn niet herzien zijn, zijn door de evolutie van richtlijn ontwikkelmethodologie de gebruikte methodes verschillend voor verschillende delen.
De delen over diagnostiek bij diepe veneuze trombose, diagnostiek longembolie, aparte categorieën in kader van diagnostiek, arteriële preventie en bijzondere situaties veneuze preventie veneuze trombo-embolie uit de CBO richtlijn van 2008 zijn zo veel mogelijk in originele structuur en stijl behouden (hoewel er aan de structuur wijzigingen zijn gemaakt zodat deze teksten conform het richtlijnendatabase format zijn). De additionele secties over medicamenteuze behandeling van veneuze trombo-embolie, niet-medicamenteuze behandeling van veneuze trombo-embolie, bijzondere situaties veneuze trombo-embolie en preventie veneuze trombo-embolie bevatten nieuwe literatuur en aanbevelingen die werden ontwikkeld volgens nieuwe methodologie. Dit heeft onvermijdelijk geleid tot inconsistenties in de stijl. Bijvoorbeeld is de GRADE methodologie gebruikt in de nieuwe teksten om de kwaliteit en sterkte van de bewijskracht en aanbevelingen te graderen in de nieuwe stukken, waar in de oude stukken gebruik is gemaakt van de oudere EBRO methodologie, of gradering van de oude ACCP richtlijn (2004) is overgenomen. Daarnaast wordt in de oude delen van de richtlijn asymptomatische DVT als uitkomstmaat gehanteerd, maar meer recentelijk wordt zowel nationaal als internationaal deze uitkomstmaat niet meer gebruikt. In de nieuwe delen worden daarom alleen de resultaten met betrekking tot symptomatische DVT gerapporteerd.
De beschrijving van de methodologie bij de verschillende teksten bevatten een beschrijving van de details met betrekking tot de methodologie voor de betreffende module.
Het is van belang om te benadrukken dat hoewel de richtlijn methodologie is veranderd, ook de oudere aanbevelingen uit de CBO richtlijn 2008 onverminderd van kracht zijn.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de werkgroep de knelpunten middels een enquête. Naast de in de kern- en klankbordgroep vertegenwoordigde partijen werden de FNT, IGJ, KiMO, NHG, NFU, NVZ, STZ, V&VN, Verenso, VIG, VWS, ZiNL en ZN uitgenodigd deze enquête in te vullen.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur conceptuitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk en onbelangrijk. Tevens definieerde de werkgroep voor de kritieke en belangrijke uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar systematische reviews [EMBASE, MEDLINE, Cochrane library]. Vervolgens werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekactie of gebruikte trefwoorden van de zoekactie en de gehanteerde selectiecriteria zijn te vinden in het hoofdstuk van desbetreffende uitgangsvraag.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen schatten. Deze beoordelingen kunt u vinden in de Risk of bias tabellen.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidence tabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org) (Schünemann H, 2013).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, matig, laag en zeer laag. Deze gradaties verwijzen naar de mate van vertrouwen in de literatuurconclusie.
|
GRADE |
Definitie |
|
Hoog |
|
|
Matig |
|
|
Laag |
|
|
Zeer laag |
|
B) Voor vragen over waarde diagnostische tests, schade of bijwerkingen, etiologie en prognose
De GRADE methodiek is door de Nederlandse werkgroep GRADE-NL (nog) niet vastgesteld voor dit type vraagstelling. De bewijskracht van de conclusie is bepaald volgens de EBRO-methode (Van Everdingen, 2004).
Belangrijkste verschillen tussen de GRADE- en ACCP-indeling
- Met de ACCP-indeling worden aanbevelingen gegradeerd, met de GRADE methodiek worden conclusies gegradeerd. In de ACCP-aanbevelingen wordt wel rekening gehouden met overige (meer subjectieve) overwegingen (bijwerkingen, kosten, gemak voor patiënt), maar dit is niet expliciet terug te vinden; dit komt terug in grootte van het effect (zie punt 2). In de GRADE methodiek worden de overige overwegingen (bijwerkingen, kosten, patiëntenperspectief, expert opinion) gewogen en transparant beschreven, deze overwegingen samen met de wetenschappelijke conclusies leiden tot de aanbevelingen;
- In de ACCP-indeling wordt onderscheid gemaakt tussen een duidelijk klinisch effect (1) en een klein of onduidelijk effect (2), volgens de GRADE-methodiek wordt vooraf benoemde klinische relevantie meegewogen in de gradering van de conclusies.
Formuleren van de conclusies
Voor vragen over de waarde van diagnostische testen, over schade of bijwerkingen, etiologie en prognose is het wetenschappelijke bewijs samengevat in één of meerdere conclusie(s), waarbij het niveau van het meest relevante bewijs is weergegeven.
Bij interventievragen verwijst de conclusie niet naar één of meer artikelen, maar wordt getrokken op basis van alle studies samen (body of evidence). Hierbij maakten de werkgroepleden de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals criteria die van invloed zijn op de aanbeveling, de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen of organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. De richtlijn bevat geen organisatie van zorg hoofdstuk, omdat er over organisatie van zorg en samenwerking binnen de keten reeds documenten bestaan (bijvoorbeeld LSKA 2.0).
Indicatorontwikkeling
Gelijktijdig met het ontwikkelen van de richtlijn werden er interne kwaliteitsindicatoren ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken (de indicatoren zijn te vinden in de aanverwante producten). Meer informatie over de methode van indicatorontwikkeling is op te vragen bij het Kennisinstituut van Medisch Specialisten (secretariaat@kennisinstituut.nl).
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is. Een overzicht van aanbevelingen voor nader/vervolg onderzoek worden toegevoegd na de commentaarfase.
Commentaar- en autorisatiefase
De conceptrichtlijn wordt aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor commentaar. De commentaren worden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren wordt de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn wordt aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor autorisatie en door hen geautoriseerd.
Zoekverantwoording
|
Uitgangsvraag: UV5 |
|
|
Database(s): Medline, Embase |
Datum: 10-01-2019 |
|
Periode: > 2000 |
Talen: Engels |
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID)
2000 – januari 2019
|
1 (Venous thrombo* or (venous adj1 thrombo) or VTE or deep vein thrombo*).ti,ab,kw. or exp Venous Thrombosis/ or DVT.ti,ab,kw. or thrombo-embolic.ti,ab,kw. or thromboembolic.ti,ab,kw. or exp VENOUS THROMBOEMBOLISM/ or exp THROMBOEMBOLISM/ or thromboembolism.ti,ab,kw. or thromboembolism*.ti,ab,kw. or pulmonary embolism.ti,ab,kw. or exp Pulmonary Embolism/ or blood clot*.ti,ab,kw. or blood coagulation.ti,ab,kw. or exp Blood Coagulation/ or thrombus.ti,ab,kw. or exp THROMBUS/ or exp THROMBOSIS/ or thrombos*.ti,ab,kw. or post-thrombotic*.ti,ab,kw. or postthrombotic*.ti,ab,kw. or post thrombotic*.ti,ab,kw. or Thrombophlebitis/ (348709) 2 exp Casts, Surgical/ or ((cast adj3 (immobil* or leg* or plaster)) or ((leg* or lower) adj3 immobil*)).ti,ab,kw. (10983) 3 1 and 2 (264) 4 limit 3 to (english language and yr="2000 - 2019") (174) 5 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (380630) 6 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1818945) 7 Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or (cohort adj (study or studies)).tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ (Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies) (3103115) 8 4 and 5 (23) 9 4 and 6 (54) 10 4 and 7 (83) 11 8 or 9 or 10 (117)
= 117 (117 uniek) |
157 |
|
Embase (Elsevier) |
('venous thrombo*':ab,ti OR ((venous NEAR/1 'thrombo*'):ab,ti) OR vte:ab,ti OR 'deep vein thrombo*':ab,ti OR dvt:ab,ti OR 'thrombo-embolic':ab,ti OR thromboembolic:ab,ti OR thromboembolism:ab,ti OR thromboembolism*:ab,ti OR 'pulmonary embolism':ab,ti OR 'blood clot':ab,ti OR 'blood coagulation':ab,ti OR thrombus:ab,ti OR thrombos*:ab,ti OR 'post-thrombotic':ab,ti OR postthrombotic:ab,ti OR 'post thrombotic':ab,ti OR 'thromboembolism'/exp/mj)
AND ('leg cast'/exp OR 'cast immobilization'/exp OR 'plaster cast'/exp OR 'cast application'/exp OR ((cast NEAR/3 (immobil* OR leg* OR plaster)):ab,ti) OR (((leg* OR lower) NEAR/3 immobil*):ab,ti))
AND (english)/lim AND (2000-2019)/py NOT 'conference abstract':it
Gebruikte filters:
Systematische reviews: ('meta analysis'/de OR cochrane:ab OR embase:ab OR psycinfo:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp)
RCT’s: ('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it
Observationeel onderzoek: 'major clinical study'/exp OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR ('prospective study'/de NOT 'randomized controlled trial'/de) OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (case:ab,ti AND ((control NEAR/1 (study OR studies)):ab,ti)) OR (follow:ab,ti AND ((up NEAR/1 (study OR studies)):ab,ti)) OR ((observational NEAR/1 (study OR studies)):ab,ti) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti)
= 135 (134 uniek) |