Tromboseprofylaxe bij arthroscopische ingreep van de knie
Uitgangsvraag
Is tromboseprofylaxe geïndiceerd bij een arthroscopische ingreep van de knie?
Aanbeveling
Geef geen tromboseprofylaxe na een routinematige arthroscopie (dit geldt ook voor een routinematige voorstekruisband reconstructie) van de knie.
Overweeg tromboseprofylaxe met LMWH (zeven dagen) na een uitgebreidere ingreep dan hierboven beschreven.
Overweeg tromboseprofylaxe met LMWH (zeven dagen) bij patiënten met een voorgeschiedenis van VTE.
Overwegingen
Na het uitkomen van de ACCP richtlijn (2012) is maar één additionele RCT gepubliceerd (Van Adrichem, 2017) die voldoet aan de PICO. De trial door Van Adrichem was wat betreft groepsgrootte voldoende voor onderzoeken van de effectiviteit op reductie van symptomatische VTE. Een meta-analyse en systematische review (Huang, 2018) liet zien dat LMWH niet effectief was voor een reductie in symptomatische VTE (RR 0,90 (95%BI 0,39 tot 2,08) bij patiënten die een knie arthroscopie ondergingen. Tevens liet deze meta-analyse zien dat er mogelijk een verhoogd risico is op ernstige bloedingen (RR 1,41, 95%BI 0,25 tot 8,15). In deze analyse werden alle studies betrokken zoals beschreven in de ACCP 2012 richtlijn plus de studie door Van Adrichem (2017). Eenzelfde conclusie werd getrokken door een twee andere reviews (Zheng, 2018 en Nemeth, 2018).
Voor patiënten die invasievere arthroscopische chirurgie ondergaan (zoals een kruisband reconstructie) zijn geen kwalitatief goede studies aanwezig die alléen deze patiënten hebben geïncludeerd. Er is geen officiële search gedaan voor deze patiëntengroep. In de trial van Camporese (2008 ) heeft ongeveer 40% van de geïncludeerde patiënten een voorste kruisband reconstructie ondergaan. In de trial van Wirth (2001) was dit 46%. Er wordt echter geen subgroep analyse gerapporteerd in deze trials. Wel is vastgesteld dat deze patiënten een duidelijk verhoogd risico hebben op symptomatische VTE (Janssen, 2016; Van Adrichem, 2015). Echter, adequate literatuur (RCT’s en systematische reviews) over deze invasievere reconstructieve of gecompliceerde en/of langdurige knieartroscopieën is niet voorhanden; dit geldt zowel voor de aard van profylaxe als de duur ervan. Tegelijkertijd kunnen ingrepen die in het verleden als zeer invasief verondersteld werden steeds meer geschaard worden onder routinematige ingrepen (voorste kruisband reconstructie). Voor artroscopieën van de enkel en andere gewrichten geldt hetzelfde.
De algemene mening over het profylaxe tromboseprofylaxe beleid bij patiënten met een verhoogd risico op VTE is dat enige vorm van overwogen kan worden. Profylaxe dient te worden beperkt tot patiënten die uitgebreide arthroscopische chirurgie ondergaan en voor patiënten met een voorgeschiedenis van VTE. Deze twee patiëntencategorieën zijn systematisch geëxcludeerd uit alle geïncludeerde RCT’s, derhalve is er geen duidelijkheid over de effectiviteit van tromboseprofylaxe voor deze patiënten. Wel is bekend dat deze patiënten een sterk verhoogd risico hebben op symptomatische VTE (Delis, 2001; Krych, 2015). De werkgroep is daarom van mening dat tromboseprofylaxe dient te worden overwogen voor deze hoog-risico groepen.
Geadviseerd wordt om de door de fabrikant geadviseerde en/of in trials geëvalueerde dosering te gebruiken bij het voorschrijven van farmacologische profylaxe. Voor deze specifieke patiënt categorieën wordt een duur van zeven dagen aanbevolen, hoewel de bewijskracht ook hiervoor laag is. In een trial van Camporese (2018) wordt een duur van 7 dagen aanbevolen vanwege een toegenomen bloedingsrisico bij 14 dagen behandeling met LMWH (Camporese, 2008).
Onderbouwing
Artroscopie van de knie is de meest uitgevoerde operatie in de orthopedische chirurgie met wereldwijd meer dan 3 miljoen ingrepen per jaar. De operatie wordt doorgaans uitgevoerd in een poliklinische setting en doorgaans bij relatief jonge patiënten. Meest uitgevoerde procedures zijn een meniscectomie, kraakbeen behandeling en voorste kruisband reconstructie. De effectiviteit van tromboseprofylaxe is voor deze groep patiënten onduidelijk. Momenteel is alleen LMWH een goedgekeurde behandeling. DOAC’s zijn daarom bij deze uitgangsvraag buiten beschouwing gelaten.
|
Redelijk GRADE |
Het is waarschijnlijk dat het gebruik van LMWH het risico op symptomatische VTE bij patiënten die artroscopie van de knie ondergaan niet verlaagt.
Bronnen: (Huang, 2018 (Wirth, 2001; van Adrichem, 2017; Roth, 1995; Michot, 2002; Marlovits, 2007; Canata, 2003; Camporese, 2008)) |
|
Laag GRADE |
Het is mogelijk dat het gebruik van LMWH het risico op ernstige bloedingen bij patiënten die artroscopie van de knie ondergaan verhoogt.
Bronnen: (Huang, 2018 (Wirth, 2001; van Adrichem, 2017; Roth, 1995; Michot, 2002; Marlovits, 2007; Canata, 2003; Camporese, 2008)) |
In totaal worden in de review van Huang (2018) 7 RCT’s met 3.879 patiënten (2.166 in de LMWH groep en 1.713 in de controlegroep) geïncludeerd (Wirth, 2001; van Adrichem, 2017; Roth, 1995; Michot, 2002; Marlovits, 2007; Canata, 2003; Camporese, 2008). De kwaliteit van de individuele studies werd in deze review beoordeeld met de Cochrane Collaboration tool (zie evidence tabel). De middelen en doseringen in de studies waren verschillend en de duur van toediening varieerde van 4 dagen postoperatief (Roth, 1995) tot 30 dagen (Michot, 2002). Het grootste aantal patiënten werd gedurende 7 dagen postoperatief behandeld. De follow-up duur was in de meerderheid van de patiënten 3 maanden.
Symptomatische VTE
Symptomatische VTE werd in 7 studies gerapporteerd. In totaal kregen 11 van de 2166 patiënten in de LMWH groep in vergelijking met 10 van de 1713 patiënten in de controlegroep symptomatische VTE. Meta-analyse van deze studies toont geen significant verschil in het optreden van symptomatische VTE bij patiënten die LMWH versus geen LMWH gebruiken na artroscopie van de knie (RR 0,90 (95%BI 0,39 tot 2,08; 7 studies, 3.879 patiënten) (zie figuur 1).
Figuur 1 Symptomatische VTE
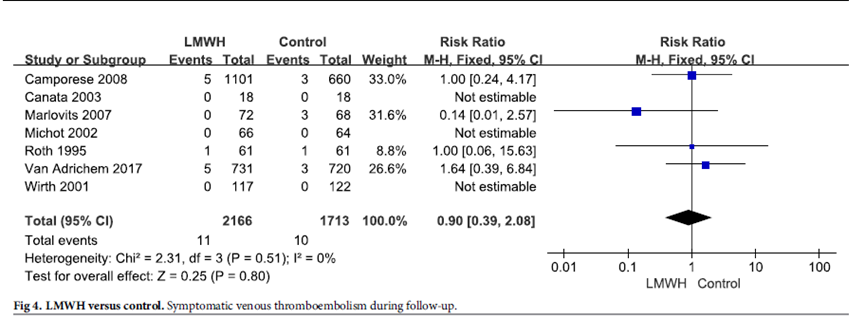
Ernstige bloedingen
De uitkomstmaat ernstige bloeding werd in 7 studies gerapporteerd. In totaal kregen 4 van de 2166 (0,2%) patiënten in de LMWH groep in vergelijking met 2 van de 1713 (0,1%) patiënten in de controlegroep symptomatische VTE. Meta-analyse van deze studies toont geen significant verschil in optreden van ernstige bloedingen bij patiënten die LMWH versus geen LMWH gebruiken na artroscopie van de knie (RR 1,41 (95%BI 0,25 tot 8,15; 7 studies, 3.879 patiënten).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat symptomatische VTE is met een niveau verlaagd naar redelijk gezien het kleine aantal events (imprecisie). Hoewel in de meerderheid van de studies patiënten en zorgverleners niet geblindeerd waren wordt de bewijskracht hier gezien de objectieve uitkomstmaten niet voor verlaagd. De bewijskracht voor de uitkomstmaat bloedingen is met twee niveaus verlaagd gezien het zeer kleine aantal events (ernstige imprecisie).
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag (vragen):
P: patiënten die een knie arthroscopie ondergaan;
I: laag-moleculair-gewicht-heparine;
C: geen behandeling of placebo.
Relevante uitkomstmaten
De werkgroep achtte symptomatische veneuze trombo-embolieën en ernstige bloedingen voor de besluitvorming cruciale uitkomstmaten. Asymptomatische VTE acht de werkgroep niet relevant gezien hier niet actief naar wordt gescreend in de klinische praktijk. Tevens is uit eerder onderzoek is gebleken dat de effectiviteit voor asymptomatische trombose en symptomatische trombose niet goed overeenkomt. Studies die de effectiviteit op asymptomatische trombose onderzoeken zijn derhalve nauwelijks relevant.
De werkgroep definieerde niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
Zoeken en selecteren (Methode)
Voor de uitwerking van deze uitgangsvraag was een recente systematische review beschikbaar (Huang, 2018). Deze review is als uitgangspunt genomen en daarom is geen aanvullende literatuursearch uitgevoerd. Voor deze review werd in Pubmed, EMBASE en Cochrane gezocht tot september 2017 (zie zoekverantwoording) naar studies bij patiënten die een arthroscopie ondergaan waarbij LMWH werd vergeleken met geen LMWH of placebo. De literatuurzoekactie leverde 245 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria: RCT, patiënten ondergingen arthroscopie van de knie, patiënten ontvingen LWMH na arthroscopie en een van de volgende uitkomstmaten wordt gerapporteerd: effectiviteit (DVT, longembolie) veiligheid (ernstige bloedingen en bloedingen). In totaal worden 7 RCT’s in de review geanalyseerd.
De resultaten van de review van Huang (2018) (met daarin 7 RCT’s) zijn opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de bewijstabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk-of-biastabellen.
- Van Adrichem RA, Nelissen RG, Schipper IB, Rosendaal FR,Cannegieter SC. Risk of venous thrombosis after arthroscopy of the knee: results from a large population-based case-control study. J Thromb Haemost. 2015; 13(8):1441±8. https://doi.org/10.1111/jth.12996 PMID: 25940206 Roth VP. Prophylaxis of deep vein thrombosis in outpatients undergoing arthroscopic meniscus operation. Orthop Prax.1995; 5:345±8.
- Van Adrichem RA, Nemeth B, Algra A, le Cessie S, Rosendaal FR, Schipper IB, et al. Thromboprophylaxis after Knee Arthroscopy and Lower-Leg Casting. N Engl J Med. 2017; 376(6):515±25. https://doi. Org/10.1056/NEJMoa1613303 PMID: 27959702.
- Camporese G, Bernardi E, Prandoni P, Noventa F, Verlato F, Simioni P, et al. Low-molecular-weight heparin versus compression stockings for thromboprophylaxis after knee arthroscopy: a randomized trial. Ann Intern Med. 2008; 149(2):73±82.PMID: 18626046.
- Delis KT, Hunt N, Strachan RK, Nicolaides AN. Incidence, natural history and risk factors of deep vein thrombosis in elective knee arthroscopy. Thromb Haemost. 2001 Sep;86(3):817-21. PubMed PMID: 11583313.
- Huang HF, Tian JL, Yang XT, Sun L, Hu RY, Yan ZH, Li SS, Xie Q, Tian XB. Efficacy and safety of low-molecular-weight heparin after knee arthroscopy: A meta-analysis. PloS One. 2018 Jun 21;13(6):e0197868. Doi: 10.1371/journal.pone.0197868. eCollection 2018. PubMed PMID: 29927930
- Krych AJ, Sousa PL, Morgan JA, Levy BA, Stuart MJ, Dahm DL. Incidence and Risk Factor Analysis of Symptomatic Venous Thromboembolism After Knee Arthroscopy. Arthroscopy. 2015 Nov;31(11):2112-8.
- Marlovits S, Striessnig G, Schuster R, Stocker R, Luxl M, Trattnig S, et al. Extended-duration thromboprophylaxis with enoxaparin after arthroscopic surgery of the anterior cruciate ligament: a prospective, randomized, placebo-controlled study. Arthroscopy. 2007; 23(7):696±702. https://doi.org/10.1016/j. arthro.2007.02.001 PMID: 17637403
- Michot M, Conen D, Holtz D, Erni D, Zumstein MD, Ruflin GB, et al. Prevention of deep-vein thrombosis in ambulatory arthroscopic knee surgery: A randomized trial of prophylaxis with lowÐmolecular weight heparin. Arthroscopy. 2002; 18(3):257±63. PMID: 11877611.
- Wirth T, Schneider B, Misselwitz F, Lomb M, TuÈyluÈ H, Egbring R, et al.Prevention of venous thromboembolism after knee arthroscopy with low-molecular weight heparin (reviparin): Results of a randomized controlled trial. Arthroscopy. 2001; 17(4):393±9. PMID: 11288011.
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control © |
Follow-up |
Outcome measures and effect size |
Comments |
|
Huang, 2018
Individual study characteristics deduced from Huang, 2018
|
SR and meta-analysis of RCT’s
Literature search up to Sept 2017
A: Roth, 1995 B: Wirth, 2001 C: Michot, 2002 D: Canata, 2003 E: Marlovita, 2007 F: Camporese, 2008 G: van Adrichem, 2017
Study design: RCT
Setting and Country: Nncludinted
Source of funding ancludincts of interest: Not reported |
Inclusion criteria SR: RCT, LMWH versus. none or placebo.
7 studies included
Important patient characteristics at baseline:
N (I, C), mean age (I, C) A: 61, 61 NA B: 117, 122, 37.6, 38.5 C: 66,64; 42, 46.5 D: 18, 18; 29.6, 32.5 E: 72, 68; 41.7% of Patients aged >30 Years, 41.2% of Patients aged >30 years F: 1101, 660 ; 42.1; 42,3 G: 731, 720; 48.1, 49.1
Groups comparable at baseline? Yes |
A: 0.3 ml Fraxiparine; 4 days after Surgery B: Reviparin; 1,750 IU; 7 to 10 days C: Dalteparin; 2,500 IU if weight <70 kg, 5,000 IU if >70 kg; 30 days D: Enoxaparin; no dose specified; 6 days E: Enoxaparin; 40 mg; 20 Days F: Nadroparin; 3800 IU; 7 days or 14 days G: Nadroparin or dalteparin; 2500 IU of dalteparin or 2850 IU of nadroparin were used for patients who weighed 100 kg or less, and a double dose was used for patients who weighed more than 100 kg; 8 days
|
A: none B: none C: none D: none E: placebo F: graduated compression stockings G: none
|
End-point of follow-up: Not reported
For how many participants were no complete outcome data available? Not reported
|
Symptomatic VTE
Pooled effect (fixed effects model): RR: 0.90; 95% confidence interval (CI): 0.39±2.08; P = 0.80, Heterogeneity (I2): 0%
Major bleeding Pooled effect (fixed effects model): RR: 0.70; 95% CI: 0.12±3.95; P = 0.68
|
Facultative:
Risk of Bias studies:
|
|
Study |
Appropriate and clearly focused question?1 |
Comprehensive and systematic literature search?2 |
Description of included and excluded studies?3 |
Description of relevant characteristics of included studies?4 |
Appropriate adjustment for potential confounders in observational studies?5 |
Assessment of scientific quality of included studies?6 |
Enough similarities between studies to make combining them reasonable?7 |
Potential risk of publication bias taken into account?8 |
Potential conflicts of interest reported?9 |
|
|
Yes/no/unclear |
Yes/no/unclear |
Yes/no/unclear |
Yes/no/unclear |
Yes/no/unclear/not applicable |
Yes/no/unclear |
Yes/no/unclear |
Yes/no/unclear |
Yes/no/unclear |
|
Huang, 2018 |
Yes |
Yes |
Yes |
Unclear (not much detail on studies) |
Not applicable |
Yes |
Yes |
No |
Yes |
Beoordelingsdatum en geldigheid
Publicatiedatum : 06-08-2020
Beoordeeld op geldigheid : 01-09-2020
Deze richtlijn is modulair herzien. Een aantal modules dienen binnen de tijdstermijn van 5 jaar herzien te worden. De NIV is daarom voornemens een deel van de werkgroep in stand te houden. Een nader uitgewerkt onderhoudsplan wordt tijdens de commentaarronde ter consultatie voorgelegd aan de NIV commissie richtlijnen en kwaliteitsmeting.
De NIV is als houder van deze richtlijn de eerstverantwoordelijke voor de actualiteit van deze richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijk verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de eerstverantwoordelijke over relevante ontwikkelingen binnen hun vakgebied.
Omdat deze richtlijn in modulair onderhoud is zullen er de komende tijd regelmatig modules van deze richtlijn worden geüpdatet of waar nodig nieuwe modules worden ontwikkeld en toegevoegd. Er volgen hiervoor nog aparte commentaar- en autorisatiefases. Zie het ‘Overzicht modulair onderhoud’ bij de aanverwante producten van deze module voor een overzicht van de vragen die momenteel uitgewerkt worden.
Algemene gegevens
Deze richtlijnmodule is goedgekeurd door:
- Patiëntenfederatie Nederland
- Harteraad
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van Medisch Specialisten (https://www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
Het doel is de multidisciplinaire nationale richtlijn Antitrombotisch beleid te herzien, waarbij er een duidelijke invulling komt van de gesignaleerde klinische knelpunten. Als voorbeeld wordt de hiaat met betrekking tot het beleid van perioperatief gebruik van antistolling herzien en wordt aandacht gegeven aan de introductie van DOACs.
Doelgroep
Deze richtlijn is geschreven voor patiënten, trombosediensten, en alle leden van de beroepsgroepen die betrokken zijn bij de zorg voor patiënten met antitrombotische therapie.
Samenstelling werkgroep
Kerngroep
- prof. dr. M.V. (Menno) Huisman, internist-vasculaire geneeskunde, LUMC, NIV (voorzitter)
- dr. M.J.H.A. (Marieke) Kruip, internist-hematoloog, ErasmusMC, NIV, NVVH (Nederlandse Vereniging voor Hematologie)
- dr. F.A. (Erik) Klok, internist-vasculaire geneeskunde, LUMC, NIV
- dr. M.A. (Marc) Brouwer, cardioloog, RadboudUMC, NVVC
- dr. H.B. (Harmen) Ettema, orthopedisch chirurg, Isala, NOV
- drs. B. (Banne) Nemeth, aios orthopedie, LUMC, NOV
- dr. A.M. (Arno) Wiersema, vaatchirurg, NVVH
- dr. M.E. (Maarten) Tushuizen, maag-darm-leverarts, LUMC, NVMDL
- dr. J.M. (Jonathan) Coutinho, neuroloog, AMC-UVA, NVN
- drs. A. (Andrew) Oostindjer, huisarts/ Kaderhuisarts HVZ, NHG
Klankbordgroep
- dr. J.J.C.M. (Sjef) van de Leur, arts klinische chemie, Isala, NVKC
- dr. A.W.M.M. (Ankie) Koopman - van Gemert, anesthesioloog, ASZ, NVA
- dr. M.G. (Mariëlle) van Pampus, gynaecoloog, OLVG, NVOG
- drs. R.J. (Repke) Snijder, longarts, Antoniusziekenhuis, NVALT
- drs. R.J. Lely, radioloog, VUMC, NVVR
- dr. C. van Montfrans, dermatoloog, ErasmusMC, NVDV
- dr. R.A. (Richard) Faaij, klinisch geriater, Diakonessenhuis, NVKG
- dr. B. van Minnen, kaakchirurg, UMCG, NVMKA
- mw. A (Annemarie) Auwerda, beleidsadviseur, Harteraad (vanaf maart 2019)
- A.M. (Anne) Kors-Walraven MSc BA, beleidsadviseur, Harteraad (van November 2018 tot maart 2019).
- prof. dr. S (Saskia) Middeldorp, internist vasculaire-geneeskunde, AMC-UVA, NIV
- M.J. (Jacqueline) Krol- van Straaten, internist – nefroloog, Hagaziekenhuis, NIV
- dr. M. (Marcel) Schouten, internist – nefroloog, Tergooi, NIV
- dr. N. (Nakisa) Khorsand, ziekenhuisapotheker, OLVG, NVZA
- dr. M.F. (Margreet) Warlé- van Herwaarden, openbaar apotheker, KNMP
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Achternaam werkgroeplid |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Getekend op |
Acties |
|
Huisman |
Internist vasculaire geneeskunde Leids Universitair Medisch Centrum |
- Voorzitter commissie herziening Antitrombotisch Beleid, onbetaald |
Adviseur farmaceutische bedrijven die (nieuwe) antistollingsmiddelen maken - betaald; gelden gaan naar afdeling Interne Geneeskunde LUMC |
Niet van toepassing |
ZONMW grant Dutch-AF - registry met onderzoek op het gebied van antistolling bij patiënten met atriumfibrilleren; betaald, gelden gaan naar afdeling Interne Geneeskunde LUMC |
Niet van toepassing |
Niet van toepassing |
14-6-2018 |
Deelname in werkgroep als voorzitter in verband met expertise op dit gebied. In verband met adviseur farmaceutische bedrijven: participeert niet bij besluitvorming middelen |
|
Kruip |
Internist-hematoloog Erasmus MC |
Medisch leider trombosedienst Star-SHL, gedetacheerd vanuit het Erasmus MC |
Geen |
Geen |
- Anti-thrombotic standardship S-team introduction (2015-2016) Boehringer-Ingelheim |
Niet van toepassing |
- 2015: bezoek Sheffield trombosekliniek / Bayer / € 500,- (reiskosten) |
26-6-2018 |
In verband met belangen geen participatie besluitvorming keuze middelen |
|
Wiersema |
Vaatchirurg in het Westfriesgasthuis te Hoorn en AUMC, locatie Vumc |
Grant onderzoek ACT en heparine arteriële vaatingrepen Medtronic, geen onderwerp van deze richtlijn |
Geen |
Geen |
Grant onderzoek ACT en heparine arteriële vaatingrepen Medtronic, geen onderwerp van deze richtlijn |
Geen |
Geen |
24-7-2018 |
Geen acties |
|
Ettema |
Orthopedisch chirurg Isala Klinieken, Zwolle |
geen |
geen van bovenstaande |
geen van bovenstaande |
In verleden deelname verschillende RCT waarvan de laatste > 2 jaar gelden |
geen van bovenstaande |
geen |
31-7-2018 |
RCT's >3 jaar geleden, geen actie |
|
Coutinho |
Neuroloog Amsterdam UMC |
geen |
geen |
geen |
RESPECT-CVT studie. Gefinancierd door Boehringer. Ondergetekende zit in het steering Committee van deze studie |
geen |
geen |
31-8-2018 |
geen actie, studie gaat over andere patiëntpopulatie |
|
Warlé-van Herwaarden |
Apotherker, Apotheek Groesbeek |
participeert af en toe in onderzoek (onbetaald) |
geen |
geen |
geen |
geen |
Geen |
3-9-2018 |
Geen acties |
|
Brouwer |
Cardioloog, Radboudumc |
Afgevaardigde van de NVVO bij LSKA (Landelijke Standaard Keten Antistolling), onbetaald |
De research-afdeling cardiologie heeft voor verschillende projecten financiële ondersteuning ontvangen van : Astra Zeneca, BMS-Pfizer, Boehringer Ingelheim, Beyer, Daiichi Sankyo |
nee |
Dutch AF registry |
Niet van toepassing |
Niet van toepassing |
8-11-2017 |
Geen, ander onderwerp |
|
Klok |
Internist Vasculair geneeskundige, LUMC, Leiden |
Adjunct Professor Universiteit van Mainz, Duitsland (onbetaald) |
Geen |
Geen |
Dr. F.A. Klok heeft financiële steun ontvangen voor studies (unrestricted research grants) van Bayer, BMS/Pfizer, Boehringer Ingelheim, Daiichi Sankyo, MSD, Actelion, Trombose Stichting Nederland en de Hartstichting. Dit betroffen allen studies naar diagnostiek van longembolie/DVT of voorkomen van langetermijn effecten (pulmonale hypertensie, lagere kwaliteit van leven et cetera). |
Geen |
Geen |
21-9-2018 |
Geen, gesponsorde studies gaan over diagnostiek. Diagnostiek komt vooralsnog niet aan bod in deze richtlijn. Mocht dit het geval zijn belangen opnieuw bespreken. Geen actie nodig |
|
Alikhil |
* Huisarts, werkzaam in huisartspraktijk Alikhil |
* Huisartsenzorg in volle breedte |
Neen |
Neen |
Neen |
Neen |
Neen |
1-11-2018 |
Geen acties |
|
Tushuizen |
MDL-arts, staflid Leids Universitair Medisch Centrum, Leiden |
MDL-arts; DC-kliniek Almere, Almere, verrichten van endoscopie (betaald) |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
14-12-2018 |
Geen acties |
|
Oostindjer |
Huisarts - eigen praktijk in Oldenzaal. |
Als Kaderhuisarts HVZ: |
Ik heb momenteel geen (financiële) belangen bij welke organisatie dan ook die producten produceert die van belang zijn voor deze richtlijn (antistolling). |
nvt |
nvt |
Ik heb geen belangen die geschaad of bevoordeeld kunnen worden. Enige wat zou kunnen is dat er meer vraag komt naar onderwijs op dit onderwerp welke ik dan zou kunnen verzorgen mogelijk een vorm van “vermarkting”. |
nvt |
19-8-2019 |
|
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiënten perspectief door een search naar het patiënten perspectief. Daarnaast zal bij de richtlijn een zogenaamde ‘option grid’ worden ontwikkeld (keuzehulp voor patiënten en zorgverleners samen) voor het onderwerp continueren antistolling.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten. De werkgroep heeft tevens interne kwaliteitsindicatoren ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken (zie indicatorenontwikkeling).
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen volgens het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II) (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is en op ‘richtlijnen voor richtlijn’ voor de beoordeling van de kwaliteit van richtlijnen (www.zorginstituutnederland.nl).
Doordat delen van de richtlijn niet herzien zijn, zijn door de evolutie van richtlijn ontwikkelmethodologie de gebruikte methodes verschillend voor verschillende delen.
De delen over diagnostiek bij diepe veneuze trombose, diagnostiek longembolie, aparte categorieën in kader van diagnostiek, arteriële preventie en bijzondere situaties veneuze preventie veneuze trombo-embolie uit de CBO richtlijn van 2008 zijn zo veel mogelijk in originele structuur en stijl behouden (hoewel er aan de structuur wijzigingen zijn gemaakt zodat deze teksten conform het richtlijnendatabase format zijn). De additionele secties over medicamenteuze behandeling van veneuze trombo-embolie, niet-medicamenteuze behandeling van veneuze trombo-embolie, bijzondere situaties veneuze trombo-embolie en preventie veneuze trombo-embolie bevatten nieuwe literatuur en aanbevelingen die werden ontwikkeld volgens nieuwe methodologie. Dit heeft onvermijdelijk geleid tot inconsistenties in de stijl. Bijvoorbeeld is de GRADE methodologie gebruikt in de nieuwe teksten om de kwaliteit en sterkte van de bewijskracht en aanbevelingen te graderen in de nieuwe stukken, waar in de oude stukken gebruik is gemaakt van de oudere EBRO methodologie, of gradering van de oude ACCP richtlijn (2004) is overgenomen. Daarnaast wordt in de oude delen van de richtlijn asymptomatische DVT als uitkomstmaat gehanteerd, maar meer recentelijk wordt zowel nationaal als internationaal deze uitkomstmaat niet meer gebruikt. In de nieuwe delen worden daarom alleen de resultaten met betrekking tot symptomatische DVT gerapporteerd.
De beschrijving van de methodologie bij de verschillende teksten bevatten een beschrijving van de details met betrekking tot de methodologie voor de betreffende module.
Het is van belang om te benadrukken dat hoewel de richtlijn methodologie is veranderd, ook de oudere aanbevelingen uit de CBO richtlijn 2008 onverminderd van kracht zijn.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de werkgroep de knelpunten middels een enquête. Naast de in de kern- en klankbordgroep vertegenwoordigde partijen werden de FNT, IGJ, KiMO, NHG, NFU, NVZ, STZ, V&VN, Verenso, VIG, VWS, ZiNL en ZN uitgenodigd deze enquête in te vullen.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur conceptuitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk en onbelangrijk. Tevens definieerde de werkgroep voor de kritieke en belangrijke uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar systematische reviews [EMBASE, MEDLINE, Cochrane library]. Vervolgens werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekactie of gebruikte trefwoorden van de zoekactie en de gehanteerde selectiecriteria zijn te vinden in het hoofdstuk van desbetreffende uitgangsvraag.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen schatten. Deze beoordelingen kunt u vinden in de Risk of bias tabellen.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidence tabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org) (Schünemann H, 2013).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, matig, laag en zeer laag. Deze gradaties verwijzen naar de mate van vertrouwen in de literatuurconclusie.
|
GRADE |
Definitie |
|
Hoog |
|
|
Matig |
|
|
Laag |
|
|
Zeer laag |
|
B) Voor vragen over waarde diagnostische tests, schade of bijwerkingen, etiologie en prognose
De GRADE methodiek is door de Nederlandse werkgroep GRADE-NL (nog) niet vastgesteld voor dit type vraagstelling. De bewijskracht van de conclusie is bepaald volgens de EBRO-methode (Van Everdingen, 2004).
Belangrijkste verschillen tussen de GRADE- en ACCP-indeling
- Met de ACCP-indeling worden aanbevelingen gegradeerd, met de GRADE methodiek worden conclusies gegradeerd. In de ACCP-aanbevelingen wordt wel rekening gehouden met overige (meer subjectieve) overwegingen (bijwerkingen, kosten, gemak voor patiënt), maar dit is niet expliciet terug te vinden; dit komt terug in grootte van het effect (zie punt 2). In de GRADE methodiek worden de overige overwegingen (bijwerkingen, kosten, patiëntenperspectief, expert opinion) gewogen en transparant beschreven, deze overwegingen samen met de wetenschappelijke conclusies leiden tot de aanbevelingen;
- In de ACCP-indeling wordt onderscheid gemaakt tussen een duidelijk klinisch effect (1) en een klein of onduidelijk effect (2), volgens de GRADE-methodiek wordt vooraf benoemde klinische relevantie meegewogen in de gradering van de conclusies.
Formuleren van de conclusies
Voor vragen over de waarde van diagnostische testen, over schade of bijwerkingen, etiologie en prognose is het wetenschappelijke bewijs samengevat in één of meerdere conclusie(s), waarbij het niveau van het meest relevante bewijs is weergegeven.
Bij interventievragen verwijst de conclusie niet naar één of meer artikelen, maar wordt getrokken op basis van alle studies samen (body of evidence). Hierbij maakten de werkgroepleden de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals criteria die van invloed zijn op de aanbeveling, de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen of organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. De richtlijn bevat geen organisatie van zorg hoofdstuk, omdat er over organisatie van zorg en samenwerking binnen de keten reeds documenten bestaan (bijvoorbeeld LSKA 2.0).
Indicatorontwikkeling
Gelijktijdig met het ontwikkelen van de richtlijn werden er interne kwaliteitsindicatoren ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken (de indicatoren zijn te vinden in de aanverwante producten). Meer informatie over de methode van indicatorontwikkeling is op te vragen bij het Kennisinstituut van Medisch Specialisten (secretariaat@kennisinstituut.nl).
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is. Een overzicht van aanbevelingen voor nader/vervolg onderzoek worden toegevoegd na de commentaarfase.
Commentaar- en autorisatiefase
De conceptrichtlijn wordt aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor commentaar. De commentaren worden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren wordt de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn wordt aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor autorisatie en door hen geautoriseerd.
Zoekverantwoording
Zoekverantwoording van systematische review van Huang (2018):
The following search terms, including keyword or entry terms, were used without limitations through September 2017: `arthroscopy OR arthroscopic OR arthroscopicaly' AND `Heparin, Low- Molecular-Weight OR Heparin, Low Molecular Weight OR LMWH OR Low Molecular
Weight Heparin OR Low-Molecular-Weight Heparin'.

