Neuromodulatie
Uitgangsvraag
Wat is de neuromodulatie van keuze bij patiënten met dwangstoornissen en bij welke patiënten wordt dit aanbevolen?
Aanbeveling
rTMS is te overwegen voor bij patiënten met OCS bij wie behandeling met cognitieve gedragstherapie en/of medicatie heeft gefaald (N.B. precieze plaats in het behandelalgoritme is nog te bepalen).
Uitvoering van rTMS vindt bij voorkeur plaats in een in rTMS bij OCS gespecialiseerde behandelsetting, waar ook verder onderzoek gedaan wordt.
Het is te overwegen om DBS aan te bieden als behandeloptie, bij ernstige therapieresistente OCS, dat wil zeggen na onvoldoende effect op gedragstherapie van voldoende duur en intensiteit, meerdere medicatiestappen van voldoende duur en dosering (SSRI, venlafaxine/clomipramine, additie antipsychoticum) en geïntensiveerde CGT. Deze behandeling dient uitgevoerd te worden in een in DBS bij OCS gespecialiseerd centrum waarbij er ook aandacht dient te zijn voor vervolgbehandeling.
Het is te overwegen om lesie-chirurgie aan te bieden als behandelingsoptie, bij ernstige therapieresistente OCS met hoge lijdensdruk, dat wil zeggen na onvoldoende effect op gedragstherapie van voldoende duur en intensiteit, meerdere medicatiestappen van voldoende duur en dosering, (SSRI, venlafaxine/clomipramine, additie antipsychoticum) en geïntensiveerde CGT en na DBS, of indien DBS gecontra-indiceerd of niet gewenst is, of de patiënt een duidelijke voorkeur heeft. Deze behandeling dient uitgevoerd te worden in een in lesie-chirurgie gespecialiseerd centrum waarbij er ook aandacht dient te zijn voor vervolgbehandeling.
Het is aan te bevelen eenduidige en uitgebreide informatie, zowel mondeling alsook schriftelijk, over de verschillende vormen van neuromodulatie te verstrekken aan patiënt en naasten over de te verwachten behandeleffecten, duur van de behandeling, uitvoering, intensiteit, nevenbehandelingen bijvoorbeeld. CGT/medicatie en bijwerkingen op korte en lange termijn.
Wat betreft de afwegingen tussen DBS of lesie-chirurgie is het aan te bevelen de patiënt en naasten actief bij deze overwegingen en keuze te betrekken.
Het is aan te bevelen om bij iedere patiënt die DBS ondergaat op systematische wijze informatie over effect en bijwerkingen van de behandeling te verzamelen tijdens de operatie (1), bij het instellen van de stimulatie (2) en daarna bijvoorbeeld jaarlijks (3).
Hetzelfde wordt aanbevolen voor lesie-chirurgie.
Het is aan te bevelen om bij iedere patiënt die neuromodulatie ondergaat voor, tijdens en na de behandeling de kwaliteit van leven te meten bijvoorbeeld met een visueel analoge schaal (VAS), door de patiënt een cijfer tussen 0 en 10 te laten scoren, of de MHQoL, zodat het effect van de behandeling goed kan worden gevolgd.
Het is aan te bevelen om verder onderzoek te verrichten naar de effecten van rTMS, locaties, frequentie, intensiteit, duur, nevenbehandelingen, alsook onderzoek te verrichten waarbij de effecten, bijwerkingen, bestendigheid en langetermijneffecten van rTMS vergeleken worden met CGT en farmacotherapie.
Overwegingen
Kwaliteit van het bewijs
Voor rTMS is het op basis van het onderzoek waarschijnlijk dat deze vorm van behandeling dwangsymptomen kan verminderen in een patiëntenpopulatie met OCS die niet of onvoldoende op een eerdere behandelstap gereageerd heeft (medicatie en/of gedragstherapie). De bijwerkingen van de behandeling zijn beperkt tot een wat onaangenaam gevoel of hoofdpijn op de plaats van de stimulatie, tijdens de stimulatie. De behandeling is eenvoudig toe te passen in een ambulante setting. Er zijn evenwel ook een aantal onduidelijkheden, zoals waar het beste gestimuleerd kan worden, wat de optimale duur van behandeling is, of combinatie met CGT en/of farmacotherapie de behandelresultaten verbetert en hoe bestendig de resultaten zijn. Vanuit ervaring lijkt rTMS als behandeling wel het meest zinvol indien ingezet als additie aan CGT. Ook is nog niet duidelijk wat de beste plaats in het behandelalgoritme van OCS is, bijvoorbeeld na onsuccesvolle CGT en voor toevoeging van farmacotherapie, of na deze stap. Verder onderzoek zal op al deze vragen antwoord moeten gaan geven.
Op dit moment lijkt het zinvol om rTMS vooral toe te passen volgens behandelprotocollen in rTMS gespecialiseerde behandelpraktijken en op tevoren afgesproken momenten het behandelresultaat te evalueren, evenals de bijwerkingen.
De kwaliteit van het bewijs t.a.v. de effecten van DBS is veelal laag. Een belangrijke reden daarvoor is dat deelnemers en beoordelaars van effecten heel moeilijk geblindeerd kunnen worden en het niet om grote patiëntenaantallen gaat. Hoewel er beperkt wetenschappelijk bewijs is t.a.v. effectiviteit van DBS bij OCS, lijkt DBS te resulteren in een duidelijke vermindering van OCS symptomen, verbetering van kwaliteit van leven in een zeer therapieresistente en geïnvalideerde patiëntenpopulatie met ernstige OCS die niet op diverse andere behandelingen gereageerd heeft (zie ook Alonso et al., 2015, Martinho et al., 2020, Hageman et al., 2021). In het recente overzicht van Hageman et al. (2021) met data van zowel DBS als lesie-chirurgie wordt de effect size “groot” genoemd. In de ‘fixed-and-random effect meta-analyse’ van Alonso et al. (2015) wordt over een periode van 1999-2014 bij totaal 116 patiënten een reductie van 45,1% in de Y-BOCS score gevonden met een responspercentage van 60%. Dit effect is zeer groot in deze zeer therapieresistente en geïnvalideerde patiëntengroep. Een vergelijkbaar groot effect wordt gevonden in de recente meta-analyse van Hageman et al. (2021) bij totaal 253 patiënten die behandeld werden met DBS waarbij het percentage responders (gedefinieerd als 35% of meer reductie op de Y-BOCS score) na 12-16 maanden 53% was en bij laatste follow-up 57%.
Dit rechtvaardigt om DBS, ook al is het een invasieve en intensieve behandeling, toch in het behandelalgoritme als overweging mee te nemen voor de groep patiënten met langdurig bestaande ernstige en therapieresistente OCS met een hoge lijdensdruk en sterk verminderde kwaliteit van leven. Dit betreft ook de groep patiënten die zeer hoog op de Y-BOCS scoren waarbij een kleine verlaging in deze score al een groot effect op het dagelijks leven kan inhouden (zogenaamd ‘ceiling-effect’) en dus een groot klinisch relevant effect heeft. DBS zou dan overwogen kunnen worden vóór lesie-chirurgie, aangezien het irreversibele karakter van deze laatste vorm van behandeling, ook al zijn de kosten van DBS hoger dan die van lesie-chirurgie. De beste locatie voor plaatsing van de elektrodes lijkt niet duidelijk te zijn. De frequentie van stimulatie dient individueel ingesteld te worden. Onduidelijk is of combinatie met CGT en/of farmacotherapie de behandelresultaten verbetert. Vanuit de klinische praktijk zijn er aanwijzingen dat toevoeging van CGT toegevoegde waarde heeft voor het uiteindelijke behandelresultaat. Er zijn vooralsnog geen aanwijzingen dat de effecten van de behandeling na verloop van tijd afnemen. Een praktisch nadeel is de beperkte levensduur van de batterij van de stimulator en de noodzakelijke vervanging na enkele jaren. Bij oplaadbare batterijen zijn de dagelijkse frequentie van opladen en de oplaadduur een nadeel.
Vanwege het belang dat patiënten toekennen aan goede informatie over te verwachten effecten en neveneffecten van DBS zou iedere behandelaar en onderzoeker deze informatie systematisch moeten verzamelen na de operatie (1), tijdens de instellingsperiode van de stimulatie (2) en daarna, bijvoorbeeld jaarlijks (3).
Ook al zijn de onderzoeken beperkt en is het niet mogelijk gerandomiseerd placebo-gecontroleerd dubbelblind onderzoek te doen, de lesie-chirurgische behandelingen via capsulotomie en cingulotomie zijn zeer effectief in het verminderen van dwangsymptomen bij een patiëntengroep met jarenlang bestaande, ernstige en therapieresistente OCS met een hoge lijdensdruk en een sterk verminderde kwaliteit van leven. In de meest recente meta-analyse van Hageman et al. (2021) bij totaal 444 patiënten is het percentage responders (gedefinieerd als 35% of meer reductie op de YBOCS score) 48% na 12-16 mnd en 56% bij laatste follow-up.
Er is geen direct vergelijkend onderzoek gedaan waarbij DBS en lesie-chirurgie vergeleken is. In de recente analyse van Hageman et al. (2021) worden de responspercentages van deze beide vormen van behandeling wel vergeleken en blijken deze niet verschillend van elkaar te zijn (53 vs. 48% na 12-14 mnd en 57 vs. 56% bij laatste follow-up). De bijwerkingen en de ernst daarvan zijn wel verschillend met meer impulsiviteit, meer agitatie, meer des inhibitie, en meer (hypo)mane symptomen in de DBS groep, die na verloop van tijd bij juiste instelling van de stimulatie weer afnemen. Gezien hetzelfde veronderstelde biologisch werkingsmechanisme van DBS en lesie-chirurgie, waarbij bij DBS een functionele onderbreking in bij OCS betrokken hersenbanen wordt gerealiseerd en bij lesie-chirurgie een anatomische onderbreking, zou verwacht kunnen worden dat de effecten van DBS en lesie-chirurgie ongeveer hetzelfde zullen zijn. De analyse van Hageman wijst ook in die richting.
Gezien de andere beschikbare behandelopties, inclusief DBS, wordt deze vorm van behandeling zeer beperkt in Nederland en Europa toegepast. Mogelijk is dit deels onterecht heeft dit te maken met onbekendheid en beperkte beschikbaarheid. De onomkeerbaarheid van de lesie-chirurgie is een belangrijk punt, ter bespreking met de patiënt en naasten. Follow-up onderzoek bij een kleine Nederlandse groep tot enkele jaren na de ingreep laat zien dat het resultaat bij meer dan de helft een duidelijke verbetering van hun functioneren opgeleverd heeft en bestendig is, met minimale bijwerkingen (van Vliet et al. 2013). Ook in de analyse van Hageman et al. (2021) blijkt het effect bij follow-up bestendig aanwezig te zijn.
Balans tussen gewenste en ongewenste effecten
De bijwerkingen van rTMS zijn meestal mild en van voorbijgaande aard en bestaan vaak uit een licht onaangenaam gevoel op de stimulatieplaats en hoofdpijn. Bij stimulatie dichter bij het gezicht kunnen bijwerkingen enigszins onaangenamer worden ervaren. Ernstige bijwerkingen zoals een epileptisch insult lijken zeldzaam. De kans hierop is niet groter bij met rTMS behandelde patiënten dan bij met sham-RTMS behandeld patiënten (0.1% bij rTMS versus 0,2% bij sham-rTMS).
Bij DBS treden bijwerkingen meer frequent op. Meest gerapporteerd zijn operatie-gerelateerde bijwerkingen, zoals intracraniële bloeding 2.6%, hoofdpijn 6%, wondinfectie 4.3%. Direct na de operatie en bij stimulatie kunnen aanwezig zijn: suïcidale gedachten 3.4%, ontremming/manie 19.8%, tijdelijke toename van angstsymptomen 21.6%, depressieve symptomen 4.3%, remming 6%, impulsiviteit 1.7%. De meeste van deze bijwerkingen zijn van voorbijgaande aard zijn en gerelateerd aan het instellen van de stimulatie (Alonso et al., 2015). Over lange termijn bijwerkingen is vooralsnog weinig bekend.
De bijwerkingen van lesie-chirurgie zijn weinig frequent en betreffen een tijdelijke toename van suïcidale gedachten en infectie van de operatiewond (hetgeen verminderd kan worden door preventieve inzet van een antibioticum). Er zijn geen duidelijke aanwijzingen voor persoonlijkheidsveranderingen (iets waar patiënten vaak vrees voor blijken te hebben) op langere termijn.
Bij vergelijking van de bijwerkingen van lesie-chirurgie met die van DBS wordt gevonden dat de aard en de ernst daarvan wel verschillend zijn, met meer impulsiviteit, meer agitatie, meer desinhibitie, en meer (hypo)mane symptomen in de DBS groep, met name in de instellingsfase (Hageman et al., 2021).
Gezien de doelgroep van deze vormen van behandeling, namelijk patiënten met therapieresistente dwangstoornis met een hoge lijdensdruk en sterk geïnvalideerd in hun dagelijks functioneren, lijken de (deels voorbijgaande) bijwerkingen op te wegen tegen de gewenste effecten van de behandeling.
Er is geen onderzoek naar eventuele bijwerkingen op lange termijn maar klinische ervaring wijst niet op grote problemen. Dit dient met de patiënt tevoren besproken te worden.
Neurostimulatie is alleen onderzocht in een volwassenenpopulatie vanaf 18 jaar. DBS en lesie-chirurgie is meest onderzocht bij patiënten van boven de 35 jaar gezien de uitgebreide behandelvoorgeschiedenis.
Patiëntenperspectief
Er is een grote behoefte bij patiënten met een ernstige vorm van OCS aan behandelingen die hun klachten en de lijdensdruk kunnen verminderen en hun kwaliteit van leven kunnen verbeteren. Dit wordt ook ondersteund door hun naasten. Dit geldt zeker voor de meest therapieresistente groep.
In het algemeen is er tevens bij de patiënten met jarenlang bestaande zeer ernstige dwangsymptomen behoefte aan begeleiding om hun leven na behandeling met minder dwangklachten weer invulling te geven. De vermindering van dwangklachten heeft ook effect op bijvoorbeeld de partnerrelatie en het leven voor de gezinsleden dus begeleiding daarbij is ook gewenst.
Een deel van de patiënten wil neuromodulatie pas overwegen bij zeer ernstige klachten die een duidelijke vermindering van hun kwaliteit van leven geven. Daarbij spelen onzekerheid over het te verwachten effect en t.a.v. mogelijke (ernstige) bijwerkingen een belangrijke rol. Goede en eenduidige voorlichting over de kans op effect en de grootte en bestendigheid daarvan, de duur en intensiteit van de behandeling, wel/niet additie van CGT en/of farmacotherapie, de bestaande ervaring met de behandeling, de mogelijke bijwerkingen op korte en lange termijn (bijvoorbeeld risico op gedragsverandering) is essentieel. Behoefte aan uitgebreide en eenduidige voorlichting is er zowel bij patiënten alsook bij hun naasten. De informatie dient zowel mondeling alsook schriftelijk gegeven te worden.
Indien neuromodulatie wordt overwogen heeft rTMS de voorkeur vanwege het niet-invasieve karakter maar de beperkte ervaring met rTMS vinden sommige patiënten wel een hindernis.
Daarnaast hebben sommige patiënten veel weerstand tegen invasieve procedures zoals DBS en vooral lesie-chirurgie (omdat dit een onomkeerbare ingreep is), soms gebaseerd op onjuiste beelden of vooronderstellingen.
Een deel van de patiënten heeft bezwaren tegen de toevoeging van cognitieve gedragstherapie aan de behandeling, vanuit eerdere ervaringen dat CGT een grote toename van hun angsten kan veroorzaken. Extra aandacht daarvoor met ondersteuning en begeleiding is gewenst.
Patiënten vinden het belangrijk dat hun naasten voldoende voorlichting en ondersteuning krijgen voor en tijdens neuromodulatie. Ook wordt gedacht aan het betrekken van naastbetrokkenen bij de CGT.
Professioneel perspectief
Ervaringen met DBS en lesie-chirurgische behandeling bij patiënten met lang bestaande ernstige klachten laten, naast een vermindering van klachten op YBOCS, ook een verbeteringen in sociaal functioneren en kwaliteit van leven zien. Bij de hoge scores op de Y-BOCS wordt dat laatste onvoldoende gemeten (zogenaamde ‘ceiling-effect’). Daarom wordt aanbevolen voor, tijdens en na de behandeling de kwaliteit van leven te meten bijvoorbeeld met een visueel analoge schaal (VAS), door de patiënt een cijfer tussen 0 en 10 te laten scoren, of met een uitgebreidere gevalideerde scoringslijst zoals de Mental Health Quality of Life Questionnaire (MHQol), zodat het effect van de behandeling goed kan worden gevolgd.
Mogelijk wordt er door de professionals te weinig aan behandelingen zoals DBS en lesie-chirurgie gedacht, als behandeloptie voor de zeer ernstig geïnvalideerde groep van therapieresistente depressie, vanwege onbekendheid met de behandeling en de mogelijke effecten, en bijwerkingen.
Middelenbeslag
Omdat lesie-chirurgie een eenmalige behandeling is en DBS meerdere procedures vergt is DBS mogelijk een duurdere behandeling. Voor zover wij weten is er tot op heden geen vergelijkend kosteneffectiviteitsonderzoek verricht. Een kosteneffectiviteitsstudie voor DBS concludeert echter wel dat DBS een kosteneffectieve procedure is voor therapieresistente OCS Moon et al., 2017).
Organisatie van zorg
Gezien de beperkte ervaringen met rTMS, DBS en lesie-chirurgie en de benodigde technische vaardigheden en faciliteiten is het advies dat deze vormen van behandeling alleen in gespecialiseerde settingen plaatsvinden. De komende jaren zal rTMS steeds meer en breder toegepast gaan worden, ook bij andere indicaties dan alleen OCS, waardoor de expertise breder beschikbaar zal zijn. Daarnaast is het wenselijk dat er verder onderzoek naar de effecten, optimalisering van de behandeling en vervolgonderzoek plaats vindt.
DBS en lesie-chirurgie dienen gezien de beperktere doelgroep voor DBS en lesie-chirurgie in hooggespecialiseerde centra plaats te vinden, met name in derdelijnsziekenhuizen en academische centra. Ook hierbij is verder onderzoek essentieel.
Wat betreft de plaats in het behandelalgoritme/stappenplan:
- Van rTMS is de plaats in de behandelvolgorde nog onduidelijk omdat vergelijkende onderzoeken met andere behandelmodaliteiten ontbreken en ook de duur van het effect nog onduidelijk is. Overwogen zou kunnen worden rTMS in te zetten indien CGT alleen of CGT + farmacotherapie onvoldoende effect gehad heeft.
- DBS en lesie-chirurgie dienen overwogen worden bij ernstige therapieresistente OCS waarbij CGT, ook intensief (ambulant of klinisch) toegepast, en farmacotherapie (SSRI, venlafaxine/clomipramine, additie antipsychoticum) onvoldoende verbetering gegeven hebben.
- Gezien het irreversibele karakter van lesie-chirurgie is mogelijk DBS, waarbij een reversibele onderbreking van hersenbanen bewerkstelligd wordt, te prefereren in de behandelvolgorde.
Maatschappelijk perspectief
Gezien de onduidelijkheden die er zijn wat betreft plaats van stimulatie, frequentie en duur is het advies om rTMS is gespecialiseerde behandelcentra met ervaring in rTMS uit te voeren en evaluatie van effect alsook verder onderzoek te verrichten.
Gezien de hooggespecialiseerde behandeling met DBS en lesie-chirurgie is het gewenst dat deze vormen van behandeling in gespecialiseerde, derdelijnsinstellingen/ziekenhuizen uitgevoerd wordt met ervaring in deze behandelingen en er ook follow-up en onderzoek verricht wordt.
Onderbouwing
Huidige praktijk
Definitie en doel van de interventie
- rTMS (Repetitieve Transcraniële Magnetische Stimulatie)
- DBS (Deep brain stimulation)
- Lesie-chirurgie (Ablatie-chirurgie)
Conclusies rTMS
|
ÅÅÅ¡ |
rTMS geeft, vergeleken met sham-rTMS als controle, een vermindering van OCS symptomen (gemiddelde vermindering van 4 punten op YBOCS schaal) waarbij er een brede spreiding in effect is. Fitzsimmons et al., 2022 |
|
|
Er zijn geen systematische reviews gevonden die lange termijn resultaten van rTMS bij OCD rapporteren. |
|
ÅÅ¡¡ |
rTMS lijkt effectief in het verbeteren van OCS symptomen bij het gebruik van hoogfrequente stimulatie van de dlPFC (bilateraal hoog-frequent DLPFC) als target van behandeling. Een hoogfrequente stimulatie van de mediale-prefrontale cortex (hoog-frequent mPFC en ACC) en OFC stimulatie met r-TMS lijken niet effectief. Fitzsimmons et al., 2022 |
|
Å¡¡¡ |
Laagfrequente rTMS van de bilaterale pre-SMA en rechter DLPFC lijken ten opzichte van sham te resulteren in een grote afname van OCS-symptomen, terwijl hoogfrequente rTMS van de rechter dlPFC ten opzichte van sham geen verschil in effect op OCS-symptomen lijken te hebben. De wetenschappelijke evidentie is zeer onzeker. Fitzsimmons et al., 2022 |
|
Å¡¡¡ |
Op basis van de huidige evidentie is het onduidelijk of de effecten van rTMS bij OCS positief worden beïnvloed door gelijktijdige toepassing van CGT en/of medicatie. Fitzsimmons et al., 2022 |
|
Å¡¡¡ |
Op basis van de huidige evidentie is het onduidelijk of de effecten van rTMS bij OCS worden beïnvloed door de mate van therapieresistentie Fitzsimmons et al., 2022 |
|
Å¡¡¡ |
Langdurig aangeboden rTMS (5- 6 weken) lijkt ten opzichte van sham geen verschil in effect te hebben op OCS-symptomen, maar de wetenschappelijke evidentie is zeer onzeker. Perera et al., 2021 |
|
ÅÅÅ¡ |
De kans op milde bijwerkingen lijkt in de rTMS behandelde groep 2.6 maal zo groot te zijn als in de sham-rTMS groep. Ernstige bijwerkingen lijken zeldzaam en de kans hierop is niet groter bij met rTMS behandelde patiënten. De kans op een epileptische aanval lijkt niet groter met rTMS (circa 0.1% vgl. 0.2% bij sham-rTMS). Zis et al., 2019 |
|
ÅÅÅ¡ |
rTMS lijkt bij circa 10% van de patiënten in tijdelijk ongemak of hoofdpijn ter plaatse van de stimulatie te resulteren. Zis et al., 2019 |
|
ÅÅÅ¡ |
De kans dat een patiënt met rTMS stopt met de behandeling vanwege een bijwerking lijkt circa 2.5%, en is vergelijkbaar met wat gezien werd bij behandeling met sham-rTMS (2.7%). Zis et al., 2019 |
Conclusies DBS
|
ÅÅΟΟ |
DBS lijkt de Y-BOCS score te verminderen met een gemiddelde afname van 7,8 punten. Martinho et al., 2020 |
|
ÅÅΟΟ |
DBS lijkt de kans op respons ((Y-BOCS verbetering > 35%) te verhogen. NNT: 3, Martinho et al., 2020 |
|
ÅÅΟΟ |
DBS lijkt de kans op remissie (Y-BOCS score<6) 1,3 maal te verhogen. Martinho et al., 2020 |
|
ÅÅΟΟ |
De kans op wondinfectie lijkt bij DBS circa 5% te bedragen. Deze kans lijkt verkleind te kunnen worden door preventief lokaal gebruik van een antibioticum (vancomycine) naast systemische profylaxe. Kantzanou et al., 2021 |
|
ÅΟΟΟ |
De evidentie is zeer onzeker over het effect van DBS op andere bijwerkingen. Martinho et al., 2020 |
|
ÅΟΟΟ |
De evidentie is zeer onzeker over het effect van DBS op ernstige bijwerkingen. Martinho et al., 2020 |
|
ÅΟΟΟ |
De evidentie is zeer onzeker over het effect van DBS op voortijdig stoppen met de behandeling. Martinho et al., 2020 |
Conclusies Lesie-chirurgie
|
ÅÅΟΟ |
Lesie-chirurgie lijkt bij therapieresistente patiënten met OCS te kunnen resulteren in een grote vermindering van de ernst van OCS. Lai et al., 2020 |
|
ÅΟΟΟ |
Het is onduidelijk of Lesie-chirurgie een verhoogde kans geeft op wondinfecties of suïcidale gedachten. Lai et al., 2020 |
|
|
Er is geen informatie over het effect op functioneel herstel, kwaliteit van leven en werkhervatting |
Resultaten rTMS
Er werd gebruik gemaakt van een Nederlandse systematische review, die van hoge kwaliteit is en de meest complete en meest recente review (Fitzsimmons et al., 2022). Drie andere recente systematische reviews werden niet verder besproken vanwege de overlap met Fitzsimmons et al en de overeenkomstige bevindingen. Alleen de lange termijn resultaten , die door 1 review werden gerapporteerd, zijn toegevoegd (Perera et al., 2021). In de Nederlandse studie zijn de resultaten beschreven van 21 placebo-gecontroleerde RCT’s (n=662) naar het effect van rTMS bij patiënten met OCS (search tot februari 2021). Verschillende vormen van rTMS (met tenminste 5 behandelsessies) met of zonder adjuvante/add-on behandeling (farmacotherapie en/of CGT) werden meegenomen (Fitzsimmons et al., 2022). De patiëntenpopulatie in 18 van de 21 studies (86%) betrof (therapieresistente) patiënten. In bijna alle RCT’s (20/21) ontvingen de patiënten een additionele (meest medicamenteuze) behandeling naast rTMS en in 2 RCT’s werd ook psychotherapie gegeven. De gemiddelde leeftijd varieerde tussen de 26 en 42 jaar. De Y-BOCS varieerde tussen de 25 en 33. De primaire uitkomst was het effect op de Y-BOCS schaal. De patiënten in de geïncludeerde studies ontvingen minimaal 10 rTMS sessies gedurende een periode van minimaal 2 weken.
In de primaire meta-analyse verbeterden de dwangsymptomen gemeten met de Y-BOCS score meer op actieve rTMS dan op placebo rTMS (Hedges’ g=-0.502 (95%CI=-0.708 -0.296). Dit komt overeen met een toegenomen verbetering van gemiddeld 4 punten op de Y-BOCS bij toepassing van rTMS vergeleken met placebo rTMS, met een grote spreiding.
Klinische moderatoren
Subgroepanalyses lieten geen ander effect zien bij gelijktijdige psychotherapie (5 studies met psychotherapie, 17 studies zonder; Subgroep analyse: p = 0.994) of t.a.v. de aanwezigheid van therapieresistentie (17 studies met therapieresistentie en 5 zonder restricties op dat gebied; subgroepanalyse: p=0.5068).
Secundaire uitkomsten
Voortijdig gestopt met de behandeling uit de studie (indicator voor verdraagbaarheid) verschilde niet tussen rTMS en placebo rTMS (OR=0.906, 95%-CI=(0.452, 1.815).
Bijwerkingen werden niet consistent gerapporteerd in de ingesloten studies. Gerapporteerde bijwerkingen waren: hoofdpijn, slaperigheid, concentratieverlies, pijn aan de schedel, zwakte, vermoeidheid, stemmingswisselingen, geheugenverlies, duizeligheid, flauwvallen, stimulatie aangezichtszenuw. Geen enkele studie rapporteerde ernstige bijwerkingen.
Netwerk meta-analyse naar het effect van target gebied
In de netwerk meta-analyse werden de studies op basis van het anatomische target gebied gegroepeerd in 3 groepen: 1. Mediale prefrontale cortex (mPFC) (inclusief preSMA en mPFC/ACC stimulatie); 2. Dorsolaterale prefrontal cortex (omvattende bilaterale, linker en rechter dlPFC stimulatie); en 3. orbitofrontale cortex (OFC; stimulatie links en rechts). Uit de resultaten van deze analyse blijkt dat dlPFC (SMD -0.67; CI -0.30, -1.04) en mediale prefrontale cortex stimulatie (SMD -0.143; CI -0.14, -0.71) betere resultaten geven dan sham stimulatie, maar dat geldt niet voor OFC stimulatie (SMD -0.53; CI -1.31, 0.25). Het was echter niet mogelijk om op basis van deze analyses een definitieve locatie of frequentie van voorkeur vast te stellen. De meeste ervaring en het smalste betrouwbaarheidsinterval bestaat voor dorsomediale (waaronder pre-SMA) stimulatie.
Lange termijn resultaten
Fitzsimmons et al. rapporteerde alleen de uitkomsten (Y-BOCS na afloop van de behandeling. Een andere systematische review, met vergelijkbare primaire uitkomsten, rapporteerde ook uitkomsten op de langere termijn (Perera et al., 2021), waarbij de verandering in Y-BOCS score werd gekozen als de uitkomstparameter. Een vrij groot effect werd waargenomen bij een follow-up van 1-2 weken (Hedges g 0.70; CI 0.30, 1.10; 11 studies). Een matig effect werd 3-4 weken na behandeling gerapporteerd (g 0.47; CI 0.17, 0.76; 9 studies) en 5-6 weken na behadeling werd geen duidelijk effect meer waargenomen (Hedges g 1.45; CI -0.17, 3.06; 6 studies).
Grade tabel rTMS versus sham voor OCS, is te vinden in Bijlage 3, sectie 3.9, tabel 2.
Perera2021
Door middel van een systematische review met meta-analyse hebben Perera en collega’s (2021) onderzoek gedaan naar de effectiviteit van rTMS voor de behandeling van OCS. In totaal zijn 26 studies meegenomen, waaraan 781 deelnemers (actief = 413, gemiddelde leeftijd = 33.35 jaar [SD = 4.69]; sham = 368, gemiddelde leeftijd = 33.86 jaar [SD = 9.36]) met een DSM-IV diagnose van OCS hebben deelgenomen. Zes RCT’s (n = 219) die zijn meegenomen in de meta-analyse, hebben het effect van langdurig (5 tot 6 weken) aangeboden rTMS op OCS-symptomen gemeten. Zie tabel 3. voor informatie over de geïncludeerde RCT’s en tabel 4. voor de rTMS parameters. Symptomen zijn gemeten door middel van de Y-BOCS. Voor 5 tot 6 weken aangeboden rTMS leek ten opzichte van sham niet te resulteren in een verschil in effect op OCS-symptomen (zie Bijlage 3, sectie 3.9, tabel 5 voor een overzicht van de vergelijking en bijhorende grading).
Tabel 3 Kenmerken van de patiëntenpopulatie van de geïncludeerde RCT’s gericht op langdurig aangeboden rTMS in Perera et al (2021)
|
Trial ID |
N |
% vrouw |
Gem. leeftijd in jaren (actief / sham) |
Therapieresistent |
|
Harika-Germaneau2019 |
28 |
53.6 |
46.3 / 48.2 |
Ja |
|
Carmi2019 |
94 |
58.5 |
41.1 / 36.5 |
Ja |
|
Carmi2018 |
30 |
46.7 |
36 / 35 |
Ja |
|
Hawken2016 |
22 |
NR |
33 / 31 |
NR |
|
Mansur2011 |
27 |
51.9 |
42.1 / 39.3 |
Ja |
|
Alonso2001 |
18 |
66.7 |
39.2 / 30.3 |
Ja |
Tabel 4 rTMS parameters van de geïncludeerde RCT’s gericht op langdurig aangeboden rTMS in Perera et al (2021)
|
Trial ID |
Stimulatiegebied |
Duur |
Sessies |
Frequentie (Hz) |
Totaal pulsen |
TPPS |
|
Harika-Germaneau2019 |
SMA |
6 weken |
30 |
50 (TBS) |
18,000 |
600 |
|
Carmi2019 |
m-PFC |
6 weken |
29 |
20 |
58,000 |
2000 |
|
Carmi2018 |
m-PFC |
5 weken |
25 |
20 |
50,000 |
2000 |
|
Hawken2016 |
SMA |
6 weken |
25 |
1 |
NR |
NR |
|
Mansur2011 |
R-DLPFC |
6 weken |
30 |
10 |
60,000 |
2000 |
|
Alonso2001 |
R-DLPFC |
6 weken |
18 |
1 |
21,600 |
1200 |
Bijwerkingen en voortijdig stoppen met de behandeling
In een aanvullende search werd 1 review gevonden, waarin bijwerkingen van rTMS werden vergeleken met die gerapporteerd in de controlegroep. Zis et al (2019) rapporteerden veiligheid en verdraagbaarheid van 2290 met rTMS en 1854 met placebo in 93 placebo gecontroleerde RCT’s behandelde patiënten. In deze review werden studies geïncludeerd waarin rTMS werd gebruikt bij diverse psychiatrische aandoeningen, waarbij depressie de meest voorkomende aandoening was en 4 RCT’s patiënten met OCS betroffen (Zis et al., 2019).
De gepoolde effectschatting van het percentage patiënten dat de behandeling niet afmaakte was 9.1% (95% CI 7.9%-10.3%) voor rTMS en voor placebo 9.4% (95% CI 8.1%-10.9%).
De gepoolde effectschatting van het percentage patiënten dat de behandeling niet afmaakte vanwege een bijwerking was 2.5% (95% CI 1.9%-3.2%) en voor placebo 2.7% (95% CI 2.0%-3.5%). De gepoolde effectschatting van het percentage patiënten met tenminste 1 bijwerking was 29.3% (95% CI 19.0%-22.6%) in de rTMS groep en 13.6% (95% CI 11.6%-15.8%) voor de placebogroep. De kans op een bijwerking was 2.6 maal groter met rTMS dan met placebo (odds ratio 2.60; 95% CI 1.75-3.86).
De meest voorkomende bijwerking was ongemak/hoofdpijn op de plek van stimulatie (10.1% (95% CI 8.4%-12.0%) en dit kwam vaker voor in de rTMS groep dan de placebo groep (odds ratio 2.19 (95% CI 1.52-3.14). Epileptische aanvallen waren zeer zeldzaam (0.1% in de rTMS groep en 0.2% in de placebo groep).
Kwaliteit van bewijs
Kwaliteit van de evidentie werd door Fitzsimmons et al (2022) beoordeeld met behulp van GRADE en een gemodificeerde versie van de Cochrane Risk of Bias tool (Sterne et al., 2019). Vier van de 21 studies vertoonden een hoog risico op bias. Een sensitiviteitsanalyse zonder deze 4 studies leverde echter een vergelijkbaar resultaat op (Hedges’ g=0.546 [95%CI=-0.793 -0.299]).
De ‘safety review’ van Zis et al (2019) was van redelijk goede kwaliteit. Daarom is de zekerheid van bewijs omlaag gegradeerd voor de kans op vertekening als gevolg van onvolledige rapportage. Een punt van aandacht is de heterogeniteit in de geïncludeerde patiëntenpopulatie, die maar in een klein deel patiënten met OCS betrof. T.a.v. TMS-specifieke bijwerkingen verwacht de richtlijnencommissie geen verschil tussen depressie en OCS. Voor de bijwerkingen maakt het uit of hoog of laag-frequent gestimuleerd wordt (bij hoog-frequent vaak meer bijwerkingen) en of wel/niet dichtbij het gezicht gestimuleerd wordt (bij DLPFC daardoor meer bijwerkingen geeft dan pre-SMA).
Lange termijn effecten
Gegevens over lange termijn effecten van rTMS ontbreken uit de gevonden onderzoeken.
Resultaten Deep brain stimulation (DBS)
De systematische review van Martinho et al., (2020) presenteerde een meta-analyse voor het gemiddelde verschil in Y-BOCS-score voor actieve stimulatie versus sham behandeling. Voor deze richtlijn is besloten daarom de resultaten hiervan weer te geven en te beoordelen op kwaliteit. In deze meta-analyse werden 85 patiënten opgenomen die deelnamen in 8 RCT’s. Informatie over de geïncludeerde RCT’s is gepresenteerd in tabel 6. In tabel 7 staan de kenmerken van de interventie voor de verschillende RCT’s uitgelicht. Het betreft patiënten met een ernstige OCS, lange ziekteduur en therapieresistentie.
Tabel 6. Kenmerken van de patiëntenpopulatie van de geïncludeerde RCT’s in Martinho et al (2020).
|
Trial ID |
n |
% vrouw |
Gem. leeftijd (jaren) |
Gemiddelde duur van ziekte (jaren) |
Gemiddelde follow-up (maanden) |
|
Abelson2005 |
4 |
50 |
40,3 |
22,5 |
12,9 |
|
Denys2010 |
16 |
44 |
43 |
28,4 |
21 |
|
Goodman2010 |
6 |
50 |
35,2 |
16,8 |
11,4 |
|
Huff2010 |
10 |
40 |
36,3 |
22,2 |
12 |
|
Luyten2016 |
24 |
12 |
40,6 |
NR |
77 |
|
Mallet2008 |
17 |
41 |
43,1 |
29,5 |
10 |
|
Nuttin2003 |
8 |
NR |
NR |
NR |
18,8 |
|
Schuurman2011 |
16 |
NR |
NR |
NR |
21 |
|
NR; niet gerapporteerd |
|||||
Tabel 7. Kenmerken van de procedure in de geïncludeerde RCT’s in Martinho et al (2020).
|
Trial ID |
Stimulatie-gebied |
Zijde van stimulatie |
Gemiddelde frequentie |
Gemiddelde puls breedte |
Gemiddeld voltage |
|
Abelson2005 |
ALIC |
Bilateraal |
125 |
172,5 |
7,4 |
|
Denys2010 |
NAcc |
Bilateraal |
123 |
180 |
4,7 |
|
Goodman2010 |
VC/VS |
Bilateraal |
133 |
165 |
5,1 |
|
Huff2010 |
ALIC/NAcc |
Rechts |
145 |
90 |
5,5 |
|
Luyten2016 |
ALIC/BST |
Bilateraal |
115 |
270 |
6,4 |
|
Mallet2008 |
STN |
Bilateraal |
130 |
60 |
NR |
|
Nuttin2003 |
ALIC |
Bilateraal |
100 |
247 |
6,1 |
|
Schuurman2011 |
NAcc |
Bilateraal |
NR |
NR |
NR |
|
ALIC; anterior limb of internal capsule, BST; bed nucleus of stria terminalis, NAcc; nucleus accumbens NR; niet gerapporteerd, STN; subthalamic nucleus, VC/VS; ventral caudate/ventral striatum. |
|||||
In de studie van Martinho werden acht RCT’s meegenomen. Resultaten per uitkomst zijn gepresenteerd in de ‘summary of findings’ tabel 8 (zie bijlage Evidence tabellen). De conclusies over (serieuze) bijwerkingen en voortijdig stoppen met de behandeling zijn gebaseerd op observationeel onderzoek, bij gebrek aan deze informatie uit RCT’s. Het placebo-effect, zoals beoordeeld tijdens de instelfase van de stimulatie is laag; patiënten merken direct of er wel of niet gestimuleerd wordt. In een onderzoek van Schruers et al. (2019) is op individuele patiëntgegevens een placebo-effect bij de eerste stimulatie van 14,9%, ofwel een daling van 4.9 op de Y-BOCS score gevonden.
Stimulatie
Grade tabel Actieve stimulatie versus Sham Stimulatie voor OCS, is te vinden in bijlage Evidence tabellen, tabel 8.
Veiligheid en verdraagbaarheid van DBS
De kans op een bijwerking was 68% (95% BI 59%-78%) en bijwerkingen waren deels tijdelijk van aard. De kans op een ernstige bijwerking was 32% (95% BI 12%-52% en de kans op niet afmaken van de behandeling was 13% (95% CI 7-16%). De meest voorkomende psychiatrische bijwerkingen waren hypomanie, slaapproblemen, prikkelbaarheid, apathie en depressie. De meest voorkomende lichamelijke bijwerkingen waren gewichtsverandering, seksuele klachten, maagdarmklachten, tintelingen, etc. N.B. De frequentie per type bijwerking is niet gerapporteerd. De relatie met voortijdig stoppen met de behandeling is evenmin gerapporteerd.
Vanwege het beperkte wetenschappelijk bewijs t.a.v. veiligheid en aanvaardbaarheid werden aanvullende studies gezocht t.a.v. deze uitkomsten. Kantzanou et al. 2021 onderzochten de prevalentie van wondinfecties bij DBS. Onder 12258 patiënten die deelnamen aan 66 studies (RCT’s en observationele studies) bij wie DBS werd toegepast bij een reeks van indicaties zoals epilepsie, bewegingsstoornissen en OCS, werd een prevalentie van 5.0% (95% CI: 4.0%–6.0%) gevonden. Er waren geen aanwijzingen dat de prevalentie sterk verschilde tussen de verschillende indicaties voor DBS. In elf studies werd het effect van preventieve interventies onderzocht. In twee daarvan werd de waarde van perioperatieve lokale applicatie van het antibioticum vancomycine onderzocht (in aanvulling op systemische antibioticaprofylaxe). Dit leek het risico op infectie te verlagen (summary odds ratio [sOR]: 0.26, 95% CI: 0.09–0.74) (Kantzanou et al. 2021).
Lesie-chirurgie/Ablatie-chirurgie
In een systematische review met meta-analyse bekeken Lai et al. (2020) het effect van verschillende typen lesie-chirurgie/ablatie-chirugie bij patiënten met een ernstige en therapieresistente dwangstoornis (OCS). Er werden 23 studies (merendeel single arm en één RCT) geïncludeerd met 487 patiënten (range gemiddelde leeftijd 28,9-46,3 jaar; range gemiddelde duur OCS 4-24 jaar). De meest onderzochte type lesie-chirurgie was capsulotomie (16 studies, N=343), gevolgd door cingulotomie (3 studies, N=62). In de meeste studies werd de procedure eenmalig toegepast (N=21) in de andere werd de procedure herhaald. Ook subcaudate tractotomie is onderzocht , maar om verschillende redenen (geen relevante uitkomst of samen met een ander type interventie toegepast) niet meegenomen in de analyse. In bijlage Evidence tabellen, tabel 10 staan de resultaten van de meta-analyse.
Zoekstrategie/ review protocol
PICO (review protocol is opgenomen in bijlagen)
|
Patient/Population (P) |
Patiënten met OCS |
|
Intervention (I) |
Neuromodulatie beperkt tot:
|
|
Comparator/Control (C) |
|
|
Outcome (O) |
Belangrijk:
|
Geïncludeerde en geëxcludeerde studies
De literatuur search (Is opvraagbaar, neem hiervoor contact op met de Richtlijnendatabase.) leverde 491 artikelen op t.a.v. de effecten van neuromodulatie bij OCS. Daarvan werden 50 artikelen full tekst beoordeeld. Redenen voor exclusie in deze stap zijn weergegeven in tabel 1. De aanvullende search naar bijwerkingen leverde 47 artikelen op. Daarvan werden 3 artikelen full tekst beoordeeld.
Tabel 1 Redenen voor exclusie van artikelen
|
Reden van exclusie |
aantal |
|
effectstudies |
|
|
geen meta-analyse uitgevoerd |
4 |
|
niet systematische review |
19 |
|
search slechts in 1 database |
1 |
|
selectiecriteria onduidelijk |
10 |
|
verkeerde interventie |
2 |
|
verkeerde onderzoeksvraag |
2 |
|
verkeerde populatie |
3 |
|
verkeerde studie design |
3 |
|
geen meta-analyse uitgevoerd |
4 |
|
|
|
|
Bijwerkingen |
|
|
Geen resultaten voor neuromodulatie |
1 |
- Abelson, J. L., Curtis, G. C., Sagher, O., Albucher, R. C., Harrigan, M., Taylor, S. F., Martis, B., & Giordani, B. (2005). Deep brain stimulation for refractory obsessive-compulsive disorder. Biological Psychiatry, 57(5), 510-516. doi:org/10.1016/j.biopsych.2004.11.042
- Alonso, P., Pujol, J., Cardoner, N., Benlloch, L., Deus, J., Menchón, J. M., Capdevila, A., & Vallejo, J. (2001). Right prefrontal repetitive transcranial magnetic stimulation in obsessive-compulsive disorder: A double-blind, placebo-controlled study. American Journal of Psychiatry, 158(7), 1143-1145. doi:10.1176/appi.ajp.158.7.1143
- Alonso, Pino, Cuadras, D., Gabriëls, L., Denys, D., Goodman, W., Greenberg, B. D., Jimenez-Ponce, F., Kuhn, J., Lenartz, D., Mallet, L., Nuttin, B., Real, E., Segalas, C., Schuurman, R., Du Montcel, S. T., & Menchon, J. M. (2015). Deep brain stimulation for obsessive-compulsive disorder: A meta-analysis of treatment outcome and predictors of response. PLoS ONE, 10(7), 1-16. doi :10.1371/journal.pone.0133591
- Carmi L, Tendler A, Bystritsky A, Hollander E, Blumberger DM, Daskalakis J, et al. (2019). Efficacy and safety of deep transcranial magnetic stimulation for obsessive-compulsive disorder: A prospec- tive multicenter randomized double-blind placebo-controlled trial. Am J Psychiatry, 176, 931-938.
- Carmi, L., Alyagon, U., Barnea-Ygael, N., Zohar, J., Dar, R., & Zangen, A. (2018). Clinical and electrophysiological outcomes of deep TMS over the medial prefrontal and anterior cingulate cortices in OCD patients. Brain Stimulation, 11(1), 158-165. doi:10.1016/j.brs.2017.09.004
- Denys, D., Mantione, M., Figee, M., Van Den Munckhof, P., Koerselman, F., Westenberg, H., Bosch, A., & Schuurman, R. (2010). Deep brain stimulation of the nucleus accumbens for treatment-refractory obsessive-compulsive disorder. Archives of General Psychiatry, 67(10), 1061-1068. doi:10.1001/archgenpsychiatry.2010.122
- Fitzsimmons, S. M. D. D., van der Werf, Y. D., van Campen, A. D., Arns, M., Sack, A. T., Hoogendoorn, A. W., van Balkom, A. J. L. M., Batelaan, N. M., Eijndhoven, P. van, Hendriks, G. J., Oostrom, I. van, Oppena, P. van, Schruers, K. R. J., Tendolkar, I., Vriend, C., & van den Heuvel, O. A. (2022). Repetitive transcranial magnetic stimulation for obsessive-compulsive disorder: A systematic review and pairwise/network meta-analysis. Journal of Affective Disorders, 302, 302-312. doi:org/10.1016/j.jad.2022.01.048
- Goodman, W. K., Foote, K. D., Greenberg, B. D., Ricciuti, N., Bauer, R., Ward, H., Shapira, N. A., Wu, S. S., Hill, C. L., Rasmussen, S. A., & Okun, M. S. (2010). Deep Brain Stimulation for Intractable Obsessive Compulsive Disorder: Pilot Study Using a Blinded, Staggered-Onset Design. Biological Psychiatry, 67(6), 535-542. doi:org/10.1016/j.biopsych.2009.11.028
- Hageman, S. B., van Rooijen, G., Bergfeld, I. O., Schirmbeck, F., de Koning, P., Schuurman, P. R., & Denys, D. (2021). Deep brain stimulation versus ablative surgery for treatment-refractory obsessive-compulsive disorder: A meta-analysis. Acta Psychiatrica Scandinavica, 143(4), 307-318. doi:10.1111/acps.13276
- Harika-Germaneau, G., Rachid, F., Chatard, A., Lafay-Chebassier, C., Solinas, M., Thirioux, B., Millet, B., Langbour, N., & Jaafari, N. (2019). Continuous theta burst stimulation over the supplementary motor area in refractory obsessive-compulsive disorder treatment: A randomized sham-controlled trial. Brain Stimulation, 12(6), 1565-1571. doi:10.1016/j.brs.2019.07.019
- Hawken, E. R., Dilkov, D., Kaludiev, E., Simek, S., Zhang, F., & Milev, R. (2016). Transcranial magnetic stimulation of the supplementary motor area in the treatment of obsessive-compulsive disorder: A multi-site study. International Journal of Molecular Sciences, 17(3). https://doi.org/10.3390/ijms17030420
- Huff, W., Lenartz, D., Schormann, M., Lee, S. H., Kuhn, J., Koulousakis, A., Mai, J., Daumann, J., Maarouf, M., Klosterkötter, J., & Sturm, V. (2010). Unilateral deep brain stimulation of the nucleus accumbens in patients with treatment-resistant obsessive-compulsive disorder: Outcomes after one year. Clinical Neurology and Neurosurgery, 112(2), 137-143. doi:10.1016/j.clineuro.2009.11.006
- Kantzanou, M., Korfias, S., Panourias, I., Sakas, D. E., & Karalexi, M. A. (2021). Deep Brain Stimulation-Related Surgical Site Infections: A Systematic Review and Meta-Analysis. Neuromodulation, 24(2), 197-211. doi:10.1111/ner.13354
- Lai, Y., Wang, T., Zhang, C., Lin, G., Voon, V., Chang, J., & Sun, B. (2020). Effectiveness and safety of neuroablation for severe and treatment-resistant obsessivecompulsive disorder: A systematic review and meta-analysis. Journal of Psychiatry and Neuroscience, 45(5), 356-369. doi:10.1503/jpn.190079
- Luyten, L., Hendrickx, S., Raymaekers, S., Gabriëls, L., & Nuttin, B. (2016). Electrical stimulation in the bed nucleus of the stria terminalis alleviates severe obsessive-compulsive disorder. Molecular Psychiatry, 21(9), 1272-1280. doi:10.1038/mp.2015.124
- Mallet, L., Polosan, M., Jaafari, N., Baup, N., Welter, M.-L., Fontaine, D., Montcel, S. T. du, Yelnik, J., Chéreau, I., Arbus, C., Raoul, S., Aouizerate, B., Damier, P., Chabardès, S., Czernecki, V., Ardouin, C., Krebs, M.-O., Bardinet, E., Chaynes, P., Pelissolo, A. (2008). Subthalamic Nucleus Stimulation in Severe ObsessiveCompulsive Disorder. New England Journal of Medicine, 359(20), 2121-2134. doi:10.1056/nejmoa0708514
- Mansur, C. G., Myczkowki, M. L., De Barros Cabral, S., Sartorelli, M. D. C. B., Bellini, B. B., Dias, Á. M. H., Bernik, M. A., & Marcolin, M. A. (2011). Placebo effect after prefrontal magnetic stimulation in the treatment of resistant obsessive-compulsive disorder: A randomized controlled trial. International Journal of Neuropsychopharmacology, 14(10), 1389-1397. doi:10.1017/S1461145711000575
- Martinho, F. P., Duarte, G. S., & do Couto, F. S. (2020). Efficacy, effect on mood symptoms, and safety of deep brain stimulation in refractory obsessive-compulsive disorder: a systematic review and meta-analysis. The Journal of Clinical Psychiatry, 81(3)(February).
- Moon, W., Kim, S. N., Park, S., Paek, S. H., & Kwon, J. S. (2017). The cost-effectiveness of deep brain stimulation for patients with treatment-resistant obsessive-compulsive disorder. Medicine (United States), 96(27), 1-8. doi:10.1097/MD.0000000000007397
- Nuttin, B. J., Gabriels, L., Van Kuyck, K., & Cosyns, P. (2003). Electrical stimulation of the anterior limbs of the internal capsules in patients with severe obsessive-compulsive disorder: Anecdotal reports. Neurosurgery Clinics of North America, 14(2), 267-274. doi:10.1016/S1042-3680(02)00117-1
- Perera, M. P. N., Mallawaarachchi, S., Miljevic, A., Bailey, N. W., Herring, S. E., & Fitzgerald, P. B. (2021). Repetitive Transcranial Magnetic Stimulation for Obsessive-Compulsive Disorder: A Meta-analysis of Randomized, Sham-Controlled Trials. Biological Psychiatry: Cognitive Neuroscience and Neuroimaging, 6(10), 947-960. doi:10.1016/j.bpsc.2021.03.010
- Schruers, K., Baldi, S., van den Heuvel, T., Goossens, L., Luyten, L., Leentjens, A. F. G., Ackermans, L., Temel, Y., & Viechtbauer, W. (2019). The effects of deep-brain non-stimulation in severe obsessive-compulsive disorder: an individual patient data meta-analysis. Translational Psychiatry, 9(1). doi:10.1038/s41398-019-0522-6
- Schuurman, P.R., Munckhof, P., Denys, D., et al. (2011). Deep brain stimulation in obsessive compulsive disorder: double-blind crossover study. Acta Neurochir (Wien), 153(3), 729-730.
- Sterne, J. A. C., Savovi?, J., Page, M. J., Elbers, R. G., Blencowe, N. S., Boutron, I., Cates, C. J., Cheng, H. Y., Corbett, M. S., Eldridge, S. M., Emberson, J. R., Hernán, M. A., Hopewell, S., Hróbjartsson, A., Junqueira, D. R., Jüni, P., Kirkham, J. J., Lasserson, T., Li, T., Higgins, J. P. T. (2019). RoB 2: A revised tool for assessing risk of bias in randomised trials. The BMJ, 366, 1-8. doi:10.1136/bmj.l4898
- Van Vliet, I.M., van Well, E.P., Bruggeman, R., Campo, J.A., Hijman, R., van Megen, H.J., van Balkom, A.J., van Rijen, P.C. (2013). An evaluation of irreversible psychosurgical treatment of patients with obsessive-compulsive disorder in the Netherlands, 2001-2008. J Nerv Ment Dis, 201(3). 226-8, doi: 10.1097/NMD.0b013e3182848b15.
- Zis, P., Shafique, F., Hadjivassiliou, M., Blackburn, D., Venneri, A., Iliodromiti, S., Mitsikostas, D. D., & Sarrigiannis, P. G. (2019). Safety, Tolerability, and Nocebo Phenomena During Transcranial Magnetic Stimulation: A Systematic Review and Meta-Analysis of Placebo-Controlled Clinical Trials. Neuromodulation, 23(3), 291-300. doi:10.1111/ner.12946
Tabel 2 Symptomatisch herstel voor OCS: rTMS versus sham (Perera 2021)
|
Interventie |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Zekerheid evidentie |
Opmerkingen |
|
|
Risico met sham |
Risico met rTMS |
|||||
|
Alle studies |
- |
SMD 0.5 SD lager |
- |
662 |
⨁⨁⨁◯ |
rTMS resulteert ten opzichte van sham waarschijnlijk in een grote afname van OCS-symptomen. |
|
bilaterale dlPFC, HF |
- |
SMD 0.91 SD lager |
- |
41 |
⨁⨁◯◯ |
Hoogfrequente rTMS van de bilaterale dlPFC lijkt ten opzichte van sham te resulteren in een grote afname van OCS-symptomen. |
|
bilaterale pre SMA, LF |
- |
SMD 0.57 SD lager |
- |
183 |
⨁◯◯◯ |
Laagfrequente rTMS van de bilaterale pre-SMA lijkt ten opzichte van sham te resulteren in een grote afname van OCS-symptomen, maar de wetenschappelijke evidentie is zeer onzeker. |
|
mPFC/ACC, HF |
- |
SMD 0.4 SD lager |
- |
117 |
⨁⨁◯◯ |
Hoogfrequente rTMS van de mPFC en ACC lijkt ten opzichte van sham geen verschil in effect op OCS-symptomen te hebben. |
|
rdlPFC, HF |
- |
SMD 0.38 SD lager |
- |
49 |
⨁◯◯◯ |
Hoogfrequente rTMS van de rechter dlPFC lijkt ten opzichte van sham geen verschil in effect op OCS-symptomen te hebben, maar de wetenschappelijke evidentie is zeer onzeker. |
|
rdlPFC, LF |
- |
SMD 1.03 SD lager |
- |
49 |
⨁⨁◯◯ |
Laagfrequente rTMS van de rechter dlPFC lijkt ten opzichte van sham te resulteren in een grote afname van OCS-symptomen, maar de wetenschappelijke evidentie is zeer onzeker. |
a Publicatie bias: sterk vermoeden
b Onnauwkeurigheid: effectschatting gebaseerd op <200 deelnemers in totaal
c Kans op vertekening: 1 studie met hoog risico op bias vanwege non-ITT analyse
d Onnauwkeurigheid: betrouwbaarheidsinterval doorkruist het gebied van klinisch niet relevant effect
e Onnauwkeurigheid: betrouwbaarheidsinterval is in zowel het voor- als nadeel van de interventie
Tabel 5 rTMS ( voor 5-6 weken aangeboden) versus sham voor OCS (Perera 2021)
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Zekerheid evidentie |
Opmerkingen |
|
|
Risico met sham |
Risico met rTMS ( voor 5-6 weken aangeboden) |
|||||
|
OCS-symptomen |
- |
SMD 1.45 SD hoger |
- |
219 |
⨁◯◯◯ |
Langdurig aangeboden rTMS lijkt ten opzichte van sham geen verschil in effect te hebben op OCS-symptomen, maar de wetenschappelijke evidentie is zeer onzeker. |
a Heterogeniteit: I2 = 95.7%
b Onnauwkeurigheid: effectschatting gebaseerd op <400 deelnemers totaal
c Onnauwkeurigheid: betrouwbaarheidsinterval is in zowel het voor- als nadeel van de interventie
d Publicatiebias: sterk vermoeden van publicatiebias
Tabel 8 Actieve stimulatie versus Sham Stimulatie voor OCS (Martinho 2020)
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Zekerheid evidentie |
Opmerkingen |
|
|
Risico met Sham Stimulatie |
Risico met Actieve stimulatie |
|||||
|
Afname in Y-BOCS score |
- |
MD 7.8 lager |
- |
142 |
⨁⨁◯◯ |
DBS lijkt de Y-BOCS score te verminderen. |
|
Complete response |
- |
- |
RR 2.4 |
- |
⨁⨁◯◯ |
DBS lijkt de kans op respons te verhogen. NNT: 3,03 |
|
Remissie. |
- |
- |
RR 1.30 |
- |
⨁⨁◯◯ |
DBS lijkt de kans op remissie te verhogen. NNT: 33,3 |
|
Depressie: eerste follow-up |
- |
MD 7.3 lager |
- |
- |
⨁⨁◯◯ |
DBS lijkt depressie te verminderen bij een relatief korte follow-up. |
|
Kans op bijwerkingen (bijwerkingen per participant) |
- |
0,68 (0,59; 0,78) |
- |
195 (30 cohorten) |
⨁◯◯◯ Zeer laage |
De evidentie is zeer onzeker wat betreft de kans op bijwerkingen na DBS |
|
Kans op ernstige bijwerkingen (ernstige bijwerkingen per participant) |
- |
0,32 (0,12; 0,52) |
- |
158 (27 cohorten) |
⨁◯◯◯ Zeer laage |
De evidentie is zeer onzeker wat betreft de kans ernstige op bijwerkingen na DBS |
|
Kans op uitval (uitval per participant) |
- |
0,13 (0,07; 0,16) |
- |
175 (30 cohorten) |
⨁◯◯◯ Zeer laagf |
De evidentie is zeer onzeker wat betreft de kans op uitval na DBS |
|
a. Risico op bias door gebrekkige blindering van participanten en uitkomst-beoordelaars bij 5 trials. b. Geen inconsistentie, betrouwbaarheidsinterval van RCT van Goodman2010 overlapt met het gepoolde effect c. Kleine populatie, ‘optimal information size’ niet bereikt d. Gebaseerd op gepresenteerde I2 geen inconsistentie e. Gebaseerd op gepresenteerde I2 aanmerkelijke inconsistentie f. weinig events RR: relatief risico |
||||||
Tabel 10 Resultaten van ablatiechirurgie bij OCS (Lai 2020)
|
Uitkomsten |
Absolute effecten* (95% CI) |
Relatief effect |
Aantal deelnemers |
Zekerheid evidentie |
Opmerkingen |
|
|
Baseline |
Na Ablatiechirurgie |
|||||
|
Ernst OCS |
Gemiddelde (mean) ernst OCS was 33.1 (33.0–33.3) |
(mean) 19.3 |
De ernst van OCS is van extreem ernstig naar matig gegaan |
459 |
⨁⨁◯◯ |
Ablatiechirurgie lijkt te kunnen resulteren in een grote vermindering van de ernst van OCS. |
|
Response (percentage patienten met ≥ 35% reductie in Y-BOCS)) |
De gemiddelde (mean) response (% patienten met ≥ 35% reductie in Y-BOCS)) was 0 |
0.55 |
- |
459 |
⨁⨁◯◯ |
Ablatiechirurgie lijkt meer kans op response te geven (ernst OCS) |
|
Bijwerkingen |
Na behandeling: In 1 studie kreeg 1 persoon (van de 19) een blaasinfectie. In 1 studie kregen 3 personen (van de 40) suïcidale gedachten. In 1 studie kreeg 1 persoon (van de 21) een postoperatieve wondinfectie |
(3 observationele studies) |
⨁◯◯◯ |
Het is onduidelijk of ablatiechirurgie een verhoogde kans geeft op infecties of suïcidale gedachten. |
||
|
Functioneel herstel, Kwaliteit van leven en Werkhervatting |
Geen resultaten met betrekking tot deze uitkomstmaten |
- |
Er is geen informatie over Functioneel herstel, Kwaliteit van leven en Werkhervatting |
|||
a. Er is niet gedowngrade voor RoB omdat al gestart is bij 'lage kwaliteit' ivm het ontbreken van een (gerandomiseerde) controle groep in de meeste studies
b. Heel weinig events.
Beoordelingsdatum en geldigheid
Publicatiedatum : 04-09-2024
Beoordeeld op geldigheid : 04-03-2024
Algemene gegevens
In opdracht van de Nederlandse Vereniging voor Psychiatrie (NVvP) en Stichting Kwaliteitsgelden Medisch Specialisten (SKMS) is de multidisciplinaire richtlijn Angst- en Dwangstoornissen voor de vierde maal geüpdatet en gereviseerd van november 2020 tot en met mei 2023. De ontwikkeling van de richtlijn werd methodologisch en organisatorisch ondersteund door het Trimbos-instituut.
Doel en doelgroep
De multidisciplinaire richtlijn Angst- en Dwangstoornissen geeft aanbevelingen en handelingsinstructies voor de samenwerking, diagnostiek en behandeling van volwassenen, kinderen en ouderen met een angst- of dwangstoornis. De richtlijn geeft aanbevelingen ter ondersteuning van de praktijkvoering van alle professionals die betrokken zijn bij de zorgverlening aan deze groepen patiënten. Op basis van de resultaten van wetenschappelijk onderzoek en praktijkoverwegingen geeft de richtlijn een overzicht van goed (‘optimaal’) handelen als waarborg voor kwalitatief hoogwaardige zorg. De richtlijn kan tevens richting geven aan de onderzoeksagenda voor wetenschappelijk onderzoek op het gebied van angststoornissen.
De richtlijn geeft aanbevelingen bij de diagnostiek en behandeling van een angst- of dwangstoornis. De aanbevelingen van de richtlijn moeten worden vertaald naar de lokale situatie in een instelling of behandelteam. Het opstellen van lokale zorgprogramma’s en andere vormen van werkkaders op basis van deze richtlijn wordt door de werkgroep aangemoedigd, omdat dat voor de implementatie van de in de richtlijn beschreven optimale zorg bevorderlijk is.
Deze multidisciplinaire richtlijn is een kwaliteitsinstrument en een beslissingsondersteunend instrument bij (gezamenlijke) beslissingen over het behandelbeleid. De richtlijn geeft aanbevelingen over het in te zetten en te volgen behandelbeleid, ter ondersteuning van de dagelijkse praktijkvoering.
Samenstelling werkgroep
De Multidisciplinaire richtlijn Angst- en Dwangstoornissen is ontwikkeld door de gelijknamige werkgroep, in opdracht van de Nederlandse Vereniging voor Psychiatrie (NVvP) en Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
De werkgroep bestond uit: psychiaters, psychologen, verpleegkundigen, huisartsen en ervaringsdeskundigen, welke door de respectievelijke beroepsverenigingen en familie- en patiëntenverenigingen werden afgevaardigd. Voorafgaande aan het ontwikkeltraject werden kennismakingsgesprekken gevoerd met verscheidene kandidaat leden voor de werkgroep. Uit deze groep belangstellenden werden de huidige werkgroepleden geselecteerd. Naast de werkgroep waren enkele adviseurs betrokken, welke delen hebben meegeschreven en die werd gevraagd voorafgaand aan de commentaarfase schriftelijk te reageren op onderdelen van de concepttekst. Deze adviseurs konden tevens worden gevraagd om tijdens een werkgroepbijeenkomst mee te denken over een specifieke uitgangsvraag. De werkgroep werd methodologisch en organisatorisch ondersteund door het technisch team van het Trimbos-instituut. Dit technisch team bestond uit een projectleider, informatiespecialist, literatuur reviewers, een notulist en een projectassistente. Onderstaande schema's geven een overzicht van de samenstelling van de werkgroep, de adviseurs en het ondersteunend technisch team. Alle werkgroepleden rapporteerden bij aanvang hun mogelijke belangenverstrengelingen en aan het begin van elke vergadering werd hen gevraagd of hier wijzigingen in waren opgetreden.
Leden Werkgroep (op alfabetische volgorde)
|
|
Naam |
Organisatie |
Beroepsvereniging |
|
1. |
Ton van Balkom (voorzitter) |
GGZinGeest AmsterdamUMC (VUMC) |
Psychiater, NVvP |
|
2. |
Neeltje Batelaan (vice-voorzitter) |
GGZinGeest AmsterdamUMC (VUMC) |
Psychiater, NVvP |
|
3. |
Martin Beeres |
Radboud MC |
Huisarts, NHG |
|
4. |
Gert-Jan Hendriks |
Pro Persona |
Psychiater, NVVP (ouderen) |
|
5. |
Mirjam Kampman |
Pro Persona |
Psycholoog, NIP (?) |
|
6. |
Tessa Magnée |
Huisartspraktijk |
POH-GGZ, LVPOHGGZ |
|
7. |
Inez Mijsberg |
Dimence |
Verpleegkundige, V&VN |
|
8. |
Maaike Nauta |
RUG |
Psycholoog, NIP (?) (kinderen) |
|
9. |
Lieke van Noord |
Angst, Dwang en Fobie Stichting |
Ervaringsdeskundige |
|
10. |
Patricia van Oppen |
GGZinGeest AmsterdamUMC (VUMC) |
Psycholoog, NVGzP |
|
11. |
Koen Schruers |
Maastricht University |
Psychiater, NVvP |
|
12. |
Sako Visser |
UVA |
Psycholoog, NIP |
|
13. |
Irene van Vliet |
LUMC |
Psychiater, NVvP |
Adviseurs
|
Hoofdstuk |
Naam |
Organisatie |
Beroep |
|
Farmacotherapie |
Chaim Huyser |
Levvel |
Kinder-en jeugd psychiater |
|
Werkhervatting |
Irene Lindenburg |
UWV |
Verzekeringsarts, NVVG |
|
Werkhervatting |
Giny Norder |
Arbo Unie |
Bedrijfsarts, NVAB |
|
Farmacotherapie / Neuromodulatie |
Chris Bervoets |
UPC KU Leuven |
Psychiater |
|
Onderhoudsbehandeling (coauteur van dit hoofdstuk) |
Leonieke Kranenburg |
Erasmus MC |
Psycholoog |
Methodologische ondersteuning
|
Naam
|
Ondersteuning |
|
Danielle van Duin / Piet Post |
Projectleider, Trimbos-instituut |
|
Egbert Hartstra |
Reviewer, Trimbos-instituut |
|
Matthijs Oud |
Reviewer, Trimbos-instituut |
|
Elena Vos |
Reviewer, Trimbos-instituut |
|
Erika Papazoglou |
Reviewer, Trimbos-instituut |
|
Bram Zwanenburg |
Reviewer, Trimbos-instituut |
|
Lex Hulsbosch |
Reviewer, Trimbos-instituut |
|
Rikie Deurenberg |
Informatiespecialist, namens Trimbos-instituut |
|
Chris van der Grinten |
Notulist, namens Trimbos-instituut |
|
Joyce Huls / Nelleke van Zon / Isa Reijgersberg |
Project assistent, Trimbos-instituut |
In totaal kwam de werkgroep Angststoornissen voorafgaand aan de commentaarfase 17 keer bijeen in een periode 30 maanden (november 2020 - april 2023). Daarnaast kwamen zij in zogeheten ‘topic-groepen’ nog in subgroepjes bijeen. In deze periode werden de stappen van de methodiek voor evidence-based richtlijnontwikkeling (EBRO) doorlopen. De informatiespecialist verrichtte in overleg met de werkgroepleden op systematische wijze literatuuronderzoek en de reviewers maakten een selectie in de gevonden onderzoeken (zie voor informatie over de zoekstrategie en de selectiecriteria: het reviewprotocol). De reviewers beoordeelden de kwaliteit en inhoud van de aldus verkregen literatuur en verwerkten deze in evidence tabellen, GRADE profielen, beschrijvingen van de wetenschappelijke onderbouwing en wetenschappelijke (gewogen) conclusies. Leden van de werkgroep gingen op basis van de gevonden literatuur met elkaar in discussie over praktijkoverwegingen (beschreven in de sectie “Praktijkoverwegingen”) en aanbevelingen. De werkgroepleden schreven samen met het technisch team van het Trimbos-instituut de concepttekst, welke ter becommentariëring openbaar is gemaakt. De ontvangen commentaren zijn verwerkt in een commentaartabel, die tijdens een werkgroepbijeenkomst is besproken. Na het doorvoeren van op deze bijeenkomst voorgestelde wijzigingen is de definitieve richtlijn aan de opdrachtgever aangeboden.
Methode ontwikkeling
Evidence based
Implementatie
Recent onderzoek laat zien dat er bij trajecten rond kwaliteit van zorg voornamelijk aandacht is voor de ontwikkeling van de kwaliteitstandaard. Planmatige opgezette en onderbouwde invoering komt maar heel beperkt van de grond. Hierop dient gericht te worden aangestuurd door financiers, zodat hier al bij de start geld voor beschikbaar is. De Regieraad voor richtlijntrajecten onderschrijft dan ook een programmatische aanpak van de ontwikkeling, invoering én evaluatie van kwaliteitsstandaarden inclusief (financiële en organisatorische) middelen, om het gebruik van de standaarden te stimuleren, monitoren en evalueren. TNO, CBO en het Trimbos-instituut besloten deze opdracht samen uit te voeren, met als doel de complementaire inzichten en expertise te vertalen in een gemeenschappelijke visie op richtlijnen en andere kwaliteitsstandaarden. Dit resulteerde in een praktisch instrument voor een analyse van richtlijntrajecten: Kwaliteit Richtlijnontwikkeling, Invoering en Evaluatie (KRIE).
Werkwijze
Afbakening
Deze richtlijn betreft diagnostiek en behandeling van mensen met een angst- en of dwangstoornis. Studies over alle levensfases (kinderen, adolescenten, volwassenen en ouderen) zijn meegenomen. In de richtlijn is gezocht naar meta-analyses en belangrijke gecontroleerde studies van 2013 tot en met heden (2022). Nog niet gepubliceerde onderzoeken zijn niet meegenomen (wel onderzoeken 'in press'). Zie voor meer informatie over de afbakening van de richtlijn in de bijlagen. Per hoofdstuk is een bijlage opgenomen met toelichting over de gebruikte reviewstrategie (reviewprotocollen per uitgangsvraag).
Uitgangsvragen
De richtlijn is ontwikkeld op geleide van uitgangsvragen, die gebaseerd zijn op knelpunten die worden ervaren rondom samenwerking, diagnostiek en behandeling van mensen met een angst- of dwangstoornis.
De richtlijn is geen leerboek waarin zoveel mogelijk beschikbare kennis over een onderwerp wordt opgenomen, maar een document met praktische aanbevelingen rondom knelpunten uit de praktijk. Dat betekent dat praktijkproblemen het uitgangspunt zijn van de teksten in de richtlijn. Er wordt niet ingegaan op de vraag door wie die problemen moeten worden aangepakt of opgelost. De richtlijn is een document waarin staat hoe optimale diagnostiek en behandeling er inhoudelijk uitziet en in welke vorm een interventie het beste aangeboden kan worden. In deze richtlijn worden de hieronder beschreven ‘klinische uitgangsvragen’ behandeld in de verschillende hoofdstukken.
Uitgangsvragen in de richtlijn Angststoornissen
|
Hoofdstuk |
Uitgangsvragen |
|
Hoofdstuk 3 Classificatie en Diagnostiek |
|
|
Hoofdstuk 4 Psychotherapie (breed) |
|
|
Hoofdstuk 5 EMDR bij angst |
|
|
Hoofdstuk 6 Vorm van aanbieden |
|
|
Hoofdstuk 7 Farmacotherapie
|
|
|
Hoofdstuk 8 Combinatiebehandeling |
|
|
Hoofdstuk 9 Neuromodulatie |
|
|
Hoofdstuk 10 Maatschappelijk participatie / werkhervatting |
|
|
Hoofdstuk 11 Onderhoudsbehandeling |
|
|
Hoofdstuk 12 Co-morbiditeit |
|
Methode: wetenschappelijke onderbouwing
De richtlijn Angststoornissen is ontwikkeld volgens de methodiek van de evidence based richtlijnontwikkeling (EBRO).
Zoekstrategie
Om de klinische uitgangsvragen te beantwoorden is door de informatiespecialist, in overleg met de werkgroepleden, op systematische wijze literatuuronderzoek verricht en is een selectie gemaakt binnen de gevonden onderzoeken volgens vooraf vastgestelde selectiecriteria. Er is gezocht naar bestaande (buitenlandse) evidence-based richtlijnen voor de zorg aan mensen met angststoornissen en dwangstoornisseen, systematische reviews en oorspronkelijke onderzoeken. In de literatuursearches is gezocht naar literatuur in de Engelse, Nederlandse, Franse, en Duitse taalgebieden. Voor het zoeken naar publicaties is gebruik gemaakt van de volgende informatiebronnen:
- Cochrane Database of Systematic Reviews (CDSR)
- Psychological Information Database (PsycINFO)
- PubMed
- Cumulative Index to Nursing and Allied Health Literature (CINAHL)
- Excerpta Medica database (Embase)
Selectiestrategie
Bij de selectie van artikelen zijn de volgende criteria gehanteerd:
- Geeft het onderwerp van het gevonden onderzoek voldoende antwoord op de uitgangsvraag: worden de binnen GRADE vastgestelde kritische en belangrijke uitkomstmaten in het onderzoek geëvalueerd? (zie voor meer informatie over GRADE verderop in deze paragraaf);
- Sluit de doelgroep van het gevonden onderzoek voldoende aan bij de doelgroep van de richtlijn;
- Is er sprake van een meta-analyse, systematic-review, randomised controlled trial (RCT), cohort onderzoek, cross-sectioneel onderzoek, patiëntcontrole onderzoek of wetenschappelijke verantwoord kwalitatief onderzoek? Bij een longitudinaal onderzoek: Is er sprake van een voldoende lange follow-up periode?;
- Zie voor meer informatie over de zoekstrategie de bijlagen per hoofdstuk en voor meer informatie over de selectiecriteria per uitgangsvraag de reviewprotocollen in de bijlagen per hoofdstuk.
Beoordeling van de kwaliteit van het bewijs
Studies werden door twee personen beoordeeld op het risico op bias met behulp van de Cochrane Collaboration Risico van Bias Assessment Tool (Higgins 2008). Elke studie werd gewaardeerd op de wijze van randomisatie en toewijzing; blindering van de deelnemers, beoordelaars, en therapeuten; gehanteerde methode om met voortijdig stoppen met de behandeling van deelnemers om te gaan; en of alle uitkomsten zijn gerapporteerd. Risico op bias kon als hoog (serieuze kans op beïnvloeding van het resultaat), laag (waarschijnlijk geen invloed op het resultaat), of onduidelijk worden beoordeeld.
Voor het bewijs rondom interventies is daarna het bewijs van de onderzoeken per uitkomstmaat gegradeerd met behulp van GRADE[1]. De kwaliteit van het bewijs kent daarbij vier niveaus, te weten; zeer laag, laag, matig en hoog. In deze richtlijn is gekozen om de GRADE niveaus weer te geven met behulp van de volgende neutrale en internationaal toepasbare weergave:
[1] GRADE: Grading of Recommendations Assessment, Development and Evaluation
|
Hoog |
|
|
Matig |
|
|
Laag |
|
|
Zeer laag |
|
Het studiedesign bepaalt de uitgangspositie van de kwaliteit van bewijs. Gerandomiseerde, gecontroleerde studies (RCT's) hebben over het algemeen meer bewijskracht dan observationele studies. Daarom is hun uitgangspositie hoog, terwijl de uitgangspositie van observationele studies laag is. De kwaliteit van het bewijs per uitkomstmaat wordt, behalve door de methodologische kwaliteit van de individuele onderzoeken, ook bepaald door andere factoren, zoals de mate van consistentie van de gevonden resultaten uit de verschillende onderzoeken en de precisie van de gevonden uitkomst (zie tabel 1).
Tabel 1 GRADE: Factoren voor downgraden en upgraden
Het niveau van de kwaliteit van het bewijs (zeer laag, laag, matig en hoog) verwijst naar de mate van vertrouwen dat men heeft in de schatting van het effect van een behandeling.
|
We downgraden het niveau van de kwaliteit van bewijs van studies met een hoge uitgangspositie (RCT’s), bij: |
We upgraden het niveau van de kwaliteit van bewijs van observationele studies bij: |
|
|
|
|
|
|
Standaard is SMD van -0,2 tm 0,2 niet klinisch relevant en bij een RR/OR is dit 0,75 tm 1,25.
Bij een Mean Difference tussen groepen wordt uit het Minimal Important Clinical Difference (MICD)van de vragenlijst gehanteerd. Is deze niet voorhanden dan moet de evidentie op minimaal 300 personen zijn gebaseerd. |
|
|
|
[2] Het blinderen van deelnemers en therapeuten is in deze richtlijn niet meegenomen in de beoordeling van studies rond psychosociale niterventies, omdat blinderen van de deelnemers en therapeuten niet goed mogelijk is bij deze interventies.
Netwerk meta-analyse
In recente jaren wordt er naast de traditionele meta-analyses steeds meer gebruik gemaakt van netwerk meta-analyses (NMA). De voordelen van een NMA is dat er vergelijkingen tussen interventies gemaakt kunnen worden die in de losse geïncludeerde studies niet direct met elkaar zijn vergeleken (indirecte vergelijkingen), alle evidentie in het model wordt meegenomen wat leidt tot verbeterde precisie bij het schatten van de interventie effecten. Deze indirecte vergelijkingen zijn echter wel gevoelig voor variabiliteit en verschillen tussen de geïncludeerde studies waardoor het van belang is dat er zorg gedragen wordt dat er geen grote heterogeniteit en inconsistentie in het model aanwezig is. Dit kan deels voorkomen worden door het includeren van studies waarbij er geen grote verschillen zijn in populatiekenmerken. Voor het bepalen van de kwaliteit van bewijs afkomstig uit een NMA is men afhankelijk van op welke wijze de auteurs de NMA hebben uitgevoerd (gemaakte aannames, uitgevoerde analyse, rapporteren van onderliggende informatie, rapporteren van CINeMA scores). De CINeMA methode heeft gelijkenissen met de GRADE methode maar is toegespitst op het gebruik bij NMA. Waar mogelijk worden deze CiNeMA scores gebuikt in de huidige richtlijn. Mochten deze ontbreken wordt er door de reviewers gekeken of de heterogeniteit en inconsistentie van het model worden gerapporteerd, mocht dit niet het geval zijn dan wordt de NMA niet meegenomen. Wanneer deze informatie wel aanwezig is wordt deze meegenomen in de GRADE beoordeling en er wordt een narratieve schatting van het risico op vertekening van uitkomsten door gebreken in de onderzoeksopzet gemaakt (Risk of Bias). . Mocht er sprake zijn van verhoogde heterogeniteit dan wordt hier voor gedowngrade en wanneer er sprake is van verhoogde inconsistentie dan wordt de NMA niet meegenomen.
Samenvatten van resultaten in ‘evidence tabel’ en ‘forest plot’
Van elk artikel is een samenvatting gemaakt in een zogenaamde 'evidence tabel', waarin de belangrijkste kenmerken van individuele onderzoeken zijn opgenomen (bij een RCT zijn dat bijvoorbeeld het doel van het onderzoek, het onderzoeksdesign, patiëntkenmerken, interventies, uitkomstmaten en de resultaten). Bij de uitgangsvragen over interventies is voor elke kritische uitkomstmaat een meta-analyse uitgevoerd, om de omvang van het klinisch effect van de interventie samen te vatten. De data uit oorspronkelijke onderzoeken worden hiervoor verwerkt in een forest plot, welke een grafische weergave van de meta-analyse geeft (zie tabel 2 voor een voorbeeld van een forest plot).
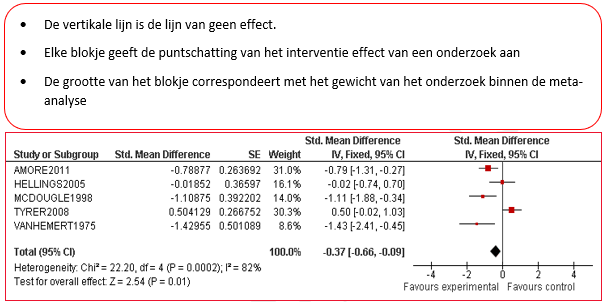
Tabel 2 Voorbeeld van een forest plot met toelichting
Wanneer er onvoldoende data beschikbaar waren om een meta-analyse uit te voeren, stelden de reviewers in enkele gevallen een narratieve (beschrijvende) review van het beschikbare bewijs op (zonder ‘gepoolde’ resultaten en berekening van mate van heterogeniteit, maar met een beschrijving van de kwaliteit). De kwaliteitsbeoordeling en een samenvattende beschrijving van de verschillende onderzoeken welke zijn geselecteerd vanuit de systematische literatuur search worden voor elke uitgangsvraag beschreven onder het kopje ‘wetenschappelijke onderbouwing’[3].
[3] Wat effectgroottes in de evidence tabellen en forest plots betreft: SMD's (standard mean differences) werden als klein beschouwd (0,2 ⩽ SMD < 0,5), matig (0,5 ⩽ SMD < 0,8) of groot (SMD ⩾ 0,8) (Cohen, 1988).
Conclusies
De formulering van de conclusies, gebaseerd op de studies uit de systematische literatuur search, is afgestemd op het GRADE niveau (zie tabel 3). Deze formulering sluit ook aan bij de ‘levels of evidence’ welke indeling (niveau 1 t/m 4) voorheen werd gebruikt in onder andere de multidisciplinaire richtlijn Schizofrenie.
Tabel 3 Formulering conclusies n.a.v. GRADE niveau
|
GRADE |
Levels of evidence |
Formulering conclusies |
|
|
Niveau 1 |
“Het is aangetoond dat…” |
|
|
Niveau 2 |
“Het is aannemelijk dat…” |
|
|
Niveau 3 |
“Er zijn aanwijzingen dat…” |
|
|
Niveau 4 |
“Er zijn voorzichtige aanwijzingen dat…” |
Van conclusies naar aanbevelingen: praktijkoverwegingen
Naast het wetenschappelijk bewijs bepalen enkele andere factoren mede of een instrument of behandeling wordt aanbevolen.
Mee te wegen factoren om te bepalen of een instrument of behandeling wordt aanbevolen:
|
1. Kwaliteit van bewijs Hoe hoger de algehele kwaliteit van het bewijs, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. |
|
2. Balans tussen gewenste en ongewenste effecten Hoe groter het verschil is tussen de gewenste en ongewenste effecten, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. Hoe kleiner dit verschil of hoe meer onzekerheid over de grootte van het verschil, des te waarschijnlijker wordt het formuleren van een conditionele aanbeveling. Toelichting:
|
|
3. Patiëntenperspectief Hoe groter de uniformiteit in waarden en voorkeuren van patiënten bij het afwegen van de voor- en nadelen van een interventie, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. De teksten onder het kopje ‘patiëntenperspectief’ zijn geschreven door de vertegenwoordiger van de patiëntenorganisatie: de Angst, Dwang en Fobie Stichting. Het is steeds gegaan om informele vragenrondes onder leden van het wetenschapspanel en de topicgroepen van deze organisatie. Gemiddeld zijn zo’n 30 à 40 personen bevraagd. |
|
4. Professioneel perspectief Hoe groter de uniformiteit in waarden en voorkeuren van professionals ten aanzien van de toepasbaarheid van een interventie, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. Toelichting:
De teksten onder het kopje ‘professioneel perspectief’ zijn geschreven door de leden van de richtlijncommissie. |
|
5. Middelenbeslag Hoe minder middelen er worden gebruikt (m.a.w. hoe lager de kosten van een interventie zijn vergeleken met de beschouwde alternatieven en andere kosten gerelateerd aan de interventie), des te waarschijnlijker wordt het formuleren van een sterke aanbeveling. Hoe meer onzekerheid over het middelenbeslag, des te waarschijnlijker wordt een conditionele aanbeveling. |
|
6. Organisatie van zorg Hoe meer onzekerheid of de geëvalueerde interventie daadwerkelijk op landelijke schaal toepasbaar is, des te waarschijnlijker wordt het formuleren van een conditionele aanbeveling. Toelichting:
|
Aanbevelingen
Afhankelijk van het bewijs en bovenstaande factoren kun je een instrument of behandeling wel of niet aanbevelen. We maken daarbij onderscheid tussen zwakke en sterke aanbevelingen. In het geval van een sterke aanbeveling zou je behandeling X voor alle patiënten met Y willen aanbevelen. Bij een zwakke aanbeveling is dit bijvoorbeeld afhankelijk van de voorkeuren van de patiënt in kwestie. Het is belangrijk in deze sectie expliciet te vermelden op grond waarvan een behandeling wel of niet wordt aanbevolen en ook waarom die aanbeveling zwak of sterk zou moeten zijn.
Voor de formulering van ‘sterke’ (onvoorwaardelijke) en ‘zwakke’ (voorwaardelijke) aanbevelingen is de volgende indeling aangehouden (zie tabel 4):
Tabel 4 GRADE Voorkeursformulering sterke / zwakke aanbevelingen
|
Gradering aanbeveling |
Betekenis |
Voorkeursformulering* |
|
STERK VOOR |
De voordelen zijn groter dan de nadelen voor bijna alle patiënten. Alle of nagenoeg alle geïnformeerde patiënten zullen waarschijnlijk deze optie kiezen. |
We bevelen [interventie] aan. |
|
ZWAK VOOR |
De voordelen zijn groter dan de nadelen voor een meerderheid van de patiënten, maar niet voor iedereen. De meerderheid van geïnformeerde patiënten zal waarschijnlijk deze optie kiezen. |
Overweeg [interventie], bespreek de voor- en nadelen). |
|
ZWAK TEGEN |
De nadelen zijn groter dan de voordelen voor een meerderheid van de patiënten, maar niet voor iedereen. De meerderheid van geïnformeerde patiënten zal waarschijnlijk deze optie kiezen. |
Wees terughoudend met [interventie], bespreek de voor- en nadelen). |
|
STERK TEGEN |
De nadelen zijn groter dan de voordelen voor bijna alle patiënten. Alle of nagenoeg alle geïnformeerde patiënten zullen waarschijnlijk deze optie kiezen. |
We bevelen [interventie] niet aan. |
* het gaat hier om voorkeursaanbevelingen, deze kunnen in een enkele geval afwijken. Voor bepaalde hoofdstukken is GRADE niet toegepast (bijv. Organisatie van zorg) daar zijn uit praktisch oogpunt ook de aanbevelingen niet volgens GRADE
Referenties
Cohen J (1988) Statistical Power Analysis for the Behavioral Sciences. Hillsdale, NJ: Lawrence Erlbaum Associates.
Gevers, J. K. M., & Aalst, A. van (1998). De rechter en het medisch handelen (3e druk). Deventer: Kluwer.
Higgins, J. P. T., Green, S., & Cochrane Collaboration (2008). Cochrane handbook for systematic Reviews of interventions. Chichester, England/Hoboken, NJ: Wiley-Blackwell.
Zoekverantwoording
Zoekstrategie – Neuromodulatie
Overzicht resultaten en zoekstrategie per database (De resultaten in Medline vormen de basis. Alleen aantal extra artikelen vermeld bij de andere databases).
|
onderwerp |
Medline |
embase |
psychinfo |
Cochrane |
Totaal |
|
Obsessive compulsive disorder |
207 |
184 |
100 |
|
491 |
|
Bijwerkingen |
8 |
36 |
3 |
1 |
47 |
Er is gezocht vanaf 2010 en de resultaten van alle 3 de onderwerpen zijn ontdubbeld via endnote
Medline
Database: Ovid MEDLINE(R) ALL <1946 to May 26, 2021>
Search Strategy:
--------------------------------------------------------------------------------
1 "voorbereiding 3 themas dwang".ti. (0)
2 "17".fc_vol. and "grant$".fc_auts. and "trial".fc_titl. and "2007".fc_pubyr. and "761".fc_pg. (1)
3 "a preliminary study of d-cycloserine".fc_titl. and "2010".fc_pubyr. (1)
4 "29".fc_vol. and "ross$".fc_auts. and "group cognitive and ".fc_titl. and "2012".fc_pubyr. and "597".fc_pg. (1)
5 2 or 3 or 4 (3)
6 morphodys*.ti. (5)
7 Body Dysmorphic Disorders/px, rh, th [Psychology, Rehabilitation, Therapy] (733)
8 (body adj2 dysmorphic adj2 (disord* or diseas*)).tw,kw. (1178)
9 ((disorde* or d?sfunct*) adj2 body adj2 imag*).tw,kw. (325)
10 Body Dysmorphic Disorders/ (1090)
11 8 or 9 or 10 (2012)
12 Body Dysmorphic Disorders/dt (32)
13 exp Psychotherapy/ (202157)
14 (psychological adj2 treatment?).ti,kw. (1123)
15 Cognitive Behavioral Therapy/ (26898)
16 ((cognit* adj2 behavio?r* adj2 therap*) or (psychotherap* adj2 cogniti*)).tw,kw. (19285)
17 or/13-16 (208667)
18 11 and (17 or 12 or 7) (884)
19 "filter SR".ti. (0)
20 meta analysis.pt. (133043)
21 (meta-anal$ or metaanal$).tw,kf. (204494)
22 (quantitativ$ adj10 (review$ or overview$)).tw. (10500)
23 (systematic$ adj10 (review$ or overview$)).tw. (228026)
24 (methodologic$ adj10 (review$ or overview$)).tw. (13087)
25 (quantitativ$ adj10 (review$ or overview$)).kf. (83)
26 (systematic$ adj10 (review$ or overview$)).kf. (25144)
27 (methodologic$ adj10 (review$ or overview$)).kf. (84)
28 medline.tw. and review.pt. (83145)
29 (pooled adj3 analy*).tw. (22638)
30 (pooled adj3 analy*).kf. (304)
31 "cochrane$".fc_jour. (15377)
32 or/20-31 (406621)
33 "einde SR filter".ti. (0)
34 (dutch or english or german).la. (28808753)
35 18 and 32 and 34 (36)
36 35 (36)
37 limit 36 to yr="2013 -Current" (25)
38 Obsessive-Compulsive Disorder/dh, dt, px, rh, su, th [Diet Therapy, Drug Therapy, Psychology, Rehabilitation, Surgery, Therapy] (9470)
39 Obsessive-Compulsive Disorder/ (14949)
40 Cycloserine/tu (541)
41 Receptors, N-Methyl-D-Aspartate/ (28252)
42 Obsessive-Compulsive Disorder/dt (2663)
43 (obsessive adj3 compulsive adj3 disorde*).ti,kw. (7763)
44 39 or 43 (16152)
45 44 and (38 or 40 or 41 or 17) and 34 and 32 (360)
46 45 (360)
47 limit 46 to yr="2013 -Current" (211)
48 *Obsessive-Compulsive Disorder/dh, dt, px, rh, su, th (5727)
49 44 and (48 or 40 or 41 or 17) and 34 and 32 (294)
50 49 (294)
51 limit 50 to yr="2013 -Current" (183)
52 Hoarding Disorder/dt, nu, px, rh, su, th [Drug Therapy, Nursing, Psychology, Rehabilitation, Surgery, Therapy] (194)
53 Hoarding Disorder/ (281)
54 (obsessive adj2 hoarding adj2 disorder?).tw,kw. (23)
55 53 or 54 (296)
56 55 and (52 or 17) and 34 and 32 (10)
57 56 (10)
58 limit 57 to yr="2013 -Current" (9)
59 obsessive-compulsive disorder.kw. (2348)
60 deep brain stimulation.kw. (3543)
61 neurosurgery.kw. (5999)
62 ((Ablative adj2 surger*) or abl or (ablative adj2 procedure?) or capsulotom* or cingulotomy).tw,kw. (19434)
63 *Obsessive-Compulsive Disorder/ (11953)
64 (obsessive adj3 compulsive adj3 disorde*).ti,kw. (7763)
65 59 or 63 or 64 (13726)
66 Neurosurgical Procedures/ (32480)
67 Deep Brain Stimulation/ (9309)
68 Transcranial Magnetic Stimulation/ (12242)
69 rtms.ti,kw. (1690)
70 62 or 66 or 67 or 68 or 69 (73067)
71 32 and 34 and 65 and 70 (40)
72 71 (40)
73 limit 72 to yr="2013 -Current" (35)=body dysmorphic disorder
74 35 (36)
75 limit 74 to yr="2010 -Current" (31)
76 49 (293)
77 limit 76 to yr="2010 -Current" (211)=OCD
78 55 and (52 or 17) and 34 and 32 (10)
79 limit 78 to yr="2010 -Current" (10)=hoarding
Embase
Database: Embase <1974 to 2021 May 26>
Search Strategy:
--------------------------------------------------------------------------------
1 "voorbereiding 3 themas dwang".ti. (0)
2 "17".fc_vol. and "grant$".fc_auts. and "trial".fc_titl. and "2007".fc_pubyr. and "761".fc_pg. (1)
3 "a preliminary study of d-cycloserine".fc_titl. and "2010".fc_pubyr. (1)
4 "29".fc_vol. and "ross$".fc_auts. and "group cognitive and ".fc_titl. and "2012".fc_pubyr. and "597".fc_pg. (1)
5 2 or 3 or 4 (3)
6 fluvoxamine/ (13343)
7 sertraline/ (26936)
8 exp antidepressant agent/dt [Drug Therapy] (180242)
9 obsession/dm, dt, rt, rh, su, th [Disease Management, Drug Therapy, Radiotherapy, Rehabilitation, Surgery, Therapy] (2296)
10 obsessive compulsive disorder/ (25428)
11 (obsessive adj3 compulsive adj3 disorde*).ti,kw. (12971)
12 *obsessive compulsive disorder/ (11145)
13 *obsessive compulsive disorder/dm, dt, rh, th (4200)
14 exp psychotherapy/ (260506)
15 (psychological adj2 treatment?).ti,kw. (1827)
16 exp cognitive behavioral therapy/ (16353)
17 ((cognit* adj2 behavio?r* adj2 therap*) or (psychotherap* adj2 cogniti*)).tw,kw. (29459)
18 or/14-17 (263533)
19 riluzole/ (4715)
20 cycloserine/ (6827)
21 19 or 20 (11416)
22 12 and (13 or 21 or 18) (4770)
23 "filter SR".ti. (0)
24 (meta-anal$ or metaanal$).tw,kw. (266348)
25 (quantitativ$ adj10 (review$ or overview$)).tw. (12589)
26 (systematic$ adj10 (review$ or overview$)).tw. (282648)
27 (methodologic$ adj10 (review$ or overview$)).tw. (15238)
28 (quantitativ$ adj10 (review$ or overview$)).kw. (151)
29 (systematic$ adj10 (review$ or overview$)).kw. (35715)
30 (methodologic$ adj10 (review$ or overview$)).kw. (90)
31 medline.tw. and review.pt. (80611)
32 (pooled adj3 analy*).tw. (34326)
33 (pooled adj3 analy*).kw. (565)
34 "cochrane$".fc_jour. (21540)
35 exp meta analysis/ (216421)
36 or/24-35 (532481)
37 "einde SR filter".ti. (0)
38 obsessive compulsive disorder/dm, dt, rh, th (7212)
39 (dutch or english or german).la. (32144867)
40 10 and (38 or 21 or 18) and 36 and 39 (724)
41 40 and 12 (309)=OCD
42 41 (309)
43 limit 42 to yr="2013 -Current" (195)
44 13 and 43 (164)
45 *riluzole/ (1135)
46 *cycloserine/ (2072)
47 hoarding/ or hoarding disorder/ (715)
48 hoarding.ti,kw. (1132)
49 47 or 48 (1425)
50 hoarding/dm, dt, rh, th or hoarding disorder/dm, dt, rh, th (75)
51 home care/ (63279)
52 (home adj3 assista*).tw,kw. (993)
53 18 or 51 or 52 (325956)
54 47 and (53 or 50) and 39 and 36 (12)
55 54 (12)
56 limit 55 to yr="2013 -Current" (11)
57 body dysmorphic disorder/dm, dt, rh, su, th [Disease Management, Drug Therapy, Rehabilitation, Surgery, Therapy] (516)
58 body dysmorphic disorder/ (3082)
59 (body adj2 dysmorphic adj2 (disord* or diseas*)).tw,kw. (1605)
60 ((disorde* or d?sfunct*) adj2 body adj2 imag*).tw,kw. (435)
61 58 or 59 or 60 (3734)
62 61 and (57 and 18) and 39 and 36 (21)
63 62 (21)
64 limit 63 to yr="2013 -Current" (10)
65 brain depth stimulation/ (44324)
66 neurosurgery/ (63761)
67 ((Ablative adj2 surger*) or abl or (ablative adj2 procedure?) or capsulotom* or cingulotomy).tw,kw. (29557)
68 exp obsessive compulsive disorder/ (41569)
69 (obsessive adj3 compulsive adj3 disorde*).ti,kw. (12971)
70 exp neurosurgery/ (266787)
71 transcranial magnetic stimulation/ (23110)
72 rtms.ti,kw. (3322)
73 68 or 69 (42147)
74 65 or 67 or 70 or 71 or 72 (354632)
75 36 and 39 and 73 and 74 (147)
76 75 (147)
77 limit 76 to yr="2010 -Current" (125)
78 limit 77 to (article or article in press or "review") (104)
79 78 (104)
80 41 (309)
81 limit 80 to yr="2010 -Current" (223)= OCD breed
82 54 (12)
83 limit 82 to yr="2010 -Current" (11)
84 62 (21)
85 limit 62 to yr="2010 -Current" (11)
86 limit 80 to (article or article in press or "review") (280)
87 limit 63 to yr="2010 -Current" (11)
Database: APA PsycInfo <1806 to June Week 1 2021>
Search Strategy:
--------------------------------------------------------------------------------
1 "voorbereiding 3 themas dwang".ti. (0)
2 "17".fc_vol. and "grant$".fc_auts. and "trial".fc_titl. and "2007".fc_pubyr. and "761".fc_pg. (1)
3 "a preliminary study of d-cycloserine".fc_titl. and "2010".fc_pubyr. (1)
4 "29".fc_vol. and "ross$".fc_auts. and "group cognitive and ".fc_titl. and "2012".fc_pubyr. and "597".fc_pg. (1)
5 2 or 3 or 4 (3)
6 obsessive compulsive disorder/ (14709)
7 exp drug therapy/ (149913)
8 exp cognitive behavior therapy/ or exp behavior therapy/ (43103)
9 ((cognit* adj2 behavio?r* adj2 therap*) or (psychotherap* adj2 cogniti*)).tw,id. (29915)
10 (obsessive adj3 compulsive adj3 disorde*).ti,id. (12457)
11 (psychological adj2 treatment?).ti,id. (3058)
12 6 or 10 (15328)
13 7 or 8 or 9 or 11 (202180)
14 12 and 13 (4574)
15 (dutch or english or german).la. (4702176)
16 "Meta Analysis".md. (24595)
17 "systematic review".md. (30369)
18 "systematic review"/ or meta analysis/ (5535)
19 "filter systematic reviews psycinfo".ti. (0)
20 (meta-anal* or metaanal*).tw. (42155)
21 (quantitativ* adj5 (review* or overview*)).tw. (2725)
22 (systematic* adj5 (review* or overview*)).tw. (40865)
23 (methodolo* adj5 (review* or overview*)).tw. (7312)
24 (medline or cochrane).tw. (19168)
25 (review* or overview*).ti. (171784)
26 (literature adj5 review).tw. (82848)
27 (synthes* adj3 (literature* or research or studies or data)).tw. (10040)
28 (pooled adj5 analys*).tw. (2542)
29 (data adj2 pool*).tw. (2501)
30 (medline or medlars or embase or cinahl or scisearch or psycinfo or psyclit or psychlit).ti. (77)
31 ((hand or manual* or database* or computer* or electronic*) adj2 search*).tw. (12474)
32 or/20-31 (280475)
33 16 or 17 or 18 or 32 (283025)
34 "nw SR filter psycinfo".ti. (0)
35 14 and 15 and 33 (458)
36 35 (458)
37 limit 36 to yr="2013 -Current" (194)
38 *obsessive compulsive disorder/ (13035)
39 10 or 38 (14671)
40 37 and 39 (189)
41 limit 40 to (all journals and yr="2013 -Current") (166)
42 hoarding disorder/ (262)
43 hoarding.ti,id. (1238)
44 42 or 43 (1247)
45 7 or 13 (202180)
46 44 and 45 and 33 and 15 (13)
47 46 (13)
48 limit 47 to (all journals and yr="2013 -Current") (11)
49 body dysmorphic disorder/ (1211)
50 (body adj2 dysmorphic adj2 (disord* or diseas*)).tw,id. (1433)
51 ((disorde* or d?sfunct*) adj2 body adj2 imag*).tw,id. (522)
52 49 or 50 or 51 (2088)
53 *body dysmorphic disorder/ (1058)
54 (body adj2 dysmorphic adj2 (disord* or diseas*)).ti,id. (1052)
55 ((disorde* or d?sfunct*) adj2 body adj2 imag*).ti,id. (177)
56 53 or 54 or 55 (1430)
57 15 and 33 and 45 and 56 (30)
58 57 (30)
59 limit 58 to (all journals and yr="2013 -Current") (10)
60 from 59 keep 1-9 (9)
61 limit 40 to (all journals and yr="2010 -Current") (166)OCD
62 limit 47 to (all journals and yr="2010 -Current") (12)hoarding
63 limit 58 to (all journals and yr="2010 -Current") (16)body dysmorphic disorders
Aanvullende search voor bijwerkingen van neuromodulatie
Database: Ovid MEDLINE(R) ALL <1946 to September 27, 2021>
Search Strategy:
--------------------------------------------------------------------------------
1 "voorbereiding 3 themas dwang".ti. (0)
2 "17".fc_vol. and "grant$".fc_auts. and "trial".fc_titl. and "2007".fc_pubyr. and "761".fc_pg. (1)
3 "a preliminary study of d-cycloserine".fc_titl. and "2010".fc_pubyr. (1)
4 "29".fc_vol. and "ross$".fc_auts. and "group cognitive and ".fc_titl. and "2012".fc_pubyr. and "597".fc_pg. (1)
5 2 or 3 or 4 (3)
6 morphodys*.ti. (5)
7 Body Dysmorphic Disorders/px, rh, th [Psychology, Rehabilitation, Therapy] (752)
8 (body adj2 dysmorphic adj2 (disord* or diseas*)).tw,kw. (1201)
9 ((disorde* or d?sfunct*) adj2 body adj2 imag*).tw,kw. (333)
10 Body Dysmorphic Disorders/ (1140)
11 8 or 9 or 10 (2057)
12 Body Dysmorphic Disorders/dt (32)
13 exp Psychotherapy/ (205646)
14 (psychological adj2 treatment?).ti,kw. (1147)
15 Cognitive Behavioral Therapy/ (27621)
16 ((cognit* adj2 behavio?r* adj2 therap*) or (psychotherap* adj2 cogniti*)).tw,kw. (19900)
17 or/13-16 (212276)
18 11 and (17 or 12 or 7) (903)
19 "filter SR".ti. (0)
20 meta analysis.pt. (142486)
21 (meta-anal$ or metaanal$).tw,kf. (215322)
22 (quantitativ$ adj10 (review$ or overview$)).tw. (10933)
23 (systematic$ adj10 (review$ or overview$)).tw. (242539)
24 (methodologic$ adj10 (review$ or overview$)).tw. (13527)
25 (quantitativ$ adj10 (review$ or overview$)).kf. (88)
26 (systematic$ adj10 (review$ or overview$)).kf. (27387)
27 (methodologic$ adj10 (review$ or overview$)).kf. (89)
28 medline.tw. and review.pt. (85304)
29 (pooled adj3 analy*).tw. (23651)
30 (pooled adj3 analy*).kf. (319)
31 "cochrane$".fc_jour. (15545)
32 or/20-31 (426443)
33 "einde SR filter".ti. (0)
34 (dutch or english or german).la. (29324061)
35 18 and 32 and 34 (38)
36 35 (38)
37 limit 36 to yr="2013 -Current" (27)
38 Obsessive-Compulsive Disorder/dh, dt, px, rh, su, th [Diet Therapy, Drug Therapy, Psychology, Rehabilitation, Surgery, Therapy] (9615)
39 Obsessive-Compulsive Disorder/ (15275)
40 Cycloserine/tu (545)
41 Receptors, N-Methyl-D-Aspartate/ (28581)
42 Obsessive-Compulsive Disorder/dt (2693)
43 (obsessive adj3 compulsive adj3 disorde*).ti,kw. (7943)
44 39 or 43 (16474)
45 44 and (38 or 40 or 41 or 17) and 34 and 32 (375)
46 45 (375)
47 limit 46 to yr="2013 -Current" (226)
48 *Obsessive-Compulsive Disorder/dh, dt, px, rh, su, th (5768)
49 44 and (48 or 40 or 41 or 17) and 34 and 32 (299)
50 49 (299)
51 limit 50 to yr="2013 -Current" (188)
52 Hoarding Disorder/dt, nu, px, rh, su, th [Drug Therapy, Nursing, Psychology, Rehabilitation, Surgery, Therapy] (203)
53 Hoarding Disorder/ (295)
54 (obsessive adj2 hoarding adj2 disorder?).tw,kw. (23)
55 53 or 54 (310)
56 55 and (52 or 17) and 34 and 32 (12)
57 56 (12)
58 limit 57 to yr="2013 -Current" (11)
59 obsessive-compulsive disorder.kw. (2498)
60 deep brain stimulation.kw. (3765)
61 neurosurgery.kw. (6287)
62 ((Ablative adj2 surger*) or abl or (ablative adj2 procedure?) or capsulotom* or cingulotomy).tw,kw. (19693)
63 *Obsessive-Compulsive Disorder/ (12254)
64 (obsessive adj3 compulsive adj3 disorde*).ti,kw. (7943)
65 59 or 63 or 64 (14043)
66 Neurosurgical Procedures/ (33639)
67 Deep Brain Stimulation/ (9686)
68 Transcranial Magnetic Stimulation/ (12775)
69 rtms.ti,kw. (1756)
70 62 or 66 or 67 or 68 or 69 (75360)
71 32 and 34 and 65 and 70 (45)
72 71 (45)
73 limit 72 to yr="2013 -Current" (40)
74 from 71 keep 1-38 (38)
75 from 73 keep 1-33 (33)
76 74 (38)
77 limit 76 to yr="2010 -Current" (38)
78 32 and 34 and 70 (2111)= sr + talen +neuromodulatie
79 exp Suicide/ (67562)
80 suicide?.tw,kw. (68748)
81 Mania/ (143)
82 (mania? or manic?).tw,kw. (18687)
83 exp Infections/ (2809103)
84 infecti*.ti,kw. (581227)
85 or/79-84 (3034876) adverse effects
86 78 and 85 (113)= sr + talen +neuromodulatie + adverse effects
87 86 and (39 or 43) (3)= sr + talen +neuromodulatie + adverse effects + OCD
88 86 (113)
89 limit 88 to yr="2021 -Current" (20)
90 Transcranial Magnetic Stimulation/ae (507)
91 ae.fs. (1837624)
92 side effect?.ti,kw. (18026)
93 90 or 91 or 92 (1843796) aanvulling adverse effects
94 78 and 93 (410) = sr + talen +neuromodulatie
95 94 and (39 or 43) (8)
96 95 not 87 (6)
97 from 87 keep 1-3 (3)
98 from 89 keep 1-20 (20)
99 from 96 keep 1-6 (6)
100 prabhav*.au. (126)
101 repetitiv*.ti. (12691)
102 100 and 101 (0)
103 39 or 59 (16332)
104 100 and 103 (0)
105 (39 or 43) and (85 or 93) and 32 and 34 and 70 (9)
106 105 (9)
107 limit 106 to yr="2010 -Current" (8)= medline resultaat
Embase
Database: Embase <1974 to 2021 September 27>
Search Strategy:
--------------------------------------------------------------------------------
1 "voorbereiding 3 themas dwang".ti. (0)
2 "17".fc_vol. and "grant$".fc_auts. and "trial".fc_titl. and "2007".fc_pubyr. and "761".fc_pg. (1)
3 "a preliminary study of d-cycloserine".fc_titl. and "2010".fc_pubyr. (1)
4 "29".fc_vol. and "ross$".fc_auts. and "group cognitive and ".fc_titl. and "2012".fc_pubyr. and "597".fc_pg. (1)
5 2 or 3 or 4 (3)
6 fluvoxamine/ (13480)
7 sertraline/ (27358)
8 exp antidepressant agent/dt [Drug Therapy] (189579)
9 obsession/dm, dt, rt, rh, su, th [Disease Management, Drug Therapy, Radiotherapy, Rehabilitation, Surgery, Therapy] (2288)
10 obsessive compulsive disorder/ (26084)
11 (obsessive adj3 compulsive adj3 disorde*).ti,kw. (10381)
12 *obsessive compulsive disorder/ (11401)
13 *obsessive compulsive disorder/dm, dt, rh, th (4297)
14 exp psychotherapy/ (265161)
15 (psychological adj2 treatment?).ti,kw. (1476)
16 exp cognitive behavioral therapy/ (17902)
17 ((cognit* adj2 behavio?r* adj2 therap*) or (psychotherap* adj2 cogniti*)).tw,kw. (28245)
18 or/14-17 (267811)
19 riluzole/ (4785)
20 cycloserine/ (6905)
21 19 or 20 (11562)
22 12 and (13 or 21 or 18) (4874)
23 "filter SR".ti. (0)
24 (meta-anal$ or metaanal$).tw,kw. (279068)
25 (quantitativ$ adj10 (review$ or overview$)).tw. (13102)
26 (systematic$ adj10 (review$ or overview$)).tw. (299442)
27 (methodologic$ adj10 (review$ or overview$)).tw. (15730)
28 (quantitativ$ adj10 (review$ or overview$)).kw. (54)
29 (systematic$ adj10 (review$ or overview$)).kw. (670)
30 (methodologic$ adj10 (review$ or overview$)).kw. (32)
31 medline.tw. and review.pt. (84137)
32 (pooled adj3 analy*).tw. (35837)
33 (pooled adj3 analy*).kw. (0)
34 "cochrane$".fc_jour. (21833)
35 exp meta analysis/ (226733)
36 or/24-35 (554340)
37 "einde SR filter".ti. (0)
38 obsessive compulsive disorder/dm, dt, rh, th (7359)
39 (dutch or english or german).la. (32735321)
40 10 and (38 or 21 or 18) and 36 and 39 (758)
41 40 and 12 (325)
42 41 (325)
43 limit 42 to yr="2013 -Current" (211)
44 13 and 43 (177)
45 *riluzole/ (1149)
46 *cycloserine/ (2077)
47 hoarding/ or hoarding disorder/ (758)
48 hoarding.ti,kw. (1049)
49 47 or 48 (1392)
50 hoarding/dm, dt, rh, th or hoarding disorder/dm, dt, rh, th (80)
51 home care/ (64275)
52 (home adj3 assista*).tw,kw. (1007)
53 18 or 51 or 52 (331221)
54 47 and (53 or 50) and 39 and 36 (15)
55 54 (15)
56 limit 55 to yr="2013 -Current" (14)
57 body dysmorphic disorder/dm, dt, rh, su, th [Disease Management, Drug Therapy, Rehabilitation, Surgery, Therapy] (523)
58 body dysmorphic disorder/ (3163)
59 (body adj2 dysmorphic adj2 (disord* or diseas*)).tw,kw. (1547)
60 ((disorde* or d?sfunct*) adj2 body adj2 imag*).tw,kw. (425)
61 58 or 59 or 60 (3774)
62 61 and (57 and 18) and 39 and 36 (21)
63 62 (21)
64 limit 63 to yr="2013 -Current" (10)
65 brain depth stimulation/ (45376)
66 neurosurgery/ (65099)
67 ((Ablative adj2 surger*) or abl or (ablative adj2 procedure?) or capsulotom* or cingulotomy).tw,kw. (29636)
68 exp obsessive compulsive disorder/ (42455)
69 (obsessive adj3 compulsive adj3 disorde*).ti,kw. (10381)
70 exp neurosurgery/ (271570)
71 transcranial magnetic stimulation/ (23576)
72 rtms.ti,kw. (3156)
73 68 or 69 (42671)
74 65 or 67 or 70 or 71 or 72 (360787)
75 36 and 39 and 73 and 74 (155)
76 75 (155)
77 limit 76 to yr="2010 -Current" (133)
78 limit 77 to (article or article in press or "review") (109)
79 78 (109)
80 41 (325)
81 limit 80 to yr="2010 -Current" (239)
82 54 (15)
83 limit 82 to yr="2010 -Current" (14)
84 62 (21)
85 limit 62 to yr="2010 -Current" (11)
86 65 or 66 or 70 or 71 or 72 (331938)
87 suicide/ or suicidal behavior/ (70931)
88 ((suicid* or self) adj1 killing).tw,kw. (113)
89 exp mania/ (79881)
90 (mania or manic).tw,kw. (25610)
91 exp infection/ (3578795)
92 infecti*.ti,kw. (662875)
93 side effect/ (326481)
94 exp obsessive compulsive disorder/dm [Disease Management] (253)
95 si.fs. (928711)
96 neuromodulation/ (43577)
97 95 and 96 (1207)
98 87 or 88 or 89 or 90 or 91 or 92 or 93 or 94 (4049366)
99 (10 or 11) and (86 or 96) and 36 and 39 and 98 (55)
100 99 (55)
101 limit 100 to yr="2010 -Current" (41)
102 exp conference paper/ (2129463)
103 from 101 keep 1-41 (41)
104 exp conference paper/ (2129463)
105 103 not 104 (37)
Database: APA PsycInfo <1806 to September Week 3 2021>
Search Strategy:
--------------------------------------------------------------------------------
1 "voorbereiding 3 themas dwang".ti. (0)
2 "17".fc_vol. and "grant$".fc_auts. and "trial".fc_titl. and "2007".fc_pubyr. and "761".fc_pg. (1)
3 "a preliminary study of d-cycloserine".fc_titl. and "2010".fc_pubyr. (1)
4 "29".fc_vol. and "ross$".fc_auts. and "group cognitive and ".fc_titl. and "2012".fc_pubyr. and "597".fc_pg. (1)
5 2 or 3 or 4 (3)
6 obsessive compulsive disorder/ (14852)
7 exp drug therapy/ (151210)
8 exp cognitive behavior therapy/ or exp behavior therapy/ (43709)
9 ((cognit* adj2 behavio?r* adj2 therap*) or (psychotherap* adj2 cogniti*)).tw,id. (30436)
10 (obsessive adj3 compulsive adj3 disorde*).ti,id. (12609)
11 (psychological adj2 treatment?).ti,id. (3092)
12 6 or 10 (15496)
13 7 or 8 or 9 or 11 (204272)
14 12 and 13 (4616)
15 (dutch or english or german).la. (4747683)
16 "Meta Analysis".md. (25225)
17 "systematic review".md. (31663)
18 "systematic review"/ or meta analysis/ (5612)
19 "filter systematic reviews psycinfo".ti. (0)
20 (meta-anal* or metaanal*).tw. (43439)
21 (quantitativ* adj5 (review* or overview*)).tw. (2799)
22 (systematic* adj5 (review* or overview*)).tw. (42640)
23 (methodolo* adj5 (review* or overview*)).tw. (7443)
24 (medline or cochrane).tw. (19856)
25 (review* or overview*).ti. (174170)
26 (literature adj5 review).tw. (84063)
27 (synthes* adj3 (literature* or research or studies or data)).tw. (10405)
28 (pooled adj5 analys*).tw. (2621)
29 (data adj2 pool*).tw. (2555)
30 (medline or medlars or embase or cinahl or scisearch or psycinfo or psyclit or psychlit).ti. (77)
31 ((hand or manual* or database* or computer* or electronic*) adj2 search*).tw. (12869)
32 or/20-31 (284639)
33 16 or 17 or 18 or 32 (287245)
34 "nw SR filter psycinfo".ti. (0)
35 14 and 15 and 33 (463)
36 35 (463)
37 limit 36 to yr="2013 -Current" (199)
38 *obsessive compulsive disorder/ (13166)
39 10 or 38 (14835)
40 37 and 39 (194)
41 limit 40 to (all journals and yr="2013 -Current") (170)
42 hoarding disorder/ (281)
43 hoarding.ti,id. (1270)
44 42 or 43 (1280)
45 7 or 13 (204272)
46 44 and 45 and 33 and 15 (14)
47 46 (14)
48 limit 47 to (all journals and yr="2013 -Current") (12)
49 body dysmorphic disorder/ (1232)
50 (body adj2 dysmorphic adj2 (disord* or diseas*)).tw,id. (1458)
51 ((disorde* or d?sfunct*) adj2 body adj2 imag*).tw,id. (532)
52 49 or 50 or 51 (2121)
53 *body dysmorphic disorder/ (1072)
54 (body adj2 dysmorphic adj2 (disord* or diseas*)).ti,id. (1069)
55 ((disorde* or d?sfunct*) adj2 body adj2 imag*).ti,id. (179)
56 53 or 54 or 55 (1450)
57 15 and 33 and 45 and 56 (30)
58 57 (30)
59 limit 58 to (all journals and yr="2013 -Current") (10)
60 (obsessive adj3 compulsive adj3 disorde*).ti,id. (12609)
61 obsessive compulsive disorder/ (14852)
62 deep brain stimulation/ (3391)
63 exp neurosurgery/ (17335)
64 ((Ablative adj2 surger*) or abl or (ablative adj2 procedure?) or capsulotom* or cingulotomy).tw,id. (395)
65 transcranial magnetic stimulation/ (9079)
66 rtms.ti,id. (1241)
67 62 or 63 or 64 or 65 or 66 (29749)
68 60 or 61 (15496)
69 15 and 33 and 67 and 68 (50)
70 69 (50)
71 limit 70 to (all journals and yr="2010 -Current") (39)
72 (6 or 10) and 15 and 32 (1157)
73 67 and 72 (50)
74 exp suicide/ (36868)
75 suicid*.tw,id. (70612)
76 exp mania/ (6499)
77 (mania? or manic?).tw,id. (20896)
78 exp infectious disorders/ (68798)
79 infecti*.ti,id. (14802)
80 neuromodulation/ (1117)
81 "side effects (treatment)"/ (3245)
82 74 or 75 or 76 or 77 or 78 or 79 or 81 (163954)
83 67 or 80 (30604)
84 (6 or 10) and 15 and 32 and (80 or 67) and 82 (5)
85 84 (5)
86 limit 85 to yr="2010 -Current" (3)
Cochrane
Search Name:
Date Run: 28/09/2021 14:48:55
Comment:
ID Search Hits
#1 MeSH descriptor: [Obsessive-Compulsive Disorder] explode all trees 1090
#2 obsessive compulsive disorder:ti 1800
#3 neuromodulat*:ti,ab 1998
#4 rtms:ti,ab 3183
#5 MeSH descriptor: [Transcranial Magnetic Stimulation] explode all trees 1468
#6 #3 or #4 or #5 5631
#7 (#1 or #2) and #6 93 met 1 SR