Obsessieve-compulsieve stoornis
Uitgangsvraag
Er is geen uitgangsvraag bij deze module geformuleerd.
Aanbeveling
STAP 1
SSRI’s als groep en de SNRI’s venlafaxine en duloxetine zijn alle effectief bij de behandeling van OCS en gezien de veiligheid en goede verdraagbaarheid worden zij sterk aanbevolen als 1e keuze bij volwassenen. Het bewijs hiervoor is sinds de vorige Richtlijn verder onderbouwd. Doseringsadviezen zijn onveranderd. Bij OCS zijn vaak hogere doseringen nodig om het gewenste resultaat te bereiken vergeleken met de doseringen bij de andere angststoornissen en die bij depressie. Het effect van de medicatie is na 12 weken te beoordelen. Indien bij 10 weken maximale dosering geen enkel effect gezien wordt, dan kan eerder naar de volgende behandelstap overgegaan worden.
Er dient aandacht te zijn voor mogelijke bijwerkingen in de beginfase van de behandeling alsook in het vervolg en deze dienen actief en bij herhaling nagevraagd te worden. Goede begeleiding van de behandelaar voorkomt voortijdig stoppen met de behandeling hierdoor. Kortdurend toevoegen van een benzodiazepine voor max. 2 weken kan helpen om de eventuele angsttoename van de opbouwfase goed door te komen. Bijwerkingen kunnen reden zijn om te switchen naar een ander middel. Bij de keuze van een middel dienen zowel de bijwerkingen op de korte alsook op de lange termijn meegewogen te worden, omdat het medicijn vaak langere tijd gebruikt wordt. Hetzelfde geldt met betrekking tot de te verwachten verschijnselen bij afbouw.
Behandeling met medicatie dient minimaal een jaar voortgezet te worden. Naast voor- en nadelen van de medicamenteuze behandeling kunnen klinische overweging (zoals ernst, eerdere recidieven, comorbiditeit, familiaire kwetsbaarheid) een rol spelen om in samenspraak met de patiënt tot een beleid ten aanzien van de lange termijn te komen. Indien gekozen wordt voor afbouw is het advies om per 2-3 maanden 1 doseringsstap te verlagen. Bij onttrekkingsverschijnselen: langzamer afbouwen; bij recidiveren van de klachten: terug naar de dosering waarop het goed ging en langer continueren en onderhoudsbehandeling overwegen. Bij OCS is met regelmaat een minimale onderhoudsdosering nodig om op een acceptabel functioneringsniveau te blijven.
STAP 2
Indien een eerste SSRI of venlafaxine/duloxetine onvoldoende effectief is, of teveel of te hinderlijke bijwerkingen geeft, wordt geadviseerd over te stappen naar een andere SSRI of venlafaxine/duloxetine.
STAP 3
Indien stap 1 en 2 onvoldoende effectief waren, of teveel hinderlijke bijwerkingen geven, wordt geadviseerd over te stappen naar clomipramine. Alhoewel niet verder onderzocht na de vorige richtlijn blijft dit een zeer effectief middel bij de behandeling van OCS, alhoewel meer (noradrenerge) bijwerkingen ervaren kunnen worden. Een bloedspiegelbepaling van clomipramine en de metaboliet desmethylclomipramine kan, bij onvoldoende effectiviteit, zinvol zijn om de verhouding te bepalen. Bij een hogere desmethylclomipraminespiegel dan die van clomipramine is het advies fluvoxamine 25-50 mg toe te voegen, om de omzetting te vertragen (en de serotonerge heropnameremming sterker wordt).
STAP 4
Bij onvoldoende effectiviteit of teveel hinderlijke bijwerkingen van de SSRI’s, venlafaxine/duloxetine en clomipramine wordt aanbevolen om een antipsychoticum aan de clomipramine toe te voegen (aripiprazol, haloperidol, olanzapine, quetiapine, risperidon), in lage dosering. Het effect hiervan kan binnen enkele weken beoordeeld worden.
Bij een partieel effect op een SSRI of venlafaxine/duloxetine (stap 2) kan deze augmentatie met een antipsychoticum ook aan dit middel gedaan worden, voordat naar clomipramine overgegaan wordt.
STAP 5
Indien stap 1 tm 4 onvoldoende effectief waren of teveel hinderlijke bijwerkingen gaven, dan is additie van een glutamaterg middel het advies, zoals memantine, lamotrigine en topiramaat. Er is toenemend onderzoek beschikbaar dat de effectiviteit van deze behandelstap aantoont.
Overige aanbevelingen Obsessieve-compulsieve stoornis
Vanwege bewezen niet-effectiviteit beveelt de Werkgroep aan om lithium, buspiron en bupremorfine niet te gebruiken bij de farmacotherapie van OCS. Hetzelfde geldt voor benzodiazepinen, tenzij er een noodzaak is voor kortdurende sedatie.
Overwegingen
Kwaliteit van het bewijs
Aanvullingen van het bewijs vanuit de nieuwe richtlijn (2023).
- De effectiviteit van de SSRI’s en SNRI’s venlafaxine en duloxetine is verder onderbouwd.
- Bij onderlinge vergelijking van de SSRI’s en SNRI venlafaxine lijken er geen grote verschillen te zijn wat betreft effectiviteit en bijwerkingen/voortijdig stoppen met de behandeling.
- Effectiviteit van augmentatie aan een SSRI is het meest duidelijk bij antipsychotica, voor glutamaterge middelen (zoals memantine, lamotrigine, topiramaat) en pindolol. Pindolol is evenwel momenteel niet meer geregistreerd/niet meer beschikbaar in Nederland. Augmentatie met antipsychotica is het meeste onderzocht.
Balans tussen gewenste en ongewenste effecten
- Het effect van augmentatie met een antipsychoticum aan een SSRI/SNRI berust waarschijnlijk op andere neurobiologische effecten (namelijk het effect op dopaminerge neurotransmissie in het OCS netwerk van het brein) dan monotherapie met een antipsychoticum bij een van de angststoornissen (met name sedatie). Dit effect bij OCS wordt ook met niet-sedatieve antipsychotica bereikt.
Onderbouwing
Conclusies / Summary of Findings
Algemene effectiviteit farmacologische interventies versus placebo
OCS-symptomen
|
⊕⊕⊕Ο |
SSRI + SNRI resulteert waarschijnlijk in een vermindering van OCS-symptomen vergeleken met placebo bij volwassenen met OCS. Gosmann et al., 2021 |
|
⊕⊕ΟΟ |
Er lijkt geen verschil te zijn in de effecitiviteit van paroxetine ten opzichte van fluoxetine in het verminderen van OCS-symptomen bij volwassenen met OCS. Gosmann et al., 2021 |
|
⊕ΟΟΟ |
Bij deze middelen lijkt er geen verschil te zijn in effectiviteit ten opzichte van fluoxetine, maar de wetenschappelijke evidentie is zeer onzeker: SSRI’s: Sertraline, fluvoxamine, citalopram en escitalopram Gosmann et al., 2021 |
Effectiviteit en bijwerkingen van farmacotherapieën onderling
Bijwerkingen
|
⊕⊕ΟΟ |
Venlafaxine lijkt te resulteren in een lagere kans op bijwerkingen vergeleken met fluvoxamine bij volwassenen met OCS. Gosmann et al., 2021 |
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van de volgende middelen op de kans op bijwerkingen bij volwassenen met OCS:
Gosmann et al., 2021 |
Algemene effectiviteit en bijwerkingen SSRI + farma augmentatie versus placebo
OCS-symptomen
SSRI + antipsychotica
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van SSRI + olanzapine/ aripiprazole/ haloperidol/ quetiapine/ risperidone/ paliperidone op OCS-symptomen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
SSRI + glutamaterge middelen
|
⊕⊕ΟΟ |
SSRI + topiramaat/ memantine lijken te resulteren in een vermindering van OCS-symptomen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van SSRI + N-acetylcysteine/ lamotrigine op OCS-symptomen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
SSRI + TCA
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van SSRI + desipramine op OCS-symptomen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
SSRI + Opioïden
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van SSRI + buprenorfine op OCS-symptomen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
SSRI + stemmingsstabilisatoren
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van SSRI + lithium op OCS-symptomen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
SSRI + betablockers
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van SSRI + pindolol op OCS-symptomen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
SSRI + buspiron
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van SSRI + buspiron op OCS-symptomen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
SSRI + diverse middelen
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van SSRI + inositol/ riluzole op OCS-symptomen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van SSRI + riluzole op OCS-symptomen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
Bijwerkingen
SSRI + antipsychotica
|
⊕⊕ΟΟ |
Paliperidone lijkt te resulteren in een verminderde kans op bijwerkingen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van SSRI + olanzapine/ aripiprazole/ haloperidol/ quetiapine/ risperidon op bijwerkingen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
SSRI + glutamaterge middelen
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van SSRI + N-acetylcysteine/ lamotrigine/ topiramaat/ memantine op bijwerkingen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
SSRI + TCA
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van SSRI + desipramine op bijwerkingen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
SSRI + Opioïden
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van SSRI + buprenorfine op bijwerkingen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
SSRI + stemmingsstabilisatoren
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van SSRI + lithium op bijwerkingen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
SSRI + betablockers
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van SSRI + pindolol op bijwerkingen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
SSRI + buspiron
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van SSRI + buspiron op bijwerkingen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
SSRI + diverse middelen
|
⊕ΟΟΟ |
Het bewijs is zeer onzeker over het effect van SSRI + inositol/ riluzole op bijwerkingen vergeleken met placebo bij volwassenen met OCS. Zhou et al., 2019 |
Samenvatting literatuur
Algemene effectiviteit farmacologische interventies (Richtlijn 2013)
De conclusies en aanbevelingen van de tweede versie van de richtlijn (2013) gaven aan dat voor de OCS alle SSRI’s, venlafaxine en clomipramine effectieve middelen zijn. De geadviseerde middelen staan in de onderstaande tabel. Ofschoon geen vergelijkende studies voorhanden waren nam de richtlijncommissie aan dat alle aangegeven middelen even effectief zijn. Effectiviteit vormde dus geen keuzecriterium voor een bepaald middel bij volwassenen.
Bij onvoldoende respons op een van de SSRI’s of clomipramine werd geadviseerd additie van een antipsychoticum te overwegen (haloperidol, risperidon of quetiapine), aangezien bij een deel van de patiënten alsnog verbetering optreedt. Aangezien er waarschijnlijk langdurig zal moeten worden behandeld en van de klassieke antipsychotica bekend was dat zij op de lange termijn tardieve dyskinesie kunnen veroorzaken, hebben de moderne atypische middelen de voorkeur, alhoewel bij deze laatste het risico op metabool syndroom meegewogen diende te worden.
Kader 4. Overzicht middelen geadviseerd in de tweede versie van de richtlijn (2013)
|
De start-, en maximale doseringen per dag voor de SSRI’s |
Startdosering |
Maximale dosering |
|
citalopram |
20 mg |
40 mg |
|
escitalopram |
10 mg |
20 mg |
|
fluoxetine |
20 mg |
60 - 80 mg |
|
fluvoxamine |
50 mg |
250 - 300 mg |
|
paroxetine |
20 mg |
60 mg |
|
sertraline |
50 mg |
200 mg |
|
De start-, streef- en maximale doseringen per dag voor |
Startdosering |
Streefdosering |
Maximale dosering |
|
clomipramine |
25 mg |
150 mg |
250 mg |
|
venlafaxine |
75 mg |
150 mg |
225-300 mg |
Nieuwe evidentie 2023; effectiviteit farmacologische interventies (Richtlijn 2023).
Voor het in kaart brengen van de effectiviteit van verschillende farmacologische interventies bij volwassenen is er gebruik gemaakt van een netwerk meta-analyse uitgevoerd door Gosmann en collega’s (2021).
Beschrijving Gosmann2021
In deze netwerk meta-analyse is de effectiviteit onderzocht van SSRI’s en SNRI’s voor de behandeling van obsessieve-compulsieve stoornis (OCS) en angststoornissen bij volwasssen. Er zijn 135 RCT’s (n = 30.245) geïncludeerd. Inclusie criteria waren: a) dubbel blind, gerandomiseerd gecontroleerde trials; b) Een diagnose van angststoornis, OCS of stress-gerelateerde stoornis volgens de DSM-III, DSM-IV, DSM-IV-TR, DSM-5, RDoC of de ICD-10 criteria; c) patiënten met comorbide stoornissen; d) alleen monotherapieën. De primaire uitkomst is internaliserende symptomen (emoties en gedragingen gerelateerd aan angst en reactie op stress). Deze uitkomst is een samenvoeging van metingen van GAS, sociale fobie, paniekstoornis, agorafobie, specifieke fobie, separatie angst stoornis, evenals somatische symptomen en algehele ernst van symptomen. Secundaire uitkomsten waren voortijdig gestopt met de behandeling (elke oorzaak), voortijdig gestopt met de behandeling (bijwerkingen) en clusters van symptomen gebaseerd op de DSM-5 diagnostische criteria (GAS, sociale fobie, somatische symptomen, paniekstoornis, specifieke fobie, OCS en PTSS). Van de 135 RCT’s, includeerden 35 studies (25.93%) patiënten met GAS, 28 (20.74%) met sociale fobie, 25 (18.52%) met paniekstoornis, 22 (16.30%) met OCS, 20 (14.81%) met PTSS en 5 (3.70%) met meerdere stoornissen. De gemiddelde leeftijd in de interventie groepen was 36.1 jaar (SD = 9.50), tegenover een gemiddelde leeftijd van 35.7 jaar in de placebogroepen. Bovendien, zijn er 117 onderzoeken gericht op volwassenen en 18 gericht op kinderen en adolescenten. Het gemiddelde aantal vrouwen in de interventie groepen was 55.1% en 53.8% in de placebo groepen.
Wanneer er gekeken wordt naar de effectiviteit van de verschillende farmacotherapeutische interventies bij volwassenen werd er een significant effect gevonden voor SSRI’s + SNRI’s in vergelijking met placebo in het verminderen van OCS DSM-specifieke symptomen. Omdat er in deze meta analyse niet gekeken is naar het effect op OCS symptomen specifiek kan er geen uitspraak gedaan worden over individuele middelen. Zie tabel 13 voor een overzicht van deze resultaten met bijbehorende GRADING.
Tabel 13 Effectiviteit, reductie in symptomen (farmacotherapie versus placebo)
|
Middel |
Effectiviteit SMD (95% BI) GRADE SCORE |
|
SSRI's + SNRI's (OCS symptomen) |
-0.59 (-0.7,-0.48)+++a |
a Kans op vertekening: er is onduidelijkheid over randomisatie (73% vd. RCT’s), blinding of outcome assessment (59% vd. RCT’s), allocation concealment (75% vd. RCT’s) en er is sprake van attrition bias (37% vd. RCT’s) en reporting bias (29% vd. RCT’s)
Verschil in effectiviteit en bijwerkingen tussen verschillende farmacologische interventies.
In Gosmann2021 heeft men doormiddel van een regressie analyse gekeken of er een verschil in effectiviteit was tussen de SSRI’s in termen van OCS symptoom reductie bij volwassenen, er bleek geen significant verschil te zijn (zie tabel 15). Wanneer er naar het optreden van bijwerkingen wordt gekeken dan werd fluvoxamine, in vergelijking met andere soorten medicatie (behalve met fluoxetine), geassocieerd met hogere uitval (voortijdig stoppen met de behandeling) door bijwerkingen (zie tabel 16). NB. Bij deze uitkomst maat zijn alle angst- en dwangstoornissen geïncludeerd.
Tabel 15 Directe vergelijkingen effectiviteit (OCS symptoom reductie) tussen middelen (middel A vs. fluoxetine)
|
|
|
Effectiviteit SMD (95% BI) GRADE SCORE |
|
Middel |
Aantal RCT’s (aantal deelnemers) |
Fluoxetine (referentie middel) |
|
Sertraline |
5 RCT’s (n=414) |
0.05 (-0.26, 0.36) + a,b, |
|
Paroxetine |
6 RCT’s (n=854) |
-0.11 (-0.41, 0.19) ++ a,c |
|
Fluvoxamine |
5 RCT’s (n=299) |
-0.21 (-0.55, 0.12) + a,c,d |
|
Citalopram |
1 RCT (n=390) |
-0.33 (-0.77, 0.10) + a,c,d |
|
Escitalopram |
1 RCT (n=232) |
-0.47 (-0.93 , 0.001) + a,c,d |
a Kans op vertekening: er is onduidelijkheid over randomisatie, blinding of outcome assessment, allocation concealment, attrition bias en reporting bias
b Ernstige onnauwkeurigheid: BI valt zowel in het voordeel als het nadeel van de interventie
c Onnauwkeurigheid: het 95% BI valt in niet-klinisch relevant gebied
d klein aantal deelnemers (n <400)
Tabel 16 Directe vergelijkingen drop-out (adverse events) tussen middelen (middel A vs. middel B). OR’s groter dan 1 geven een voordeel aan voor de in de kolom genoemde interventie
|
|
Drop-out (adverse events) OR (95% Crl) GRADE SCORE |
||||||
|
Middel |
Fluoxetine |
Sertraline |
Paroxetine |
Fluvoxamine |
Citalopram |
Escitalopra |
Venlafaxine |
|
Sertraline |
1.04 (0.39, 2.77) + a,b,c |
|
|
|
|
|
|
|
Paroxetine |
0.88 (0.37, 2.08) + a,b,c |
0.85 (0.52, 1.38) + a,b,c |
|
|
|
|
|
|
Fluvoxamine |
2.65 (0.78, 9.03) + a,b,d |
2.56 (1.07, 6.13) + a,b,c |
3.01 (1.20, 7.57) + a,b,c |
|
|
|
|
|
Citalopram |
0.53 (0.16, 1.78) + a,b,c |
0.51 (0.18, 1,48) + a,b,c |
0.60 (0.23, 1.60) + a,b,c |
0.20 (0.05, 0.75) + a,b,c |
|
|
|
|
Escitalopram |
0.69 (0.27, 1.82) + a,b,c |
0.67 (0.33, 1.36) + a,b,c |
0.79 (0.44, 1,42) + a,b,c |
0.26 (0.09, 0.76) + a,b,c |
1.31 (0.46, 3.71) + a,b,c |
|
|
|
Venlafaxine |
0.74 (0.29, 1.87) + a,b,c |
0.71 (0.43, 1.18) + a,b,d |
0.84 (0.58, 1.23) + a,b,d |
0.28 (0.11, 0.70)++ a,b |
1.39 (0.50, 3.85) + a,b,c |
1.07 (0.59, 1.93) + a,b,c |
|
|
Duloxetine |
0.76 (0.25, 2.31) + a,b,c |
0.73 (0.36, 1.49) + a,b,c |
0.86 (0.41, 1.81) + a,b,c |
0.29 (0.11, 0.77) + a,b,d |
1.43 (0.44, 4.66) + a,b,c |
1.09 (0.48, 2.45) + a,b,c |
1.02 (0.51, 2.04) + a,b,c |
a Kans op vertekening: er is onduidelijkheid over randomisatie, blinding of outcome assessment, allocation concealment, attrition bias en reporting bias
b Indirectheid: alle stoornissen worden mee genomen
c Ernstige onnauwkeurigheid: BI valt zowel in het voordeel als het nadeel van de interventie
d Onnauwkeurigheid: het 95% BI valt in niet-klinisch relevant gebied
Augmentatiestrategieën
Farmacologische augmentatie bij SSRI’s
In een netwerk meta-analyse uitgevoerd door Zhou en collega’s (2019), is de effectiviteit onderzocht van augmentatie middelen voor SSRI’s voor de behandeling van therapie-resistente OCS bij volwassenen.
Beschrijving Zhou2019
Er zijn 34 RCT’s (n = 1.216) geïncludeerd. Inclusie criteria waren: a) patiënten met een primaire OCS diagnose volgens gestandaardiseerde diagnostische criteria, die niet of deels reageren op minimaal 1 trial van SSRI’s; b) interventies die augmentatie middelen gebruiken voor doorlopend SSRI gebruik; c) vergeleken met placebo of andere augmentatie middelen; d) de ernst van symptomen werd gemeten met behulp van de Yale-Brown Obsessive Compulsive Scale (YBOCS); e) dubbel blinde RCT’s met een parallele of crossover design. Antipsychotica was onderzocht door 47,1% van de RCT’s, gevolgd door glutamaterge middelen (32,4%) en andere middelen (20,5%).
De primaire uitkomst is effectiviteit gemeten met de Yale-Brown Obsessive Compulsive Scale (YBOCS) en de secundaire uitkomsten waren voortijdig gestopt met de behandeling door bijwerkingen en voortijdig gestopt met de behandeling door alle oorzaken.
De netwerk meta-analyse liet zien dat memantine, risperidon, topiramaat, lamotrigine en aripiprazol significant effectiever zijn in het verminderen van OCS-symptomen dan placebo.
In de pairwise meta-analyse zijn verschillende geneesmiddelgroepen vergeleken met placebo. Hier kwam uit dat zowel antipsychotica als glutamaterge middelen significant effectiever zijn dan placebo. Zie tabel 17 voor een overzicht van deze resultaten en bijbehorende grading.
Verder bleek uit de netwerk meta-analyse dat er geen significante verschillen in voortijdig gestopt met de behandeling (alle oorzaken) waren tussen de verschillende middelen ten opzichte van placebo. Wel lieten topiramaat en paliperidone een significant verhoogd risico zien vergeleken met placebo op voortijdig gestopt met de behandeling door bijwerkingen.
Uit de pairwise meta-analyse naar geneesmiddelgroepen lieten zowel antipsychotica als glutamaterge middelen een verhoogd risico zien ten opzichte van placebo op voortijdig gestopt met de behandeling door bijwerkingen. Zie tabel 18 voor een overzicht van deze resultaten en bijbehorende GRADING.
Tabel 18 Algemeen effect (SSRi + farma augmentatie versus placebo). MD scores kleiner dan 0 indiceren een voordeel voor de interventie (met uitzondering van riluzole). OR scores groter dan 1 indiceren een voordeel voor de interventie (met uitzondering van pindolol)
|
SSRI + Middel |
Effectiviteit (symptoom reductie) |
Drop-out door bijwerkingen |
|
Antipsychotica |
|
|
|
Olanzapine |
-2.85 (-8.65 , 2.92) + a,b,d |
0.46 (0.05-3.05) + a,b,d |
|
Aripiprazole |
-5.14 (-9.95 , -0.28) + a,b,c |
0.60 (0.03-12.86+ a,b,d |
|
Haloperidol |
-5.07 (-13.22 , 3.07) + a,b,d |
0.86 (0.00->100) + a,b,d |
|
Quetiapine |
-3.88 (-7.75 , 0.07) + a,b,d |
0.26 (0.04-1.20) + a,b,c |
|
Risperidone |
-4.47 (-8.75 , -0.17) + a,b,c |
0.82 (0.11-4.32) + a,b,d |
|
Paliperidone |
-2.12 (-12.00 , 7.75) + a,b,d |
0.02 (0.00-0.47) ++ a,b |
|
Glutamaterge middelen |
|
|
|
Topiramaat |
-6.05 (-10.89 , -1.20) ++ a,b |
0.20 (0.04-0.85) + a,b,c |
|
Memantine |
-8.94 (-14.42 , -3.42) ++ a,b |
0.97 (0.05-18.19) + a,b,d |
|
N-acetylcysteine |
-3.14 (-8.84 , 2.65) + a,b,d |
0.16 (0.00-1.81) + a,b,d |
|
Lamotrigine |
-6.07 (-11.61 , -0.50) ++ a,b,c |
0.12 (0.00-1.20) + a,b,c |
|
TCA |
|
|
|
Desipramine |
-3.09 (-14.03 , 7.82) + a,b,d, |
|
|
Opioïden |
|
|
|
Bupremorphine |
-2.77 (-10.59 , 5.02) + a,b,d |
1.04 (0.00->100) + a,b,d |
|
Stemmings-stabilisatoren |
|
|
|
Lithium |
-0.36 (-6.35 , 5.58) + a,b,d |
1.21 (0.02-87.64)+ a,b,d |
|
Betablocker |
|
|
|
Pindolol |
-7.37 (-15.39 , 0.66) + a,b,d |
0.08 (0.00-2.20) + a,b,d |
|
Partiële 5HT1A-agonist |
|
|
|
Buspiron |
0.90 (-7.57 , 9.39) + a,b,d |
1.53 (0.00->100) + a,b,d |
|
Divers |
|
|
|
Inositol |
-2.56 (-12.81 , 7.67) + a,b,d |
|
|
Riluzole |
1.11 (-7.21 , 9.47) + a,b,d |
1.12 (0.00->100) + a,b,d |
a Kans op vertekening: er is onduidelijkheid over random sequence generation, allocation concealment en blinding of outcome assesment bij de helft van de geïncludeerde studies, bij een vierde deel van de studies is er onduidelijkheid over blinding of participants en bij een derde deel van de studies is er sprake van selective reporting en andere bias
b Inconsistentie: er is sprake van heterogeniteit
c Onnauwkeurigheid: het 95% BI valt in niet-klinisch relevant gebied
d Ernstige onnauwkeurigheid: het 95% BI is in het voordeel van zowel de behandel- als controlegroep
Zoeken en selecteren
Zoekstrategie en selectie van studies
PICO (Review Protocol is opgenomen als Bijlage).
|
Patient/Population (P) |
|
|
Intervention (I) |
|
|
Comparator/Control http |
|
|
Outcome (O) |
Cruciaal:
Belangrijk: • Respons |
Selectie van studies
Op 12 april 2022 is er een zoekactie uitgevoerd in de Medline, PsycInfo, Embase en Cochrane databases. De specifieke searchtermen zijn opvraagbaar. Neem hiervoor contact op met de Richtlijnendatabase. Er is specifiek gekeken naar systematische reviews en meta-analyses (van RCT’s). Na beoordeling op titel en abstract bleven er 17 referenties (Patterson et al., 2016; Steenen et al., 2016; Cuijpers et al., 2014; Roosenfield et al., 2016; Wang et al., 2016; Carl et al., 2020; Kong et al., 2020; Brakoulias et al., 2015; Tao et al., 2022; Gosmann et al., 2021; Zhou et al., 2019; Guzick et al., 2018; Sassano-Higgings et al., 2015; Du et al., 2021; Masdrakis et al., 2021; Moylan et al., 2011; Williams et al., 2020) over voor de selectie op basis van de volledige teksten. Het lezen van volledige teksten leidde tot de exclusie van 9 artikelen (Carl et al., 2020; Patterson et al., 2016; Steenen et al., 2016; Cuijpers et al., 2014; Roosenfield et al., 2016; Wang et al., 2016; Brakoulias et al., 2015; Sassano-Higgings et al., 2015; Masdrakis et al., 2021). In totaal zijn er 8 artikelen (Kong et al., 2020; Tao et al., 2022; Gosmann et al., 2021; Zhou et al., 2019; Guzick et al., 2018; Du et al., 2021; Moylan et al., 2011; Williams et al., 2020) overgebleven die relevant waren en binnen de inclusiecriteria pasten, waarvan bij de artikelen van Tao et al., 2022; en Wang et al (2017) (deels) over kinderen en adolescenten gingen. Deze studies worden in de volgende paragrafen per afzonderlijke angststoornis beschreven.
Referenties
- Balasubramaniam, M., Joshi, P., Alag, P., Gupta, S., Maher, S., Tampi, D., . . . Tampi, R. R. (2019). Antidepressants for anxiety disorders in late-life: A systematic review. Ann Clin Psychiatry, 31(4), 277-291.
- Brakoulias, V., Eslick, G. D., & Starcevic, V. (2015). A meta-analysis of the response of pathological hoarding to pharmacotherapy. Psychiatry Research, 229(1-2), 272276. doi:10.1016/J.PSYCHRES.2015.07.019
- Burschinski, A., Schneider-Thoma, J., Chiocchia, V., Schestag, K., Wang, D., Siafis, S., . . . Leucht, S. (2023). Metabolic side effects in persons with schizophrenia during mid- to long-term treatment with antipsychotics: a network meta-analysis of randomized controlled trials. World Psychiatry, 22: 116-128
- Carl, E., Witcraft, S. M., Kauffman, B. Y., Gillespie, E. M., Becker, E. S., Cuijpers, P., . . . Powers, M. B. (2019). Psychological and pharmacological treatments for generalized anxiety disorder (GAD): a meta-analysis of randomized controlled trials. Cognitive Behaviour Therapy, 49(1):1-21. doi:10.1080/16506073.2018.1560358
- Du, Y., Du, B., Diao, Y., Yin, Z., Li, J., Shu, Y., Zhang, Z., & Chen, L. (2021). Comparative efficacy and acceptability of antidepressants and benzodiazepines for the treatment of panic disorder: A systematic review and network meta-analysis. Asian Journal of Psychiatry, 60, 102664. doi:10.1016/J.AJP.2021.102664
- Gonçalves, D. C., & Byrne, G. J. (2012). Interventions for generalized anxiety disorder in older adults: systematic review and meta-analysis. J Anxiety Disord, 26(1), 1-11. doi:10.1016/j.janxdis.2011.08.010
- Gosmann, N. P., de Abreu Costa, M., de Barros Jaeger, M., Souza, L. M., Júlia Frozi, Spanemberg, L., Gus, G. M., . . . Abrahão, G. S. (2021). Selective serotonin reuptake inhibitors, and serotonin and norepinephrine reuptake inhibitors for anxiety, obsessive-compulsive, and stress disorders: A 3-level network meta-analysis. PLOS Medicine. doi:10.1371/journal.pmed.1003664
- Guzick, A. G., Cooke, D. L., Gage, N., & McNamara, J. P. H. (2018). CBT-Plus: A meta-analysis of cognitive behavioral therapy augmentation strategies for obsessive-compulsive disorder. Journal of Obsessive-Compulsive and Related Disorders, 19, 6- 14. doi:10.1016/J.JOCRD.2018.07.001
- Højlund, M., Andersen, K., Ernst, M. T., Correll, C. U., & Hallas, J. (2022). Use of low?dose quetiapine increases the risk of major adverse cardiovascular events: results from a nationwide active comparator?controlled cohort study. World Psychiatry, 21(3), 444-451. doi:10.1002/wps.21010
- Kong, W., Deng, H., Wan, J., Zhou, Y., Zhou, Y., Song, B., & Wang, X. (2020). Comparative remission rates and tolerability of drugs for generalised anxiety disorder: a systematic review and network meta-analysis of double-blind randomized controlled trials. Frontiers in Pharmacology, 11, 580858. doi:10.3389/fphar.2020.580858
- Masdrakis, V. G., & Baldwin, D. S. (2021). Anticonvulsant and antipsychotic medications in the pharmacotherapy of panic disorder: a structured review. Therapeutic Advances in Psychopharmacology 11:20451253211002320 . doi:10.1177/20451253211002320
- Moylan, S., Staples, J., Ward, S. A., Rogerson, J., Stein, D. J., & Berk, M. (2011). The efficacy and safety of alprazolam versus other benzodiazepines in the treatment of panic disorder. Journal of Clinical Psychopharmacology, 31(5), 647-652. doi:10.1097/JCP.0B013E31822D0012
- Patterson, B., & Van Ameringen, M. (2016). Augmentation strategies for treatment-resistant anxiety disorders: a systematic review and meta-analysis. Depression and Anxiety, 33(8), 728-736. doi:10.1002/DA.22525
- Pinquart, M., & Duberstein, P. R. (2007). Treatment of anxiety disorders in older adults: a meta-analytic comparison of behavioral and pharmacological interventions. Am J Geriatr Psychiatry, 15(8), 639-651. doi:10.1097/JGP.0b013e31806841c8
- Rosenfield, D., Smits, J. A. J., Hofmann, S. G., Mataix-Cols, D., Fernández De La Cruz, L., . . . Otto, A. M. (2019). Changes in Dosing and Dose Timing of D-Cycloserine Explain Its Apparent Declining Efficacy for Augmenting Exposure Therapy for Anxiety-related Disorders: An Individual Participant-data Meta-analysis. doi:10.1016/j.janxdis.2019.102149
- Sassano-Higgins, S. A., & Pato, M. T. (2016). Pindolol augmentation of selective serotonin reuptake inhibitors and clomipramine for the treatment of obsessive-compulsive disorder: A meta-analysis. Journal of Pharmacology and Pharmacotherapeutics, 6(1), 36-38. doi:10.4103/0976-500X.149143
- Steenen, S. A., van Wijk, A. J., van der Heijden, G. J., van Westrhenen, R., de Lange, J., & de Jongh, A. (2016). Propranolol for the treatment of anxiety disorders: Systematic review and meta-analysis. Journal of Psychopharmacology, 30(2), 128-139. doi:10.1177/0269881115612236
- Tao, Y., Li, H., Li, L., Zhang, H., Xu, H., Zhang, H., . . . Yin, L. (2022). Comparing the efficacy of pharmacological and psychological treatment, alone and in combination, in children and adolescents with obsessive-compulsive disorder: A network meta-analysis. Journal of Psychiatric Research, 148, 95-102. doi:10.1016/J.JPSYCHIRES.2022.01.057
- Wang, Z., H Whiteside, S. P., Sim, L., Farah, W., Morrow, A. S., Alsawas, M., . . . Hassan Murad, M. (2017). Comparative Effectiveness and Safety of Cognitive Behavioral Therapy and Pharmacotherapy for Childhood Anxiety Disorders A Systematic Review and Meta-analysis. JAMA Pediatrics, 171(11), 1049-1056. doi:10.1001/jamapediatrics.2017.3036
- Wetherell, J. L., Petkus, A. J., White, K. S., Nguyen, H., Kornblith, S., Andreescu, C., . . . Lenze, E. J. (2013). Antidepressant medication augmented with cognitive-behavioral therapy for generalized anxiety disorder in older adults. Am J Psychiatry, 170(7), 782-789. doi:10.1176/appi.ajp.2013.12081104
- Williams, T., Mccaul, M., Schwarzer, G., Cipriani, A., Stein, D. J., & Ipser, J. (2020). Pharmacological treatments for social anxiety disorder in adults: a systematic review and network meta-analysis. Oxford Health NHS Foundation Trust, Warneford Hospital, 32(4). doi:10.1017/neu.2020.6
- Zhou, D. D., Zhou, X. X., Li, Y., Zhang, K. F., Lv, Z., Chen, X. R., . . . Kuang, L. (2019). Augmentation agents to serotonin reuptake inhibitors for treatment-resistant obsessive-compulsive disorder: A network meta-analysis. Progress in Neuro-Psychopharmacology and Biological Psychiatry, 90, 277-287. doi:10.1016/J.PNPBP.2018.12.
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 04-09-2024
Beoordeeld op geldigheid : 04-03-2024
Algemene gegevens
In opdracht van de Nederlandse Vereniging voor Psychiatrie (NVvP) en Stichting Kwaliteitsgelden Medisch Specialisten (SKMS) is de multidisciplinaire richtlijn Angst- en Dwangstoornissen voor de vierde maal geüpdatet en gereviseerd van november 2020 tot en met mei 2023. De ontwikkeling van de richtlijn werd methodologisch en organisatorisch ondersteund door het Trimbos-instituut.
Doel en doelgroep
De multidisciplinaire richtlijn Angst- en Dwangstoornissen geeft aanbevelingen en handelingsinstructies voor de samenwerking, diagnostiek en behandeling van volwassenen, kinderen en ouderen met een angst- of dwangstoornis. De richtlijn geeft aanbevelingen ter ondersteuning van de praktijkvoering van alle professionals die betrokken zijn bij de zorgverlening aan deze groepen patiënten. Op basis van de resultaten van wetenschappelijk onderzoek en praktijkoverwegingen geeft de richtlijn een overzicht van goed (‘optimaal’) handelen als waarborg voor kwalitatief hoogwaardige zorg. De richtlijn kan tevens richting geven aan de onderzoeksagenda voor wetenschappelijk onderzoek op het gebied van angststoornissen.
De richtlijn geeft aanbevelingen bij de diagnostiek en behandeling van een angst- of dwangstoornis. De aanbevelingen van de richtlijn moeten worden vertaald naar de lokale situatie in een instelling of behandelteam. Het opstellen van lokale zorgprogramma’s en andere vormen van werkkaders op basis van deze richtlijn wordt door de werkgroep aangemoedigd, omdat dat voor de implementatie van de in de richtlijn beschreven optimale zorg bevorderlijk is.
Deze multidisciplinaire richtlijn is een kwaliteitsinstrument en een beslissingsondersteunend instrument bij (gezamenlijke) beslissingen over het behandelbeleid. De richtlijn geeft aanbevelingen over het in te zetten en te volgen behandelbeleid, ter ondersteuning van de dagelijkse praktijkvoering.
Samenstelling werkgroep
De Multidisciplinaire richtlijn Angst- en Dwangstoornissen is ontwikkeld door de gelijknamige werkgroep, in opdracht van de Nederlandse Vereniging voor Psychiatrie (NVvP) en Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
De werkgroep bestond uit: psychiaters, psychologen, verpleegkundigen, huisartsen en ervaringsdeskundigen, welke door de respectievelijke beroepsverenigingen en familie- en patiëntenverenigingen werden afgevaardigd. Voorafgaande aan het ontwikkeltraject werden kennismakingsgesprekken gevoerd met verscheidene kandidaat leden voor de werkgroep. Uit deze groep belangstellenden werden de huidige werkgroepleden geselecteerd. Naast de werkgroep waren enkele adviseurs betrokken, welke delen hebben meegeschreven en die werd gevraagd voorafgaand aan de commentaarfase schriftelijk te reageren op onderdelen van de concepttekst. Deze adviseurs konden tevens worden gevraagd om tijdens een werkgroepbijeenkomst mee te denken over een specifieke uitgangsvraag. De werkgroep werd methodologisch en organisatorisch ondersteund door het technisch team van het Trimbos-instituut. Dit technisch team bestond uit een projectleider, informatiespecialist, literatuur reviewers, een notulist en een projectassistente. Onderstaande schema's geven een overzicht van de samenstelling van de werkgroep, de adviseurs en het ondersteunend technisch team. Alle werkgroepleden rapporteerden bij aanvang hun mogelijke belangenverstrengelingen en aan het begin van elke vergadering werd hen gevraagd of hier wijzigingen in waren opgetreden.
Leden Werkgroep (op alfabetische volgorde)
|
|
Naam |
Organisatie |
Beroepsvereniging |
|
1. |
Ton van Balkom (voorzitter) |
GGZinGeest AmsterdamUMC (VUMC) |
Psychiater, NVvP |
|
2. |
Neeltje Batelaan (vice-voorzitter) |
GGZinGeest AmsterdamUMC (VUMC) |
Psychiater, NVvP |
|
3. |
Martin Beeres |
Radboud MC |
Huisarts, NHG |
|
4. |
Gert-Jan Hendriks |
Pro Persona |
Psychiater, NVVP (ouderen) |
|
5. |
Mirjam Kampman |
Pro Persona |
Psycholoog, NIP (?) |
|
6. |
Tessa Magnée |
Huisartspraktijk |
POH-GGZ, LVPOHGGZ |
|
7. |
Inez Mijsberg |
Dimence |
Verpleegkundige, V&VN |
|
8. |
Maaike Nauta |
RUG |
Psycholoog, NIP (?) (kinderen) |
|
9. |
Lieke van Noord |
Angst, Dwang en Fobie Stichting |
Ervaringsdeskundige |
|
10. |
Patricia van Oppen |
GGZinGeest AmsterdamUMC (VUMC) |
Psycholoog, NVGzP |
|
11. |
Koen Schruers |
Maastricht University |
Psychiater, NVvP |
|
12. |
Sako Visser |
UVA |
Psycholoog, NIP |
|
13. |
Irene van Vliet |
LUMC |
Psychiater, NVvP |
Adviseurs
|
Hoofdstuk |
Naam |
Organisatie |
Beroep |
|
Farmacotherapie |
Chaim Huyser |
Levvel |
Kinder-en jeugd psychiater |
|
Werkhervatting |
Irene Lindenburg |
UWV |
Verzekeringsarts, NVVG |
|
Werkhervatting |
Giny Norder |
Arbo Unie |
Bedrijfsarts, NVAB |
|
Farmacotherapie / Neuromodulatie |
Chris Bervoets |
UPC KU Leuven |
Psychiater |
|
Onderhoudsbehandeling (coauteur van dit hoofdstuk) |
Leonieke Kranenburg |
Erasmus MC |
Psycholoog |
Methodologische ondersteuning
|
Naam
|
Ondersteuning |
|
Danielle van Duin / Piet Post |
Projectleider, Trimbos-instituut |
|
Egbert Hartstra |
Reviewer, Trimbos-instituut |
|
Matthijs Oud |
Reviewer, Trimbos-instituut |
|
Elena Vos |
Reviewer, Trimbos-instituut |
|
Erika Papazoglou |
Reviewer, Trimbos-instituut |
|
Bram Zwanenburg |
Reviewer, Trimbos-instituut |
|
Lex Hulsbosch |
Reviewer, Trimbos-instituut |
|
Rikie Deurenberg |
Informatiespecialist, namens Trimbos-instituut |
|
Chris van der Grinten |
Notulist, namens Trimbos-instituut |
|
Joyce Huls / Nelleke van Zon / Isa Reijgersberg |
Project assistent, Trimbos-instituut |
In totaal kwam de werkgroep Angststoornissen voorafgaand aan de commentaarfase 17 keer bijeen in een periode 30 maanden (november 2020 - april 2023). Daarnaast kwamen zij in zogeheten ‘topic-groepen’ nog in subgroepjes bijeen. In deze periode werden de stappen van de methodiek voor evidence-based richtlijnontwikkeling (EBRO) doorlopen. De informatiespecialist verrichtte in overleg met de werkgroepleden op systematische wijze literatuuronderzoek en de reviewers maakten een selectie in de gevonden onderzoeken (zie voor informatie over de zoekstrategie en de selectiecriteria: het reviewprotocol). De reviewers beoordeelden de kwaliteit en inhoud van de aldus verkregen literatuur en verwerkten deze in evidence tabellen, GRADE profielen, beschrijvingen van de wetenschappelijke onderbouwing en wetenschappelijke (gewogen) conclusies. Leden van de werkgroep gingen op basis van de gevonden literatuur met elkaar in discussie over praktijkoverwegingen (beschreven in de sectie “Praktijkoverwegingen”) en aanbevelingen. De werkgroepleden schreven samen met het technisch team van het Trimbos-instituut de concepttekst, welke ter becommentariëring openbaar is gemaakt. De ontvangen commentaren zijn verwerkt in een commentaartabel, die tijdens een werkgroepbijeenkomst is besproken. Na het doorvoeren van op deze bijeenkomst voorgestelde wijzigingen is de definitieve richtlijn aan de opdrachtgever aangeboden.
Methode ontwikkeling
Evidence based
Implementatie
Recent onderzoek laat zien dat er bij trajecten rond kwaliteit van zorg voornamelijk aandacht is voor de ontwikkeling van de kwaliteitstandaard. Planmatige opgezette en onderbouwde invoering komt maar heel beperkt van de grond. Hierop dient gericht te worden aangestuurd door financiers, zodat hier al bij de start geld voor beschikbaar is. De Regieraad voor richtlijntrajecten onderschrijft dan ook een programmatische aanpak van de ontwikkeling, invoering én evaluatie van kwaliteitsstandaarden inclusief (financiële en organisatorische) middelen, om het gebruik van de standaarden te stimuleren, monitoren en evalueren. TNO, CBO en het Trimbos-instituut besloten deze opdracht samen uit te voeren, met als doel de complementaire inzichten en expertise te vertalen in een gemeenschappelijke visie op richtlijnen en andere kwaliteitsstandaarden. Dit resulteerde in een praktisch instrument voor een analyse van richtlijntrajecten: Kwaliteit Richtlijnontwikkeling, Invoering en Evaluatie (KRIE).
Werkwijze
Afbakening
Deze richtlijn betreft diagnostiek en behandeling van mensen met een angst- en of dwangstoornis. Studies over alle levensfases (kinderen, adolescenten, volwassenen en ouderen) zijn meegenomen. In de richtlijn is gezocht naar meta-analyses en belangrijke gecontroleerde studies van 2013 tot en met heden (2022). Nog niet gepubliceerde onderzoeken zijn niet meegenomen (wel onderzoeken 'in press'). Zie voor meer informatie over de afbakening van de richtlijn in de bijlagen. Per hoofdstuk is een bijlage opgenomen met toelichting over de gebruikte reviewstrategie (reviewprotocollen per uitgangsvraag).
Uitgangsvragen
De richtlijn is ontwikkeld op geleide van uitgangsvragen, die gebaseerd zijn op knelpunten die worden ervaren rondom samenwerking, diagnostiek en behandeling van mensen met een angst- of dwangstoornis.
De richtlijn is geen leerboek waarin zoveel mogelijk beschikbare kennis over een onderwerp wordt opgenomen, maar een document met praktische aanbevelingen rondom knelpunten uit de praktijk. Dat betekent dat praktijkproblemen het uitgangspunt zijn van de teksten in de richtlijn. Er wordt niet ingegaan op de vraag door wie die problemen moeten worden aangepakt of opgelost. De richtlijn is een document waarin staat hoe optimale diagnostiek en behandeling er inhoudelijk uitziet en in welke vorm een interventie het beste aangeboden kan worden. In deze richtlijn worden de hieronder beschreven ‘klinische uitgangsvragen’ behandeld in de verschillende hoofdstukken.
Uitgangsvragen in de richtlijn Angststoornissen
|
Hoofdstuk |
Uitgangsvragen |
|
Hoofdstuk 3 Classificatie en Diagnostiek |
|
|
Hoofdstuk 4 Psychotherapie (breed) |
|
|
Hoofdstuk 5 EMDR bij angst |
|
|
Hoofdstuk 6 Vorm van aanbieden |
|
|
Hoofdstuk 7 Farmacotherapie
|
|
|
Hoofdstuk 8 Combinatiebehandeling |
|
|
Hoofdstuk 9 Neuromodulatie |
|
|
Hoofdstuk 10 Maatschappelijk participatie / werkhervatting |
|
|
Hoofdstuk 11 Onderhoudsbehandeling |
|
|
Hoofdstuk 12 Co-morbiditeit |
|
Methode: wetenschappelijke onderbouwing
De richtlijn Angststoornissen is ontwikkeld volgens de methodiek van de evidence based richtlijnontwikkeling (EBRO).
Zoekstrategie
Om de klinische uitgangsvragen te beantwoorden is door de informatiespecialist, in overleg met de werkgroepleden, op systematische wijze literatuuronderzoek verricht en is een selectie gemaakt binnen de gevonden onderzoeken volgens vooraf vastgestelde selectiecriteria. Er is gezocht naar bestaande (buitenlandse) evidence-based richtlijnen voor de zorg aan mensen met angststoornissen en dwangstoornisseen, systematische reviews en oorspronkelijke onderzoeken. In de literatuursearches is gezocht naar literatuur in de Engelse, Nederlandse, Franse, en Duitse taalgebieden. Voor het zoeken naar publicaties is gebruik gemaakt van de volgende informatiebronnen:
- Cochrane Database of Systematic Reviews (CDSR)
- Psychological Information Database (PsycINFO)
- PubMed
- Cumulative Index to Nursing and Allied Health Literature (CINAHL)
- Excerpta Medica database (Embase)
Selectiestrategie
Bij de selectie van artikelen zijn de volgende criteria gehanteerd:
- Geeft het onderwerp van het gevonden onderzoek voldoende antwoord op de uitgangsvraag: worden de binnen GRADE vastgestelde kritische en belangrijke uitkomstmaten in het onderzoek geëvalueerd? (zie voor meer informatie over GRADE verderop in deze paragraaf);
- Sluit de doelgroep van het gevonden onderzoek voldoende aan bij de doelgroep van de richtlijn;
- Is er sprake van een meta-analyse, systematic-review, randomised controlled trial (RCT), cohort onderzoek, cross-sectioneel onderzoek, patiëntcontrole onderzoek of wetenschappelijke verantwoord kwalitatief onderzoek? Bij een longitudinaal onderzoek: Is er sprake van een voldoende lange follow-up periode?;
- Zie voor meer informatie over de zoekstrategie de bijlagen per hoofdstuk en voor meer informatie over de selectiecriteria per uitgangsvraag de reviewprotocollen in de bijlagen per hoofdstuk.
Beoordeling van de kwaliteit van het bewijs
Studies werden door twee personen beoordeeld op het risico op bias met behulp van de Cochrane Collaboration Risico van Bias Assessment Tool (Higgins 2008). Elke studie werd gewaardeerd op de wijze van randomisatie en toewijzing; blindering van de deelnemers, beoordelaars, en therapeuten; gehanteerde methode om met voortijdig stoppen met de behandeling van deelnemers om te gaan; en of alle uitkomsten zijn gerapporteerd. Risico op bias kon als hoog (serieuze kans op beïnvloeding van het resultaat), laag (waarschijnlijk geen invloed op het resultaat), of onduidelijk worden beoordeeld.
Voor het bewijs rondom interventies is daarna het bewijs van de onderzoeken per uitkomstmaat gegradeerd met behulp van GRADE[1]. De kwaliteit van het bewijs kent daarbij vier niveaus, te weten; zeer laag, laag, matig en hoog. In deze richtlijn is gekozen om de GRADE niveaus weer te geven met behulp van de volgende neutrale en internationaal toepasbare weergave:
[1] GRADE: Grading of Recommendations Assessment, Development and Evaluation
|
Hoog |
|
|
Matig |
|
|
Laag |
|
|
Zeer laag |
|
Het studiedesign bepaalt de uitgangspositie van de kwaliteit van bewijs. Gerandomiseerde, gecontroleerde studies (RCT's) hebben over het algemeen meer bewijskracht dan observationele studies. Daarom is hun uitgangspositie hoog, terwijl de uitgangspositie van observationele studies laag is. De kwaliteit van het bewijs per uitkomstmaat wordt, behalve door de methodologische kwaliteit van de individuele onderzoeken, ook bepaald door andere factoren, zoals de mate van consistentie van de gevonden resultaten uit de verschillende onderzoeken en de precisie van de gevonden uitkomst (zie tabel 1).
Tabel 1 GRADE: Factoren voor downgraden en upgraden
Het niveau van de kwaliteit van het bewijs (zeer laag, laag, matig en hoog) verwijst naar de mate van vertrouwen dat men heeft in de schatting van het effect van een behandeling.
|
We downgraden het niveau van de kwaliteit van bewijs van studies met een hoge uitgangspositie (RCT’s), bij: |
We upgraden het niveau van de kwaliteit van bewijs van observationele studies bij: |
|
|
|
|
|
|
Standaard is SMD van -0,2 tm 0,2 niet klinisch relevant en bij een RR/OR is dit 0,75 tm 1,25.
Bij een Mean Difference tussen groepen wordt uit het Minimal Important Clinical Difference (MICD)van de vragenlijst gehanteerd. Is deze niet voorhanden dan moet de evidentie op minimaal 300 personen zijn gebaseerd. |
|
|
|
[2] Het blinderen van deelnemers en therapeuten is in deze richtlijn niet meegenomen in de beoordeling van studies rond psychosociale niterventies, omdat blinderen van de deelnemers en therapeuten niet goed mogelijk is bij deze interventies.
Netwerk meta-analyse
In recente jaren wordt er naast de traditionele meta-analyses steeds meer gebruik gemaakt van netwerk meta-analyses (NMA). De voordelen van een NMA is dat er vergelijkingen tussen interventies gemaakt kunnen worden die in de losse geïncludeerde studies niet direct met elkaar zijn vergeleken (indirecte vergelijkingen), alle evidentie in het model wordt meegenomen wat leidt tot verbeterde precisie bij het schatten van de interventie effecten. Deze indirecte vergelijkingen zijn echter wel gevoelig voor variabiliteit en verschillen tussen de geïncludeerde studies waardoor het van belang is dat er zorg gedragen wordt dat er geen grote heterogeniteit en inconsistentie in het model aanwezig is. Dit kan deels voorkomen worden door het includeren van studies waarbij er geen grote verschillen zijn in populatiekenmerken. Voor het bepalen van de kwaliteit van bewijs afkomstig uit een NMA is men afhankelijk van op welke wijze de auteurs de NMA hebben uitgevoerd (gemaakte aannames, uitgevoerde analyse, rapporteren van onderliggende informatie, rapporteren van CINeMA scores). De CINeMA methode heeft gelijkenissen met de GRADE methode maar is toegespitst op het gebruik bij NMA. Waar mogelijk worden deze CiNeMA scores gebuikt in de huidige richtlijn. Mochten deze ontbreken wordt er door de reviewers gekeken of de heterogeniteit en inconsistentie van het model worden gerapporteerd, mocht dit niet het geval zijn dan wordt de NMA niet meegenomen. Wanneer deze informatie wel aanwezig is wordt deze meegenomen in de GRADE beoordeling en er wordt een narratieve schatting van het risico op vertekening van uitkomsten door gebreken in de onderzoeksopzet gemaakt (Risk of Bias). . Mocht er sprake zijn van verhoogde heterogeniteit dan wordt hier voor gedowngrade en wanneer er sprake is van verhoogde inconsistentie dan wordt de NMA niet meegenomen.
Samenvatten van resultaten in ‘evidence tabel’ en ‘forest plot’
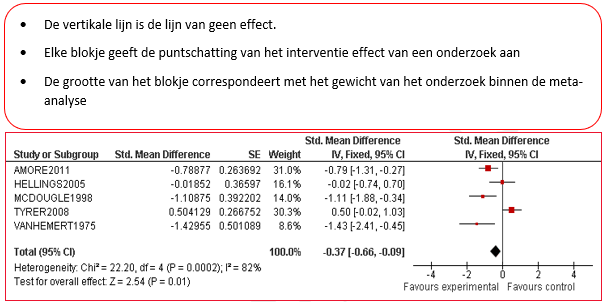
Van elk artikel is een samenvatting gemaakt in een zogenaamde 'evidence tabel', waarin de belangrijkste kenmerken van individuele onderzoeken zijn opgenomen (bij een RCT zijn dat bijvoorbeeld het doel van het onderzoek, het onderzoeksdesign, patiëntkenmerken, interventies, uitkomstmaten en de resultaten). Bij de uitgangsvragen over interventies is voor elke kritische uitkomstmaat een meta-analyse uitgevoerd, om de omvang van het klinisch effect van de interventie samen te vatten. De data uit oorspronkelijke onderzoeken worden hiervoor verwerkt in een forest plot, welke een grafische weergave van de meta-analyse geeft (zie tabel 2 voor een voorbeeld van een forest plot).
Tabel 2 Voorbeeld van een forest plot met toelichting
Wanneer er onvoldoende data beschikbaar waren om een meta-analyse uit te voeren, stelden de reviewers in enkele gevallen een narratieve (beschrijvende) review van het beschikbare bewijs op (zonder ‘gepoolde’ resultaten en berekening van mate van heterogeniteit, maar met een beschrijving van de kwaliteit). De kwaliteitsbeoordeling en een samenvattende beschrijving van de verschillende onderzoeken welke zijn geselecteerd vanuit de systematische literatuur search worden voor elke uitgangsvraag beschreven onder het kopje ‘wetenschappelijke onderbouwing’[3].
[3] Wat effectgroottes in de evidence tabellen en forest plots betreft: SMD's (standard mean differences) werden als klein beschouwd (0,2 ⩽ SMD < 0,5), matig (0,5 ⩽ SMD < 0,8) of groot (SMD ⩾ 0,8) (Cohen, 1988).
Conclusies
De formulering van de conclusies, gebaseerd op de studies uit de systematische literatuur search, is afgestemd op het GRADE niveau (zie tabel 3). Deze formulering sluit ook aan bij de ‘levels of evidence’ welke indeling (niveau 1 t/m 4) voorheen werd gebruikt in onder andere de multidisciplinaire richtlijn Schizofrenie.
Tabel 3 Formulering conclusies n.a.v. GRADE niveau
|
GRADE |
Levels of evidence |
Formulering conclusies |
|
|
Niveau 1 |
“Het is aangetoond dat…” |
|
|
Niveau 2 |
“Het is aannemelijk dat…” |
|
|
Niveau 3 |
“Er zijn aanwijzingen dat…” |
|
|
Niveau 4 |
“Er zijn voorzichtige aanwijzingen dat…” |
Van conclusies naar aanbevelingen: praktijkoverwegingen
Naast het wetenschappelijk bewijs bepalen enkele andere factoren mede of een instrument of behandeling wordt aanbevolen.
Mee te wegen factoren om te bepalen of een instrument of behandeling wordt aanbevolen:
|
1. Kwaliteit van bewijs Hoe hoger de algehele kwaliteit van het bewijs, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. |
|
2. Balans tussen gewenste en ongewenste effecten Hoe groter het verschil is tussen de gewenste en ongewenste effecten, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. Hoe kleiner dit verschil of hoe meer onzekerheid over de grootte van het verschil, des te waarschijnlijker wordt het formuleren van een conditionele aanbeveling. Toelichting:
|
|
3. Patiëntenperspectief Hoe groter de uniformiteit in waarden en voorkeuren van patiënten bij het afwegen van de voor- en nadelen van een interventie, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. De teksten onder het kopje ‘patiëntenperspectief’ zijn geschreven door de vertegenwoordiger van de patiëntenorganisatie: de Angst, Dwang en Fobie Stichting. Het is steeds gegaan om informele vragenrondes onder leden van het wetenschapspanel en de topicgroepen van deze organisatie. Gemiddeld zijn zo’n 30 à 40 personen bevraagd. |
|
4. Professioneel perspectief Hoe groter de uniformiteit in waarden en voorkeuren van professionals ten aanzien van de toepasbaarheid van een interventie, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling. Toelichting:
De teksten onder het kopje ‘professioneel perspectief’ zijn geschreven door de leden van de richtlijncommissie. |
|
5. Middelenbeslag Hoe minder middelen er worden gebruikt (m.a.w. hoe lager de kosten van een interventie zijn vergeleken met de beschouwde alternatieven en andere kosten gerelateerd aan de interventie), des te waarschijnlijker wordt het formuleren van een sterke aanbeveling. Hoe meer onzekerheid over het middelenbeslag, des te waarschijnlijker wordt een conditionele aanbeveling. |
|
6. Organisatie van zorg Hoe meer onzekerheid of de geëvalueerde interventie daadwerkelijk op landelijke schaal toepasbaar is, des te waarschijnlijker wordt het formuleren van een conditionele aanbeveling. Toelichting:
|
Aanbevelingen
Afhankelijk van het bewijs en bovenstaande factoren kun je een instrument of behandeling wel of niet aanbevelen. We maken daarbij onderscheid tussen zwakke en sterke aanbevelingen. In het geval van een sterke aanbeveling zou je behandeling X voor alle patiënten met Y willen aanbevelen. Bij een zwakke aanbeveling is dit bijvoorbeeld afhankelijk van de voorkeuren van de patiënt in kwestie. Het is belangrijk in deze sectie expliciet te vermelden op grond waarvan een behandeling wel of niet wordt aanbevolen en ook waarom die aanbeveling zwak of sterk zou moeten zijn.
Voor de formulering van ‘sterke’ (onvoorwaardelijke) en ‘zwakke’ (voorwaardelijke) aanbevelingen is de volgende indeling aangehouden (zie tabel 4):
Tabel 4 GRADE Voorkeursformulering sterke / zwakke aanbevelingen
|
Gradering aanbeveling |
Betekenis |
Voorkeursformulering* |
|
STERK VOOR |
De voordelen zijn groter dan de nadelen voor bijna alle patiënten. Alle of nagenoeg alle geïnformeerde patiënten zullen waarschijnlijk deze optie kiezen. |
We bevelen [interventie] aan. |
|
ZWAK VOOR |
De voordelen zijn groter dan de nadelen voor een meerderheid van de patiënten, maar niet voor iedereen. De meerderheid van geïnformeerde patiënten zal waarschijnlijk deze optie kiezen. |
Overweeg [interventie], bespreek de voor- en nadelen). |
|
ZWAK TEGEN |
De nadelen zijn groter dan de voordelen voor een meerderheid van de patiënten, maar niet voor iedereen. De meerderheid van geïnformeerde patiënten zal waarschijnlijk deze optie kiezen. |
Wees terughoudend met [interventie], bespreek de voor- en nadelen). |
|
STERK TEGEN |
De nadelen zijn groter dan de voordelen voor bijna alle patiënten. Alle of nagenoeg alle geïnformeerde patiënten zullen waarschijnlijk deze optie kiezen. |
We bevelen [interventie] niet aan. |
* het gaat hier om voorkeursaanbevelingen, deze kunnen in een enkele geval afwijken. Voor bepaalde hoofdstukken is GRADE niet toegepast (bijv. Organisatie van zorg) daar zijn uit praktisch oogpunt ook de aanbevelingen niet volgens GRADE
Referenties
Cohen J (1988) Statistical Power Analysis for the Behavioral Sciences. Hillsdale, NJ: Lawrence Erlbaum Associates.
Gevers, J. K. M., & Aalst, A. van (1998). De rechter en het medisch handelen (3e druk). Deventer: Kluwer.
Higgins, J. P. T., Green, S., & Cochrane Collaboration (2008). Cochrane handbook for systematic Reviews of interventions. Chichester, England/Hoboken, NJ: Wiley-Blackwell.
Zoekverantwoording
Zoekstrategie – Farmacotherapie
Database: Ovid MEDLINE(R) ALL <1946 to April 11, 2022>
Search Strategy:
--------------------------------------------------------------------------------
1 "angststoornissen behandeling".ti. (0)
2 anxiety disorders/ or agoraphobia/ or obsessive-compulsive disorder/ or hoarding disorder/ or panic disorder/ or phobic disorders/ or phobia, social/ (67501)
3 ((panic adj1 disorder?) or (anxiety adj1 neurosis) or (anxiety adj neuros?s) or (acute adj1 stress adj1 disorder*) or (anxiety adj1 neuros*) or (stress adj1 disorder?) or (generalized adj1 anxiety adj1 disorder*)).tw,kw. (51031)
4 *anxiety disorders/ or *agoraphobia/ or *obsessive-compulsive disorder/ or *hoarding disorder/ or *panic disorder/ or *phobic disorders/ or *phobia, social/ (50010)
5 ((panic adj1 disorder?) or (anxiety adj1 neurosis) or (anxiety adj neuros?s) or (acute adj1 stress adj1 disorder*) or (anxiety adj1 neuros*) or (stress adj1 disorder?) or (generalized adj1 anxiety adj1 disorder*)).ti,kw. (20273)
6 4 or 5 (63863)
7 (dutch or english or german).la. (30115589)
8 6 and 7 (59894)
9 cognitive behavioral therapy/ or "acceptance and commitment therapy"/ or mindfulness/ (33707)
10 exp computer simulation/ or virtual reality/ (274717)
11 group?.tw,kw. (4109869)
12 person*.tw,kw. (798556)
13 internet/ or internet-based intervention/ (79631)
14 internet*.tw,kw. (65010)
15 ((acceptance adj2 commitment therap*) or (acceptance adj2 treatm*) or (cognitive adj3 therap*) or (cognitive adj3 treatm*) or cbt or icbt).ti,kw. (13945)
16 cognitive behavioral therapy/mt or "acceptance and commitment therapy"/mt or mindfulness/mt (15606)
17 10 or 11 or 12 or 13 or 14 (5066270)
18 9 and 17 (15926)
19 16 or 18 (23375)
20 8 and 19 (3762)
21 "filter medline systematic reviews".ti. (0)
22 meta analysis.pt. (157355)
23 (meta-anal$ or metaanal$).tw,kf. (232881)
24 (systematic$ adj10 (review$ or overview$)).tw,kf. (267679)
25 (quantitativ$ adj10 (review$ or overview$)).tw,kf. (11714)
26 (methodologic$ adj10 (review$ or overview$)).tw,kf. (14309)
27 medline.tw. and review.pt. (89518)
28 (pooled adj3 analy*).tw,kf. (25278)
29 "cochrane$".fc_jour. (15800)
30 or/22-29 (457879)
31 20 and 30 (345)
32 31 (345)
33 limit 32 to yr="2010 -Current" (289)
34 Program Evaluation/ (66544)
35 "quality of life"/ (237895)
36 Social Participation/ (3130)
37 Cost-Benefit Analysis/ (89130)
38 (benifit? or gain* or efficacy or effectiven*).ti,kw. (330444)
39 (benifit? or gain* or efficacy or effectiven*).tw,kw. (1804426)
40 34 or 35 or 36 or 37 or 39 (2095442)
41 33 and 40 (208)
42 exp Eye Movement Desensitization Reprocessing/ (333)
43 ((eye adj2 movement adj3 desen*) or emdr).ti,kw. (586)
44 42 or 43 (689)
45 8 and 44 (188)
46 "medline filter rct".ti. (0)
47 controlled-clinical-trial.pt. (94810)
48 randomized-controlled-trial.pt. (564284)
49 randomized controlled trial/ (564284)
50 randomi?ed controlled trial?.tw. (218083)
51 randomi?ed controlled trial?.kf. (15686)
52 random-allocation.tw,kf. (1902)
53 double-blind-method.tw,kf. (525)
54 single-blind-method.tw,kf. (94)
55 (random adj8 (selection? or sample?)).kf,tw. (49597)
56 random*.tw,kf. (1309706)
57 or/47-56 (1524612)
58 45 and 57 (75)
59 efficacy.ti. (185281)
60 emdr.ti. (312)
61 *anxiety disorders/th or *agoraphobia/th or *obsessive-compulsive disorder/th or *hoarding disorder/th or *panic disorder/th or *phobic disorders/th or *phobia, social/th (8711)
62 (exposure and response).ti. (5515)
63 "Exposure and response prevention".kw. (85)
64 psychotherapy/ or art therapy/ or exp behavior therapy/ (138732)
65 ((psychological or behavior) adj2 treatment?).ti,kw. (2111)
66 exp cognitive behavioral therapy/ or exp desensitization, psychologic/ or exp relaxation therapy/ or exp feedback, psychological/ or exp hypnosis/ or exp psychoanalytic therapy/ or exp psychotherapeutic processes/ or exp socioenvironmental therapy/ (122531)
67 *anxiety disorders/th or *agoraphobia/th or *obsessive-compulsive disorder/th or *hoarding disorder/th or *panic disorder/th or *phobic disorders/th or *phobia, social/th (8711)
68 *"Stress Disorders, Post-Traumatic"/ (31355)
69 ((posttraumatic adj2 stress adj2 disorder*) or PTSD).ti,kw. (17589)
70 ((posttraumatic adj2 stress adj2 disorder*) or PTSD).ab. (32614)
71 68 or 69 or 70 (44799)
72 (schema adj2 (therap* or treat*)).tw,kw. (475)
73 psychotherapy/ or psychotherapy, psychodynamic/ or schema therapy/ (56985)
74 (psychother* adj2 psychodyn*).tw,kw. (1359)
75 9 or 10 or 15 or 61 or 62 or 63 or 64 or 65 or 66 or 72 or 73 or 74 (481781)
76 6 and 7 and 75 (12968)
77 76 not 71 (11009)
78 30 and 77 (688)
79 78 (688)
80 limit 79 to yr="2010 -Current" (523)
81 *anxiety disorders/dt or *agoraphobia/dt or *obsessive-compulsive disorder/dt or *hoarding disorder/dt or *panic disorder/dt or *phobic disorders/dt or *phobia, social/dt (5794)
82 exp Serotonin Uptake Inhibitors/ (44659)
83 exp Monoamine Oxidase/ (11654)
84 exp Benzodiazepines/ (67908)
85 exp Adrenergic beta-Antagonists/ (86139)
86 exp Antidepressive Agents, Tricyclic/ (31496)
87 Clomipramine/ (2826)
88 or/82-87 (223911)
89 exp Anti-Anxiety Agents/ (72282)
90 88 or 89 (244139)
91 6 and 90 (7934)
92 81 or 91 (9398)
93 7 and 30 and 91 (379)
94 (6 and 7 and 30 and (91 or 81)) not 71 (448)
95 94 (448)
96 limit 95 to yr="2010 -Current" (263)=SR
Database: Embase <1974 to 2022 April 11>
Search Strategy:
--------------------------------------------------------------------------------
1 "psychotherapie angst".ti. (0)
2 anxiety disorder/ or acute stress disorder/ or anxiety neurosis/ or generalized anxiety disorder/ or exp obsessive compulsive disorder/ or exp panic/ or phobia/ or separation anxiety/ (161790)
3 ((panic adj1 disorder?) or (anxiety adj1 neurosis) or (anxiety adj neuros?s) or (acute adj1 stress adj1 disorder*) or (anxiety adj1 neuros*) or (stress adj1 disorder?) or (generalized adj1 anxiety adj1 disorder*)).tw,kw. (63503)
4 *anxiety disorder/ or *acute stress disorder/ or *anxiety neurosis/ or *generalized anxiety disorder/ or exp *obsessive compulsive disorder/ or exp *panic/ or *phobia/ or *separation anxiety/ (65227)
5 ((panic adj1 disorder?) or (anxiety adj1 neurosis) or (anxiety adj neuros?s) or (acute adj1 stress adj1 disorder*) or (anxiety adj1 neuros*) or (stress adj1 disorder?) or (generalized adj1 anxiety adj1 disorder*)).ti,kw. (24439)
6 4 or 5 (81108)
7 (dutch or english or german).la. (33691565)
8 6 and 7 (75618)
9 cognitive behavioral therapy/ or cognitive behavioral stress management/ or cognitive processing therapy/ or dialectical behavior therapy/ (19912)
10 cognitive therapy/ or "acceptance and commitment therapy"/ or cognitive remediation therapy/ (46870)
11 ((acceptance adj2 commitment therap*) or (acceptance adj2 treatm*) or (cognitive adj3 therap*) or (cognitive adj3 treatm*)).ti,kw. (17079)
12 virtual reality/ (21930)
13 group therapy/ (19878)
14 computer simulation/ (130508)
15 web-based intervention/ (1615)
16 "Internet-Delivered Cognitive Behavioral Therapy for Anxiety Disorders in Open Community Versus Clinical Service Recruitment: Meta-Analysis".fc_titl. (1)
17 iCBT.ti,kw. (170)
18 "program impact"/ (1228)
19 exp program evaluation/ (30466)
20 group?.tw,kw. (5722138)
21 person*.tw,kw. (1038893)
22 ((internet or web*) adj2 based*).ti,kw. (14956)
23 9 or 10 or 11 (68483)
24 8 and 23 (8233)
25 "emb SR filter".ti. (0)
26 meta analysis/ (243088)
27 "systematic review"/ (340736)
28 (meta-analy$ or metaanaly$).tw,kw. (300581)
29 (systematic$ adj4 (review$ or overview$)).tw,kw. (321453)
30 (quantitativ$ adj5 (review? or overview?)).tw,kw. (6646)
31 (methodologic adj5 (overview? or review?)).tw,kw. (415)
32 (review$ adj3 (database? or medline or embase or cinahl)).tw,kw. (34574)
33 (pooled adj3 analy$).tw,kw. (38116)
34 (extensive adj3 review$ adj3 literature).tw,kw. (4367)
35 (meta or synthesis or (literature adj8 database?) or extraction).tw,kw. (1640494)
36 review.pt. (2886152)
37 35 and 36 (201226)
38 or/26-34,37 (718263)
39 24 and 38 (908)
40 12 or 13 or 14 or 15 or 17 or 18 or 19 or 20 or 21 or 22 (6674066)
41 39 and 40 (352)
42 26 or 28 (347693)
43 41 and 42 (245)
44 43 (245)
45 limit 44 to yr="2010 -Current" (192)
46 exp *program evaluation/ (5625)
47 "quality of life"/ (549842)
48 social participation/ (8295)
49 adverse outcome/ or exp *disease course/ or exp *disease severity/ (700696)
50 *adverse event/ (13040)
51 *disease management/ (5950)
52 or/46-51 (1255732)
53 45 and 52 (39)
54 ((posttraumatic adj stress adj disorder) or PTSD).ti,kw. (22398)
55 45 not 54 (167)
56 55 (167)
57 limit 56 to conference abstract status (6)
58 56 not 57 (161)
59 "eye movement desensitization and reprocessing"/ (503)
60 ((eye adj2 movement adj3 desen*) or emdr).ti,kw. (776)
61 59 or 60 (1025)
62 8 and 61 (252)
63 "rct filter embase".ti. (0)
64 randomization/ (93746)
65 exp randomized controlled trial/ (706155)
66 exp controlled clinical trial/ (895747)
67 Major Clinical Study/ (4436038)
68 random$.tw,kw. (1782701)
69 double blind procedure/ (194083)
70 or/64-69 (5965989)
71 38 or 70 (6443324)
72 62 and 71 (114)
73 72 (114)
74 limit 73 to yr="2010 -Current" (90)
75 ((posttraumatic adj stress adj disorder) or PTSD).ti,kw. (22398)
76 74 not 75 (37)
77 body dysmorphic disorder/ (3303)
78 exp hoarding disorder/ (693)
79 4 or 5 or 77 or 78 (84211)
80 7 and 79 (78541)
81 exp psychotherapy/ (272473)
82 exp behavior therapy/ (65690)
83 (behavio* adj (counsel* or intervention or train* or treatment or therapy or psychotherapy)).tw,kw. (49674)
84 (exposure and response).ti. (7027)
85 erp.ti. (4303)
86 *"exposure and response prevention therapy"/ (11)
87 "Exposure and response prevention".kw. (158)
88 (mindfulness adj2 therap*).tw,kw. (997)
89 "Acceptance and commitment therapy".tw,kw. (1905)
90 exp mindfulness/ (12302)
91 schema therapy/ (133)
92 psychodynamic psychotherapy/ (1585)
93 problem solving/ (37182)
94 or/81-93 (328973)
95 "alle interventies psychotherapie".ti. (0)
96 80 and 94 (15716)
97 38 and 96 (1385)
98 97 (1385)
99 limit 98 to yr="2010 -Current" (1022)
100 26 or 28 (347693)
101 99 and 100 (616)
102 posttraumatic stress disorder/ (70622)
103 75 or 102 (72212)
104 101 not 103 (421)
105 exp "quality of life"/ (575790)
106 recovery.mp. (681592)
107 rehabilitation/ (89045)
108 from 104 keep 1-413 (413)
109 105 or 106 or 107 (1314569)
110 104 and 109 (61)
111 99 and 109 (156)
112 111 not 110 (95)
113 112 not 103 (41)
114 8 and 94 (15258)
115 ((posttraumatic adj2 stress adj2 disorder*) or PTSD).ti,kw. (22528)
116 ((posttraumatic adj2 stress adj2 disorder*) or PTSD).ab. (41814)
117 102 or 115 or 116 (75754)
118 114 not 117 (11710)
119 38 and 118 (926)
120 119 (926)
121 limit 120 to yr="2010 -Current" (654)
122 *anxiety disorder/dt or *acute stress disorder/dt or *anxiety neurosis/dt or *generalized anxiety disorder/dt or exp *obsessive compulsive disorder/dt or exp *panic/dt or *phobia/dt or *separation anxiety/dt (13240)
123 exp serotonin uptake inhibitor/ (295359)
124 "amine oxidase (flavin containing)"/ (11494)
125 exp benzodiazepine derivative/ (244191)
126 exp beta adrenergic receptor blocking agent/ (313306)
127 exp tricyclic antidepressant agent/ (113914)
128 clomipramine/ (18114)
129 exp anxiolytic agent/ (239237)
130 tranquilizer/ (8725)
131 or/123-130 (832074)
132 (dutch or english or german).la. (33691565)
133 6 and (131 or 122) and 38 and 132 (1165)
134 133 not 103 (917)
135 limit 134 to yr="2010 -Current" (571)=SR
Database: APA PsycInfo <1806 to April Week 1 2022>
Search Strategy:
--------------------------------------------------------------------------------
1 "angststoornissen en cbt".ti. (0)
2 anxiety disorders/ or generalized anxiety disorder/ or exp obsessive compulsive disorder/ or panic attack/ or panic disorder/ or phobias/ or separation anxiety disorder/ or trichotillomania/ or social anxiety/ (55021)
3 ((panic adj1 disorder?) or (anxiety adj1 neurosis) or (anxiety adj neuros?s) or (acute adj1 stress adj1 disorder*) or (anxiety adj1 neuros*) or (stress adj1 disorder?) or (generalized adj1 anxiety adj1 disorder*)).ti,id. (35926)
4 *anxiety disorders/ or *generalized anxiety disorder/ or exp *obsessive compulsive disorder/ or *panic attack/ or *panic disorder/ or *phobias/ or *separation anxiety disorder/ or *trichotillomania/ or *social anxiety/ (47479)
5 3 or 4 (73333)
6 (dutch or german or english).la. (4850500)
7 5 and 6 (68897)
8 cognitive behavior therapy/ or "acceptance and commitment therapy"/ or cognitive processing therapy/ or prolonged exposure therapy/ (24610)
9 ((acceptance adj2 commitment therap*) or (acceptance adj2 treatm*) or (cognitive adj3 therap*) or (cognitive adj3 treatm*) or cbt or icbt).ti,id. (32135)
10 computer simulation/ or exp virtual reality/ (14926)
11 group?.tw,id. (957898)
12 group psychotherapy/ (20597)
13 individual psychotherapy/ (3158)
14 online therapy/ (3595)
15 (individual* or online).ti,id. (149205)
16 or/10-15 (1083760)
17 8 or 9 (37078)
18 7 and 16 and 17 (2058)
19 "psycinfo SR filer".ti. (0)
20 (meta-anal* or metaanal*).tw. (45667)
21 (quantitativ* adj5 (review* or overview*)).tw. (2908)
22 (quantitativ* adj5 (review* or overview*)).id. (73)
23 (systematic* adj5 (review* or overview*)).tw,id. (45663)
24 (methodolo* adj5 (review* or overview*)).tw,id. (7713)
25 ((medline or cochrane) adj5 (review* or overview*)).tw,id. (3379)
26 (literature adj5 (overview or review)).tw,id. (88205)
27 (synthes* adj3 (literature* or research or studies or data)).tw,id. (11018)
28 (pooled adj5 analys*).tw,id. (2757)
29 (data adj2 pool*).tw,id. (2646)
30 ((hand or manual* or database* or computer* or electronic*) adj2 search*).tw,id. (13597)
31 "literature review"/ or meta analysis/ (27934)
32 "systematic review"/ (696)
33 or/20-32 (174338)
34 meta analysis/ (5196)
35 20 or 34 (45846)
36 18 and 35 (127)
37 36 (127)
38 limit 37 to yr="2010 -Current" (105)
39 38 (105)
40 limit 39 to all journals (101)
41 ((posttraumatic adj stress adj disorder) or PTSD).ti,id. (29512)
42 40 not 41 (78)
43 eye movement desensitization therapy/ (1738)
44 ((eye adj2 movement adj3 desen*) or emdr).ti,id. (1870)
45 43 or 44 (1924)
46 "psycinfo filter rct".ti. (0)
47 randomi?ed controlled trial*.tw. (37969)
48 randomi?ed controlled trial*.id. (4795)
49 controlled clinical trial*.tw,id. (3343)
50 ((random adj allocation) or (double adj blind adj (method* or stud*))).tw,id. (2978)
51 single blind stud*.tw,id. (161)
52 clinical trials/ or exp randomized controlled trials/ (13181)
53 exp randomized controlled trials/ (1169)
54 or/47-51,53 (44186)
55 33 or 54 (209447)
56 7 and 45 and 55 (123)
57 56 not 41 (29)
58 57 (29)
59 limit 58 to yr="2010 -Current" (26)
60 body dysmorphic disorder/ (1269)
61 hoarding disorder/ (313)
62 exp obsessive compulsive disorder/ (16303)
63 3 or 4 or 60 or 61 or 62 (75728)
64 6 and 63 (71143)
65 8 or 9 or 10 or 12 or 13 or 14 (75170)
66 schema therapy/ or psychodynamic psychotherapy/ or psychotherapeutic techniques/ (23102)
67 problem solving/ or solution focused therapy/ (30032)
68 65 or 66 or 67 (123894)
69 "alle interventies".ti. (0)
70 6 and 33 and 63 and 68 (640)
71 70 (640)
72 limit 71 to yr="2010 -Current" (452)
73 exp posttraumatic stress disorder/ (36970)
74 41 or 73 (38665)
75 72 not 74 (322)
76 35 and 75 (209)
77 76 (209)
78 limit 77 to all journals (186)
79 exp "quality of life"/ (47964)
80 from 76 keep 1-206 (206)
81 from 78 keep 1-183 (183)
82 well being/ (52549)
83 "recovery (disorders)"/ (13913)
84 79 or 82 or 83 (110150)
85 75 and 84 (9)
86 exp drug therapy/ (153890)
87 exp serotonin reuptake inhibitors/ or exp serotonin norepinephrine reuptake inhibitors/ (14139)
88 exp monoamine oxidases/ (1496)
89 exp benzodiazepines/ (11082)
90 exp adrenergic receptors/ (1701)
91 exp tricyclic antidepressant drugs/ (6472)
92 exp chlorimipramine/ (1151)
93 exp tranquilizing drugs/ (48093)
94 or/87-93 (71114)
95 5 and 6 and 33 and (94 or 86) (642)
96 95 not 74 (513)
97 96 (513)
98 limit 97 to (all journals and yr="2010 -Current") (203)=SR
Cochrane search SR op 20220412
#23 anxiety near/2 disord*:ti 2828
#24 Benzodiazepines versus placebo for panic disorder in adults:ti 24
#25 (panic NEAR/1 disorde*):ti,ab,kw 2339
#26 (Agoraphobi* or (social NEAR/2 phobi*) or (generalized NEAR/2 anxiety NEAR/2 disord*) or (specific NEAR/2 phobic*) or (obsessive NEAR/2 compulsive NEAR/2 disorde*)):ti,kw 5891
#27 MeSH descriptor: [Anxiety Disorders] explode all trees and with qualifier(s): [drug therapy - DT] 2020
#28 MeSH descriptor: [Obsessive-Compulsive Disorder] explode all trees and with qualifier(s): [drug therapy - DT] 411
#29 #25 or #26 7446
#30 MeSH descriptor: [Serotonin Uptake Inhibitors] explode all trees 2865
#31 MeSH descriptor: [Monoamine Oxidase] explode all trees 110
#32 MeSH descriptor: [Benzodiazepines] explode all trees 9917
#33 MeSH descriptor: [Adrenergic beta-Antagonists] explode all trees 4629
#34 MeSH descriptor: [Antidepressive Agents, Tricyclic] explode all trees 974
#35 MeSH descriptor: [Clomipramine] explode all trees 412
#36 MeSH descriptor: [Anti-Anxiety Agents] explode all trees 2217
#37 (#30 or #31 or #32 or #33 or #34 or #34 or #35 or #36) and #29 1066
#38 (#30 or #31 or #32 or #33 or #34 or #34 or #35 or #36) and (#29 or #23 or #25) 1142
#39 #38 not #37 76
#40 (compulsive NEAR/2 disord*):ti,kw 2384
#41 (#30 or #31 or #32 or #33 or #34 or #34 or #35 or #36) and (#29 or #23 or #25 or #40) 1146 met 20 SRs