Tromboseprofylaxe bij obesitas
Uitgangsvraag
Wat is de optimale dosering voor tromboseprofylaxe bij patiënten met obesitas die een chirurgische ingreep ondergaan onder algehele anesthesie?
Aanbeveling
Overweeg bij patiënten met een lichaamsgewicht ≥100 kg die een chirurgische ingreep ondergaan tromboseprofylaxe in een dubbele dosering LMWH toe te dienen.
Houd hierbij rekening met het werkelijke risico op veneuze trombo-embolie op basis van patiëntfactoren, co-morbiditeit en voorgeschiedenis.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
De werkgroep heeft een literatuuronderzoek verricht naar het effect van een hoge dosis tromboseprofylaxe vergeleken met een standaarddosering tromboseprofylaxe in chirurgische patiënten met obesitas. Er werd één Cochrane review geïncludeerd, waarin voor deze vergelijking drie RCT’s waren geïncludeerd die voldeden aan onze inclusiecriteria.
De cruciale uitkomstmaten waren mortaliteit en incidentie van veneuze trombo-embolie.
Voor beide uitkomstmaten konden geen conclusies getrokken worden, vanwege een zeer lage bewijskracht. Er werd afgewaardeerd omdat de optimal information size (OIS) niet behaald werd. Voor incidentie van veneuze trombo-embolie (VTE) werd ook nog afgewaardeerd voor risico op bias, omdat twee van de drie RCT’s niet geblindeerd waren. Concluderend is de overall bewijskracht zeer laag. Hier ligt dan ook een kennislacune ten aanzien van de genoemde eindpunten.
De belangrijke uitkomstmaten waren incidentie van grote bloedingen en hemoglobine waarde. Voor incidentie van grote bloedingen konden ook geen conclusies worden getrokken. Ook voor deze uitkomstmaat was de bewijskracht zeer laag. Hemoglobine waardes werden niet gerapporteerd. Daarom konden de belangrijke uitkomstmaten geen verdere richting geven aan de besluitvorming.
Vanuit verschillende observationele studies en meta-analyses, o.a. Liu (2023), Hany (2023) en He (2017) zijn er wel aanwijzingen dat een hogere profylactische dosis LMWH op basis van gewicht ook zal leiden tot minder trombo-embolische events bij patiënten met obesitas. Zij geven echter ook aan dat het bewijs beperkt is en grotere gerandomiseerde studies nodig zijn, waardoor de resultaten met voorzichtigheid geïnterpreteerd moeten worden.
Op het gebied van de farmacokinetiek van LMWH’s bij patiënten met obesitas is er daarnaast aanvullend bewijs om aan te nemen dat bij een hoger gewicht op enig moment ook een hogere profylactische dosis LMWH moet worden toegediend ter preventie van VTE’s. In farmacokinetiek-studies worden hiervoor veelal anti-Xa concentraties bepaald als surrogaatmarker om het effect van LMWH’s te kunnen monitoren.
In de studie van Heizmann (2002) wordt bij een twee keer hogere profylactische dosis van een LMWH (Nadroparine 5700IE vs Nadroparine 2850IE) een 1,4 keer hogere anti-Xa spiegel gevonden in een groep patiënten met obesitas (109 – 152 kg), die twee keer zwaarder waren dan in de controlegroep zonder obesitas. Dit impliceert dat er bij een bepaald gewicht inderdaad hoger gedoseerd moet worden, maar dat dit niet lineair zal zijn.
In de studie van Schijns (2018) wordt geconcludeerd dat in een groep patiënten met een totaal lichaamsgewicht (TBW) >140 kg, een dubbele dosis van een LMWH (Nadroparine 5700IE) in 32% een te lage blootstelling voor voldoende profylaxe wordt bereikt op basis van anti-Xa spiegels (referentie is 0,2-0,5 IU/ml). Daarbij is een sterke correlatie gevonden tussen een adequate anti-Xa spiegel en Lean Body Weight (LBW) en wordt de suggestie gedaan om bij LBW >80 kg Nadroparine 7600IE te doseren. Dit is een substantieel hogere dosis dan de standaard dosis Nadroparine 2850IE.
Diepstraten (2015) laat hetzelfde zien op basis van simulaties met een farmacodynamisch model waarbij patiënten met morbide obesitas (BMI ≥40 kg/m²) Nadroparine 5700IE toegediend kregen voor profylaxe en adequate anti-Xa spiegels bereikten, echter bij een LBW >90 kg bleek dit subprofylactisch te zijn en wordt ook het voorstel gedaan om Nadroparine 7600IE te doseren.
Celik (2015) toonde hetzelfde aan voor een andere LMWH, Enoxaparine, waarbij een hogere profylactische dosis van 40 mg resulteerde in adequate anti-Xa spiegels in een groep obese patiënten met een TBW <110 kg, echter in de groep met TBW >150 kg werd bij 38% van de patiënten met obesitas een subprofylactische anti-Xa spiegel gevonden en zou dus een hogere dosis Enoxaparine noodzakelijk zijn voor adequate anti-Xa spiegels, danwel hiervoor een tweemaal daagse dosering van Enoxaparine 30 mg aan te houden om het risico op eventuele bloedingen te reduceren.
Op basis van resultaten uit farmacokinetiek-studies kan worden overwogen om bij patiënten met een obesitas vanaf 100 kg, voor het voorkomen van trombo-embolische events na chirurgie, een dubbele profylactische dosis LMWH aan te houden voor voldoende adequate anti-Xa spiegels. Bij een morbide obesitas van 160-180 kg is op basis van farmacokinetische studies eventueel zelfs een driedubbele profylactische dosis LMWH te overwegen.
Hierbij moet ook het werkelijke VTE-risico op basis van patiëntfactoren, co-morbiditeit en voorgeschiedenis worden meegenomen in de overweging.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Vooraf moet de patiënt uitleg krijgen over het nut van LMWH ter preventie van trombose. De gevolgen van een dergelijke trombose kunnen ernstig zijn. In het geval van het preventief dan wel therapeutisch toedienen van LMWH is in Nederland Nadroparine het meest gebruikt. Bij profylaxe gaat het enkel om de dosis en hoeft het medicament niet vaker gebruikt te worden. Dit zorgt ervoor dat de dosis voor de patiënt wellicht niet uitmaakt. Uit onderzoek is niet te concluderen, vooralsnog, dat het bloedingsrisico voor de patiënt toeneemt met een hogere dosering.
Kosten (middelenbeslag)
In het geval van het optreden van trombose, wat kan gebeuren bij onderdosering van de patiënt met obesitas, kan er sprake zijn van extra kosten door extra onderzoeken, eventuele complicaties en een langere ziekenhuisopname. Als er sprake is van een ernstige trombose, bijvoorbeeld een ruiterembolie, kan het zelfs levensbedreigend zijn.
Aanvaardbaarheid, haalbaarheid en implementatie
Verhoging van de dosering LMWH voor patiënten met obesitas wordt in de meeste centra in Nederland al toegepast. Er zijn geen belemmerende factoren op het gebied van implementatie voor het aanpassen van de dosering.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
De huidige literatuur geeft onvoldoende bewijs dat een hogere dosis tromboseprofylaxe bij patiënten met obesitas leidt tot minder trombose. Het is alleen niet de verwachting dat een studie naar verhoogde doseringen bij patiënten met obesitas op harde eindpunten nog zal worden uitgevoerd. Echter, de productinformatie van LMWH’s (bijvoorbeeld Nadroparine) beschrijft voor profylaxe van trombo-embolische aandoeningen bij een hoger lichaamsgewicht een dubbele dosering LMWH toe te dienen.
Op basis van farmacokinetisch onderzoek leidt een hogere dosis LMWH bij obesitas tot vergelijkbare anti-Xa levels als bij patiënten met een normaal gewicht die een standaard dosis krijgen toegediend. Daarom kan worden overwogen om bij patiënten met een gewicht vanaf 100 kg voor het voorkomen van trombo-embolische events na chirurgie, een verhoogde dubbele profylactische dosis LMWH aan te houden voor voldoende adequate anti-Xa spiegels. De zorgverlener zal op basis van een individuele risico-inschatting kunnen afzien van een dosisverhoging.
Onderbouwing
Er is bewijs dat profylactisch laag-molecuulgewicht heparine (LMWH) rondom operatieve ingrepen superieur is aan placebo voor het voorkomen van postoperatieve veneuze trombose (VTE). Volgens de officiële productinformatie worden LMWHs op gewicht gedoseerd bij therapeutische toediening van LMWH, maar ook bij bijna alle profylactische indicaties zoals bij orthopedische ingrepen, opname op IC en bij dialysepatiënten. In Nederland is nadroparine het meest gebruikte LMWH. Voor >70 kg wordt voor Nadroparine een hogere dosering beschreven voor deze indicaties. Daarnaast is recent aan de productinformatie van Nadroparine toegevoegd om bij profylaxe van trombo-embolische aandoeningen bij volwassenen > 100 kg een aangepaste, verhoogde dosering Nadroparine 5700IE subcutaan eenmaal per dag te overwegen. De enige uitzondering in de productinformatie van bijvoorbeeld Nadroparine is algemene chirurgische profylaxe waarbij niet specifiek genoemd staat dat er een hogere dosis nodig is bij een hoger gewicht, maar nog de standaarddosis van 2850IE eenmaal per dag. Regelmatig komt de vraag op of een hogere, op gewicht gebaseerde profylactische dosis bij algemene chirurgie effectiever is dan de standaard dosis, dan wel of deze hogere dosis leidt tot meer complicaties zoals een verhoogd bloedingsrisico.
|
Very low GRADE |
The evidence is very uncertain about the effect of higher dose LMWH on all-cause mortality when compared with standard dose LMWH in patients with obesity undergoing surgery requiring general anesthesia with an indication for thromboprophylaxis.
Source: Amaral, 2022 (Ebrahimifard, 2012; Imberti, 2014; Steib, 2016) |
|
Very low GRADE |
The evidence is very uncertain about the effect of higher dose LMWH on VTE when compared with standard dose LMWH in patients with obesity undergoing surgery requiring general anesthesia with an indication for thromboprophylaxis.
Source: Amaral, 2022 (Ebrahimifard, 2012; Imberti, 2014; Steib, 2016) |
|
Very low GRADE |
The evidence is very uncertain about the effect of higher dose LMWH on major bleeding when compared with standard dose LMWH in patients with obesity undergoing surgery requiring general anesthesia with an indication for thromboprophylaxis.
Source: Amaral, 2022 (Ebrahimifard, 2012; Imberti, 2014; Steib, 2016) |
|
No GRADE |
No evidence was found regarding the effect of higher dose LMWH on hemoglobin levels when compared with standard dose LMWH in patients with obesity undergoing surgery requiring general anesthesia with an indication for thromboprophylaxis.
Source: - |
Description of studies
Amaral (2022) conducted a Cochrane review to evaluate the benefits and harms of pharmacological interventions (alone or in combination) on venous thromboembolism and other health outcomes in people undergoing bariatric surgery compared to the same pharmacological intervention administered at a different dose or frequency, the same pharmacological intervention or started at a different time point, another pharmacological intervention, no intervention or placebo. The search date was performed in November 2021. The primary outcomes were VTE and major bleeding. The secondary outcomes were all‐cause mortality, VTE‐related mortality, pulmonary embolism, deep vein thrombosis (DVT), adverse effects and quality of life. Comparison 1: Higher‐dose heparin versus standard‐dose heparin was considered relevant for the current literature analysis. For this comparison in the current analysis, three relevant RCTs (537 participants) were included, as shown in Table 1. The duration of the interventions ranged from seven to 15 days, and follow‐up ranged from 10 to 180 days. The certainty of the evidence is limited by small sample sizes, few or no events, and risk of bias concerns (no blinding by Imberti 2014, Steib 2016).
Table 1. Overview of the included studies from Amaral (2022).
|
Author, year |
N (I/C) |
Population |
Intervention |
Control |
Follow-up |
|
Ebrahimifard, 2012 |
71/68 |
Bariatric surgery (72% LRYGB, 25% sleeve gastrectomy, 1.4% gastric banding, 0.7% gastric plication)
Mean age: 36.7 (SD 9.5) y
Sex (M/F): 13/126
Mean BMI: 44.29 (SD 6.9) |
Unfractionated heparin 5000 IU TID |
Unfractionated heparin 5000 IU BID |
10 days |
|
Imberti, 2014 |
119/131 |
Bariatric surgery (68% LRYGB, 8.8% sleeve gastrectomy, 8.4% gastric banding, 9.6% biliopancreatic diversion, 0.4% vertical gastroplasty)
Mean age: 40.9 (SD 9.7) y
Sex (M/F): 51/199
Mean BMI: 44.2 (SD 5.4)/ 44.6 (5.4) |
Parnaparin 6400 IU/day starting 12 hours preoperatively for a period of 9 days |
Parnaparin 4250 IU/day starting 12 hours preoperatively for a period of 9 days |
3 months |
|
Steib, 2016 |
100/48 |
Bariatric surgery (100% LRYGB)
Mean age: 40 (SD 1.5)/39 (SD 1.5) y
Sex (male/female): 29/107
BMI: 47 (SD 1)/ 48 (SD 1) |
Enoxaparin 6000 IU/day |
Enoxaparin 4000 IU/day |
30 days |
BID: bis in die, twice a day; BMI: Body Mass Index; IU: international units; (L)RYGB: (laparoscopic) Roux-en-Y gastric bypass; TID: ter in die: three times a day.
Results
All-cause mortality
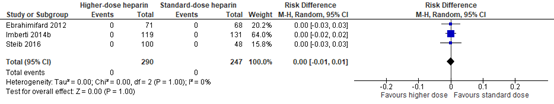
Three studies reported all-cause mortality. A meta-analysis is shown in figure 1. The risk difference (RD) was 0.00 (95% confidence interval (CI) -0.01 to 0.01). There is no clinically relevant difference.
Figure 1. All-cause mortality; higher dose versus standard dose LMWH
Z: p-value of overall effect; df: degrees of freedom; I2: statistical heterogeneity; CI: confidence interval
Venous thromboembolism
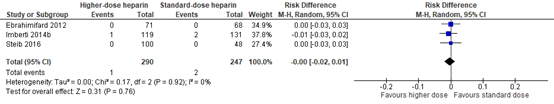
Three studies reported the incidence of venous thromboembolism. A meta-analysis is shown in figure 2. The RD was -0.00 (95% CI -0.02 to 0.01). There is no clinically relevant difference.
Figure 2. Venous thromboembolism; higher dose versus standard dose LMWH
Z: p-value of overall effect; df: degrees of freedom; I2: statistical heterogeneity; CI: confidence interval
Major bleeding
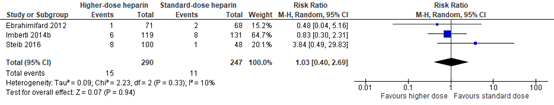
Three studies reported the incidence of major bleeding. A meta-analysis is shown in figure 3. The relative risk (RR) was 1.03 (95% CI 0.40 to 2.69). This difference is not clinically relevant.
Figure 3. Major bleeding; higher dose versus standard dose LMWH
Z: p-value of overall effect; df: degrees of freedom; I2: statistical heterogeneity; CI: confidence interval
Hemoglobin levels
Hemoglobin levels were not reported.
Level of evidence of the literature
The level of evidence regarding the outcome measure all-cause mortality was downgraded by three levels because the optimal information size was not met and no events were reported (imprecision, -3). The level of evidence is very low.
The level of evidence regarding the outcome measure VTE was downgraded by three levels because of the optimal information size was not met and very few events were reported (imprecision, -3). The level of evidence is very low.
The level of evidence regarding the outcome measure major bleeding was downgraded by three levels because of study limitations (risk of bias due to lack of blinding, -1); and conflicting results (inconsistency, -1) and a very low number of events (imprecision, -1). The level of evidence is very low.
The level of evidence regarding the outcome measure ‘hemoglobin levels’ could not be assessed, as this outcome was not reported.
A systematic review of the literature was performed to answer the following question:
What is the (un)favorable effect of a high dose low-molecular-weight-heparin (LMWH) based on total body weight compared to a standard dose LMWH in patients with obesity undergoing surgery requiring general anesthesia?
| P: | Patients with obesity undergoing surgery requiring general anesthesia with an indication for thromboprophylaxis |
| I: | High dose LMWH based on total body weight |
| C: | ‘Standard’ low dose LMWH |
| O: | Mortality, venous thromboembolism (VTE), major bleeding, hemoglobin (Hb) levels |
Relevant outcome measures
The guideline development group considered mortality and VTE as critical outcome measures for decision making; and postoperative hemorrhage and Hb levels as important outcome measures for decision making.
The working group defined the outcome measures as follows:
Major bleeding: bleeding that requires an intervention or blood transfusion of ≥ 2 units of red blood cells within one week of surgery.
A priori, the working group did not define the other outcome measures listed above but used the definitions used in the studies.
The working group defined the following as a minimal clinically (patient) important difference:
Mortality: 0.95≥ risk relative (RR) ≥1.05 or -0.05≥ risk difference (RD) ≥ 0.05
VTE: 0.95≥RR≥ 1.05 or -0.05≥RD≥0.05
Major bleeding: 0.95≥RR≥ 1.05 or -0.05≥RD≥0.05
Hb levels: MD> 1.2 g/dL
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms from 2005 until June 1st, 2023. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 352 hits. Studies were selected based on the following criteria: 1) a systematic review randomized controlled trials (RCTs), or an RCT, 2) published after 2005, 3) including patients with obesity and an indication for thromboprophylaxis undergoing surgery 4) comparing High dose LMWH based on total body weight with a ‘standard’ low dose LMWH, 5) reporting at least one of the following outcome measures: mortality, VTE, postoperative hemorrhage, or Hb levels.
Seventeen studies were initially selected based on title and abstract screening. After reading the full text, sixteen studies were excluded (see the table with reasons for exclusion under the tab Methods), and one study was included.
Results
One Cochrane review included in the analysis of the literature. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
- Amaral FC, Baptista-Silva JC, Nakano LC, Flumignan RL. Pharmacological interventions for preventing venous thromboembolism in people undergoing bariatric surgery. Cochrane Database Syst Rev. 2022 Nov 22;11(11):CD013683. doi: 10.1002/14651858.CD013683.pub2. PMID: 36413425; PMCID: PMC9680918.
- Celik F, Huitema AD, Hooijberg JH, van de Laar AW, Brandjes DP, Gerdes VE. Fixed-dose enoxaparin after bariatric surgery: the influence of body weight on peak anti-Xa levels. Obes Surg. 2015 Apr;25(4):628-34. doi: 10.1007/s11695-014-1435-3. PMID: 25223871.
- Diepstraten J, Janssen EJ, Hackeng CM, van Dongen EP, Wiezer RJ, van Ramshorst B, Knibbe CA. Population pharmacodynamic model for low molecular weight heparin nadroparin in morbidly obese and non-obese patients using anti-Xa levels as endpoint. Eur J Clin Pharmacol. 2015 Jan;71(1):25-34. doi: 10.1007/s00228-014-1760-4. Epub 2014 Oct 12. PMID: 25304008.
- Hany M, Abouelnasr AA, Agayby ASS, Abdelsattar A, Torensma B. Towards Zero Thromboembolic Events After Bariatric Metabolic Surgery. Obes Surg. 2023 May;33(5):1606-1612. doi: 10.1007/s11695-023-06511-8. Epub 2023 Mar 4. PMID: 36869255; PMCID: PMC10156778.
- He Z, Morrissey H, Ball P. Review of current evidence available for guiding optimal Enoxaparin prophylactic dosing strategies in obese patients-Actual Weight-based vs Fixed. Crit Rev Oncol Hematol. 2017 May;113:191-194. doi: 10.1016/j.critrevonc.2017.03.022. Epub 2017 Mar 22. PMID: 28427508.
- Heizmann M, Baerlocher GM, Steinmann F, Horber FF, Wuillemin W. Anti-Xa activity in obese patients after double standard dose of nadroparin for prophylaxis. Thromb Res. 2002 May 15;106(4-5):179-81. doi: 10.1016/s0049-3848(02)00188-3. PMID: 12297122.
- Liu J, Qiao X, Wu M, Wang H, Luo H, Zhang H, Chen Y, Sun J, Tang B. Strategies involving low-molecular-weight heparin for the treatment and prevention of venous thromboembolism in patients with obesity: A systematic review and meta-analysis. Front Endocrinol (Lausanne). 2023 Mar 8;14:1084511. doi: 10.3389/fendo.2023.1084511. PMID: 36967796; PMCID: PMC10031025.
- Schijns W, Deenen MJ, Aarts EO, Homan J, Janssen IMC, Berends FJ, Kaasjager KAH. The Effect of Obesity on Anti-Xa Concentrations in Bariatric Patients. Obes Surg. 2018 Jul;28(7):1997-2005. doi: 10.1007/s11695-018-3130-2. PMID: 29404935.
Evidence table for systematic review of RCTs and observational studies (intervention studies)
Research question: What is the (un)favorable effect of a high dose low-molecular-weight-heparin (LMWH) based on total body weight compared to a standard dose LMWH in patients with obesity undergoing surgery requiring general anesthesia?
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C)
|
Follow-up |
Outcome measures and effect size |
Comments |
|
Amaral, 2022
[individual study characteristics deduced from [1st author, year of publication ]]
PS., study characteristics and results are extracted from the SR (unless stated otherwise) |
SR and meta-analysis of [RCTs / cohort / case-control studies]
Literature search up to [month/year]
A: Ebrahimifard, 2012 B: Imberti, 2014 C: Steib, 2016
Study design: RCT
Setting and Country: A: Iran B: Italy C: France
Source of funding and conflicts of interest: [commercial / non-commercial / industrial co-authorship] A: institutional support, no financial disclosure B: commercial: "The sponsor had no role in the design and conduct of the study, management, analysis, interpretation of the data and preparation, review or approval of the manuscript" C: Sponsored two thirds by institutional grants (Program of Interregional Research) and one third by industrial grants (Sanofi-Aventis). Funding was managed by the Research Department of Strasbourg University Hospital." Quote: "Financial supporters had no role in the design and conduct of the study, in the collection and analysis of the data, or in the preparation of the manuscript." |
Inclusion criteria SR: RCTs and quasi-RCTs in males and females of any age undergoing bariatric surgery comparing pharmacological interventions for VTE (alone or in combination) with the same pharmacological intervention administered at a different dose or frequency, the same pharmacological intervention started at a different time point, a different pharmacological intervention, no treatment or placebo.
Exclusion criteria SR: participants receiving treatment for current VTE episodes, and those treated for VTE within the previous 30 days.
Out of the 7 studies included in the Cochrane review, 3 studies were included in the current analysis
Important patient characteristics at baseline:
N, mean age A: 71/68 patients, 36.7 yrs B: 119/131, 40.9 yrs C: 100/48, 40 yrs
Sex M/F: A: 13/126 B: 51/199 C: 29/107
Mean BMI: A: 44.29 (SD 6.9) B: 44.2 (SD 5.4) C: 47 (SD 1)
Groups comparable at baseline? Yes |
Describe intervention:
A: Unfractionated heparin 5000 IU TID B: Parnaparin 6400 IU/day starting 12 hours preoperatively for a period of 9 days C: Enoxaparin 6000 IU/day
|
Describe control:
A: Unfractionated heparin 5000 IU BID B: Parnaparin 4250 IU/day starting 12 hours preoperatively for a period of 9 days C: Enoxaparin 4000 IU/day
|
End-point of follow-up:
A: 10 days B: 3 months C: 30 days
For how many participants were no complete outcome data available? (intervention/control) A: 0/0 B: 8 (3.1%) participants were excluded after randomisation. There is no substantial difference between the number of participants in the groups (experimental 119 (47.6%) and control 131 (52.4%)). C: 16 participants were not treated according to protocol (9%), but the reasons were reported, and the losses were balanced between the groups.
|
All-cause mortality The eKect of higher-dose heparin on all-cause mortality compared to standard-dose heparins from 10 to 90 days was not estimable (no events in either group; low-certainty evidence). We downgraded the certainty of the evidence by two levels due to imprecision (no events). The test for subgroup differences and the sensitivity analysis were not applicable because there were no events.
Venous thromboembolism Only Imberti 2014b reported VTE events. The other studies reported no events in either group. Higher-dose heparin may result in little or no difference in VTE compared to standard-dose heparin in people undergoing bariatric surgery (RR 0.55, 95% CI 0.05 to 5.99).
Major bleeding Higher-dose heparin may result in little or no difference in major bleeding compared to standard-dose heparin in people undergoing bariatric surgery (RR 1.19, 95% CI 0.48 to 2.96; I2 = 8%)
|
Risk of bias (high, some concerns or low): Tool used by authors: Cochrane risk of bias tool
A: Some concerns B: Some concerns C: Some concerns
Facultative:
Brief description of author’s conclusion
“Compared to standard-dose heparin, higher-dose heparin may result in little or no difference in the risk of VTE (RR 0.55, 95% CI 0.05 to 5.99; 4 studies, 597 participants) or major bleeding (RR 1.19, 95% CI 0.48 to 2.96; I2 = 8%; 4 studies, 597 participants; low-certainty) in people undergoing bariatric surgery. The evidence on all-cause mortality, VTE-related mortality, PE, DVT and adverse events (thrombocytopenia) is uncertain (effect not estimable or very low-certainty evidence).”
Personal remarks on study quality, conclusions, and other issues (potentially) relevant to the research question One study (Kalfarentzos 2001) used a relatively high dose of LMWH (nadroparin 5700 IU/day) and therefore was excluded from our current analysis. This did not have a major effect on the conclusions. |
For the risk of bias table, we refer to the Cochrane review by Amaral (2022).
Risk of bias was judged as some concerns for the outcome ‘major bleeding’ due to lack of blinding.
Table of excluded studies
|
Reference |
Reason for exclusion |
|
Liu J, Qiao X, Wu M, Wang H, Luo H, Zhang H, Chen Y, Sun J, Tang B. Strategies involving low-molecular-weight heparin for the treatment and prevention of venous thromboembolism in patients with obesity: A systematic review and meta-analysis. Front Endocrinol (Lausanne). 2023 Mar 8;14:1084511. doi: 10.3389/fendo.2023.1084511. PMID: 36967796; PMCID: PMC10031025. |
overlaps with included studies |
|
Venclauskas L, Maleckas A, Arcelus JI; ESA VTE Guidelines Task Force. European guidelines on perioperative venous thromboembolism prophylaxis: Surgery in the obese patient. Eur J Anaesthesiol. 2018 Feb;35(2):147-153. doi: 10.1097/EJA.0000000000000703. PMID: 29112546. |
narrative review |
|
Minze MG, Kwee YY, Hall RG 2nd. Low-Molecular-Weight Heparin Prophylaxis Dosing: Is Weight an Issue? J Pharm Technol. 2016 Apr;32(2):75-80. doi: 10.1177/8755122515617200. Epub 2015 Nov 18. PMID: 34860988; PMCID: PMC5998535. |
no RCTs included |
|
Bartlett MA, Mauck KF, Daniels PR. Prevention of venous thromboembolism in patients undergoing bariatric surgery. Vasc Health Risk Manag. 2015 Aug 17;11:461-77. doi: 10.2147/VHRM.S73799. PMID: 26316771; PMCID: PMC4544624. |
overlaps with included studies |
|
Willett KC, Alsharhan M, Durand C, Cooper MR. Dosing of enoxaparin for venous thromboembolism prophylaxis in obese patients. Ann Pharmacother. 2013 Dec;47(12):1717-20. doi: 10.1177/1060028013507902. Epub 2013 Dec 3. PMID: 24301685. |
no RCTs included |
|
Brotman DJ, Shihab HM, Prakasa KR, Kebede S, Haut ER, Sharma R, Shermock K, Chelladurai Y, Singh S, Segal JB. Pharmacologic and mechanical strategies for preventing venous thromboembolism after bariatric surgery: a systematic review and meta-analysis. JAMA Surg. 2013 Jul;148(7):675-86. doi: 10.1001/jamasurg.2013.72. PMID: 23754086. |
no RCTs included |
|
Hamad GG, Bergqvist D. Venous thromboembolism in bariatric surgery patients: an update of risk and prevention. Surg Obes Relat Dis. 2007 Jan-Feb;3(1):97-102. doi: 10.1016/j.soard.2006.10.002. Epub 2006 Dec 27. PMID: 17196437. |
wrong study design |
|
Gaborit B, Moulin PA, Bege T, Boullu S, Vincentelli C, Emungania O, Morange PE, Berdah S, Salem JE, Dutour A, Frere C. Lean body weight is the best scale for venous thromboprophylaxis algorithm in severely obese patients undergoing bariatric surgery. Pharmacol Res. 2018 May;131:211-217. doi: 10.1016/j.phrs.2018.02.012. Epub 2018 Feb 13. PMID: 29452290. |
not randomized |
|
Imberti D, Legnani C, Baldini E, Cini M, Nicolini A, Guerra M, De Paoli M, Zanardi A, Palareti G. Pharmacodynamics of low molecular weight heparin in patients undergoing bariatric surgery: a prospective, randomised study comparing two doses of parnaparin (BAFLUX study). Thromb Res. 2009 Dec;124(6):667-71. doi: 10.1016/j.thromres.2009.04.021. Epub 2009 May 30. PMID: 19482341. |
wrong outcomes |
|
Zhao Y, Ye Z, Lin J, Zhang Z, Tian P, Zhang Z, Zhang P, Cui X. Efficacy and Safety of Pharmacoprophylaxis for Venous Thromboembolism in Patients Undergoing Bariatric Surgery: a Systematic Review and Meta-analysis. Obes Surg. 2022 May;32(5):1701-1718. doi: 10.1007/s11695-021-05825-9. Epub 2022 Mar 17. PMID: 35296968. |
overlaps with included studies |
|
Ceccato D, Di Vincenzo A, Pagano C, Pesavento R, Prandoni P, Vettor R. Weight-adjusted versus fixed dose heparin thromboprophylaxis in hospitalized obese patients: A systematic review and meta-analysis. Eur J Intern Med. 2021 Jun;88:73-80. doi: 10.1016/j.ejim.2021.03.030. Epub 2021 Apr 19. PMID: 33888393. |
overlaps with included studies |
|
Shaikh S, Boneva D, Hai S, McKenney M, Elkbuli A. Venous thromboembolism chemoprophylaxis regimens in trauma and surgery patients with obesity: A systematic review. J Trauma Acute Care Surg. 2020 Apr;88(4):522-535. doi: 10.1097/TA.0000000000002538. PMID: 31688792. |
overlaps with included studies |
|
He Z, Morrissey H, Ball P. Review of current evidence available for guiding optimal Enoxaparin prophylactic dosing strategies in obese patients-Actual Weight-based vs Fixed. Crit Rev Oncol Hematol. 2017 May;113:191-194. doi: 10.1016/j.critrevonc.2017.03.022. Epub 2017 Mar 22. PMID: 28427508. |
does not include relevant RCTs, mainly observational studies |
|
Shelkrot M, Miraka J, Perez ME. Appropriate enoxaparin dose for venous thromboembolism prophylaxis in patients with extreme obesity. Hosp Pharm. 2014 Sep;49(8):740-7. doi: 10.1310/hpj4908-740. PMID: 25477599; PMCID: PMC4252202. |
no RCTs included |
|
Ikesaka R, Delluc A, Le Gal G, Carrier M. Efficacy and safety of weight-adjusted heparin prophylaxis for the prevention of acute venous thromboembolism among obese patients undergoing bariatric surgery: a systematic review and meta-analysis. Thromb Res. 2014 Apr;133(4):682-7. doi: 10.1016/j.thromres.2014.01.021. Epub 2014 Jan 23. PMID: 24508449. |
overlaps with included studies |
|
Becattini C, Agnelli G, Manina G, Noya G, Rondelli F. Venous thromboembolism after laparoscopic bariatric surgery for morbid obesity: clinical burden and prevention. Surg Obes Relat Dis. 2012 Jan-Feb;8(1):108-15. doi: 10.1016/j.soard.2011.09.005. Epub 2011 Sep 16. PMID: 22014482. |
not the best SR |
|
Imberti D, Baldini E, Pierfranceschi MG, Nicolini A, Cartelli C, De Paoli M, Boni M, Filippucci E, Cariani S, Bottani G. Prophylaxis of venous thromboembolism with low molecular weight heparin in bariatric surgery: a prospective, randomised pilot study evaluating two doses of parnaparin (BAFLUX Study). Obes Surg. 2014 Feb;24(2):284-91. doi: 10.1007/s11695-013-1105-x. PMID: 24163189; PMCID: PMC3885801. |
included in Amaral 2022 |
|
Kalfarentzos F, Stavropoulou F, Yarmenitis S, Kehagias I, Karamesini M, Dimitrakopoulos A, Maniati A. Prophylaxis of venous thromboembolism using two different doses of low-molecular-weight heparin (nadroparin) in bariatric surgery: a prospective randomized trial. Obes Surg. 2001 Dec;11(6):670-6. doi: 10.1381/09608920160558588. PMID: 11775562. |
included in Amaral 2022 |
|
Abildgaard A, Madsen SA, Hvas AM. Dosage of Anticoagulants in Obesity: Recommendations Based on a Systematic Review. Semin Thromb Hemost. 2020 Nov;46(8):932-969. doi: 10.1055/s-0040-1718405. Epub 2020 Dec 23. PMID: 33368113. |
wrong study design |
|
Hussain Z, Curtain C, Mirkazemi C, Zaidi STR. Peri-operative Medication Dosing in Adult Obese Elective Surgical Patients: A Systematic Review of Clinical Studies. Clin Drug Investig. 2018 Aug;38(8):673-693. doi: 10.1007/s40261-018-0662-0. PMID: 29855999. |
overlaps with included studies |
|
Kalfarentzos F, Stavropoulou F, Yarmenitis S, Kehagias I, Karamesini M, Dimitrakopoulos A, Maniati A. Prophylaxis of venous thromboembolism using two different doses of low-molecular-weight heparin (nadroparin) in bariatric surgery: a prospective randomized trial. Obes Surg. 2001 Dec;11(6):670-6. doi: 10.1381/09608920160558588. PMID: 11775562. |
Wrong dosis, not conform Dutch clinical setting |
Beoordelingsdatum en geldigheid
Publicatiedatum : 15-04-2025
Beoordeeld op geldigheid : 09-04-2025
Algemene gegevens
De ontwikkeling van deze richtlijn werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
De financier heeft geen enkele invloed gehad op de inhoud van de richtlijn.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2022 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de anesthesiologische zorg voor patiënten met obesitas.
Werkgroep
Dr. T.A. Brouwer, anesthesioloog, NVA
Drs. M.A.M. Siepel, anesthesioloog, NVA
Drs. A.D. Pot, anesthesioloog, NVA
Drs. S.D.X. Oei, AIOS anesthesiologie, NVA (vanaf september 2022)
Dr. B. Torensma, PhD, anesthesiemedewerker, NVAM
Drs. J.A. Apers, chirurg, NVvH
Dr. L. Freeman, gynaecoloog, NVOG (tot oktober 2022)
Dr. D.D.C.A. Henriquez, gynaecoloog, NVOG (vanaf oktober 2022)
Prof. dr. C. A. J. Knibbe, ziekenhuisapotheker, NVZA
Drs. M.A. Damhof, ziekenhuisapotheker, NVZA (vanaf december 2023)
Dr. H.J. Reesink, longarts, NVALT
Drs. H.L. Lutgers, internist-endocrinoloog, NIV (vanaf april 2023)
N.G. Cnossen, patiëntvertegenwoordiger, Nederlandse Stichting Over Gewicht
Klankbordgroep
Dr. M. Klemt-Kropp, MDL-arts, NVMDL
Drs. Ö. Engin, oogarts, NOG
Dr. H. Buter, internist-intensivist, NVIC
N.J.C. Raeijmaekers, BSc, diëtist, NVD/NDBC
Met ondersteuning van
Drs. I. van Dusseldorp, literatuurspecialist, Kennisinstituut van de Federatie van Medisch Specialisten
Dr. J.C. Maas, adviseur, Kennisinstituut van de Federatie van Medisch Specialisten
Drs. I. van Dijk, adviseur, Kennisinstituut van de Federatie van Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Tammo Brouwer (voorzitter) |
Anesthesioloog, vrij ondernemer. |
Geen |
Geen |
Geen restricties |
|
Alice Dorien Pot |
Anesthesioloog in Meander Medisch Centrum Amersfoort |
Co-auteur boek 'klinische kinderanesthesiologie in de praktijk', initiatief vanuit NVA, uitgeverij Prelum (onbetaald). |
Geen |
Geen restricties |
|
Bart Torensma |
Klinisch epidemioloog en data scientist via eigen bedrijf Torensma Research Consultancy BV. |
"Dagelijks bestuurslid (penningmeester) Stichting COREON Algemeen bestuurslid Vereniging voor epidemiologen. Lesgeven aan de research verpleegkundige Breederode hogeschool Rotterdam
Masterclass gemaakt samen met Medtronic AUE over ERABS en team samenwerkingen." |
Voor PhD (<3 jaar geleden) onderzoek gedaan naar deep block verslapping bij patiënten met obesitas. Deze studie is destijds door MSD gesponsord in de vorm van gratis ampullen sugammadex.
|
Geen restricties |
|
Catherijne A.J. Knibbe |
Ziekenhuisapotheker-klinisch farmacoloog, St. Antonius ziekenhuis Nieuwegein en Utrecht, afdeling Klinische farmacie |
Lid CCMO, Lid Board ACCP |
Diverse studies gefinancierd door ZonMw of Antonius Onderzoeksfonds. De onderzoeken zijn niet gerelateerd aan de richtlijn. |
Geen restricties |
|
Dacia Henriquez |
Gynaecoloog, Amphia Ziekenhuis |
Geen |
Geen |
Geen restricties |
|
Helen Lutgers |
Internist in Ommelander Ziekenhuis Groningen |
Geen |
Geen |
Geen restricties |
|
Herre Reesink |
Longarts, OLVG Amsterdam |
Geen |
Geen |
Geen restricties |
|
Jan Apers |
Chirurg Franciscus Gasthuis & Vlietland |
NVGIC bestuur Dutch Obesity Academy |
Geen |
Geen restricties |
|
Liv Freeman |
Gynaecoloog Ikazia Ziekenhuis Rotterdam |
Voorzitter samenwerking obstetrie anesthesie (onbetaald)
|
Geen |
Geen restricties |
|
Michiel Damhof
|
Ziekenhuisapotheker Medisch Centrum Leeuwarden |
Geen |
Geen |
Geen restricties |
|
Muriel Arianne Michelle Siepel |
Anesthesioloog OLVG Amsterdam |
Geen |
Geen |
Geen restricties |
|
Nienke Cnossen |
Patiëntvertegenwoordiger |
Geen |
Geen |
Geen restricties |
|
Sander Oei |
Aios anesthesiologie. ErasmusMC |
SITdiensten Park Medisch Centrum, betaald. 1-2x/mnd ANWdiensten verpleeghuizen, betaald. 1x/mnd |
Geen |
Geen restricties |
|
Hanneke Buter |
Intensivist |
bestuurslid NVIC |
Geen |
Geen restricties |
|
Michael Klemt-Kropp |
MDL-arts |
Geen |
Geen |
Geen restricties |
|
Natascha Raeijmaekers |
Diëtist Obesitas Centrum, ETZ. Betaald. |
Bestuur Netwerk Diëtisten Bariatrische chirurgie, onbetaald. |
Geen |
Geen restricties |
|
Ozlem Engin |
Oogarts |
Geen |
Geen |
Geen restricties |
|
Irma van Dijk |
Adviseur kennisinstituut van de Federatie Medisch Specialisten |
Geen |
Geen |
Geen restricties |
|
José Maas |
Adviseur kennisinstituut van de Federatie Medisch specialisten |
Geen |
Geen |
Geen restricties |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door het uitnodigen van een afvaardiging van de Nederlandse ‘Stichting ‘Overgewicht’ in de werkgroep. Het verslag van de knelpunteninventarisatie [zie aanverwante producten] is besproken in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de Stichting en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijn op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Module |
Uitkomst raming |
Toelichting |
|
Module Tromboseprofylaxe |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het overgrote deel (±90%) van de zorgaanbieders en zorgverleners al aan de norm voldoet. Er worden daarom geen substantiële financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de anesthesiologische zorg voor patiënten met obesitas. Tevens zijn er knelpunten aangedragen door relevante partijen via een schriftelijke knelpunteninventarisatie. Een verslag hiervan is opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effect model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Literature search strategy
|
Richtlijn: NVA Anesthesie bij obesitas |
|
|
Uitgangsvraag: Wat is de optimale dosis voor tromboseprofylaxe bij patiënten met obesitas die een chirurgische ingreep ondergaan?
|
|
|
Database(s): Ovid/Medline, Embase |
Datum:1-6-2023 |
|
Periode: 2005- |
Talen: nvt |
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SRs |
174 |
108 |
195 |
|
RCTs |
119 |
95 |
157 |
|
Totaal |
|
|
352 |
Zoekstrategie
Embase
|
No. |
Query |
Results |
|
#25 |
#10 OR #24 |
293 |
|
#24 |
#5 AND #23 NOT #10 RCT |
119 |
|
#23 |
'randomized controlled trial'/exp OR random*:ti,ab OR (((pragmatic OR practical) NEAR/1 'clinical trial*'):ti,ab) OR ((('non inferiority' OR noninferiority OR superiority OR equivalence) NEAR/3 trial*):ti,ab) OR rct:ti,ab,kw |
2058547 |
|
#22 |
#13 AND #21 |
4 |
|
#21 |
'14651858':is OR 'cochrane database of systematic reviews'/jt |
17197 |
|
#20 |
#18 NOT #19 |
1 |
|
#19 |
#13 AND #18 1 sleutelartikel niet gevonden vanwege jaartal |
3 |
|
#18 |
#14 OR #15 OR #16 OR #17 sleutelartikelen |
4 |
|
#17 |
'low-molecular-weight heparins in renal impairment and obesity: available evidence and clinical practice recommendations across medical and surgical settings' |
1 |
|
#16 |
'new protocol for venous thromboembolism prophylaxis in bariatric surgery' |
1 |
|
#15 |
'prophylaxis of venous thromboembolism using two different doses of low-molecular-weight heparin (nadroparin) in bariatric surgery: a prospective randomized trial' |
1 |
|
#14 |
'population pharmacodynamic model for low molecular weight heparin nadroparin in morbidly obese and non-obese patients using anti-xa levels as endpoint' |
1 |
|
#13 |
#10 OR #11 OR #12 |
1296 |
|
#12 |
#5 AND (#8 OR #9) NOT #10 NOT #11 |
707 |
|
#11 |
#5 AND #7 NOT #10 |
415 |
|
#10 |
#5 AND #6 SR |
174 |
|
#9 |
'case control study'/de OR 'comparative study'/exp OR 'control group'/de OR 'controlled study'/de OR 'controlled clinical trial'/de OR 'crossover procedure'/de OR 'double blind procedure'/de OR 'phase 2 clinical trial'/de OR 'phase 3 clinical trial'/de OR 'phase 4 clinical trial'/de OR 'pretest posttest design'/de OR 'pretest posttest control group design'/de OR 'quasi experimental study'/de OR 'single blind procedure'/de OR 'triple blind procedure'/de OR (((control OR controlled) NEAR/6 trial):ti,ab,kw) OR (((control OR controlled) NEAR/6 (study OR studies)):ti,ab,kw) OR (((control OR controlled) NEAR/1 active):ti,ab,kw) OR 'open label*':ti,ab,kw OR (((double OR two OR three OR multi OR trial) NEAR/1 (arm OR arms)):ti,ab,kw) OR ((allocat* NEAR/10 (arm OR arms)):ti,ab,kw) OR placebo*:ti,ab,kw OR 'sham-control*':ti,ab,kw OR (((single OR double OR triple OR assessor) NEAR/1 (blind* OR masked)):ti,ab,kw) OR nonrandom*:ti,ab,kw OR 'non-random*':ti,ab,kw OR 'quasi-experiment*':ti,ab,kw OR crossover:ti,ab,kw OR 'cross over':ti,ab,kw OR 'parallel group*':ti,ab,kw OR 'factorial trial':ti,ab,kw OR ((phase NEAR/5 (study OR trial)):ti,ab,kw) OR ((case* NEAR/6 (matched OR control*)):ti,ab,kw) OR ((match* NEAR/6 (pair OR pairs OR cohort* OR control* OR group* OR healthy OR age OR sex OR gender OR patient* OR subject* OR participant*)):ti,ab,kw) OR ((propensity NEAR/6 (scor* OR match*)):ti,ab,kw) OR versus:ti OR vs:ti OR compar*:ti OR ((compar* NEAR/1 study):ti,ab,kw) OR (('major clinical study'/de OR 'clinical study'/de OR 'cohort analysis'/de OR 'observational study'/de OR 'cross-sectional study'/de OR 'multicenter study'/de OR 'correlational study'/de OR 'follow up'/de OR cohort*:ti,ab,kw OR 'follow up':ti,ab,kw OR followup:ti,ab,kw OR longitudinal*:ti,ab,kw OR prospective*:ti,ab,kw OR retrospective*:ti,ab,kw OR observational*:ti,ab,kw OR 'cross sectional*':ti,ab,kw OR cross?ectional*:ti,ab,kw OR multicent*:ti,ab,kw OR 'multi-cent*':ti,ab,kw OR consecutive*:ti,ab,kw) AND (group:ti,ab,kw OR groups:ti,ab,kw OR subgroup*:ti,ab,kw OR versus:ti,ab,kw OR vs:ti,ab,kw OR compar*:ti,ab,kw OR 'odds ratio*':ab OR 'relative odds':ab OR 'risk ratio*':ab OR 'relative risk*':ab OR 'rate ratio':ab OR aor:ab OR arr:ab OR rrr:ab OR ((('or' OR 'rr') NEAR/6 ci):ab))) |
14134447 |
|
#8 |
'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'comparative study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) |
6767914 |
|
#7 |
'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti |
3302394 |
|
#6 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
931763 |
|
#5 |
#4 AND [2005-2023]/py NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
1820 |
|
#4 |
#3 NOT (('adolescent'/exp OR 'child'/exp OR adolescent*:ti,ab,kw OR child*:ti,ab,kw OR schoolchild*:ti,ab,kw OR infant*:ti,ab,kw OR girl*:ti,ab,kw OR boy*:ti,ab,kw OR teen:ti,ab,kw OR teens:ti,ab,kw OR teenager*:ti,ab,kw OR youth*:ti,ab,kw OR pediatr*:ti,ab,kw OR paediatr*:ti,ab,kw OR puber*:ti,ab,kw) NOT ('adult'/exp OR 'aged'/exp OR 'middle aged'/exp OR adult*:ti,ab,kw OR man:ti,ab,kw OR men:ti,ab,kw OR woman:ti,ab,kw OR women:ti,ab,kw)) |
3147 |
|
#3 |
#1 AND #2 |
3234 |
|
#2 |
'thrombosis prevention'/exp OR 'thromboprophylaxis':ti,ab,kw OR (((thrombo* OR vte OR dvt) NEAR/3 (preventi* OR prophylax*)):ti,ab,kw) OR 'low molecular weight heparin'/exp OR 'bm 2123':ti,ab,kw OR 'bm2123':ti,ab,kw OR 'choay':ti,ab,kw OR 'depolymerized heparin':ti,ab,kw OR 'ebpm 1':ti,ab,kw OR 'ebpm 2':ti,ab,kw OR 'ebpm 3':ti,ab,kw OR 'ebpm1':ti,ab,kw OR 'ebpm2':ti,ab,kw OR 'ebpm3':ti,ab,kw OR 'ff 1034':ti,ab,kw OR 'ff1034':ti,ab,kw OR 'fr 860':ti,ab,kw OR 'fr860':ti,ab,kw OR 'gag 869':ti,ab,kw OR 'heparin lmw 2133':ti,ab,kw OR 'low molecular heparin':ti,ab,kw OR 'low molecular weight heparin':ti,ab,kw OR 'nm heparin':ti,ab,kw OR 'pk 007':ti,ab,kw OR 'sandoz 5100':ti,ab,kw OR 'sandoz 6700':ti,ab,kw OR 'traxyparine':ti,ab,kw OR 'nadroparin'/exp OR 'cy 216':ti,ab,kw OR 'cy 216d':ti,ab,kw OR 'cy216':ti,ab,kw OR 'cy216d':ti,ab,kw OR 'fraxiparin':ti,ab,kw OR 'fraxodi':ti,ab,kw OR 'nadroparin*':ti,ab,kw OR 'seledie':ti,ab,kw OR 'seleparina':ti,ab,kw OR 'seleparine':ti,ab,kw OR 'tedegliparin':ti,ab,kw |
109622 |
|
#1 |
'obesity'/exp/mj OR 'bariatric surgery'/exp OR 'obese patient'/exp OR obes*:ti,ab,kw OR obesit*:ti,ab,kw OR overweight*:ti,ab,kw OR 'over weight*':ti,ab,kw OR 'adipositas':ti,ab,kw OR 'adiposity':ti,ab,kw OR 'excess body weight':ti,ab,kw OR 'corpulen*':ti,ab,kw OR 'fat overload syndrome':ti,ab,kw OR 'increased bmi':ti,ab,kw OR bariatr*:ti,ab,kw |
695364 |
Ovid/Medline
|
# |
Searches |
Results |
|
9 |
7 or 8 |
203 |
|
8 |
(4 and 6) not 7 RCT |
95 |
|
7 |
4 and 5 SR |
108 |
|
6 |
exp randomized controlled trial/ or randomized controlled trials as topic/ or random*.ti,ab. or rct?.ti,ab. or ((pragmatic or practical) adj "clinical trial*").ti,ab,kf. or ((non-inferiority or noninferiority or superiority or equivalence) adj3 trial*).ti,ab,kf. |
1616235 |
|
5 |
meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf. |
671116 |
|
4 |
3 not ((Adolescent/ or Child/ or Infant/ or adolescen*.ti,ab,kf. or child*.ti,ab,kf. or schoolchild*.ti,ab,kf. or infant*.ti,ab,kf. or girl*.ti,ab,kf. or boy*.ti,ab,kf. or teen.ti,ab,kf. or teens.ti,ab,kf. or teenager*.ti,ab,kf. or youth*.ti,ab,kf. or pediatr*.ti,ab,kf. or paediatr*.ti,ab,kf. or puber*.ti,ab,kf.) not (Adult/ or adult*.ti,ab,kf. or man.ti,ab,kf. or men.ti,ab,kf. or woman.ti,ab,kf. or women.ti,ab,kf.)) |
1053 |
|
3 |
1 and 2 |
1078 |
|
2 |
exp Heparin, Low-Molecular-Weight/ or Nadroparin/ or ((Thrombosis/ or Venous Thrombosis/ or Thromboembolism/) and exp Primary Prevention/) or thromboprophylaxis.ti,ab,kf. or ((thrombo* or vte or dvt) adj3 (preventi* or prophylax*)).ti,ab,kf. or bm 2123.ti,ab,kf. or bm2123.ti,ab,kf. or choay.ti,ab,kf. or depolymerized heparin.ti,ab,kf. or ebpm 1.ti,ab,kf. or ebpm 2.ti,ab,kf. or ebpm 3.ti,ab,kf. or ebpm1.ti,ab,kf. or ebpm2.ti,ab,kf. or ebpm3.ti,ab,kf. or ff 1034.ti,ab,kf. or ff1034.ti,ab,kf. or fr 860.ti,ab,kf. or fr860.ti,ab,kf. or gag 869.ti,ab,kf. or heparin lmw 2133.ti,ab,kf. or low molecular heparin.ti,ab,kf. or low molecular weight heparin.ti,ab,kf. or nm heparin.ti,ab,kf. or "pk 007".ti,ab,kf. or sandoz 5100.ti,ab,kf. or sandoz 6700.ti,ab,kf. or traxyparine.ti,ab,kf. or cy 216.ti,ab,kf. or cy 216d.ti,ab,kf. or cy216.ti,ab,kf. or cy216d.ti,ab,kf. or fraxiparin.ti,ab,kf. or fraxodi.ti,ab,kf. or nadroparin*.ti,ab,kf. or seledie.ti,ab,kf. or seleparina.ti,ab,kf. or seleparine.ti,ab,kf. or tedegliparin.ti,ab,kf. |
36359 |
|
1 |
exp Obesity/ or obese*.ti,ab,kf. or obesit*.ti,ab,kf. or overweight*.ti,ab,kf. or 'over weight*'.ti,ab,kf. or exp Bariatric Surgery/ or bariatr*.ti,ab,kf. |
460469 |