Behandeling pericolisch extraluminaal lucht
Uitgangsvraag
Wat dient het beleid te zijn bij patiënten met pericolisch extraluminaal lucht?
Aanbeveling
Behandel patiënten met diverticulitis en geïsoleerd pericolisch extraluminaal lucht initieel conservatief en laat de behandelstrategie daarna afhangen van het klinisch beloop.
Overweeg patiënten met diverticulitis en geïsoleerd pericolisch extraluminaal lucht routinematig met antibiotica te behandelen.
Overweeg bij patiënten met diverticulitis en geïsoleerd pericolisch extraluminaal lucht een routinematige klinische opname om het ziektebeloop te monitoren.
Overwegingen
Despite the frequent occurrence of pericolic extraluminal air in acute diverticulitis patients (up to 15%), little is known about the natural course and required treatment. Current treatment is based on individual opinion and experiences and it is not clear whether extraluminal air should be considered mild diverticulitis with a benign disease course or complicated diverticulitis requiring more aggressive treatment.
Seven studies reported rates of need for emergency surgery during the initial episode of diverticulitis with pericolic extraluminal air. Six of those studies reported crude data, yielding a pooled need for emergency surgery in 6% of the patients (95% CI 3% to 12%). The need for percutaneous abscess drainage was reported in 3 studies including only 56 patients; no events were observed. No adequate comparisons between uncomplicated patients and pericolic extraluminal air patients could be made. Therefore, these results can only be compared with available rates from other literature including uncomplicated diverticulitis. These rates of 1% to 2% need for emergency surgery in uncomplicated diverticulitis are slightly lower than the 6% in pericolic extraluminal air patients. (Chabok, 2012; Daniels, 2017; Hong, 2015) Some limitations should be considered for interpretation of these results. First, all studies were observational cohort studies and 4 out of the 7 studies were retrospective. Second, most studies did not define the decision-making process for emergency surgery. Therefore it is unclear for which reasons the patents needed emergency surgery. The presence of extraluminal air may lower the threshold for surgery because of the fear of progression into free perforation. Consequently, the found rate of 6% may be an overestimation. Third, the need for percutaneous abscess drainage was only reported 3 studies including 56 patients. Since percutaneous interventions represent an increasing part of all interventions, the lack of reports about the need for percutaneous abscess drainage may have led to an underestimation of the actual need for interventions. Fourth, since almost all studies treated the patients with antibiotics routinely, the role of antibiotics remains unclear.
Although the need for emergency surgery rate in pericolic extraluminal air patients is slightly higher than in uncomplicated patients, the vast majority has a benign course and does not need intervention. This 94% success rate of non-operative treatment in these patients seems to justify a conservative approach. Since evidence on non-antibiotic treatment of these patients is lacking, routine antibiotic treatment seems appropriate. Also, due to the suggestion of a slightly more virulent course than uncomplicated diverticulitis patients, these patients seem not to be candidates for outpatient treatment.
Onderbouwing
Although approximately 15% of all acute diverticulitis patients have pericolic extraluminal air on computed tomography (CT), studies on the natural course in these patients are scarce and consensus about the treatment is lacking. It is not clear whether these patients behave as mild uncomplicated diverticulitis or as severe diverticulitis needing more aggressive treatment. Currently, these patients are treated based on personal experiences and opinions of the treating physician which may cause over- or under treatment in these patients.
|
Zeer laag GRADE |
Ongeveer 6% van de patiënten met diverticulitis en geïsoleerd pericolisch extraluminaal lucht ondergaan acute chirurgie tijdens de initiële diverticulitis episode.
Bronnen (Costi, 2012; Dharmarajan, 2011; Lahat, 2013; Mora, 2013; Sallinen, 2014; Sallinen, 2015; Thorisson, 2016) |
|
Zeer laag GRADE |
De patiëntaantallen in de literatuur zijn vooralsnog te laag voor duidelijke conclusies ten aanzien van de noodzaak tot percutane drainage in het beloop van de ziekte.
Bronnen (Dharmarajan, 2011; Lahat, 2013; Mora, 2013) |
Three prospective cohort studies (Lahat, 2013; Mora, 2013; Thorisson, 2016) and 4 retrospective cohort studies (Costi, 2012; Dharmarajan, 2011; Sallinen, 2014; Sallinen, 2015) were included. Six studies were conducted in Europe and 1 study in the United States of America. Although all studies reported pericolic extraluminal air patients separately from distant free air patients, a wide variety of definitions for pericolic extraluminal air was used. Only 3 studies clearly specified the location of the extraluminal air as within 5 centimetres of the inflamed bowel segment. Other studies used definitions such as contained perforation, localized pericolic free air and air within the mesentery. Since pericolic extraluminal air was not the primary aim of all studies, some studies applied inclusion criteria that may have caused selection bias in patients with pericolic extraluminal air. A Spanish study particularly, only included patients without comorbidity and with absence of all systemic inflammatory response syndrome (SIRS) criteria. (Mora, 2013) Five studies treated all patients with antibiotics, 1 study (Thorisson, 2016) only treated part of the patients with antibiotics and 1 study (Sallinen, 2015) did not state anything about antibiotic treatment. Need for emergency surgery was reported in 7 studies and need for percutaneous abscess drainage in 3 studies. A control group was included in 3 studies. Although, only 1 study (Mora, 2013) compared the pericolic extraluminal air patients to uncomplicated diverticulitis patients. The other two studies (Sallinen, 2015; Thorisson, 2016) made a comparison with a group of patients containing perforations or abscesses.
A total of 195 pericolic extraluminal air patients was included in this review. Rates of emergency surgery were reported in 195 patients and rates of percutaneous abscess drainage in 56 patients.
Resultaten
Need for emergency surgery
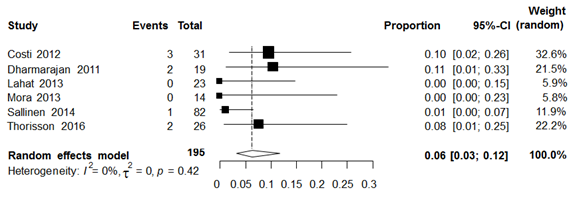
Seven studies reported rates of emergency surgery. Six studies provided crude data and could be pooled in a forest plot. (Figure 1) A pooled rate of 6% (95% CI 3% to 12%) of pericolic extraluminal air patients underwent emergency surgery. One study (Sallinen, 2015) only reported an adjusted odds ratio for the need for emergency surgery (0.03, 95% CI 0.01 to 0.08). However, since the control group consisted of all patients including free perforation, interpretation of this odds ratio is hampered. A comparison of rates of emergency surgery between pericolic extraluminal air patients and uncomplicated diverticulitis patients was reported in 1 study. (Mora, 2013) In the pericolic extraluminal air group 0% (0/14) underwent emergency surgery versus 0% (0/54) in the uncomplicated group.
 Figure 1 Forest plot of pooled rate of need for emergency surgery in pericolic extraluminal air patients.
Figure 1 Forest plot of pooled rate of need for emergency surgery in pericolic extraluminal air patients.
Need for percutaneous abscess drainage
The need for percutaneous abscess drainage was only reported in 3 studies. From a combined total of 56 patients, no patients underwent percutaneous abscess drainage. Only 1 study compared the need for percutaneous abscess drainage between pericolic extraluminal air patients and uncomplicated diverticulitis patients with no events in both groups. (Mora, 2013)
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat noodzaak tot spoedoperatie begon op ‘laag’ aangezien het bewijs afkomstig is uit observationeel onderzoek. Vervolgens is de bewijskracht met één niveau verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias); tegenstrijdige resultaten (inconsistentie); (bias ten gevolge van indirectheid); het geringe aantal patiënten (imprecisie).
De bewijskracht voor de uitkomstmaat noodzaak tot percutane abcesdrainage begon op ‘laag’ aangezien het bewijs afkomstig is uit observationeel onderzoek. Vervolgens is de bewijskracht met één niveau verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias); tegenstrijdige resultaten (inconsistentie (bias ten gevolge van indirectheid); het geringe aantal patiënten (imprecisie).
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag:
Wat zijn de (on)gunstige effecten van een conservatieve behandeling van diverticulitis met pericolisch extraluminaal lucht (eventueel met antibiotica) ten opzichte van een directe interventie, chirurgisch dan wel percutaan (eventueel met antibiotica) bij patiënten met diverticulitis met geïsoleerd pericolisch extraluminaal lucht?
Patiënt: diverticulitis met geïsoleerd pericolisch extraluminaal lucht;
Interventie: conservatieve behandeling van diverticulitis met pericolisch extraluminaal lucht (eventueel met antibiotica);
Controle: directe interventie, chirurgisch dan wel percutaan (eventueel met antibiotica);
Outcome: noodzaak tot (aanvullende) spoedoperatie en/of percutane abcesdrainage.
Relevante uitkomstmaten
De werkgroep achtte noodzaak tot spoedoperatie en/of percutane abcesdrainage voor de besluitvorming kritieke uitkomstmaten. De werkgroep definieerde niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
Zoeken en selecteren (Methode)
In de databases Medline (OVID), EMBASE en de Cochrane Library (Wiley) is met relevante zoektermen gezocht naar systematische reviews, gerandomiseerde klinische onderzoeken en observationele onderzoeken. Tevens zijn de gerelateerde artikelen handmatig doorzocht. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 5857 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria:
- Volledige tekst artikelen beschikbaar (geen taalrestricties);
- Vergelijkend of beschrijvend onderzoek;
- Linkszijdige diverticulitis;
- Studies die een onderscheid maakten tussen de locatie van het extraluminale lucht waarbij voor deze uitgangsvraag studies die pericolisch extraluminaal lucht (of een verwant synoniem) apart beschreven werden geïncludeerd;
- Geïsoleerd pericolisch extraluminaal lucht (niet in combinatie met abces of lucht op afstand);
- Minimaal één van de uitkomsten beschreven;
- Diagnose diverticulitis bevestigd middels CT;
- Case reports en patiënten series van 5 patiënten of kleiner werden geëxcludeerd.
Op basis van titel en abstract werden in eerste instantie 189 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 182 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording) en 7 studies definitief geselecteerd.
Zeven onderzoeken zijn opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidence-tabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk of bias tabellen.
- Chabok A, Påhlman L, Hjern F, et al. AVOD Study Group. Randomized clinical trial of antibiotics in acute uncomplicated diverticulitis. Br J Surg. 2012;99(4):532-9. doi: 10.1002/bjs.8688. Epub 2012 Jan 30. PubMed PMID: 22290281.
- Costi R, Cauchy F, Le Bian A, et al. Challenging a classic myth: pneumoperitoneum associated with acute diverticulitis is not an indication for open or laparoscopic emergency surgery in hemodynamically stable patients. A 10-year experience with a nonoperative treatment. Surg Endosc. 2012;26:2061-71.
- Daniels L, Unlu C, de Korte N, et al. Randomized clinical trial of observational versus antibiotic treatment for a first episode of CT-proven uncomplicated acute diverticulitis. Br J Surg. 2017;104:52-61.
- Dharmarajan S, Hunt SR, Birnbaum EH, et al. The efficacy of nonoperative management of acute complicated diverticulitis. Dis Colon Rectum. 2011;54:663-71.
- Hong MK, Tomlin AM, Hayes IP, et al. Operative intervention rates for acute diverticulitis: a multicentre state-wide study. ANZ J Surg. 2015;85:734-8.
- Lahat A, Avidan B, Sakhnini E, et al. Acute diverticulitis: a decade of prospective follow-up. J Clin Gastroenterol. 2013;47:415-9.
- Mora Lopez L, Serra Pla S, Serra-Aracil X, et al. Application of a modified Neff classification to patients with uncomplicated diverticulitis. Colorectal Dis. 2013;15:1442-7.
- Sallinen VJ, Mentula PJ, Leppaniemi AK. Nonoperative management of perforated diverticulitis with extraluminal air is safe and effective in selected patients. Dis Colon Rectum. 2014;57:875-81.
- Sallinen VJ, Leppaniemi AK, Mentula PJ. Staging of acute diverticulitis based on clinical, radiologic, and physiologic parameters. J Trauma Acute Care Surg. 2015;78:543-51.
- Thorisson A, Smedh K, Torkzad MR, et al. CT imaging for prediction of complications and recurrence in acute uncomplicated diverticulitis. Int J Colorectal Dis. 2016;31:451-7.
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Costi, 2012
|
Type of study: retrospective cohort study
Setting: monocentre
Country: France
Source of funding: none |
Inclusion criteria: Pericolic extradigestive air (within 5cm from the sigmoid colon), hemodynamically stable patients without early surgery (<24h from admission)
Exclusion criteria: none
N total at baseline: Intervention: 31
Important prognostic factors2: Mean age 54.7y ± 13.7 |
Antibiotic and supportive treatment |
None |
Length of follow-up: Not mentioned
Loss-to-follow-up: Not mentioned
Incomplete outcome data: Not mentioned |
Need for emergency surgery 9.7% (3/31)
Need for percutaneous abscess drainage Not reported |
|
|
Dharmarajan, 2011
|
Type of study: retrospective cohort study
Setting: monocentre
Country: USA
Source of funding: none |
Inclusion criteria: Localized free air
Exclusion criteria: Earlier sigmoid resection, not operative candidates due to poor general medical condition or refused operative intervention
N total at baseline: 19
Important prognostic factors2: Not reported |
Antibiotic and supportive treatment |
None |
Length of follow-up: Not mentioned
Loss-to-follow-up: Not mentioned
Incomplete outcome data: Not mentioned |
Need for emergency surgery 10.5% (2/19)
Need for percutaneous abscess drainage 0.0% (0/19) |
|
|
Lahat, 2013
|
Type of study: prospective cohort study
Setting: monocentre
Country: Israel
Source of funding: not mentioned |
Inclusion criteria: Peridiverticular air
Exclusion criteria: none
N total at baseline: 23
Important prognostic factors2: Not reported |
Antibiotic and supportive treatment |
None |
Length of follow-up: Not mentioned
Loss-to-follow-up: Not mentioned
Incomplete outcome data: Not mentioned |
Need for emergency surgery 0.0% (0/23)
Need for percutaneous abscess drainage 0.0% (0/23)
|
|
|
Mora Lopez, 2013
|
Type of study: prospective cohort study
Setting: monocentre
Country: Spain
Source of funding: none |
Inclusion criteria: Localized pneumoperitoneum in the form of air bubbles
Exclusion criteria: Prior diverticulitis, patients with comorbidity or one of the SIRS criteria
N total at baseline: Intervention: 14 Control: 54
Important prognostic factors2: Not reported |
Antibiotic and supportive treatment |
Antibiotic and supportive treatment |
Length of follow-up: Not mentioned
Loss-to-follow-up: Not mentioned
Incomplete outcome data: Not mentioned |
Need for emergency surgery Pericolic air group 0.0% (0/14) Control group 0.0% (0/54)
Need for percutaneous abscess drainage Pericolic air group 0.0% (0/14) Control group 0.0% (0/54)
|
Control group consisted of patients without any type of perforation. |
|
Sallinen, 2014
|
Type of study: retrospective cohort study
Setting: monocentre
Country: Finland
Source of funding: none |
Inclusion criteria: Air bubbles or air collection within 5 cm of the inflamed bowel segment without distant air
Exclusion criteria: none
N total at baseline: 82
Important prognostic factors2: Age >65y n=12 (15%) |
Antibiotic and supportive treatment |
None |
Length of follow-up: initial hospital stay
Loss-to-follow-up: None
Incomplete outcome data: None |
Need for emergency surgery 1.2% (1/82)
Need for percutaneous abscess drainage Not reported |
|
|
Sallinen, 2015
|
Type of study: retrospective cohort study
Setting: monocentre
Country: Finland
Source of funding: funded by Martti I. Turunen foundation, Vatsatautien Tutkimussaatio Foundation, Mary and Georg Ehrnrooth’s Foundation, Finnish Surgical Society, and Governmental Competitive Funds (EVO). |
Inclusion criteria: Pericolic air (air bubbles or air collection within 5cm of the affected bowel segment without an abscess)
Exclusion criteria: none
N total at baseline: Not reported
Important prognostic factors2: Not reported
|
Not mentioned
|
Not mentioned |
Length of follow-up: Not mentioned
Loss-to-follow-up: Not mentioned
Incomplete outcome data: Not mentioned |
Need for emergency surgery Adjusted odds ratio 0.03 (95% CI 0.01 to 0.08)
Need for percutaneous abscess drainage Not reported |
Control group consisted of all other patients including abscess or free fluid. |
|
Thorisson, 2016
|
Type of study: prospective cohort study
Setting: multicentre
Country: Sweden, Iceland
Source of funding: not reported |
Inclusion criteria: Extraluminal pericolic air
Exclusion criteria: none
N total at baseline: Intervention: 26 Control: 596
Important prognostic factors2: Not reported |
Antibiotic (n=16) or observational (n=10) and supportive treatment |
Antibiotic or observational and supportive treatment |
Length of follow-up: initial hospital stay
Loss-to-follow-up: none
Incomplete outcome data: none |
Need for emergency surgery Pericolic air group 7.7% (2/26) Control group 0.5% (3/596)
Need for percutaneous abscess drainage Not reported |
|
Risk of bias tabel
|
Study reference
(first author, year of publication) |
Bias due to a non-representative or ill-defined sample of patients?1
(unlikely/likely/unclear) |
Bias due to insufficiently long, or incomplete follow-up, or differences in follow-up between treatment groups?2
(unlikely/likely/unclear) |
Bias due to ill-defined or inadequately measured outcome ?3
(unlikely/likely/unclear) |
Bias due to inadequate adjustment for all important prognostic factors?4
(unlikely/likely/unclear) |
|
Costi, 2012 |
Unlikely |
Unclear |
Unlikely |
Likely due to the lack of control group |
|
Dharmarajan, 2011 |
Unlikely |
Unclear |
Unlikely |
Likely due to the lack of control group |
|
Lahat, 2013 |
Unlikely |
Unclear |
Unlikely |
Likely due to the lack of control group |
|
Mora, 2013 |
Likely due to exclusion of patients with comorbidity or any SIRS criteria |
Unclear |
Unlikely |
Likely due to lack of adjustment for confounders |
|
Sallinen, 2014 |
Unlikely |
Unlikely |
Unlikely |
Likely due to the lack of control group |
|
Sallinen, 2015 |
Unlikely |
Unclear |
Unlikely |
Likely due to a not comparable control group and lack of adequate adjustment |
|
Thorisson, 2016 |
Unlikely |
Unlikely |
Unlikely |
Likely due to lack of adjustment for confounders |
Beoordelingsdatum en geldigheid
Publicatiedatum : 31-05-2018
Beoordeeld op geldigheid : 09-05-2018
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep niet in stand gehouden. Uiterlijk in 2023 bepaalt het bestuur van de Nederlandse Vereniging voor Heelkunde of de modules van deze richtlijn nog actueel zijn. Op modulair niveau is een onderhoudsplan beschreven. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De Nederlandse Vereniging voor Heelkunde is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (http://www.kennisinstituut.nl) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). Patiëntenparticipatie bij deze richtlijn werd mede gefinancierd uit de Kwaliteitsgelden Patiënten Consumenten (SKPC) binnen het programma KIDZ. De SKMS heeft geen enkele invloed gehad op de inhoud van de richtlijn.
Doel en doelgroep
Doel
Deze richtlijn is bedoeld om een evidence-based beleid voor de zorg voor patiënten met diverticulitis in de tweede lijn op te stellen.
Doelgroep
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen die betrokken zijn bij de zorg voor patiënten met diverticulitis, te weten chirurgen, maag- lever- darmartsen, internisten, radiologen en huisartsen. Een secundaire doelgroep zijn zorgverleners uit de eerste lijn die betrokken zijn bij de zorg rondom patiënten met diverticulitis, waaronder huisarts, verpleegkundigen (waaronder continentieverpleegkundige en verpleegkundig specialisten) en physician assistants.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2016 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met diverticulitis te maken hebben. Het Nederlands Huisartsen Genootschap (NHG) en de Nederlandse Vereniging voor Spoedeisende Hulp Artsen (NVSHA) zijn uitgenodigd om te participeren in de werkgroep maar heeft geen gebruik gemaakt van de uitnodiging.
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname.
De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn. Stefan van Dijk heeft onder begeleiding van Marja Boermeester de systematische analyses van de literatuur uitgewerkt.
Werkgroep
- Prof. dr. M.A. Boermeester, chirurg, Amsterdam UMC locatie AMC, Amsterdam, NVvH (voorzitter)
- Dr. M.G.J. de Boer, internist, infectioloog, Leids Universitair Medisch Centrum, Leiden, NIV
- S. van Dijk, MSc, arts-onderzoeker chirurgie, Amsterdam UMC locatie AMC, Amsterdam, NVvH
- Dr. W.A. Draaisma, chirurg, Jeroen Bosch Ziekenhuis, Den Bosch, NVvH
- Dr. R.J.F. Felt-Bersma, MDL-arts, VU Medisch Centrum, Amsterdam, NVMDL
- Dr. B.R. Klarenbeek, chirurg, Radboud UMC, Nijmegen, NVvH
- Dr. J.A. Otte, internist, ZorgSaam Zeeuws-Vlaanderen, Terneuzen, NIV
- Dr. J.B.C.M. Puylaert, radioloog, Medisch Centrum Haaglanden, Den Haag, NVvR
Met ondersteuning van:
- Dr. W.A. van Enst, senior-adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De KNMG-Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of ze in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Boermeester |
Gastrointestinaal chirurg, hoogleraar chirurgie van abdominale infecties, chirurgisch hoofd van darmfalenteam AMC |
Geen |
"Niet gerelateerd aan deze richtlijn. Niet-gerelateerde institutional grants van J&J/Ethicon, Acelity/KCI, Ipsen, Baxter, Bard, Mylan" |
Geen |
|
De Boer |
Internist, LUMC |
Geen |
Geen |
Geen |
|
Draaisma |
Chirurg, AMC |
lid werkgroep richtlijn Pleuravocht |
Geen |
Geen |
|
Felt-Bersma |
MDL arts, VUMC |
Consultant in de Proctoskliniek Bilthoven |
TEVA sponsort een studie tvgl 3 laxeermiddelen wat we op 1 dec 2016 gaan doen, de gelden komen ten bate van het onderzoek en de ANIOS aanstelling voor 2 mnd |
Geen |
|
Klarenbeek |
Gastrontestinaal en oncologisch chirurg, Radboud UMC |
Geen betaalde nevenfuncties |
ZonMw doelmatigheidssubsidie voor FORCE-trail (BFT na LAR voor rectumcarcinoom). MITEC-subsidies (intern Radboudumc) voor MRI en fluorescentie onderzoek bij oesofaguscarcinoom" |
Geen |
|
Otte |
Internist, ZorgSaam Zeeuws-Vlaanderen |
onbetaald |
Geen |
Geen |
|
Puylaert |
Radioloog, Medisch Centrum Haaglanden |
Geen |
Geen |
Geen |
|
Van Dijk |
Arts-onderzoeker chirurgie, AMC |
Betaald promotieonderzoek bij professor M.A. Boermeester over diverticulitis appendicitis en secundaire peritonitis. |
Geen |
Geen |
|
Van Enst |
Senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten, |
Lid van de GRADE working group/ Dutch GRADE Network |
Geen |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door een focusgroep te houden. Deze werd georganiseerd door de Patiëntenfederatie Nederland. Een verslag hiervan (zie aanverwante producten) is besproken in de werkgroep en de belangrijkste knelpunten zijn verwerkt in de richtlijn. De conceptrichtlijn wordt tevens voor commentaar voorgelegd aan de Patiëntenfederatie.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van de Federatie Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Stakeholders zijn uitgenodigd voor een knelpuntenbijeenkomst (Invitational conference). Vanwege het lage aantal aanmeldingen (twee, NHG en ZN) is de bijeenkomst geannuleerd. Gevraagd is schriftelijk op het raamwerk te reageren. Daarop kwamen geen reacties.
De werkgroep beoordeelde de aanbevelingen uit de eerdere richtlijn (NVvH, 2014) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen vanuit een patiëntenfocusgroep. De werkgroep stelde vervolgens een long list met knelpunten op en prioriteerde de knelpunten op basis van: (1) klinische relevantie, (2) de beschikbaarheid van (nieuwe) evidence van hoge kwaliteit, (3) en de te verwachten impact op de kwaliteit van zorg, patiëntveiligheid en (macro)kosten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter, arts-onderzoeker en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk (maar niet kritiek) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de kritieke uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De adviseur of werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie voor de oriënterende zoekactie en patiëntenperspectief zijn opgenomen onder aanverwante producten.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR – voor systematische reviews; Cochrane – voor gerandomiseerd gecontroleerd onderzoek; ACROBAT-NRS – voor observationeel onderzoek; QUADAS II – voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidence-tabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor Grading Recommendations Assessment, Development and Evaluation (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008), en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje Overwegingen.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje Overwegingen.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag.
Indicatorontwikkeling
Gelijktijdig met het ontwikkelen van de conceptrichtlijn heeft de werkgroep overwogen om interne kwaliteitsindicatoren te ontwikkelen om het toepassen van de richtlijn in de praktijk te volgen en te versterken. De werkgroep heeft besloten geen indicatoren te ontwikkelen bij de huidige richtlijn, omdat er of geen substantiële barrières konden worden geïdentificeerd die implementatie van de aanbeveling zouden kunnen bemoeilijken. Meer informatie over de methode van indicatorontwikkeling is op te vragen bij het Kennisinstituut van Medisch Specialisten (secretariaat@kennisinstituut.nl).
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de Kennislacunes beschreven (onder aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn wordt aan de betrokken (wetenschappelijke) verenigingen en de Patiëntenfederatie Nederland voorgelegd ter commentaar. De commentaren worden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren zal de conceptrichtlijn aangepast worden en definitief vastgesteld door de werkgroep. De definitieve richtlijn wordt aan de deelnemende (wetenschappelijke) verenigingen en de Patiëntenfederatie Nederland voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
- Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
- Medisch Specialistische Richtlijnen 2.0. Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html. 2012.
- Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html. 2013.
- Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
- Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van de Federatie Medisch Specialisten.
Zoekverantwoording
|
Databases:
Geraadpleegd tussen: 01-01-2010 en 11-11-2016 |
Zoekstrategie: (Diverticulitis(Mesh) OR “diverticulitis, colonic”(Mesh) OR diverticulitis(tiab) OR diverticular(tiab)) AND (Complicated[tiab] OR air(tiab) OR perforat*(tiab) OR microperforation(tiab) OR pneumoperitoneum(tiab) OR bubbl*(tiab) OR gas(tiab)) |
Resultaten: Pubmed 2584 hits Embase 3496 hits Cochrane 0 hits
Duplicaten: 1315 hits
Inclusie: 7 artikelen |
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Adamova 2012 |
No computed tomography used for confirmation of diagnosis |
|
Akarsu 2016 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Alecha 2014 |
No computed tomography used for confirmation of diagnosis |
|
Alvarez 2007 |
No computed tomography used for confirmation of diagnosis |
|
Alvarez 2009 |
No computed tomography used for confirmation of diagnosis |
|
Ambrosetti 2012 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Ambrosetti 2008 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Ambrosetti 2002 |
Case report or patient series smaller than 5 patients |
|
Ambrosetti 1997 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Ambrosetti 1998 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Ambrosetti 1993 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Ambrosetti 1992 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Bahadursingh 2003 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Bandera 2013 |
Case report or patient series smaller than 5 patients |
|
Ben Maamer 2012 |
No computed tomography used for confirmation of diagnosis |
|
Beuran 2009 |
No computed tomography used for confirmation of diagnosis |
|
Binda 2012 |
No computed tomography used for confirmation of diagnosis |
|
Binda 2012 |
No computed tomography used for confirmation of diagnosis |
|
Boudart 2008 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Bridoux 2014 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Buchs 2013 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Chapman 2005 |
No computed tomography used for confirmation of diagnosis |
|
Chautems 2002 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Edna 2014 |
No computed tomography used for confirmation of diagnosis |
|
Eglinton 2010 |
No computed tomography used for confirmation of diagnosis |
|
Etzioni 2010 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Fang 2003 |
No computed tomography used for confirmation of diagnosis |
|
Faria 2011 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Farmakis 1994 |
No computed tomography used for confirmation of diagnosis |
|
Flor 2015 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Freischlag 1986 |
No computed tomography used for confirmation of diagnosis |
|
Frileux 2010 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Fung 2015 |
Case report or patient series smaller than 5 patients |
|
Gala 2014 |
No computed tomography used for confirmation of diagnosis |
|
Garcia, 2016 |
No isolated pericolic extraluminal air |
|
Gielens 2012 |
Only patients that underwent emergency surgery |
|
Gouge 1983 |
No computed tomography used for confirmation of diagnosis |
|
Greif 1980 |
No computed tomography used for confirmation of diagnosis |
|
Griffith 2009 |
No computed tomography used for confirmation of diagnosis |
|
Guzzo 2004 |
No computed tomography used for confirmation of diagnosis |
|
Hachigian 1992 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Ha 2015 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Hall 2010 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Hall 2011 |
No outcomes of interest reported |
|
Hansen 1998 |
Only patients that underwent emergency surgery |
|
Holmer 2011 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Holmer 2011 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Hong 2015 |
No computed tomography used for confirmation of diagnosis |
|
Horesh 2016 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Ho 2015 |
No computed tomography used for confirmation of diagnosis |
|
Hsieh 2000 |
No computed tomography used for confirmation of diagnosis |
|
Humes 2009 |
No computed tomography used for confirmation of diagnosis |
|
Humes 2012 |
No computed tomography used for confirmation of diagnosis |
|
Hussain 2008 |
No computed tomography used for confirmation of diagnosis |
|
Illert 2001 |
No computed tomography used for confirmation of diagnosis |
|
Isacson 2014 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Issa 2009 |
Only patients that underwent emergency surgery |
|
Jacobsen 1996 |
No computed tomography used for confirmation of diagnosis |
|
Jafferji 2014 |
Only patients that underwent emergency surgery |
|
John 2007 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Jong 2010 |
No computed tomography used for confirmation of diagnosis |
|
Jurowich 2011 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Kaewlai 2007 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Kaiser 2005 |
No computed tomography used for confirmation of diagnosis |
|
Kim 2010 |
No computed tomography used for confirmation of diagnosis |
|
Kircher 2002 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Kotzampassakis 2010 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Krzewicki 2006 |
No computed tomography used for confirmation of diagnosis |
|
Linhardt 1982 |
No computed tomography used for confirmation of diagnosis |
|
Lohrmann 2005 |
Only patients that underwent emergency surgery |
|
Lorimer 2007 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Mali 2016 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Makela 2009 |
No computed tomography used for confirmation of diagnosis |
|
Manabe 2015 |
No computed tomography used for confirmation of diagnosis |
|
Moghadayeghaneh 2015 |
No computed tomography used for confirmation of diagnosis |
|
Morris 2008 |
No computed tomography used for confirmation of diagnosis |
|
Morris 2003 |
No computed tomography used for confirmation of diagnosis |
|
Morris 1986 |
No computed tomography used for confirmation of diagnosis |
|
Morton 1995 |
No computed tomography used for confirmation of diagnosis |
|
Mueller 2005 |
No computed tomography used for confirmation of diagnosis |
|
Murphy 2016 |
No computed tomography used for confirmation of diagnosis |
|
Nelson 2006 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Nemitz 2001 |
No computed tomography used for confirmation of diagnosis |
|
Occhionorelli 2016 |
No computed tomography used for confirmation of diagnosis |
|
Oertli 1993 |
No computed tomography used for confirmation of diagnosis |
|
O’Leary 2012 |
No computed tomography used for confirmation of diagnosis |
|
Pappalardo 2013 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Park 2010 |
No perforations reported |
|
Park 2013 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Paterson 2015 |
No computed tomography used for confirmation of diagnosis |
|
Piccolini 2003 |
No computed tomography used for confirmation of diagnosis |
|
Piccolini 2007 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Piekarek 2008 |
No computed tomography used for confirmation of diagnosis |
|
Pillari 1984 |
Case report or patient series smaller than 5 patients |
|
Pittet 2009 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Porta 1994 |
No computed tomography used for confirmation of diagnosis |
|
Proposito 1995 |
No computed tomography used for confirmation of diagnosis |
|
Rao 1998 |
No perforations reported |
|
Reynolds 2016 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Richelme 1984 |
No computed tomography used for confirmation of diagnosis |
|
Ritz 2007 |
No computed tomography used for confirmation of diagnosis |
|
Ritz 2013 |
Only patients that underwent emergency surgery |
|
Ritz 2011 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Ritz 2011 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Rodriguez 2015 |
No computed tomography used for confirmation of diagnosis |
|
Rodriguez 2015 |
No computed tomography used for confirmation of diagnosis |
|
Rose 2015 |
No computed tomography used for confirmation of diagnosis |
|
Salem 2006 |
No computed tomography used for confirmation of diagnosis |
|
Salem 2007 |
No computed tomography used for confirmation of diagnosis |
|
Sallinen 2015 |
No outcomes of interest reported |
|
Shah 2011 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Shaikh 2007 |
No computed tomography used for confirmation of diagnosis |
|
Shen 2002 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Somasekar 2002 |
No computed tomography used for confirmation of diagnosis |
|
Sorser 2009 |
No computed tomography used for confirmation of diagnosis |
|
Suarez Munoz 1988 |
No computed tomography used for confirmation of diagnosis |
|
Sugihara 1984 |
No computed tomography used for confirmation of diagnosis |
|
Tan 2013 |
No computed tomography used for confirmation of diagnosis |
|
Tan 2009 |
Only patients that underwent emergency surgery |
|
Toh 2016 |
Case report or patient series smaller than 5 patients |
|
Tuchmann 2000 |
Only patients that underwent emergency surgery |
|
Tudor 1994 |
No computed tomography used for confirmation of diagnosis |
|
Tursi 2008 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Tyau 1991 |
No computed tomography used for confirmation of diagnosis |
|
Unlu 2013 |
No computed tomography used for confirmation of diagnosis |
|
Unlu 2013 |
No computed tomography used for confirmation of diagnosis |
|
Wehrli 1987 |
No computed tomography used for confirmation of diagnosis |
|
Wehrli 1988 |
No computed tomography used for confirmation of diagnosis |
|
Werner 2003 |
No distinction made in types of extraluminal air in patients or outcome(s) |
|
Wong 1997 |
No computed tomography used for confirmation of diagnosis |
