Verzorging van de appendix stomp
Uitgangsvraag
Wat is de optimale verzorging van de stomp bij een laparoscopische appendectomie?
Aanbeveling
Gebruik ligatuur of clips bij een goed te mobiliseren appendix met een niet ontstoken basis van de appendix.
Overweeg stompverzorging met een stapler bij een patiënt met een ontstoken basis van de appendix of wanneer de appendix niet goed te mobiliseren is en retrograad (eerste de basis doornemen) verwijderd moet worden.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Voor zowel het gebruik van staplers, clips of ligatuur wordt in de huidige literatuur geen verschil gevonden voor het aantal complicaties, de ligduur of het aantal heropnames. De bewijskracht van de gevonden literatuur is zeer laag, waardoor de werkgroep op basis van de gevonden literatuur geen harde evidence-based uitspraken kan doen.
Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)
De werkgroep is van mening dat het gebruik van een clip, stapler of ligatuur voor de patiënt gelijkwaardige uitkomsten geeft. De patiënt merkt zelf niet welke techniek gebruikt is voor het sluiten van de appendix stomp en de pijnbeleving zal eerder afhankelijk zijn van het type operatie (open of laparoscopisch). Op basis de huidige literatuur kunnen op basis van de gevonden literatuur kunnen er geen harde evidence-based uitspraken worden gedaan over het effect op effect op morbiditeit, heropnames en ligduur.
Kosten (middelenbeslag)
Ondanks dat er geen kosteneffectiviteit analyses zijn gedaan in gerandomiseerde studies, is er wel een duidelijk verschil in materiaalkosten. Deze kosten verschillen per product en per ziekenhuis, maar men kan ervan uit gaan dat het gebruik van een staple device duurder is dan het gebruik van een ligatuur. Kosten voor een endoloop(ligatuur) liggen rond de €50, waar het gebruik van een staple device in de orde van grootte van €300 ligt (Mehdorn, 2017). Clips zijn mogelijk nog een goedkoper alternatief, in de orde van grootte van €20 (Wilson, 2018)
Het gebruik van een ligatuur of clip is een stuk goedkoper dan een stapler en zou peroperatief in de overwegingen meegenomen kunnen worden bij de keuze van het type stompverzorging.
Aanvaardbaarheid voor de overige relevante stakeholders
Bij een complexe appendicitis, waarbij de appendix goed te mobiliseren is en de basis van de stomp niet gangreneus ontstoken is, heeft het gebruik van clips of ligatuur gezien het kosten aspect de voorkeur hebben wanneer de operateur hiermee vertrouwd is.
Stompverzorging met een stapler is een goed alternatief bij de patiënt met een ontstoken basis van de appendix of wanneer de appendix niet goed te mobiliseren is en retrograad (eerste de basis doornemen) vrijgeprepareerd moet worden.
Onderbouwing
Er zijn meerdere manieren om de appendix stomp tijdens laparoscopische appendectomie te sluiten. De meest voorkomende technieken zijn: endostapler of ligatuur (meestal endoloop) of endoclips. Discussie blijft bestaan omtrent de meest veilige manier van sluiting. De keuze lijkt voornamelijk gebaseerd te zijn op de persoonlijke voorkeur van de chirurg of het ziekenhuis. Eerdere observationele studies uit eigen land laten geen verschil zien tussen het gebruik van endoloops of de endostapler (Van Rossem, 2017; Swank, 2014). We zullen in de literatuursearch op zoek gaan naar gerandomiseerde studies.
|
Zeer laag GRADE |
We zijn onzeker over het effect van het type stompverzorging van de appendix (stapler, clip of ligatuur) op de morbiditeit (gedefinieerd als complicaties, oppervlakkige infecties, diepe infecties of re-interventies) bij een appendectomie.
Bronnen: (Delibegovic, 2018; Mannu, 2017; Sadat-Safavi, 2016) |
|
Zeer laag GRADE |
We zijn onzeker over het effect van het type stompverzorging van de appendix (stapler, clip of ligatuur) op het aantal heropnames bij een appendectomie.
Bronnen: (Mannu, 2017) |
|
Zeer laag GRADE |
We zijn onzeker over het effect van het type stompverzorging van de appendix (stapler, clip of ligatuur) op de ligduur bij een appendectomie.
Bronnen: (Delibegovic, 2018; Mannu, 2017; Sadat-Safavi, 2016) |
Beschrijving studies
Het Cochrane review van Mannu (2017) is geïncludeerd en als uitgangspunt. Mannu (2017) includeerde 8 RCTs met 850 patiënten. Twee van deze studies includeerden alleen kinderen (n=199 kinderen) (Akbiyik, 2011; Ortega, 1995).
Vijf studies vergeleken titanium clips versus ligatuur, twee studies vergeleken een endoscopic stapler device versus ligatuur, en één studie vergeleek een endoscopic stapler device, titanium clips en ligatuur met elkaar (zie evidence tabel).
Het systematische review werd aangevuld met 2 RCTs gepubliceerd na de zoekdatum van Mannu (2017). Sadat-Safavi (2016) vergeleek endoclips met endoloop bij 76 patiënten en Delibegovic (2018) vergeleek een staplers met twee soorten clips en een endoop bij 120 patiënten.
Resultaten
1. Morbiditeit
Alle studies (n=10) rapporteerden morbiditeit. Dit werd opgesplitst in complicaties (zowel intraoperatieve als postoperatieve complicaties) en re-interventies.
Totaal aantal complicaties
Sluiting middels een device versus versus ligatuur
Alle studies (n=10) rapporteerden complicaties bij het gebruik van sluiting middels een device (met endoscopic stapler of clip(s)) versus ligatuur (met endoloop of intracorporale knoop) ligatuur bij totaal 1046 patiënten. Er werden meer complicaties gerapporteerd bij patiënten met een ligatuur (87 (17,9%)) dan patiënten bij met een stapler of clip (66 (11,8%)), waarvan Ortega, 1995 62 complicaties rapporteerde in de ligatuur groep. De gepoolde resultaten lieten zien dat patiënten in de ligatuur groep 8% minder kans hadden op complicaties (RR 1,08; 95% BI 0,43 tot 2,70) (figuur 1), waarbij het betrouwbaarheidsinterval de grens van klinische besluitvorming overschrijdt.
Figuur 1 Morbiditeit (complicaties) Sluiting middels een device versus ligatuur
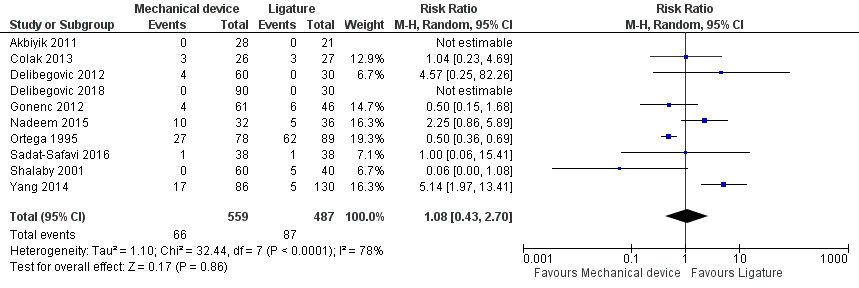
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Stapler versus ligatuur
Drie studies uit het review van Mannu (2017) rapporteerden complicaties bij het gebruik van staplers versus ligatuur, deze resultaten werden aangevuld met de resultaten uit de studie van Delibegovic (2018) (totaal 387 patiënten). Er werden meer complicaties gerapporteerd bij patiënten waarbij de stomp met een ligatuur behandeld is (67 (35,4%)) dan bij patiënten met een stapler (29 (14,6%)) (RR 0,51; 95% BI 0,09 tot 2,84) (figuur 2), waarbij het betrouwbaarheidsinterval de grens van klinische besluitvorming overschrijdt.
Figuur 2 Morbiditeit (complicaties) stapler versus ligatuur
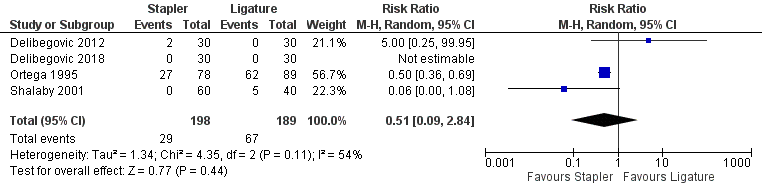
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Clips versus ligatuur
Zes studies uit het review van Mannu (2017) rapporteerden complicaties bij het gebruik van clips versus ligatuur, deze resultaten werden aangevuld met de resultaten uit de studie van Delibegovic (2018) en Sadat-Safavi (2016) (totaal 719 patiënten). Er werden meer complicaties gerapporteerd bij patiënten met clips (37 (10,2%)) dan bij patiënten met een ligatuur (20 (5,6%)) (RR 1,76; 95% BI 0,76 tot 4,06) (figuur 3), waarbij het betrouwbaarheidsinterval de grens van klinische besluitvorming overschrijdt.
Figuur 3 Morbiditeit (complicaties) clips versus ligatuur
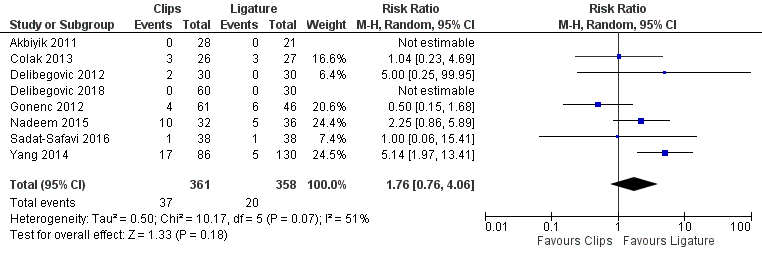
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Stapler versus clips
Eén studie in het review van Mannu (2017) (Delibegovic, 2012) vergeleek complicaties bij 30 patiënten met een stapler versus 30 patiënten met clips. In beide groepen werden 2 patiënten met complicaties gerapporteerd (RR 1,00; 95% BI 0,15 tot 6,64).
Bewijskracht van de literatuur
De bewijskracht is gebaseerd op gerandomiseerd onderzoek en start derhalve hoog (zie Werkwijze op het tabblad Verantwoording). De bewijskracht voor de uitkomstmaat morbiditeit (gedefinieerd als complicaties) is met drie niveaus verlaagd naar zeer laag vanwege hoog risico op bias (geen blindering, onduidelijke randomisatie, toewijzen van allocatie en selectief rapporteren), inconsistentie (substantiële heterogeniteit) en imprecisie (geringe aantal events met brede betrouwbaarheidsintervallen).
Oppervlakkige infecties
Sluiting middels een device versus ligatuur
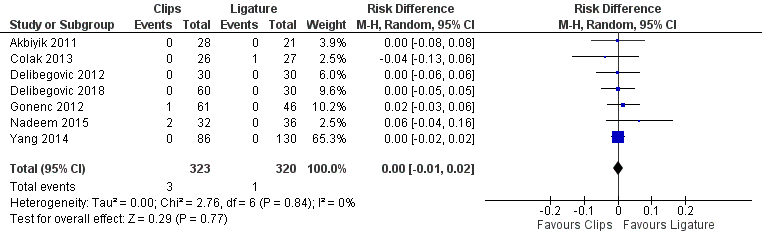
Alle studies (n=10) rapporteerden morbiditeit gedefinieerd als oppervlakkige infecties bij het gebruik van sluiting middels een device (met endoscopic stapler of clip(s)) versus ligatuur (met endoloop of intracorporale knoop) bij totaal 1046 patiënten. Er werden meer oppervlakkige infecties gerapporteerd bij patiënten met een ligatuur (12 (2,5%)) dan patiënten bij met een stapler of clip (6 (1,1%)) (risico verschil -0,01; 95% BI -0,02 tot 0,01) (figuur 4). Dit is geen klinisch relevant verschil.
Figuur 4 Morbiditeit (oppervlakkige infecties) Sluiting middels een device versus ligatuur
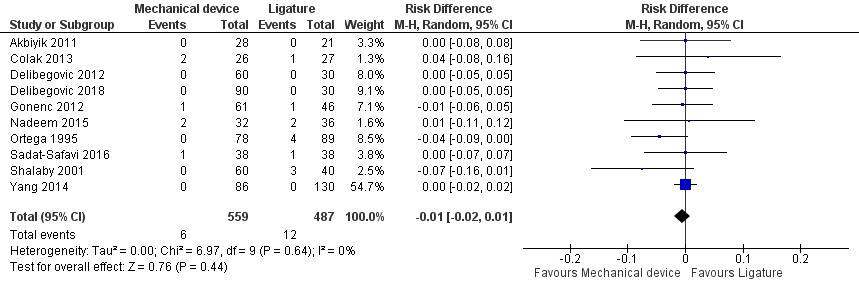
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Stapler versus ligatuur
Drie studies uit het review van Mannu (2017) rapporteerden oppervlakkige infecties bij het gebruik van staplers versus ligatuur, deze resultaten werden aangevuld met de resultaten uit de studie van Delibegovic (2018) (totaal 387 patiënten). Er werden meer complicaties gerapporteerd bij patiënten met een ligatuur (7 (3,7%)) dan bij patiënten met een stapler (0) (risico verschil -0,03; 95% BI -0,06 tot 0,01) (figuur 5), maar dit is geen klinisch relevant verschil.
Figuur 5 Morbiditeit (oppervlakkige infecties)) stapler versus ligatuur
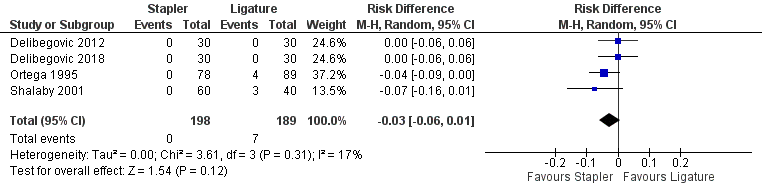
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Clips versus ligatuur
Zes studies uit het review van Mannu (2017) rapporteerden oppervlakkige infecties bij het gebruik van clips versus ligatuur, deze resultaten werden aangevuld met de resultaten uit de studie van Delibegovic (2018) en Sadat-Safavi (2016) (totaal 719 patiënten). Er werd één oppervlakkige infectie meer gerapporteerd bij patiënten met clips (6 (1,7%)) dan bij patiënten met een ligatuur (5 (1,5%)) (risico verschil 0,00; 95% BI -0,02 tot 0,02) (figuur 6).
Figuur 6 Morbiditeit (oppervlakkige infecties) clips versus ligatuur
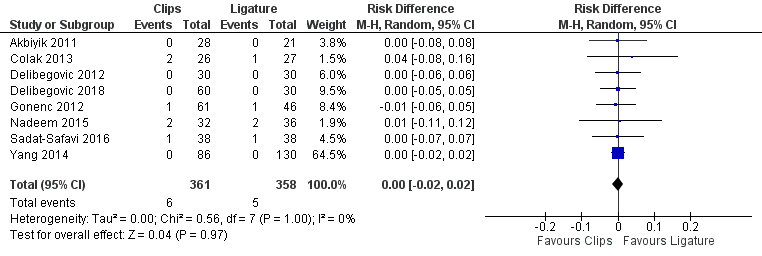
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Stapler versus clips
Eén studie in het review van Mannu (2017) (Delibegovic, 2012) vergeleek complicaties bij 30 patiënten met een stapler versus 30 patiënten met clips. In beide groepen werden geen patiënten met oppervlakkige infecties gerapporteerd (risico verschil 0,00; 95% BI -0,06 tot 0,06).
Bewijskracht van de literatuur
De bewijskracht is gebaseerd op gerandomiseerd onderzoek en start derhalve hoog (zie Werkwijze op het tabblad Verantwoording). De bewijskracht voor de uitkomstmaat morbiditeit (gedefinieerd als oppervlakkige infecties) is met drie niveaus verlaagd naar zeer laag één niveau vanwege hoog risico op bias (geen blindering, onduidelijke randomisatie, toewijzen van allocatie en selectief rapporteren) en twee niveaus voor imprecisie (zeer gering aantal events met brede betrouwbaarheidsintervallen).
Diepe infecties
Sluiting middels een device versus ligatuurligatuur
Negen studies uit het review van Mannu (2017) rapporteerden morbiditeit (gedefinieerd als diepe infecties) bij het gebruik sluiting middels een device (met endoscopic stapler of clip(s)) versus ligatuur (met endoloop of intracorporale knoop), deze resultaten werden aangevuld met de resultaten uit de studie van Delibegovic (2018) (totaal 970 patiënten). Er werden meer diepe infecties gerapporteerd bij patiënten met een ligatuur (11 (2,4%)) dan patiënten bij met een stapler of clip (5 (1%)) (risico verschil -0,01; 95% BI -0,01 tot 0,01) (figuur 7). Dit is geen klinisch relevant verschil.
Figuur 7 Morbiditeit (diepe infecties) Sluiting middels een device versus ligatuur
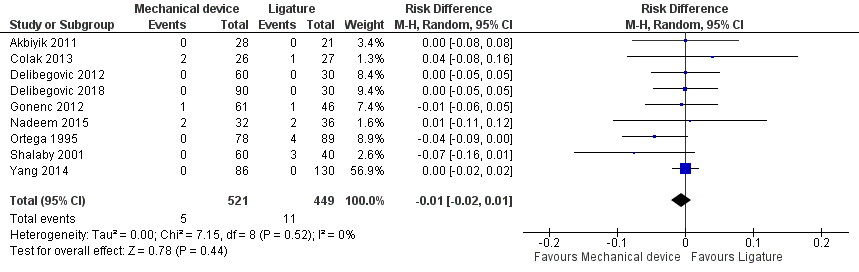
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Stapler versus ligatuur
Drie studies uit het review van Mannu (2017) rapporteerden diepe infecties bij het gebruik van staplers versus ligatuur, deze resultaten werden aangevuld met de resultaten uit de studie van Delibegovic (2018) (totaal 387 patiënten). Er werden meer diepe infecties gerapporteerd bij patiënten met een ligatuur (5 (2,6%)) dan bij patiënten met een stapler (2 (1%)) (risico verschil -0,01; 95% BI -0,04 tot 0,02) (figuur 8), maar dit is geen klinisch relevant verschil.
Figuur 8 Morbiditeit (diepe infecties) stapler versus ligatuur
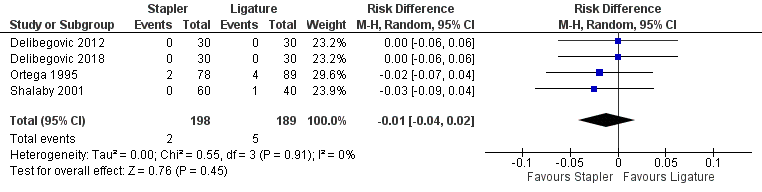
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Clips versus ligatuur
Zes studies uit het review van Mannu (2017) rapporteerden diepe infecties bij het gebruik van clips versus ligatuur, deze resultaten werden aangevuld met de resultaten uit de studie van Delibegovic (2018) bij totaal 643 patiënten. Er werden meer complicaties gerapporteerd bij patiënten met clips (3 (0,9%)) dan bij patiënten met een ligatuur (1 (0,3%)) (risico verschil 0,00; 95% BI -0,01 tot 0,02) (figuur 9), maar dit is geen klinisch relevant verschil.
Figuur 9 Morbiditeit (complicaties) clips versus ligatuur
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Stapler versus clips
Eén studie in het review van Mannu (2017) (Delibegovic, 2012) vergeleek diepe infecties bij 30 patiënten met een stapler versus 30 patiënten met clips. In beide groepen werden geen patiënten met oppervlakkige infecties gerapporteerd (risico verschil 0,00; 95% BI -0,06 tot 0,06).
Bewijskracht van de literatuur
De bewijskracht is gebaseerd op gerandomiseerd onderzoek en start derhalve hoog (zie Werkwijze op het tabblad Verantwoording). De bewijskracht voor de uitkomstmaat morbiditeit (gedefinieerd als diepe infecties) is met drie niveaus verlaagd naar zeer laag één niveau vanwege hoog risico op bias (geen blindering, onduidelijke randomisatie, toewijzen van allocatie en selectief rapporteren) en twee niveaus voor imprecisie (zeer gering aantal events met brede betrouwbaarheidsintervallen).
Re-interventie
Clips versus ligatuur
Twee studies binnen het review van Mannu (2017) die clips vergeleken met ligatuur rapporteerden hoeveel patiënten opnieuw geopereerd moesten worden. Deze resultaten werden aangevuld met de studie van Sadat-Safavi (2016) (totaal 251 patiënten). Twee (1,7%) patiënten met clips moesten opnieuw geopereerd worden versus geen patiënten in de ligatuur groep (RD 0,01; 95% BI -0,02 tot 0,05). Dit is geen klinisch relevant verschil (figuur 10).
Figuur 10 Morbiditeit (re-interventie) clips versus ligatuur
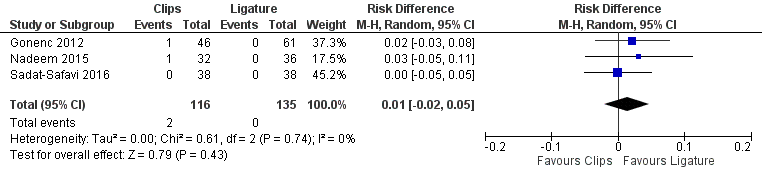
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Bewijskracht van de literatuur
De bewijskracht is gebaseerd op gerandomiseerd onderzoek en start derhalve hoog (zie Werkwijze op het tabblad Verantwoording). De bewijskracht voor de uitkomstmaat morbiditeit (gedefinieerd als re-interventie) is met drie niveaus verlaagd naar zeer laag één niveau vanwege hoog risico op bias (geen blindering, onduidelijke randomisatie, toewijzen van allocatie en selectief rapporteren) en twee niveaus voor imprecisie (zeer gering aantal events met brede betrouwbaarheidsintervallen).
2. Heropname
Clips versus ligatuur
Twee studies binnen het review van Mannu (2017) die clips met ligatuur vergeleken bij totaal 175 patiënten rapporteerden heropnames. Er werden 5 (6,4%)) patiënten met clips heropgenomen versus 4 (4,1%) patiënten met een ligatuur (RR 1,60; 95% BI 0,45 tot 5,75). Dit is geen klinisch relevant verschil (figuur 11).
Figuur 11 Heropname clips versus ligation
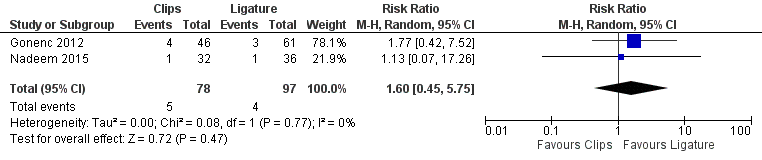
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Stapler versus ligatuur
Eén studie binnen het review van Mannu (2017) die stapler vergeleek met ligatuur rapporteerde het aantal heropnames bij 167 patiënten. Eén (1,3%) patiënt in de stapler groep versus 6 (6,7%) patiënten in de ligatuur groep werden heropgenomen (RR 0,19; 95% BI 0,02 tot 1,55). Dit is geen klinisch relevant verschil.
Bewijskracht van de literatuur
De bewijskracht is gebaseerd op gerandomiseerd onderzoek en start derhalve hoog (zie Werkwijze op het tabblad Verantwoording). De bewijskracht voor de uitkomstmaat heropname is met drie niveaus verlaagd naar zeer laag één niveau vanwege hoog risico op bias (geen blindering, onduidelijke randomisatie, toewijzen van allocatie en selectief rapporteren) en twee niveaus vanwege imprecisie (zeer geringe aantal events met brede betrouwbaarheidsintervallen).
3. Ligduur (dagen)
Sluiting middels een device versus ligatuur
Alle studies (n=10) rapporteerden de ligduur in dagen bij het gebruik van sluiting middels een device (met endoscopic stapler of clip(s)) versus ligatuur (met endoloop of intracorporale knoop) bij totaal 1046 patiënten. De gemiddelde ligduur in de sluiting middels een device was 0,04 dagen langer (95% BI -0,09 tot 0,16 (figuur 12)) dan in de ligatuur groep.
Figuur 12 Ligduur (dagen) sluiting middels een device versus ligatuur
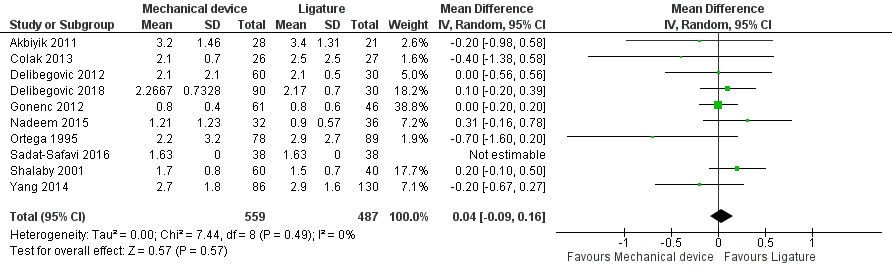
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Stapler versus ligatuur
Drie studies uit het review van Mannu (2017) rapporteerden de ligduur bij het gebruik van staplers versus ligatuur, deze resultaten werden aangevuld met de resultaten uit de studie van Delibegovic (2018) (totaal 387 patiënten). De gemiddelde ligduur in de stapler groep was 0,02 dagen langer (95% BI -0,23 tot 0,26 (figuur 13)) dan in de ligatuur groep.
Figuur 13 Ligduur (dagen) stapler versus ligatuur
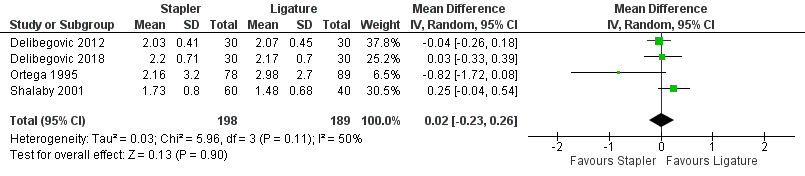
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Clips versus ligatuur
Zes studies uit het review van Mannu (2017) rapporteerden complicaties bij het gebruik van clips versus ligatuur, deze resultaten werden aangevuld met de resultaten uit de studie van Delibegovic (2018) en Sadat-Safavi (2016) (totaal 719 patiënten). Er werd was gemiddeld genomen geen verschil in de ligduur tussen patiënten met clips versus ligatuur (gemiddeld verschil 0,00 dagen; 95% BI -0,13 tot 0,12 (figuur 14)).
Figuur 14 Ligduur (dagen) clips versus ligatuur
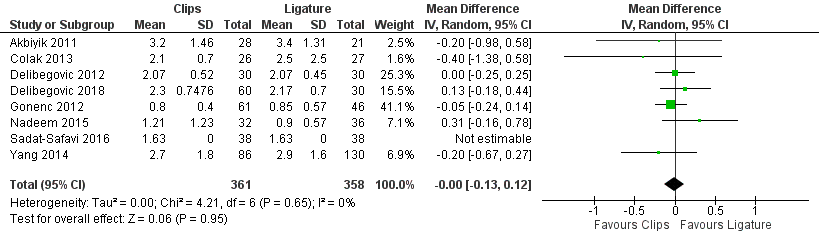
Z: p-waarde van gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Stapler versus clips
Eén studie binnen het review van Mannu (2017) die staplers vergeleek met clips rapporteerde de ligduur bij 60 patiënten. De patiënten met clips lagen gemiddeld 0,04 (95% BI -0,28 tot 0,20) dagen korter dan patiënten met ligatuur.
Bewijskracht van de literatuur
De bewijskracht is gebaseerd op gerandomiseerd onderzoek en start derhalve hoog (zie Werkwijze op het tabblad Verantwoording). De bewijskracht voor de uitkomstmaat ligduur is met drie niveaus verlaagd naar zeer laag vanwege hoog risico op bias (geen blindering, onduidelijke randomisatie, toewijzen van allocatie en selectief rapporteren), inconsistentie (substantiële heterogeniteit) en imprecisie (geringe aantal patiënten met brede betrouwbaarheidsintervallen).
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvragen:
- Wat zijn de (on)gunstige effecten van een appendix afgestapled na een laparoscopische appendectomie, in vergelijking met een ligatuur?
- Wat zijn de (on)gunstige effecten van een appendix met endoclips na een laparoscopische appendectomie, in vergelijking met een ligatuur?
- Wat zijn de (on)gunstige effecten van een appendix afgestapled na een laparoscopische appendectomie, in vergelijking met endoclips?
P (Patiënten): patiënten met een acute appendicitis;
I (Interventie): appendix stomp met endostapler, ligatuur of endoclips;
C (Comparison): appendix stomp met één van bovengenoemde methoden;
O (Outcomes): (30 dagen) morbiditeit (infectieuze complicaties, noodzaak tot re-interventie), heropname en ligduur.
Relevante uitkomstmaten
De werkgroep achtte 30 dagen morbiditeit, heropname en ligduur voor de besluitvorming cruciale uitkomstmaten; en kosten voor de besluitvorming belangrijke uitkomstmaten.
De werkgroep definieerde niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
De werkgroep definieerde voor geen van de uitkomstmaten klinische (patiënt) relevante verschillen. We hanteerden daarom, indien van toepassing, de onderstaande grenzen voor klinische relevantie en vergeleken de resultaten met deze grenzen: RR < 0,75 of > 1,25) (GRADE recommendation) of Standardized mean difference (SMD=0,2 (klein); SMD=0,5 (matig); SMD=0,8 (groot). De interpretatie van continue uitkomstmaten is sterk context gebonden en hiervoor werden a priori geen grenzen voor klinische relevante benoemd. Voor dichotome uitkomstmaten werd het absolute effect berekend (Number Needed to Treat; NNT of Number Needed to Harm; NNH).
Zoeken en selecteren (Methode)
In de databases Medline (via OVID) en Embase (via Embase.com) is op 9 mei 2018 met relevante zoektermen gezocht naar Engelstalige systematische reviews, gerandomiseerde gecontroleerde studies (RCTs), gecontroleerde klinische studie (CCTs) en vergelijkend observationeel onderzoek studies gepubliceerd vanaf 1946 gericht op de verzorging van de stomp na een appendectomie.
De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 354 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria: gerandomiseerde gecontroleerde trials die endostapler, ligatuur of endoclips vergelijken bij een laparoscopische appendectomie en ten minste één van de volgende uitkomstmaten hanteren: (30 dagen) morbiditeit (infectieuze complicaties, noodzaak tot re-interventie), heropname en ligduur.
Op basis van titel en abstract werden in eerste instantie 79 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 76 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording), en 3 studies definitief geselecteerd.
Eén systematische review en 2 RCT’s zijn opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidencetabellen. De beoordeling van de individuele studieopzet (risk-of-bias) is opgenomen in de risk-of-bias tabellen. De beoordeling van de individuele studieopzet (risk-of-bias) is opgenomen in de risk-of-bias tabellen.
Relevante gepoolde en eventueel gestandaardiseerde effectmaten werden berekend met Review Manager 5.3 (Cochrane Collaboration, Oxford, United Kingdom) indien zinvol. Wanneer samenvatten niet mogelijk bleek, werden de uitkomsten en resultaten van de statistische toetsing gerapporteerd zoals beschreven door de auteurs van de betreffende publicatie.
- Delibegovic S, Mehmedovic Z. The influence of the different forms of appendix base closure on patient outcome in laparoscopic appendectomy: a randomized trial. Surg Endosc. 2018 May;32(5):2295-2299. doi: 10.1007/s00464-017-5924-z. Epub 2017 Nov 2. PubMed PMID: 29098432.
- Mannu GS, Sudul MK, Bettencourt-Silva JH, Cumber E, Li F, Clark AB, Loke YK. Closure methods of the appendix stump for complications during laparoscopic appendectomy. Cochrane Database Syst Rev. 2017 Nov 13;11:CD006437. doi: 10.1002/14651858.CD006437.pub3. Review. PubMed PMID: 29190038.
- Mehdorn M, Schürmann O, Mehdorn HM, Gockel I. Intended cost reduction in laparoscopic appendectomy by introducing the endoloop: a single center experience. BMC Surg. 2017 Jul 11;17(1):80. doi: 10.1186/s12893-017-0277-z. PubMed PMID: 28693476; PubMed Central PMCID: PMC5504743.
- Sadat-Safavi SA, Nasiri S, Shojaiefard A, Jafari M, Abdehgah AG, Notash AY Jr, Soroush A. Comparison the effect of stump closure by endoclips versus endoloop on the duration of surgery and complications in patients under laparoscopic appendectomy: A randomized clinical trial. J Res Med Sci. 2016 Oct 18;21:87. doi: 10.4103/1735-1995.192503. eCollection 2016. PubMed PMID: 28163733; PubMed Central PMCID: PMC5244687.
- Wilson M, Maniam P, Ibrahim A, Makaram N, Knight SR, Patil P. Polymeric clips are a quicker and cheaper alternative to endoscopic ligatures for securing the appendiceal stump during laparoscopic appendicectomy. Ann R Coll Surg Engl. 2018 Jul;100(6):454-458. doi: 10.1308/rcsann.2018.0036. Epub 2018 Mar 15. PubMed PMID: 29543058; PubMed Central PMCID: PMC6111912.
Table of quality assessment for systematic reviews of RCTs and observational studies
|
Study
First author, year |
Appropriate and clearly focused question?
Yes/no/unclear |
Comprehensive and systematic literature search?
Yes/no/unclear |
Description of included and excluded studies?
Yes/no/unclear |
Description of relevant characteristics of included studies?
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?
Yes/no/unclear |
Potential risk of publication bias taken into account?
Yes/no/unclear |
Potential conflicts of interest reported?
Yes/no/unclear |
|
Mannu, 2017 |
Yes |
Yes |
Yes |
Yes |
Not applicable |
Yes |
Yes |
Yes |
SR: yes, RCTs: unclear |
Evidence table for systematic review of RCTs and observational studies (intervention studies)
NR: not reported
Risk-of-bias table for intervention studies (randomized controlled trials)
|
Study reference
(first author, publication year) |
Describe method of randomisation |
Bias due to inadequate concealment of allocation?
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?
(unlikely/likely/unclear) |
Bias due to loss to follow-up?
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?
(unlikely/likely/unclear) |
|
Delibegovic, 2018 |
The nurse designated for participation in this study allocated the patients randomly into four groups by selecting a sealed opaque envelope from a box and opening it in the operating room. A card inside the envelope contained the name of the treatment. All the envelopes were prepared in advance, in a ratio of 1:4, shuffled well, and placed in the box by the same nurse. |
Unlikely |
Likely |
Likely |
Likely |
Unlikely |
Unlikely |
Unlikely |
|
Sadat-Safavi, 2016 |
Not described (Patients were randomly assigned into two groups.) |
Unclear |
Unclear |
Likely |
Unclear |
Unlikely |
Unlikely |
Unlikely |
Evidence table for intervention studies
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C)
|
Follow-up |
Outcome measures and effect size |
Comments |
|
Delibegovic, 2018 |
Type of study: RCT
Setting: University Clinical Center Tuzla, a tertiary referral center in Tuzla, Bosnia and Herzegovina
Country: Bosnia and Herzegovina
Source of funding: not reported |
Inclusion criteria: Patients with acute appendicitis diagnosed at the surgical emergency department, laparoscopic appendectomy performed by a surgeon who had performed more than twenty laparoscopic appendectomies, patients older than 18 years.
Exclusion criteria: Patients with secondary appendicitis caused by other clinical entities, patients in whom conversion to open appendectomy was done, laparoscopic appendectomy performed by a surgeon who had performed fewer than 20 laparoscopic appendectomies, patients’ age < 18 years.
N total at baseline: Intervention 1: 30 Intervention 2: 30 Intervention 3: 30 Control: 30
Important prognostic factors2: age ± SD (year): I1: 30.93 ± 12.34 I2: 32.63 ± 13.97 I3: 29.53 ± 14.65 C: 31.17 ± 13.45
Groups comparable at baseline? Yes
|
Describe intervention (treatment/procedure/test):
Intervention 1: 45-mm stapling device Intervention 2: one non-absorbable XL Hem-o-lok clip90 Intervention 3: Titanium DS clip
|
Describe control (treatment/procedure/test):
Loop ligature |
Length of follow-up: 30 days
Loss-to-follow-up: 0
Incomplete outcome data: 0
|
Outcome measures and effect size (include 95%CI and p-value if available):
Outcome measure-1 Morbidity No morbidity was recorded in any group.
Outcome measure-2 Readmission NR
Outcome measure-3 Hospital stay (in days) I1: 2.2 ± 0.71 I2: 2.23 ± 0.78 I3: 2.37 ± 0.72 C: 2.17 ± 0.70 P=0.727 |
Author’s conclusion: All forms of closure of the appendix base are acceptable, but Hem-o-lok and DS clips have the best potential for further development, and will probably become the method of choice in securing the base of the appendix. |
|
Type of study: RCT
Setting: Emergency ward of Shariati Hospital
Country: Iran
Source of funding: Shariati Hospital and Tehran University of Medical Sciences |
Inclusion criteria: Patients diagnosed with acute appendicitis applying to the emergency ward of Shariati Hospital between March 1, 2013 and May 25, 2015.
Exclusion criteria: Patients who were in pain more than 4 days, finding a mass in the right lower quadrant area in the examination, phlegmon in images or peritonitis symptoms also the patients who underwent surgeries which turned into open laparoscopic due to adhesion and improper anatomic conditions were excluded from the study (did not occur in our study).
N total at baseline: Intervention: 38 Control: 38
Important prognostic factors2: Age ± SD: I: 22±3.6 C: 24.26±5.9
Sex, n M/F: I: 18/ 20 C: 19/ 22
Groups comparable at baseline? Yes
|
Describe intervention (treatment/procedure/test):
Endoclips
|
Describe control (treatment/procedure/test):
Endoloop |
Length of follow-up: NR
Loss-to-follow-up: 0
Incomplete outcome data: 0
|
Outcome measures and effect size (include 95%CI and p-value if available):
Outcome measure-1 Morbidity Defined as complications C: 1 (wound infection) I: 1 (clips falling off)
Defined as reoperation C: 0 I: 0
Outcome measure-2 Readmission NR
Outcome measure-3 Hospital stay (in days) C: 1.63 I: 1.63 P=1 |
Author’s conclusion: The effect of stump closure with endoloop versus endoclips is not different for complications, but the duration of surgery was shorter in endoclips method. Both methods could be used based on the opinion of the surgeon without expecting a statistically significant difference in the results |
Beoordelingsdatum en geldigheid
Publicatiedatum : 22-07-2019
Beoordeeld op geldigheid : 01-07-2019
|
Module |
Regiehouder(s) |
Jaar van autorisatie |
Eerstvolgende beoordeling actualiteit richtlijn |
Frequentie van beoordeling op actualiteit |
Wie houdt er toezicht op actualiteit |
Relevante factoren voor wijzigingen in aanbeveling |
|
Verzorging van de appendix stomp |
NVvH |
2019 |
2024 |
Eens in de vijf jaar |
NVvH |
- |
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep niet in stand gehouden. Uiterlijk in 2024 bepaalt het bestuur van de Nederlandse Vereniging voor Heelkunde of de modules van deze richtlijn nog actueel zijn. Op modulair niveau is een onderhoudsplan beschreven. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De Nederlandse Vereniging voor Heelkunde is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (https://www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijn.
Doel en doelgroep
Doel
Deze richtlijn is bedoeld om een evidence-based beleid voor de zorg voor patiënten met acute appendicitis in de tweede op te stellen.
Doelgroep
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen die betrokken zijn bij de zorg voor patiënten met acute appendicitis, zowel bij kinderen als bij volwassenen. Dit zijn onder andere chirurgen, kinderchirurgen, radiologen, kinderartsen, gynaecologen en SEH-artsen. Een secundaire doelgroep zijn zorgverleners uit de eerste lijn die betrokken zijn bij de zorg rondom patiënten met acute appendicitis, waaronder de huisarts, verpleegkundig specialist en physician assistants.
Samenstelling werkgroep
Voor de herziening van de richtlijn is in 2017 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met acute appendicitis te maken hebben.
Werkgroep:
- Dr. C.C. van Rossem, gastro-intestinaal chirurg, werkzaam in Maasstad Ziekenhuis, namens NVvH (voorzitter)
- Drs. A.L. van den Boom, fellow gastro-intestinale chirurgie, werkzaam in het UMCG, namens NVvH
- Drs. W.J. Bom, arts-onderzoeker chirurgie, werkzaam in Amsterdam UMC locatie AMC, namens NVvH
- Drs. M.E. Bos, arts in opleiding, werkzaam in Spoedeisende Geneeskunde regio VUmc, locatie Westfriesgasthuis, namens NVSHA
- Dr. A.A.W. van Geloven, gastro-intestinaal chirurg, werkzaam in Tergooi, namens NVvH
- Dr. R.R. Gorter, fellow kinderchirurgie, werkzaam in Amsterdam UMC, namens NVvH
- Dr. B.C. Jacod, gynaecoloog-perinatoloog, werkzaam in OLVG, namens NVOG
- Drs. M. Knaapen, arts-onderzoeker kinderchirurgie, werkzaam in Amsterdam UMC, namens NVvH
- R. Lammers, MSc, beleidsadviseur, werkzaam voor de Patiëntenfederatie Nederland
- Drs. A.H.J. van Meurs, algemeen kinderarts, werkzaam in HagaZiekenhuis, namens NVK
- Dr. J. Nederend, radioloog, werkzaam in Catharina Ziekenhuis Eindhoven, namens NVvR
- Dr. J.B.C.M. Puylaert, radioloog, werkzaam in Haaglanden Medisch Centrum, namens NVvR
Samenstelling klankbordgroep:
- Dr. A.K. van der Bij, arts-microbioloog, werkzaam in Diakonessenhuis, NVMM
- Dr. R. Bakx, kinderchirurg, werkzaam in Amsterdam UMC, namens NVvH
Met ondersteuning van:
- Dr. S.N. Hofstede, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- L. Boerboom MSc, literatuurspecialist, Kennisinstituut van de Federatie Medisch Specialisten
- D.M.J. Tennekes, directiesecretaresse, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoek financiering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Van Rossem |
Gastro-intestinaal chirurg, Maasstad Ziekenhuis |
Geen |
Geen |
Geen actie |
|
Van Geloven |
Gastro-intestinaal chirurg, Tergooi |
Geen |
Geen |
Geen actie |
|
Gorter |
Fellow Kinderchirurgie Amsterdam UMC |
Onderzoeker kinderchirurgie Vumc & AMC |
Projectleider APAC-studie Non-operatieve behandeling van appendicitis bij kinderen. ZonMw Dossiernummer: 843002708 |
Geen actie |
|
Van Meurs |
Algemeen kinderarts, Juliana Kinderziekenhuis (HagaZiekenhuis) |
Onderwijs aan studenten geneeskunde LUMC |
Geen |
Geen actie |
|
Jacod |
Gynaecoloog, Radboud UMC |
Secretaris werkgroep Samenwerking Obstetrie-Anesthesiologie, NVOG-NVA, onbetaald |
Geen |
Geen actie |
|
Puylaert |
Radioloog HMC |
Geen |
Geen |
Geen actie |
|
Nederend |
Radioloog Catharina Ziekenhuis Eindhoven |
Screeningsradioloog Bevolkingsonderzoek, betaald Secretaris Sectie Abdominale Radiologie, NVvR, onbetaald |
Onderzoek naar de waarden van MRI bij PIPAC-behandeling, deels gefinancieerd (unresticted grant) door Bracco Imaging Europe B.V. |
Geen actie |
|
Bos |
AIOS Spoedeisende Geneeskunde regio Vumc, locatie Westfriesgasthuis |
Algemeen lid congrescommissie NVSHA - onbetaald |
Geen |
Geen actie |
|
Van den Boom |
fellow gastro-intestinale chirurgie |
Geen |
Principal investigator van APPIC trial (short versus long antibiotic treatment after appendectomy for complex appendicitis), gefinancierd door ZonMw ontvangen (Goed Gebruik Geneesmiddelen) |
Geen actie |
|
Bom |
Arts-onderzoeker chirurgie, AMC |
Geen |
Ik word betaald vanuit de EPOCH studie, gefinancieerd door ZonMw. Dit is een RCT naar het voorkomen van wondinfecties. Dit is op geen enkele wijze gelieerd aan de richtlijn appendicitis. Derhalve heb ik geen belangen bij extern gefinancierd onderzoek. |
Geen actie |
|
Knaapen |
Arts-onderzoeker kinderchirurgie Amsterdam UMC |
Geen |
Coördinerend onderzoeker APAC-studie Non-operatieve behandeling van appendicitis bij kinderen. ZonMw Dossiernummer: 843002708 |
Geen actie |
|
Lammers |
Beleidsadviseur, Patiëntenfederatie |
Geen |
Geen |
Geen actie |
|
Hofstede |
Adviseur, Kennisinstituut van de Federatie Medisch Specialisten |
Geen |
Geen |
Geen actie |
|
Van Enst |
Senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten |
Lid van de GRADE working group/ Dutch GRADE Network |
Geen |
Geen actie |
|
Klankbordgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Van der Bij |
Arts-microbioloog Diakonessenhuis Utrecht/MSBD |
Voorzitter commissie kwaliteitsbeheersing NVMM, onbetaald |
Geen |
Geen actie |
|
Bakx |
Kinderchirurg, Kinderchirurgisch centrum Amsterdam |
Voorzitter richtlijnencommissie NVvH, onbetaald, bestuurslid Stichting spoedeisende hulp bij kinderen, onbetaald, APLS instructeur, onbetaald |
Principal investigator APAC-studie Non-operatieve behandeling van appendicitis bij kinderen. ZonMw Dossiernummer: 843002708 |
Geen actie |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door een afgevaardigde patiëntenvereniging in de werkgroep op te nemen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de Patiëntenfederatie.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten. De werkgroep heeft tevens interne kwaliteitsindicatoren ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken (zie Indicatorontwikkeling).
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van de Federatie Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. De werkgroep beoordeelde de aanbevelingen uit de eerdere richtlijn (NVvH, 2010) op noodzaak tot revisie. Tevens werden stakeholders uitgenodigd voor een knelpuntenbijeenkomst (Invitational conference). Vanwege het lage aantal aanmeldingen (drie, IGZ, NVA en de Patiëntenfederatie) is de bijeenkomst geannuleerd. Gevraagd is schriftelijk op het raamwerk te reageren. Er zijn schriftelijk knelpunten aangedragen door NVKC, NVSHA, NVvH, NVZ en V&VN. Een verslag hiervan is opgenomen onder aanverwante producten. De werkgroep stelde vervolgens een long list met knelpunten op en prioriteerde de knelpunten op basis van: (1) klinische relevantie, (2) de beschikbaarheid van (nieuwe) evidence van hoge kwaliteit, (3) en de te verwachten impact op de kwaliteit van zorg, patiëntveiligheid en (macro)kosten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar bestaande buitenlandse richtlijnen, systematische reviews (Medline (OVID)), en literatuur over patiëntvoorkeuren (patiëntenperspectief; Medline (OVID)). Vervolgens werd voor de afzonderlijke uitgangsvragen werd aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie voor de oriënterende zoekactie en patiëntenperspectief zijn opgenomen onder aanverwante producten.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk-of-bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk-of-Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR – voor systematische reviews; Cochrane – voor gerandomiseerd gecontroleerd onderzoek; ACROBAT-NRS – voor observationeel onderzoek; QUADAS II – voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk* |
|
|
Laag |
|
|
Zeer laag |
|
*in 2017 heeft het Dutch GRADE Network bepaalt dat de voorkeursformulering voor de op een na hoogste gradering ‘redelijk’ is in plaats van ‘matig’
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008), en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk-of-bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de cruciale uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag.
Gelijktijdig met het ontwikkelen van de conceptrichtlijn werden er interne kwaliteitsindicatoren ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken. Meer informatie over de methode van indicatorontwikkeling is op te vragen bij het Kennisinstituut van de Federatie Medisch Specialisten (secretariaat@kennisinstituut.nl).
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de Kennislacunes beschreven (onder aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. Link: https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Wessels M, Hielkema L, van der Weijden T. How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. J Med Libr Assoc. 2016 Oct;104(4):320-324. PubMed PMID: 27822157; PubMed Central PMCID: PMC5079497.
Zoekverantwoording
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID)
1946 – juni 2018 |
1 exp APPENDICITIS/ or appendi*.ti,ab. or exp APPENDECTOMY/ or appendectom*.ti,ab. or exp APPENDIX/ (45898) 2 (stump* or endoligat* endoloop* or loop ligat* or endostapler* or stapler* or endoclip* or clip* or suture*).ti,ab. (105337) 3 1 and 2 (880) 4 limit 3 to english language (655) 5 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (358230) 6 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1765066) 7 Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or (cohort adj (study or studies)).tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ (Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies) (2990105) 8 exp Pregnancy/ or exp Pregnant Women/ or pregnan*.ti,ab. or gravidit*.ti,ab. or gestation*.ti,ab. or placentat*.ti,ab. or prepregnan*.ti,ab. or conception*.ti,ab. or preconception*.ti,ab. (1005612) 9 neonates/ or premature infants/ or preterm*.ti,ab. or prematur*.ti,ab. or postmatur*.ti,ab. or perinat*.ti,ab. or postnat*.ti,ab. or neonat*.ti,ab. or newborn*.ti,ab. or new-born.ti,ab. or infant, newborn/ or infant/ or infant behavior/ or infan*.ti,ab. or toddler*.ti,ab. or baby*.ti,ab. or babies.ti,ab. or child behavior/ or child development/ or child psychiatry/ or orthopsychiatry/ or child psychology/ or child behavior disorders/ or pediatrics/ or paediat*.ti,ab. or pediat*.ti,ab. or child/ or child*.ti,ab. or kid.ti,ab. or kids.ti,ab. or puberty/ or puberty.ti,ab. or pubescen*.ti,ab. or prepubescen*.ti,ab. or prepuberty*.ti,ab. or teen*.ti,ab. or young*.ti,ab. or youth*.ti,ab. or minors*.ti,ab. or under ag*.ti,ab. or underag*.ti,ab. or juvenile*.ti,ab. or preadolesc*.ti,ab. or adolescent/ or adolescent behavior/ or adolescent development/ or adolescent psychiatry/ or adolescent psychology/ or adolesc*.ti,ab. or young adult/ or girl*.ti,ab. or boy*.ti,ab. or schools, nursery/ or nursery.ti,ab. or child day care centers/ or child care/ or early childhood education.ti,ab. or kindergarten*.ti,ab. or child, preschool/ or preschool*.ti,ab. or elementary education.ti,ab. or primary education.ti,ab. or K-12*.ti,ab. or K12.ti,ab. or secondary education.ti,ab. or junior high*.ti,ab. or highschool*.ti,ab. or college*.ti,ab. or tertiary education.ti,ab. or postsecondary education.ti,ab. or undergrad*.ti,ab. or education, graduate/ or universities/ or universit*.ti,ab. or students/ or student*.ti,ab. or schools/ or school*.ti,ab. or classroom*.ti,ab. (5137910) 10 4 and 8 (13) 11 5 and 10 (1) 12 6 and 10 (0) 13 7 and 10 (3) 14 10 not 11 not 13 (9) 15 4 and 9 (269) 16 5 and 15 (5) 17 6 and 15 (46) 18 7 and 15 (135) 19 4 and 5 (29) 20 19 not 11 not 16 (23) 2 4 and 6 (92) 22 21 not 17 (46) 23 4 and 7 (232) 24 23 not 13 not 18 (97) 25 11 or 12 or 13 or 14 or 16 or 17 or 18 or 20 or 22 or 24 (283) 26 20 or 22 or 24 (121) = 121 |
168 |
|
Embase (Elsevier) |
((('appendicitis'/exp OR appendi*:ti,ab OR 'appendectomy'/exp OR appendectom*:ti,ab OR 'appendix'/exp) AND ('stump appendicitis'/exp OR 'loop ligator'/exp OR 'endostapler'/exp OR 'endoclip'/exp OR 'gastrointestinal clip applier'/exp OR 'suture'/exp OR stump*:ti,ab OR endoloop*:ti,ab OR endoligat*:ti,ab OR 'loop ligat*':ti,ab OR endostapler*:ti,ab OR stapler:ti,ab OR endoclip*:ti,ab OR clip*:ti,ab OR suture*:ti,ab) AND (english)/lim NOT 'conference abstract':it)
Gebruikte filters: Systematic Reviews: (('meta analysis'/de OR cochrane:ab OR embase:ab OR psycinfo:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp)) = 19 Randomized Controlled Trials: (('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it))) = 72 Observationele studies: ('clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR ('prospective study'/de NOT 'randomized controlled trial'/de) OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (case:ab,ti AND ((control NEAR/1 (study OR studies)):ab,ti)) OR (follow:ab,ti AND ((up NEAR/1 (study OR studies)):ab,ti)) OR ((observational NEAR/1 (study OR studies)):ab,ti) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti)) = 58
= 114
|
Exclusietabel
|
Auteur en jaartal |
Redenen van exclusie |
|
Escolino 2018 |
Retrospectief dossieronderzoek |
|
Pogorelic 2017 |
Geen RCT |
|
Giesen 2017 |
Retrospectief dossieronderzoek |
|
Yavuz 2016 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Reinke 2016 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Rakic 2014 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Rickert 2012 |
Geen vergelijkend onderzoek |
|
Gonenc 2012 |
Geïncludeerd in Cochrane review |
|
Delibegovic 2012 |
Geïncludeerd in Cochrane review |
|
Sahm 2011 |
Geen RCT |
|
Miyano 2011 |
Geen RCT |
|
Miyano 2011 |
Geen RCT |
|
Partecke 2010 |
Geen RCT |
|
Koluh 2010 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Shalaby 2001 |
Geïncludeerd in Cochrane review |
|
Osime 1988 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Watters 1984 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Hooper 1977 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Mehdorn 2017 |
Geen RCT |
|
Lucchi 2017 |
Geen RCT |
|
Abbott 2017 |
Geen RCT |
|
Soll 2016 |
Geen RCT |
|
Naiditch 2015 |
Geen RCT |
|
Safavi 2012 |
Geen RCT |
|
Jenwithseesuk 2012 |
Geen RCT |
|
Akkoyun 2012 |
Geen RCT |
|
Akbiyik 2011 |
Geïncludeerd in Cochrane review |
|
Delibegovic 2009 |
Geen RCT |
|
Aydogan 2009 |
Geen RCT |
|
Wehrman 2007 |
Geen RCT |
|
Klaiber 1994 |
Geen RCT |
|
Sculco 1973 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Antoniou 2017 |
Cochrane review als uitgangspunt genomen |
|
Shaikh 2015 |
Cochrane review als uitgangspunt genomen |
|
Qian 2015 |
Cochrane review als uitgangspunt genomen |
|
D’Souza 2011 |
Cochrane review als uitgangspunt genomen |
|
Sajid 2009 |
Cochrane review als uitgangspunt genomen |
|
Sauerland 2007 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Humes 2007 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Kazemier 2006 |
Cochrane review als uitgangspunt genomen |
|
Wilson 2018 |
Geen RCT |
|
Van Rossum 2017 |
Geen RCT |
|
Al-Temimi 2017 |
Geen RCT |
|
Nadeem 2016 |
Geïncludeerd in Cochrane review |
|
Lv 2016 |
Voldoet niet aan PICO, 2 verschillende clips worden vergeleken |
|
Rickert 2015 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Blake 2015 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Caglia 2014 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Delibegovi 2013 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Colak 2013 |
Geïncludeerd in Cochrane review |
|
Gomes 2012 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Ates 2012 |
Quasi-gerandomiseerd onderzoek |
|
Delibegovic 2011 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Yildez 2009 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Beldi 2004 |
Quasi-gerandomiseerd onderzoek |
|
Lavonius 1993 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Dass 1989 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Engstrom 1985 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Rosenberg 1974 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Palakhumus 2017 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Elía-Guedea 2017 |
Geen RCT |
|
Yildiz 2016 |
Geen RCT |
|
Strzalka 2016 |
Geen RCT |
|
Delibegovic 2016 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Wright 2015 |
Geen RCT |
|
Matyja 2015 |
Geen RCT |
|
Swank 2014 |
Geen RCT |
|
Bozkurt 2014 |
Geen RCT |
|
Kiudelis 2013 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Hue 2013 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Gomes 2013 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Galatioto 2013 |
Geen RCT |
|
Hanssen 2007 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Alcovedo 2007 |
Gepubliceerd voor searchdatum Cochrane met zelfde PICO |
|
Beldi 2006 |
Geen RCT |
|
Street 1988 |
Geen RCT |
