Techniek van opereren
Uitgangsvraag
Welke operatietechniek heeft de voorkeur bij een achillespeesruptuur?
Aanbeveling
Communiceer met de patiënt de beschikbare opties, de voor- en nadelen van de gebruikte techniek en het bijpassende complicatieprofiel.
Gebruik de operatieve techniek (minimaal invasief of open techniek) waarin bekwaamheid en kennis is opgebouwd.
Indien een minimaal invasieve techniek wordt gekozen, kies een benadering waar men zich in bekwaamd heeft en welke passend is.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Er is literatuuronderzoek verricht om te onderzoeken welke operatieve techniek de voorkeur heeft bij een chirurgische behandeling van een primaire, acute achillespeesruptuur. De functionele uitkomst, zoals dagelijks functioneren werd gedefinieerd als cruciale uitkomst. Re-rupturen, complicaties (zoals diepe veneuze trombose en infecties), range of motion, terugkeer naar sport, kwaliteit van leven, terugkeer naar werk en re-operatie werden als belangrijke uitkomsten beschouwd.
PICO 1: Minimaal invasieve chirurgische techniek versus een open chirurgische techniek
Voor de cruciale uitkomst dagelijks functioneren werd, met redelijk robuuste bewijskracht, geen klinisch relevant verschil gevonden. Dit resultaat was vergelijkbaar tussen minimaal invasieve chirurgische techniek en een open chirurgische techniek voor de belangrijke uitkomst re-rupturen (lage bewijskracht). Daardoor lijkt er weinig tot geen verschil in het niveau van dagelijks functioneren en het aantal re-rupturen te zijn als er wordt behandeld middels een minimaal invasieve chirurgische techniek in vergelijking met een open chirurgische techniek. De resultaten van de ATRS-score in de studie van Myhrvold (2022) konden vanwege het ontbreken van statistische informatie niet worden gepoold met de studies van Makaluvicius (2020), Manent (2019) en Rozis (2019). Echter, Myhrvold (2022) includeerde individueel al meer patiënten dan deze drie studies gezamenlijk en liet, net als het gepoolde resultaat, geen verschil zien in dagelijks functioneren na behandeling met een minimaal invasieve techniek en een open techniek. Hierdoor kan met een redelijke bewijskracht worden gesteld dat er geen verschil is in het effect van een minimaal invasieve techniek in vergelijking met een open techniek op dagelijks functioneren na een jaar follow-up.
Het valt op dat in de studie van Manent (2019) de resultaten een flink lagere ATRS-score laten zien dan de andere drie studies m.b.t. het herstel van de functie van de achillespees. Het valt echter niet te achterhalen wat er aan deze heterogeniteit tussen de studies ten grondslag ligt. In de studie van Myhrvold (2022) lijken de resultaten te impliceren dat patiënten bij de follow-up meting achteruit zijn gegaan ten opzichte van baseline. Echter, de baseline scores in Myhrvold (2022) werden retrospectief bepaald door patiënten te vragen hoe ze hun dagelijks functioneren zouden beoordelen voorafgaand aan de achillespeesruptuur. Dit is een mogelijke verklaring waarom de ATRS-scores na één jaar follow-up lager uitvielen in vergelijking met baseline.
Uit de resultaten voor de belangrijke uitkomst complicaties blijkt dat een minimaal invasieve techniek mogelijk tot minder oppervlakkige infecties (NNH 28.6) leidt maar tot meer letsel aan de nervus suralis (NNH 27.8). Deze complicatie komt zeer waarschijnlijk vaker voor na de minimaal invasieve techniek door het subcutaan tunnelen van de hechtdraad. De bewijskracht voor deze complicaties was laag. De ervaring van de werkgroep is echter dat deze complicatie in de praktijk zelden door patiënten spontaan gerapporteerd wordt. Dat deze complicatie in gerandomiseerde studies frequent naar voren komt zou verklaard kunnen worden, doordat er proactief naar gevraagd wordt (in tegenstelling tot observationele database studies). Het is daarom onduidelijk welk effect deze complicatie op het dagelijks functioneren heeft. Behandeling middels een minimaal invasieve techniek resulteert daarentegen mogelijk niet in een afname van het aantal diepe infecties ten opzichte van een open techniek (NNH 166.7). De literatuur is hier erg onzeker over (GRADE zeer laag). Ook voor de uitkomstmaat range of motion van de enkel is de literatuur erg onzeker (GRADE zeer laag). Er kon geen uitspraak worden gedaan voor de uitkomsten kwaliteit van leven, terugkeer naar werk en re-operatie, omdat in geen van de geïncludeerde studies één van deze uitkomsten werd gerapporteerd.
Hoewel er, aangaande re-operatie, geen uitspraak gedaan kan worden op basis van de huidige geïncludeerde literatuur kan uit het aantal re-rupturen en nagenoeg gelijke aantal diepe infecties wel het een en ander worden afgeleid. Logischerwijs is het namelijk zo dat na zowel open als minimaal invasieve techniek de kans op een re-ruptuur of diepe infectie gelijk is. Dit zijn de twee voornaamste redenen om tot eventuele re-operatie over te gaan. Het hogere aantal oppervlakkige infecties lijkt hiervoor minder relevant aangezien deze doorgaans van beperkte klinische consequenties zijn (expert opinion werkgroep).
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Het primaire doel van een operatie is herstel van de functie van de achillespees om zo de dagelijkse, sport- en werkactiviteiten te kunnen hervatten op het niveau van voor het letsel. Dit geldt voor zowel de open als voor de minimaal invasieve techniek. De beschikbare wetenschappelijke literatuur laat geen verschil zien in de uitkomstmaten dagelijks functioneren en re-rupturen. De voor- en nadelen van beide technieken voor de patiënt zijn dus uiteindelijk de complicatierisico’s van beide technieken. Bovendien zijn de verschillen tussen de beide methoden op het gebied van complicaties zeer klein en afhankelijk van de geraadpleegde literatuur. Zo laten de geïncludeerde meta-analyses zien dat er een suggestie is van minder oppervlakkige wondinfecties na minimaal invasieve techniek ten opzichte van open techniek, maar meer nervus suralis letsel. Voor de diepe wondinfecties lijkt geen verschil te zijn. Echter, de studie van Myhrvold (2022) laat enkel een verschil in nervus suralis letsel zien (5.2% na minimaal invasief versus 2.8% na open techniek). Deze studie laat geen verschil in oppervlakkige of diepe infecties zien. Patiënten moeten dus geïnformeerd worden dat; 1) de functionele uitkomst en re-ruptuur kans gelijk zijn, 2) na minimaal invasieve techniek mogelijk meer nervus suralis letsel ontstaat maar dat de klinische consequentie of beperking op functioneren, klachten of kwaliteit van leven onbekend is en 3) de kans op een oppervlakkige of diepe infectie gelijk lijkt. Wat voor de patiënt als mogelijke afweging resteert is dat de locatie van de incisie, lengte van de incisie en gebruik van percutane techniek met eventueel boortunnel in de calcanus anders is bij een minimaal invasieve versus open techniek. Het wordt uit geen van de geïncludeerde studies duidelijk wat de voorkeur of tevredenheid van patiënten is met de gekozen behandelopties. Het is dus niet duidelijk wat de consequentie(s) van deze complicaties zijn voor de patiënt en in hoeverre zij de tevredenheid met de gekozen behandeling beïnvloeden.
Er is geen Nederlands onderzoek naar de tevredenheid van patiënten na minimaal invasieve of open techniek van het hechten van een acute achillespeesruptuur. Een meta-analyse (McMahon, 2011) rapporteert de gepoolde resultaten van drie studies, welke onafhankelijk geen significant verschil laten zien in mate van tevredenheid. De gepoolde resultaten laten een odds-ratio van 2,99 (95% BI 1,03 tot 8,69) zien voor het rapporteren van een ‘goede’ of ‘uitstekende’ uitkomst bij patiënten (67/73 patiënten = 92% geeft aan tevreden te zijn na minimaal invasieve techniek en 52/68 patiënten 77% na open techniek). Het is dubieus of hier zwaarwegende conclusies aan verbonden kunnen worden aangezien het slechts 141 patiënten betreft welke niet in de Nederlandse setting zijn onderzocht.
De werkgroep is, gelet op bovenstaande, van mening dat de methode waarin de chirurg bekwaam is en waarmee hij/zij zich vertrouwd voelt de techniek is waarmee de patiënt het beste geholpen wordt.
Er is geen wetenschappelijk bewijs dat bepaalde subgroepen meer gebaat zijn bij minimaal invasieve dan wel een open techniek.
Kosten (middelenbeslag)
Er is geen kosteneffectiviteitsanalyse uit de Nederlandse setting aangaande minimaal invasief versus een open techniek ten behoeve van een acute achillespeesruptuur. Echter, de werkgroep geeft aan dat logischerwijs beredeneerd kan worden dat de kosten waarschijnlijk op zowel individueel als maatschappelijk niveau gelijk zullen zijn. Dit omdat de directe operatiekosten voor beide technieken waarschijnlijk gelijk zijn, het gebruikte materiaal gelijk is en de duur van de operatie en de nabehandeling niet anders zal zijn. De literatuur laat zien dat functionele uitkomsten, het risico op een re-ruptuur, infectierisico en terugkeer naar werk waarschijnlijk niet verschilt tussen de minimaal invasieve techniek en een open techniek.
Aanvaardbaarheid, haalbaarheid en implementatie
De werkgroep voorziet geen bezwaren in haalbaarheid en aanvaardbaarheid bij de arts ten aanzien van de aanbevelingen in deze richtlijn. Deze wijken waarschijnlijk niet of nauwelijks af van de huidige manier van werken en zetten niet aan tot nieuwe technieken om een acute achillespeesruptuur te behandelen. De richtlijn laat daarom voldoende ruimte voor de behandelend arts om de best beheerste techniek (open of minimaal invasieve techniek) toe te passen.
De aanbevelingen in deze richtlijn laten voldoende ruimte om samen met de patiënt tot een passend behandelplan te komen. De verwachting is dat de benodigde middelen reeds aanwezig zijn en de behandeling uitgevoerd kan worden.
Er is geen kwantitatief of kwalitatief onderzoek gedaan naar de aanvaardbaarheid, haalbaarheid of implementatie van een minimaal invasieve of een open techniek in Nederland.
Aangezien een operatieve behandeling van een acute achillespeesruptuur in veel Nederlandse ziekenhuizen wordt aangeboden verwacht de werkgroep geen problemen met gezondheidsgelijkheid in het kader van toegankelijkheid van zorg. Er lijken ook geen belemmerende factoren om deze zorg te leveren in de ziekenhuizen. In alle gevallen gaat het om verzekerde zorg (minimaal invasieve of open techniek). Het grootste deel van deze zorg wordt geleverd door SEH-artsen, traumachirurgen of orthopedisch chirurgen en deze zijn in de meeste ziekenhuizen in een of andere verhouding aanwezig.
Gelet op de lage complexiteit van de interventies wordt aangenomen dat in alle ziekenhuizen in Nederland wordt voldaan aan de voorwaarden om deze zorg goed uit te voeren.
Er zijn geen subgroepen waarvoor aanvullende overwegingen nodig zijn. De richtlijn geeft voldoende handvatten voor implementatie.
PICO 1: Minimaal invasieve chirurgische techniek versus een andere minimaal invasieve chirurgische techniek
Uit het literatuuronderzoek kwamen geen studies naar voren die rapporteerden over de effectiviteit tussen verschillende minimaal invasieve chirurgische technieken. Er kon zodoende geen literatuuranalyse worden uitgevoerd en er konden geen GRADE-conclusies worden opgesteld voor deze vergelijking.
Rationale van de eerste aanbeveling: weging van argumenten voor en tegen de interventie
Voor de cruciale uitkomstmaat dagelijks functioneren is geen verschil gevonden tussen een minimaal invasieve of open techniek ten behoeve van het operatief herstel van een acute achillespeesruptuur.
Hetzelfde geldt voor de belangrijke uitkomstmaat re-ruptuur. Er is kwalitatief hoogwaardige literatuur beschikbaar die een re-ruptuur percentage van 0,6 tot 2,5% laat zien voor zowel open als minimaal invasieve techniek. Zoals in module 2 reeds besproken, is dit significant lager dan na conservatieve behandeling. Er is dus geen verschil in re-ruptuur risico na minimaal invasieve of open techniek.
Uit de beschikbare literatuur is het niet geheel duidelijk of er een verschil is in complicaties. Zo lijkt er na een open techniek vaker een oppervlakkige infectie op te treden maar niet voor de diepe infecties. De bewijskracht hiervoor is respectievelijk laag en zeer laag. Voor nervus suralisletsel geldt het tegenovergestelde, ten faveure van de open techniek, gebaseerd op een lage bewijskracht. Voor de overige uitkomsten als optreden van diep veneuze trombose, terugkeer naar sport of werk zijn geen verschillen gevonden. Deze bevindingen komen overeen met de heersende tendens in Nederland, waar de minimaal invasieve techniek het meeste toegepast lijkt te worden maar waar ook nog een open techniek gebruikt wordt. De beschikbare literatuur en de opinie van de werkgroep geven dan ook geen aanleiding om de ene techniek over de ander te verkiezen. De werkgroep adviseert de benadering te gebruiken die door de chirurg adequaat beheerst wordt, waar men zich in bekwaamd heeft en welke het beste past bij de pathologie, eventuele co-morbiditeit en wensen van de patiënt.
Op de vraag welke minimaal invasieve techniek de voorkeur heeft is geen wetenschappelijk onderbouwd antwoord te geven vanwege het ontbreken van gedegen klinische studies. De werkgroep is van mening dat hiervoor ook geen advies op basis van expert opinion gegeven kan worden.
Onderbouwing
De operatieve behandeling van een acute achillespeesruptuur geschiedt in Nederland op vele verschillende manieren. Zo is er onder andere verschil in de benadering, hechttechniek en hechtmateriaal. Generaliserend wordt vaak gesproken over minimaal invasief of een open techniek. Met minimaal invasief wordt doorgaans bedoeld dat de incisie net proximaal van het letsel zit en de draad subcutaan getunneld wordt om distaal van het letsel verankerd te worden. Hierbij worden de peeseindes naar elkaar gebracht zonder dat deze primair gehecht zijn. Bij een open techniek wordt doorgaans bedoeld dat de huid wordt geopend ter plaatse van de laesie en de achillespees primair gehecht wordt. Echter, er zijn hierover geen strikte definities. Tevens zijn er veel verschillende technieken in gebruik bij zowel de open als minimaal invasieve procedure.
Beide technieken verschillen, zowel technisch als ook met betrekking tot de potentiële complicaties. Het is echter niet duidelijk of er verschillen in uitkomst zijn, daarom wordt dit in deze module onderzocht. De vraagstelling van deze module is dan ook welke techniek de voorkeur heeft; open versus minimaal invasief. Gezien het frequente gebruik van de minimaal invasieve techniek in Nederland is een andere vraagstelling welke minimaal invasieve techniek de voorkeur heeft?
PICO 1: minimally invasive surgical techniques versus open repair techniques
1. Daily functioning
Achilles Tendon Rupture Score (ATRS)
|
Moderate GRADE |
Treatment with minimally invasive surgery techniques likely results in little to no difference in daily functioning when compared with open repair in patients with primary, acute Achilles tendon ruptures.
Sources: Attia (2021) & Meulenkamp (2021): Makulavicius (2020); Manent (2019); Rozis (2018). Myhrvold (2022). |
2. Re-rupture
|
Low GRADE |
Treatment with minimally invasive surgery techniques may result in little to no difference in the number of re-ruptures when compared with open repair in patients with primary, acute Achilles tendon ruptures.
Sources: Attia (2021) & Meulenkamp (2021): Aisaiding (2018); Aktas (2009); Karabinas (2014); Kolodziej (2013); Lim (2001); Makulavicius (2020); Manent (2019); Rozis (2018). |
3. Complications
3.a. Deep venous thrombosis
|
Very low GRADE |
The evidence is very uncertain about the effect of minimally invasive surgery techniques on deep venous thrombosis when compared with open repair in patients with primary, acute Achilles tendon ruptures.
Sources: Aktas (2021) & Meulenkamp (2021): Aktas (2009); Makulavicius (2020). Fischer (2020); Myhrvold (2022). |
3.b. Superficial infections
|
Low GRADE |
Treatment with minimally invasive surgery techniques may reduce the number of superficial infections when compared with open repair in patients with primary, acute Achilles tendon ruptures.
Sources: Attia (2021) & Meulenkamp (2021): Aktas (2009); Karabinas (2014); Kolodziej (2013); Makulavicius (2020); Manent (2019); Rozis (2019. Myhrvold (2022). |
3.c. Deep infections
|
Low GRADE |
Treatment with minimally invasive surgery techniques may result in little to no difference in the number of deep infections when compared with open repair in patients with primary, acute Achilles tendon ruptures.
Sources: Attia (2021) & Meulenkamp (2021): Aktas (2009); Karabinas (2014); Kolodziej (2013); Makulavicius (2020); Manent (2019); Rozis (2019). Myhrvold (2022). |
3.d. Sural nerve injury
|
Low GRADE |
Treatment with minimally invasive surgery techniques may increase the number of sural nerve injuries when compared with open repair in patients with primary, acute Achilles tendon ruptures.
Sources: Attia (2021) & Meulenkamp (2021): Aktas (2009); Karabinas (2014); Kolodziej (2013); Makulavicius (2020); Manent (2019); Rozis (2019). |
4. Range of motion
4.a. Dorsiflexion of the ankle
|
Very low GRADE |
The evidence is very uncertain about the effect of minimally invasive surgery techniques on dorsiflexion of the ankle when compared with open repair in patients with primary, acute Achilles tendon ruptures.
Sources: Attia (2021) & Meulenkamp (2021): Kolodziej (2013); Rozis (2018). |
4.b. Plantarflexion
|
Very low GRADE |
The evidence is very uncertain about the effect of minimally invasive surgery techniques on plantarflexion of the ankle when compared with open repair in patients with primary, acute Achilles tendon ruptures.
Sources: Attia (2021) & Meulenkamp (2021): Kolodziej (2013); Manent (2019). |
5. Return to sport
|
Low GRADE |
Treatment with minimally invasive surgery techniques may result in little to no difference in the number of patients that returned to sport when compared with open repair in patients with primary, acute Achilles tendon ruptures.
Sources: Attia (2021) & Meulenkamp (2021): Aktas (2009); Karabinas (2014); Kolodziej (2013); Lim (2001); Manent (2019); Makulavicius (2020). Fischer (2020). |
6. Quality of life
|
No GRADE |
Due to a lack of relevant literature, it was not possible to draw any conclusion with regards to the outcome quality of life for the comparison of minimally invasive surgery compared with open repair in patients with primary, acute Achilles tendon ruptures.
Sources: - |
7. Return to work
|
No GRADE |
Due to a lack of relevant literature, it was not possible to draw any conclusion with regards to the outcome return to work for the comparison of minimally invasive surgery compared with open repair in patients with primary, acute Achilles tendon ruptures.
Sources: - |
8. Re-operation
|
No GRADE |
Due to a lack of relevant literature, it was not possible to draw any conclusion with regards to the outcome re-operation for the comparison of minimally invasive surgery compared with open repair in patients with primary, acute Achilles tendon ruptures.
Sources: - |
PICO 2: minimally invasive surgical techniques versus minimally invasive surgical techniques compared with each other
|
No GRADE |
Due to a lack of relevant literature, it was not possible to draw any conclusion with regards to the outcomes re-rupture, daily functioning; range of motion (such as dorsiflexion and plantarflexion of the ankle); complications (such as superficial and deep infections, deep venous thrombosis; sural nerve injury); return to sport; quality of life; return to work; re-operation for the comparison of minimally invasive surgery technique compared with a different minimally invasive surgery technique in patients with primary, acute Achilles tendon ruptures.
Sources: - |
Description of studies
PICO 1: minimally invasive surgical techniques versus open repair techniques
The systematic review of Attia (2021) investigated the effectiveness of minimally invasive surgery techniques in comparison with open repair of Achilles tendon ruptures. Attia (2021) conducted a literature search through the electronic databases of Medline, PubMed, Embase, Google Scholar, Scopus, and Cochrane Library databases up to July 2020. Randomized controlled trials on outcomes and complications of open versus percutaneous repair of Achilles tendon ruptures reporting the AOFAS score, ATRS score, sural nerve injuries, infections, skin complications, re-ruptures, ankle range of motion, and calf circumferences were included. Studies not reporting any of the outcomes of interest or the full text not being available in English, German, Spanish, Portuguese, or Arabic were excluded. In total, Attia (2021) included ten studies. Of these, seven studies met the inclusion criteria of this guideline (Aktas, 2009; Karabinas, 2014; Kolodziej, 2013; Lim 2001; Makulavicius, 2020; Manent, 2019; Rozis, 2018). These seven studies involved 379 participants of which 308 participants were males and mean age ranged from 39.2 to 44.8 years. The investigated minimally invasive surgery techniques in the included studies were the Achillon, Ma and Griffith, modified Ma and Griffith, and modified Bunnell technique, while the investigated open repair techniques were the Krakow, Kessler, Bunnell plus crown, and Double Bunnell technique. The risk of bias was assessed with the Newcastle-Ottawa scale. The reported outcomes were daily functioning as measured with the ATRS score, re-rupture, sural nerve injuries, infections, and return to sports.
The systematic review of Meulenkamp (2021) investigated the effectiveness of minimally invasive surgery techniques in comparison with open repair techniques in patients with acute Achilles tendon ruptures. Meulenkamp (2021) conducted a literature search through the electronic databases of Medline, Embase, CINAHL, PEDro, and Cochrane Central Register of Controlled Trials up to the 30th of September 2019. Studies were eligible for inclusion if they met the following inclusion criteria: randomized controlled trials directly comparing minimally invasive or open repair interventions for the treatment of first-time, acute (less than four weeks since injury) Achilles tendon ruptures with a minimum follow-up of six months. Minimally invasive surgery treatment included all surgical modalities that did not completely open and reflect the paratenon, including limited transverse incisions, suture-shuttling techniques, and device-assisted techniques. Studies with patients younger than sixteen years of age, chronic tendon ruptures, tendon re-ruptures, inclusion of patients with preexisting Achilles tendinopathy, and musculotendinous junction tears were excluded. In total, Meulenkamp (2021) included seventeen studies. Of these, only six studies met the inclusion criteria of this guideline (Aisaiding, 2018; Aktas, 2009; Karabinas, 2014; Kolodziej, 2013; Lim 2001; Rozis, 2018). These six studies involved 321 participants of which 253 participants were males and mean age ranged from 39.2 to 56 years. The investigated minimally invasive surgery techniques in the included studies were the Achillon, Tenolig, Ma and Griffith, modified Ma and Griffith, and Krakow techniques, while the investigated open repair techniques were the Achillon, modified Ma and Griffith, Krakow, and Kessler techniques. The risk of bias was assessed with the Cochrane Risk of Bias assessment tool. The reported outcome in Meulenkamp (2021) was re-rupture.
The randomized controlled trial of Myhrvold (2022) investigated the effect of minimally invasive surgery compared with open repair in patients with acute Achilles’ tendon ruptures. In total, 554 patients were included and randomly allocated to minimally invasive surgery or open repair. Patients in the intervention group (n=172) were treated with the Dresden technique, while patients in the control group (n=176) were treated with the Krakow technique. The maximum length of follow-up was twelve months. The reported outcomes in the study of Myhrvold (2022) were re-ruptures and complications, such as deep venous thrombosis and deep infections.
The randomized controlled trial of Fischer (2020) investigated the effect of minimally invasive surgery compared with open repair in patients with acute Achilles tendon ruptures. In total, 60 participants were included and randomly allocated to minimally invasive surgery or open repair. Both the conventional open suture group (n=30) and the minimally invasive suture group (n=30) used the “Dresden instrument”. The maximum length of follow-up was 24 months. The reported outcomes in the study of Fischer (2020) were re-ruptures, complications, such as thrombosis and return to sports.
PICO 2: any kind of minimally invasive surgical technique versus a different minimally invasive surgical technique
Due to the absence of studies meeting the selection criteria, no studies were included in the literature analysis.
Results
PICO 1: minimally invasive surgical techniques versus open repair techniques
1. Daily functioning
Achilles Tendon Rupture Score (ATRS)
ATRS scores were reported in three studies, derived from the systematic review of Attia (2021) and Meulenkamp (2021) (Makulavicius, 2020; Manent, 2019; Rozis, 2018) and in one additional trial of Myhrvold (2022). The results were pooled in a meta-analysis, except for the results in Myhrvold (2022) because the trial only reported mean changes from baseline for both treatment groups, without a standard deviation.
The pooled mean difference (MD) of Makulavicius (2020), Manent (2019), and Rozis (2018) was 0.59 (95% CI -0.27 to 1.45) points between the MIS group (n=95) and open repair group (n=97) (figure 1). This was not considered as a clinically relevant difference.
Myhrvold (2022) reported the mean change in ATRS-score from baseline with a 95% confidence interval. The mean (SD) baseline score in the MIS group (n=172) was 93.9 (15.1) and 94.2 (12.9) in the open repair group (n=176). Baseline scores for the Achilles’ tendon Total Rupture Score in Myhrvold (2022) were determined retrospectively by instructing the patients to answer the questionnaires at the time of enrollment (after the application of the equinus cast but before randomization) according to their preinjury status. At one year follow-up, the mean (95% CI) change from baseline in the MIS group was -14.7 (95% CI -17.9 to -11.6) points, compared to -16.0 (95% CI -19.0 to -12.9) points in the open repair group. This was not considered as a clinically relevant difference.
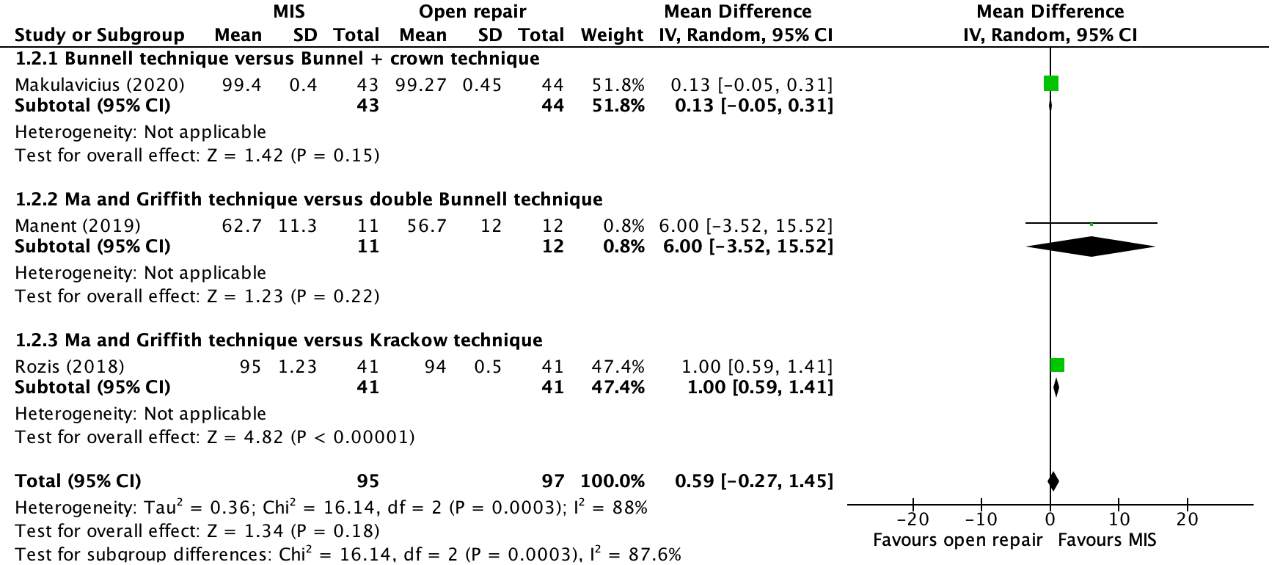
Figure 1. Forest plot showing the comparison between MIS to open repair for ATRS-scores. Pooled mean difference, random effects model. Z: p-value of overall effect; df: degrees of freedom; I2; SD: standard deviation; statistical heterogeneity; CI: confidence interval.
2. Re-rupture
Re-ruptures were reported in eight studies, derived from the systematic review of Attia (2021) and Meulenkamp (2021) (Aisaiding, 2018; Aktas, 2009; Karabinas, 2014; Kolodziej, 2013; Lim 2001; Makulavicius, 2020; Manent, 2019; Rozis, 2018) and two additional studies (Fischer, 2020; Myhrvold, 2022). The results were pooled in a meta-analysis. The pooled number of re-ruptures in the minimally invasive treatment group was 5/408 (1.2%), compared to 7/418 (1.7%) in the open repair group. This resulted in a pooled risk difference (RD) of -0.00 (95% CI -0.01 to 0.01), not in favor of any of the treatments (figure 2). This was not considered as a clinically relevant difference.
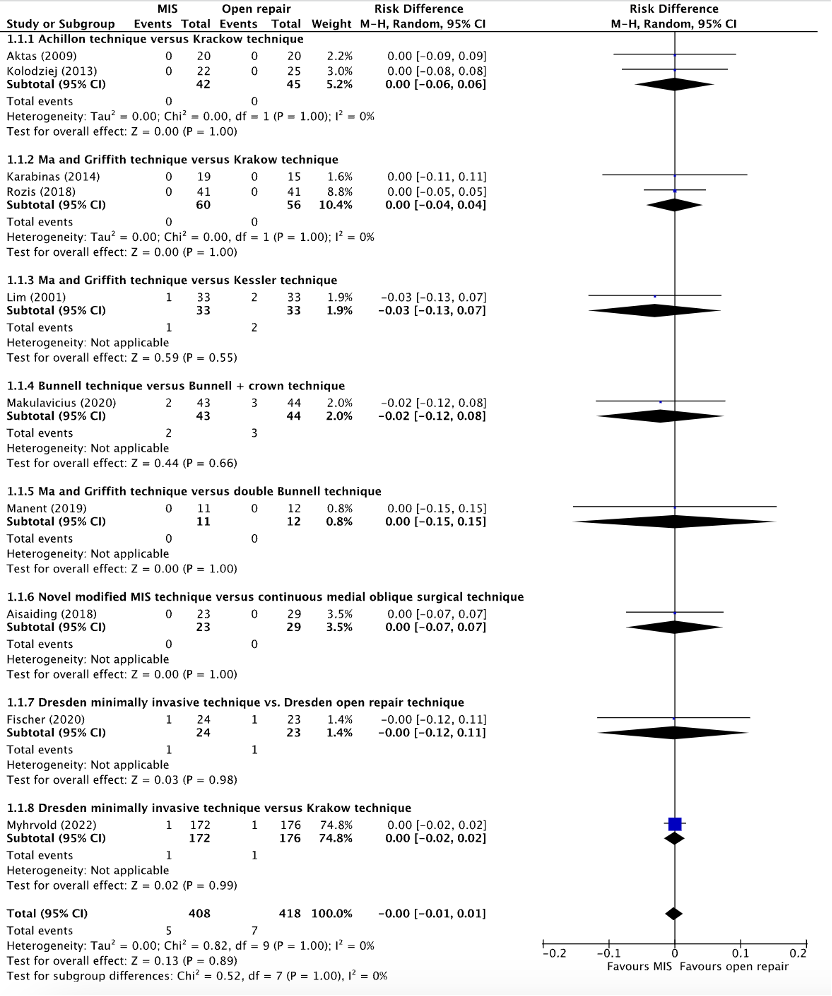
Figure 2. Forest plot showing the comparison between MIS to open repair for re-ruptures. Pooled risk difference, random effects model. Z: p-value of overall effect; df: degrees of freedom; I2; SD: standard deviation; statistical heterogeneity; CI: confidence interval.
3. Complications
3.a. Deep venous thrombosis
Deep venous thrombosis was reported in two studies, retrieved from the systematic review of Attia (2021) and Meulenkamp (2021) (Aktas, 2009; Makulavicius, 2020), and in two additional studies (Fischer, 2020; Myhrvold, 2022). The results were pooled in a meta-analysis. The pooled number of patients who experienced thrombosis in the MIS group was 2/259 (0.8%), compared to 5/263 (1.9%) in the open repair group. This resulted in a pooled relative risk ratio (RR) of 0.54 (95% CI 0.13 to 2.28) and a number needed to harm of 90.9, in favor of the MIS group (see figure 3). This was not considered as a clinically relevant difference.
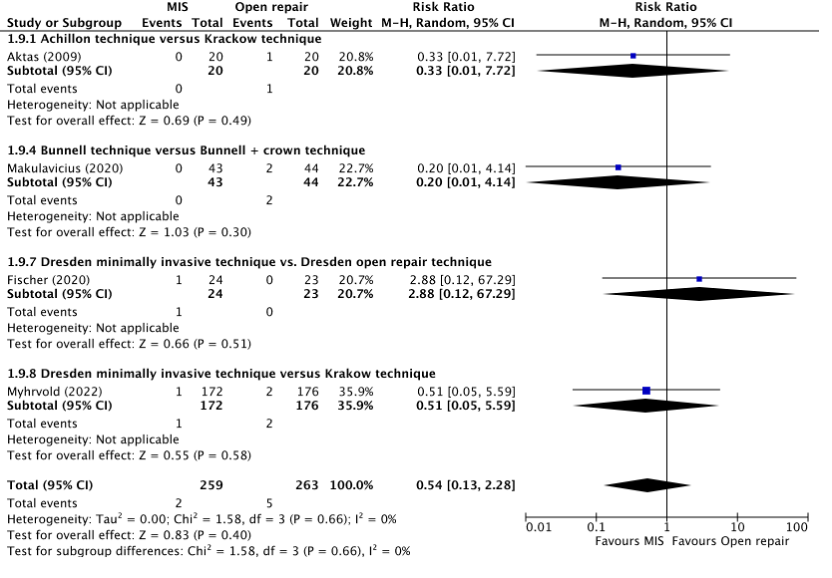
Figure 3. Forest plot showing the comparison between MIS to open repair for deep venous thrombosis. Pooled risk difference, random effects model. Z: p-value of overall effect; df: degrees of freedom; I2; SD: standard deviation; statistical heterogeneity; CI: confidence interval.
3.b. Superficial infections
Superficial infections were reported in seven studies, derived from the systematic reviews of Attia (2021) and Meulenkamp (2021) (Aktas, 2009; Karabinas, 2014; Kolodziej, 2013; Makulavicius, 2020; Manent, 2019; Rozis, 2019) and in one additional study (Myhrvold, 2022). The results were pooled in a meta-analysis. The pooled number of superficial infections in the MIS group was 2/366 (0.5%), compared to 15/371 (4.0%) in the open repair group. This resulted in a pooled risk difference (RD) of -0.03 (95% CI -0.07 to 0.01) and a number needed to harm (NNH) of 28.6, in favor of the MIS group (figure 4). This was considered as a clinically relevant difference.
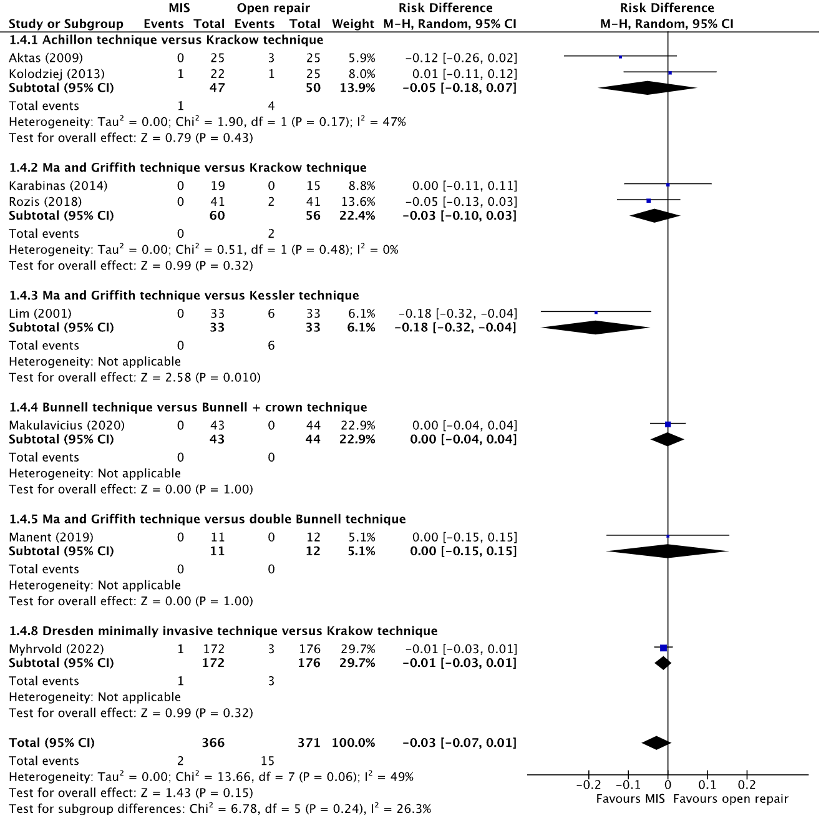
Figure 4. Forest plot showing the comparison between MIS to open repair for superficial infections. Pooled risk difference, random effects model. Z: p-value of overall effect; df: degrees of freedom; I2; SD: standard deviation; statistical heterogeneity; CI: confidence interval.
3.c. Deep infections
Deep infections were reported in seven studies, derived from the systematic reviews of Attia (2021) and Meulenkamp (2021) (Aktas, 2009; Karabinas, 2014; Kolodziej, 2013; Lim, 2001; Makulavicius, 2020; Manent, 2019; Rozis, 2019) and in one additional study (Myhrvold, 2022). The results were pooled in a meta-analysis. The pooled number of deep infections in the MIS group was 3/353 (0.8%), compared to 5/355 (1.4%). This resulted in a pooled risk difference (RD) of -0.00 (95% CI -0.02 to 0.02) and a number needed to harm (NNH) of 166.7, in favor of the MIS group (figure 5). This was not considered as a clinically relevant difference.
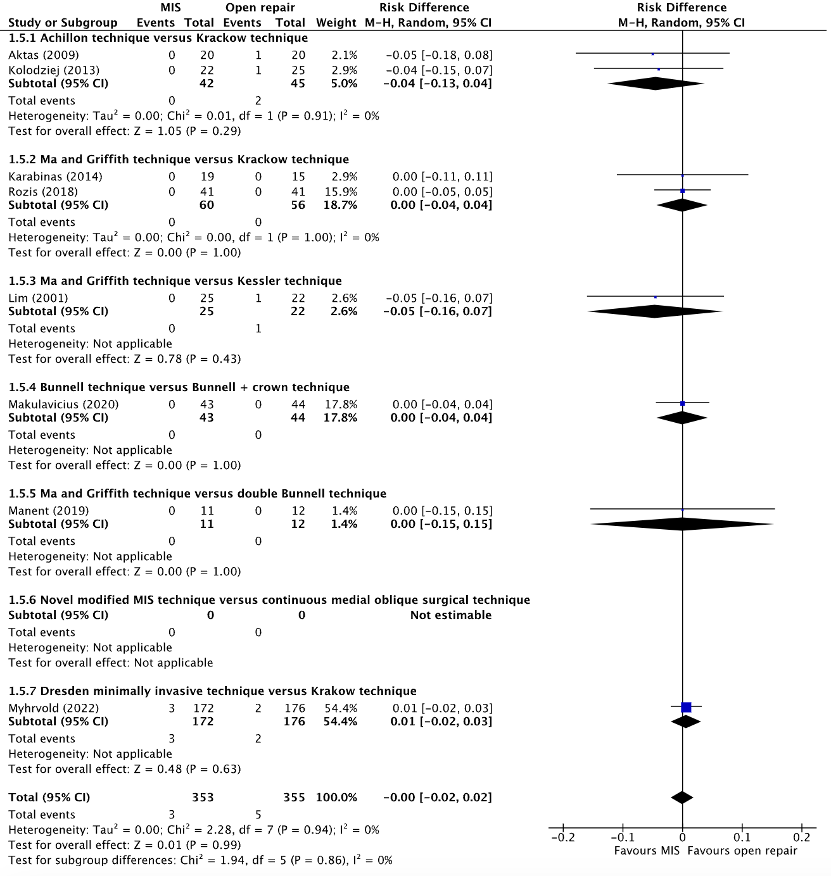
Figure 5. Forest plot showing the comparison between MIS to open repair for deep infections. Pooled risk difference, random effects model. Z: p-value of overall effect; df: degrees of freedom; I2; SD: standard deviation; statistical heterogeneity; CI: confidence interval.
3.d. Sural nerve injury
Sural nerve injury was reported in seven studies, retrieved from the systematic reviews of Attia (2021) and Meulenkamp (2021) (Aktas, 2009; Karabinas, 2014; Kolodziej, 2013; Lim, 2001; Makulavicius, 2020; Manent, 2019; Rozis, 2019) and in one additional study (Myhrvold, 2022). The results were pooled in a meta-analysis. The pooled number of sural nerve injuries in the MIS group was 18/361 (5.0%), compared to 5/366 (1.4%) in the open repair group. This resulted in a pooled risk difference (RD) of 0.03 (95% CI 0.00 to 0.06) and a number needed to harm (NNH) of 27.8, in favor of the open repair group (figure 6). This was considered as a clinically relevant difference.
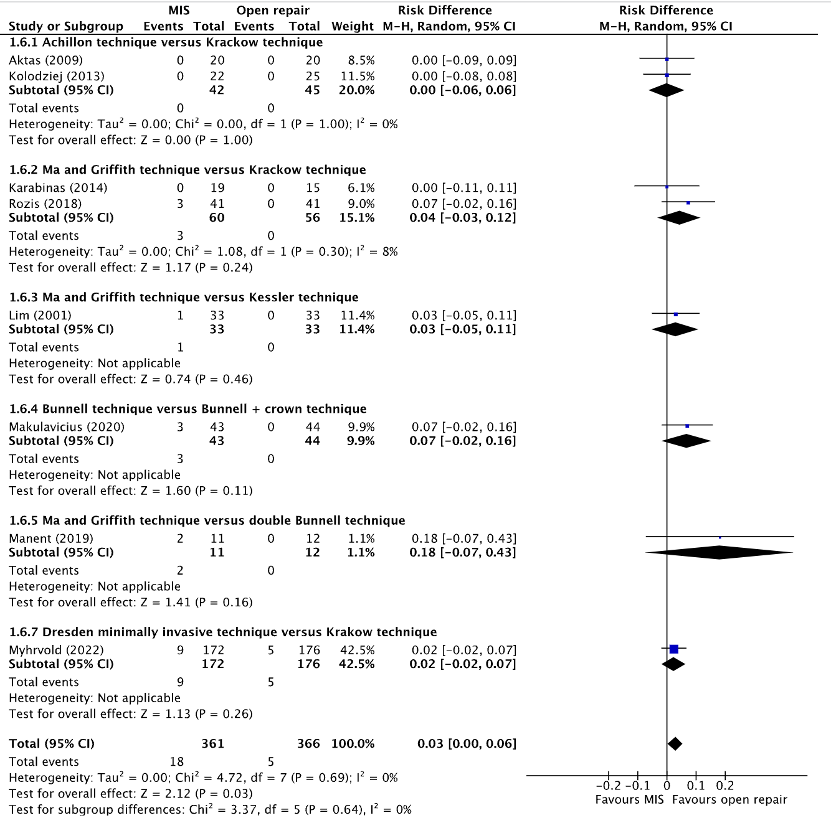
Figure 6. Forest plot showing the comparison between MIS to open repair for sural nerve injuries. Pooled risk difference, random effects model. Z: p-value of overall effect; df: degrees of freedom; I2; SD: standard deviation; statistical heterogeneity; CI: confidence interval.
4. Range of motion
4.a. Dorsiflexion of the ankle
Dorsiflexion of the ankle was reported in two studies, retrieved from the systematic reviews of Attia (2021) and Meulenkamp (2021) (Kolodziej, 2013; Rozis, 2018). Kolodziej (2013) reported the mean (SD) dorsiflexion of the ankle. Rozis (2018) only reported the mean dorsiflexion of the ankle without reporting a standard deviation.
The mean (SD) dorsiflexion of the ankle in the study of Kolodziej (2013) in the MIS group (n=22) was 39.6 (8.1) degrees, compared to 41.6 (10.8) degrees in the open repair group (n=25). This resulted in a mean difference (MD) of -2.00 (95% CI -7.42 to 3.42), in favor of the open repair group. This was not considered as a clinically relevant difference.
The mean dorsiflexion of the ankle in the study of Rozis (2018) in the MIS group (n=41) was 17.2 degrees, compared to 15.8 degrees in the open repair group. A mean difference could not be calculated.
4.b. Plantarflexion
Plantarflexion of the ankle was reported in two studies, retrieved from the systematic reviews of Attia (2021) and Meulenkamp (2021) (Kolodziej, 2013; Manent, 2019). Kolodziej (2013) reported the mean (SD) plantarflexion. Manent (2019) only reported the median (IQR) plantarflexion.
The mean (SD) plantarflexion in the study of Kolodziej (2013) in the MIS group (n=22) was 14.2 (5.1) degrees, compared to 12.6 (4.2) degrees in the open repair group (n=25). This resulted in a mean difference (MD) of 1.60 (95% CI -1.09 to 4.29) degrees, in favor of the MIS group. This was not considered as a clinically relevant difference.
The median (IQR) plantarflexion in the study of Manent (2019) in the MIS group (n=11) was 20 (10 to 30) degrees, compared to 15 (10 to 30) degrees in the open repair group (n=12). A mean difference could not be calculated.
5. Return to sport
Return to sport was reported in six studies, retrieved from the systematic reviews of Attia (2021) and Meulenkamp (2021) (Aktas, 2009; Karabinas, 2014; Kolodziej, 2013; Lim, 2001; Manent, 2019; Makulavicius, 2020) and one additional RCT (Fischer, 2020). The length of follow-up varied between the studies. Aktas (2009), Fischer (2020), Karabinas (2014), Kolodziej (2013), and Malukavicius (2020) reported return to sport at approximately two years follow-up. Lim (2001) and Manent (2019) reported return to sport at one year follow-up. The results were pooled in a meta-analysis. The pooled number of patients that returned to sports in the MIS group was 120/146 (82.2%), compared to 106/140 (75.7%) in the open repair group. This resulted in a pooled relative risk ratio (RR) of 1.03 (95% CI 0.94 to 1.12), in favor of the MIS group (figure 7). This was not considered as a clinically relevant difference.
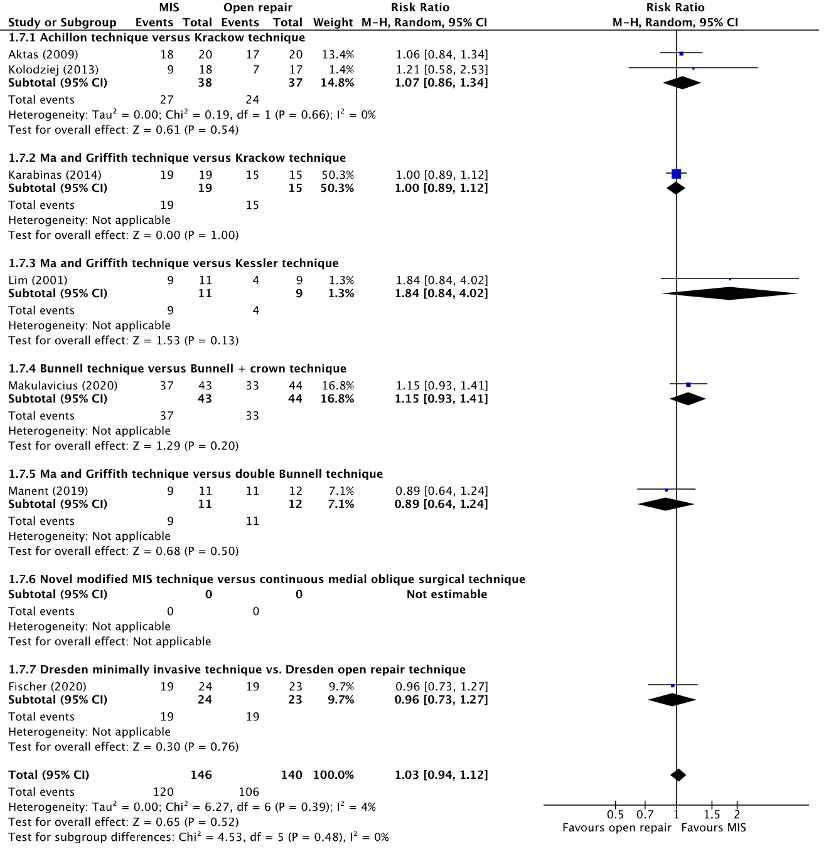
Figure 7. Forest plot showing the comparison between MIS to open repair for return to sport. Pooled relative risk ratio, random effects model. Z: p-value of overall effect; df: degrees of freedom; I2; SD: standard deviation; statistical heterogeneity; CI: confidence interval.
6. Quality of life
None of the included studies reported information regarding the outcome quality of life for the comparison of minimally invasive surgery with open repair in patients with primary, acute Achilles tendon ruptures.
7. Return to work
None of the included studies reported information regarding the outcome return to work for the comparison of minimally invasive surgery with open repair in patients with primary, acute Achilles tendon ruptures.
8. Re-operation
None of the included studies reported information regarding the outcome re-operation for the comparison of minimally invasive surgery with open repair in patients with primary, acute Achilles tendon ruptures.
Level of evidence of the literature
1. Daily functioning
Achilles Tendon Rupture Score (ATRS)
The level of evidence regarding the outcome daily functioning was derived from randomized controlled trials and therefore started high. The level of evidence was downgraded by one level because of a lack of information regarding blinding in the included studies (risk of bias, -1). The level of evidence was considered as moderate.
2. Re-rupture
The level of evidence regarding the outcome re-rupture was derived from randomized controlled trials and therefore started high. The level of evidence was downgraded by two levels because of the small number of events (imprecision, -2). The level of evidence was considered as low.
3. Complications
3.a. Deep venous thrombosis
The level of evidence regarding the outcome deep venous thrombosis was derived from a randomized controlled trial and therefore started high. The level of evidence was downgraded by three levels because of the small number of events, and the wide confidence interval crossing the upper and lower boundaries of clinical relevance (imprecision, -3). The level of evidence was considered as very low.
3.b. Superficial infections
The level of evidence regarding the outcome superficial infections was derived from randomized controlled trials and therefore started high. The level of evidence was downgraded by two levels because of a lack of information regarding blinding in the included studies (risk of bias, -1), and the small number of events (imprecision, -1). The level of evidence was considered as low.
3.c. Deep infections
The level of evidence regarding the outcome deep infections was derived from randomized controlled trials and therefore started high. The level of evidence was downgraded by two levels because of a lack of information regarding blinding in the included studies (risk of bias, -1), and the small number of events (imprecision, -1). The level of evidence was considered as low.
3.d. Sural nerve injury
The level of evidence regarding the outcome sural nerve injury was derived from randomized controlled trials and therefore started high. The level of evidence was downgraded by two levels because of a lack of information regarding blinding in the included studies (risk of bias, -1), and the small number of events (imprecision, -1). The level of evidence was considered as low.
4. Range of motion
4.a. Dorsiflexion of the ankle
The level of evidence regarding the outcome dorsiflexion of the ankle was derived from randomized controlled trials and therefore started high. The level of evidence was downgraded by three levels because of a lack of information regarding blinding in the included studies (risk of bias, -1) and the small number of patients in the included studies (imprecision, -2). The level of evidence was considered as very low.
4.b. Plantarflexion
The level of evidence regarding the outcome plantarflexion was derived from randomized controlled trials and therefore started high. The level of evidence was downgraded by three levels because of a lack of information regarding blinding in the included studies (risk of bias, -1) and the small number of patients in the included studies (imprecision, -2). The level of evidence was considered as very low.
5. Return to sport
The level of evidence regarding the outcome return sport was derived from randomized controlled trials and therefore started high. The level of evidence was downgraded by two levels because of a lack of information regarding blinding in the included studies (risk of bias, -1), and the small number of events (imprecision, -1). The level of evidence was considered as low.
6. Quality of life
Because of a lack of data, it was not possible to grade the literature for the outcome quality of life in patients with primary, acute Achilles tendon ruptures undergoing minimally invasive surgery compared with open repair.
7. Return to work
Because of a lack of data, it was not possible to grade the literature for the outcome return to work in patients with primary, acute Achilles tendon ruptures undergoing minimally invasive surgery compared with open repair.
8. Re-operation
Because of a lack of data, it was not possible to grade the literature for the outcome re-operation in patients with primary, acute Achilles tendon ruptures undergoing minimally invasive surgery compared with open repair.
PICO 2: any kind of minimally invasive surgical technique versus a different minimally invasive surgical technique
Due to the absence of studies meeting the selection criteria, no studies were included that reported information regarding the outcomes daily functioning; re-rupture; complications (such as superficial and deep infections, deep venous thrombosis; sural nerve injury); range of motion (such as dorsiflexion and plantarflexion of the ankle); return to sport; quality of life; return to work and re-operation in patients with a primary, acute Achilles tendon rupture undergoing surgery with a minimally invasive surgical technique versus a different minimally invasive surgical technique.
PICO 1:
A systematic review of the literature was performed to answer the following question: What is the effectiveness and safety of a minimally invasive surgical technique compared to an open surgical technique in patients with a primary, acute Achilles tendon rupture?
P: Patients with a primary, acute Achilles tendon rupture.
I: Minimally invasive surgery techniques.
C: Open repair techniques.
O: Daily functioning (measured with the Achilles Tendon Rupture Score*); re-rupture; complications (such as superficial and deep infections, deep venous thrombosis; sural nerve injury); range of motion (such as dorsiflexion and plantarflexion of the ankle); return to sport; quality of life; return to work; re-operation.
PICO 2:
A systematic review of the literature was performed to answer the following question: What is the effectiveness and safety of different minimally invasive surgical techniques in patients with a primary, acute Achilles tendon rupture?
P: Patients with a primary, acute Achilles tendon rupture.
I: Minimally invasive surgery techniques.
C: A different minimally invasive surgery technique.
O: Daily functioning (measured with the Achilles Tendon Rupture Score*); re-rupture; complications (such as superficial and deep infections, deep venous thrombosis; sural nerve injury); range of motion (such as dorsiflexion and plantarflexion of the ankle); return to sport; quality of life; return to work; re-operation.
*The Achilles Tendon Rupture Score (ATRS) is a disease-specific, self-administered PROM that can be used to quantify functional outcomes related to symptoms and physical activity after treatment in patients with an Achilles tendon rupture (10 questions using an 11-point (0-10) Likert scale, in which 0 means maximum disability and 100 points means no symptoms and full function/recovery).
Relevant outcome measures
The guideline development group considered functional outcomes (such as daily function) as a critical outcome measure for decision making; and re-ruptures, complications (such as superficial and deep infections, deep venous thrombosis, and sural nerve injury), range of motion, return to sport, quality of life, return to work, and re-operation as an important outcome measure for decision making.
The working group defined a threshold of 10% for continuous outcomes and a relative risk (RR) for dichotomous outcomes of <0.80 and >1.25 as a minimal clinically (patient) important difference.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms from 2002 until the 12th of May 2022. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 80 hits. Studies were selected based on the following criteria: systematic reviews and randomized controlled trials from 2000 onwards on minimal invasive surgical techniques for Achilles tendon ruptures. Twelve studies were initially selected based on title and abstract screening. After reading the full text, eight studies were excluded (see the table with reasons for exclusion under the tab Methods), and four studies were included.
Results
Four studies were included in the analysis of the literature (two systematic reviews and two randomized controlled trials). Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
- Aisaiding A, Wang J, Maimaiti R, Jialihasi A, Aibek R, Qianman B, Shawutali N, Badelihan A, Bahetiya W, Kubai A, Kelamu M, Nuerdoula Y, Makemutibieke E, Bakyt Y, Wuerliebieke J, Jielile J. A novel minimally invasive surgery combined with early exercise therapy promoting tendon regeneration in the treatment of spontaneous Achilles tendon rupture. Injury. 2018 Mar;49(3):712-719. doi: 10.1016/j.injury.2017.10.046. Epub 2017 Oct 31. PMID: 29153451.
- Aktas S, Kocaoglu B. Open versus minimal invasive repair with Achillon device. Foot Ankle Int. 2009 May;30(5):391-7. doi: 10.3113/FAI-2009-0391. PMID: 19439137.
- Attia AK, Mahmoud K, d'Hooghe P, Bariteau J, Labib SA, Myerson MS. Outcomes and Complications of Open Versus Minimally Invasive Repair of Acute Achilles Tendon Ruptures: A Systematic Review and Meta-analysis of Randomized Controlled Trials. Am J Sports Med. 2021 Dec 15:3635465211053619. doi: 10.1177/03635465211053619. Epub ahead of print. PMID: 34908499.
- Fischer S, Colcuc C, Gramlich Y, Stein T, Abdulazim A, von Welck S, Hoffmann R. Prospective randomized clinical trial of open operative, minimally invasive and conservative treatments of acute Achilles tendon tear. Arch Orthop Trauma Surg. 2021 May;141(5):751-760. doi: 10.1007/s00402-020-03461-z. Epub 2020 May 4. PMID: 32367375.
- Karabinas PK, Benetos IS, Lampropoulou-Adamidou K, Romoudis P, Mavrogenis AF, Vlamis J. Percutaneous versus open repair of acute Achilles tendon ruptures. Eur J Orthop Surg Traumatol. 2014 May;24(4):607-13. doi: 10.1007/s00590-013-1350-7. Epub 2013 Nov 5. PMID: 24190345.
- Kołodziej L, Bohatyrewicz A, Kromuszczyńska J, Jezierski J, Biedroń M. Efficacy and complications of open and minimally invasive surgery in acute Achilles tendon rupture: a prospective randomised clinical study--preliminary report. Int Orthop. 2013 Apr;37(4):625-9. doi: 10.1007/s00264-012-1737-9. Epub 2012 Dec 19. PMID: 23250350; PMCID: PMC3609980.
- Lim J, Dalal R, Waseem M. Percutaneous vs. open repair of the ruptured Achilles tendon--a prospective randomized controlled study. Foot Ankle Int. 2001 Jul;22(7):559-68. doi: 10.1177/107110070102200705. PMID: 11503980.
- Makulavičius A, Mazarevičius G, Klinga M, Urmanavičius M, Masionis P, Oliva XM, Uvarovas V, Porvaneckas N. Outcomes of open "crown" type v. percutaneous Bunnell type repair of acute Achilles tendon ruptures. Randomized control study. Foot Ankle Surg. 2020 Jul;26(5):580-584. doi: 10.1016/j.fas.2019.07.011. Epub 2019 Aug 3. PMID: 31548150.
- Manent A, López L, Corominas H, Santamaría A, Domínguez A, Llorens N, Sales M, Videla S. Acute Achilles Tendon Ruptures: Efficacy of Conservative and Surgical (Percutaneous, Open) Treatment-A Randomized, Controlled, Clinical Trial. J Foot Ankle Surg. 2019 Nov;58(6):1229-1234. doi: 10.1053/j.jfas.2019.02.002. Erratum in: J Foot Ankle Surg. 2020 Jul - Aug;59(4):874. PMID: 31679677.
- McMahon SE, Smith TO, Hing CB. A meta-analysis of randomised controlled trials comparing conventional to minimally invasive approaches for repair of an Achilles tendon rupture. Foot Ankle Surg. 2011 Dec;17(4):211-7. doi: 10.1016/j.fas.2010.11.001. Epub 2010 Dec 16. PMID: 22017889.
- Meulenkamp B, Woolnough T, Cheng W, Shorr R, Stacey D, Richards M, Gupta A, Fergusson D, Graham ID. What Is the Best Evidence to Guide Management of Acute Achilles Tendon Ruptures? A Systematic Review and Network Meta-Analysis of Randomized Controlled Trials. Clin Orthop Relat Res. 2021 Oct 1;479(10):2119-2131. doi: 10.1097/CORR.0000000000001861. PMID: 34180874; PMCID: PMC8445578.
- Myhrvold SB, Brouwer EF, Andresen TKM, Rydevik K, Amundsen M, Grün W, Butt F, Valberg M, Ulstein S, Hoelsbrekken SE. Nonoperative or Surgical Treatment of Acute Achilles' Tendon Rupture. N Engl J Med. 2022 Apr 14;386(15):1409-1420. doi: 10.1056/NEJMoa2108447. PMID: 35417636.
- Rozis M, Benetos IS, Karampinas P, Polyzois V, Vlamis J, Pneumaticos SG. Outcome of Percutaneous Fixation of Acute Achilles Tendon Ruptures. Foot Ankle Int. 2018 Jun;39(6):689-693. doi: 10.1177/1071100718757971. Epub 2018 Mar 12. PMID: 29528724.
Evidence tabel
Systematic review(s)
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C)
|
Follow-up |
Outcome measures and effect size |
|
Attia (2021) |
SR and meta-analysis of RCTs
Literature search up to July 2020
A: Aktas (2009) B: Karabinas (2014) C: Kolodziej (2013) D: Lim (2001) E: Makulavicius (2020) F: Manent (2019) G: Rozis (2018)
Study design: All studies were parallel RCTs.
Setting and Country: A: Turkey B: Greece C: Poland D: United Kingdom E: Lithuania F: Spain G: Greece
Source of funding and conflict of interest: One or more of the authors has declared the following potential conflict of interest or source of funding: K.M. has received education support from Arthrex. J.B. has received consulting fees from Stryker and MedShape. S.A.L. has received consulting fees from Arthrosurface, Stryker, and Heron Ther- apeutics; grants from Zimmer Biomet Biologics; hospitality payments from Exactech; and education support from Arthrex and United Orthopedics. S.A.L. also holds stock options in MedShape. M.S.M. has received grants from Zimmer Biomet; grants, personal fees and royalties from Paragon 28; royalties from Wright Medical and DePuy Synthes; grants and consulting fees from Integra LifeSciences; and personal fees from Elsevier. AOSSM checks author disclosures against the Open Payments Database (OPD). AOSSM has not conducted an independent investigation on the OPD and disclaims any liability or responsibility relating thereto.
|
Inclusion criteria SR:
Exclusion criteria SR:
Seven studies included
Important patient characteristics at baseline:
N A: N=40 B: N=34 C: N=47 D: N=66 E: N=87 F: N=23 G: N=82
mean age (I vs C) A: 39.2 vs 40.6 B: 42 (25-58) vs 40 (28-50) C: 44.8 (9.2) vs 47.1 (13.3) D: 40.1 vs 36.9 E: 35.93 (9.49) vs 37.82 (10.10) F: 41.0 (18-50) vs 40.5 (28-51) G: 43 (18.5) vs 41 (19.5)
Sex: (M/F) A: 18/2 vs 17/3 B: 15/4 vs 13/2 C: 21/1 vs 24/1 D: 19/14 vs 20/13 E: 38/5 vs 39/5 F: 10/1 vs 11/1 G: 31/10 vs 32/9
Groups comparable at baseline? Yes. |
Describe intervention:
A: MIS – Achillon B: MIS – Ma and Griffith C: MIS – Achillon D: MIS – Ma and Griffith E: MIS- Bunnell F: MIS – Ma and Griffith G: MIS – Ma and Griffith
|
Describe control:
A: Open - Krackow B: Open - Krackow C: Open - Krackow D: Open - Kessler E: Open – Bunnell + crown F: Open – Double Bunnell G: Open - Krackow |
End-point of follow-up:
A: 22.5 vs 22.2 months B: 20 (9-24) vs 22 (10-24) months C: 24 vs 24 months D: 6 vs 6 months E: 27 (12-36) vs 27 (12-36 months F: 12 vs 12 months G: 12 vs 12 months
|
Outcome measure: total complications, n/N (%)
A (Aktas, 2009) I: 1/20 (5.0%) C: 7/20 (35.0%)
B (Karabinas, 2014) I: 0/19 (0%) C: 1/15 (6.7%)
C (Kolodziej, 2013) I: 2/22 9.1%) C: 1/25 (4.0%)
D (Lim, 2001) I: 5/33 (15.2%) C: 12/33 (36.4%)
E (Makulavicius, 2020) I: 8/43 (18.6%) C: 5/44 (11.4%)
F (Manent, 2019) I: 5/11 (45.5%) C: 2/12 (16.7%)
G (Rozis, 2018) I: 3/41 (7.3%) C: 3/41 (7.3%)
Outcome measure: re-rupture rate, n/N (%)
A (Aktas, 2009) I: 0/20 (0%) C: 0/20 (0%)
B (Karabinas, 2014) I: 0/19 (0%) C: 0/15 (0%)
C (Kolodziej, 2013) I: 0/22 (0%) C: 0/25 (4.0%)
D (Lim, 2001) I: 1/33 (3.3%) C: 2/33 (6.6%)
E (Makulavicius, 2020) I: 2/43 (4.7%) C: 3/44 (6.8%)
F (Manent, 2019) I: 0/11 (0%) C: 0/12 (0%)
G (Rozis, 2018) I: 0/41 (0%) C: 0/41 (0%)
Outcome measure: sural nerve palsy rate, n/N (%)
A (Aktas, 2009) I: 0/20 (0%) C: 0/20 (0%)
B (Karabinas, 2014) I: 0/19 (0%) C: 0/15 (0%)
C (Kolodziej, 2013) I: 0/22 (0%) C: 0/25 (0%)
D (Lim, 2001) I: 0/33 (0%) C: 1/33 (3.3%)
E (Makulavicius, 2020) I: 3/43 (7.0%) C: 0/44 (0%)
F (Manent, 2019) I: 2/11 (18.2%) C: 0/12 (0%)
G (Rozis, 2018) I: 3/41 (7.3%) C: 0/41 (0%)
Outcome measure: deep infection, n/N (%)
A (Aktas, 2009) I: 0/20 (0%) C: 1/20 (5.0%)
B (Karabinas, 2014) I: 0/19 (0%) C: 0/15 (0%)
C (Kolodziej, 2013) I: 0/22 (0%) C: 1/25 (4.0%)
D (Lim, 2001) I: 0/25 (0%) C: 1/22 (4.5%)
E (Makulavicius, 2020) I: 0/43 (0%) C: 0/44 (0%)
F (Manent, 2019) I: 0/11 (0%) C: 0/12 (0%)
G (Rozis, 2018) I: 0/41 (0%) C: 0/41 (0%)
Outcome measure: ATRS-score, mean (SD)
E (Makulavicius, 2020) I: 99.4 (0.4) (n=43) C: 99.27 (0.45 (n=44)
F (Manent, 2019) I: 62.7 (11.3) (n=11) C: 56.7 (12.0) (n=12)
G (Rozis, 2018) I: 95 (1.23) (n=41) C: 94 (0.5) (n=41)
Outcome measure: return to previous level of sports, n/N (%)
A (Aktas, 2009) I: 18/20 (90.0%) C: 17/20 (85.0%)
B (Karabinas, 2014) I: 19/19 (100%) C: 15/15 (100%)
C (Kolodziej, 2013) I: 9/18 (50%) C: 7/17 (41.2%)
D (Lim, 2001) I: 9/11 (81.8%) C: 4/9 (44.4%)
E (Makulavicius, 2020) I: 37/43 (86.0%) C: 33/44 (75.0%)
F (Manent, 2019) I: 9/11 (81.8%) C: 11/12 (91.7%)
Outcome measure: range of motion
Plantarflexion
D (Kolodziej, 2013), mean (SD) I: 14.2 (5.1) (n=22) C: 12.6 (4.2) (n=25)
F (Manent, 2019), median (IQR) I: 20 (10 to 30) degrees C: 15 (10 to 30) degrees
Dorsalflexion
D Kolodziej (2013) I: 39.6 (8.1) (n=22) C: 41.6 (10.8) (n=25)
G (Rozis, 2018) I: 17.2 C: 15.8
|
|
Meulenkamp (2021) |
SR and meta-analysis of [RCTs / cohort / case-control studies]
Literature search up to
A: Aisaiding (2018) B: Aktas (2009) C: Karabinas (2014) D: Kolodziej (2013) E: Lim (2001) F: Rozis (2018)
Study design: RCT [parallel / cross-over], cohort [prospective / retrospective], case-control
Setting and Country:
Source of funding
Conflicts of interest: [commercial / non-commercial / industrial co-authorship]
|
Inclusion criteria SR:
Exclusion criteria SR:
Six studies included
Important patient characteristics at baseline:
N A: N=42 B: N=40 C: N=34 D: N=47 E: N=66 F: N=82
mean age A: 56 (47 to 75) B: 39.2 vs 40.6 C: 42 (25-58) vs 40 (28-50) D: 44.8 (9.2) vs 47.1 (13.3) E: 40.1 vs 36.9 F: 43 (18.5) vs 41 (19.5)
Sex: (M/F) A: 43/9 B: 18/2 vs 17/3 C: 15/4 vs 13/2 D: 21/1 vs 24/1 E: 19/14 vs 20/13 F: 31/10 vs 32/9
Groups comparable at baseline? Yes. |
Describe intervention:
A: MIS – Achillon B: MIS – Temolig C: MIS – Ma and Griffith D: MIS – Krakow technique, absorbable suture E: MIS – Ma and Griffith F: MIS – Ma and Griffith |
Describe control:
A: Open – Achillon B: Open – Ma and Griffith C: Open – Krakow D: Open – Achillon, absorbable suture E: Open – Kessler F: Open – Krakow |
End-point of follow-up:
A: 24 months. B: 22.5 vs 22.2 months C: 20 (9-24) vs 22 (10-24) months D: 24 vs 24 months E: 6 vs 6 months F: 12 vs 12 months
|
Outcome measure: total complications, n/N (%)
A (Aisaiding (2018) I: 0/23 (0%) C: 0/29 (0%)
B (Aktas, 2009) I: 1/20 (5.0%) C: 7/20 (35.0%)
C (Karabinas, 2014) I: 0/19 (0%) C: 1/15 (6.7%)
D (Kolodziej, 2013) I: 2/22 9.1%) C: 1/25 (4.0%)
E (Lim, 2001) I: 5/33 (15.2%) C: 12/33 (36.4%)
F (Rozis, 2018) I: 3/41 (7.3%) C: 3/41 (7.3%)
Outcome measure: re-rupture rate, n/N (%)
B (Aktas, 2009) I: 0/20 (0%) C: 0/20 (0%)
C (Karabinas, 2014) I: 0/19 (0%) C: 0/15 (0%)
D (Kolodziej, 2013) I: 0/22 (0%) C: 0/25 (4.0%)
E (Lim, 2001) I: 1/33 (3.3%) C: 2/33 (6.6%)
F (Rozis, 2018) I: 0/41 (0%) C: 0/41 (0%)
Outcome measure: sural nerve palsy rate, n/N (%)
B (Aktas, 2009) I: 0/20 (0%) C: 0/20 (0%)
C (Karabinas, 2014) I: 0/19 (0%) C: 0/15 (0%)
D (Kolodziej, 2013) I: 0/22 (0%) C: 0/25 (0%)
E (Lim, 2001) I: 0/33 (0%) C: 1/33 (3.3%)
F (Rozis, 2018) I: 3/41 (7.3%) C: 0/41 (0%)
Outcome measure: deep infection, n/N (%)
B (Aktas, 2009) I: 0/20 (0%) C: 1/20 (5.0%)
C (Karabinas, 2014) I: 0/19 (0%) C: 0/15 (0%)
D (Kolodziej, 2013) I: 0/22 (0%) C: 1/25 (4.0%)
E (Lim, 2001) I: 0/25 (0%) C: 1/22 (4.5%)
F Rozis, 2018) I: 0/41 (0%) C: 0/41 (0%)
Outcome measure: ATRS-score, mean (SD)
F (Rozis, 2018) I: 95 (1.23) (n=41) C: 94 (0.5) (n=41)
Outcome measure: return to previous level of sports, n/N (%)
B (Aktas, 2009) I: 18/20 (90.0%) C: 17/20 (85.0%)
C (Karabinas, 2014) I: 19/19 (100%) C: 15/15 (100%)
D (Kolodziej, 2013) I: 9/18 (50%) C: 7/17 (41.2%)
E (Lim, 2001) I: 9/11 (81.8%) C: 4/9 (44.4%)
|
Randomized controlled trial(s)
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
|
Fischer (2020) |
Type of study: RCT
Setting and country: Sweden.
Funding and conflicts of interest: None declared. |
Inclusion criteria:
Exclusion criteria:
N total at baseline: Intervention: N=30 Control: N=30
Important prognostic factors2: age ± SD: I: 39.3 (7.9) C: 39.6 (7.3)
Sex: I: 2/30 (7%) M C: 4/30 (13%) M
Groups comparable at baseline? Yes.
|
Describe intervention (treatment/procedure/test):
MIS – Dresden instrument.
|
Describe control (treatment/procedure/test):
Open – Conventional open suture. |
Length of follow-up: 24 months.
Loss-to-follow-up: Intervention: N=3
Control: N=1
|
Outcome measure: re-rupture, n/N (%)
I: 1/24 (4.2%) C: 1/23 (4.3%)
Outcome measure: Thrombosis, n/N (%)
I: 1/24 (4.2%) C: 0/23 (0%)
Outcome measure: Quality of life (mental component summary) measured with the SF-36, mean (SD)
I: 53.6 (50.1) (n=24) C: 52.7 (50.1) (n=23)
Outcome measure: Quality of life (physical component summary) measured with the SF-36, mean (SD)
I: 55.2 (51.5) (n=24) C: 55.9 (51.5) (n=23)
Outcome measure: Pain (measured with the VAS 0-100), mean (SD)
I: 95.5 C: 95.5
|
Author’s conclusion:
Regardless of the therapy, all patients with AATR achieved a very good clinical outcome after 24 months as assessed by AOFAS-AH. This requires the initial complete approxima- tion of the tendon stumps. The objectifiable Biodex® measurement confirms a positive correlation between AOFAS- AH and the plantar flexion force. Thus, the Biodex® measurement appears to be suitable as an additional outcome parameter after injury to the Achilles tendon. The results of the ultrasound examination correlate neither with the results of the scores nor with the objectifiable force measurement.
|
|
Manent (2019) |
Type of study: RCT
Setting and country: Spain. Funding and conflicts of interest: None declared. |
Inclusion criteria:
Exclusion criteria:
N total at baseline: Intervention: N=11 Control: N=12
Important prognostic factors2: age ± SD: I: 41 (18 to 50) C: 40.5 (28 to 51)
Sex: I: 10/11 (90%) M C: 11/12 (91.2%) M
Groups comparable at baseline? Yes.
|
Describe intervention (treatment/procedure/test):
MIS – Ma and Griffith
|
Describe control (treatment/procedure/test):
Open – Double Bunnell suture |
Length of follow-up: 1 year.
Loss-to-follow-up: Intervention: N=0
Control: N=0
|
Outcome measure:
|
Author’s conclusion: |
Risk of bias tabel
Systematic review(s)
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/not applicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Attia (2021) |
Yes |
Yes |
Yes |
Yes |
Not applicable |
Yes |
Yes |
Yes |
Yes |
|
Meulenkamp (2021) |
Yes |
Yes |
No |
No |
Not applicable |
Yes |
Yes |
Yes |
Yes |
Randomized controlled trial(s)
|
Study reference
(first author, publication year) |
Was the allocation sequence adequately generated?
Definitely yes Probably yes Probably no Definitely no |
Was the allocation adequately concealed?
Definitely yes Probably yes Probably no Definitely no |
Blinding: Was knowledge of the allocated interventions adequately prevented?
Definitely yes Probably yes Probably no Definitely no |
Was loss to follow-up (missing outcome data) infrequent?
Definitely yes Probably yes Probably no Definitely no |
Are reports of the study free of selective outcome reporting?
Definitely yes Probably yes Probably no Definitely no |
Was the study apparently free of other problems that could put it at a risk of bias?
Definitely yes Probably yes Probably no Definitely no |
Overall risk of bias If applicable/necessary, per outcome measure
LOW Some concerns HIGH
|
|
Aisaiding (2018) |
Definitely yes
Reason: Fifty-two patients with acute closed spontaneous Achilles tendon rupture were randomly classified into 2 groups.
|
No information.
Reason: - |
No information.
Reason: - |
Probably yes.
Reason: The study does not report any patient lost to follow-up |
Definitely yes
Reason: All predefined outcomes were reported. |
No information.
Reason: - |
Some concerns.
Reason: No information regarding blinding and allocation concealment. |
|
Aktas (2009) |
Definitely yes
Reason: Equal numbers of patients were randomized.
|
Definitely yes
Reason: randomly allocated to either treatment.
|
Only patients were blinded. Evaluators were not.
Reason: The randomization was blinded and the patients received written and verbal information about the study and its purpose. The clinical evaluators were not blinded.
|
Probably yes
Reason: No lost to follow-up reported. |
Definitely yes
Reason: All predefined outcomes were reported. |
No information.
Reason: |
Low |
|
Fischer (2020) |
Probably yes
Reason: not specifically described. |
No information
Reason: |
No blinding
Reason: “Some limitations of this study need to be considered. The design of the study did not allow blinding.” |
Probably yes
Reason: little lost to follow-up. |
Definitely yes
Reason: all predefined outcomes were reported. |
Probably yes
Reason: no other problems reported. |
High
Reason: possible selection bias and no blinding |
|
Karabinas (2014) |
Definitely yes
Reason: The patients were randomly allocated into the two treatment groups according to the order of their presentation (one by one); the last two patients had percutaneous repair because of the surgeon’s preference.
|
Definitely yes.
Reason: according to the order of their presentation (one by one); the last two patients had percutaneous repair because of the surgeon’s preference. |
No information
Reason: |
Probably yes
Reason: No lost to follow-up reported. |
Definitely yes
Reason: All predefined outcomes were reported. |
No information
Reason: - |
Some concerns.
Reason: No information regarding blinding. |
|
Kolodziej (2013 |
Definitely yes.
Reason: We implemented a simple randomisation protocol, where patients were asked to choose one of two opaque envelopes that contained a paper indicating the type of surgery.
|
Definitely yes.
Reason: We implemented a simple randomisation protocol, where patients were asked to choose one of two opaque envelopes that contained a paper indicating the type of surgery.
|
Probably no.
Reason: A limitation of our study was that we did not use a blinding method to avoid a detection bias.
|
Probably yes.
Reason: Four patients were lost to follow-up but equally distributed over the two groups. |
Definitely yes
Reason: All predefined outcomes were reported. |
No information.
Reason: - |
Low. |
|
Lim (2001) |
Definitely yes.
Reason: Randomization to percutaneous or open surgical groups was done using the last digit of the patient's hospital number.
|
Definitely yes.
Reason: If the digit was odd then percutaneous repair was chosen and if even, open repair.
|
Probably yes.
Reason: The patients were blinded to the randomization process. Evaluators unclear.
|
Probably yes.
Reason: No lost to follow-up reported. |
Definitely yes
Reason: All predefined outcomes were reported. |
No information.
Reason: - |
Low |
|
Makulavicius (2020) |
Definitely yes.
Reason: One hundred patients were included and randomised in two groups
|
Definitely yes.
Reason: using sealed opaque numbered envelopes, taken one by one before each procedure.
|
No information.
Reason: - |
Probably yes.
Reason: No lost to follow-up reported. |
Definitely yes
Reason: All predefined outcomes were reported. |
No information.
Reason: - |
Some concerns.
Reason: No information regarding blinding. |
|
Manent (2019) |
Probably yes.
Reason: A computer-generated randomization schedule was prepared at the start of the study with stratification by 4 variables (to minimize possible bias) according to age (>40 years); whether the patient was a professional athlete or performed regular sports (>4 times per week for 30 min); whether the patient had a previous pathology such as diabetes mellitus, rheumatic diseases, or collagen diseases; and whether the patient had been treated with quinolones or systemic/local corticosteroids.
|
Definitely yes.
Reason: A computer-generated randomization schedule was prepared at the start of the study with stratification by 4 variables (to minimize possible bias) according to age (>40 years); whether the patient was a professional athlete or performed regular sports (>4 times per week for 30 min); whether the patient had a previous pathology such as diabetes mellitus, rheumatic diseases, or collagen diseases; and whether the patient had been treated with quinolones or systemic/local corticosteroids. |
Probably yes.
Reason: Access to this schedule was limited to the staff who generated it and the staff in charge of assigning the randomization. The investigator who evaluated efficacy was not involved in the treatment assignment, the treatment performed, or the follow-up visits of the patients.
|
Probably yes.
Reason: No lost to follow-up reported. |
Definitely yes
Reason: All predefined outcomes were reported. |
No information.
Reason: - |
Low. |
|
Rozis (2018) |
Definitely yes.
Reason: From those, 82 patients (62.6%) met the inclusion criteria and were randomly assigned into 2 treatment groups.
|
Definitely yes.
Reason: Our randomization protocol was based on patient admission order (one by one) fol- lowing the same method as in our former study
|
No information.
Reason: - |
Probably yes.
Reason: No lost to follow-up reported. |
Definitely yes
Reason: All predefined outcomes were reported. |
No information.
Reason: - |
Some concerns.
Reason: No information regarding blinding. |
Exclusie tabel
|
Author and year |
Reason for exclusion |
|
Aisaiding (2018) |
Included in systematic review of Meulenkamp (2021) and Attia (2021). |
|
Aktas (2009) |
Included in systematic review of Meulenkamp (2021) and Attia (2021). |
|
Alcelik (2018) |
|
|
Gatz (2021) |
|
|
Karabinas (2013) |
Included in systematic review of Meulenkamp (2021) and Attia (2021). |
|
Kolodziej (2013) |
Included in systematic review of Meulenkamp (2021) and Attia (2021). |
|
McMahon (2011) |
|
|
Myhrvold (2022) |
Included in systematic review of Meulenkamp (2021) and Attia (2021). |
|
Wu (2019) |
|
Beoordelingsdatum en geldigheid
Publicatiedatum : 14-12-2023
Beoordeeld op geldigheid : 22-09-2023
Algemene gegevens
De ontwikkeling van deze richtlijnmodules werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Werkgroep
- Dr. E.J.M.M. (Egbert Jan) Verleisdonk, chirurg, Nederlandse Vereniging voor Heelkunde.
- Dr. M. (Maayke) van Sterkenburg, chirurg, Nederlandse Vereniging voor Heelkunde (Nederlandse Vereniging voor Traumachirurgie).
- Dr. S. (Steven) Ferree, AIOS-chirurgie, Nederlandse Vereniging voor Heelkunde (Nederlandse Vereniging voor Traumachirurgie).
- Dr. M. (Matthijs) van Ark, fysiotherapeut, Koninklijk Nederlands Genootschap voor Fysiotherapie.
- Dr. D.E. (Duncan) Meuffels, orthopedisch chirurg, Nederlandse Orthopaedische Vereniging.
- Drs. T.E. (Ties) Maijs, radioloog, Nederlandse Vereniging voor Radiologie.
- Drs. L.N. (Lisanne) Hollander, spoedeisende hulp arts, Nederlandse Vereniging voor Spoedeisende Hulp Artsen.
- Dr. R.J. (Robert-Jan) de Vos, sportarts, Vereniging voor Sportgeneeskunde.
Meelezers
- Drs. K. (Klaartje) Spijkers, Patiëntenfederatie Nederland.
Met ondersteuning van:
- Dr. A.C.J. (Astrid) Balemans, adviseur, Kennisinstituut van Medisch Specialisten.
- M. (Mitchel) Griekspoor MSc, adviseur, Kennisinstituut van Medisch Specialisten.
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Dhr. dr. E.J.M.M. (Egbert Jan) Verleisdonk |
Chirurg. |
Voorzitter stichting ALSG (onbezoldigd).
|
Persoonlijke financiële belangen Geen.
Persoonlijke relaties Geen.
Extern gefinancierd onderzoek Geen.
Intellectuele belangen en reputatie Geen.
Overige belangen Geen.
|
Geen. |
|
Mevr. dr. M. (Maayke) van Sterkenburg
|
Chirurg. |
Geen. |
Persoonlijke financiële belangen Geen.
Persoonlijke relaties Geen.
Extern gefinancierd onderzoek Geen.
Intellectuele belangen en reputatie Geen.
Overige belangen Geen.
|
Geen. |
|
Dhr. dr. S. (Steven) Ferree
|
AIOS-chirurgie. |
Geen. |
Persoonlijke financiële belangen Geen.
Persoonlijke relaties Geen.
Extern gefinancierd onderzoek Geen.
Intellectuele belangen en reputatie Geen.
Overige belangen Geen.
|
Geen. |
|
Dhr. dr. M. (Matthijs) van Ark
|
Docent onderzoeker B - Opleiding Fysiotherapie (0,7 FTE)
|
(Onbetaald) Lid projectteam bij het project: Deïmplementatie operatieve behandeling AchillesPeesruPtuur. Het bevorderen van gepaste zorg en terugdringen van ‘niet-gepaste zorg'.
|
Persoonlijke financiële belangen Geen.
Persoonlijke relaties Geen.
Extern gefinancierd onderzoek Geen.
Intellectuele belangen en reputatie Geen.
Overige belangen Geen.
|
Geen |
|
Dhr. dr. D.E. (Duncan) Meuffels
|
Orthopaedisch Chirurg en Universitair Hoofd Docent Erasmus MC (fulltime).
|
Voorzitter Nederlandse Orthopaedie Traumatologie en Sport Werkgroep (onbezoldigd)
Associate editor van British Journal of Sports Medicine
|
Persoonlijke financiële belangen Geen.
Persoonlijke relaties Geen.
Extern gefinancierd onderzoek Geen.
Intellectuele belangen en reputatie Geen.
Overige belangen Geen.
|
Geen |
|
Dhr. drs. T.E. (Ties) Maijs
|
Radioloog. |
Geen. |
Persoonlijke financiële belangen Geen. Persoonlijke relaties Geen.
Extern gefinancierd onderzoek Geen.
Intellectuele belangen en reputatie Geen.
Overige belangen Geen.
|
Geen.
|
|
Mevr. drs. L.N. (Lisanne) Hollander
|
Spoedeisende hulp arts KNMG. |
Lid van richtlijnen commissie NVSHA, onbetaald
|
Persoonlijke financiële belangen Geen.
Persoonlijke relaties Geen.
Extern gefinancierd onderzoek Geen.
Intellectuele belangen en reputatie Geen.
Overige belangen Geen.
|
Geen. |
|
Dhr. dr. R.J. (Robert Jan) de Vos
|
Sportarts en Universitair Hoofddocent, Erasmus MC Universitair Medisch Centrum Rotterdam (0.8 fte)
|
Associate editor British Journal of Sports Medicine (onbetaald) Werkgroeplid SKMS richtlijnen commissie (betaald)
|
Persoonlijke financiële belangen Geen.
Persoonlijke relaties Geen.
Extern gefinancierd onderzoek In de afgelopen 5 jaar zijn er onderzoeksprojecten uitgevoerd onder mijn supervisie die zijn gefinancierd door ReumaNederland, Annafonds, ZonMw, Maria SklodowskaCurie, GE Healthcare en de National Basketball Association (NBA). Deze financiers hebben echter geen belangen bij de aanbevelingen die zullen worden gedaan in deze richtlijn. Consultancy functie voor een project naar nieuwe injectie behandeling voor Achilles tendinopathie, gesponsord door Novartis.
Intellectuele belangen en reputatie Eén van de persoonlijke drijfveren om als werkgroeplid te fungeren in deze richtlijn is dat het meer expertise zal verschaffen en daardoor zal leiden tot een betere reputatie in het wetenschappelijke veld. Een neveneffect kan zijn dat het leidt tot
Overige belangen Geen.
|
Geen. |
|
Mw. drs. K. (Klaartje) Spijkers |
Senior Adviseur Patientenbelang bij Patientenfederatie Nederland.
|
Niet van toepassing. |
Persoonlijke financiële belangen Niet van toepassing.
Persoonlijke relaties Niet van toepassing.
Extern gefinancierd onderzoek Niet van toepassing.
Intellectuele belangen en reputatie Niet van toepassing.
Overige belangen Niet van toepassing. |
Geen. |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door het uitnodigen van de Patiëntenfederatie Nederland voor de schriftelijke knelpuntenanalyse en door een patiëntenvertegenwoordiger in de klankbordgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptmodules zijn tevens voor commentaar voorgelegd aan de Patiëntenfederatie Nederland en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Methode ontwikkeling
Evidence based
Implementatie
|
Aanbeveling |
Tijdspad voor implementatie: 1 tot 3 jaar of > 3 jaar |
Verwacht effect op kosten |
Randvoorwaarden voor implementatie (binnen aangegeven tijdspad) |
Mogelijke barrières voor implementatie1 |
Te ondernemen acties voor implementatie2 |
Verantwoordelijken voor acties3 |
Overige opmerkingen |
|
Alle aanbevelingen |
< 1 jaar |
Geen. |
Geen. |
Geen. |
Presenteren van de nieuwe richtlijn achillespeesruptuur tijdens congresdagen/traumadagen. Daarnaast kan er een verzoek worden ingediend voor het schrijven van een artikel in het NTvG. De laatste keer dat er een artikel in het NTvG is gepubliceerd m.b.t. achillespeesrupturen was in de 2009. Er vindt tevens een jaarlijks sport-medisch congres plaats waar de nieuwe richtlijn onder de aandacht gebracht kan worden. |
Wetenschappelijke verenigingen en de werkgroepleden van de huidige werkgroep achillespeesruptuur.
|
Geen. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten die een achillespeesruptuur ervaren. Tevens zijn er knelpunten aangedragen door middel van een schriftelijke knelpuntenanalyse. Een verslag hiervan is opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Algemene informatie
|
Richtlijn: NVvH Achillespeesruptuur |
|
|
Uitgangsvraag: Minimale invasieve chirurgische technieken versus open chirurgie
|
|
|
Database(s): Ovid/Medline, Embase |
Datum: 12-5-2022 |
|
Periode: 2000- |
Talen: nvt |
|
Literatuurspecialist: Ingeborg van Dusseldorp |
|
|
BMI zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Bij gebruikmaking van een volledig zoekblok zal naar de betreffende link op de website worden verwezen. |
|
|
Toelichting: Voor deze vraag is gezocht met de volgende elementen: Achillespeesruptuur EN minimale invasieve chirurgie |
|
|
Te gebruiken voor richtlijnen tekst: In de databases Embase en Ovid/Medline is op 12-5-2022 met relevante zoektermen gezocht naar systematische reviews en RCTs vanaf 2000 over minimale invasieve chirurgische technieken bij achillespeesruptuur . De literatuurzoekactie leverde 74 unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SRs |
31 |
29 |
28 |
|
RCTs |
24 |
39 |
46 |
|
Observationele studies |
|
|
|
|
Overig |
|
|
|
|
Totaal |
|
|
74 |
Zoekstrategie
Embase
|
No. |
Query |
Results |
|
#9 |
#8 NOT #7 RCT |
24 |
|
#8 |
#4 AND #6 |
41 |
|
#7 |
#4 AND #5 SR |
31 |
|
#6 |
'randomized controlled trial'/exp OR random*:ti,ab OR (((pragmatic OR practical) NEAR/1 'clinical trial*'):ti,ab) OR ((('non inferiority' OR noninferiority OR superiority OR equivalence) NEAR/3 trial*):ti,ab) OR rct:ti,ab,kw |
1908825 |
|
#5 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
823468 |
|
#4 |
#3 AND [1-1-2000]/sd NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
270 |
|
#3 |
#1 AND #2 |
316 |
|
#2 |
'minimally invasive procedure'/exp OR 'laparoscopy'/exp OR laparoscop*:ti,ab,kw OR ((minimal* NEAR/2 invasive):ti,ab,kw) |
385965 |
|
#1 |
'achilles tendon rupture'/exp OR (((achill* OR calcane*) NEAR/5 (rupture* OR tenorraph* OR tear*)):ti,ab,kw) OR (('achilles tendon'/exp OR achill*:ti,ab,kw OR calcane*) AND ('rupture'/exp OR rupture*:ti,ab,kw OR tear*:ti,ab,kw)) |
5940 |
Ovid/Medline
|
# |
Searches |
Results |
|
10 |
9 not 8RCT |
39 |
|
9 |
5 and 7 |
51 |
|
8 |
5 and 6 SR |
29 |
|
7 |
(exp randomized controlled trial/ or randomized controlled trials as topic/ or random*.ti,ab. or rct?.ti,ab. or ((pragmatic or practical) adj "clinical trial*").ti,ab,kf. or ((non-inferiority or noninferiority or superiority or equivalence) adj3 trial*).ti,ab,kf.) not (animals/ not humans/) |
1374211 |
|
6 |
(meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf.) not (comment/ or editorial/ or letter/ or ((exp animals/ or exp models, animal/) not humans/)) |
564192 |
|
5 |
4 not ((exp animals/ or exp models, animal/) not humans/) not (letter/ or comment/ or editorial/) |
424 |
|
4 |
limit 3 to yr="2000 -Current" |
449 |
|
3 |
1 and 2 |
459 |
|
2 |
exp Minimally Invasive Surgical Procedures/ or (minimal* adj2 invasive).ti,ab,kf. or laparoscop*.ti,ab,kf. |
665820 |
|
1 |
achilles tendon/in, pa, pp or ((exp *achilles tendon/ or achill*.ti,ab,kf. or Tendoachill*.ti,ab,kf. or calcane*.ti,ab,kf.) and (exp *rupture/ or exp *Tendon Injuries/ or rupture*.ti,ab,kf. or tear*.ti,ab,kf.)) or ((Achill* or Tendoachill* or calcane*) adj5 (rupture* or tenorraph* or tear*)).ti,ab,kf. |
7100 |
