Beeldvormende diagnostiek bij verdenking op een (partiële) supraspinatuspees ruptuur
Uitgangsvraag
Welke aanvullende beeldvormende diagnostiek heeft een meerwaarde voor het behandeltraject van SAPS?
Aanbeveling
Verricht echografie indien aanvullende beeldvorming is geïndiceerd bij patiënten met klinische verdenking op een (partiële dikte) ruptuur van de supraspinatuspees.
Overweeg MRI bij patiënten met klinische verdenking op een (partiële dikte) ruptuur van de supraspinatuspees als echografie niet beschikbaar of inconclusief is.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
De werkgroep heeft systematisch literatuuronderzoek verricht naar de diagnostische accuratesse van echografie in vergelijking met MRI om een partiële ruptuur van de supraspinatuspees te detecteren in patiënten met schouderpijn verdacht op het hebben van deze ruptuur, waarvoor zij een operatie (artroscopie) ondergingen. De operatie was hierbij de referentiestandaard. Het doel van dit literatuuronderzoek was onderzoeken of de diagnostische accuratesse van echografie voldoende is om te helpen sturen in de keuze voor conservatieve of operatieve therapie.
Alleen studies die echografie en MRI (en artroscopie als referentie standaard) in dezelfde populatie beoordeelden werden geïncludeerd in de literatuursamenvatting.
Voor de cruciale uitkomstmaten specificiteit, positief voorspellende waarde, foutpositieven en echt negatieven lijkt er geen verschil te zijn tussen echografie en MRI voor het detecteren van een partiële ruptuur van de supraspinatuspees. Ook voor de belangrijke uitkomstmaten sensitiviteit, negatief voorspellende waarde, foutnegatieven en echt positieven lijkt er geen verschil te zijn. Klinische uitkomsten werden niet gerapporteerd.
Er is voldoende wetenschappelijk onderzoek beschikbaar over het gebruik van echografie of MRI voor het aantonen van rotator cuff letsels, maar ook voldoende studies die MRI vergelijken met echografie voor het aantonen of uitsluiten van rotator cuff letsels.
Op basis van de literatuur kan voldoende zeker worden gesteld dat echografie, mits uitgevoerd door een professional met voldoende ervaring in de uitvoering hiervan en gebruikmakend van apparatuur die past in de huidige standaard van zorg (high-end echografie), gelijkwaardig is aan non-contrast MRI voor het aantonen en uitsluiten van supraspinatuspeesletsels.
Een vergelijking tussen echografie en MRI-arthrografie (MRA) valt buiten de zoekopdrachten van deze richtlijn. Een meta-analyse van DeJesus (2009) laat zien dat MRA superieur is aan echografie en non-contrast MRI met een sensitiviteit van 95% voor volledige dikte scheuren en 86% voor partiele dikte scheuren versus respectievelijk 92% en 64% voor non-contrast MRI en 92% en 67% voor echografie. De specificiteit van MRA is 99% voor volledige scheuren en 96% voor partiele scheuren versus 93% en 92% voor MRI en 94% en 94% voor echografie. Nadelen van MRA zijn het invasieve karakter waarbij er via een punctie contrast in het gewricht gebracht wordt, en de kans op een allergische reactie op het contrastmiddel. Daarnaast is MRA duurder en minder goed toegankelijk dan non-contrast MRI en belastender voor de patiënt. Wanneer een grote mate van zekerheid wordt vereist van de beeldvorming, bijvoorbeeld bij jonge, actieve patiënten die voor (top)sport of werk afhankelijk zijn van een goede schouderfunctie, moet MRA sterk worden overwogen.
Voor de beoordeling van vetinfiltratie in de spierbuiken van de rotatorcuff (voornamelijk de m. supraspinatus) is geen geschikte literatuur gevonden die echografie en MRI vergelijkt. Voor het beschrijven van de mate van vetinfiltratie is de Goutallier classificatie waarschijnlijk de bekendste (Goutallier, 1994). Deze is oorspronkelijk ontwikkeld voor CT onderzoeken, maar kan ook met de aanpassingen volgens Fuchs (1999) op MRI worden toegepast. De correlatie tussen CT en MRI voor de mate van vervetting is beperkt, door het vermogen van MRI om spierweefsel beter te onderscheiden van fibreus weefsel.
Deze vetinfiltratie kan ook met echografie worden beoordeeld, bijvoorbeeld met de techniek van Strobel (2005), waarbij de echogeniciteit en architectuur van de rotator-cuffspierbuiken worden vergeleken met de overliggende spieren. De correlatie tussen echografie en MRI is redelijk tot goed (Peeters, 2023). Dit levert echter beperkingen op wanneer de overliggende spieren ook afwijkend zijn, of wanneer de rotatorcuff spieren te diep liggen om goed te kunnen visualiseren. Dit is vooral een probleem bij de m. supraspinatus (Park, 2020), welke het vaakst betrokken is bij rotator cuff letsel. Het gebruik van shear-wave elastografie is inferieur aan MRI gebleken in recente onderzoeken (Peeters, 2023).
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Voor patiënten is het belangrijkste dat de beeldvorming een goed oordeel geeft. Aangezien de echografie ook een goede beoordeling geeft, er een lagere belasting is voor de patiënt, het onderzoek sneller is, minder contra-indicaties kent en claustrofobie geen probleem is, zullen patiënten een voorkeur voor echografie hebben. Daarnaast is echografie veel breder beschikbaar dan MRI.
Voor patiënten is het in ieder geval belangrijk dat meteen juist worden geïndiceerd en het juiste middel wordt ingezet, zodat patiënten niet met pijn nog een beeldvormend onderzoek moeten ondergaan.
Kosten (middelenbeslag)
Over het algemeen is MRI een duurder onderzoek dan echografie. Daarnaast kost MRI meer tijd, kent meer contra-indicaties, vereist duurdere apparatuur en in het geval van een MRA is de procedure ook meer invasief.
Aanvaardbaarheid, haalbaarheid en implementatie
Er zijn verschillende oorzaken voor het ontstaan van een subacromiaal pijn syndroom. Om aan te tonen of er een (partiele) ruptuur van de rotator cuff bestaat, is echografie zeer geschikt. Voorop bij het stellen van de diagnose staat echter het lichamelijk onderzoek. Indien er sprake is van instabiliteit van de schouder met secundaire subacromiaal pijn syndroom dan heeft een MRA de voorkeur boven echografie.
Echografie is breed beschikbaar en kan laagdrempelig uitgevoerd worden. Wel is het van belang dat de apparatuur van goede kwaliteit is en de professional ervaring heeft met het uitvoeren van dit onderzoek. Aan deze beide criteria zal in Nederland vrijwel overal kunnen worden voldaan. De werkgroep voorziet dan ook geen problemen met het implementeren van de aanbeveling.
Rationale van de aanbeveling: weging van argumenten voor en tegen de diagnostische procedure
Echografie heeft een diagnostische accuratesse die gelijk is aan MRI voor het aantonen en uitsluiten van supraspinatuspeesletsels. Gezien de goede beschikbaarheid van echografie, lagere kosten, lage belasting voor de patiënt en afwezigheid van significante contraindicaties, heeft dit de voorkeur als eerste modaliteit voor het aantonen of uitsluiten van supraspinatuspeesrupturen.
Bij een slechte beschikbaarheid van echografie, een inconclusief echografieonderzoek, discrepantie tussen kliniek en beeldvorming, of andere redenen waarom echografie niet mogelijk of wenselijk is, kan MRI worden ingezet.
Voor het beoordelen van vetinfiltratie verdient MRI de voorkeur, gezien de ruime ervaring op dit gebied. Bij contra-indicaties kan voor CT of echografie worden gekozen.
Onderbouwing
Achtergrond
The diagnosis of subacromial pain syndrome (SAPS) is made using clinical tests. An ultrasound or Magnetic Resonance Imaging (MRI) can be performed to assess whether there is underlying cuff pathology. The advantage of ultrasound examination over MRI is that it is readily available and inexpensive, and has a high specificity and sensitivity in the diagnosis of SAPS. When assessing the indication for rotator cuff repair surgery, it is important to also assess tendon and muscle retraction and degree of fatty infiltration of the rotator cuff. This can be assessed well with the MRI, but this is a burdensome and expensive examination.
Conclusies
Diagnostic accuracy outcomes
FP, TN, specificity and PPV (crucial outcomes)
|
Low GRADE |
The use of US may not differ in FP, TN, specificity and PPV compared to MRI in patients who are suspected to have a partial thickness tear in the supraspinatus tendon.
Source: Li, 2023; Zhu, 2022; Abd-ElGawad, 2013; Day, 2016; Elmorsy, 2017; Rutten, 2010; Sabharwal, 2019 |
FN, TP, sensitivity and NPV (important outcomes)
|
Low GRADE |
The use of US may not differ in FN, TP, sensitivity and NPV compared to MRI in patients who are suspected to have a partial thickness tear in the supraspinatus tendon.
Source: Li, 2023; McGuire, 2023; Zhu, 2022; Abd-ElGawad, 2013; Day, 2016; Elmorsy, 2017; Rutten, 2010; Sabharwal, 2019 |
Clinical outcomes (important outcomes)
|
No GRADE |
No evidence was found regarding whether the use of US results in differences in fatty infiltration, percentage tear rupture, and return to work or leisure when compared to MRI in patients who are suspected to have a partial thickness tear in the supraspinatus tendon.
Sources: - |
Samenvatting literatuur
Description of studies
All three studies examined the diagnostic accuracy of US and MRI in the preoperative diagnosis of partial thickness rupture with arthroscopy as the reference standard. Relevant study characteristics are shown in table 2.
Farooqi (2021) performed a SR and meta-analysis in which they evaluated the diagnostic accuracy of US for partial- and full-thickness rotator cuff tears and biceps tendon tears, and compared diagnostic values with those of MRI using arthroscopy as the reference standard. The literature search was performed up to January 1, 2010, and April 1, 2020. Five studies of the 23 included studies in de SR compared the diagnostic capability of US and MRI for partial supraspinatus tears using arthroscopy as the reference standard and were included in the current literature review (Abd-ElGawad, 2013; Day, 2016; Rutten, 2010; Sabharwal, 2019). The overall risk of bias among the included studies was low or unclear, with one study (Abd-ElGawad, 2013) exhibiting a high risk of bias in patient selection, and two studies (Abd-ElGawad, 2013; Elmorsy 2017) exhibiting >6 months of mean time between US and surgery.
Li (2023) performed a retrospective patient record study to explore the feasibility and diagnostic value of percutaneous US-guided subacromial bursography (PUSB) in evaluating rotator cuff tears. In total 78 patients with shoulder arthroscopic surgery and images of conventional US, MRI and PUSB were examined between July 2019 to October 2021. The risk of bias was unclear for blinding of the radiologists and surgeon.
McGuire (2023) performed a retrospective patient record study to compare the diagnostic sensitivity of ultrasound and MRI in the pre-operative diagnosis of partial thickness tears (PTT) and full thickness tears (FTT) of supraspinatus tendons compared to shoulder arthroscopy to assess if differences in detection rates exist. In total 103 patients that had a shoulder arthroscopic repair performed within 3 months of a positive supraspinatus tear diagnosed by both MRI and ultrasound were included (collected over
a period from August 2020 to August 2021). The risk of bias was unclear for blinding of the radiologists and surgeon.
Table 2 Study characteristics
|
First author, year |
design |
N, mean age (years) |
Selected cases |
Prevalence PTT |
Index and comparator |
Reference standard |
|
Farooqi, 2021 |
||||||
|
Abd-ElGawad, 2013 |
Retrospective study |
40, 55
|
partial supraspinatus tears |
13 (32.5%)
|
US (GE Logiq 5, 12 MHz)[operator: general radiologist]
1T MRI |
arthroscopy |
|
Day, 2016 |
Prospective study |
19, 55
|
partial supraspinatus tears |
7 (36.8%)
|
US [operator: surgeon]
MRI (not further specified) |
arthroscopy |
|
Elmorsy, 2017 |
Retrospective study |
125, 52
|
partial supraspinatus tears |
13 (10.4%)
|
US [operator: MSK radiologist]
1.5/ 3 T MRI |
arthroscopy |
|
Rutten, 2010 |
Retrospective study |
48, 68
|
partial supraspinatus tears |
9 (18.4%)
|
US [operator: MSK radiologist]
1.5 T MRI |
arthroscopy |
|
Sabharwal, 2019 |
Prospective study |
60, 45 |
partial supraspinatus tears |
20 (33.3%) |
US (GE Voluson P8, 7-12 MHz) [operator: general radiologist]
MRI (not further specified) |
arthroscopy |
|
Additional studies |
||||||
|
Li, 2023
|
Retrospective study |
78, 53.9 |
partial-thickness rotator cuf tears (supraspinatus tendon) |
42 (48%) |
US with a 6-18 MHz linear array probe (18L6).
1.5T MRI with a special coil for the shoulder joint.
|
shoulder arthroscopy performed by an associate chief physician with more than 10 years of shoulder arthroscopy experience |
|
McGuire, 2023 |
Retrospective study |
103, 64 |
partial thickness tears (PTT) of supraspinatus tendons |
40 (38.8%) |
US (10–15 MHz )[operator: general sonographers]
1.5-T/ 3 T MRI |
shoulder arthroscopic repair |
Results
The analyses were based on direct comparisons. The diagnostic accuracy measure outcomes for the tests are shown in Tables 3 and 4. The prevalence of partial thickness tears ranged from 18.4% to 38% (see Table 1).
FP, TN, specificity and PPV (Crucial outcomes)
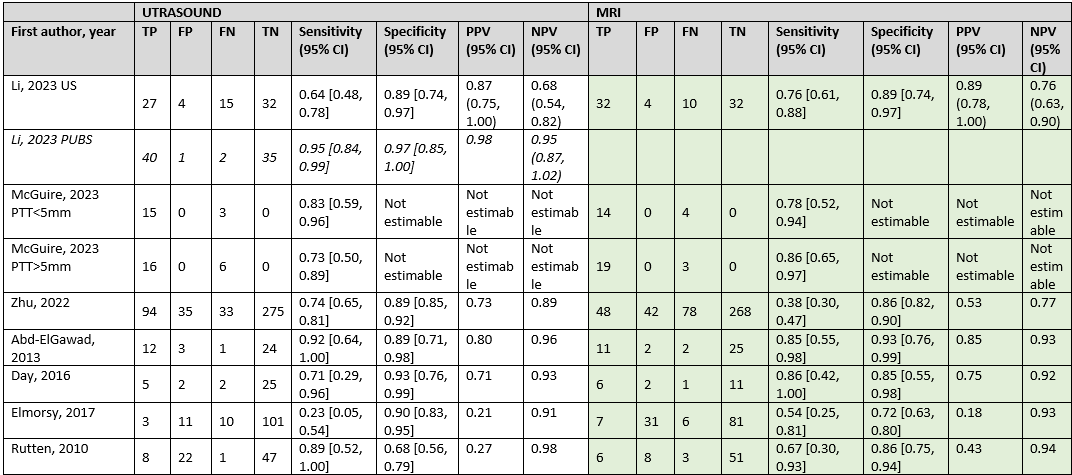
Seven studies investigated the specificity of US and MRI (Li, 2023; Zhu, 2022; Abd-ElGawad, 2013; Day, 2016; Elmorsy, 2017; Rutten, 2010; Sabharwal, 2019). The specificity for the use of US varied from 0.68 (95%CI 0.56 to 0.79) to 0.93 (95%CI 0.80 to 0.98). In the same study population, specificity for the use of MRI varied from 0.72 (95%CI 0.63 to 0.80) to 0.93 (95%CI 0.76 to 0.99). The PPV for the use of US varied from 0.21 to 0.92; compared to PPV for the use of MRI ranging from 0.18 to 0.89. The test with better values for specificity, number of FP, number of TN and PVV varied between the studies – but overall, the differences were small.
FN, TP, sensitivity and NPV (Important outcomes)
All studies investigated the sensitivity of US and MRI. The sensitivity for the use of US varied from 0.23 (95%CI 0.05 to 0.54) to 0.95 (95%CI 0.75 to 1.00). In the same study population, sensitivity for the use of MRI varied from 0.38 (95%CI 0.30 to 0.47) to 0.86 (95%CI 0.42 to 1.00). The NPV for the use of US varied from 0.68 to 0.98; compared to NPV for the use of MRI ranging from 0.76 to 0.94. The test with better values for sensitivity, number of FN, number of TP and NPV varied between the studies – but overall, the differences were small.
Table 3. Diagnostic accuracy ultrasound
|
First author, year |
TP |
FP |
FN |
TN |
Sensitivity (95% CI) |
Specificity (95% CI) |
PPV (95% CI) |
NPV (95% CI) |
|
Li, 2023 US |
27 |
4 |
15 |
32 |
0.64 [0.48, 0.78] |
0.89 [0.74, 0.97] |
0.87 (0.75, 1.00) |
0.68 (0.54, 0.82) |
|
McGuire, 2023 PTT<5mm |
15 |
0 |
3 |
0 |
0.83 [0.59, 0.96] |
Not estimable |
Not estimable |
Not estimable |
|
McGuire, 2023 PTT>5mm |
16 |
0 |
6 |
0 |
0.73 [0.50, 0.89] |
Not estimable |
Not estimable |
Not estimable |
|
Zhu, 2022 |
94 |
35 |
33 |
275 |
0.74 [0.65, 0.81] |
0.89 [0.85, 0.92] |
0.73 |
0.89 |
|
Abd-ElGawad, 2013 |
12 |
3 |
1 |
24 |
0.92 [0.64, 1.00] |
0.89 [0.71, 0.98] |
0.80 |
0.96 |
|
Day, 2016 |
5 |
2 |
2 |
25 |
0.71 [0.29, 0.96] |
0.93 [0.76, 0.99] |
0.71 |
0.93 |
|
Elmorsy, 2017 |
3 |
11 |
10 |
101 |
0.23 [0.05, 0.54] |
0.90 [0.83, 0.95] |
0.21 |
0.91 |
|
Rutten, 2010 |
8 |
22 |
1 |
47 |
0.89 [0.52, 1.00] |
0.68 [0.56, 0.79] |
0.27 |
0.98 |
|
Sabharwal, 2019 |
19 |
3 |
1 |
37 |
0.95 [0.75, 1.00] |
0.93 [0.80, 0.98] |
0.86 |
0.97 |
CI = confidence interval; FN = false negatives; FP = false positives; NPV = negative prediction value; NR = not reported; TN = true negatives; TP = true positives; PPV = positive prediction value
Table 4. Diagnostic accuracy MRI
|
First author, year |
TP |
FP |
FN |
TN |
Sensitivity (95% CI) |
Specificity (95% CI) |
PPV (95% CI) |
NPV (95% CI) |
|
Li, 2023 |
32 |
4 |
10 |
32 |
0.76 [0.61, 0.88] |
0.89 [0.74, 0.97] |
0.89 (0.78, 1.00) |
0.76 (0.63, 0.90) |
|
McGuire, 2023 PTT<5mm |
14 |
0 |
4 |
0 |
0.78 [0.52, 0.94] |
Not estimable |
Not estimable |
Not estimable |
|
McGuire, 2023 PTT>5mm |
19 |
0 |
3 |
0 |
0.86 [0.65, 0.97] |
Not estimable |
Not estimable |
Not estimable |
|
Zhu, 2022 |
48 |
42 |
78 |
268 |
0.38 [0.30, 0.47] |
0.86 [0.82, 0.90] |
0.53 |
0.77 |
|
Abd-ElGawad, 2013 |
11 |
2 |
2 |
25 |
0.85 [0.55, 0.98] |
0.93 [0.76, 0.99] |
0.85 |
0.93 |
|
Day, 2016 |
6 |
2 |
1 |
11 |
0.86 [0.42, 1.00] |
0.85 [0.55, 0.98] |
0.75 |
0.92 |
|
Elmorsy, 2017 |
7 |
31 |
6 |
81 |
0.54 [0.25, 0.81] |
0.72 [0.63, 0.80] |
0.18 |
0.93 |
|
Rutten, 2010 |
6 |
8 |
3 |
51 |
0.67 [0.30, 0.93] |
0.86 [0.75, 0.94] |
0.43 |
0.94 |
|
Sabharwal, 2019 |
17 |
3 |
3 |
37 |
0.85 [0.62, 0.97] |
0.93 [0.80, 0.98] |
0.85 |
0.93 |
CI = confidence interval; FN = false negatives; FP = false positives; NPV = negative prediction value; NR = not reported; TN = true negatives; TP = true positives; PPV = positive prediction value
Fatty-infiltration (important outcome)
Not reported
Percentage tear rupture (important outcome)
Not reported
Return to work or leisure (important outcome)
Not reported
Level of evidence of the literature
FP, TN, specificity and PPV (crucial outcomes)
The level of evidence regarding the outcome measures FP, TN, specificity and PPV was downgraded by two levels because of study limitations (risk of bias, -1) and limited number of included patients (imprecision, -1).
FN, TP, sensitivity and NPV (important outcomes)
The level of evidence regarding the outcome measures FN, TP, sensitivity and NPV was downgraded by two levels because of study limitations (risk of bias, -1) and limited number of included patients (imprecision, -1).
Clinical outcomes: fatty-infiltration and percentage tear rupture, return to work or leisure (important outcomes)
The level of evidence regarding fatty-infiltration,percentage tear rupture, and return to work or leisure could not be determined due to a lack of data.
Table 5. Overview of study results
Zoeken en selecteren
A systematic review of the literature was performed to answer the following question:
What is the value of ultrasonography versus MRI in patients who are suspected to have a partial thickness tear in the supraspinatus tendon?
Relevant outcome measures
The guideline development group considered FP, specificity and PPV as critical outcome measures for decision making; and FN, sensitivity, NPV, TP, and TN, fatty-infiltration, percentage tear rupture, and return to work or leisure as important outcome measures for decision making.
The guideline development group defined a difference of 10% in specificity and PPV and a difference of 100 per 1000 patients in FP and 200 per 1000 FN as a minimal clinically (patient) important difference.
For the clinical outcomes fatty-infiltration, percentage tear rupture, and return to work or leisure, a difference of 25% was considered clinically relevant (RR≤0.8 or RR≥1.25).
Table 1 Consequences of diagnostic test characteristics
|
Outcome |
Consequences |
Relevance |
|
Positive prediction value (PPV) |
Proportion of patients who are justifiably not diagnosed with partial thickness tear in the supraspinatus or subscapulair tendon |
Crucial |
|
False positives (FP), low specificity |
Patients are unjustifiably diagnosed with partial thickness tear in the supraspinatus or subscapulair tendon; giving treatment is unjustified |
Crucial |
|
True positives (TP), high sensitivity |
Patients are justifiably diagnosed partial thickness tear in the supraspinatus or subscapulair tendon; giving treatment is justified |
Important |
|
True negatives (TN), high specificity |
Patients are justifiably not diagnosed with partial thickness tear in the supraspinatus or subscapulair tendon; not giving treatment is justified |
Important |
|
False negatives (FN), low sensitivity |
Patients are unjustifiably not diagnosed with partial thickness tear in the supraspinatus or subscapulair tendon; not giving treatment is unjustified |
Important |
|
Negative prediction value (NPV) |
Proportion of patients who are unjustifiably not diagnosed with partial thickness tear in the supraspinatus or subscapulair tendon |
Important |
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms until 06-06-2023. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 639 hits. Studies were selected based on the following criteria:
- Systematic reviews, RCTs or observational studies
- Publication date ≥ 2010 (due to advancement in techniques)
- Patients with suspected partial thickness rupture tear in the supraspinatus tendon
- Ultrasound, MRI in the same population
- Using current standard of care (non-handheld) ultrasound devices
- Arthroscopy as reference standard
- Reporting one or more of the following diagnostic accuracy measures: false negatives (FN), sensitivity, negative prediction value (NPV), false positives (FP), true positives (TP), true negatives (TN), specificity, positive prediction value (PPV) Diagnostic values as outcome measures
Twenty-nine studies were initially selected based on title and abstract screening. After reading the full text, 26 studies were excluded (see the table with reasons for exclusion under the tab Methods), and three studies were included.
Results
Three studies (one systematic reviews and two additional observational studies) were included in the analysis of the literature. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
Referenties
- de Jesus JO, Parker L, Frangos AJ, Nazarian LN (2009) Accuracy of MRI, MR arthrography, and ultrasound in the diagnosis of rotator cuff tears: a meta-analysis. AJR Am J Roentgenol 192(6):1701-1707
- Farooqi AS, Lee A, Novikov D, Kelly AM, Li X, Kelly JD 4th, Parisien RL. Diagnostic Accuracy of Ultrasonography for Rotator Cuff Tears: A Systematic Review and Meta-analysis. Orthop J Sports Med. 2021 Oct 11;9(10):23259671211035106. doi: 10.1177/23259671211035106. PMID: 34660823; PMCID: PMC8511934.
- Fuchs B, Weishaupt D, Zanetti M et al (1999) Fatty degeneration of the muscles of the rotator cuff: assessment by computed tomography versus magnetic resonance imaging. J Shoulder Elbow Surg 8:599-605. https://doi.org/10.1016/s1058-2746(99)90097-6
- Goutallier D, Postel JM, Bernageau J, Lavau L, Voisin MC. Fatty muscle degeneration in cuff ruptures. Pre- and postoperative evaluation by CT scan. Clin Orthop Relat Res. 1994 Jul;(304):78-83. PMID: 8020238.
- Li R, Li M, Cui Y, Yang P, Zhang C. The value of percutaneous ultrasound-guided subacromial bursography in the diagnosis of rotator cuff tears. Med Ultrason. 2023 Mar 30;25(1):48-55. doi: 10.11152/mu-3913. PMID: 36996393.
- McGuire LB, Quinton AE, Cossetto DJ, Hanchard TJ, Spurway JF, Quinton AE. Diagnostic sensitivity of ultrasound of the supraspinatus tendon when compared to magnetic resonance imaging prior to arthroscopy: A retrospective study. Sonography. 2023 Mar 18; 10(2):51-56. doi:10.1002/sono.12348
- Park BK, Hong SH, Jeong WK. Effectiveness of Ultrasound in Evaluation of Fatty Infiltration in Rotator Cuff Muscles. Clin Orthop Surg. 2020 Mar;12(1):76-85. doi: 10.4055/cios.2020.12.1.76. Epub 2020 Feb 13. PMID: 32117542; PMCID: PMC7031432.
- Peeters, N.H.C., van der Kraats, A.M., van der Krieken, T.E. et al. The validity of ultrasound and shear wave elastography to assess the quality of the rotator cuff. Eur Radiol 34, 1971-1978 (2024). https://doi.org/10.1007/s00330-023-10037-z
- Rutten MJ, Spaargaren GJ, van Loon T, de Waal Malefijt MC, Kiemeney LA, Jager GJ. Detection of rotator cuff tears: the value of MRI following ultrasound. Eur Radiol. 2010 Feb;20(2):450-7. doi: 10.1007/s00330-009-1561-9. Epub 2009 Sep 2. PMID: 19727754; PMCID: PMC2814028.
- Strobel K, Hodler J, Meyer DC, Pfirrmann CW, Pirkl C, Zanetti M. Fatty atrophy of supraspinatus and infraspinatus muscles: accuracy of US. Radiology. 2005;237(2):584-589.
Evidence tabellen
|
Study reference |
Study characteristics |
Patient characteristics
|
Index test (test of interest) |
Reference test
|
Follow-up |
Outcome measures and effect size |
Comments |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Farooqi, 2021
PS., study characteristics and results are extracted from the SR (unless stated otherwise: * indicates data was extracted from individual studies) |
SR and meta-analysis
Literature search up to January 1, 2010, and April 1, 2020
Five studies of the 23 included studies in de SR compared the diagnostic capability of US and MRI for partial supraspinatus tears using arthroscopy as the reference standard and were included:
B: Day (2016)10 C: Elmorsy (2017)15 D: Rutten (2010)48 E: Sabharwal (2019)50
Study design: cohort, case-control [prospective / retrospective]
A: Abd-ElGawad (2013)2 B: Day (2016)10 C: Elmorsy (2017)15 D: Rutten (2010)48 E: Sabharwal (2019)50
Setting and Country: USA
Source of funding and conflicts of interest: One or more of the authors has declared the following potential conflict of interest or source of funding: X.L. has received consulting fees and royalties from FH Ortho. J.D.K. has received consulting fees from Flexion and royalties from SLACK and Springer. R.L.P. has received grant/educational support from Arthrex. AOSSM checks author disclosures against the Open Payments Database (OPD). AOSSM has not conducted an independent investigation on the OPD and disclaims any liability or responsibility relating thereto.
|
Inclusion criteria SR: studies that evaluated the diagnostic accuracy of US in rotator cuff tears utilizing arthroscopy as the reference standard
Exclusion criteria SR: review articles, meta-analyses, systematic reviews, case reports, cadaveric studies, non-English text, studies with <10 patients, studies including massive tears without reporting diagnostic data for specific tendons, and studies lacking diagnostic outcome data.
Important patient characteristics:
N, mean age A: 40, 55 yrs B: 19, 55 yrs C: 125, 52 yrs D: 48, 68 yrs E: 60, 45 yrs |
Index (1) and comparator tests (2)* and cut-off point(s):
A-1: US (GE Logiq 5, 12 MHz); cut-off NA [operator: general radiologist] A-2: MRI, cut-off NA MRI examinations were performed with a 1TMR Imagingunit(Intera, Philips Medical Systems, NeberlandB.V) and one surface coil was used
B-1: US; cut-off NA [operator: surgeon] B-1: MRI, cut-off NA (MRI details/transducer not reported)
C-1: US; cut-off NA [operator: MSK radiologist] C-2: MRI, cut-off NA MRI scans were performed using 1.5 or 3 Tesla MRI scanners
D-1: US; cut-off NA [operator: MSK radiologist] D-2: MRI, cut-off NA All MRI examinations were performed with an 1.5-T MR system (Signa Horizon, GE, ‘s-Hertogenbosch, The Netherlands).
E-1: US (GE Voluson P8, 7-12 MHz); cut-off NA [operator: general radiologist] E-2: MRI, cut-off NA (MRI details/transducer not reported) |
Reference test and cut-off point(s):
A: arthroscopy; cut-off NR B: arthroscopy; cut-off NR C: arthroscopy; cut-off NR D: arthroscopy; cut-off NR E: arthroscopy; cut-off NR
Prevalence partial thickness cuff tear (PPT) (%)* [based on refence test at specified cut-off point] A: 13 (32.5%) B: 7 (36.8%) C: 13 (10.4%) D: 9 (18.4%) E: 20 (33.3%)
For how many participants were no complete outcome data available? N (%) A: NR B: NR C: NR D: NR E: NR
Reasons for incomplete outcome data described? A: NR B: NR C: NR D: NR E: NR
|
Endpoint of follow-up: A: NR B: NR C: NR D: NR E: NR
|
TP/FP/FN/TN*: A:
B:
C:
D:
E:
Sensitivity/ specificity/ diagnostic accuracy-1/2* A-1: 92.3%/ 92.6%/ 92.5% A-2: 84.6%/ 92.6%/ 90%
B-1: 0.71/1.00/ 74% B-2: 1.00/ 1.00/ 100% But for all tears, no distinction in partial/ full tears à own calculations
C-1: 23%/ 90.1% C-2: 54.1% (P=0.333) / 72.6% (P=0.0008)
D-1: 89% [52%-100%]/ 80% [67%-89%]/ 81% [70%-89%] D-2: 67% [30%-93%]/ 86% [75%-94%]/ 84% [73%-92%]
E-1: 95.0%/ 92.5%/ 93.3% E-2: 85.0%/ 92.5%/ 90.0%
US median sensitivity 0.89 US median specificity 0.89 MRI median sensitivity 0.85 MRI median specificity 0.87
Pooled characteristics: sensitivity = –2.36 [95% CI, –21.51 to 16.79], P = .81 specificity = 4.30 [95% CI, –7.06 to 15.66], P = .46 diagnostic accuracy = 5.25 [95% CI, –1.60 to 12.10], P = .13
Heterogeneity (reasons): No significant heterogeneity was observed among the studies in US and MRI diagnostic outcomes when evaluating partial-thickness tears (I2 = 0%-41%; P = 0.15-0.50)
PPV/NPV-1/2* A-1: NR (own calculations) A-2: NR (own calculations)
B-1: 1.00/ 0.29 B-2: 1.00/ 1.00
C-1: 21.4%/ 90.9% C-2: 30.9% (p=0.73) / 87.5% (p=0.48)
D-1: 40% [19%-64%]/ 98% [89%-100%] D-2: 43% [18%-71%]/ 94% [85%-99%]
E-1: 86.4%/ 97.4% E-2: 85.0%/ 92.5% |
Study aim: To evaluate the diagnostic accuracy of US for partial- and full-thickness rotator cuff tears and biceps tendon tears, compare diagnostic values with those of magnetic resonance imaging (MRI) using arthroscopy as the reference standard, assess longitudinal improvements in accuracy, and compare diagnostic values from operators with different training backgrounds.
Study quality (ROB): The quality and risk of bias for each included study was assessed by 2 authors (A.S.F. and A.L.) using the Quality Assessment of Diagnostic Accuracy Studies–2 (QUADAS-2) Tool across 4 domains (For each domain, studies were assigned a score of low (low risk of bias or low concern regarding applicability), unclear, or high (high risk of bias or high concern regarding applicability).):
Patient selection A: high B: low C: low D: low E: low
Index test – US A: unclear B: low C: unclear D: low E: low
Index test – MRI A: unclear B: low C: unclear D: NA E: low
Reference standard A: unclear B: low C: unclear D: low E: low
Flow and Timing A: high B: unclear C: high D: unclear E: unclear
Place of the index test in the clinical pathway: add-on (MRI after US)
Choice of cut-off point: visual via operation
Brief description of author’s discussion/ conclusion: “This study demonstrated that US is highly sensitive and specific in the diagnosis of supraspinatus tears and is more accurate in the diagnosis of full-thickness tears as compared to partial-thickness tears.”
“[..] US demonstrated a lower median sensitivity and specificity for partial thickness tears, at 0.65 and 0.86, respectively. In support of these findings, 1 study reported that diagnostic accuracy increased with tear size for full-thickness supraspinatus tears.9 One proposed contributing factor to the lower US sensitivity realized for partial-thickness tears may be the variable echogenicity of synovial proliferation, granulation, and scar tissue formation surrounding a partial tear, thus impeding clear tissue differentiaiton.40 Because of the lower US sensitivity for partial-thickness tears, it has been recommended to follow a negative US examination with an MRI in patients who do not experience symptomatic relief following conservative treatment.53 We propose a similar diagnostic US screening algorithm shown in Figure 5.” |
*comparator test equals the C of the PICO; two or more index/ comparator tests may be compared; note that a comparator test is not the same as a reference test (golden standard)
|
Study reference |
Study characteristics |
Patient characteristics
|
Index test (test of interest) |
Reference test
|
Follow-up |
Outcome measures and effect size |
Comments |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Li, 2023 |
Type of study: retrospective study; to explore the feasibility and diagnostic value of percutaneous US-guided subacromial bursography (PUSB) in evaluating rotator cuff tears
Setting and country: single-centre, China
Funding and conflicts of interest: Funding: NR; Conflict of interest: none |
Inclusion criteria: : 1) having complete clinical, US, MRI and PUSB data; 2) underwent shoulder arthroscopy surgery.
Exclusion criteria: 1) having incomplete imaging data; 2) patients unsuitable for PUSB examination; 3) patients who have already undergone previous surgery on the shoulder area
N=Seventy-eight patients with shoulder arthroscopic surgery and images of conventional US, MRI and PUSB examined in our department between July 2019 to October 2021.
Prevalence: 42 cases of PTTs (48%)
Mean age (range): mean age 53.9±9.1 years; age range, 31-70 years
Sex: 32 males, 46 females |
Index test 1: US US and PUSB examinations were performed using SIEMENS ACUSON Sequoia (Siemens Medical Solu_tions, USA). US examination was performed with a 6-18 MHz linear array probe (18L6). The patient was seated and facing the operator, who performs the procedure according to the shoulder US technical guidelines recommended by the European Society of Musculoskeletal Radiology [15]. The biceps long-head tendon, subscapularis tendon, supraspinatus tendon, infraspinatus and teres minor tendons were examined successively. Transverse and longitudinal images were performed, and the dynamic and static images were retained.
Index test 2: a 4-10 MHz linear array probe (10L4) was used to perform PUSB. The tip of the needle was directed into the subacromial bursa and the contrast agent was slowly injected. At the same time, the probe was rotated to observe the distribution of contrast agent in the bursa and tendon. Typical images were captured and stored during the inspection for recording and analysis. After the examination, the puncture site was disinfected and covered with a sterile dressing.
Comparator test: MRI MRI was performed with 1.5 T superconducting MRI equipment from the German Siemens Magnetom Avanto, equipped with a special coil for the shoulder joint. For coronal section scanning, the scanning plane was perpendicular to the glenoid cavity and ranged from the acromion to subscapular humerus with a fast-spin echo T2-weighted sequence (TR/TE=2200 ms/84 ms) and a spin echo T1 weighted sequence (TR/TE=450 ms/16 ms). For oblique coronal scanning, the scanning plane was parallel to the long axis of the supraspinatus muscle and ranged from the outer end of the clavicle to the ac_romion with rapid spin echo T2-weighted imaging (TR/ TE= 2370 ms/39 ms). The scanning parameters were as follows: a FOV = 20 cm×20 cm; a matrix =257×192; a layer thickness =4 mm; and a layer spacing = 4.8 mm.
Cut-off point(s): Diagnostic criteria
MRI: (1) Full-thickness tear: the supraspinatus tendon was thickened and twisted, with a high signal involving the whole layer. (2) Partial-thickness tear: the supraspinatus tendon was irregular in shape, with a focal high signal, and the whole layer is not involved [16,17].
US: (1) Full-thickness tear: (i) a hypoechoic defect extends from the bursal to the articular sides; (ii) local defects involving both the bursal and articular sides in the short-axis and long-axis views; and (iii) the rotatorcuff not visible due to extensive full-thickness tears and retraction below the acromion. (2) Partial-thickness tear: (i) an obvious hypoechoic defect area or a discontinuous area on the bursal or articular sides of the tendon is pre_sent; (ii) focal hypoechoic defects within the tendon are seen in the longitudinal and transverse planes [18]. (3) No tear (NTs): a normal subacromial-subdeltoid bursa (SASD) appeared as a hypoechoic line between two hy_perechoic planes, with total thickness of less than 2 mm [12].
PUSB: (1) Full-thickness tear: the contrast agent leaks from the defect area of the bursal side through the supraspinatus into the articular side. (2) Partial-thickness tear: for the part of bursal-side tears, PUSB shows that the contrast agent filled the bursal-side tear part and the contrast agent flows from the subacromial bursa to the bursal-side tears area in the PUSB dynamic imaging. For the intratendinous or articular side partial-thickness tears, the contrast agent can be observed in tendons or from tendons to the articular side by injecting it into the area of the suspected tendon lesion directly. (3) No tear: the contrast agent is scattered only in the subacromial bursa, outlines the regular surface of the rotator cuff, and does not leak into the rotator cuff.
|
Reference test: shoulder arthroscopy performed by an associate chief physician with more than 10 years of shoulder arthroscopy experience
Cut-off point(s): diagnostic criteria
the types of rotator cuff tears were classified as full-thickness tears, partial-thickness tears and no tears according to whether there were any rotator cuff defects and the location and size of defects.
|
Time between the index test and reference test: NR
For how many participants were no complete outcome data available? N (%): NR, it was an exclusion criterium
Reasons for incomplete outcome data described? NR, it was an exclusion criterium |
TP/FP/FN/TN*:
Sensitivity: US: 64.3 (49.17,79.40) PUBS: 95.2 (88.52,101.95) MRI: 76.2 (62.76,89.62)
Specificity: US: 88.9 (78.10,99.67) PUBS: 97.2 (91.58,102.86) MRI: 88.9 (78.10,99.67)
PPV: US: 87.1 (74.60,99.60) PUBS: 97.6 (92.63,102.49) MRI: 88.9 (78.10,99.67)
NPV: US: 68.1 (54.25,81.92) PUBS: 94.6 (86,95,102.24) MRI: 76.2 (62.76,89.62)
|
Author conclusion: In conclusion, PUSB is highly accurate, sensitive, and specific for the diagnosis of rotator cuff tears. At the same time, PUSB can be used to dynamically observe the rotator cuff tears in a timely manner. When patients have MRI contraindications or MRI cannot accurately deter_mine the types of rotator cuff tears, PUSB can be used for auxiliary diagnosis with decreased cost and increased efficiency, making this method a good choice for patients in urgent need of surgery. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
McGuire, 2023 |
Type of study: retrospective, quantitative study with data collected from participants' medical records; to compare the diagnostic sensitivity of USS and MRI in the pre-operative diagnosis of partial thickness tears (PTT) and full thickness tears (FTT) of supraspinatus tendons compared to gold-standard shoulder arthroscopy to assess if differences in detection rates exist.
Setting and country: single-centre, Australia
Funding and conflicts of interest: Funding: NR; Conflict of interest: Ann Quinton is an editorial board member for Sonography and a coauthor on this article. Other declare no conflict of interest. |
Inclusion criteria: NR
Exclusion criteria: those who had a longer than 3-month period between diagnosis and arthroscope, and whose pathology was unrelated to the supraspinatus tendon and participants aged less than 18 years.
N= One hundred and three participants who had arthroscopic shoulder repair had their data reviewed comparing the diagnostic accuracy of pre-operative USS and MRI with arthroscopy used as gold standard. Overall, there were 63 FTT and 40 PTT diagnosed by arthroscopy. Prevalence PTT: 40 (38.8%)
Mean age (SD): 64 (10.8) years.
Sex: 63 males, 40 females |
Index test: US Ultrasounds were performed by general sonographers. Ultrasound machines involved in the study included Philips Epiq5, Canon Aplio 500, and General Electric Logiq E9. These machines are equipped with high frequency linear probes in the range of 10–15 MHz appropriate for musculoskeletal scanning.
Comparator test: MRI The MRI machines in this study included a Philips Ingenia 1.5 T, Philips Ingenia 3.T and a Siemens Magnetom 1.5 T. One orthopaedic practice was used to collate the data where there are two orthopaedic surgeons.
Cut-off point(s): Data were analysed reporting on number of supraspinatus tears reported as sensitivity (true positive case) for USS and MRI and categorised into 1. number and sensitivity of partial thickness tears <than 5 mm 2. number and sensitivity of partial thickness tears >than 5 mm 3. number and sensitivity of full thickness tears
|
Reference test: shoulder arthroscopic repair Cut-off point(s): NR
|
Time between the index test and reference test: NR For how many participants were no complete outcome data available? N (%): NR
Reasons for incomplete outcome data described? NR
Specificity could not be calculated as people with negative results did not present for surgery. |
TP/FP/FN/TN*:
Partial thickness tear <5 mm
Sensitivity: US: 83.3% MRI: 77.7%
Partial thickness tear >5 mm
Sensitivity: US: 73.3% MRI: 86.4%
|
Author conclusion: Advances in USS shoulder imaging due to increased spatial resolution has revolutionised shoulder imaging over the last 20 years. This study indicates substantial agreement for supraspinatus tear diagnosis when comparing MRI to USS performed in general imaging departments. Given USS is less expensive and more available, it could be considered as a first line screening tool when the main question is one of tendon integrity. However, where the patient has significant underlying osteoarthritis, MRI should be included in the imaging workup prior to surgery. As technology continues to improve with ultra-high frequency ultrasound probes, further studies to assess accuracy of supraspinatus tear detection should be evaluated, the assumption is that in future, USS will have the capacity to serve as a stand-alone diagnostic tool in accurately assessing supraspinatus tears prior to arthroscopy. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Zhu, 2022 |
Type of study: prospective diagnostic accuracy study; to evaluate the diagnostic reliability of ultrasonography (US) and magnetic resonance imaging (MRI) for subscapularis (SSC) tears with shoulder arthroscopy as the gold standard and to investigate the diagnostic value of 2 MRI signs (lesser tuberosity cysts and subcoracoid cysts) for SSC tears.
Setting and country: single-centre, China
Funding and conflicts of interest: The authors report the following potential conflicts of interest or sources of funding: this work was supported by grant from Chongqing medical scientific research project (No. 2021MSXM032). Full ICMJE author disclosure forms are available for this article online, as supplementary material. |
Inclusion criteria: (1) patients who were diagnosed with RCTs by physical examination, US, and MRI; and (2) preoperative MRI scans and US were performed within 3 months of the arthroscopic shoulder procedures.
Exclusion criteria: (1) patients with previous shoulder surgery or shoulder fracture; (2) recurrent shoulder instability; and (3) systemic inflammatory disease.
N=437 (consecutive patient selection jan 2019- dec 2020)
Prevalence articular-side partial-thickness SSC tears: 126 (29%)
Mean age ± SD:
Sex: % M / % F
Other important characteristics:
|
Index test: real-time US scanner (HI Vision Ascendus, Hitachi Medical, Japan) and linear-array transducer with a frequency of 12 to 18 MHz by a single experienced sonographer who specialized in musculoskeletal US.
Cut-off point(s): NR
Comparator test: MRI was performed using 1.5-T MRI equipment (Magnetom Essenza; Siemens Healthcare, Erlangen, Germany) with a dedicated shoulder coil.
Cut-off point(s): NR
|
Reference test: Diagnostic Shoulder Arthroscopy
Cut-off point(s): NR
|
Time between the index test en reference test: < 3 months
For how many participants were no complete outcome data available? N (%): NR
Reasons for incomplete outcome data described? NR |
Sensitivity: US: 73.8% [65.5%-80.7%] (93/126) MRI: 38.1% [29.7%-47.2%] (48/126)
Specificity: US: 88.7% [84.8%-91.8%] (276/311) MRI: 86.5% [82.3%-89.9%] (269/311)
Accuracy: US: 84.4% [80.7%-87.5%] (369/437) MRI: 72.5% [68.2%-76.5%] (317/437)
PPV: US: 72.7% [65.5%-80.7%] (93/128) MRI: 53.3% [43.1%-63.3%] (48/90)
NPV: US: 89.3% [85.4%-92.3%] (276/309) MRI: 77.5% [72.8%-81.6%] (269/347)
|
Author conclusion: The most important finding of the present study was that the diagnostic accuracy of US was significantly better than that of MRI for SSC tears. The data suggested that 1.5-T MRI was not quite reliable for diagnosing partial-thickness SSC tears, the sensitivity of which was only 38.1%, whereas a standardized and systematic US evaluation could provide much superior reliability, with 73.8% sensitivity and 88.7% specificity. |
Risk of bias tabellen
Table of quality assessment for systematic reviews of diagnostic studies
Based on AMSTAR checklist (Shea et al.; 2007, BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher et al 2009, PLoS Med 6: e1000097; doi:10.1371/journal.pmed1000097)
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Assessment of scientific quality of included studies?5
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?6
Yes/no/unclear |
Potential risk of publication bias taken into account?7
Yes/no/unclear |
Potential conflicts of interest reported?8
Yes/no/unclear |
|
Farooqi, 2021 |
Yes,
Purpose: To evaluate the diagnostic accuracy of US for partial- and full-thickness rotator cuff tears and biceps tendon tears, compare diagnostic values with those of magnetic resonance imaging (MRI) using arthroscopy as the reference standard |
Yes,
This systematic review was done in accordance with PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses) guidelines. The PubMed and Cochrane Library databases were systematically searched for full-text journal articles in English published in the past 10 years, between January 1, 2010, and April 1, 2020. The search strings are shown in Appendix Table A1. Previous systematic reviews identified via the PubMed and Cochrane Library search were also assessed for relevant studies. These studies were also considered for inclusion in this systematic review. |
Yes,
A total of 804 articles were identified from the initial PubMed and Cochrane Library database search (Figure 1). An additional 367 studies were considered because of inclusion in relevant systematic reviews identified during the database search. Of the 1171 total studies reviewed, 1113 were excluded based on title and abstract, while 58 were further assessed for eligibility. Of these studies, 15 did not use arthroscopy as the reference standard, 4 were not in English, 2 included massive tears, and 4 lacked sufficient outcome data. After the removal of duplicates, 23 eligible studies involving 2054 shoulders were included in this systematic review.
And figure with study screening and selection process. |
Yes, table 1
|
Yes,
Use of the g the Quality Assessment of Diagnostic Accuracy Studies–2 (QUADAS-2) Tool and funnel plots for assessment of publication bias in RevMan.
Results of the Quality Assessment of Diagnostic Accuracy Studies–2 quality and bias assessment presented in figure 2 (see copied figure below this table). |
Yes, in accordance with predefined inclusion criteria |
Yes (see column 6) |
Yes,
One or more of the authors has declared the following potential conflict of interest or source of funding: X.L. has received consulting fees and royalties from FH Ortho. J.D.K. has received consulting fees from Flexion and royalties from SLACK and Springer. R.L.P. has received grant/educational support from Arthrex. AOSSM checks author disclosures against the Open Payments Database (OPD). AOSSM has not conducted an independent investigation on the OPD and disclaims any liability or responsibility relating thereto. |
Risk of bias assessment diagnostic accuracy studies (QUADAS II, 2011)
|
Study reference |
Patient selection
|
Index test |
Reference standard |
Flow and timing |
Comments with respect to applicability |
|
McGuire, 2023 |
Was a consecutive or random sample of patients enrolled? Consecutive sample, retrospective study between August 2020 – August 2021
Was a case-control design avoided? Yes
Did the study avoid inappropriate exclusions? Yes
|
Were the index test results interpreted without knowledge of the results of the reference standard? Unclear, not stated in the text
If a threshold was used, was it pre-specified? n.a.
|
Is the reference standard likely to correctly classify the target condition? Yes, shoulder arthroscopy
Were the reference standard results interpreted without knowledge of the results of the index test? Unclear, not stated in the text
|
Was there an appropriate interval between index test(s) and reference standard? Yes
Did all patients receive a reference standard? Yes (retrospective study, inclusion criterium)
Did patients receive the same reference standard? Yes (retrospective study, inclusion criterium)
Were all patients included in the analysis? Yes
|
Are there concerns that the included patients do not match the review question? No
Are there concerns that the index test, its conduct, or interpretation differ from the review question? No
Are there concerns that the target condition as defined by the reference standard does not match the review question? No
|
|
CONCLUSION: Could the selection of patients have introduced bias?
RISK: LOW |
CONCLUSION: Could the conduct or interpretation of the index test have introduced bias?
RISK: UNCLEAR, blinding radiologists
|
CONCLUSION: Could the reference standard, its conduct, or its interpretation have introduced bias?
RISK: UNCLEAR, blinding of surgeon
|
CONCLUSION Could the patient flow have introduced bias?
RISK: LOW |
||
|
Li, 2023 |
Was a consecutive or random sample of patients enrolled? Consecutive sample, retrospective study between July 2019 – October 2021
Was a case-control design avoided? Yes
Did the study avoid inappropriate exclusions? Yes
|
Were the index test results interpreted without knowledge of the results of the reference standard? No/Unclear, this is not explicitly stated in the text
“The imaging results of US and PUSB were independently interpreted by 2 sonographers with 10 and 8 years of experience in musculoskeletal US. Similarly, 2 radiologists with 9 and 8 years of experience in musculoskeletal MRI, evaluated all images independently. When the results were inconsistent, multidisciplinary consultation was conducted, and a consensus was reached. Finally, the results of MRI, US and PUSB were compared with those of arthroscopy.”
If a threshold was used, was it pre-specified? n.a.
|
Is the reference standard likely to correctly classify the target condition? Yes, shoulder arthroscopy
Were the reference standard results interpreted without knowledge of the results of the index test? Unclear, this is not explicitly stated in the text
|
Was there an appropriate interval between index test(s) and reference standard? Yes
Did all patients receive a reference standard? Yes (retrospective study, inclusion criterium)
Did patients receive the same reference standard? Yes (retrospective study, inclusion criterium)
Were all patients included in the analysis? Yes |
Are there concerns that the included patients do not match the review question? No
Are there concerns that the index test, its conduct, or interpretation differ from the review question? No
Are there concerns that the target condition as defined by the reference standard does not match the review question? No
|
|
|
CONCLUSION: Could the selection of patients have introduced bias? No
RISK: LOW |
CONCLUSION: Could the conduct or interpretation of the index test have introduced bias?
RISK: UNCLEAR, blinding radiologists
|
CONCLUSION: Could the reference standard, its conduct, or its interpretation have introduced bias?
RISK: UNCLEAR, blinding of surgeon |
CONCLUSION Could the patient flow have introduced bias?
RISK: LOW |
Table of excluded studies
|
Reference |
Reason for exclusion |
|
Agarwal, A., Vani, K., Batta, A. et al. Can ultrasound suffice for triaging patients requiring surgical correction of rotator cuff tears—a comparative evaluation of ultrasound and magnetic resonance imaging. Egypt J Radiol Nucl Med 52, 119 (2021). https://doi.org/10.1186/s43055-021-00477-2 |
No reference standard |
|
Barad HV, Patel V, Patel S, Patel M. To determine the role of ultrasonography as a primary imaging modality as compared to MRI in patients with shoulder pain. J Family Med Prim Care. 2022 May;11(5):2119-2122. doi: 10.4103/jfmpc.jfmpc_2509_20. Epub 2022 May 14. PMID: 35800509; PMCID: PMC9254755. |
Wrong reference (USG vs MRI) |
|
Chauhan, N. S. and Ahluwalia, A. and Sharma, Y. P. and Thakur, L. A prospective comparative study of high resolution ultrasound and MRI in the diagnosis of rotator cuff tears in a tertiary hospital of North India. Polish Journal of Radiology. 2016; 81 :491-497 |
Wrong reference (MRI) |
|
Day, M. and McCormack, R. A. and Nayyar, S. and Jazrawi, L. Physician training: Ultrasound and accuracy of diagnosis in rotator cuff tears. Bulletin of the Hospital for Joint Diseases. 2016; 74 (3) :207-211 |
Wrong outcome (learning curve of orthopaedic surgeon) |
|
Fischer, C. A. and Weber, M. A. and Neubecker, C. and Bruckner, T. and Tanner, M. and Zeifang, F. Ultrasound vs. MRI in the assessment of rotator cuff structure prior to shoulder arthroplasty. Journal of Orthopaedics. 2015; 12 (1) :23-30 |
Wrong reference (MRI)
|
|
Fujiwara Y, Yamamoto S, Kato Y, Kurata S, Fujii S, Inoue K, Inoue T, Mondori T, Nakagawa Y, Tanaka Y. Usefulness of ultrasound in diagnosing long head of the biceps tendon malposition in patients with rotator cuff tears. J Med Ultrason (2001). 2022 Apr;49(2):289-295. doi: 10.1007/s10396-022-01200-y. Epub 2022 Mar 23. Erratum in: J Med Ultrason (2001). 2022 Apr 15;: PMID: 35320435. |
Wrong P, no partial tears |
|
Gallagher V, Buchanan J, Harris J, McCrum C. Audit: sonographic report correlation against surgical findings during elective shoulder surgery. Ultrasound. 2022 May;30(2):141-148. doi: 10.1177/1742271X211033314. Epub 2021 Aug 4. PMID: 35509294; PMCID: PMC9058382. |
Wrong P: suspected full thickness tear of rotator cuff and imaging reports |
|
Henderson RE, Walker BF, Young KJ. The accuracy of diagnostic ultrasound imaging for musculoskeletal soft tissue pathology of the extremities: a comprehensive review of the literature. Chiropr Man Therap. 2015 Nov 5;23:31. doi: 10.1186/s12998-015-0076-5. PMID: 26543553; PMCID: PMC4634582. |
Wrong comparison (MSK-DUSI vs appropriate reference standard ) |
|
Lenza M, Buchbinder R, Takwoingi Y, Johnston RV, Hanchard NC, Faloppa F. Magnetic resonance imaging, magnetic resonance arthrography and ultrasonography for assessing rotator cuff tears in people with shoulder pain for whom surgery is being considered. Cochrane Database Syst Rev. 2013 Sep 24;2013(9):CD009020. doi: 10.1002/14651858.CD009020.pub2. PMID: 24065456; PMCID: PMC6464715. |
Included studies in this review are published before 2010 |
|
Liu F, Dong J, Shen WJ, Kang Q, Zhou D, Xiong F. Detecting Rotator Cuff Tears: A Network Meta-analysis of 144 Diagnostic Studies. Orthop J Sports Med. 2020 Feb 5;8(2):2325967119900356. doi: 10.1177/2325967119900356. PMID: 32076627; PMCID: PMC7003181. |
Better research designs are available for inclusion |
|
Nabetani, Y. and Watanabe, T. and Terabayashi, N. and Hirose, A. and Nohisa, Y. and Shinoda, K. and Furuta, N. and Ito, H. and Matsuoka, T. and Seishima, M. [Diagnostic ability of ultrasonography for the rotator cuff tear: comparison with ultrasonography and MRI findings]. Rinsho byori. The Japanese journal of clinical pathology. 2014; 62 (1) :31-37 |
Reference not available |
|
Ok, J. H. and Kim, Y. S. and Kim, J. M. and Yoo, T. W. Learning curve of office-based ultrasonography for rotator cuff tendons tears. Knee Surgery, Sports Traumatology, Arthroscopy. 2013; 21 (7) :1593-1597 |
MRA used instead of MRI |
|
Okoroha, K. R. and Mehran, N. and Duncan, J. and Washington, T. and Spiering, T. and Bey, M. J. and Van Holsbeeck, M. and Moutzouros, V. Characterization of rotator cuff tears: Ultrasound versus magnetic resonance imaging. Orthopedics. 2017; 40 (1) :e124-e130 |
Wrong patient group (only full-thickness tears) |
|
Ottenheijm, R. P. and Jansen, M. J. and Staal, J. B. and Van Den Bruel, A. and Weijers, R. E. and De Bie, R. A. and Dinant, G. J. Accuracy of diagnostic ultrasound in patients with suspected subacromial disorders: A systematic review and meta-analysis. Archives of Physical Medicine and Rehabilitation. 2010; 91 (10) :1616-1625 |
No comparison between US and MRI |
|
Reddy KVK, Babu MML, Suresh A, Gupta S, Chalavadi DVKH. Clinico-radiological correlation of shoulder pain. European Journal of Molecular and Clinical Medicine 2022 Summer;9(4):60-69 |
Reference not available |
|
Roy, Jean-Sebastien and Braen, Caroline and Leblond, Jean and Desmeules, Francois and Dionne, Clermont E. and MacDermid, Joy C. and Bureau, Nathalie J. and Fremont, Pierre Diagnostic accuracy of ultrasonography, MRI and MR arthrography in the characterisation of rotator cuff disorders: a systematic review and meta-analysis. British journal of sports medicine. 2015; 49 (20) :1316-28 |
Included studies that do not compare US with MRI, but report on US or MRI solely. |
|
Saraya, S. and El Bakry, R. Ultrasound: Can it replace MRI in the evaluation of the rotator cuff tears?. Egyptian Journal of Radiology and Nuclear Medicine. 2016; 47 (1) :193-201 |
No reference standard |
|
Saremi, Hossein and Seifrabiei, Mohamadali Subscapularis tendon tear classification and diagnosis: A systemic review and meta-analysis. Frontiers in surgery. 2023; 10 :916694
|
"Search date: from the first date available to March 2022 Only subscapularis tears" |
|
Sipola, P. and Niemitukia, L. and Kröger, H. and Höfling, I. and Väätäinen, U. Detection and quantification of rotator cuff tears with ultrasonography and magnetic resonance imaging - A prospective study in 77 consecutive patients with a surgical reference. Ultrasound in Medicine and Biology. 2010; 36 (12) :1981-1989 |
MRA used instead of MRI |
|
Tenbrunsel TN, Whaley JD, Golchian D, Malone DL, Lima DJL, Sabesan VJ. Efficacy of Imaging Modalities Assessing Fatty Infiltration in Rotator Cuff Tears. JBJS Rev. 2019 Apr;7(4):e3. doi: 10.2106/JBJS.RVW.18.00042. PMID: 30969180. |
No comparison between US and MRI. |
|
Wall, L. B. and Teefey, S. A. and Middleton, W. D. and Dahiya, N. and Steger-May, K. and Kim, H. M. and Wessell, D. and Yamaguchi, K. Diagnostic performance and reliability of ultrasonography for fatty degeneration of the rotator cuff muscles. Journal of Bone and Joint Surgery. 2012; 94 (12) :e83(1) |
Wrong reference (MRI) |
|
And Alternative Medicine EC. Retracted: Comparative Analysis of Real-Time Dynamic Ultrasound and Magnetic Resonance Imaging in the Diagnosis of Rotator Cuff Tear Injury. Evid Based Complement Alternat Med. 2023 Jun 21;2023:9876180. doi: 10.1155/2023/9876180. PMID: 37388047; PMCID: PMC10307386. |
Retracted article |
Verantwoording
Autorisatiedatum en geldigheid
Laatst beoordeeld : 03-02-2025
Laatst geautoriseerd : 03-02-2025
Geplande herbeoordeling : 03-02-2028
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het herzien van de richtlijnmodules is in 2022 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met Subacromiaal Pijnsyndroom van de Schouder (SAPS).
Werkgroep
dr. J.J.A.M (Jos) van Raaij, orthopedisch chirurg Martiniziekenhuis Groningen, NOV (voorzitter)
dr. C.P.J. (Cornelis) Visser, orthopedisch chirurg Alrijne en Eisenhower Kliniek, NOV
dr. F.O. (Okke) Lambers Heerspink, orthopedisch chirurg VieCuri Medisch Centrum, NOV
dr. E.J.D. (Bart Jan) Veen, orthopedisch chirurg Medisch Spectrum Twente, NOV
dr. O. (Oscar) Dorrestijn, orthopedisch Chirurg Sint Maartenskliniek, NOV
dr. M.J.C. Maarten Leijs, orthopedisch chirurg Reinier Haga Orthopedisch Centrum , NOV
dr. D. (Dennis) van Poppel, manueel therapeut, sportfysiotherapeut PECE Zorg, Fontys Paramedisch, KNGF
drs. P.A. (Peter) Stroomberg, radioloog, Isala, NVvR
dr. R.P.G. (Ramon) Ottenheijm, huisarts, vakgroep huisartsgeneeskunde, Universiteit Maastricht, NHG
dr. J.W. (Jan Willem) Kallewaard, anesthesioloog Rijnstate, NVA
drs. T.J.W. (Tjerk) de Ruiter, revalidatiearts De Ruiter Revalidatie, VRA
dr. H.A. (Henk) Martens, reumatoloog Sint Maartenskliniek, NVR
Klankbordgroep
drs. R.J. (René) Naber, Bedrijfsarts arbodienst Amsterdam UMC, NVAB
drs. Y.B. (Yvonne) Suijkerbuijk, Arts-onderzoeker Amsterdam UMC en verzekeringsarts UWV, NVVG
Met ondersteuning van
dr. J.G.M. (Jacqueline) Jennen, adviseur, Kennisinstituut van de Federatie Medisch Specialisten (oktober 2023 tot mei 2024)
drs. T. (Tessa) Geltink, adviseur, Kennisinstituut van de Federatie Medisch Specialisten (tot mei 2024)
drs. F.M. (Femke) Janssen, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten (tot oktober 2023, vanaf mei 2024)
dr. M.S. (Matthijs) Ruiter, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten (vanaf mei 2024)
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
Werkgroep
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Van Raaij (voorzitter) |
Voorzitter werkgroep |
Orthopedisch chirurg, wetenschappelijk medewerker (stichting orthoresearch noord) Martiniziekenhuis Groningen (onbezoldigd). Bestuurslid werkgroep schouder/elleboog NOV (onbezoldigd) Lid registratie adviesraad (RAR) LROI (Landelijke Registratie Orthopedische Implantaten) (onbezoldigd). Lid LEARN, (Rijksuniversiteit Groningen) (onderzoek naar opleiding/onderwijs) (onbezoldigd). Cursusleider vaardigheidstraining voor aios orthopedie (Techmed Centre, University of Twente) (onbezoldigd). Voorzitter werkgroep herziening richtlijn SAPS (FMS, kennisinstituut).
Lid werkgroep richtlijn chronische instabiliteit schouder (FMS, kennisinstituut)
Voorzitter cluster richtlijnen bovenste extremiteit (FMS,kennisinstituut)
Lid werkgroep ontwikkeling richtlijn schouderklachten, KNGF (fysiotherapie)
|
Geen |
Geen restricties
|
|
Visser
|
Orthopedisch chirurg Alrijne |
Orthopedisch chirurg Eisenhowerkliniek; Lid wetenschappelijke adviesraad (WAR) LROI (Landelijke Registratie Orthopedische Implantaten) (onbezoldigd); Lid kascommissie van de NOV (onbezoldigd) |
Geen |
Geen restricties
|
|
|
Orthopedisch chirurg VieCuri Medisch Centrum
|
Commissie van onderzoek VieCuri (onbetaald) ] Lid wetenschapscommissie VieCuri (onbetaald) Voorzitter BELG (Bovenste Extremiteit Limburgs genootschap) (onbetaald)
|
Presentatie orthopedische firma (Arthrex) betreffende proximale humerusfracuur (betaald)
Extern gefinancieerd onderzoek (Financier, (inhoud)): Arthrex en Fons Wetenschap Innovatie Viecuri (optimale positionering glenoid bij revers schouderprothese), Fons wetenschap innovatie Viecuri (Nabehandeling schouderprothese middels app), Fonds Wetenschap Innovatie Viecuri (Voorkomen van cristallopathie bij patienten met een degeneratieve rotator cuff ruptuur). |
Geen restricties, onderwerp van extern gefinancierd onderzoek valt buiten het bestek van de richtlijn
|
|
Veen
|
Orthopedisch chirurg, Medisch Spectrum Twente |
Geen |
Geen |
Geen restricties
|
|
Dorrestijn
|
Orthopedisch chirurg |
Dienstverband Sint Maartenskliniek - echter geen direct financieel voordeel |
Geen |
Geen restricties
|
|
Leijs
|
Clubarts Excelsior en orthopedisch chirurg |
Geen |
Geen |
Geen restricties
|
|
Van Poppel
|
Manueel therapeut, sportfysiotherapeut, bewegingswetenschapper, docent, onderzoeker bij PECE Zorg, Schouder Expertise Centrum en Fontys Hogescholen. |
Zelfstandig docent, auteur, onderzoeker, betaald.
Docent Master Opleiding Sportfysiotherapie Hogeschool Rotterdam, betaald.
Lid werkgroep ontwikkeling richtlijn schouderklachten, KNGF (fysiotherapie).
Auditeur Health Care Auditing, betaald.
Lid Regionaal Tuchtcollege Gezondheidszorg, betaald. |
Geen |
Geen restricties
|
|
Deelname vanaf 09-10-2023 |
Tot 31-10-2024: Fellow Radioloog, Rijnstate Ziekenhuis
Vanaf 01-11-2024: Radioloog Isala
|
Geen |
Geen |
Geen restricties |
|
Koen
Deelname t/m 09-10-2023 |
Radioloog bij het Meander Medisch Centrum, Screeningsradioloog bevolkingsonderzoek borstkanker. |
Geen |
Geen |
Geen restricties
|
|
Ottenheijm
|
Universitair docent; Vakgroep Huisartsgeneeskunde, Universiteit Maastricht; Kaderhuisartsbewegingsapparaat: werkzaam als ZZPer voor MCC Omnes, Pluspunt MC en ZBC Optimus Orthopedie |
Voorzitter Stichting Optimus Klinieken (ZBC) (onbetaald) Medisch Directeur van Optimus Orthopedie BV (onbetaald) Bestuurder van de NHG-expertgroep Het Beweegkader (vereniging van kaderhuisartsen bewegingsapparaat) t/m juni 2022.
|
Werkzaam als ZZP kaderhuisarts op 1,5 lijnspoli's en in een ZBC orthopedie, waar zorg voor schouderpatienten wordt geleverd. Mede-aandeelhouder Optimus Orthopedie BV
Mede-aanvrager van een door ZonMW gefinanceerd doelmatigheidsonderzoek schouderklachten in de huisartspraktijk (Hoofdaanvrager werkzaam bij Erasmus MC) |
Geen restricties
|
|
Kallewaard
|
Anesthesioloog, Rijnstate Ziekenhuis |
Betrokken bij andere richtlijnen: bbc nva sectie pijn nva hoofd clusterpijn deelnemer |
Extern gefinancierd onderzoek (Financier, inhoud): Boston Scientific (Neuromodulatie en endometriose), Saluda (neuromodulatie psps2), Dtm (neuromodulatie virgin back). |
Geen restricties, onderwerp van extern gefinancierd onderzoek valt buiten het bestek van de richtlijn
|
|
De Ruiter
|
Revalidatiearts bij De Ruiter Revalidatie |
Rotterdam Knowledge Ambassador, Onbetaald.
Adviseur Stichting Mobiliteit voor Gehandicapten, Onbetaald.
Oprichter Perpetual Prosthetics, Onbetaald.
Lid Membership Committee, International Society on Prosthetics and Orthotics, onbetaald. |
Geen |
Geen restricties
|
|
Martens
|
Reumatoloog bij de Sint Maartenskliniek |
Geen |
Geen |
Geen restricties
|
Klankbordgroep
|
Klankbordgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Naber |
Bedrijfsarts AUMC
|
Secretaris NVAB werkgroep Bedrijfsartsen in de Zorg (onbetaald)
|
Geen |
Geen restricties
|
|
Suijkerbuijk |
Arts-onderzoeker (promovenda) Kenniscentrum Verzekeringsgeneeskunde, Amsterdam UMC, locatie AMC (betaald)
|
-Lid commissie wetenschap NVVG: beoordelen en deelname aan ontwikkeling van richtlijnen. Momenteel deelname aan ontwikkeling multidisciplinaire richtlijn Depressie (Trimbos) (onbetaald)
|
promotieonderzoek gefinancierd door UWV
|
Geen restricties
|
Met ondersteuning van
|
Janssen |
Junior adviseur Kennisinstituut van de Federatie Medisch Specialisten |
Geen |
Geen |
Geen acties |
|
Ruiter |
Senior adviseur Kennisinstituut van de Federatie Medisch Specialisten |
Geen |
Geen |
Geen acties |
|
Geltink |
Adviseur Kennisinstituut van de Federatie Medisch Specialisten |
Geen |
Geen |
Geen acties |
|
Jennen |
Adviseur Kennisinstituut van de Federatie Medisch Specialisten |
Geen |
Geen |
Geen acties |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntperspectief door het uitnodigen van de Patiëntenfederatie Nederland voor de invitational conference (knelpuntenanalyse). Het verslag hiervan is besproken in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan Patiëntenfederatie Nederland en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Module |
Uitkomst raming |
Toelichting |
|
Beeldvormende diagnostiek bij verdenking op een (partiële) supraspinatuspees ruptuur (herzien) |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn, volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van het zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 3.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten met SAPS. Tevens zijn er knelpunten aangedragen door de IGJ, NFU, NHG, NVZ, PF NL, STZ, V&VN, NAPA, ZiNL, ZKN, ZN, VIG, NOV, KNGF, NVvR, NHG, NVA, PFNL, VRA, NVR, NVAB, en Verzekeringsgeneeskundigen, via een knelpuntenanalyse (invitational conference). Een verslag hiervan is opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een [random-effects model]. [Review Manager 5.4] werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zou de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Zoekacties zijn opvraagbaar. Neem hiervoor contact op met de Richtlijnendatabase.