Overzicht geneesmiddelenreacties, differentiaal diagnoses en het effect van labelen
Uitgangsvraag
- Wat zijn de verschillende type geneesmiddelenreacties?
- Wat zijn de relevante differentiaal diagnoses bij acute vertraagd type cutane geneesmiddelenreacties?
- Wat is het effect van terecht en onterecht labelen van vertraagd type geneesmiddelenreacties?
Aanbeveling
Wees bewust van de impact van terecht en onterecht labelen van een geneesmiddelenreactie.
Stel de diagnose cutane geneesmiddelenreactie zo concreet mogelijk met differentiatie van de subtypen
Overwegingen
Allereerst is het van belang na te gaan of er überhaupt een verdenking bestaat op een geneesmiddelenreactie. De belangrijkste differentiaal diagnose van een geneesmiddel geïnduceerd exantheem betreft een exantheem veroorzaakt door een infectie. Bij kinderen betreft het vaak een virale infectie, bij volwassenen kan het viraal of bacterieel zijn. Naast een para-infectieuze rash kan iedere vorm van een exantheem in het kader van een dermatose (niet geïnduceerd door een geneesmiddelenreactie) in de differentiaaldiagnose worden opgenomen.
Wanneer er aan een geneesmiddelenreactie wordt gedacht is het in de eerste plaats van belang het type geneesmiddelenreactie te identificeren, aangezien dit van essentieel belang is voor de identificatie van het causale geneesmiddel en het verdere management voor de patiënt. Herkenning van de klinische presentatie speelt hierbij een belangrijke rol, waarbij er aandacht dient te zijn voor een grondig klinisch onderzoek en correcte descriptie van morfologische kenmerken van de huid (efflorescenties).
Definities/Classificatie
Geneesmiddelenreacties (“adverse drug reactions (ADR)”) worden ingedeeld in type A- en B-reacties (Figuur 1). De type A-reacties (in 85-90% van de gevallen), voornamelijk bijwerkingen, zijn terug te voeren op het farmacologisch effect van het medicijn, zijn voorspelbaar, dosisafhankelijk en veelvoorkomend. Daarentegen zijn de type B-reacties (10-15%) meestal onvoorspelbaar, niet of minder dosisafhankelijk en minder voorkomend; zij hebben een meer patiëntgebonden karakter (Smith, 2013; Rawlins, 1977; Meyboom, 2000). In slechts 5% hiervan (dus in 0,5-0,75% van het totaal) is sprake van een allergische reactie (“drug hypersensitivity reaction (DHR)” (Celik 2009), waarbij objectiveerbare, reproduceerbare symptomen aanwezig zijn na inname van het causale geneesmiddel (Brockow, 2019).
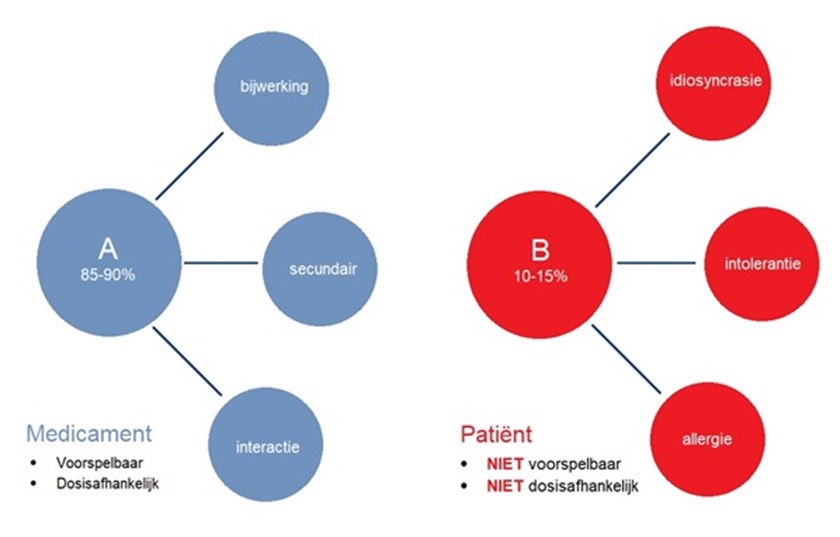
Figuur 1 Overzicht geneesmiddelenreacties, ingedeeld in type A en B. Geadapteerd uit Celik et al. 2009.
Onder een bijwerking wordt verstaan elke reactie op een geneesmiddel die: (i) schadelijk en onbedoeld is, (ii) kan voortkomen uit het gebruik van het product (a) binnen of buiten de voorwaarden van de gerelateerde vergunning voor het in de handel brengen, inclusief off-label gebruik, overdosis, verkeerd gebruik, misbruik en medicatiefouten of (b) na beroepsmatige blootstelling (Geneesmiddelenwet, 2007).
Intolerantie gaat over medicatie die vermeden moeten worden om metabole, genetische of farmacologische redenen zonder dat ooit bij expositie sprake is geweest van een geneesmiddelenreactie (Macy, 2020).
Een allergische reactie op een geneesmiddel wordt gedefinieerd als een reactie die al of niet na een eerdere sensibilisatie het gevolg is van door medicatie gemedieerde immuun- dan wel inflammatoire cel reactie (Brockow, 2019).
Uit een systematische review van studies met zelf gerapporteerde geneesmiddelenallergie blijkt dat de prevalentie van geneesmiddelenreacties bij vrouwen 11,4% is, dat is meer dan bij mannen (7,2%), meer bij volwassenen (10%) dan bij kinderen (in 5,1%) en meer in een klinische setting (klinisch 15,9% versus 11,4% poliklinisch). Meta-analyse geeft een overall prevalentie aan van 7,9%. Bij kinderen levert dit een geschatte prevalentie van geneesmiddelenallergie op van maximaal 0,5% (Sousa-Pinto, 2017). Exacte data ontbreken omdat er landelijk geen officiële registratie bestaat.
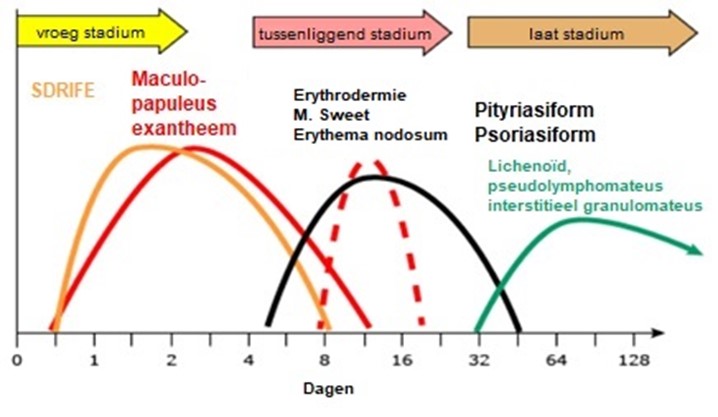
Bij type IV-reacties spelen huidsymptomen een belangrijke rol, omdat de huid een opslagplaats is voor grote aantallen T-(memory) cellen. Deze zijn vaak geneesmiddelenspecifiek “geprimed”. Snelle allergeenpenetratie door de huidbarrière of diffusie vanuit de circulatie naar de huid draagt bij aan de zeer frequente betrokkenheid van de huid bij geneesmiddelenreacties. Virale infecties kunnen T-cel gemedieerde overgevoeligheidsreacties op geneesmiddelen faciliteren door verschillende mechanismen, zoals het ondersteunen van T-cel receptor co-stimulatie of verhoging van receptoraffiniteit (Pichler, 2023). Vele, meestal ongecompliceerde, reacties kunnen in verloop van tijd bij geneesmiddel-geïnduceerde exanthemen optreden bij tevoren gesensibiliseerde patiënten (Celik, 2009) (Figuur 2).
Figuur 2 Chronologie van ongecompliceerde geneesmiddelexanthemen (Celik 2009). De hoogte van de lijn geeft de ernst van de reactie aan. De rood gestippelde lijn is het typische begin van exantheem bij nieuw gesensibiliseerde patiënten tussen de 8ste en 20ste dag. SDRIFE; symmetrical drug-related intertriginous and flexural exanthema.
Geneesmiddelenreacties worden daarnaast onderverdeeld in ernstige cutane reacties (severe cutaneous adverse reactions (SCAR)) en milde ongecompliceerde reacties. Voor een overzicht van de belangrijkste cutane geneesmiddelenreacties, zie Tabel 1. (geadapteerd en geactualiseerd naar Scherer, 2009 en Bircher, 2010).
Tabel 1 Overzicht cutane geneesmiddelenreacties (geadapteerd en geactualiseerd naar Scherer 2009 en Bircher 2010).
|
Type reactie |
Incidentie |
Klinisch huidbeeld |
Belangrijke symptomen, bevindingen of complicaties |
Diagnostische tests |
Klinisch bruikbare algoritmen |
Belangrijkste differentiaaldiagnosen |
|
Ernstige cutane geneesmiddelenreacties (SCAR) |
||||||
|
Drug reaction with eosinophilia and systemic symptoms (DRESS) synoniem: Drug-induced hypersensitivity syndrome (DIHS) |
0.9 - 2 per 100.000 patiënten per jaar. |
Erythemateuze rash, >50% lichaam, faciaal oedeem. Variabel: purpura en pustels |
Koorts, algehele malaise, eosinofilie, lymfeklierzwelling, orgaanbetrokkenheid met leverenzymstijging / hepatitis. Variabel: herpesvirus reactivatie m.n. HHV6 (CMV, EBV). Mogelijk myocarditis, interstitiële pneumonie, nefritis, thryreoïditis, artritis, verhoogde kans op auto-immuunziektes en lymfadenopathie. |
Klinisch beeld. Laboratoriumonderzoek: afwijkende leukocyten differentiatie en orgaanfunctie (lever-/nierfunctiestoornissen). Histologie passend bij geneesmiddelenreactie / DRESS . |
RegiSCAR-score (Kardaun 2007), zie Tabel 2. Geeft waarschijnlijkheid van diagnose weer. |
Viraal exantheem, MPE en AGEP. |
|
Stevens-Johnson syndroom (SJS) en Toxische Epidermale Necrolyse (TEN) |
SJS: 5 - 7,5 per 1 miljoen patiënten per jaar. TEN: 1 - 2 per 1 miljoen patiënten per jaar. |
Grijs/livide erytheem, maculeus/bulleus exantheem, atypische target laesies, mucocutane laesies (90%), epidermale necrose (<10% in SJS, 10-30% in SJS/TEN, >30% in TEN) en positief teken van Nikolsky. |
Prodromale koorts, algehele malaise, bovenste luchtweg symptomen (pneumonie), pijnlijke huid, dysfagie, fotofobie en urethritis. |
Klinisch beeld. Laboratoriumonderzoek: lymfopenie, anemie, neutropenie. Histologie: subepidermale blaren met transepidermale necrose. |
ALDEN-score (Sassolas 2010) Ter identificatie causaal geneesmiddel. |
Andere bulleuze dermatosen. Bulleus Graft-versus-Host Disease. |
|
Acute Gegeneraliseerde Exanthemateuze Pustulose (AGEP) |
1 - 5 per 1 miljoen patiënten per jaar. |
Verspreid steriel pustuleus erytheem, faciaal oedeem. Typische start in het gelaat of plooien met disseminatie binnen enkele uren. |
Hoge koorts (en zelden nierfalen). |
Klinisch beeld. Laboratoriumonderzoek: leucocytose met neutrofilie. Histologie: pustulaire dermatose. |
EuroSCAR- score (Sidoroff 2007) Geeft ernst van de aandoening weer. |
Psoriasis pustulosa generalisata (ziekte van Zumbusch), impetigo, IgA pemphigus, pemphigus foliaceus en Sneddon-Wilkinson. |
|
Generalized fixed drug eruption (GFDE) (Barootes 2021) |
Prevalentie: zeldzaam. |
Schemerend rood-livide of bruin kleurige annulaire, erythemateuze of pijnlijke bulleuze plaques mogelijk op romp, lippen > extremiteiten. Huid tussen lesies niet aangedaan. |
Jeuk en brandend gevoel met hyperpigmentatie. Bij re-administratie heroptreden van klachten. |
Klinisch beeld. Histologie: grensvlakdermatitis met eosinofielen. |
Geen |
SJS / TEN. Bulleuze toxicodermie, bulleus pemphigoid. |
|
Drug-induced linear IgA bullous dermatosis (LABD) (Fortuna 2012, Ho 2007) |
0,5 - 2,3 per 1 miljoen patiënten per jaar. |
Verspreide annulaire (parelsnoer) vesiculae / bullae op erythemateuze grond, mn op onderbuik, bovenbenen en liezen; mucocutaane afwijkingen zeldzaam. Niet aangedane huid tussen lesies. |
Ernstige jeuk en IgA nefropathie. |
Directe immuno-fluorescentie: lineaire IgA-depositie op de dermo-epidermale overgang Lymfocyten stimulatietest met verdachte medicatie.
|
Geen |
Auto-immuun bulleuze dermatosen. |
|
Milde, ongecompliceerde vertraagde geneesmiddelenreacties |
||||||
|
Maculopapuleus Exantheem (MPE) |
Onbekend, zeer frequent. |
Maculae en papels. Romp > extremiteiten. |
Soms bijkomende (milde) koorts/subfebriel en pruritus. |
Klinisch beeld en eventueel histologie. |
Geen |
Para-infectieus exantheem. |
|
Symmetrical Drug-Related Intertriginous and Flexural Erythema (SDRIFE) |
Onbekend |
Intertrigineus en flexuraal exantheem V-vormig gluteaal/perigenitaal. Scherp omschreven erytheem in de flexuren/plooien. |
Normaliter geen systemische betrokkenheid. |
Klinisch beeld: symmetrie, betrokkenheid lichaamsplooien, relatief scherpe begrenzingen. Laboratoriumonderzoek en histologie: geen afwijkingen. |
Geen |
Erythrasma, seborrhoisch eczeem en intertrigineus eczeem. |
|
Fixed drug eruption (Barootes 2021) |
Prevalentie: 10%; 14 - 22% van alle cutane medicatiereacties. |
Schemerend rood-livide of bruinkleurige annulaire, erythemateuze of pijnlijke bulleuze plaques mogelijk op romp > lippen > extremiteiten. Solitaire laesies. |
Jeuk en brandend gevoel met hyperpigmentatie. Bij opnieuw toediening van het geneesmiddel heroptreden van klachten. |
Klinisch beeld (typische trigger). Histologie: grensvlakdermatitis met eosinofielen. |
Geen |
Culicosis, erythema exsudativum multiforme, erythema chronicum migrans, lichen planus, tinea corporis, erythema annulare centrifugum, bulleuze toxicodermie, bulleus pemphigoid, bulleuze contactdermatitis, impetigo bullosa, bullosis diabeticorum en pseudoporfyrie. |
|
Drug-induced systemische lupus erythematosus (Borchers 2007, Yung 2002, El-Hallak 2008) |
Schatting 15.000 – 30.000 patiënten per jaar (VS) |
Annulaire erythemato-squameuze plaques, mogelijk fotosensitieve component. |
Koorts, fotosensitiviteit, arthralgie / arthritis, myalgie, rash en/of serositis, pleuritis, pericarditis, vasculitis, nefritis, neurologische afwijkingen. |
Histologie: passend bij lupus erythematodes (LE). |
Geen |
Niet geneesmiddelen geïnduceerd LE, (geneesmiddelen geïnduceerde) psoriasis, tinea corporis, tinea incognito, mycosis fungoides, nummulair eczeem |
|
Geneesmiddel geïnduceerde vasculitis |
Onbekend |
Palpabele purpura, (donker) erythemateuze, soms livide papels, voornamelijk onderste extremiteiten. Eventueel noduli en bullae. |
Systemische orgaan betrokkenheid, bloeding en/of necrose. |
Klinisch beeld (purpura). Histologie: passend bij (leucocytoclastische) vasculitis. |
Geen |
Niet door geneesmiddelen geïnduceerde vasculitiden. |
|
(Systemische) fotoallergische/-toxische reactie |
Onbekend |
Dermatitis op zon beschenen huid, eventueel uitbreidend. |
Typisch tijdsbeloop tussen zonexpositie en het ontstaan van klachten: foto-allergisch: dagen (soms weken), foto-toxisch: uren |
Klinisch beeld, photopatch test en minimale erytheem dosis (MED). |
Geen |
Overige foto-dermatosen. |
|
Injection site reactie |
Onbekend |
Erythemateuze plaque op injectie plaats. |
Geen systemische symptomen, eventueel “strooireactie”. |
Klinisch beeld (injectieplaats). |
Geen |
Infectie, sarcoïdose en insect bite-reactions, |
|
Urticariele reacties (met/zonder vertraagd angio-oedeem) |
Onbekend |
Generaliseerd, bij angio-oedeem ook slijmvliezen. Vluchtige, verspringende, iets verheven confluerende urticae, jeuk/pijn. |
Geen systemische symptomen. |
Klinisch beeld. |
Urticaria vragenlijst |
Chronische spontane urticaria, fysische urticaria, erfelijke dan wel verworven C1-esteraseremmer deficiëntie, factor XII-mutatie. |
|
Geneesmiddel geïnduceerde psoriasiforme reacties |
Onbekend |
klinisch beeld van psoriasis. |
Huidbeeld |
Klinisch beeld en histologie passend bij psoriasis. |
Geen |
Pityriasis rosea, pityriasis lichenoides chronica et acuta (PLEVA), lues II, viraal exantheem, lichen planus, cutaan T-cel lymfoom, psoriasis guttata en psoriasis vulgaris. |
|
Geneesmiddel geïnduceerde lichenoide pseudolymfomateuze reacties |
Onbekend |
Bij lichenoíde reacties voorkeur voor polsen en slijmvliezen (oraal en genitaal). |
Geen systemische symptomen. |
Klinisch beeld, laboratoriumonderzoek (serologie, bloedbeeld) en fysieke testen. Histologie: lichenoide dermatitis. |
Geen |
Lichen planus met klinische differentiaaldiagnose van lichen planus: lichen simplex chronicus, lichen striatus, verruca planae, verruca vulgaris, mollusca contagiosa, lichen nitidus, lichenoïde geneesmiddelen eruptie, drug-induced lichen planus, en porokeratosis. |
|
Geneesmiddel geïnduceerde acneiforme erupties |
Onbekend |
Voorkeurslocaties van acne vulgaris, ook romp. |
Huidbeeld |
Klinisch beeld, histologie en bacteriële kweek. |
Geen |
Rosacea (geen comedonen), pityrosporen folliculitis, dermatitis perioralis demodex folliculitis folliculitis n.n.o., steatocystoma multiplex en syringomata. |
|
Vesiculobulleuze geneesmiddelenreacties: Drug induced bulleus pemphigoid Pemphigus Porphyrie |
Zeldzaam |
Afhankelijk van geïnduceerde (vesiculo)bulleuze dermatose.
|
Huidbeeld passend bij de betreffende primaire (vesiculo)bulleuze dermatose. |
Klinisch beeld en histologie/immuunfluorescentie onderzoek. |
Geen |
Niet door geneesmiddelen geïnduceerde autoimmuun bulleuze dermatosen. |
|
Geneesmiddel geïnduceerde Morbus Sweet |
Onbekend |
Klinisch beeld van Morbus Sweet. |
Huidbeeld. Koorts, algemene malaise, systemische klachten |
Klinisch beeld, laboratoriumonderzoek. Histologie: neutrofiele dermatose. |
Geen |
M. Sweet en overige neutrofiele dermatosen. |
Bij ernstige medicatie-geïnduceerde huidreacties (SCAR) bestaan bij drie ziektebeelden een gevalideerde klinische score, waarmee de waarschijnlijkheid van de diagnose (DRESS, RegiSCAR score), de identificatie van het causale geneesmiddel (SJS/TEN, ALDEN score) en de ernst van de aandoening (AGEP, EuroSCAR score) beoordeeld kan worden.
De RegiSCAR score beschrijft een tiental klinische parameters dat gescoord kan worden met +1, 0 of -1, waarna de totaalscore de waarschijnlijkheid van de diagnose DRESS bepaalt, zie Tabel 2 (Kardaun, 2007).
Bij de ALDEN score is een speciaal algoritme ontwikkeld als hulpmiddel om zorgvuldig het verdachte geneesmiddel op te sporen dat het klinisch beeld van SJS/TEN veroorzaakt; dit is met name zinvol bij polyfarmacie. Elk potentieel verdacht geneesmiddel wordt gescoord op zes parameters. De totaalscore kan liggen tussen -12 en 10, waarop het betreffende medicament als veroorzaker geëxcludeerd, onwaarschijnlijk, mogelijk, waarschijnlijk of zeer waarschijnlijk ingeschat wordt (Sassolas, 2010). Zie bijlage 4, tabel 2.
Bij de EuroSCAR score wordt een totaalscore berekend uit 18 items: de morfologie en distributie van het huidbeeld van pustels en erytheem, het tijdstip van ontstaan en herstel van het huidbeeld, naast al of niet koorts en aanwezigheid van polymorfe neutrofielen en het histologisch beeld. De score bepaalt de waarschijnlijkheid van de diagnose AGEP en een score tussen 8-12 geeft de ernst aan (Sidoroff, 2001). Zie bijlage 4, tabel 3.
Tabel 2 RegiSCAR score (Kardaun, 2007)
|
Score |
-1 |
0 |
1 |
2 |
Min |
Max |
|
Koorts >38.5 °C |
N |
J |
|
|
-1 |
0 |
|
Vergrote lymfeklieren (>1cm, >2 locaties) |
|
N/O |
J |
|
0 |
1 |
|
Eosinofilie |
|
N/O |
700-1499/µL of 10-19,9% |
≥1500/µL of ≥20% |
0 |
2 |
|
Atypische lymfocyten |
|
N/O |
J |
|
0 |
1 |
|
Betrokkenheid huid |
|
|
|
|
|
|
|
Uitbreiding exantheem (% BSA) |
|
N/O |
>50% |
|
|
|
|
Exantheem duidend op DRESS (≥2 van volgende: gezichtsoedeem, purpura, infiltratie, desquamatie) |
N |
O |
J |
|
-2 |
2 |
|
Biopt suggestief voor DRESS |
N |
J/O |
|
|
|
|
|
Betrokkenheid andere organen waaronder lever, nieren, longen, spieren, hart, pancreas of een ander orgaan. |
|
|
1 |
2 |
0 |
2 |
|
Verbetering in ≥ 15 dagen |
N |
J |
|
|
-1 |
0 |
|
Evaluatie van andere potentiële oorzaken: Serologie voor HAV/HBV/HCV, bloedkweek. Anti-nucleaire antistof, chlamydia, mycoplasma |
|
|
J (indien geen positief is en er >3 negatief zijn. |
|
0 |
1 |
|
Totaal score, waarschijnlijkheid diagnose DRESS |
< 2: onwaarschijnlijk 2-3: mogelijk 3-5: waarschijnlijk >5: zeker |
|
|
|||
Legenda: N, nee; J, ja; O, onbekend; BSA, body surface area; HAV, hepatitis A virus; HBV, hepatitis B virus; HCV, hepatitis C virus.
Figuur 3 Algoritme voor cutane geneesmiddelenreacties, gericht op de belangrijkste typen reacties (naar Brockow, 2019.)
Het effect van terecht en onterecht labelen
Het exact vastleggen en documenteren van een terecht label medicatie-allergie is de sleutel voor een goede clinicus practicus om ervoor te zorgen dat patiënten niet blootgesteld worden aan medicatie waarvoor ze allergisch zijn. Hierdoor voorkomt men de kans op een ernstige allergische reactie (als iatrogene ziekte), met eventuele opname en mortaliteit tot gevolg. Bij geneesmiddelenallergie is helaas vaak sprake van verkeerd labelen: misdiagnose, veel onderdiagnose (door onderrapportage) en met name overdiagnose (ten gevolge van overmatig gebruik van de term allergie). 10% krijgt een levenslang etiket “allergie”, terwijl bijvoorbeeld bij penicillineallergie 90-95% na anamnese en aanvullend onderzoek tolerant blijkt te zijn voor het verdachte geneesmiddel (Macy, 2020; Demoly, 2014; CIOMS Ooms, 2017; Cardona, 2020; Muzumdar, 2019). Vooral bij kinderen dient de diagnose geneesmiddelenallergie secuur, goed gedocumenteerd en snel gesteld te worden, omdat dit later vaak niet goed geverifieerd kan worden.
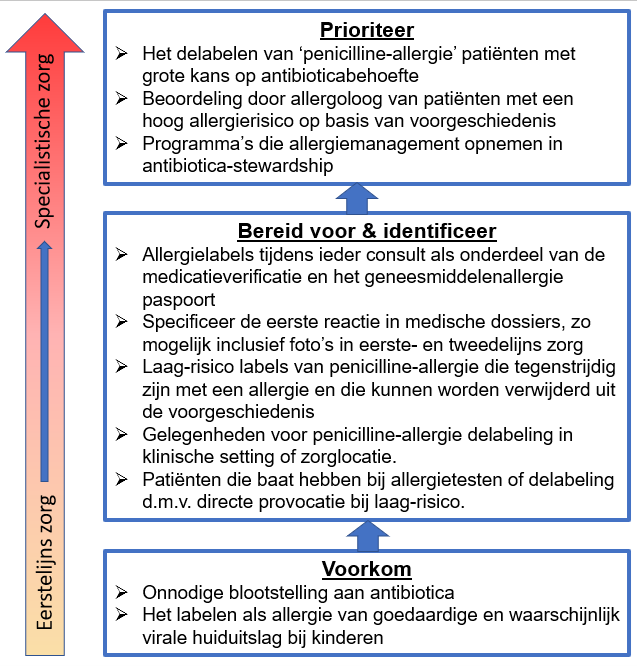
Onterechte of onjuiste registratie van het etiket “geneesmiddelenallergie” kan leiden tot minder behandelopties en meer gebruik van tweede keus medicatie, die potentieel meer toxisch, mogelijk minder effectief, vaak duurder is en in geval van antibiotica gepaard kan gaan met antimicrobiële resistentie en hiermee ongunstig Antimicrobial Stewardship. Het hoofddoel van Antimicrobial Stewardship is het optimaliseren van klinische uitkomsten en kosteneffectieve behandelingen, waarbij de onbedoelde gevolgen van het gebruik van antimicrobiële middelen, zoals toxiciteit, het selecteren op pathogene micro-organismen en resistentieontwikkeling, worden geminimaliseerd (SWAB, 2016). Ongunstig Antimicrobial Stewardship zorgt voor meer gebruik van reserve antibiotica, langdurige ziekenhuis opnames, en een grotere kans op overlijden tijdens opname (van Dijk, 2006; Macy, 2014). Het is dus van essentieel belang om niet alleen onterecht labelen te voorkomen maar ook een breed gedragen (door huisartsen, apothekers, medisch specialisten en ziekenhuisbestuur) strategische aanpak te hebben. Phillips et al. geven in hun artikel uit 2022 een implementatieplan weer van zo’n strategische aanpak voor penicilline-allergie. Een vertaling hiervan is weergegeven in Figuur 4. In dit kader heeft de Nederlandse SWAB-werkgroep (Stichting Werkgroep Antibioticabeleid) de richtlijn “The Dutch Working Party on Antibiotic Policy (SWAB) guideline for the approach to suspected Antibiotic Allergy” ontwikkeld met adviezen betreffende het beleid bij patiënten (kinderen en volwassenen) met een antibiotica allergie-label tijdens opname in het ziekenhuis (SWAB, 2022).
De dermatoloog heeft een zeer belangrijke rol tijdens de beoordeling van een patiënt met een mogelijke door een geneesmiddel-induceerde cutane reactie.
Een terecht label geneesmiddelallergie, het delabelen of het vermijden van een onterecht label “geneesmiddelenallergie” vereist een adequaat management van een patiënt met een acute presentatie van een mogelijk vertraagd type geneesmiddelenreactie.
Figuur 4 Implementatieplan voor een strategische aanpak van onterechte labeling van een penicilline-allergie. Naar: Phillips, 2022.
Onderbouwing
Achtergrond
Er zijn verschillende differentiaal diagnoses voor vertraagd type cutane geneesmiddelenreacties. Voor het opstellen van een volledige en correcte differentiaal diagnose is adequate kennis noodzakelijk van de verschillende typen cutane geneesmiddelenreacties, overige huidreacties en hun klinisch beeld en beloop.
Bewust is ervoor gekozen om de kruisreactiviteit van geneesmiddelen bij geneesmiddelenreacties niet uitgebreid te bespreken, aangezien deze richtlijn beoogt overzichtelijke adviezen te geven ten aanzien van de diagnostiek en behandeling van geneesmiddelenreacties. Voor een verdere inhoudelijke verdieping van deze belangrijke problematiek, wordt verwezen naar recente literatuur (Khan, 2022).
Zoeken en selecteren
Voor deze vragen is niet naar wetenschappelijke literatuur gezocht. Binnen de GRADE-methodiek is het systematisch literatuuronderzoek gebaseerd op vergelijkend onderzoek, veelal gerandomiseerd onderzoek. Het is niet aannemelijk dat de genoemde uitgangsvragen met dit type onderzoek beantwoord kunnen worden, of dat dergelijk onderzoek in dit kader is verricht. Voor de uiteenzetting van verschillende differentiaal diagnoses werd met name gebruik gemaakt van het artikel “EAACI position paper on how to classify cutaneous manifestations of drug hypersensitivity” van de European Academy of Allergy and Clinical Immunology (Brockow, 2019). Dit betreft een internationaal consensus document. Er werd tevens het naslagwerk van A.C. de Groot gebruikt (de Groot, 2022). In de referentielijst worden deze bronnen en de overige overzichtsartikelen en boeken vermeld die zijn gebruikt voor de uitwerking van deze uitgangsvragen.
Referenties
- - Barootes H, Peebles E, Matsui D et al. Severe Generalized Bullous Fixed Drug Eruption Treated with Cyclosporine: A Case Report and Literature Review. Case Rep Dermatol 2021;13:154-63.
- - Bircher AJ, Scherer K. Delayed cutaneous manifestations of drug hypersensitivity. Med Clin North Am 2010; 94:711.
- - Blumenthal KG, Peter JG, Trubiano JA et al. Antibiotic allergy. Lancet 2019;393:183-98
- - Borchers AT, Keen CL, Gershwin ME. Drug-induced lupus. Ann N Y Acad Sci. 2007;1108:166.
- - Brockow K, Ardern-Jones MR, Mockenhaupt M et al. EAACI position paper on how to classify cutaneous manifestations of drug hypersensitivity. Allergy. 2019;74(1):14-27.
- - Cardona V, Ansotegui IJ, Ebisawa M et al. World allergy organization anaphylaxis guidance 2020. The World Allergy Organization journal. 2020;13(10):100472.
- - Celik G, Pichler WJ, Adkinson NF Jr. Drug Allergy. In: Middleton's Allergy Principles & Practice, 7th ed, Adkinson NF, et al (Ed), Mosby Elsevier, Philadelphia 2009:1205-26.
- - CIOMS Ooms. Reporting adverse drug reactions. 2017. Via: https://cioms.ch/wp-content/uploads/2017/01/reporting_adverse_drug.pdf.
- - Demoly P, Adkinson NF, Brockow K, Castells M, Chiriac AM, Greenberger PA, Khan DA, Lang DM, Park HS, Pichler W, Sanchez-Borges M, Shiohara T, Thong BY. International Consensus on drug allergy. Allergy. 2014 Apr;69(4):420-37.
- - Dijk, van SM, Gardarsdottir H, Wassenberg MW, Oosterheert JJ, de Groot MC, Rockmann H. The High Impact of Penicillin Allergy Registration in Hospitalized Patients. J Allergy Clin Immunol Pract. 2016 Sep-Oct;4(5):926-31.
- - Uptodate. Drug induced lupus. Via: www.uptodate.com/contents/drug-induced-lupus/abstract/65
- - Fortuna G, Salas-Alanis JC, Guidetti E, Marinkovich MP. A critical reappraisal of the current data on drug-induced linear immunoglobulin A bullous dermatosis: a real and separate nosological entity? J Am Acad Dermatol 2012;66:988.
- - Geneesmiddelenwet. Ministerie van Volksgezondheid, Welzijn en Sport. Nederland. 2007. Via: https://wetten.overheid.nl/BWBR0021505/2022-01-31
- - Groot, de AC. Monographs in Contact Allergy Volume 4. Systemic Drugs. Boca Raton. CRC Press. 2022. ISDN 978-0-367-43649-0
- - Ho JC, Ng PL, Tan SH, Giam YC. Childhood linear IgA bullous disease triggered by amoxicillin-clavulanic acid. Pediatr Dermatol 2007;24:E40.
- - Khan DA, Banerji A, Blumenthal KG, Phillips EJ, Solensky R, White AA, et al. Joint Task Force on Practice Parameters Reviewers:; Bernstein JA, Chu DK, Ellis AK, Golden DBK, Greenhawt MJ, Horner CC,et al. Drug allergy: A 2022 practice parameter update. J Allergy Clin Immunol. 2022 Dec;150(6):1333-1393.
- - Kardaun SH, Sidoroff A, Valeyrie-Allanore L, Halevy S, Davidovici BB, Mockenhaupt M, Roujeau JC. Variability in the clinical pattern of cutaneous side-effects of drugs with systemic symptoms: does a DRESS syndrome really exist? Br J Dermatol. 2007 Mar;156(3):609-11.
- - Kardaun SH, Sekula P, Valeyrie-Allanore L, et al. Drug reaction with eosinophilia and systemic symptoms (DRESS): an original multisystem adverse drug reaction. Results from the prospective RegiSCAR study. Br J Dermatol 2013; 169:1071.
- - Macy E. Addressing the epidemic of antibiotic allergy over-diagnosis. Ann Allergy Asthma Immunol. (124) 2020 Dec 550-7.
- - Macy E, Contreras R. Health care use and serious infection prevalence associated with penicillin "allergy" in hospitalized patients: A cohort study. J Allergy Clin Immunol. 2014 Mar;133(3):790-6.
- - Meyboom RH, Lindquist M, Egberts AC. An ABC of drug-related problems. Drug Saf. 2000;22:415-23.
- - Muzumdar S et al. The rash with maculopapules with fever in children. Clin Dermatol 2019;37(2):119-128.
- - Phillips EJ, Demoly P, Torres MJ. Addressing beta-lactam allergy: A time for action. Allergy. 2022 Apr;77(4):1091-1093.
- - Rawlins MD, Thompson JW. Pathogenesis of adverse drug reactions. In: Davies DM, editor. Textbook of adverse drug reactions. Oxford: Oxford University Press; 1977.
- - Roujeau JC, Stern RS. Severe adverse cutaneous reactions to drugs. N Engl J Med. 1994;331(19):1272-85.
- - Sassolas B et al. ALDEN, an algorithm for assessment of drug causality in Stevens-Johnson Syndrome and toxic epidermal necrolysis: comparison with case-control analysis. Clin Pharmacol Ther. 2010 Jul;88(1):60-8
- - Scherer K, Bircher A. Adverse drug reactions and the skin--from trivial to fire signal. Internist (Berl) 2009; 50:171
- - Sidoroff A, Halevy S, Bavinck JN, Vaillant L, Roujeau JC. Acute generalized exanthematous pustulosis (AGEP)--a clinical reaction pattern. J Cutan Pathol. 2001 Mar;28(3):113-9. Smith W. Adverse drug reaction. Allergy? Side-effect? Intolerance? Aust Fam Phys. 2013;42: 12-6.
- - Sousa-Pinto B, Fonseca J and Gomes E, Frequency of self-reported drug allergy: A systematic review and meta-analysis with meta-regression; Ann Allergy Asthma Immunol, Oct 2017;119(4):362-73.
- - SWAB. Antimicrobial Stewardship / 2016. Via: https://swab.nl/nl/antimicrobial-stewardship. Geraardpleegd op 31-01-2023.
- - SWAB. Wijnakker R, et al. The Dutch Working Party on Antibiotic Policy (SWAB) guideline for the approach to suspected Antibiotic Allergy. April 2022. Via: https://swab.nl/nl/vermoeden-van-antibiotica-allergie-algemene-informatie. Geraadpleegd op: 31-01-2023.
- Yung R, Richardson B. Drug-induced rheumatic syndromes. Bull Rheum Dis 2002; 51:1.
Verantwoording
Autorisatiedatum en geldigheid
Laatst beoordeeld : 05-06-2023
Laatst geautoriseerd : 05-06-2023
Geplande herbeoordeling :
De Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
Wkkgz & Kwalitatieve raming van mogelijke substantiële financiële gevolgen
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (gebaseerd op het stroomschema ontwikkeld door FMS).
Uit de kwalitatieve raming blijkt dat er waarschijnlijk geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
|
Module |
Uitkomst Raming |
Toelichting |
|
Behandeling cutane geneesmiddelenreacties |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
Aanleiding
Op initiatief van de Nederlandse Vereniging voor Dermatologie en Venereologie is de richtlijn “management van de acute fase van vertraagd type overgevoeligheidsreacties op geneesmiddelen” ontwikkeld. Voor dit onderwerp was nog geen richtlijn beschikbaar, terwijl het een belangrijk onderwerp is voor zowel patiënt als zorgverlener. Beoogd is een evidence-based richtlijn te ontwikkelen waarin staat welke diagnostiek er plaats moet vinden indien een behandelaar vermoedt dat er een reactie op een geneesmiddel is opgetreden, en men het van belang acht de oorzakelijke factor op te sporen. Het is belangrijk voor de patiënt te weten welk geneesmiddel beter vermeden kan worden. Daarnaast moet men voorkómen dat de patiënt onnodig essentiële geneesmiddelen wordt onthouden.
Afbakening onderwerp
In deze richtlijn worden adviezen gegeven ten aanzien van de diagnostiek en behandeling van acute fase van vertraagd type geneesmiddelenreacties en dient als leidraad voor de dermatoloog en andere zorgprofessionals die hiermee in aanraking komen. De werkgroep heeft gekozen om drug reaction with eosinophilia and systemic symptoms (DRESS), acute gegeneraliseerde exanthemateuze pustulose (AGEP) en maculopapuleus exantheem (MPE) verder uit te werken in deze richtlijn, omdat het hier de meest voorkomende geneesmiddelenreacties betreft.
Definities
In de titel van deze richtlijn is ervoor gekozen de meest correcte benaming van het type reactie te gebruiken dat in deze richtlijn besproken wordt. De benaming ‘vertraagd type geneesmiddelenreactie’ is echter ook gebruikelijk. Omdat deze term beter werkbaar is, wordt in deze richtlijn vaak voor deze benaming gekozen.
De WHO definieert een bijwerking als een reactie op een geneesmiddel die schadelijk en onbedoeld is en die ontstaat bij gebruikelijke doseringen (WHO, 2002). Zowel allergische als niet-allergische mechanismen kunnen ten grondslag liggen aan geneesmiddelenreacties. Allergische reacties ontstaan pas nadat sensibilisatie is opgetreden. De reacties worden bij een eerste blootstelling meestal pas manifest 7-21 dagen na de start van het geneesmiddel. De reactie kan van milde ernst zijn, zoals een lichte huiduitslag, maar kunnen ook ernstige levensbedreigende reacties veroorzaken die niet alleen tot de huid beperkt zijn. Huidafwijkingen veroorzaakt door geneesmiddelen (geneesmiddelenerupties) kunnen zich onder andere uiten als erytheem (roodheid), papels, pustels, pruritus en als levensbedreigende situaties, zoals toxische epidermale necrolyse (TEN) of DRESS. Als algemene benaming van huiduitslag wordt vaak de term exantheem gebruikt: een plotseling, voorbijgaande, uitgebreide huiduitslag die meestal wordt veroorzaakt door een infectie of door de inname van een geneesmiddel. Exacte gegevens over de incidentie van geneesmiddelenerupties ontbreken, zeer waarschijnlijk ten gevolge van onderrapportage. Onderzoeken naar de prevalentie van bijwerkingen onder patiënten die in het ziekenhuis zijn of worden opgenomen, komen uit op 10-20% van de opgenomen patiënten; 1-20% van hen heeft een huidreactie. Bij oudere patiënten wordt vaker een geneesmiddeleneruptie gediagnosticeerd dan bij jongere, hetgeen waarschijnlijk het toenemend medicijngebruik bij het stijgen van de leeftijd reflecteert (Beijer, 2002).
In deze richtlijn staan vertraagd type overgevoeligheidsreacties op geneesmiddelen centraal. Dit kunnen geneesmiddelen op recept zijn, maar ook vrij verkrijgbare geneesmiddelen en supplementen. In deze richtlijn wordt de overkoepelende term geneesmiddelen gebruikt.
Doel en doelgroep
Deze richtlijn is een document met aanbevelingen ter ondersteuning van de dagelijkse praktijkvoering. De richtlijn berust op de resultaten van wetenschappelijk onderzoek en aansluitende meningsvorming gericht op het vaststellen van goed medisch handelen. De richtlijn geeft aanbevelingen over begeleiding en behandeling van patiënten in de acute fase van een vertraagd type geneesmiddelenreactie. Er wordt een overzicht gegeven van de geneesmiddelenreacties, de verschillende huidreacties, hun reactietype en de relevante differentiaal diagnoses. Daarnaast wordt er gekeken naar het effect van onterecht labelen en de plaats van aanvullend onderzoek in de acute fase.
Doelgroep
De richtlijn is bestemd voor leden van de medische en paramedische beroepsgroep. Daartoe behoren onder andere: dermatologen, pathologen, medisch microbiologen, kinderartsen, apothekers, internisten, (kinder)allergologen, verpleegkundig specialisten, physician assistants, huidtherapeuten, dermatologieverpleegkundigen en diegenen die voor deze beroepen in opleiding zijn. Voor huisartsen geldt dat zij primair gebruik maken van NHG-richtlijnen. Als deze richtlijnen voor hen ontoereikend blijken te zijn, kunnen zij gebruik maken van deze richtlijn. Voor patiënten werd informatie op thuisarts.nl en een patiëntenfolder ontwikkeld.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn werd een multidisciplinaire werkgroep ingesteld. Bij het samenstellen van de werkgroep werd rekening gehouden met de geografische spreiding van de werkgroepleden en met een evenredige vertegenwoordiging van academische en niet-academische achtergrond. De werkgroepleden hebben onafhankelijk gehandeld en geen enkel lid ontving gunsten met het doel de richtlijnen te beïnvloeden.
|
Vereniging |
|
|
Dr. H. Röckmann (voorzitter) |
NVDV |
|
Prof. dr. T. Rustemeyer |
NVDV |
|
Dr. A.J. Oosting |
NVDV |
|
Drs. M. ter Avest |
NVZA |
|
Drs. G.H.P.R. Slabbers |
NVK |
|
Dr. G.F.H. Diercks |
NVVP |
|
Drs. Z. Tempels-Pavlica |
NIV |
|
Dr. I. Terreehorst |
NIV |
|
Dr. A.A.J.M. van der Ven |
NIV |
|
Prof. dr. R. Aarnoutse |
NVZA |
|
Drs. M.H.E. Vos |
Arts-onderzoeker NVDV |
|
Drs. Z. Çiftçi |
Arts-onderzoeker NVDV |
|
Drs. D.M. van Loon |
Arts-onderzoeker NVDV |
|
Drs. M. Stolting |
Arts-onderzoeker NVDV |
|
Drs. E. van Veen |
Arts-onderzoeker NVDV |
|
Drs. A.C. de Waal |
Arts-onderzoeker NVDV |
|
Ondersteuning werkgroep |
Vereniging |
|
Dr. W.A. van Enst |
Klinisch epidemioloog NVDV |
Tabel 1 Overzicht betrokken partijen
|
Overzicht betrokken partijen* |
Zitting neming in werkgroep |
Knelpunten analyse |
Commentaarfase |
Autorisatie |
Opmerkingen |
|
Wetenschappelijke verenigingen |
|||||
|
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
X |
X |
X |
X |
|
|
Nederlandse Vereniging voor Kindergeneeskunde (NVK) |
X |
X |
X |
X |
|
|
Nederlandse Internisten Vereniging (NIV) |
X |
X |
X |
X |
|
|
Nederlands Huisartsen Genootschap (NHG) |
|
X |
X |
|
|
|
Nederlandse Vereniging voor Medische Microbiologie (NVMM) |
|
X |
X |
|
|
|
Nederlandse Vereniging voor Klinische Geriatrie (NVKG) |
|
X |
X |
|
|
|
Nederlandse Vereniging voor ZiekenhuisApothekers (NVZA) |
X |
X |
X |
X |
|
|
Nederlandse Vereniging voor Pathologie (NVVP) |
X |
|
X |
X |
|
|
Nederlandse Vereniging voor Klinische Farmacologie (NVKFB) |
|
|
X |
|
|
|
Vereniging van Specialisten Ouderengeneeskunde (Verenso) |
|
|
X |
|
|
|
Overige organisaties |
|
|
|
|
|
|
Nederlandse Vereniging Huidtherapeuten (NVH) |
|
|
X |
|
|
|
Verpleegkundigen & Verzorgenden Nederland (V&VN) |
|
|
X |
|
|
|
Stichting Werkgroep Antibiotica Beleid (SWAB) |
|
X |
X |
|
|
|
Patiëntenverenigingen |
|||||
|
Huid Nederland (HN) |
|
|
X |
X |
|
|
Patiëntenfederatie Nederland |
|
|
X |
X |
|
|
Stakeholders |
|||||
|
Nederlandse Vereniging Ziekenhuizen (NVZ) |
|
|
X |
|
|
|
Nederlandse Federatie van Universitair Medische Centra (NFU) |
|
|
X |
|
Geen respons |
|
Zelfstandige klinieken Nederland (ZKN) |
|
|
X |
|
Geen deelname |
|
Zorgverzekeraars Nederland (ZN) |
|
|
X |
|
Geen deelname |
|
Zorginstituut Nederland (ZiN) |
|
|
X |
|
Geen deelname |
|
Vereniging Innovatieve Geneesmiddelen (VIG) |
|
|
X |
|
Geen deelname |
|
Inspectie Gezondheidszorg en Jeugd (IGJ) |
|
|
X |
|
Geen deelname |
*alle partijen werden uitgenodigd voor de knelpuntenanalyse (invitational conference) en de commentaarfase.
Deelname aan de werkgroep en autorisatie wordt enkel aan de wetenschappelijke verenigingen, patiëntenverenigingen en overige organisaties voorgelegd.
Belangenverklaringen
De KNMG-Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of ze in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van de Nederlandse Vereniging voor Dermatologie en Venereologie.
|
Werkgroeplid |
Hoofdfunctie(s) |
Nevenfunctie(s) |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Getekend op |
|
Dr. H. (Heike) Röckmann (voorzitter) |
Dermatoloog UMC Utrecht |
* Klinische adviesraad Lareb (onbezoldigd) |
Geen |
Nee |
Geen |
Geen |
Geen |
3-9-2020 |
|
Prof. Dr. T. (Thomas) Rustemeyer |
Dermatoloog Amsterdam UMC, locatie VUMC |
Geen |
nvt |
nvt |
nvt |
nvt |
nvt |
7-9-2020 |
|
Dr. A.J. (Bert) Oosting |
Dermatoloog Spaarne Gasthuis |
* Docent bij Uconsultancy, onderwijs doktersassistenten * Adviesraad Uconsultancy |
Geen |
Geen |
Geen |
Geen |
Geen |
2-9-2020 |
|
Drs. M. (Mendy) ter Avest |
Ziekenhuisapotheker in opleiding in het RadbouUMC/CWZ en PhD student in het RadboudUMC |
Geen |
nvt |
Nee |
Nee |
Nee |
Nee |
2-9-2020 |
|
Drs. G.H.P.R. (Gordon) Slabbers |
Kinderarts Ziekenhuis Bernhoven Uden |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
7-9-2020 |
|
Dr. M.B. (Miquel) Ekkelenkamp |
Arts-microbioloog UMC Utrecht |
Lid SWAB-ledenraad (onbetaald) |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
26-8-2020 |
|
Drs. Z. (Zana) Tempels-Pavlica |
Internist-allergoloog Diakonessenhuis |
* Lid commissie accreditatie en visitatie van NVvAKI (onbetaald) |
Geen |
Nee |
Geen |
Voornaamste belang is landelijk een duidelijk beleid opstellen. Mijn ziekenhuis zal daar ook van profiteren net als alle andere ziekenhuizen in NL. In mijn ziekenhuis wordt geneesmiddelen diagnostiek reeds volop gedaan dus er is geen marketing winst. |
Nee |
28-8-2020 |
|
Dr. I. (Ingrid) Terreehorst |
* Internist-allergoloog en staflid KNO bij AmsterdamUMC, 0,8FTE |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
3-9-2020 |
|
Dr. A.A.J.M. (Annick) van de Ven |
Internist-allergoloog-immunoloog UMC Groningen |
Geen |
Geen |
Geen |
Geen |
Geen |
Niet voor zover bekend |
31-8-2020 |
|
Drs. M (Marit) Stolting |
Arts-onderzoeker NVDV |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
30-09-2021 |
|
Drs. A.C. (Ayla) de Waal |
Arts-onderzoeker NVDV |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
21-10-2022 |
|
Drs. D.M. (Diederik) van Loon |
Arts-onderzoeker NVDV |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
21-10-2022 |
|
Drs. Z. (Zekeriya) Çiftçi |
Arts-onderzoeker NVDV |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Niet getekend; uit dienst oktober 2021 |
|
Drs. E. (Esther) van Veen |
Arts-onderzoeker NVDV |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Niet getekend; uit dienst april 2022 |
Inbreng patiëntenperspectief
Er is aandacht besteed aan het patiëntenperspectief door de bespreking van de waarden en voorkeuren voor de patiënt in de modules over behandeling. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de patiëntenvereniging Huid Nederland.
Implementatie
In de verschillende fasen van de ontwikkeling van de richtlijn is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. De richtlijn wordt via het internet verspreid onder alle relevante beroepsgroepen en ziekenhuizen en er zal in verschillende specifieke vaktijdschriften aandacht worden besteed aan de richtlijn. Tevens zal een samenvatting worden gemaakt. Het volledige implementatieplan is opgenomen in dit bijlagedocument.
Werkwijze
Knelpuntenanalyse
In de voorbereidingsfase heeft een bijeenkomst plaatsgevonden waarvoor alle belanghebbenden zijn uitgenodigd. In deze bijeenkomst zijn knelpunten aangedragen door de werkgroepleden. Hierbij zijn leden van de volgende verenigingen aanwezig geweest: NVDV, NVZA, NVK, NVMM, NIV, NVGK, NVVP en SWAB. Tevens werden de volgende verenigingen/instanties uitgenodigd, maar zijn niet aanwezig geweest: NHG (knelpunten wel aangedragen), NVKFB, Nederlandse Vereniging van Ziekenhuizen (NVZ), Zorginstituut Nederland (ZiN), Inspectie Gezondheidszorg en Jeugd (IGJ), Verenso, V&VN, Huid Nederland (HN) en de Nederlandse Federatie van Universitair Medische Centra (NFU).
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse heeft de werkgroep uitgangsvragen opgesteld. Daarbij inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken.
Strategie voor zoeken en selecteren van literatuur
Voor de afzonderlijke uitgangsvragen werd aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen en consultatie van experts. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. Literatuur is geselecteerd op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in Bijlage 4: Tabellen en figuren
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR - voor systematische reviews; Cochrane - voor gerandomiseerd gecontroleerd onderzoek; Newcastle-Ottowa - voor observationeel onderzoek; QUADAS II - voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen zijn overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE
|
Definitie |
|
Hoog
|
|
|
Redelijk
|
|
|
Laag
|
|
|
Zeer laag
|
|
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008) en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
C) Voor vragen over de waarde van meet- of classificatie-instrumenten (klinimetrie)
Deze instrumenten werden beoordeeld op validiteit, intra- (test-hertest) en inter-beoordelaarsbetrouwbaarheid, responsiviteit (alleen bij meetinstrumenten) en bruikbaarheid in de praktijk. (naar keuze: optie-1 ‘Bij ontbreken van een gouden standaard, werd een beoordeling van de bewijskracht van literatuurconclusies achterwege gelaten.’ Of optie-2 ‘De kracht van het wetenschappelijk bewijs werd bepaald met de generieke GRADE-methode’).
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg
Indicatorontwikkeling
Er werden geen indicatoren ontwikkeld voor deze richtlijn.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling beschreven (zie
Bijlage 10: Kennislacunes).
Juridische betekenis van richtlijnen
Richtlijnen zijn geen wettelijke voorschriften maar wetenschappelijk onderbouwde en breed gedragen inzichten en aanbevelingen waaraan zorgverleners zouden moeten voldoen om kwalitatief goede zorg te verlenen. Aangezien richtlijnen uitgaan van ‘gemiddelde patiënten’, kunnen zorgverleners in individuele gevallen zo nodig afwijken van de aanbevelingen in de richtlijn. Afwijken van richtlijnen is, als de situatie van de patiënt dat vereist, soms zelfs noodzakelijk. Een richtlijn beschrijft wat goede zorg is, ongeacht de financieringsbron (Zorgverzekeringswet (Zvw), Wet langdurige zorg (Wlz), Wet maatschappelijke ondersteuning (Wmo), aanvullende verzekering of eigen betaling door de cliënt/patiënt). Opname van een richtlijn in een register betekent dus niet noodzakelijkerwijs dat de in de richtlijn beschreven zorg verzekerde zorg is. Informatie over kosten zoals beschreven in de richtlijn is gebaseerd op beschikbare gegevens ten tijde van schrijven.
Commentaar- en autorisatiefase
De conceptrichtlijn is aan de betrokken (wetenschappelijke) verenigingen, (patiënt) organisaties en stakeholders voorgelegd ter commentaar. De commentaren zijn verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren is de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn is aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter autorisatie.
Referenties
- Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
- Higgins JPT, Green S (editors). Cochrane Handbook for Systematic Reviews of Interventions Version 5.1.0 [updated March 2011]. The Cochrane Collaboration, 2011. Available from www.handbook.cochrane.org.
- Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit.. Online beschikbaar op http://richtlijnendatabase.nl/ Laatst geraadpleegd op [DATUM geraadpleegd voor concepttekst]
- Van Everdingen JJE, Burgers JS, Assendelft WJJ, et al. Evidence-based richtlijnontwikkeling. Bohn Stafleu Van Loghum 2004.
- Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html
- Beijer HJ, de Blaey CJ. Hospitalisations caused by adverse drug reactions (ADR): a meta-analysis of observational studies. Pharm World Sci. 2002 Apr;24(2):46-54.
- Safety of Medicines. A guide to detecting and reporting adverse drug reactions. World Health Organization. Geneva. 2002. p.5.