Organisatie van zorg
Aanbeveling:
|
Zorg dat er binnen een week vanuit de afdeling longziekten contact wordt opgenomen met de patiënt na een longaanval astma waarvoor presentatie op de SEH of opname in het ziekenhuis nodig was. Indien dit daarna verantwoord wordt geacht, kan de patiënt overgedragen worden aan de huisarts. |
|
Reik aan elke astmapatiënt in de tweede lijn het astma actieplan (AAP) uit wanneer de diagnose astma wordt gesteld en bespreek dit plan. Op dit plan dient ook vermeld te worden welke zorgverlener(s) kan (kunnen) worden geraadpleegd in geval van problemen, zoals bijvoorbeeld een astmaconsulent, ook buiten kantoortijden. |
In dit hoofdstuk beschrijven wij de optimale zorg tijdens toename van de astmaklachten, een longaanval astma en de bijbehorende nazorg.
Er zijn 3 periodes te onderscheiden bij een longaanval astma. Deze periodes worden beschreven in de drie secties van deze module.
- Toename klachten van astma
- Longaanval astma
- Behandeling longaanval astma in de 1e lijn
- Behandeling longaanval astma in het ziekenhuis/SEH
- Nazorgperiode na verblijf ziekenhuis/SEH
1. Toename klachten van astma
Bij toename van astmaklachten hoort de patiënt zijn eigen astma actieplan te starten. Dit is belangrijk omdat hier bij uitstek de mogelijkheid ligt middels behandeling en instructies aan de patiënt om een longaanval astma te voorkómen. Een astma actieplan, geschreven of digitaal, is een ondersteuning voor de patiënt om klachten van astma te herkennen en zelf adequaat te handelen om verergering te voorkomen. Er is wetenschappelijk aangetoonde meerwaarde van een schriftelijk astma actieplan (Gibson, 2004; GINA, 2022; Schatz, 2009). Een opzet voor een astma actieplan is in samenwerking met de patiëntenverenigingen, NHG, NVALT en KNMP gemaakt, https://nederland-davos.nl/persoonlijk-astma-actie-plan/ of https://www.longfonds.nl/nieuws/houd-klachten-stabiel-met-het-persoonlijk-astma-actieplan-0. Dit astma actieplan kan worden gestart in de 1e lijn of in de 2e/3e lijn.
In dit plan staan twee dingen duidelijk beschreven:
1. wanneer en hoe de medicatie aan te passen
en
2. wanneer een patiënt contact moet zoeken met zijn zorgverlener of bij een longaanval astma naar een huisartsenpost, of SEH moet gaan.
Bij een levensbedreigende situatie zal 112 gebeld moeten worden.
2. Longaanval astma
1e lijn:
De astmazorg in de eerste lijn is beschreven in de NHG-standaard Astma bij volwassenen. Hier zijn ook criteria te vinden wanneer patiënt moet worden verwezen naar de 2e lijn bij een longaanval astma:
https://richtlijnen.nhg.org/standaarden/astma-bij-volwassenen
2e lijn:
Poliklinisch
Wanneer poliklinisch een longaanval astma wordt vastgesteld is het aan de polihoofdbehandelaar om in te schatten of dit ambulant behandeld kan worden of dat patiënt verwezen moet worden naar de SEH van het ziekenhuis. De behandeling van de longaanval astma op de SEH wordt in deze richtlijn beschreven, module 3 behandelt de prednisonstootkuur.
Management op SEH(/ziekenhuis).
Indien een patiënt zich op een SEH presenteert met verdenking op een longaanval astma moet eerst een inschatting worden gemaakt van de ernst. Ga altijd na of er wel sprake is van een longaanval astma of dat een alternatieve diagnose mogelijk is en onderzoek dat.
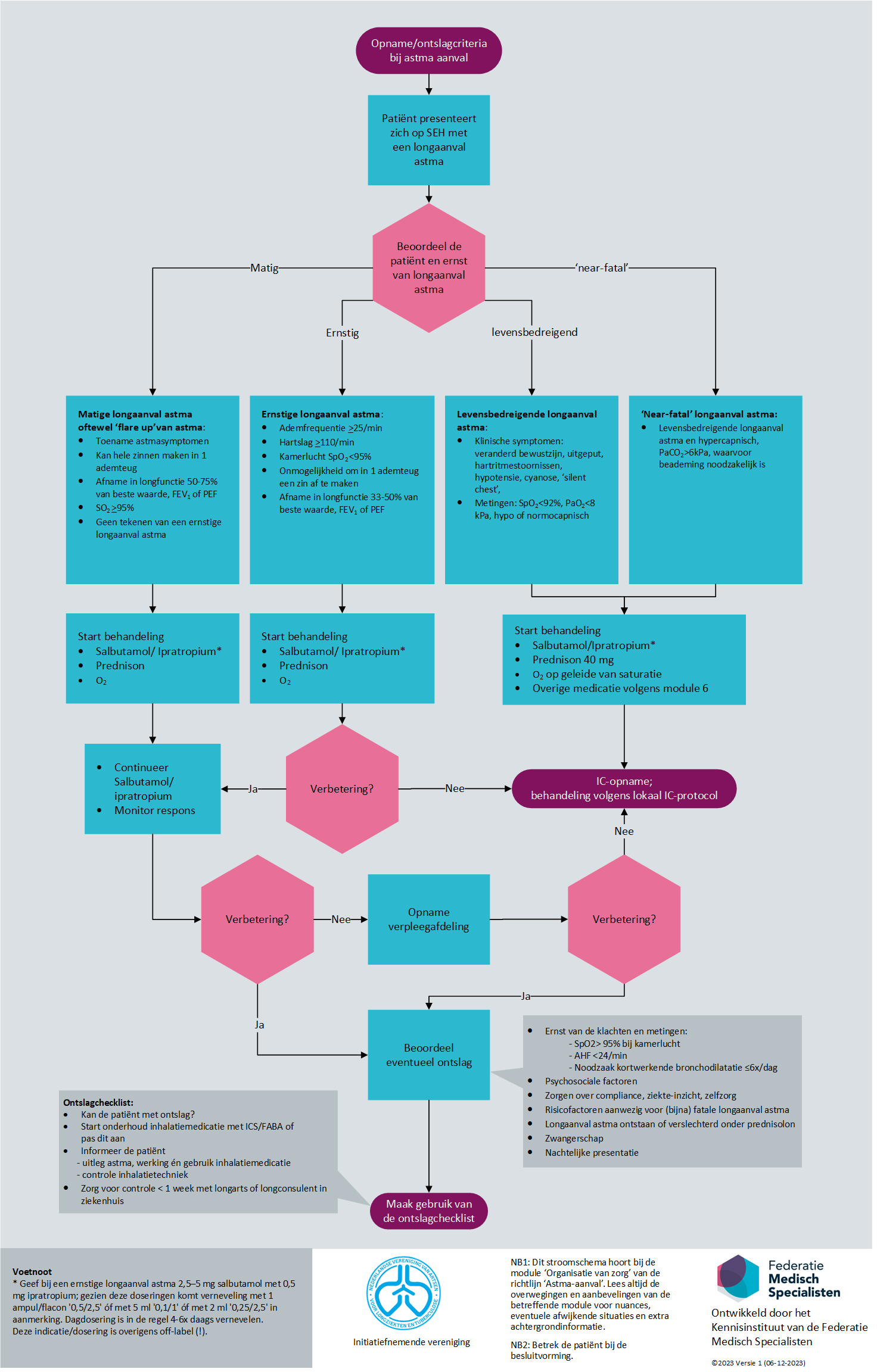
Bij het maken van een inschatting van de ernst van de aanval wordt gebruik gemaakt van objectieve metingen en klinische observaties (zie onderstaande Lijst 1 - Inschatting ernst longaanval astma). Tevens moet bekeken worden of er risicofactoren zijn voor een ernstige afloop (zie tabel 1). Dit bepaalt samen óf en waar (afdeling/IC) patiënt moet worden opgenomen. Het verrichten van een arterieel bloedgas wordt sterk aangeraden, zeker als de saturatie <95% is. Overweeg daarnaast het inzetten van virale diagnostiek in de vorm van een keelswab en het maken van een thoraxfoto. Het standaard blazen van longfunctie in de acute setting wordt niet aangeraden (zie Module Diagnostiek longfunctiemeters).
Lijst 1 - Inschatting ernst longaanval astma
https://www.brit-thoracic.org.uk/quality-improvement/guidelines/asthma/
- Matige longaanval astma oftewel ‘flare up’ van astma:
- Toename astmasymptomen
- Kan hele zinnen maken in 1 ademteug
- SpO2 >95%
- Geen tekenen van een ernstige longaanval astma
- Ernstige longaanval astma:
- Onmogelijkheid om in 1 ademteug een zin af te maken
- Ademfrequentie >25/min
- Hartslag >110/min
- Kamerlucht SpO2 <95%
- Levensbedreigende longaanval astma:
- Klinische symptomen: veranderd bewustzijn, uitgeput, hartritmestoornissen, hypotensie, cyanose, ‘silent chest’,
- Ademfrequentie >25/min
- Hartslag >110/min
- Kamerlucht SpO2<92%,
- Bloedgas: PaO2<8 kPa (60 mmHg), hypo- of normocapnisch.
- ‘near-fatal’ longaanval astma:
- Levensbedreigende longaanval astma en hypercapnisch, PaCO2>6kPa (45 mmHg), waarvoor beademing noodzakelijk is.
Tabel 1 - Patiënten met verhoogd risico op het ontwikkelen van een levensbedreigende longaanval astma – naar BTS Guideline, 2019
|
Een combinatie van ernstig astma gekenmerkt door: |
EN risicoverhogende factoren, psychologische of gedragskenmerken, waaronder één of meer van: |
|
|
Bij het stellen van de diagnose longaanval astma moet zo snel mogelijk gestart worden met behandelen:
Geef:
- Bronchodilatatie middels beta2-agonisten (SABA) in combinatie met kortwerkende parasympaticolytica (SAMA) middels een dosisaerosol met voorzetkamer of middels vernevelingen, zie module 5.
- Prednisolon 40mg per os en als dit niet mogelijk is iv, gedurende 5 dagen, en wanneer onvoldoende effect maximaal 14 dagen, zie module 3.
- O2 suppletie, waarbij een SpO2 >94% moet worden nagestreefd en bij zwangere vrouwen >95%.
Monitor de patiënt en de metingen nauwlettend en stuur afhankelijk hiervan de behandeling en het beleid bij. Let hierbij op de klinische conditie van de patiënt, de saturatie en de ademhalingsfrequentie.
Vraag de intensivist in consult bij uitblijven van snelle verbetering en/of bij een ernstige aanval.
Controleer en evalueer de onderhoudsbehandeling (in principe ICS/LABA) voor astma bij een bekende patiënt en start deze bij een patiënt met een nieuwe (veronderstelde) diagnose astma.
Eventuele voor de hand liggende triggers zoals roken, LWI of allergie kunnen alvast met patiënt besproken/geadresseerd worden.
Ter beoordeling of patiënt klaar is voor een ontslag naar huis moeten onderstaande factoren worden meegewogen:
Lijst 2 – ontslagomstandigheden
- Ernst van de klachten en metingen:
- SpO2> 95% bij kamerlucht
- AHF <24/min
- Noodzaak kortwerkende bronchodilatatie ≤6x/dag
- Psychosociale factoren
- Zorgen over compliance, ziekte-inzicht, zelfzorg
- Risicofactoren voor (bijna) fatale longaanval astma (zie tabel)
- Longaanval astma ontstaan of verslechterd onder prednisolon
- Zwangerschap
- Nachtelijke presentatie
Als besloten is om patiënt wel op te nemen voor verdere monitoring en behandeling dan is goede informatievoorziening aan patiënt, van grote meerwaarde.
Zorg daarom vóór ontslag voor:
- Uitleg over astma, werking en gebruik (inhalatie)medicatie. Hierbij kan gebruik gemaakt worden van (digitale) schriftelijke informatie/website/e-health en thuisarts.nl.
- Geef patiënt instructie bij welke klachten hij/zij contact op moet nemen en met wie, geef dit op papier of digitaal mee.
- Controle inhalatietechniek (door bijvoorbeeld (long)verpleegkundige of medewerker apotheek)
- Zie hiervoor: www.inhalatorgebruik.nl
- Een controle binnen 1 week (zie hoofdstuk Corticosteroïden bij longaanval astma)
Zowel astmapatiënten als hun zorgverleners ervaren dat gegevensuitwisseling tussen de verschillende zorgverleners (huisarts-ziekenhuis-apotheek) niet altijd optimaal verloopt. Dit kan negatieve gevolgen hebben zoals tijdsverlies, kans op fouten, en verlies aan vertrouwen van de patiënt die vaker dan nodig is zijn/haar verhaal moet vertellen. Een ontslagbrief van de SEH en de afdeling zal <24 uur moeten worden verstuurd. Zelfs dan is de informatievoorziening nog niet altijd optimaal. Er bestaat volgens de werkgroep dan ook een grote wens om dit op nationaal niveau te verbeteren. Het persoonlijk zorgdossier zou de communicatie tussen hulpverleners dan ook kunnen verbeteren.
Tabel 2 - Checklist voor ontslag van de SEH of na opname
|
Zie Lijst 2 - Ontslagomstandigheden |
|
|
||
|
||
|
a. uitleg astma, werking én gebruik inhalatiemedicatie
|
||
|
b. controle inhalatietechniek
|
||
|
||
3. Na verblijf in het ziekenhuis
Het is belangrijk dat ook de zorg ná het verblijf in het ziekenhuis goed geregeld is omdat:
Patiënten in deze periode nog veel klachten kunnen hebben die adequaat behandeld moeten (blijven) worden.
De klachten weer kunnen toenemen en patiënten moeten weten wat ze dan moeten doen.
Patiënten soms nog onvoldoende bekend zijn met hun ziekte, behandeling en hoe hiermee om te gaan.
Ter preventie van een recidief en bereiken van aanhoudend goede astmacontrole
De toename van klachten gepaard kan gaan met onzekerheid en negatieve gevoelens.
Juist daarom beveelt de werkgroep aan in de eerste week na opname/SEH-presentatie een contactmoment te plannen voor een eerste evaluatie. Dit betreft dan een afspraak met de longarts of een andere deskundige zoals bijvoorbeeld een astmaconsulent of physician assistent of een verpleegkundig specialist. Hierbij dient aan bod te komen:
- Klachten.
- Astma actieplan indien reeds in bezit.
- Medicatiegebruik.
- Mogelijkheid om in te gaan op vragen/zorgen.
- Eventueel al ingaan op meest relevante triggers/treatable traits.
- Inschatting maken op welke termijn patiënt op de poli moet komen voor verdere evaluatie en aanvullend onderzoek zoals longfunctie en fenotypering volgens de richtlijn Tweedelijns Astmazorg .
Indien al gebruikt gemaakt wordt van telemonitoring dan kan dit juist nu goed worden ingezet.
Tevens wordt geadviseerd om zo snel mogelijk na het verblijf op SEH/ziekenhuis een astma actieplan mee te geven indien patiënt deze nog niet heeft LINK naar eerste stukje over AAP.
Een opname in een ziekenhuis of SEH-presentatie in verband met een longaanval astma is een sterk signaal dat er sprake is van:
- ernstige klachten en/of
- onvoldoende goede behandeling en/of
- onvoldoende zelfmanagement
Daarom bevelen wij aan dat deze patiënten in principe eerst onder behandeling blijven staan van de longarts en/of longverpleegkundige. Pas als zij voldoende in kaart gebracht zijn en de inschatting is dat dat kan, zal de patiënt weer overgedragen worden aan de huisarts. Zie hiervoor ook de richtlijn Tweedelijns astmazorg (in ontwikkeling)
Figuur 1 – Stroomschema met opname- en ontslagcriteria bij patiënten met een longaanval astma.
Afkortingen: FABA, fast-acting-β2-agonists
Belangrijkste adviezen vanuit de werkgroep:
- Elke patiënt moet een AAP krijgen mét 24/7 contactinformatie
- Na verblijf ziekenhuis/SEH i.v.m. een longaanval astma: eerst follow up via 2e lijn
- Binnen 1 week na ontslag contactmoment voor eerste evaluatie
Potentieel knelpunt:
Implementatie van bovenstaande: met name de beschikbaarheid van astmaconsulent die binnen 1 week contact kan opnemen met patiënt en er moet ook voldoende capaciteit zijn om uiteindelijk aan iedereen een longaanval astma actieplan mee te geven en te bespreken. Onze inschatting is dat juist een longaanval astma actie plan eventuele toekomstige zorgconsumptie kan voorkomen.
Websites:
https://www.longfonds.nl/longziekten/astma/omgaan-met-astma/astma-aanval
https://nederland-davos.nl/persoonlijk-astma-actie-plan/
https://richtlijnen.nhg.org/standaarden/astma-bij-volwassenen
Onderbouwing
Referenties
- Gibson PG, Powell H. Written action plans for asthma: an evidence-based review of the key components. Thorax. 2004 Feb;59(2):94-9. doi: 10.1136/thorax.2003.011858. PMID: 14760143; PMCID: PMC1746945.
- Reddel HK, Bacharier LB, Bateman ED, Brightling CE, Brusselle GG, Buhl R, Cruz AA, Duijts L, Drazen JM, FitzGerald JM, Fleming LJ, Inoue H, Ko FW, Krishnan JA, Levy ML, Lin J, Mortimer K, Pitrez PM, Sheikh A, Yorgancioglu AA, Boulet LP. Global Initiative for Asthma Strategy 2021: executive summary and rationale for key changes. Eur Respir J. 2021 Dec 31;59(1):2102730. doi: 10.1183/13993003.02730-2021. PMID: 34667060; PMCID: PMC8719459.
- Schatz M, Rachelefsky G, Krishnan JA. Follow-up after acute asthma episodes: what improves future outcomes? Proc Am Thorac Soc. 2009 Aug 1;6(4):386-93. doi: 10.1513/pats.P09ST6. PMID: 19675349.
Verantwoording
Autorisatiedatum en geldigheid
Laatst beoordeeld : 19-02-2024
Laatst geautoriseerd : 19-02-2024
Geplande herbeoordeling : 19-02-2027
Algemene gegevens
De ontwikkeling van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2020 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg rondom de longaanval astma.
Samenstelling werkgroep
- Dr. E.J.M. (Els) Weersink, longarts, Amsterdam UMC te Amsterdam, NVALT (voorzitter)
- Drs. A. (Annelies) Beukert, longarts, Martini Ziekenhuis te Groningen, NVALT
- Dr. G.J. (Gert-Jan) Braunstahl, longarts, Franciscus Gasthuis & Vlietland te Rotterdam, NVALT
- Drs. R.C. (Rachel) Numan, AIOS longgeneeskunde, HagaZiekenhuis te ’s Gravenhage, NVALT
- Drs. L.C. (Louise) Urlings-Strop, intensivist, Reinier de Graaf Ziekenhuis, Delft, NVIC
- Drs. F.E.C. Geijsel, SEH-artsKNMG, OLVG te Amsterdam, NVSHA
- Dr. E.C. (Erwin) Vasbinder, ziekenhuisapotheker, Franciscus Gasthuis & Vlietland te Rotterdam, NVZA
- Prof. Dr. J.W.M. (Jean) Muris, huisarts en hoogleraar huisartsgeneeskunde, Maastricht UMC+ te Maastricht, NHG
- M.H.A. (Mariëtte) Scholma MSc, verpleegkundig specialist longziekten, Wilhelmina Ziekenhuis Assen te Assen, V&VN
- L.A.M. (Betty) Frankemölle, patiëntvertegenwoordiger, Longfonds
- M.A.P. (Marjo) Poulissen, patiëntvertegenwoordiger, Longfonds
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Weersink* |
Longarts, afdeling longziekten Academisch Medisch Centrum, Amsterdam |
voorzitter RL ernstig astma (afgerond) |
In 2017 voor meerdere farmaceutische bedrijven een betaald adviseurschap. (GSK, Novartis, TEVA, Chiesi Boehringer). In 2019-2020 nog wel adviseurschap niet meer tegen betaling. 2019: dienstverlening, bijdrage aan sympsoium van Astra Zeneca, Novartis, Genzyme BV 2019: vergoeding gastvrijheid Genzyme BV.
Bestuurslid stichting RAPSODI, de stichting die de database voor ernstig astma beheerd en mede gefinancierd wordt door ZONMW, Novartis, GSK, TEVA, Astra Zeneca en Sanofi. Hier is inmiddels een governance vastgelegd welke rol de farmaceuten hierbij hebben. |
Geen actie |
|
Urlings |
Intensivist (longarts) – Reinier de Graaf Gasthuis |
Waarneming diverse ziekenhuizen Intensive Care – betaald |
Geen |
Geen actie |
|
Vasbinder |
ziekenhuisapotheker |
Redacteur van medisch-farmaceutisch handboek “Praktische Farmacotherapie bij Longaandoeningen”, betaald door uitgever Lannoo Campus |
Betrokken bij meerdere onderzoeken bij patiënten met moeilijk behandelbaar/ernstig astma dat financieel wordt ondersteund door: * diverse zorgverzekeraars * TEVA (farmaceutische industrie) * Astra Zeneca (hoofdonderzoeker)
Geneesmiddeleninkoop voor het ziekenhuis, waaronder biologicals, verwachting dat deze binnen het kader van deze RL niet relevant zijn |
Geen actie |
|
Muris |
Universiteit Maastricht 1.0 fte Huisartspraktijk Geulle 17 werkdagen spreekuur / jaar |
Geen |
Webinar over orale corticosteroïden bij astma (GSK) |
Geen actie |
|
Geijsel |
SEH arts KNMG bij OLVG, tevens plaatsvervangend opleider en fellow opleider (95%) SEH arts bij MyEmergencyDoctor, Australische werkgever, telehealth (5%) |
EM-masterclass ontwikkelaar en faculty (betaald) |
Geen |
Geen actie |
|
Poulissen |
Projectleider zorg Longfonds full time (met detachering voor 12 uur naar astmaVereniging Nederland en Davos). |
Geen |
Geen |
Geen actie |
|
Beukert |
longarts te Martini Ziekenhuis Groningen tot 1-8-2021 Longarts te Deventer Ziekenhuis, Deventer, vanaf 23-8-2021 |
Secretaris Sectie Astma en Allergie (SAA) van de NVALT, onbetaald Lid werkgroep binnen SAA over biologicals, onbetaald |
Enkele keer deelname aan een betaalde adviesraadbijeenkomst (laatste in 2021, over biologicals) bij farmaceut maar dat houdt m.i. geen relatie met de inhoud van deze richtlijn |
Geen actie |
|
Numan |
AIOS longgeneeskunde HAGA ziekenhuis |
Geen |
Geen |
Geen actie |
|
Frankemölle |
Vrijwilligster bij het Longfonds, lid van de Longfonds Ervaringsdeskundigengroep. astmaVereniging Nederland en Davos Vrijwilligster European Lung Foundation, lid van SHARP |
Ik neem deel aan diverse werkgroepen maar geen van allen heeft als hoofdthema astma-aanval. |
Geen |
Geen actie |
|
Braunstahl |
Longarts, Franciscus Gasthuis & Vlietland Rotterdam |
Null-aanstelling ErasmusMC voor onderzoek: onbetaald. Deelname RL ernstig astma en KNO-RL, obesitas |
Vergoeding: Presentaties en incidenteel advieswerk voor Boehringer Ingelheim, Sanofi, Novartis, GSK, AstraZeneca, ALK, MEDA en Chiesi. (wrsch speelt deze longmedicatie geen rol in deze richtlijn)
Deelname richtlijn ernstig astma Deelname klankbordgroep van het project ‘Obesitas volwassenen’
Webinar over orale corticosteroïden bij astma (GSK)
Geen vergoeding: Redactie NTvAAKI Bestuur RoLeX astma/COPD nascholingen Bestuur Rapsodi, ernstig astma database NL Voorzitter astmasectie NVALT Wetenschappelijke adviescommissie Longfonds |
Geen actie |
|
Scholma |
Verpleegkundig specialist longziekten Wilhelmina Ziekenhuis Assen |
vrijwilliger longfonds, expertgroep zorgaanpak COPD (chiesi). Geen relatie met longaanval astma voorzitter kwaliteitsteam Assen van de HZD |
Geen |
Geen actie |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntperspectief door afgevaardigde patiëntenvereniging Longfonds in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan het Longfonds en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Wkkgz & Kwalitatieve raming van mogelijke substantiële financiële gevolgen
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming blijkt dat er waarschijnlijk geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
|
Module |
Uitkomst raming |
Toelichting |
|
Module Organisatie van zorg |
Geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten) en zal daarom naar verwachting geen substantiële financiële gevolgen hebben voor de collectieve uitgaven. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten met een longaanval astma.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodi
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. Doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. Doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. Doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. Doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. Doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. Doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.