Spondylodese techniek lage rugpijn
Uitgangsvraag
Wat is de beste chirurgische techniek van spondylodese voor de indicatie chronische lage rugpijn?
Aanbeveling
Er is geen verschil in effectiviteit tussen de verschillende technieken van spondylodese bij patiënten met chronische lage rugpijn. De techniek van voorkeur dient te worden bepaald door de specifieke pathologie van de individuele patiënt en de expertise van de behandelend chirurg.
Het wordt aanbevolen lumbale spondylodese bij patiënten met chronische lage rugpijn bij voorkeur in trial verband plaats te laten vinden. De indicatie tot spondylodese dient te worden gesteld in een multidisciplinair overleg na falen van langdurige gestructureerde conservatieve therapie.
Overwegingen
Minimaal invasieve versus open technieken
Argumenten pro: een mogelijk kortere opnameduur met snellere revalidatie/return-to-work.
Argumenten contra: learning curve met mogelijk (aanvankelijk) meer complicaties.
De klinische relevantie van de resultaten is onduidelijk. Korte termijn resultaten van de minimaal invasieve technieken werden niet gegeven. Hier kan juist de klinische relevantie van minimaal invasieve chirurgie liggen, in de zin van een vlotter herstel met snellere return-to-work. Op de langere termijn zijn er geen verschillen voor effectiviteit. Bij een gebrek aan gegevens over kosteneffectiviteit van beide technieken kan ook op dat aspect geen afweging gemaakt worden.
Posterolaterale (PLF) versus intervertebrale spondylodese (TLIF/PLIF)
Argumenten pro: een intervertebrale cage kan bijdragen aan een stabielere spondylodese met minder kans op pseudarthrose en mogelijk beter herstel van het alignement van de lumbale wervelkolom.
Argumenten contra: het gebruik van cages gaat gepaard met hogere kosten, voor een circumferentiële spondylodese met ALIF geldt daarbij nog tevens de extra chirurgische benadering met dito verhoogd complicatie risico en de verlengde OK-tijd. Voor een TLIF/PLIF ten opzichte van posterolaterale spondylodese geldt de langere OK-tijd met meer bloedverlies (Hoy, 2013) en verhoogd complicatie-risico (2,4 keer zoveel complicaties bij cages ten opzichte van PLF (Fritzell, 2002).
Er zijn geen verschillen in klinische effectiviteit, maar mogelijk wel in kosten. Er zijn nog onvoldoende gegevens over de kosteneffectiviteit van de PLF en TLIF/PLIF bij deze patiënten. Toekomstige studies zullen hier meer informatie over moeten verstrekken.
Op basis van de wetenschappelijke literatuur kan er geen eenduidig antwoord worden gegeven wat de beste chirurgische techniek van spondylodese is bij de indicatie chronische lage rugpijn. Literatuur conclusies rondom de technieken PLF, PLIF en TLIF en hun klinische resultaat bij patiënten met chronische lage rugpijn zijn van lage kwaliteit en onvoldoende discriminerend om een eenduidige uitspraak te kunnen doen betreffende de vraagstelling in deze module.
Indien overwogen wordt om patiënten met primaire rugpijn op basis van degeneratieve wervelkolomafwijkingen te behandelen, dienen ook factoren als veiligheid, kosteneffectiviteit, voorkeur operateur en de beschikbaarheid van een geprotocolleerd na-traject te worden meegenomen.
Kennishiaat
Wat is de waarde van een lumbale spondylodese bij chronische lage rugpijn na falen van gestructureerde multidisciplinaire conservatieve therapie en hoe kunnen de juiste patiënten hiervoor geselecteerd worden.
Onderbouwing
Achtergrond
Er bestaan diverse chirurgische benaderingen en operatietechnieken voor het verrichten van een geïnstrumenteerde spondylodese van de lumbale wervelkolom. Hierin is de afgelopen jaren een enorme ontwikkeling geweest qua aantallen operaties en qua diversiteit aan operatieve technieken en implantaten, mede gedreven door de omvangrijke industrie op dit gebied. Uiteraard is de keuze van de chirurgische benadering (anterieur, posterieur, lateraal of circumferent) afhankelijk van de specifieke indicatie en de aard van de aandoening waarvoor de spondylodese wordt verricht. Ook andere factoren zoals voorkeur van de patiënt en de chirurg of comorbiditeit kunnen daarbij een rol spelen. Maar los van deze overwegingen rijst de vraag of de effectiviteit van de verschillende beschikbare technieken op voldoende bewijs is gebaseerd en of een bepaalde techniek betere resultaten en/of minder complicaties geeft dan de andere.
Conclusies
Indicatie chronische lage rugpijn
|
Zeer laag |
Minimaal invasieve TLIF (Mini-open) spondylodese leidt tot een vergelijkbare pijnvermindering ten opzichte van de open TLIF-procedure.
Bronnen (Rodriguez-Vela, 2013) |
|
Zeer laag |
Minimaal invasieve(Mini-open) TLIF leidt tot een vergelijkbare verbetering qua functioneren ten opzichte van de open TLIF.
Bronnen (Rodriguez-Vela, 2013) |
|
Zeer laag |
Minimaal invasieve(Mini-open) TLIF leidt niet tot een betere kwaliteit van leven dan open chirurgie TLIF.
Bronnen (Rodriguez-Vela, 2013) |
|
Hoog |
PLIF geeft vergelijkbare vermindering van pijn als PLF.
Bronnen (Christensen, 2002; Videbaek, 2006; Videbaek, 2010; Videbaek, 2011; Soegaard, 2007; Hoy, 2013; Christensen, 2014; Fritzell, 2002; Fritzell, 2003) |
|
Hoog |
PLIF geeft vergelijkbare verbetering qua functioneren als PLF.
Bronnen (Christensen, 2002; Videbaek, 2006; Videbaek, 2010; Videbaek, 2011; Soegaard, 2007; Hoy, 2013; Christensen, 2014; Fritzell, 2002; Fritzell, 2003) |
|
Gemiddeld |
Er werd geen verschil gezien tussen PLIF en PLF wat betreft kwaliteit van leven.
Bronnen (Christensen, 2002; Videbaek, 2006; Videbaek, 2010; Videbaek, 2011; Soegaard, 2007; Hoy, 2013; Christensen, 2014; Fritzell, 2002; Fritzell, 2003) |
Samenvatting literatuur
Minimaal invasieve versus open technieken
Voor de vergelijking van minimaal invasieve en open technieken, in dit geval voor het uitvoeren van een TLIF, werd één RCT (Rodriguez-Vela, 2013) geïncludeerd met een hoog risico op bias door gebrekkige randomisatie techniek en beschrijving van de resultaten, zie ‘Table of quality assessment’ onder evidence tabellen.
Pijn (VAS-schaal)
Zij vonden geen verschillen tussen de groepen in been- of rugpijn na drie jaar. De preoperatieve VAS was 70 voor minimaal invasieve chirurgie en 71 voor open chirurgie De VAS-resultaten waren respectievelijk 34 mm rugpijn voor minimaal invasieve chirurgie en 46 rugpijn voor open chirurgie (Rodriguez-Vela, 2013).
Functioneren (Disability)
Er waren geen verschillen (p=0,07) in functioneren (ODI) na drie jaar. De preoperatieve ODI was 27,2 (sd 8,2) voor minimaal invasieve chirurgie en 28,9 (sd 5,5) voor open chirurgie. De postoperatieve ODI was 12,1 (sd 7,6) voor minimaal invasieve chirurgie en 18.1 (sd 12,5) voor open chirurgie (Rodriguez-Vela, 2013).
Kwaliteit van leven
Zij vonden geen verschillen in kwaliteit van leven (SF36) na drie jaar. De SF-36 was 59 (sd 19) voor de minimaal invasieve chirurgie en 52 (sd 23) voor de open chirurgie (Rodriguez-Vela, 2013).
Posterolaterale (PLF) versus posterieure intervertebrale spondylodese (PLIF)
Voor de vergelijking van posterolaterale lumbale spondylodese (PLF) en posterieure lumbale intervertebrale spondylodese (PLIF of TLIF) werden 3 RCTs (Christensen, 2002; Fritzell, 2002; Hoy, 2013) geïncludeerd.
Rugpijn (VAS-schaal)
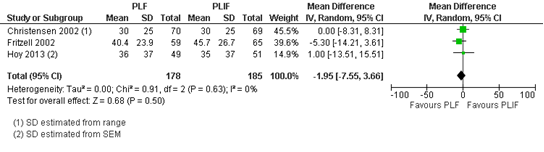
Drie RCTs (Christensen, 2002; Fritzell, 2002; Hoy, 2013) lieten een gemiddeld gepoolde rugpijnscore zien na twee jaar follow-up van -1,95 (95%BI [-7,55; 0,66]) (zie figuur 1), dit verschil is niet statistisch significant.
Figuur 1 Gepoolde VAS-rugpijn scores twee jaar na posterolaterale lumbale spondylodese dan wel posterieure lumbale intervertebrale spondylodese.
Functioneren (Disability)
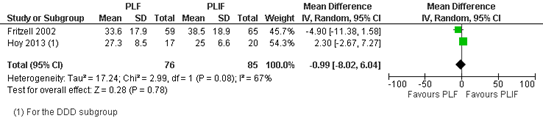
Twee RCTs (Fritzell, 2002; Hoy, 2013) lieten geen verschil zien in functioneren na twee jaar (figuur 2), gemiddeld verschil -0,99 (95% BI [-8,02; 6,04]).
Figuur 2 Gepoolde Oswestry Disability Index scores rugpijn scores twee jaar na posterolaterale lumbale spondylodese dan wel posterieure lumbale intervertebrale spondylodese.
Kwaliteit van leven
Twee RCTs (Christensen, 2002; Hoy, 2013) lieten geen verschil zien in kwaliteit van leven (werk (DPQ), SF-36) na twee jaar. De studie van Christensen (secondaire publicatie van Videbeak 2006) liet significante meer verbetering zien op de SF-36 physical component scale na vijf tot negen jaar voor de PLIF-groep (33 versus 39, p=0,005), met geen verschil in de mental component score.
Bewijskracht van de literatuur
Minimaal invasieve versus open technieken
Aangezien er slechts één RCT (Rodriquez-Vela, 2013) werd gevonden die overigens van lage kwaliteit is wegens slechte randomisatie en blindering, is het uiteindelijke oordeel over de bewijskracht van alle uitkomstparameters “zeer laag” (één studie, bewijskracht verlaagd wegens high risk of bias).
Posterolaterale (PLF) versus posterieure lumbale intervertebrale spondylodese (PLIF/TLIF)
Drie RCTs van goede kwaliteit (Christensen, 2002; Fritzell, 2002; Hoy, 2013) laten een consistent resultaat zien op pijn en functioneren, waardoor het uiteindelijke oordeel over de bewijskracht hoog is.
Zoeken en selecteren
In de databases Medline (Pubmed), Embase en Cochrane is met relevante zoektermen gezocht naar studies over geïnstrumenteerde chirurgische ingrepen bij lage rug- en/of beenpijn. Er werd eerst een overkoepelende search verricht gericht op reviews en vervolgens een aanvullende search naar mogelijke nieuwe primaire studies.
De volgende PICO geldt als uitgangspunt voor de zoekstrategie:
P: patiënten met lumbale spondylolisthesis, adulte deformiteiten, failed back surgery syndroom, (recidief) HNP, recessus-, neuroforamen- of kanaalstenose, of patiënten met chronische lage rugpijn en aspecifieke degeneratieve kenmerken op beeldvorming;
I en C: interventies en controlebehandelingen kunnen zijn: anterieur; intercorporeel (ALIF), posterieur; posterolaterale spondylodese of intercorporeel (PLIF), lateraal; intercorporeel (XLIF), circumferent; anterieur of lateraal gecombineerd met posterieur, of minimaal invasief;
O: outcomes dienen te zijn: pijnbeleving (VAS); functioneren (ODI; SF-36; EQ-5D); kwaliteit van leven (psychosociaal functioneren); majeure postoperatieve complicaties, fusion rate, of adjacent segment disease rate.
De zoekverantwoording is weergegeven onder zoekverantwoording. De literatuurzoekactie leverde 899 mogelijke systematische reviews op. Studies werden geselecteerd op grond van de volgende selectiecriteria:
- de studie was een systematische review naar chirurgische interventies voor aandoeningen aan de lage rug;
- de zoekstrategie en inclusiecriteria waren gericht op de selectie van gerandomiseerde trials;
- de aandoening die onderzocht werd betrof disc herniatie met radiculopathie, spondylolisthesis, spinale stenose, degenerative deformiteiten (scoliose), re-herniatie (inclusief “failed back surgery syndrome”), of degeneratieve disc aandoeningen. Studies gericht op fracturen, maligniteiten, ankyloserende spondylitis en cauda equina syndroom werden geëxcludeerd. Als een serie indicaties werd gepresenteerd, maar niet per aandoening geanalyseerd, werd het artikel geëxcludeerd;
- de interventies die bestudeerd werden betroffen chirurgische interventies zoals decompressie of spondylodese chirurgie, vergeleken met conservatieve therapie of pijnbehandelingen;
- uitsluitend systematische reviews met een beschreven search strategie (i.e., meerdere databases (inclusief Pubmed en Cochrane (CDSR and DARE) en extensief gebruik van search string combinaties) en een risk of bias assessment (ten minste gericht op selectie bias) werden geïncludeerd;
- studies gepubliceerd voor 2001 werden geëxcludeerd aangezien deze niet meer representatief worden geacht voor de huidige behandelingen.
Op basis van titel en abstract werden in eerste instantie negen systematische reviews voorgeselecteerd (zie Bijlage: Selectie overkoepelende search systematische reviews). Na raadpleging van de volledige tekst, werden vervolgens vier reviews geëxcludeerd, en vijf reviews definitief geselecteerd (Fallatah, 2013; Jacobs, 2006; Liu, 2014; Martin, 2007; Watters, 2009) die alle de indicatie Spondylolisthesis, spondylolysis of spondylolytische spondylolisthesis behandelden. Voor de indicatie adulte deformiteiten werden geen systematische reviews van voldoende kwaliteit gevonden.
Voor de indicatie chronische lage rugpijn werden geen systematische reviews van voldoende kwaliteit gevonden. Voor de vergelijking van minimaal invasieve en open technieken werd één RCT (Rodriguez-Vela, 2013) geïncludeerd. Voor de vergelijking van posterolaterale lumbale spondylodese (PLF) en posterieure lumbale intervertebrale spondylodese (PLIF of TLIF) werden drie RCTs geïncludeerd, met zes secundaire publicaties.
Relevante uitkomstmaten
De werkgroep achtte pijnbeleving op een visueel analoge schaal (VAS); functioneren (Oswestry Disability Index (ODI)); kritieke uitkomstmaten; en kwaliteit van leven (SF-36; EQ-5D) en psychosociaal functioneren zijn belangrijke uitkomstmaten voor de besluitvorming.
Pijn (VAS-schaal)
Pijn werd gemeten met de VAS-schaal. Scores op deze schaal lopen van 0 tot 100, waarbij 0 geen pijn aangeeft en 100 de ergst voorstelbare pijn.
Functioneren (Disability)
Invaliditeit werd gemeten met behulp van de Oswestry Disability Index score (ODI). Scores op deze schaal lopen van 0 tot 100, waarbij lagere scores minder ernstige invaliditeit aangeven.
Kwaliteit van leven
Functionaliteit werd gemeten met de SF-36 vragenlijst en EQ-5D vragenlijst. Scores op de SF-36 vragenlijst lopen van 0 tot 100, waarbij hogere scores een betere gezondheidsstatus aangeven.
Referenties
- Christensen FB, Hansen ES, Eiskjaer SP, et al. Circumferential lumbar spinal fusion with Brantigan cage versus posterolateral fusion with titanium Cotrel-Dubousset instrumentation: a prospective, randomized clinical study of 146 patients. Spine (Phila Pa 1976). 2002;27(23):2674-83. PubMed PMID: 12461393.
- Fallatah S, Wai E, Baily CS. The value of adding posterior interbody fusion in the surgical treatment of degenerative lumbar spine disorders: A systematic review. Int J Spine Surg. 2013;7:e24-8.
- Fritzell P, Hägg O, Wessberg P, et al. Chronic low back pain and fusion: a comparison of three surgical techniques: a prospective multicenter randomized study from the Swedish lumbar spine study group. Spine (Phila Pa 1976). 2002;27(11):1131-41. PubMed PMID: 12045508.
- Høy K, Bünger C, Niederman B, et al. Transforaminal lumbar interbody fusion (TLIF) versus posterolateral instrumented fusion (PLF) in degenerative lumbar disorders: a randomized clinical trial with 2-year follow-up. Eur Spine J. 2013;22(9):2022-9.
- Jacobs WC, Vreeling A, De Kleuver M. Fusion for low-grade adult isthmic spondylolisthesis: a systematic review of the literature. Eur Spine J. 2006;15(4):391-402. Review. PubMed PMID: 16217665; PubMed Central PMCID: PMC3489314.
- Liu X, Wang Y, Qiu G, et al. A systematic review with meta-analysis of posterior interbody fusion versus posterolateral fusion in lumbar spondylolisthesis. Eur Spine J. 2014;23(1):43-56.
- Martin CR, Gruszczynski AT, Braunsfurth HA, et al. The surgical management of degenerative lumbar spondylolisthesis: a systematic review. Spine (Phila Pa 1976). 2007;32(16):1791-8. PubMed PMID: 17632401.
- Rodríguez-Vela J, Lobo-Escolar A, Joven E, et al. Clinical outcomes of minimally invasive versus open approach for one-level transforaminal lumbar interbody fusion at the 3- to 4-year follow-up. Eur Spine J. 2013;22(12):2857-63. doi: 10.1007/s00586-013-2853-y.
- Videbaek TS, Christensen FB, Soegaard R, et al. Circumferential fusion improves outcome in comparison with instrumented posterolateral fusion: long-term results of a randomized clinical trial. Spine (Phila Pa 1976). 2006;31:2875-2880
- Watters. North American Spine Society. (2008). Evidence-based clinical guidelines for multidisciplinary spine care.
Evidence tabellen
Table of quality assessment
Research question: Wat is de beste chirurgische techniek van spondylodese?
Indicatie discogene lage rugpijn, lage rugpijn met aspecifieke degeneratieve kenmerken
Risk of bias table for intervention studies (randomized controlled trials)
|
Study reference
(first author, publication year) |
Bias due to method of randomisation (Describe method) 1
(unlikely/likely/unclear) |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Rodriguez-Vela (2013) |
Likely |
Likely |
Likely |
Likely |
Likely |
Unclear |
Unlikely |
Unlikely |
|
Robinson 2013 |
No RCT |
|
|
|
|
|
|
|
|
Madan 2003 |
No RCT |
|
|
|
|
|
|
|
|
Christensen 2002, Videbaek 2006, 2010, 2011, Soegaard 2007 |
Unlikely |
Unlikely |
likely |
likely |
likely |
unlikely |
unlikely |
unlikely |
|
Hoy 2013, Christensen 2014 |
Unlikely |
Unlikely |
likely |
likely |
likely |
unlikely |
unlikely |
unlikely |
|
Fritzell 2002, 2003 |
Unlikely |
Unlikely |
likely |
likely |
likely |
unlikely |
unlikely |
likely |
Evidence tables
Research question: Wat is de beste chirurgische techniek van spondylodese?
Indicatie discogene lage rugpijn, lage rugpijn met aspecifieke degeneratieve kenmerken
Intervention studies (randomized controlled trials and non-randomized observational studies [cohort studies, case-control studies, case series])1
|
Study reference Ref |
Study characteristics Type of study: Setting: Country: Source of funding: |
Patient characteristics 2 Inclusion criteria: Exclusion criteria: N total at baseline: Important prognostic factors2:
|
Intervention (I) Describe intervention (treatment/procedure/test):
|
Comparison / control (C) 3 Describe control (treatment/procedure/test):
|
Follow-up Length of follow-up: Loss-to-follow-up: Incomplete outcome data:
|
Outcome measures and effect size 4 Outcome measures and effect size (include 95%CI and p-value if available): Disability (Oswestry index, mean change, mixed model): Pain (VAS): Functional (SF-36) Functional EQ-5D Quality of life Psychosocial functioning |
Comments |
|
Rodriguez-Vela (2013) |
qRCT single center Spain No funding obtained |
degenerative disc disease. 6 months of failed nonoperative treatment or neurologic deficit progression. Exclusion criteria lumbar stenosis or isthmic spondylolisthesis, previous lumbar spine surgery (except single discectomy) or presence of MRI degenerative changes in other lumbar levels. N=50 |
Mini open technique |
Standard technique |
>3 years (36-54 months) |
VAS leg pain (n.s.) VAS low back pain(n.s.) North American Spine Society (NASS) Low Back Pain Outcome instrument(n.s.) ODI(n.s.) SF-36(n.s.) |
|
|
Robinson 2013 |
Spine registry National Sweden Government funded |
operated on for painful DDD using any posterior method for lumbar fusion |
uninstrumented fusion (UIF) . |
instrumented posterolateral fusion (IPF) Instrumented Interbody fusion (IIF) |
2 years |
Back pain (VAS): Interbody fusion better than UIF 33 (28–38), p = 0.02 Leg pain (VAS) (n.s.) ODI: (n.s.) SF-36 (n.s.): EQ-5D (n.s.) |
|
|
Madan 2003 |
Observational Single center UK Funding not reported |
Inclusion criteria: Severe symptoms of low back pain not responding to medication, rehabilitation and conservative treatment Low back pain >2 years Follow-up of >2 years Age 24–67 years Positive provocative discography and MRI scan correlating with patient’s symptoms and signs Exclusion criteria Disc herniation, spinal stenosis, and isthmic spondylolisthesis Previous spinal operations like fusion, decompression or discectomy N=74 |
ALIF with Hartshill horseshoe (anterior instrumentation) |
PLIF with circumferential fusion (ant and post instrumentation) |
>2 years, av 2.4 y and 3.1 y |
Back pain (VAS) (n.s.) Leg pain (VAS) (n.s.) ODI (n.s.) Modified Somatic Perception Questionnaire (MSPQ) Zung Depression Scale (ZDS) |
|
|
Fritzell 2002, 2003 |
RCT Multicenter Sweden Supported by Acromed Corporation, Cleveland, Ohio and Ossano Scandinavica AB, Stockholm, Sweden. |
Severe CLBP assessed by the treating surgeon L4 to L5, L5–S1, or both unaccompanied by dominant leg pain Pain duration >2 years no psychiatric illness 1 year sick leave or equivalent pain and disability no response to conservative treatment and life adjustments Degenerative changes (spondylosis) on x-ray, CT, and/or MRI No isthmic spondylolisthesis, spinal stenosis, fractures, infection, inflammatory process, or neoplasm Disc herniation if clinical signs of nerve root compression absent No previous spine surgery except for successful removal of a herniated disc more than 2 years preceding entrance to the study and no persistent nerve root symptoms |
Group 1: posterolateral fusion without internal fixation n = 73 |
Group 2: posterolateral fusion combined with variable screw placement and an internal fixation device; N = 74 Group 3: posterolateral fusion combined with variable screw placement and interbody fusion, a “circumferential” [360°] fusion N = 75 |
2 years + pain and complications at 6 and 12 months |
VAS Back pain VAS Leg pain ODI Million score General function score Zung There were no significant differences among the groups regarding the changes in each group after 2 years, according to the Kruskal-Wallis test. Complications (Fritzell 2003): early complications increased significantly with increasing technicality of the surgical procedure.(p=0.001) |
|
|
Fritzell 2002, 2003 |
See above |
See above |
Group 2: posterolateral fusion combined with variable screw placement and an internal fixation device; N = 74 |
Group 3: posterolateral fusion combined with variable screw placement and interbody fusion, a “circumferential” [360°] fusion N = 75 |
See above |
See above |
|
|
Hoy 2013, Christensen 2014 |
RCT Single center Denmark No conflict of interest declared |
severe CLBP and/or leg pain, static or dynamic localized lumbar or lumbosacral segmental instability, spinal stenosis at levels L2–S1 or isthmic spondylolisthesis (grade 1 and 2). Exclusion Age <25 years Osteoporosis, severe cardiac or vascular disease, brain disorders, kidney problems, former or actual malignancy, use of medicine reducing bone metabolism, dementia or abnormal psychological behaviour, and language problems |
posterolateral fusion with titanium TSRH (Medtronic) pedicle instrumentation (PLF group) |
transforaminal fusion in the form of a tantalum cage (Implex/Zimmer) placed using an approach lateral to the facet joint (TLIF group) (Fig. 2). The anterior interbody fusion device was supported by a posterolateral fusion using pedicle screws (titanium TSRH, Medtronic). |
1 and 2 years |
Dallas Pain Questionnaire (DPQ) (n.s.) the pain index from the low back pain rating Scale (LBPRS) (n.s.) ODI (n.s.) SF-36 (n.s.) Cost effectiveness (Christensen 2014): (n.s.) |
|
|
Christensen 2002, Videbaek 2006, 2010, 2011, Soegaard 2007 |
RCT Single center Denmark Not funded |
severe clbp and leg pain, static or dynamic, from localized lumbar or lumbosacral segmental instability caused by isthmic spl (Gr 1 and 2), primary degeneration (no previous surgery), secondary or accelerated degeneration after decompressive surgery, Exclusion criteria: previous fusion, age <20 or >65 years, metabolic bone disease including osteoporosis, one or more comorbidities, psychosocial instability, and previous retroperitoneal surgery. N=148 |
Posterolateral spinal fusion with titanium Cotrel–Dubousset instrumentation (CDI) (posterolateral group),
|
Circumferential spinal fusion in the form of anterior lumbar interbody fusion with the use of a radiolucent Brantigan cage, using a retroperitoneal approach. |
1 year 2 years (5% Ltfu) 5-9 years (9% ltfu) |
Dallas Pain Questionnaire (DPQ) (n.s.) Low Back Pain Rating Scale (LBPR). circumferential fusion significantly less leg pain at 1 y (P 0.03), not at 2 y. Fusion 2-y: superiority for circumferential approach (P 0.04). Work (n.s.) EQ5D/Cost favours circumferential ($12,943 (21,442 to 5428) p0.012 |
|
Notes:
- Prognostic balance between treatment groups is usually guaranteed in randomized studies, but non-randomized (observational) studies require matching of patients between treatment groups (case-control studies) or multivariate adjustment for prognostic factors (confounders) (cohort studies); the evidence table should contain sufficient details on these procedures
- Provide data per treatment group on the most important prognostic factors [(potential) confounders]
- For case-control studies, provide sufficient detail on the procedure used to match cases and controls
- For cohort studies, provide sufficient detail on the (multivariate) analyses used to adjust for (potential) confounders
Verantwoording
Autorisatiedatum en geldigheid
Laatst beoordeeld : 22-04-2017
Laatst geautoriseerd : 22-04-2017
Geplande herbeoordeling : 01-01-2022
Uiterlijk in 2021 bepaalt het bestuur van de NOV of deze richtlijn nog actueel is. Zo nodig wordt een nieuwe werkgroep geïnstalleerd om de richtlijn te herzien. De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De NOV is als houder van deze richtlijn de eerstverantwoordelijke voor de actualiteit van deze richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijk verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de eerstverantwoordelijke over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel van de richtlijn
Het doel van deze richtlijn is het ontwikkelen van een eenduidige indicatiestelling voor geïnstrumenteerde wervelkolomchirurgie (operaties met gebruik van spinale implantaten) en het beoordelen van de effectiviteit van dergelijke ingrepen bij degeneratieve aandoeningen van de thoracolumbosacrale wervelkolom. Deze ingrepen beogen correctie en/of stabilisatie van de wervelkolom, al dan niet gepaard met neurologische decompressie. In de praktijk betreft het voornamelijk patiënten met degeneratieve scoliose, spondylolysis/spondylolisthesis, of patiënten met chronische lage rug- en/of beenpijn verondersteld te zijn veroorzaakt door discusdegeneratie en/of facetartrose die op beeldvorming werd geconstateerd.
Deze richtlijn beoogt een bijdrage te leveren aan het verhogen van de kwaliteit van zorg met betrekking tot de geïnstrumenteerde operatieve behandeling van degeneratieve wervelkolomaandoeningen. Daarbij is tevens het doel om middels heldere, eenduidige indicatiestelling ongewenste praktijkvariatie terug te dringen.
Afbakening van de richtlijn
De richtlijn richt zich op alle patiënten:
- van 18 jaar en ouder;
- met langer dan drie maanden bestaande rug- en/of beenpijn op basis van degeneratieve aandoeningen van de thoracolumbosacrale wervelkolom;
- bij wie conservatieve behandeling, indien geïndiceerd, met multidisciplinaire gestructureerde oefenprogramma’s inclusief psychologische screening en eventuele pijninterventies, onvoldoende baat heeft gehad;
- die door hun klachten dermate ernstig zijn geïnvalideerd dat ze gemotiveerd zijn om een wervelkomingreep met bijbehorende herstelfase en revalidatie te doorlopen.
Specifiek gaat het in deze richtlijn om de volgende patiëntencategorieën:
- lumbale spondylolysis / laaggradige (graad I of II) spondylolisthesis: patiënten met degeneratieve spondylolisthesis, spondylolysis of spondylolytische spondylolisthesis. Laaggradige lumbale spondylolisthesis kan gepaard gaan met rugpijn en/of radiculaire of niet-radiculaire beenpijn of neurogene claudicatie;
- adulte deformiteiten: het betreft hier patiënten met degeneratieve scoliose op basis van progressie van een reeds bestaande idiopathische scoliose, dan wel patiënten met een nieuw ontstane “De Novo” scoliose van de lumbale wervelkolom; daarnaast patiënten met een alignementsstoornis of deformiteit van de wervelkolom na trauma, tumor, infectie of chirurgie aan de wervelkolom in het verleden;
- chronische lage rug- en/of beenpijn: patiënten met lage rugpijn bij facetarthrosis of discusdegeneratie op röntgenfoto en/of MRI (osteofyten, discusversmalling, black discs, Modic veranderingen, annulus scheuren).
Instrumentatie betekent hier het gebruik van spinale implantaten. Hieronder vallen schroef-/haak- en staafconstructies, intervertebrale cages, discusprotheses en interspinosale spacers.
Deze richtlijn gaat niet over patiënten die geïnstrumenteerde chirurgie van de thoracolumbosacrale wervelkolom ondergaan wegens een tumor, infectie, fractuur of een congenitale afwijking. Zoals reeds vermeld zal voor ongeïnstrumenteerde operatieve behandeling bij HNP en lumbale kanaalstenose een separaat, hieraan gekoppelde richtlijn worden ontwikkeld, welke start in 2015. Ook operatieve behandeling van de cervicale wervelkolom valt buiten de huidige richtlijn.
Beoogde gebruikers van de richtlijn
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen die betrokken zijn bij de zorg voor patiënten met degeneratieve aandoeningen van de wervelkolom, voor patiënten en voor beleidsmedewerkers in de gezondheidszorg: In het bijzonder is de richtlijn opgesteld voor orthopedisch chirurgen en neurochirurgen die zich bezighouden met de operatieve behandeling van degeneratieve aandoeningen van de wervelkolom. Daarnaast biedt de richtlijn houvast voor anesthesiologen en andere (para)medici die betrokken zijn bij de zorg voor patiënten met degeneratieve aandoeningen van de wervelkolom.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2013 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met aspecifieke degeneratieve rugklachten, spondylolisthesis en scoliose te maken hebben (zie hiervoor de samenstelling van de werkgroep).
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep werkte gedurende drie jaar aan de totstandkoming van de richtlijn. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
- Dr. P.C. Willems, orthopedisch chirurg, Maastricht universitair medisch centrum, namens de Nederlandse Orthopaedische Vereniging (NOV), (voorzitter)
- Drs. E.A. Hoebink, othopedisch chirurg, Amphia ziekenhuis Breda, namens de NOV
- Prof. dr. B.J. van Royen, othopedisch chirurg, VUMC Amsterdam, namens de NOV
- Dr. G.J. Bouma, Amsterdam Medisch Centrum UvA, namens de Nederlandse Vereniging voor Neurochirurgie (NVvN)
- Dr. M.P. Arts, MC Haaglanden, namens de NVvN
- Dr. J.M.A. Kuijlen, Universitair Medisch Centrum Groningen, namens de NVvN
- Dhr. L. Voogt, namens de Nederlandse Vereniging voor Rugpatiënten
- Drs. M.A.M.B. Terheggen, Rijnstate ziekenhuis Arnhem, namens de Nederlandse Vereniging voor Anesthesiologie
- Dr. H. van de Meent, Radboud Universitair Medisch Centrum Nijmegen namens de Vereniging van Revalidatieartsen
- Dr. T. Hoogeboom, IQ Healthcare Nijmegen, namens het Koninklijk Nederlands Genootschap voor Fysiotherapie
- Dr. C.G.J. Saris, Radboud Universitair Medisch Centrum Nijmegen, namens de Nederlandse Vereniging voor Neurologie
Met ondersteuning van:
- Dr. M.L. Molag, adviseur, Kennisinstituut van Medisch Specialisten Utrecht
Met dank aan:
- Dr. W.H.G. Jacobs, epidemioloog, Dutch Spine Society
Belangenverklaringen
De werkgroepleden hebben schriftelijk verklaard of ze in de laatste vijf jaar een (financieel ondersteunde) betrekking onderhielden met commerciële bedrijven, organisaties of instellingen die in verband staan met het onderwerp van de richtlijn. Tevens is navraag gedaan naar persoonlijke financiële belangen, belangen door persoonlijke relaties, belangen door middel van reputatiemanagement, belangen vanwege extern gefinancierd onderzoek, en belangen door kennisvalorisatie. Een overzicht van de ingevulde belangenverklaringen vindt u bij de verantwoording.
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door deelname van een vertegenwoordiger van patiëntenvereniging de Wervelkolom aan de werkgroep. Er werd reeds een focusgroep gehouden met rugpatiënten tijdens de ontwikkeling van de richtlijn Wervelkolom gerelateerde pijnklachten, een belangrijk uitgangspunt voor de huidige richtlijn. Afgesproken werd om voor deze richtlijn geen nieuwe focusgroep te houden. De conceptrichtlijn zullen we tijdens de commentaarfase laten lezen door rugpatiënten via de Wervelkolom om op die manier hun input op de aanbevelingen te kunnen gebruiken. De verslagen van de invitational conference en focusgroep zijn besproken in de werkgroep en de belangrijkste knelpunten zijn verwerkt in de richtlijn. Het verslag is te vinden in de bijlage.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen volgens het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwalititeit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II) (www.agreecollaboration.org), dat een internationaal breed geaccepteerd instrument is en op ‘richtlijnen voor richtlijn’ voor de beoordeling van de kwaliteit van richtlijnen.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens zijn er knelpunten aangedragen tijdens een invitational conference met de Vereniging van Scoliosepatiënten, patiëntenvereniging de Wervelkolom, zorgverzekeraars, Inspectie voor de Gezondheidszorg en Zorginstituut Nederland en door een focusgroepbijeenkomst met patiënten. Een verslag hiervan kunt u vinden onder aanverwante items.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang als cruciaal, belangrijk en onbelangrijk.
Als relevante uitkomstmaten waarop studies zullen worden geselecteerd en beoordeeld heeft de werkgroep gekozen:
- pijn middels een Visual Analogue Scale (VAS-beenpijn, VAS-rugpijn);
- functionele beperkingen middels gevalideerde vragenlijsten, zoals Oswestry Disability Index (ODI), Quebec Back Pain Disability Scale (QBPDS) of Roland Morris Disability Questionnaire (RMDQ);
- kwaliteit van Leven middels EuroQoL, EQ5D, SF-36;
- patiënt-tevredenheid.
De werkgroep wil benadrukken dat een deel van de vastgestelde conclusies sterk samenhangt met de door de werkgroep vastgestelde klinisch relevante verschillen tussen groepen patiënten die in studies zijn vergeleken. Klinisch relevante verschillen werden door de werkgroep vastgesteld op basis van een consensus—artikel van Ostelo (Ref Ostelo, Spine 2008). De resultaten kunnen uiteraard anders uitpakken als deze grenzen tussen succes en falen iets hoger of lager worden gelegd.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar bestaande buitenlandse richtlijnen en naar systematische reviews in Medline, Cochrane en Cinahl. Vervolgens werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekactie of gebruikte trefwoorden van de zoekactie en de gehanteerde selectiecriteria zijn te vinden in de module van desbetreffende uitgangsvraag.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld door de adviseur en medisch specialist, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (bias) te kunnen inschatten.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij voldoende overeenkomsten tussen de studies werden de gegevens ook opgenomen in een meta-analyse.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) voor interventievragen:
de kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor Grading Recommendations Assessment, Development and Evaluation (zie http://www.gradeworkinggroup.org/) (Atkins, 2004).
B) voor vragen over waarde diagnostische tests, schade of bijwerkingen, etiologie en prognose:
bij dit type vraagstelling kan GRADE (nog) niet gebruikt worden. De bewijskracht van de conclusie is bepaald volgens de gebruikelijke EBRO-methode (Van Everdingen, 2004).
Formuleren van de conclusies
Voor vragen over waarde diagnostische tests, schade of bijwerkingen, etiologie en prognose is het wetenschappelijke bewijs samengevat in een of meerdere conclusies, waarbij het niveau van het meest relevante bewijs is weergegeven.
Bij interventievragen verwijst de conclusie niet naar één of meer artikelen, maar wordt getrokken op basis van alle studies samen (body of evidence). Hierbij maakten de werkgroepleden de balans op van elke interventie. Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen.
Overwegingen
Voor een aanbeveling zijn naast het wetenschappelijke bewijs ook andere aspecten belangrijk, zoals de expertise van de werkgroepleden, patiëntenvoorkeuren, kosten, beschikbaarheid van voorzieningen of organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven een antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module ‘Organisatie van zorg bij spinaalchirurgie’.
Indicatorontwikkeling
De werkgroep kiest ervoor om aan te sluiten bij de Kwaliteitsindicatoren die door het DICA worden uitgevraagd in het kader van de Dutch Spine Registry.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is, dat is aangegeven waar van toepassing.
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor autorisatie en door hen geautoriseerd.
Literatuur
- Appraisal of Guidelines for Research & Evaluation II, www.agreecollaboration.org.
- Atkins D, Best D, Briss PA, et al. Grading quality of evidence and strength of recommendations. BMJ 2004;328(7454):1490.
- Van Everdingen JJE, Burgers JS, Assendelft WJJ, et al. Evidence-based richtlijnontwikkeling. Bohn Stafleu Van Loghum, 2004.
Zoekverantwoording
Zoekacties zijn opvraagbaar. Neem hiervoor contact op met de Richtlijnendatabase.
