Eiwitbeperking bij chronische nierschade
Uitgangsvraag
Eiwitbeperking van 0,8 g/kg ideaal lichaamsgewicht per dag wordt geadviseerd in geval van eGFR <30 ml/min/1,73m2. Moet een dergelijke dieetinterventie niet al geadviseerd worden in geval van patiënten met chronische nierschade met een eGFR ≥ 30 ml/min/1,73m2, met name indien zij ook verhoogde albuminurie hebben?
Aanbeveling
Eiwitbeperking van 0,8g/kg ideaal lichaamsgewicht per dag wordt niet aanbevolen voor patiënten met chronische nierschade en een eGFR ≥ 30 ml/min/1,73 m2.
Eiwitbeperking van 0,8 g/kg ideaal lichaamsgewicht per dag wordt, conform eerdere richtlijnen, wel aanbevolen voor patiënten met chronische nierschade en eGFR < 30 ml/min/1,73 m2.
Overwegingen
De kwaliteit van het bewijs is matig; voor een deel is dit te wijten aan een wat hogere eiwitintake dan gepland in een interventiegroep. Het is mogelijk dat strikte toepassing van het eiwitbeperkte dieet tot 0,8 g/kg wel tot statistisch significante verschillen zou leiden. Overigens is het dan de vraag of dit statistisch significante verschil ook een klinisch relevant verschil zou betekenen.
Naast mogelijke voordelen van een eiwitbeperkt dieet op de nierfunctie en cardiovasculaire of renale eindpunten, gaat deze interventie ook gepaard met nadelen. Het volgen van een strikt eiwitbeperkt dieet vereist waarschijnlijk aanpassingen in het dagelijks leven van de patiënt, ten aanzien van consumptie. Dit kan invloed hebben op de door de patiënt ervaren kwaliteit van leven. Bovendien bestaat bij het volgen van een eiwitbeperkt dieet het gevaar van een slechtere voedingstoestand door te weinig calorieënintake, met name bij oudere patiënten.
Voor begeleiding bij een eiwitbeperkt dieet en het voorkomen van een slechte voedingstoestand is een dieetbehandeling door een diëtist (nierziekten) aangewezen. Daarnaast is eiwitbeperking niet zinvol bij patiënten met een beperkte levensverwachting.
De werkgroep vindt het verstandig een hoge eiwitinname (> 1,3 g/kg ideaal lichaamsgewicht per dag) te vermijden bij patiënten met CNS.
Onderbouwing
Conclusies
|
matig |
Meta-analyses over het effect op achteruitgang van nierfunctie laten geen statistisch significant en klinisch relevant voordeel zien van het beperken van de eiwitintake van 0,8 g/kg ideaal lichaamsgewicht per dag bij patiënten met chronische nierschade met eGFR ≥ 30 ml/min/1,73m2, ook niet bij patiënten met verhoogde albuminurie. Nezu, 2013; Rughooputh, 2015, Fouque, 2009 |
Samenvatting literatuur
Het artikel van Kopple bleek bij bestudering van de volledige tekst in plaats van het abstract geen origineel onderzoek te beschrijven, maar een editorial te zijn en is daarom alsnog geëxcludeerd [Kopple, 2008]. Het artikel van Kaysen et al. bleek bij bestudering van de volledige tekst in plaats van het abstract een narratieve in plaats van een systematische review te beschrijven en is daarom alsnog geëxcludeerd [Kaysen, 2013].
Rughooputh et al. publiceerden een systematische review van randomised controlled trials (RCT’s), inclusief meta-analyse, over het effect van eiwitbeperking op de nierfunctie (eGFR) bij patiënten met CNS [Rughooputh, 2015]. In deze review werden trials geïncludeerd met een studieduur van 12 maanden (om permanente wijzigingen in de eGFR te kunnen aantonen). Inclusie van trials liep tot september 2014. De literatuursearch voor deze richtlijn leverde geen aanvullende trials op na die publicatiedatum. In de review werden 14 RCT’s geïncludeerd, gepubliceerd tussen 1989 en 2013, met in totaal 1965 patiënten. De systematische review, inclusief meta-analyse, is goed uitgevoerd; in de onderliggende studies is enig risico op bias geconstateerd met name ten aanzien van allocation concealment, maar het overall risico op bias wordt laag geschat.
In de review is een subgroepanalyse gemaakt voor patiënten met een eGFR ≥ 60 ml/min/1,73m2 (gebaseerd op de gemiddelde baseline eGFR van de studie). In deze subgroepanalyse werden de resultaten van 8 studies, met in totaal 618 patiënten, betrokken. De geplande eiwitintake in de interventiegroepen bedroeg hierbij over het algemeen 0,6-0,8 g/kg/dag en in de controlegroepen 1,0-1,2 g/kg/dag. De werkelijke eiwitintake (gemeten met urine-analyse) bedroeg in de interventiegroepen 0,8-1,1 g/kg/dag en in de controlegroepen 1,0-1,1g/kg/dag. Er werd een effect van lage eiwitintake op de eGFR gevonden van -0,35 ml/min/1,73m2 per jaar. Het 95% betrouwbaarheidsinterval was -1,40 tot 0,70; dit effect was niet statistisch significant.
Voor de ontwikkeling van deze richtlijn werd een nieuwe meta-analyse gedaan van de studies met een gemiddelde baseline eGFR tussen 30 en 60 ml/min/1,73m2. Hierin werden 4 studies uit de review van Rughooputh et al. geïncludeerd, met in totaal 789 patiënten. De geplande eiwitintake in de interventiegroepen bedroeg hierbij over het algemeen 0,6-0,8 g/kg/dag en in de controlegroepen 1,0-1,3 g/kg/dag. De werkelijke eiwitintake (gemeten met urine-analyse) bedroeg in de interventiegroepen 0,7-0,9 g/kg/dag en in de controlegroepen 1,1-1,5g/kg/dag. Bij patiënten met een gemiddelde baseline eGFR tussen 30 en 60 ml/min/1,73m2 was de achteruitgang in nierfunctie in de groep met verlaagde eiwitintake 1,43 ml/min/1,73m2 per jaar gunstiger dan in de groep met normale eiwitintake (gedurende follow-up van 12 tot 35 maanden). Het 95% betrouwbaarheidsinterval liep van -3,09 tot 0,23; het verschil was niet statistisch significant (zie figuur 1). In de in de meta-analyse geïncludeerde studies van Zeller et al. en de beide studies van Meloni et al. hadden de patiënten naast een verlaagde nierfunctie ook ernstig verhoogde albumine excretie (gemiddeld respectievelijk 3625, 2500 en 1999 mg/24 uur). In de studie van Klahr et al. staat dit niet vermeld. Exclusie van de studie van Klahr uit de meta-analyse levert een gemiddeld verschil op tussen verlaagde eiwitintake en normale eiwitintake van 1,93 ml/min/1,73 m2 (95% BI: -4,09 tot 0,22; niet significant).

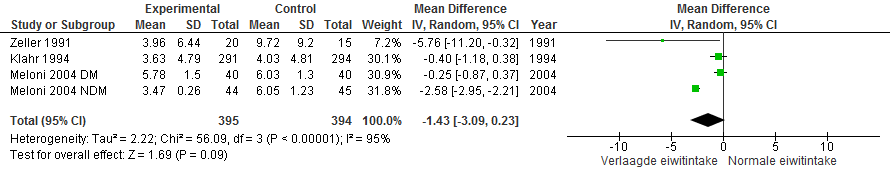
Figuur 1. Meta-analyse verlaagde versus normale eiwitintake bij patiënten met gemiddelde eGFR 30-60 ml/min/1,73m2
Ook werd een nieuwe meta-analyse uitgevoerd, waarbij beide bovenstaande groepen zijn gecombineerd. Bij patiënten met een gemiddelde baseline eGFR ≥ 30 ml/min/1,73m2 was de achteruitgang in nierfunctie in de groep met verlaagde eiwitintake 0,95 ml/min/1,73m2 per jaar gunstiger dan in de groep met normale eiwitintake (gedurende follow-up van 12 tot 60 maanden). Het 95% betrouwbaarheidsinterval liep van -2,12 tot 0,22; het verschil was niet statistisch significant (zie figuur 2).

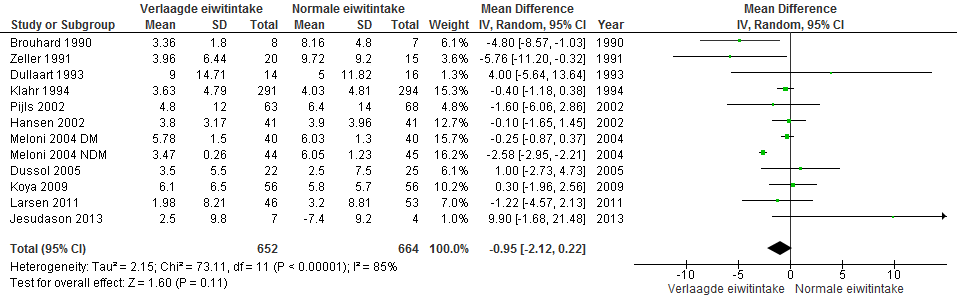
Figuur 2. Meta-analyse verlaagde versus normale eiwitintake bij patiënten met gemiddelde eGFR ≥30 ml/min/1,73m2
Nezu et al. voerden eveneens een systematische review, met meta-analyse, uit omtrent het effect van een dieet met weinig eiwit op de nierfunctie, bij patiënten met diabetische nefropathie [Nezu, 2013]. De in deze studie geïncludeerde RCT’s vertonen grote overeenkomsten met die van Rughooputh et al., waarbij studies onder patiënten zonder diabetische nefropathie uiteraard niet zijn geïncludeerd, en een 4-tal studies met een looptijd van 3-6 maanden wel. De auteurs van deze studie vonden een statistisch significant resultaat van een eiwitbeperkt dieet op de eGFR (gemiddeld verschil 5,82 (95% BI: 2,30-9,33)). Het verschil met de studie van Rughooputh is geheel te verklaren door de inclusie van de studies met een looptijd korter dan 1 jaar. Vanwege het gegeven dat het effect van eiwitbeperking pas consequenties heeft na langdurige toepassing, is besloten de resultaten van het onderzoek van Nezu et al. niet separaat mee te nemen. De Cochrane systematische review van Robertson et al. over eiwitrestrictie bij patiënten met diabetes mellitus en nierschade bevatte geen andere RCT’s dan die van Nezu et al. en Rughooputh et al. en richtte zich ook niet op andere uitkomstmaten [Robertson, 2007]. Deze review is daarom ook niet verder geanalyseerd.
Met de studies in de review van Nezu et al. is een meta-analyse gedaan voor de subpopulatie van patiënten met eGFR 30-60 ml/min/1,73 m2 en verhoogde albuminurie. Hierin werden drie studies geïncludeerd met in totaal 90 patiënten. De studieduur varieerde van 4 tot 24 maanden. Als uitkomstmaat werd gekeken naar het effect op ernstig verhoogde albuminurie. Het gestandaardiseerd gemiddeld verschil bedroeg -0,28 (95% BI -0,71 tot 0,16; niet significant), zie figuur 3.

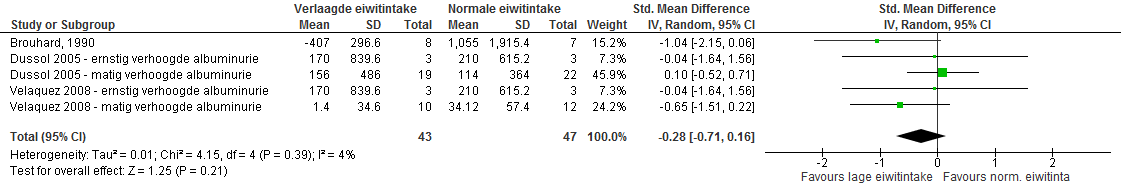
Figuur 3. Meta-analyse verlaagde versus normale eiwitintake bij patiënten met gemiddelde eGFR 30-60 ml/min/1,73m2 en verhoogde albuminurie; uitkomst: effect op ernstig verhoogde albuminurie
Fouque et al. schreven een Cochrane systematische review waarin zij het effect van een eiwitbeperkt dieet op het vertragen van de tijd tot nierfunctievervangende therapie onderzochten [Fouque, 2009]. In deze review includeerden zij 10 studies met in totaal 2000 patiënten, van wie er 1002 een eiwitbeperkt dieet volgden. Patiënten hadden matige tot ernstige nierschade en werden ten minste één jaar gevolgd, waarbij werd gekeken naar eindstadium nierfalen (gedefinieerd als noodzaak tot starten van dialyse, niertransplantatie of mortaliteit). Het relatieve risico op nierfalen was 0,68 (95% BI: 0,55-0,84) bij het volgen van een eiwitbeperkt dieet. De NNT om bij één patiënt nierfalen te voorkomen was 2-56 bij het gedurende een jaar volgen van een eiwitbeperkt dieet. Op basis van de beschikbare data uit de geïncludeerde studies kon hierbij geen onderscheid gemaakt worden in stadia van CNS, of aanwezigheid van verhoogde albuminurie.
De kwaliteit van het gevonden bewijs is matig, vanwege enige beperkingen in de opzet van de onderliggende onderzoeken (allocation concealment) en omdat de gemiddelde eiwitintake in de interventiegroep van een enkele geïncludeerde studie hoger was dan 0,8 g/kg (zie de GRADE profile onder aanverwante producten).
Zoeken en selecteren
Voor een antwoord op deze uitgangsvraag is op 12 februari 2016 naar literatuur gezocht in Medline (zie de zoekverantwoording). Dit leverde (ontdubbeld) 133 abstracts op. Deze abstracts zijn op onderwerp (sluit het artikel aan bij de uitgangsvraag?) en research design (systematische reviews) geselecteerd, wat resulteerde in 5 artikelen, die fulltekst zijn beoordeeld. Na beoordeling door experts in de werkgroep werd een extra systematische review toegevoegd. Deze review was niet eerder geselecteerd, vanwege de beschikbaarheid van recentere reviews, maar bleek toch belangrijke informatie over patiëntrelevante uitkomsten te bevatten.
Referenties
- Fouque D, Laville M. Low protein diets for chronic kidney disease in non diabetic adults. Cochrane Database of Systematic Reviews 2009, Issue 3. Art. No.: CD001892. DOI: 10.1002/14651858.CD001892.pub3
- Kaysen GA, Odabaei G. Dietary protein restriction and preservation of kidney function in chronic kidney disease. Blood Purif 2013; 35: 22-5.
- Kopple JD. Do low-protein diets retard the loss of kidney function in patients with diabetic nephropathy? Am J Clin Nutr 2008; 88: 593-4.
- Nezu U, Kaminaya H, Kondo Y, Sakuma M, Morimoto T, Ueda S. Effect of low-protein diet on kidney function in diabetic nephropathy: meta-analysis of randomised controlled trials. BMJ Open 2013; 3: e002934.
- Robertson LM, Waugh N, Robertson A. Protein restriction for diabetic renal disease. Cochrane database of systematic reviews 2007, issue 4. Art. No.: CD002181. DOI: 10.1002/14651858.CD002181.pub2.
- Rughooputh MS, Zeng R, Yao Y. Protein diet restriction slows chronic kidney disease progression in non-diabetic and in type 1 diabet-ic patients, but not in type 2 diabetic patients: a meta-analysis of randomized controlled trials using glomerular filtration rate as a surrogate. PLOS One 2015; 10: e0145505.
Verantwoording
Autorisatiedatum en geldigheid
Laatst beoordeeld : 18-01-2018
Laatst geautoriseerd : 18-01-2018
Geplande herbeoordeling :
Jaarlijks wordt door de initiatiefnemers van de ontwikkeling van deze richtlijn bepaald of actualisatie van de richtlijn nodig is. Indien actualisatie gewenst is, spannen de initiatiefnemers zich in om de hiervoor noodzakelijke voorwaarden (bijvoorbeeld financiering, samenstelling werkgroep) te realiseren. Nieuwe of nog niet behandelde knelpunten kunnen aanleiding zijn tot actualisatie van de richtlijn.
Algemene gegevens
Deze richtlijn is ontwikkeld in samenwerking met:
- Koninklijke Nederlandse Maatschappij ter Bevordering der Pharmacie
- Nederlandse Federatie voor Nefrologie
- Nederlandse Vereniging van Diëtisten / Diëtisten Nierziekten Nederland
- Nederlandse Vereniging van Ziekenhuisapothekers
- Nederlandse Vereniging voor Klinische Chemie en Laboratoriumgeneeskunde
- Nierpatiënten Vereniging Nederland
Met ondersteuning van:
- Nederlands Huisartsen Genootschap
- Nederlandse Internisten Vereniging
- PROVA
De ontwikkeling van deze richtlijn is gefinancierd vanuit een projectbudget door de Stichting Kwaliteitsgelden Medisch Specialisten en het Nederlands Huisartsen Genootschap.
Doel en doelgroep
Doel
Het doel van deze richtlijn is de kwaliteit van zorg en patiëntveiligheid van patiënten met CNS te waarborgen en waar mogelijk te verbeteren. In deze richtlijn zijn aanbevelingen geformuleerd die professionals in de zorg hiertoe handvaten geven. Daarbij is het doel bovendien de zorg in de eerste en tweede lijn zoveel mogelijk op elkaar af te stemmen en daarbij uitdrukkelijk het patiëntenperspectief een plaats te geven.
Doelgroep
De doelgroep van deze richtlijn zijn professionals die zich bezig houden met de zorg voor patiënten met CNS. Hieronder worden in ieder geval verstaan: huisartsen, internisten, internist-nefrologen, apothekers, laboratoriumspecialisten klinische chemie en diëtisten. Ook andere professionals, zoals andere medisch specialisten, verpleegkundigen en maatschappelijk werkenden, kunnen hun voordeel doen met deze richtlijn.
Samenstelling werkgroep
Voor de ontwikkeling van deze richtlijn is een multidisciplinaire werkgroep ingesteld, onder voorzitterschap van dhr. dr. Marc Hemmelder, internist-nefroloog, en mw. drs. Jacintha van Balen, huisarts. In de werkgroep hebben gemandateerde vertegenwoordigers van de volgende beroepsverenigingen zitting:
- Koninklijke Nederlandse Maatschappij ter Bevordering der Pharmacie
- Nederlands Huisartsen Genootschap
- Nederlandse Internisten Vereniging / Nederlandse Federatie voor Nefrologie
- Nederlandse Vereniging van Diëtisten / Diëtisten Nierziekten Nederland
- Nederlandse Vereniging van Ziekenhuisapothekers
- Nederlandse Vereniging voor Klinische Chemie en Laboratoriumgeneeskunde
Om het patiëntenperspectief in de werkgroep te waarborgen, hadden twee vertegenwoordigers van de Nierpatiënten Vereniging Nederland zitting in de werkgroep. De werkgroep werd procedureel en methodologisch ondersteund door PROVA. Logistieke ondersteuning is gegeven door de Nederlandse Internisten Vereniging en het Nederlands Huisartsen Genootschap. Het secretariaat is gevoerd door het Nederlands Huisartsen Genootschap.
Synchroon aan de ontwikkeling van deze multidisciplinaire richtlijn zijn de NHG-Standaard Chronische Nierschade en aanvullende NIV-modules Chronische Nierschade ontwikkeld. De werkgroepleden van de Standaardwerkgroep en van de NIV-werkgroep maakten deel uit van de werkgroep van de multidisciplinaire richtlijn, om zo alle trajecten zo veel mogelijk op elkaar af te stemmen.
- Mw. drs. Jacintha van Balen, huisarts, Nederlands Huisartsen Genootschap, Utrecht, namens het Nederlands Huisartsen Genootschap – voorzitter
- Dhr. dr. Marc Hemmelder, internist-nefroloog, Nefrovisie, Utrecht, namens de Nederlandse Internisten Vereniging en de Nederlandse Federatie voor Nefrologie – voorzitter
- Mw. drs. Mariska Tuut, epidemioloog, PROVA, Varsseveld – secretaris
- Dhr. Peter van Cuijk, Apeldoorn, ervaringsdeskundige, namens de Nierpatiënten Vereniging Nederland
- Dhr. prof. dr. Ron Gansevoort, internist-nefroloog, UMC Groningen, namens de Nederlandse Internisten Vereniging en de Nederlandse Federatie voor Nefrologie
- Dhr. dr. Wim de Grauw, huisarts te Berghem, Radboudumc, Nijmegen, namens het Nederlands Huisartsen Genootschap
- Mw. Inez Jans, diëtist, Ziekenhuis Gelderse Vallei, Ede, namens Nederlandse Vereniging van Diëtisten en Diëtisten Nierziekten Nederland
- Mw. dr. Birgit Koch, ziekenhuisapotheker-klinisch farmacoloog, Erasmus MC, Rotterdam, namens de Nederlandse Vereniging van Ziekenhuisapothekers
- Mw. drs. Karen de Leest, apotheker, Apotheek de Roerdomp, Nieuwegein, namens de Koninklijke Nederlandse Maatschappij ter Bevordering der Pharmacie
- Mw. drs. Karen Prantl, Bussum, coördinator kwaliteit & onderzoek, Nierpatiënten Vereniging Nederland, namens de Nierpatiënten Vereniging Nederland
- Dhr. dr. Paul Schenk, laboratoriumspecialist klinische chemie / klinisch chemicus, LUMC, Leiden, namens de Nederlandse Vereniging voor Klinische Chemie en Laboratoriumgeneeskunde
- Mw. dr. Nynke Scherpbier, huisarts, Radboudumc, Nijmegen, namens het Nederlands Huisartsen Genootschap
- Mw. drs. Judith Tjin-A-Ton, huisarts, Amstelveen, namens het Nederlands Huisartsen Genootschap
- Mw. dr. Neelke van der Weerd, internist-nefroloog, AMC, Amsterdam, namens de Nederlandse Internisten Vereniging en de Nederlandse Federatie voor Nefrologie
Belangenverklaringen
|
Naam |
Namens |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Reputatie-management |
Extern gefinancierd onderzoek |
Kennis-valorisatie |
Overige belangen |
|
Jacintha van Balen |
NHG |
Huisarts 0,6 FTE; Teamleider afdeling Richtlijnen en Wetenschap |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
|
Marc Hemmelder |
NIV / NFN |
Internist-nefroloog Medisch Centrum Leeuwarden (0,6 FTE) Uitvoerend bestuurder Nefrovisie (0,4 FTE) |
Geen |
Geen |
Geen |
Geen |
Dolomites studie van Astellas |
Renine, registratie van patiënten met nierfunctievervaning in Nederland. Onderdeel van Nefrovisie |
Geen |
|
Mariska Tuut |
onafhankelijk |
Eigenaar PROVA, adviesbureau voor procesmatige en methodologische ondersteuning bij de ontwikkeling van evidence-based richtlijnen en andere kwaliteitsinstrumenten |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
|
Peter van Cuijk |
NVN |
Ruim 35 jaar gewerkt in de Jeugdhulpverlening als orthopedagoog en manager. Ervaring in diverse settingen en diverse functie's, zowel inhoudelijk, uitvoerend en in de aansturing/management. |
bestuursfunctie (penningmeester) amateur-theatervereniging De Apeldoornse Komedie |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
|
Ron Gansevoort |
NIV / NFN |
Internist-nefroloog, UMCG |
Lid bestuur Nederlandse Federatie voor Nefrologie (sectie Wetenschap); Lid Wetenschappelijke Adviesraad Nierstichting; Lid redactie wetenschappelijke tijdschriften: American Journal of Kidney Diseases, Clinical Journal of the American Society of Neprology, European Medical Journal Nephrology, Journal of Nephrology, Nephrology Dialysis and Transplantation, Nephron Clinical Practice (alle functies onbetaald) |
Geen |
Geen |
Lid wetenschappelijke adviesraad Nierstichting |
Geen |
Geen |
Geen |
|
Wim de Grauw |
NHG |
Huisarts te Berghem (0,7 fte); Senior staflid huisarts-onderzoeker afdeling Eerstelijns Geneeskunde Radboudumc Nijmegen (0,3 fte) |
Herder bij diverse professionele begrazingsbedrijven |
Geen |
Geen |
Onderzoek op het gebied van Chronische Nierschade is een belangrijk onderdeel van de onderzoekslijn vaatschade van de afdeling Eerstelijnsgeneeskunde Radboudumc in samenwerking met de afdeling Nefrologie Radboudumc |
De afdeling Eerstelijns Geneeskunde ontvangt subsidie van de Nierstichting Nederland voor onderzoek op het gebied van Chronische Nierschade |
Afdeling Eerstelijnsgeneeskunde Radboudumc heeft samen met de afdeling Nefrologie Radboudumc en Zorgdomein Telenefrologie ontwikkeld, een e-health applicatie voor consultatie tussen huisarts en nefroloog |
Geen |
|
Inez Jans |
NVD / DNN |
Diëtist, aandachtsgebied nierziekten en voedingsteam, Ziekenhuis Gelderse Vallei (fulltime dienstverband) |
Extern assessor Hogeschool van Arnhem en Nijmegen, opleiding Voeding en Diëtetiek (flex contract); Actief lid Diëtisten Nierziekten Nederland (voorzitter DNN werkgroep kwaliteit; lid DNN werkgroep richtlijnen); vanuit die rol lid van de werkgroep multidisciplinaire richtlijn chronisch nierfalen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
|
Birgit Koch |
NVZA |
Ziekenhuisapotheker-klinisch farmacoloog 0,85 FTE |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
ZonMw: PK/PD antipsychotica; Stichting Coolsingel: middelenmisbruik zwangerschap |
n.v.t. |
n.v.t. |
|
Karen de Leest |
KNMP |
Apotheker, Apotheek de Roerdomp, Nieuwegein, 24 uur/week |
Wetenschappelijk medewerker KNMP, 10 uur/week |
Geen |
Geen |
Redactielid Vascuzine, tijdschrift v.d. Vasculitis patiënten vereniging, vrijwilligerswerk, geen boegbeeldfunctie |
Geen |
Geen |
Nee |
|
Karen Prantl |
NVN |
Beleidsmedewerker kwaliteit |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
|
Paul Schenk |
NVKC |
Klinisch chemicus/ laboratoriumspecialist Klinische chemie, LUMC Leiden (voltijds, loondienst) |
Geen nevenwerkzaamheden buiten LUMC |
Geen persoonlijke financiële belangen |
Geen relevante persoonlijke relaties als hier bedoeld |
Geen relevante posities als hier bedoeld |
Geen relevant extern gefinancierd onderzoek |
Geen relevante valorisatie |
Nee, geen relevante overige belangen |
|
Nynke Scherpbier |
NHG |
Opleidingsdirecteur extramurale vervolgopleidingen RadboudUMC 0,8 FTE; huisarts 0,2 FTE |
Council member EURACT, Europese organisatie voor opleiden in de huisartsgeneeskunde (onbetaald) |
Geen |
Geen |
Geen |
Ik ben co-promotor van een promotietraject dat wordt gefinancierd door de Nierstichting met als doel te onderzoeken: 1. wat belemmerende en bevorderende factoren zijn in het naleven van de LTA; 2. hoe patiënten de voorlichting over CNS ervaren; 3. of het mogelijk is om veilige wijze bepaalde patiënten terug te verwijzen vanuit de tweede naar de eerste lijn |
Afdeling Eerstelijnsge-neeskunde Radbou-dumc heeft samen met de afdeling Nefro-logie Radboudumc en Zorgdomein Telenefrologie ontwikkeld, een e-health applicatie voor consultatie tus-sen huisarts en nefroloog |
Geen |
|
Judith Tjin-A-Ton |
NHG |
Huisarts |
Kaderhuisarts hart- en vaatziekten: kwaliteitscommissie en werkgroep HVZ bij Amstellandzorg BV (betaald) |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
|
Neelke van der Weerd |
NIV / NFN |
Internist-nefroloog AMC Amsterdam |
- |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
Methode ontwikkeling
Evidence based
Implementatie
Gedurende het hele proces van richtlijnontwikkeling is rekening gehouden met implementatie van de richtlijn in de praktijk, bijvoorbeeld bij de samenstelling van de werkgroep, de brede knelpunteninventarisatie en de uitgebreide commentaarronde. De werkgroep heeft adviezen voor implementatie (implementatieplan) en indicatoren geformuleerd. Deze zijn opgenomen onder de aanverwante producten.
Na autorisatie van de richtlijn wordt deze ten minste op de website van de Nederlandse Internisten Vereniging en het Nederlands Huisartsen Genootschap gepubliceerd. Ook andere deelnemende partijen zijn vrij de richtlijn op hun website te publiceren. De richtlijn wordt ter publicatie aangeboden aan www.richtlijnendatabase.nl. Daarnaast wordt getracht samenvattingen van de richtlijn in Nederlandse tijdschriften te publiceren, aandacht aan de richtlijn te besteden op congressen, en nascholingsmateriaal en voorlichtingsmateriaal te ontwikkelen, om zo de implementatie van de richtlijn te bevorderen.
Een voor patiënten begrijpelijke samenvatting van de aanbevelingen uit deze richtlijn komt beschikbaar via www.thuisarts.nl. Een verdieping daarvan komt beschikbaar via de website van de Nierstichting/Nederlandse Vereniging van Nierpatiënten.
Werkwijze
Knelpunteninventarisatie
De richtlijnwerkgroep heeft in de eerste werkgroepvergadering knelpunten benoemd in de zorg voor patiënten met CNS. Deze knelpunten zijn in een invitational conference voorgelegd aan belanghebbenden, waarbij ook is gediscussieerd over aanvullende knelpunten. Voor deze invitational conference zijn, naast vertegenwoordigers van verenigingen die in de werkgroep afgevaardigd zijn, de volgende partijen uitgenodigd:
- Federatie Medisch Coördinerende Centra
- Inspectie voor de Gezondheidszorg
- Nederlandse Federatie van Universitair Medische Centra
- Nederlandse Vereniging van Ziekenhuizen
- Nederlandse Zorgautoriteit
- Nierstichting Nederland
- Patiëntenfederatie Nederland
- Vereniging Innovatieve Geneesmiddelen
- Vereniging Maatschappelijk Werk Nefrologie
- Verpleegkundigen & Verzorgenden Nederland
- ZorgInstituut Nederland
- Zorgverzekeraars Nederland
De richtlijnwerkgroep heeft de input vanuit de knelpunteninventarisatie geanalyseerd en in de tweede werkgroepvergadering de knelpunten en uitgangsvragen vastgesteld.
Uitwerking knelpunten en uitgangsvragen in conceptrichtlijn
Per knelpunt werd door de werkgroep vooraf bepaald op welke wijze dit knelpunt zou worden behandeld: met behulp van systematisch literatuuronderzoek (evidence-based) of meer op basis van bestaande richtlijnen en professionele expertise in de werkgroep. Er was financiering voor de uitwerking van een beperkt aantal vragen met behulp van systematisch literatuuronderzoek. Om toch ook de andere belangrijke knelpunten een plaats te geven in deze richtlijn, is voor uitwerking van de resterende knelpunten voor een minder arbeidsintensieve wijze gekozen. De wijze van uitwerking van de knelpunten/uitgangsvragen staat per uitgangsvraag vermeld in de verschillende modules van deze richtlijn. De keuze van de knelpunten die met systematisch literatuuronderzoek zijn beantwoord is gemaakt door de gezamenlijke werkgroep, op basis van verwachting dat het literatuuronderzoek mogelijk tot nieuwe inzichten zou leiden en de afwezigheid van recente internationale richtlijnen over de specifieke uitgangsvraag.
De uitwerking van de knelpunten in conceptteksten werd voorbereid door de epidemioloog die bij de ontwikkeling van de richtlijn betrokken was. Per knelpunt werd deze inhoudelijk bijgestaan door een aantal werkgroepleden, afhankelijk van het onderwerp. De conceptteksten werden plenair tijdens de werkgroepvergaderingen besproken, en na discussie bijgesteld. De richtlijnwerkgroep is 9 maal bijeen geweest, alvorens de conceptrichtlijn is vastgesteld.
Bij veel uitgangsvragen is voor de onderbouwing gebruik gemaakt van internationale richtlijnen op het gebied van CNS. De KDIGO richtlijn en de NICE richtlijn over chronische nierschade zijn op kwaliteit beoordeeld bij aanvang van de ontwikkeling van deze multidisciplinaire richtlijn. De wijze van onderbouwing van deze internationale richtlijnen werd door de richtlijnwerkgroep als adequaat beoordeeld. Beide richtlijnen maakten gebruik van de GRADE methodiek.
Voor de uitgangsvragen die met behulp van systematisch literatuuronderzoek zijn uitgewerkt, is gebruik gemaakt van de principes van de GRADE Working Group. Voor achtergrondinformatie over deze methodiek wordt verwezen naar het Dutch GRADE Network (www.dutchgradenetwork.org). Vanwege de verschillende totstandkoming van de diverse aanbevelingen heeft de werkgroep ervoor gekozen om het graderen van aanbevelingen, zoals dit wordt gepropageerd in de GRADE-methodiek, niet door te voeren in deze richtlijn. Hiermee is eenheid in de formulering van aanbevelingen gecreëerd.
De module ‘Samenwerking bij CNS’ bevat samenwerkingsafspraken: aanbevelingen voor consultatie en verwijzing tussen eerste en tweede lijn, en aanbevelingen voor samenwerking met laboratoriumspecialisten klinische chemie, diëtisten en apothekers. Hierbij zijn geen specifieke uitgangsvragen genoemd, maar is uitgegaan van eerdere samenwerkingsafspraken en uitgangspunten en aanbevelingen uit de modules ‘Diagnostiek en stadiëring bij CNS’ en ‘Beleid en behandeling bij CNS’.
Daar waar in deze richtlijn ‘hij’ genoemd staat, kan ook ‘zij’ gelezen worden.
Commentaar en autorisatie
De conceptrichtlijn is ter commentaar aangeboden aan alle partijen die bij de knelpunteninventarisatie om input gevraagd zijn. Het binnengekomen commentaar is door de werkgroep beoordeeld en verwerkt in de richtlijn. Daarbij is beargumenteerd welke commentaren wel en welke niet zijn overgenomen.
Daarna is de richtlijn ter autorisatie voorgelegd aan de partijen die in de werkgroep vertegenwoordigd zijn. De richtlijn is geautoriseerd door de Nederlandse Internisten Vereniging, het Nederlands Huisartsen Genootschap, de Nederlandse Vereniging voor Diëtisten, de Nederlandse Vereniging voor Ziekenhuisapothekers en de Nederlandse Vereniging voor Klinische Chemie en Laboratoriumgeneeskunde. Ook is de richtlijn goedgekeurd door de Nierpatiënten Vereniging Nederland.
Juridische betekenis van richtlijnen
Richtlijnen zijn geen wettelijke voorschriften, maar op ‘evidence' gebaseerde inzichten en aanbevelingen waaraan zorgverleners moeten voldoen om kwalitatief goede zorg te verlenen. Na autorisatie van de richtlijn door een beroepsvereniging, wordt de richtlijn gezien als deel van de ‘professionele standaard'. Aangezien de aanbevelingen hoofdzakelijk gebaseerd zijn op de ‘gemiddelde patiënt', kunnen zorgverleners op basis van hun professionele autonomie waar nodig afwijken van de richtlijn. Afwijken van richtlijnen kan in bepaalde situaties zelfs noodzakelijk zijn. Wanneer van de richtlijn wordt afgeweken, dient dit beargumenteerd en gedocumenteerd te worden.
Zoekverantwoording
Zoekacties zijn opvraagbaar. Neem hiervoor contact op met de Richtlijnendatabase.
