Samenvatting stollingssysteem
Het stollingssysteem is een belangrijk verdedigingsmechanisme van het lichaam om bloedverlies te voorkomen of te beperken. Hiervoor zijn voldoende functionele trombocyten, stollingseiwitten (activerende en remmende) en voor de stolselafbraak (fibrinolyse) eiwitten (activerende en remmende) nodig. Om trombose te voorkomen is het belangrijk dat dit mechanisme onder controle wordt gehouden, zo nodig medicamenteus. Het stollingssysteem kan worden onderverdeeld in drie onderling samenhangende processen.
Bij een beschadiging van de vaatwand wordt als eerste maatregel een prop bestaande uit bloedplaatjes en fibrinogeen gevormd (primaire hemostase). Deze is instabiel, houdt maar enkele uren stand en moet verstevigd worden door een netwerk van fibrinedraden. Dit netwerk wordt gevormd tijdens de secundaire hemostase waarin de stollingseiwitten de hoofdrol spelen. Voor het opruimen van het fibrinestolsel en de wondgenezing zorgt het fibrinolytische systeem.
Primaire hemostase
Bij het verloren gaan van de integriteit van de vaatwand is de primaire hemostase het eerste verdedigingsmechanisme van het lichaam tegen te veel bloedverlies. Trombocyten hechten aan het endotheel door middel van de glycoproteïnereceptor Ib in hun membraan, waarbij de circulerende Von Willebrand-factor als ligans optreedt (adhesie). Bij het geactiveerde bloedplaatje komt dan het membraanglycoproteïnecomplex IIb-IIIa aan de oppervlakte en door binding van fibrinogeen aan deze receptor kunnen trombocyten aggregeren. Bij activering wordt arachidonzuur (uit de bloedplaatjesmembraan) via een reeks enzymatische reacties omgezet in verschillende eicosanoïden, zoals tromboxaan A2 en prostaglandinen, met onder andere vasoconstrictoire activiteit en een agonistisch effect op verdere bloedplaatjesactivering. Acetylsalicylzuur inactiveert dit enzym, waardoor de aggregatie wordt geremd. Het geeft een blijvend effect, daar er geen eiwitsynthese plaatsvindt in de trombocyt. Na enkele dagen gebruik, is de remming van het tromboxaan-A2 maximaal. Na staken van acetylsalicylzuur herstelt de trombocytenaggregatie zich weer door productie van nieuwe trombocyten, ongeveer 10 tot 15% van de circulerende trombocytenpool per dag (George, 2000). Een andere klasse trombocytenaggregatieremmers zoals clopidogrel, prasugrel en ticagrelor grijpen aan op de P2Y12 receptor van de trombocyt. Hierdoor wordt de binding van adenosinedifosfaat (ADP) afhankelijk van het geneesmiddel, reversibel of irreversibel geblokkeerd, hetgeen resulteert in een verminderde aggregatie (figuur 3.1). GPIIb/IIIa-receptorantagonisten binden aan de GPIIb/IIIa-receptor op het oppervlak van de trombocyt en remmen de binding van geactiveerde trombocyten aan onder andere fibrinogeen en de Von Willebrand-factor. Doordat daarmee niet alleen de meest belangrijke stap in de trombocytenaggregatie maar ook de trombinevorming wordt beïnvloed is het bloedingsrisico bij gebruik van deze middelen groter dan dat van de overige trombocytenaggregatieremmers.
Figuur 3.1 Overzicht stollingssysteem
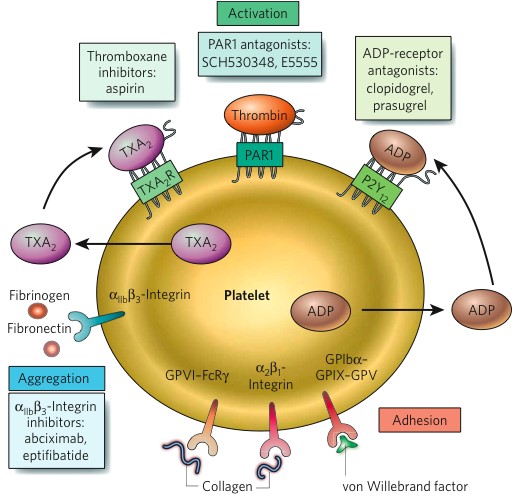
Overgenomen met toestemming van Macmillan Publishers Ltd: Nature (Mackman N. Triggers, targets and treatments for thrombosis. 21, 451 (7181), 914-8. doi: 10.1038/nature06797), copyright (2008).
Secundaire hemostase
Om te zorgen dat de gevormde trombocytenprop niet uiteenvalt, vindt via activatie van stollingsfactoren op fosfolipiden membranen(geactiveerde trombocyten) trombinevorming plaats. Dit proces wordt secundaire hemostase genoemd. De secundaire hemostase start als celgebonden tissue factor (TF), in aanraking komt met het circulerend bloed. TF bindt aan geactiveerd factor VII. Dit complex bindt en activeert vervolgens factor X tot factor Xa. Het TF/factor VIIa complex wordt geremd door TF pathway inhibitor (TFPI), en pas als het TF/factor VIIa complex ook factor IX activeert wordt samen met cofactor Va het protrombine (factor II) omgezet in trombine (factor IIa). Vervolgens versterkt trombine via de intrinsieke route door de activering van factor XI en factor IX samen met factor FVIIIa (tenase complex) de activering van factor FX en vervolgens de eigen vorming via omzetting van protrombine in trombine via het protrombinase complex (factor Xa met behulp van factor Va). Het gevormde trombine zet ten slotte fibrinogeen om in een fibrine. Dit vormt een netwerk dat de trombocytenplug stabiliseert en met behulp van factor XIIIa een stevig fibrine stolsel vormt. In dit proces zijn snelheid en hoeveelheid van de trombinevorming bepalend voorde resistentie van het stolsel tegen lysis. Met als referentie het werk van Bouma en Mosnier postuleren Rosencher et al., dat op deze manier na acht uur een dusdanig stabiel stolsel is gevormd dat afbraak door antistollingsmiddelen niet meer plaatsvindt (Bouma et al., 2006; Rosencher et al., 2007). Naast al deze procoagulante factoren zijn er ook circulerende eiwitten die het stollingssysteem kunnen remmen en verdere stolselaangroei voorkomen. Naast de reeds genoemde TF pathway inhibitor (TFPI), worden de cofactoren Va en VIIIa geremd door geactiveerd proteïne C en S en remt het antitrombine de factoren IIa, Xa, XIIa, XIa, IXa. Heparine, ongefractioneerd heparine (Ongefractioneerd heparine) en laag moleculair heparine (LMWH) binden aan antitrombine en versterken het effect hiervan. Dit heeft als gevolg een effectievere remming van factor Xa en factor IIa (trombine, afhankelijk van concentratie en molecuulgrootte.
Vitamine K antagonisten (acenocoumarol en fenprocoumon) antagoneren de voor stolling noodzakelijke carboxylering van de vitamine K-afhankelijke stollingsfactoren II, VII, IX en X waardoor deze niet op fosfolipiden membranen kunnen binden en remmen zo indirect het stollingsproces. Reeds gevormde (geactiveerde) stollingsfactoren worden niet beïnvloed en derhalve is het volledig antistollend effect afhankelijk van de halfwaardetijd van de stollingsfactoren, het kortst (± zes uur) voor factor VII en het langst (± 60 uur) voor factor II. De nieuwe generatie directe stollingsremmers werken door een direct inhiberend effect op zowel het stolsel gebonden als vrije factor Xa en factor IIa direct en kortdurend door een relatief korte halfwaardetijd. Ten opzichte van de vitamine K antagonisten hebben de (Nieuwe) Directe Orale Anticoagulantia een vaste, nierfunctieafhankelijke, dosering en vereisen in de meeste gevallen, door voorspelbare farmacokinetiek en farmacodynamiek, geen laboratorium monitoring.
Figuur 3.2 Aangrijpingspunt van antistollingsmiddelen
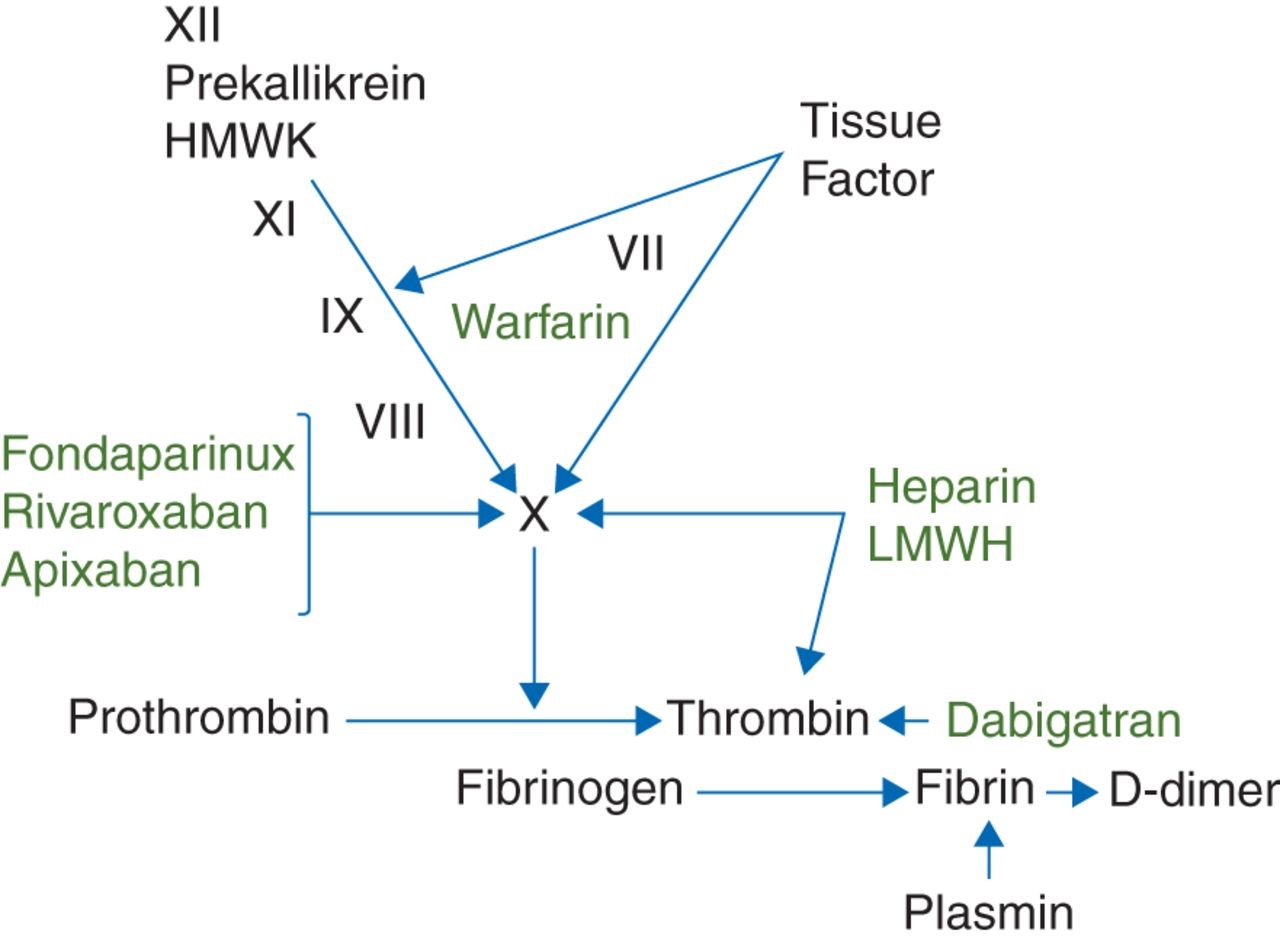
Bron: (Benzon et al., 2013)
Fibrinolyse
Fibrinolyse is het proces waarbij het stolsel weer opgeruimd wordt. Inactief plasminogeen bindt op het fibrine oppervlak en wordt door activerende stoffen uit het endotheel (endogeen-weefsel-plasminogeenactivator t-PA,) omgezet in plasmine. Plasmine breekt fibrine af in oplosbare afbraakproducten. Met synthetische fibrine specifieke en niet-fibrine specifieke plasminogeen activatoren (trombolytica) kan het oplossen van het stolsel door het lichaam sterk worden versneld.
Onderbouwing
Conclusies / Summary of Findings
Referenties
- Benzon, H.T., Avram, M.J., Green, D., & Bonow, R.O. (2013). New oral anticoagulants and regional anaesthesia. Br J Anaesth., Suppl 1, 96-113.
- Bouma, B.N., &Mosnier, L.O. (2006). Thrombin activatable fibrinolysis inhibitor (TAFI)--how does thrombin regulate fibrinolysis? Ann Med., 38(6), 378-88.
- George, J.N. (2000). Platelets. Lancet.,355, 15319.
- Hall, R., &Mazer, C.D. (2011). Antiplatelet drugs: a review of their pharmacology and management in the perioperative period. Anesth Analg., 112(2), 292-318.
- Rosencher, N., Bonnet, P., &Sessler, D.I. (2007). Selected new antithrombotic agents and neuraxiaal anaesthesia for major orthopaedic surgery: management strategies . Anaesthesia., 62, 11541160.
- Mackman, N. (2008). Triggers, targets and treatments for thrombosis. Nature., 451 (7181), 914-8.
- Michelson, A.D. (2010). Antiplatelet therapies for the treatment of cardiovascular disease. Nat Rev Drug Discov., 9(2), 154-169.
Verantwoording
Beoordelingsdatum en geldigheid
Laatst beoordeeld : 16-12-2014
Uiterlijk in 2018 bepaalt het bestuur van de NVA of deze richtlijn nog actueel is. Zo nodig wordt een nieuwe commissie geïnstalleerd om de richtlijn te herzien. De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De NVA is als houder van deze richtlijn de eerstverantwoordelijke voor de actualiteit van deze richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijk verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de eerstverantwoordelijke over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van Medisch Specialisten en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
Deze richtlijn geeft aanbevelingen voor de diagnostiek, het preventieve en postoperatieve beleid en het curatieve beleid in geval van complicaties, bij patiënten die antistolling gebruiken en ingepland zijn voor het ondergaan van een locoregionale zenuw- dan wel neuraxisblokkade, in electieve en acute situaties.
Naar verwachting draagt de richtlijn bij aan een toename van de kennis omtrent het beleid rondom de nieuwe antistollingsmiddelen, met als doel het aantal complicaties laag te houden.
De commissie wil verder een tweetal belangrijke aanbevelingen meegeven:
- een neuraxisblokkade en/of perifere zenuwblokkade dan wel interventionele pijntechnieken dient alleen verricht te worden indien in voorkomende gevallen voldaan is aan de gestelde tijdsintervallen van staken van antistollingsmiddelen;
- raadpleeg bij twijfel de lokaal verantwoordelijk stollingsdeskundige.
Doelgroep
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen die betrokken zijn bij patiënten die een neuraxis- dan wel zenuwblokkade ondergaan.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2012 een multidisciplinaire commissie ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die te maken hebben met een neuraxisblokkade (zie hiervoor de samenstelling van de commissie).
De commissieleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De commissie werkte gedurende twee jaar aan de totstandkoming van de richtlijn. De commissie is verantwoordelijk voor de integrale tekst van deze richtlijn.
- Mevr. dr. A.W.M.M. Koopman-van Gemert, anesthesioloog, Albert Schweitzer ziekenhuis, Dordrecht, voorzitter, namens de NVA
- Mevr. drs. T. Dijkstra, ziekenhuisapotheker, Vlietland ziekenhuis, Schiedam, namens de NVZA
- Dhr. dr. M.M.C. Hovens, internist-vasculair geneeskundige, Rijnstate ziekenhuis, Arnhem, namens de NIV
- Dhr. dr. M. Lancé, anesthesioloog, Maastricht Universitair Medisch Centrum, Maastricht, namens de NVA
- Dhr. dr. L. van den Broek, anesthesioloog, Ziekenhuis groep Twente, Almelo, namens de NVA
- Dhr. dr. S. H. Renes, anesthesioloog, Radboudumc, Nijmegen, namens de NVA
- Dhr. dr. M.F.Termaat, traumachirurg, Leids Universitair Medisch Centrum, Leiden, namens de NVvH
- Mevr. dr. E.C.M. van Pampus, hematoloog-transfusiespecialist, Radboudumc, Nijmegen, namens de NIV
Met ondersteuning van
- Mevr. dr. M.L. Molag, adviseur, Kennisinstituut van Medisch Specialisten
Belangenverklaringen
De commissieleden hebben schriftelijk verklaard of ze in de laatste vijf jaar een (financieel ondersteunde) betrekking onderhielden met commerciële bedrijven, organisaties of instellingen die in verband staan met het onderwerp van de richtlijn. Een overzicht hiervan vindt u hieronder, de volledige belangenverklaringen kunnen worden opgevraagd bij het secretariaat.
Overzicht van ingevulde verklaringen omtrent mogelijk belangenverstrengeling met betrekking tot de richtlijn ‘Neuraxisblokkade’
|
Commissielid |
Belangen afgelopen vijf jaar en/of gedurende looptijd van het project ja /nee |
Zo ja, welke |
|
Mevr. dr. A.W.M.M. Koopman-van Gemert |
Nee |
n.v.t. |
|
Mevr. drs. T. Dijkstra |
Nee |
n.v.t. |
|
Dhr. dr. M.M.C. Hovens |
Nee |
n.v.t. |
|
Dhr. dr. M. Lancé |
Nee |
n.v.t. |
|
Dhr. dr. L. van den Broek |
Nee |
n.v.t. |
|
Dhr. dr. S. H. Renes |
Nee |
n.v.t. |
|
Dhr. dr. M.F. Termaat |
Nee |
n.v.t. |
Inbreng patiëntenperspectief
Patiëntenparticipatie was voor deze richtlijn niet van toepassing. Er werd aandacht besteed aan het patiëntenperspectief door casereports te bestuderen. De belangrijkste knelpunten zijn verwerkt in de richtlijn.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren.
De richtlijn is/wordt digitaal verspreid onder alle relevante beroepsgroepen. Daarnaast is/wordt er een samenvatting van de richtlijn aangeboden aan het tijdschrift Anesthesia. Ook is de richtlijn te downloaden vanaf de website van de Nederlandse Vereniging voor Anesthesiologie (NVA): www.anesthesiologie.nl.
Werkwijze
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de commissie en de adviseur de knelpunten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de commissie besproken waarna de commissie de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de commissie per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De commissie waardeerde deze uitkomstmaten volgens hun relatieve belang als cruciaal, belangrijk en onbelangrijk. Tevens definieerde de commissie, voor zover mogelijk, wat zij voor een bepaalde uitkomstmaat een klinisch relevant verschil vond, dat wil zeggen wanneer de verbetering in uitkomst een verbetering voor de patiënt is.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar bestaande buitenlandse richtlijnen (Medline (OVID) en de database van het Guidelines International Network –GIN-) en naar systematische reviews (Medline-OVID-). Vervolgens werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De commissieleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekactie of gebruikte trefwoorden van de zoekactie en de gehanteerde selectiecriteria zijn te vinden in het hoofdstuk van desbetreffende uitgangsvraag.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de kolom ‘Beoordeling kwaliteit studie’ van een evidencetabel.
Formuleren van de conclusies
Voor vragen over waarde diagnostische tests, schade of bijwerkingen, etiologie en prognose is het wetenschappelijke bewijs samengevat in een of meerdere conclusie, waarbij het niveau van het meest relevante bewijs is weergegeven.
Bij interventievragen verwijst de conclusie niet naar een of meer artikelen, maar wordt getrokken op basis van alle studies samen (body of evidence). Hierbij maakten de commissieleden de balans op van elke interventie. Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen.
Overwegingen
Voor een aanbeveling zijn naast het wetenschappelijke bewijs ook andere aspecten belangrijk, zoals de expertise van de commissieleden, patiëntenvoorkeuren, kosten, beschikbaarheid van voorzieningen of organisatorische zaken.
Formuleren van aanbevelingen
De aanbevelingen geven een antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen.
Indicatorontwikkeling
Gelijktijdig met het ontwikkelen van de conceptrichtlijn werden er interne kwaliteitsindicatoren ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken. Meer informatie over de methode van indicatorontwikkeling is op te vragen bij KiMS.
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor commentaar. De commentaren werden verzameld en besproken met de commissie. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de commissie. De definitieve richtlijn werd aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor autorisatie.
Onderhoud richtlijn Neuraxisblokkade en antistolling
De richtlijn Neuraxisblokkade en antistolling richt zich op de zorg voor patiënten die
antistollingsmiddelen gebruiken en een locoregionale zenuw- of neuraxisblokkade krijgen. Alle soorten antistollingsmiddelen en combinaties van antistollingsmiddelen worden besproken.
De volgende groepen van geneesmiddelen worden in de richtlijn onderscheiden:
A. Trombocytenaggregatieremmers
- Acetylsalicylzuur.
- Clopidogrel.
- Prasugrel.
- Ticagrelor.
- Dipyridamol.
- Non-Steroidal Anti-Inf lammatory Drugs (NSAID’s).
- Metamizol.
- Specifieke Serotonine Heropname Remmers (SSRI’s).
B. GPIIB/IIIa-receptorantagonisten
C. Vitamine-K-antagonisten (cumarinederivaten)
D. Indirecte factor Xa-remmers
- Laagmoleculair heparine.
- Fondaparinux.
- Danaparoid.
E. Ongefractioneerd heparine
F. Trombolytica/fibrinolytica
G. Factor IIa-remmers
- Argatroban.
- Bivalirudine.
- Dabigatran.
H. Directe orale Factor Xa-remmers (rivaroxaban, apixaban)
I. Combinaties van antistollingsmiddelen
De NVA stelt in overleg met andere betrokken wetenschappelijke verenigingen (tenminste NIV, NVZA) een gremium aan om de actualiteit van de richtlijn te bewaken. Deze groep beoordeelt één keer per jaar of er belangrijke wijzigingen zijn die maken dat de richtlijn moet worden aangepast. Afspraken over onder andere mandaat, voorzitterschap en tijdslijnen worden vastgelegd.
Nieuwe ontwikkelingen die invloed kunnen hebben op de inhoud van de richtlijn kunnen betreffen:
- Nieuwe kennis over reeds in de richtlijn opgenomen middel, bijvoorbeeld over dosering, risico’s of antidotum
- Nieuwe combinatie van middelen
- Nieuw middel binnen bepaalde groep
- Nieuwe groep geneesmiddelen
- Nieuwe (binnen- of buitenlandse) richtlijnen
- Andere ontwikkelingen (denk aan implementatieproblemen/organisatieaspecten, financiering, patiëntenvoorkeuren)
Een belangrijke vraag die deze groep zich moet stellen is of de verwachting is dat één of meerdere aanbevelingen veranderen door de wijzigingen. Criteria die hierbij moeten worden meegewogen zijn: mate van verandering aanbeveling, omvang patiëntenpopulatie, patiëntveiligheid, impact op kwaliteit van zorg, behoefte bij beroepsgroep, impact op (macro)kosten.
Daarnaast is het goed om te beseffen dat de literatuur over bloedingen bij neuraxisblokkade vooral bestaat uit patiëntenseries en case reports. Slechts voor een beperkt aantal middelen zijn vergelijkende studies gevonden.
Ad 1. Nieuwe kennis over reeds in de richtlijn opgenomen middel, bijvoorbeeld over dosering, bepaling, risico’s of antidotum
- De werkgroep bepaalt of deze nieuwe kennis aanleiding is om een nieuwe systematische literatuuranalyse te doen.
- Onderbouwing, overwegingen en aanbeveling worden (indien nodig) aangepast.
- De werkgroep adviseert de NVA of er sprake is van een inhoudelijke aanpassing die voor commentaar en autorisatie moet worden voorgelegd.
- Zo ja, commentaarfase en autorisatie zoals gebruikelijk (met eventueel aangepaste termijn).
- Zo nee, wijzigingen worden ter kennisgeving gecommuniceerd naar de betrokken wv-en.
Ad 2. Nieuwe combinatie van middelen
- De werkgroep bepaalt of deze nieuwe combinatie aanleiding is om een nieuwe systematische literatuuranalyse te doen.
- Onderbouwing, overwegingen en aanbeveling worden (indien nodig) aangepast.
- De werkgroep adviseert de NVA of er sprake is van een inhoudelijke aanpassing die voor commentaar en autorisatie moet worden voorgelegd.
- Zo ja, commentaarfase en autorisatie zoals gebruikelijk (met eventueel aangepaste termijn).
- Zo nee, wijzigingen worden ter kennisgeving gecommuniceerd naar de betrokken wv-en.
Ad 3: Nieuw middel binnen bepaalde groep
Wanneer dit leidt tot een nieuwe submodule (bijvoorbeeld nieuwe factor IIa-remmer):
- De werkgroep bepaalt of hiervoor een nieuwe werkgroep wordt ingesteld of dat zij dit zelf ter hand neemt.
- Er wordt een systematische literatuuranalyse uitgevoerd.
- Onderbouwing, overwegingen en aanbevelingen worden opgesteld.
- Commentaarfase en autorisatie zoals gebruikelijk (met eventueel aangepaste termijn).
Wanneer dit leidt tot een aanpassing van een bestaande (sub)module (bijvoorbeeld nieuwe factor Xa-remmer):
- De werkgroep bepaalt of hiervoor een nieuwe werkgroep wordt ingesteld of dat zij dit zelf ter hand neemt.
- Er wordt een systematische literatuursearch uitgevoerd voor het nieuwe middel (of voor hele module?).
- Onderbouwing, overwegingen en aanbeveling worden (indien nodig) aangepast.
- De werkgroep adviseert de NVA of er sprake is van een inhoudelijke aanpassing die voor commentaar en autorisatie moet worden voorgelegd.
- Zo ja, commentaarfase en autorisatie zoals gebruikelijk (met eventueel aangepaste termijn).
- Zo nee, wijzigingen worden ter kennisgeving gecommuniceerd naar de betrokken wv-en.
Ad 4: Nieuwe groep geneesmiddelen
Dit zal altijd leiden tot een uitbreiding van de richtlijn met een tenminste één extra module.
- Het is waarschijnlijk dat hiervoor een nieuwe werkgroep wordt ingesteld dan wel de bestaande werkgroep zo nodig wordt uitgebreid.
- Er wordt/worden (een) systematische literatuuranalyse(s) uitgevoerd afhankelijk van de te beantwoorden uitgangsvragen.
- Onderbouwing, overwegingen en aanbevelingen worden opgesteld.
- Commentaarfase en autorisatie zoals gebruikelijk (met eventueel aangepaste termijn).
Ad 5. Nieuwe (binnen- of buitenlandse) richtlijnen
- De werkgroep bepaalt of de nieuwe richtlijn afwijkt van de richtlijn Neuraxisblokkade en antistolling
- Zo nee: geen actie nodig (eventueel verwijzing opnemen?)
- Zo ja: is er reden de huidige richtlijn aan te passen?
- Richtlijn van goede methodologische kwaliteit?
- Belangen opstellers openbaar?
- Geen andere bezwaren?
Dan eventueel informatie met bronvermelding overnemen
Als nieuwe richtlijn niet aan eisen voldoet maar wel aanleiding is tot aanpassen richtlijn Neuraxisblokkade: zie bovenstaande situaties
- De werkgroep adviseert de NVA of er sprake is van een inhoudelijke aanpassing die voor commentaar en autorisatie moet worden voorgelegd.
- Zo ja, commentaarfase en autorisatie zoals gebruikelijk (met eventueel aangepaste termijn).
- Zo nee, wijzigingen worden ter kennisgeving gecommuniceerd naar de betrokken wv-en.
Ad 6. Andere ontwikkelingen (overige modules, waaronder implementatieproblemen, organisatieaspecten, financiering, patiëntenvoorkeuren)
- De werkgroep bepaalt of deze nieuwe ontwikkeling aanleiding is om de richtlijn aan te passen.
- De werkgroep bepaalt of een nieuwe systematische literatuuranalyse gedaan wordt.
- Onderbouwing, overwegingen en aanbeveling worden (indien nodig) aangepast.
- De werkgroep adviseert de NVA of er sprake is van een inhoudelijke aanpassing die voor commentaar en autorisatie moet worden voorgelegd.
- Zo ja, commentaarfase en autorisatie zoals gebruikelijk (met eventueel aangepaste termijn).
- Zo nee, wijzigingen worden ter kennisgeving gecommuniceerd naar de betrokken wv-en.
Zoekverantwoording
Zoekacties zijn opvraagbaar. Neem hiervoor contact op met de Richtlijnendatabase.
