Hyperbare zuurstoftherapie
Uitgangsvraag
C4.2 Wat is de plaats van systemische hyperbare zuurstoftherapie (HBOT) bij patiënten met diabetes mellitus en een voetulcus?
Aanbeveling
Overweeg systemische hyperbare zuurstof therapie (HBOT) bij een diabetisch voetulcus, ter verbetering van wondgenezing, uitsluitend indien het ulcus niet geneest binnen 12 weken ondanks optimale behandeling in een multidisciplinair voetenteam.
Indien voor hyperbare zuurstoftherapie wordt gekozen:
- dient dit uitsluitend plaats te vinden na verwijzing door en in nauwe samenwerking met een multidisciplinair voetenteam;
- dienen de behandeling en resultaten hiervan op systematische wijze geregistreerd te worden, zodat landelijke evaluatie mogelijk wordt.
In een register voor systemische hyperbare zuurstoftherapie (HBOT) dienen tenminste de volgende patiënt- en behandelkarakteristieken, en resultaten te worden geregistreerd:
- Classificatie van het voetulcus volgens de Nederlandse richtlijn Diabetische Voet.
- Vaatlaboratorium: EAI, teendruk, tcpO2.
- Wel/geen revascularisatie voorafgaand aan HBOT. Indien ischemie en geen revascularisatie, waarom niet?
- Wondgenezing als uitkomstmaat: weer te geven als wondoppervlakte per cm2, twee weken en een week voorafgaand aan start HBOT, bij stop HBOT en 1 maand nadien.
- Amputatie als uitkomstmaat: onderscheid hierbij grote en kleine amputatie, en vermeld de tijdsduur tot amputatie gerekend vanaf start HBOT.
- Duur en intensiteit behandeling, totaal aantal behandelsessies.
- Overige behandelingen naast HBOT
- Complicaties.
Overwegingen
Op basis van de huidige literatuur (zie samenvatting literatuur) is het onmogelijk sterke aanbevelingen te formuleren. De effectiviteit van systemische hyperbare zuurstoftherapie (HBOT) is volgens de werkgroep alleen enigszins onderbouwd betreffende wondgenezing. Twee RCT’s van hoge methodologische kwaliteit (Abidia, 2003; Löndahl, 2010) laten een statistisch significante en klinisch relevante verbetering (NNT respectievelijk 1,8 en 4,1) van de wondgenezing zien. Wel moet hierbij worden opgemerkt dat de RCT’s slechts een gering aantal patiënten en events betreffen, wat de bewijskracht verlaagt.
Er zijn aanwijzingen dat hyperbare zuurstoftherapie het risico op grote amputaties bij patiënten met een diabetisch ulcus verlaagt, deze conclusie is echter gebaseerd op studies van matige of lage methodologische kwaliteit (Faglia, 1996; Doctor, 1992; Duzgun, 2008). Twee RCT’s van hoge methodologische kwaliteit hadden een te gering aantal grote amputaties om hierover conclusies te trekken(Abidia, 2003; Löndahl, 2010). De werkgroep is daarom van mening dat de bewijsvoering betreffende afname van grote amputaties onvoldoende is.
De huidige literatuur laat geen uitspraak toe of HBOT effect heeft op ischemische of niet-ischemische ulcera. Op basis van het hypothetische werkingsmechanisme van HBOT (Stoekenbroek, 2014) zou een eventueel effect van hyperbare zuurstoftherapie met name bij ischemische voetulcera te verwachten zijn en de studie van Abidia (2003) toont inderdaad een significant effect bij ischemische ulcera. In tegenstelling tot bovenstaande veronderstelling werd bij een aanvullende (post hoc) analyse in de RCT van Löndahl (2010) gevonden dat een hogere transcutane zuurstofspanning (TcPO2) in de voet – passend bij betere doorbloeding – correleerde met een groter effect van HBOT op de wondgenezing (Löndahl, 2011).
Tenslotte kan de werkgroep geen uitspraken doen over de invloed van de aanwezigheidsduur van het ulcus, intensiteit hyperbare zuurstof therapie en kosteneffectiviteit van hyperbare zuurstof therapie door de grote klinische heterogeniteit tussen de studies.
De werkgroep is van mening dat de bewijsvoering voldoende is om bij patiënten met diabetes mellitus en een ulcus, dat met reguliere behandeling niet geneest, hyperbare zuurstoftherapie onder strikte voorwaarden te overwegen. Onze aanbeveling is strijdig met een recent retrospectief, observationeel onderzoek (Margolis, 2013). Echter deze studie gaat gepaard met bekende beperkingen behorend bij dit soort onderzoek, zoals selectiebias.
Bij de keuze voor hyperbare zuurstoftherapie moet onder andere rekening worden gehouden met de belasting van de patiënt (vijf dagen per week, gemiddeld totaal 52 uur HBOT behandeling, en reistijd) en kosten (behandelkosten en reiskosten). De werkgroep beoordeelt de behandeling als veilig. De meest voorkomende complicatie is een barotrauma van het middenoor (gemiddeld 4% in drie studies), wat meestal binnen enkele dagen spontaan herstelt. Het centrum dat de hyperbare zuurstof therapie uitvoert moet in staat zijn om bij deze complexe patiënten de zorg volgens vigerende richtlijnen te geven. Deze behandeling dient plaats te vinden in nauwe samenwerking met het verwijzend multidisciplinair behandelteam.
Vanwege de eerder genoemde beperkingen van de huidige literatuur vindt de werkgroep het van belang dat behandeling en resultaten hiervan op systematische wijze geregistreerd wordt zodat (landelijke) evaluatie mogelijk wordt.
Onderbouwing
Achtergrond
Ondanks de huidige geaccepteerde behandeling van diabetische voetulcera geneest een deel (19 tot 35%) van de ulcera niet. Er is een dringende wens voor aanvullende therapeutische mogelijkheden. Hyperbare zuurstoftherapie (HBOT, hyperbaric oxygen therapy) wordt gesuggereerd als mogelijke aanvullende therapie. De uitgangsvraag beperkt zich tot de systemische toepassing van hyperbare zuurstof (HBOT), de lokale toepassing van hyperbare zuurstof (TOT, topical oxygen therapy) vormt geen onderdeel van de uitgangsvraag.
Conclusies
|
MATIG GRADE |
Hyperbare zuurstoftherapie (systemisch) lijkt de wondgenezing bij patiënten met diabetes en een voetulcus te doen toenemen.
Bronnen (Abidia, 2003; Kessler, 2003; Ma, 2013; Löndahl, 2010; Doctor, 1992; Duzgun, 2008) |
|
Geen gradering |
In hoeverre de effecten van hyperbare zuurstoftherapie (systemisch) op de wondgenezing verschillen tussen ischemisch dan wel niet-ischemische ulcera, is onbekend.
Bronnen (Abidia, 2003; Kessler, 2003; Ma, 2013) |
|
LAAG GRADE |
Er zijn aanwijzingen dat hyperbare zuurstoftherapie (systemisch) het risico op grote amputaties bij patiënten met diabetes en een voetulcus verlaagt.
Bronnen (Faglia, 1996; Abidia, 2003; Kessler, 2003; Ma, 2013; Löndahl, 2010; Doctor, 1992; Duzgun, 2008) |
|
ZEER LAAG GRADE |
Er zijn aanwijzingen dat hyperbare zuurstoftherapie (systemisch) het risico op kleine amputaties bij patiënten met diabetes en een voetulcus niet verlaagt.
Bronnen (Faglia, 1996; Abidia, 2003; Kessler, 2003; Ma, 2013; Löndahl, 2010; Doctor, 1992; Duzgun, 2008) |
|
Geen gradering |
In hoeverre de effecten van hyperbare zuurstoftherapie (systemisch) op het amputatierisico afhangen van de status van de ulcus, ischemisch of niet-ischemisch, is onbekend.
Dit geldt voor zowel het risico op grote als kleine amputaties.
Bronnen (Faglia, 1996; Abidia, 2003; Kessler, 2003; Ma, 2013) |
|
LAAG GRADE |
Er zijn geen aanwijzingen dat hyperbare zuurstoftherapie (systemisch) leidt tot ernstige bijwerkingen of complicaties bij patiënten met diabetes en een voetulcus.
Gebaseerd op gerandomiseerd onderzoek van beperkte omvang.
Bronnen (Faglia, 1996; Abidia, 2003; Kessler, 2003; Ma, 2013; Löndahl, 2010; Doctor, 1992; Duzgun, 2008) |
Samenvatting literatuur
De systematische review van Stoekenbroek (2014) is een recente systematische review van goede kwaliteit (zie evidencetabellen). Een eerdere Cochrane review (Kranke 2012) dekt de literatuur tot jan 2012. Stoekenbroek (2014) dekt de literatuur tot augustus 2013 en includeert zeven RCT’s gepubliceerd tussen 1992 en 2013 (376 patiënten) met een studiegrootte tussen 18 en 100 patiënten en een follow-up van twee weken tot 2 jaar. Indien gespecificeerd, betrof het met name patiënten met type 2 diabetes (67% tot 86%; Kessler, 2003; Löndahl, 2010; Ma, 2013). In alle gevallen werd HBOT gecombineerd met standaardtherapie (multidisciplinaire wondzorg).
Onder de geïncludeerde RCT’s is sprake van grote klinische en methodologische heterogeniteit. De klinische heterogeniteit heeft met name betrekking op de wondkarakteristieken, aanwezigheid van ischemie, HBOT regime, definitie van uitkomstmaten en lengte van follow-up.
De drie grootste RCT’s includeren alleen patiënten met diabetische ulcera Wagner gradering 2 tot 4 (Faglia, 1996; Duzgun, 2008; Löndahl, 2010), twee RCT’s includeren ook Wagner grade 1, bij de overige twee RCT’s wordt de ernst van de voetulcera niet gespecificeerd. De RCT’s hanteren verschillende definities voor ischemie (zie evidencetabel). In Löndahl (2010) werden patiënten die op baseline in aanmerking kwamen voor revascularisatie geëxcludeerd. De HBOT regimes verschillen tussen de RCT’s, met name in intensiteit (eenmaal of tweemaal daags) en totaal aantal behandelsessies (20 tot 45 sessies; slechts vier sessies in Doctor, 1992). In twee RCT’s wordt HBOT vergeleken met hyperbare lucht (Abidia, 2003; Löndahl, 2010) waardoor blindering van patiënt en behandelaar mogelijk wordt maar de effecten van HBOT (100% zuurstof onder hoge druk) wellicht worden onderschat door een therapeutisch effect van lucht (20% zuurstof onder hoge druk) in de controlegroep. In de overige vijf RCT’s werd geen hogedrukbehandeling toegepast in de controlegroep. Duzgun (2008) hanteert een afwijkende definitie voor wondgenezing door genezing na behandeling in de operatiekamer uit te sluiten. Daarnaast worden door Duzgun (2008) kleine en grote amputaties gedefinieerd ten opzichte van het metatarsophalangeale gewricht waardoor een transmetatarsale amputatie wordt geclassificeerd als een grote amputatie. In de overige RCT’s wordt een definitie gebruikt ten opzichte van het enkelgewricht, en worden transmetatarsale amputaties als mineur geclassificeerd. Een meerderheid van de RCT’s kent een zeer korte duur van follow-up van enkele weken of maanden, drie RCT’s hebben een langetermijn follow-up van een jaar of meer (Abidia, 2003; Duzgun, 2008; Löndahl, 2010).
Stoekenbroek (2014) beoordeelt de studiekwaliteit van de RCT’s met een gemodificeerde versie van de Cochrane checklist (Verhagen, 1998) op onder andere randomisatie, blindering van toewijzing van de behandeling, en blindering van behandelaar, patiënt en effectbeoordelaar (zie evidencetabel). De methodologische kwaliteit van de RCT’s is overwegend matig. Bij een meerderheid van de RCT’s zijn blindering van de randomisatie, en blindering van patiënt en behandelaar onvoldoende beschreven. slecht twee RCT’s zijn van hoge methodologische kwaliteit (Abidia, 2003; Löndahl, 2010).
Op basis van het hypothetische werkingsmechanisme van HBOT maakt Stoekenbroek (2014) onderscheid tussen ischemische en niet-ischemische voetulcera. Een drietal RCT’s hebben volgens Stoekenbroek betrekking op patiënten met ischemische ulcera (N=182 patiënten; Faglia, 1996; Abidia, 2003; Löndahl, 2010), twee RCT’s betreffen niet-ischemische ulcera (N=64; Kessler, 2003; Ma, 2013) en bij de overige twee RCT’s wordt dit niet gespecificeerd (N=130; Doctor, 1992; Duzgun, 2008). In onderstaande analyse wordt op een punt afgeweken van de indeling van Stoekenbroek (2014). Een aanzienlijk deel (43%) van de studiepopulatie in Löndahl (2010) bestaat namelijk uit patiënten met niet-ischemische ulcera. In onderstaande analyses wordt Löndahl (2010) niet ingedeeld onder ‘ischemische ulcera’, maar onder ‘combinatie van ulcera met en zonder ischemie Door de grote klinische heterogeniteit met betrekking tot studiepopulaties, interventies en uitkomstmaten, is een meta-analyse niet te rechtvaardigen.
Wondgenezing (intacte huid) – kritieke uitkomstmaat
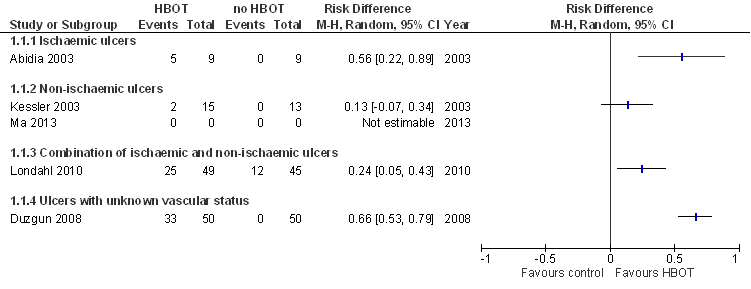
Zie figuur 1 voor een overzicht van de resultaten met betrekking tot de effecten van hyperbaar zuurstof (HBOT) op de wondgenezing bij einde follow-up.
Ischemische ulcera. Wondgenezing wordt gerapporteerd in één RCT (Abidia, 2003), die 18 patiënten met ischemische ulcera includeert. De studie is van hoge methodologische kwaliteit, en vindt een statistisch significante en klinisch relevante verbetering van de wondgenezing in de interventiegroep (HBOT) ten opzichte van de controlegroep (hyperbare lucht) na een jaar follow-up: NNT=1,8 (95% betrouwbaarheidsinterval, 95%BI=[1,1; 4,6]).
Niet-ischemische ulcera. Wondgenezing wordt gerapporteerd in twee RCT’s (Kessler, 2003; Ma, 2013), die respectievelijk 28 en 36 patiënten includeren met adequate perifere bloedcirculatie. De studies zijn van matige methodologische kwaliteit en vinden geen statistische significante verbetering van de wondgenezing in de interventiegroep (HBOT) ten opzichte van de controlegroep (geen HBOT) na twee tot vier weken follow-up. Door de geringe studieomvang en de korte follow-up is er echter niet of nauwelijks sprake van events (: volledige wondgenezing) in zowel controle- als interventiegroep.
Combinatie van ulcera met en zonder ischemie
Löndahl (2010) rapporteert wondgenezing bij 94 patiënten met adequate distale perfusie of niet-reconstrueerbare perifeer vaatlijden. De studie is van hoge methodologische kwaliteit, en vindt een statistisch significante en klinisch relevante verbetering van de wondgenezing in de interventiegroep (HBOT) ten opzichte van de controlegroep (hyperbare lucht), na een jaar follow-up: NNT=4,1 (95%BI=[2,3;19]; Löndahl, 2010).
Ulcera met onbekende status (ischemisch of niet-ischemisch). Wondgenezing wordt gerapporteerd in één RCT (Duzgun, 2008;). De RCT van Duzgun (2008) includeert 100 patiënten met ulcera waarvan de status onbekend is, de studie is van lage methodologische kwaliteit en vindt een statistisch significante en klinisch relevante verbetering van de wondgenezing in de interventiegroep (HBOT) ten opzichte van de controlegroep (geen HBOT) na twee jaar follow-up: NNT=1,5 (95%BI=[1,3; 1,9]). Duzgun (2008) hanteert echter een afwijkende definitie voor wondgenezing, door genezing na behandeling in de operatiekamer van de definitie uit te sluiten. Als hiervoor wordt gecorrigeerd (zie Löndahl, 2013) bedraagt het risicoverschil, RD=0,16 (95%BI=[-0,01; 0,33]) in het voordeel van HBOT maar statistisch niet significant.
Figuur 1 Forest plot van de effecten van hyperbaar zuurstof (HBOT) op de wondgenezing bij einde follow-up. Verschil in absoluut risico (RD, risk difference) ten opzichte van controle. Gebaseerd op Stoekenbroek (2014). Een meta-analyse ontbreekt vanwege onacceptabele klinische en statistische heterogeniteit (meta-analyse van relatieve risico’s, overall heterogeniteit, random effects model: I2 = 78%).
Amputatierisico – kritieke uitkomstmaat
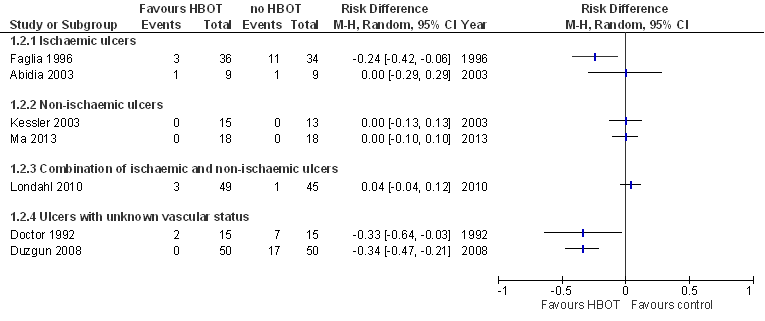
Zie figuur 2 en 3 voor een overzicht van de resultaten met betrekking tot de effecten van hyperbaar zuurstof (HBOT) op het risico van een grote amputatie (figuur 2) en kleine amputatie (figuur 3).
Grote amputaties (amputaties boven de enkel)
Ischemische ulcera. Grote amputaties worden gerapporteerd in twee RCT’s (Faglia, 1996; Abidia, 2003;) die respectievelijk 70, en 18 patiënten includeren. Faglia (1996) is van matige methodologische kwaliteit, en vindt een statisch significante en klinisch relevante afname in het aantal grote amputaties in de interventiegroep (HBOT) ten opzichte van de controlegroep (geen HBOT) gedurende ongeveer twee maanden follow-up (precieze lengte van follow-up wordt niet gerapporteerd): NNT=4,2 (95%BI=[2,4; 17]). Faglia (1996) vindt echter tegelijkertijd een toename in het aantal kleine amputaties (onder de enkel) in de interventiegroep (zie de paragraaf met betrekking tot kleine amputaties). Abidia (2003) is van hoge methodologische kwaliteit maar kent een gering aantal events en vindt geen afname in het aantal grote amputaties in de interventiegroep (HBOT) na een jaar follow-up.
Niet-ischemische ulcera. Grote amputaties worden gerapporteerd in twee RCT’s (Kessler, 2003; Ma, 2013) van matige methodologische kwaliteit, die respectievelijk 28 en 36 patiënten includeren. Door de geringe studieomvang en korte follow-up (twee tot vier weken) ontbreken events, er zijn geen amputaties in controle- en interventiegroep.
Combinatie van ulcera met en zonder ischemie
De RCT van Löndahl (2010; 94 patiënten) is van hoge methodologische kwaliteit maar kent een gering aantal events en vindt na een jaar follow-up geen statistisch significant verschil in het aantal grote amputaties tussen de interventiegroep (HBOT) en de controlegroep (hyperbare lucht), 6% vs. 2%.
Ulcera met onbekende status (ischemisch of niet-ischemisch). Grote amputaties worden gerapporteerd in twee RCT’s (Doctor, 1992; Duzgun, 2008) die respectievelijk 30 en 100 patiënten includeren. Doctor (1992) is van matige methodologische kwaliteit en specificeert het aantal grote amputaties in interventie- en controlegroep (2 versus 7; p<0,05) bij een follow-up van ongeveer twee maanden (precieze lengte van follow-up wordt niet gerapporteerd), maar niet de groepsgroottes. Uitgaande van een gelijk aantal patiënten in interventie- en controlegroep (n=15) bedraagt het risicoverschil, RD=0,33 (95%BI=[0,64; 0,03]) in het voordeel van HBOT. Tegelijkertijd wordt echter geen afname gevonden in het aantal kleine amputaties in de interventiegroep (zie de paragraaf met betrekking tot kleine amputaties). Duzgun (2008) is van lage methodologische kwaliteit en vindt een statistisch significante en klinisch relevante afname in het aantal grote amputaties in de interventiegroep (HBOT) ten opzichte van de controlegroep (geen HBOT) tijdens twee jaar follow-up: NNT=2,9 (95% BI=[2,1; 4,8]). Duzgun (2008) hanteert echter een afwijkende definitie voor grote amputaties waarbij ook transmetatarsale amputaties worden meegerekend, waardoor het aantal grote amputaties mogelijk wordt overschat. In tegenstelling tot Doctor (1992) vindt Duzgun (2008) ook een afname in het aantal kleine amputaties na HBOT (zie de paragraaf met betrekking tot kleine amputaties).
Figuur 2 Forest plot van de effecten van hyperbaar zuurstof (HBOT) op het amputatierisico (grote amputaties) bij einde follow-up. Verschil in absoluut risico (RD, risk difference) ten opzichte van controle. Gebaseerd op Stoekenbroek (2014). Een meta-analyse ontbreekt vanwege onacceptabele klinische en statistische heterogeniteit (meta-analyse van relatieve risico’s, overall heterogeniteit, random effects model: I2 = 50%). Doctor (1992) vermeldt alleen de totale studiegrootte, in de tabel wordt verondersteld dat de patiënten gelijkelijk zijn verdeeld over interventie- en controlegroep.
Kleine amputaties (amputaties onder de enkel):
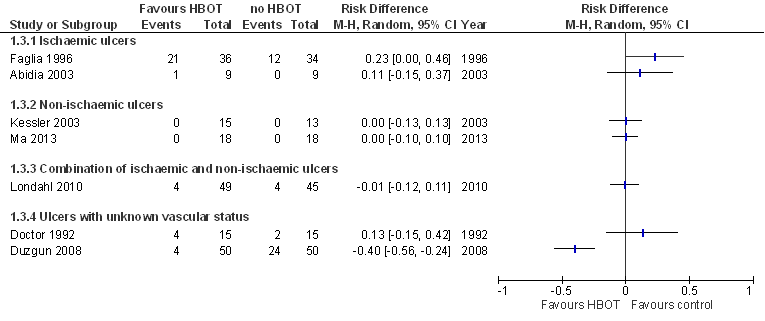
Ischemische ulcera. Kleine amputaties worden gerapporteerd in twee RCT’s (Faglia, 1996; Abidia, 2003; die respectievelijk 70 en 18, patiënten includeren. Faglia (1996) is van matige methodologische kwaliteit, en vindt geen afname maar een toename in het aantal kleine amputaties in de interventiegroep (HBOT) ten opzichte van de controlegroep (geen HBOT) gedurende twee maanden follow-up: het risicoverschil bedraagt, RD=0,23 (95%BI=[0,00; 0,46]; p<0,05) in het voordeel van de controlegroep. Tegelijkertijd is er wel sprake van een afname in het aantal grote amputaties in de interventiegroep (zie de paragraaf met betrekking tot grote amputaties). Deze resultaten zijn mogelijk vertekend door een gebrekkige blindering van de behandelaar. Eerder ingrijpen in de interventiegroep zou de relatieve toename van het aantal kleine amputaties kunnen verklaren, terwijl het uitvoeren van meer kleine amputaties het risico op een grote amputatie in de interventiegroep verkleint. Abidia (2003) is van hoge methodologische kwaliteit en vindt geen statistisch significant verschil in het aantal kleine amputaties tussen interventiegroep (HBOT) en controlegroep (hyperbare lucht) na een jaar follow-up.
Niet-ischemische ulcera. Kleine amputaties worden gerapporteerd in twee RCT’s (Kessler, 2003; Ma, 2013) van matige methodologische kwaliteit, die respectievelijk 28 en 36 patiënten includeren. Door de geringe studieomvang en korte follow-up (twee tot vier weken) ontbreken events, er zijn geen kleine (of grote) amputaties in controle- en interventiegroep.
Combinatie van ulcera met en zonder ischemie
De RCT van Londahl (2010; 94 patiënten) is van hoge methodologische kwaliteit en vindt geen statistisch significant verschil in het aantal kleine amputaties tussen interventiegroep (HBOT) en controlegroep (hyperbare lucht) na een jaar follow-up.
Ulcera met onbekende status (ischemisch of niet-ischemisch). Kleine amputaties worden gerapporteerd in twee RCT’s (Doctor, 1992; Duzgun, 2008;) die respectievelijk 30 en 100 patiënten includeren. Doctor (1992) is van matige methodologische kwaliteit en vindt geen statistisch significant verschil in het aantal kleine amputaties tussen interventiegroep en controlegroep bij een follow-up van twee maanden. Duzgun (2008) is van lage methodologische kwaliteit en vindt een statistisch significante en klinisch relevante afname in het aantal kleine amputaties in de interventiegroep (HBOT) ten opzichte van de controlegroep (geen HBOT) tijdens twee jaar follow-up: NNT=2,5 (95% BI=[1,8; 4,1]). Duzgun (2008) hanteert echter een afwijkende definitie voor kleine amputaties waarbij transmetatarsale amputaties niet worden meegerekend, en het aantal kleine amputaties mogelijk wordt onderschat.
Figuur 3 Forest plot van de effecten van hyperbaar zuurstof (HBOT) op het amputatierisico (kleine amputaties) bij einde follow-up. Verschil in absoluut risico (RD, risk difference) ten opzichte van controle. Gebaseerd op Stoekenbroek (2014). Een meta-analyse ontbreekt vanwege onacceptabele klinische en statistische heterogeniteit (: meta-analyse van relatieve risico’s, overall heterogeniteit, random effects model: I2 = 79%). Doctor (1992) vermeldt alleen de totale studiegrootte, in de tabel wordt verondersteld dat de patiënten gelijkelijk zijn verdeeld over interventie- en controlegroep.
Bijwerkingen en complicaties – belangrijke uitkomstmaat
Vijf RCT’s rapporteren bijwerkingen als uitkomstmaat (adverse events; Löndahl, 2010; Abidia, 2003; Faglia, 1996; Kessler, 2003; Ma, 2013). Abidia (2003) en Ma (2013) vonden geen bijwerkingen. In drie RCT’s werd barotraumatische otitis geconstateerd in de interventiegroep, met een gemiddelde incidentie van 4%: 1/49 patiënten (2%; Löndahl 2010), 1/36 (3%; Faglia, 1996), en 2/15 (13%; Kessler, 2003). Tenminste eenmaal leidde dit tot beëindiging van de behandeling met hyperbare zuurstof. In Löndahl (2010) werd bij 2/49 patiënten (4%) in de interventiegroep (HBOT) en bij 2/45 patiënten (4%) in de controlegroep (hyperbare lucht) een trommelvliesbuisje geplaatst vanwege pijn veroorzaakt door het niet kunnen klaren van de oren tijdens de hogedrukbehandeling. Löndahl (2010) rapporteert hypoglykemie bij 2/49 (4%) en 4/45 (9%) patiënten in respectievelijk de interventiegroep (HBOT) en controlegroep (hyperbare lucht). In de HBOT groep kwam bij 1/49 patiënten (2%) duizeligheid voor, en bij 1/49 (2%) patiënten was sprake van een verslechtering van cataract (Löndahl 2010).
Bewijskracht van de literatuur
In alle gevallen is de bewijskracht gebaseerd op gerandomiseerd onderzoek en is het startpunt bij het bepalen van de bewijskracht (GRADE) hoog. De bewijskracht voor de uitkomstmaat wondgenezing bij patiënten met een diabetische ulcus is matig, want de bewijskracht is verlaagd met één niveau vanwege imprecisie (gering aantal patiënten en events). Een conclusie of hyperbare zuurstoftherapie een gunstig effect heeft op de wondgenezing bij ischemische dan wel niet-ischemische ulcera is niet mogelijk vanwege een gebrek aan bewijs (vrijwel geen events in interventie- en controlegroep bij de studies met uitsluitend ischemische ulcera of uitsluitend niet-ischemische ulcera).
De bewijskracht voor de uitkomstmaat grote amputaties is laag, want de bewijskracht is verlaagd met twee niveaus vanwege beperkingen in de onderzoeksopzet (ontbreken van blindering) en imprecisie (gering aantal patiënten en events).
De bewijskracht voor de uitkomstmaat kleine amputaties is zeer laag, want de bewijskracht is verlaagd met drie niveaus vanwege beperkingen in de onderzoeksopzet (ontbreken van blindering), inconsistentie (tegenstrijdige resultaten) en imprecisie (gering aantal patiënten en events).
Net zoals bij de wondgenezing, is een conclusie of hyperbare zuurstoftherapie een gunstig effect heeft op het amputatierisico (grote of kleine amputaties) bij ischemische dan wel niet-ischemische ulcera is niet mogelijk vanwege een gebrek aan bewijs (vrijwel geen events in interventie- en controlegroep bij de studies met uitsluitend ischemische ulcera of uitsluitend niet-ischemische ulcera).
De bewijskracht voor de uitkomstmaat bijwerkingen en complicaties als gevolg van behandeling met hyperbare zuurstof (ongeacht de status van de ulcus, ischemisch of niet-ischemisch) is laag, want de bewijskracht is verlaagd met twee niveaus vanwege ernstige imprecisie (gering aantal patiënten en events).
Zoeken en selecteren
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende wetenschappelijke vraagstelling: wat zijn de gunstige en ongunstige effecten van een aanvullende behandeling van een diabetische voetulcus met hyperbaar zuurstof (systemisch) in vergelijking tot alleen reguliere behandeling, bij volwassen patiënten met diabetes type 1 of 2, en met wondgenezing, amputatierisico, bijwerkingen en complicaties, en kosten als relevante uitkomstmaten. De werkgroep benoemde wondgenezing (volledige wondgenezing) en amputatierisico (kleine en grote amputaties) als kritieke uitkomstmaten, en bijwerkingen en complicaties als belangrijke uitkomstmaten voor de besluitvorming. De werkgroep definieerde niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
De werkgroep achtte voor de kritieke uitkomstmaten (wondgenezing, amputatierisico) een verschil in absoluut risico van tenminste 5% (number needed to treat, NNT van maximaal 20), als klinisch (patiënt) relevant.
Zoeken en selecteren (Methode)
In de databases Medline (OVID), Embase and Cochrane is met relevante zoektermen gezocht vanaf 2012 naar vergelijkend onderzoek van behandeling van diabetische voetulcera met hyperbaar zuurstof. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 114 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria: systematische review of RCT naar de effecten van een aanvullende behandeling van diabetische voetulcera met hyperbaar zuurstof (systemisch) op wondgenezing en amputatierisico. Op basis van titel en abstract werden in eerste instantie 29 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 28 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording), en één systematische review definitief geselecteerd (Stoekenbroek 2014). Deze systematische review van RCT’s dekt de literatuur tot augustus 2013, er werden geen recentere RCT’s gevonden die aan de inclusiecriteria voldeden. De beoordeling van de kwaliteit van de systematische review, de in- en exclusiecriteria, de studiekarakteristieken en de resultaten van de geïncludeerde studies, zijn opgenomen in de evidencetabellen en waar nodig gecompleteerd door raadpleging van de originele publicaties.
Referenties
- Abidia A, Laden G, Kuhan G, et al. The role of hyperbaric oxygen therapy in ischaemic diabetic lower extremity ulcers: a double-blind randomised-controlled trial. Eur J Vasc Endovasc Surg. 2003;25(6):513-518. PubMed PMID: 12787692.
- Doctor N, Pandya S, Supe A. Hyperbaric oxygen therapy in diabetic foot. J Postgrad Med. 1992;38(3):112-114. PubMed PMID: 1303408.
- Duzgun AP, Satir HZ, Ozozan O, et al. Effect of hyperbaric oxygen therapy on healing of diabetic foot ulcers. J Foot Ankle Surg. 2008;47(6):515-9. doi: 10.1053/j.jfas.2008.08.002. Epub 2008 Sep 16. PubMed PMID: 19239860.
- Faglia E, Favales F, Aldeghi A, et al. Adjunctive systemic hyperbaric oxygen therapy in treatment of severe prevalently ischemic diabetic foot ulcer. A randomized study. Diabetes Care. 1996;19(12):1338-1343. PubMed PMID: 8941460.
- Kessler L, Bilbault P, Ortéga Fm, et al. Hyperbaric oxygenation accelerates the healing rate of nonischemic chronic diabetic foot ulcers: a prospective randomized study. Diabetes Care. 2003;26(8):2378-2382. PubMed PMID: 12882865.
- Kranke P, Bennett MH, Martyn-St James M, et al. Hyperbaric oxygen therapy for chronic wounds. Cochrane Database Syst Rev. 2012;4:CD004123. doi: 10.1002/14651858.CD004123.pub3. PubMed PMID: 22513920.
- Löndahl M, Katzman P, Hammarlund C, et al. Relationship between ulcer healing after hyperbaric oxygen therapy and transcutaneous oximetry, toe blood pressure and ankle-brachial index in patients with diabetes and chronic foot ulcers. Diabetologia. 2011;54(1):65-8. doi: 10.1007/s00125-010-1946-y. Epub 2010 Oct 19. PubMed PMID: 20957342.
- Löndahl M, Katzman P, Nilsson A, et al. Hyperbaric oxygen therapy facilitates healing of chronic foot ulcers in patients with diabetes. Diabetes Care. 2010;33(5):998-1003. doi: 10.2337/dc09-1754. PubMed PMID: 20427683.
- Löndahl M. Hyperbaric oxygen therapy as adjunctive treatment of diabetic foot ulcers. Med Clin North Am. 2013;97(5):957-980. doi: 10.1016/j.mcna.2013.04.004. Epub 2013 Jul 6. Review. PubMed PMID: 23992903.
- Ma L, Li P, Shi Z, et al. A prospective, randomized, controlled study of hyperbaric oxygen therapy: effects on healing and oxidative stress of ulcer tissue in patients with a diabetic foot ulcer. Ostomy Wound Manage. 2013;59(3):18-24. PubMed PMID: 23475448.
- Margolis DJ, Gupta J, Hoffstad O, et al. Lack of effectiveness of hyperbaric oxygen therapy for the treatment of diabetic foot ulcer and the prevention of amputation: a cohort study. Diabetes Care. 2013;36(7):1961-6. doi: 10.2337/dc12-2160. Epub 2013 Feb 19. PubMed PMID: 23423696; PubMed Central PMCID: PMC3687310.
- NDF (2015). Zorgstandaard Diabetes. Link: http://www.zorgstandaarddiabetes.nl/ [geraadpleegd op 20 januari 2017].
- Stoekenbroek RM, Santema TB, Koelemay MJ, et al. Is additional hyperbaric oxygen therapy cost-effective for treating ischemic diabetic ulcers? Study protocol for the Dutch DAMOCLES multicenter randomized clinical trial DAMOCLES. J Diabetes. 2015;7(1):125-32. doi: 10.1111/1753-0407.12155. Epub 2014 Apr 28. PubMed PMID:24674297.
- Stoekenbroek RM, Santema TB, Legemate DA, et al. Hyperbaric oxygen for the treatment of diabetic foot ulcers: a systematic review. Eur J Vasc Endovasc Surg. 2014;47(6):647-655. doi: 10.1016/j.ejvs.2014.03.005. Epub 2014 Apr 14. Review. PubMed PMID:24726143.
- Verhagen AP, de Vet HC, de Bie RA, et al. The Delphi list: a criteria list for quality assessment of randomized clinical trials for conducting systematic reviews developed by Delphi consensus. J Clin Epidemiol. 1998;51(12):1235-1241. PubMed PMID: 10086815.
Evidence tabellen
Exclusietabel
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Oliveira 2014 |
Retrospective case series; niet vergelijkend |
|
Brimson 2013 |
Narrative review |
|
Carter 2013 |
Geen origineel onderzoek |
|
Chantelau 2013 |
Geen origineel onderzoek |
|
Hawkins 2013 |
Geen origineel onderzoek |
|
Liu 2013 |
Geen origineel onderzoek |
|
Liu 2013 |
Minder recente SR; overlapt met Stoekenbroek 2014 |
|
Londahl 2013 |
Geen origineel onderzoek |
|
Londahl 2013 |
Narrative review |
|
Londahl 2013 |
Minder recente SR; overlapt met Stoekenbroek 2014 |
|
Ma 2013 |
RCT maakt deel uit van de SR van Stoekenbroek 2014 |
|
Margolis 2013 |
Geen RCT |
|
Margolis 2013 |
Geen origineel onderzoek |
|
Murad 2013 |
Geen origineel onderzoek |
|
O’Reilly 2013 |
Minder recente SR; overlapt met Stoekenbroek 2014 |
|
Santema 2013 |
Geen origineel onderzoek |
|
Sherlock 2013 |
Geen origineel onderzoek |
|
Strauss 2013 |
Geen origineel onderzoek |
|
Bishop 2012 |
Minder recente SR; overlapt met Stoekenbroek 2014 |
|
Aal 2012 |
Narrative review |
|
Bennett 2012 |
Geen origineel onderzoek |
|
Kranke 2012 |
Cochrane review; overlapt met Stoekenbroek 2014 |
|
Kranke 2012 |
Geen origineel onderzoek |
|
Londahl 2012 |
Minder recent dan Londahl 2013; voegt niets toe |
|
Londahl 2012 |
Geen origineel onderzoek |
|
Mills 2012 |
Narrative review |
|
O’Reilly 2012 |
Geen origineel onderzoek |
|
Tiaka 2012 |
Narrative review |
Overige evidencetabellen afhankelijk van type uitgangsvraag.
Tabel Quality assessment of systematic reviews
Table of quality assessment for systematic reviews of RCTs and observational studies
Based on AMSTAR checklist (Shea et al.; 2007, BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher et al 2009, PLoS Med 6: e1000097; doi:10.1371/journal.pmed1000097)
Research question: should hyperbaric oxygen therapy (HBOT) be used in the treatment of diabetic foot ulcers?
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Stoekenbroek 2014 |
Yes |
Yes |
Yes |
Yes |
Not applicable |
Yes |
No*1 |
Yes |
Unclear*3 |
*1 Meta-analysis was not performed because study populations, interventions and (definition of) outcome measures were widely heterogeneous; statistical heterogeneity was also high. Data are presented in 3 subgroups but this grouping of studies is questionnable
*2 Assessment of (potential) publication bias was planned (methods section), but results are not reported (pooling was deemed inappropriate, and number of studies is less than 10).
*3 Potential conflicts of interest reported for SR, but not for individual studies included in the SR.
- Research question (PICO) and inclusion criteria should be appropriate and predefined
- Search period and strategy should be described; at least Medline searched; for pharmacological questions at least Medline + EMBASE searched
- Potentially relevant studies that are excluded at final selection (after reading the full text) should be referenced with reasons
- Characteristics of individual studies relevant to research question (PICO), including potential confounders, should be reported
- Results should be adequately controlled for potential confounders by multivariate analysis (not applicable for RCTs)
- Quality of individual studies should be assessed using a quality scoring tool or checklist (Jadad score, Newcastle-Ottawa scale, risk of bias table etc.)
- Clinical and statistical heterogeneity should be assessed; clinical: enough similarities in patient characteristics, intervention and definition of outcome measure to allow pooling? For pooled data: assessment of statistical heterogeneity using appropriate statistical tests (e.g. Chi-square, I2)?
- An assessment of publication bias should include a combination of graphical aids (e.g., funnel plot, other available tests) and/or statistical tests (e.g., Egger regression test, Hedges-Olken). Note: If no test values or funnel plot included, score “no”. Score “yes” if mentions that publication bias could not be assessed because there were fewer than 10 included studies.
- Sources of support (including commercial co-authorship) should be reported in both the systematic review and the included studies. Note: To get a “yes,” source of funding or support must be indicated for the systematic review AND for each of the included studies.
Evidence table for systematic review of RCTs and observational studies (intervention studies)
Research question: should hyperbaric oxygen therapy (HBOT) be used in the treatment of diabetic foot ulcers?
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C) |
Follow-up |
Outcome measures and effect size |
Comments |
|
Stoekenbroek 2014
(individual study characteristics deduced from Stoekenbroek 2014, unless stated otherwise) |
SR of 7 RCTs
Literature search up to aug 2013
A: Doctor 1992 B: Faglia 1996 C: Abidia 2003 D: Kessler 2003 E: Duzgun 2008 F: Löndahl 2010 G: Ma 2013
Study design: RCT [parallel]
Setting and Country: A: Univ Hosp India B: Univ Hosp Italy C: Unvi Hosp UK D: UnivHospFrance E: Univ Hosp Turkey F: UnivHospSweden G: Univ Hosp China
Source of funding: [commercial / non-commercial / industrial co-authorship] A: not stated B: not stated C: not stated D: non-commerc E: stated ‘none’ F: non-commerc G: non-commerc
|
Inclusion criteria SR: diabetes; ulcer of lower extremity; RCT; standard care with or without HBOT ( irrespective use of sham treatment); report of amputation rates, wound healing, or additional interventions
7 studies included
Important patient characteristics at baseline: Ischaemic/non-ischaemic,Wagner grade, N, Diabetes type, insulin use
Status ulcer B and C primarily include ischaemic ulcers; D and G include only non-ischaemic ulcers; status of the ulcers is unknown in A and E, and F contains both ischaemic and non-ischaemic ulcers (foot ischaemia defined as toe blood pressure <60 mmHg was present in 57% of study population)
[Note: in Stoekenbroek study F is grouped with ischaemic ulcers, while in the current evidence table, study F is grouped with ‘mixed or unknown’]
Wagner I/II/III/IV A: ?/?/?/? B: -/13/25/62% C: -/6/94/- D: ?/?/?/- E: -/18/37/45 F: -/26/56/18 G: 25/28/47/-
Number patients A: 30 B: 70 C: 18 D: 28 E: 100 F: 94 G: 36
Diabetes type (%type-2); insulin therapy (%) A: ?; ? B: ?; 63% C: ?; 56% D: 86%; 93% E: ?; 86% F: 67%; 90% G: 86%; 92%
Groups comparable at baseline? Yes (except Duzgun 2008; see ROB assessment) |
HBOT + routine care
Meta-analysis inappropriate: analysis per clinically relevant subgroup
(1) Ischaemic ulcers
Number of patients B: 36 C: 9
No sessions; duration (min) B: 38; 90 C: 30; 90
(2) non-ischaemic ulcers
Number of patients D: 15 G: 18
No sessions; duration (min) D: 20; 90 G: 20; 90
(3) mixed or unknown
Number of patients A: ? (assumed 15) E: 50 F: 49
No sessions; duration (min) A: 4; 45 E: 30-45; 90 F: 40; 85 |
No HBOT: Sham + routine care (C,F) Routine care (A,B,D,E,G)
Sham = hyperbaric air (C,F) Routine care = multidiscipl wound care
B: 34 C: 9
B: - C: 30; 90 (sham)
D: 13 G: 18
D: - G: -
A: ? (assumed 15) E: 50 F: 45
A: - E: - F: 40; 85 (sham)
|
B: ~7 weeks (not stated) C: 1 year
D: 4 weeks G: 2 weeks
A: ~2 months (not stated) E: 92 weeks (~2 years) F: 1 year
For how many participants were no complete outcome data available? See ROB assessment
|
Wound healing; major amputations; minor amputations; adverse effects
RD and NNT [95% CI]
Wound healing = complete healing; Minor amputations = below ankle; Major amputations = above ankle
Wound healing HBOT / Control n (%); RD NNT Ischaemic B: not reported C: 5(56%)/0(0%) RD=56[22;89] NNT=1.8[1.1;4.6] Non-ischaemic D: 2(13%)/0(0%) RD=13[-6.9;34] G: 0(0%)/0(0%) RD=0[-10;10] Mixed or unknown A: not reported E: 33(66%)/0(0%) RD=66[53;79] NNT=1.5[1.3;1.9] F: 25(51%)/12(27%) RD=24[5.3;43] NNT=4.1[2.3;19]
Major amputations RD and NNT [95% CI] n (%); RD NNT Ischaemic B: 3(8%)/11(32%) RD=-24[-42;-5.9] NNT=4.2[2.4;17] C: 1(11%)/1(11%) RD=0[-29;29] Non-ischaemic D: 0(0%)/0(0%) RD=0[-13;13] G: 0(0%)/0(0%) RD=0[-10;10] Mixed or unknown A: 2(13%)/7(47%) RD=33[-64;-3] E: 0(0%)/17(34%) RD=-34[-47;-21] NNT=2.9[2.1;4.8] F: 3(6%)/1(2%) RD=3.9[-4.1;12]
Minor amputations RD and NNT [95% CI] n (%); RD [NNT] Ischaemic B: 21(58%)/12(35%) RD=23[0.3;46] NNH=4.3[2.2;345] (number needed to harm) C: 1(11%)/0(0%) RD=11[-15;37] Non-ischaemic D: 0(0%)/0(0%) RD=0[-13;13] G: 0(0%)/0(0%) RD=0[-10;10] Mixed or unknown A:4(27%)/2(13%) RD=13[-15;42] E: 4(8%)/24(48%) RD=-40[-56;-24] NNT=2.5[1.8;4.1] F: 4(8%)/4(9%) RD=-0.7[-12;11]
Adverse events AEs as outcome measure in B,C,D,F,G >> No AEs: C,G Barotraumatic otitis: 1/49 (2%) in F, 1/36 (3%) in B, and 2/15 (13%) in D Other AEs: in F, myringotomy with tube placement due to pain caused by the inability to equilibrate air pressure through the Eustachian tube was performed in 2/49 (4%) patients in HBOT group, and in 2/45 (4%) in hyperbaric air group; hypoglycaemia was reported in 2/49 (4%) and 4/45 (9%) patients in HBOT and hyperbaric air group, respectively; dizziness and worsening of cataract were each described in 1/49 (2%) patients. |
Author’s conclusion: ‘Current evidence shows some evidence of the effectiveness of HBOT in improving the healing of diabetic leg ulcers in patients with concomitant ischaemia. Larger trials of higher quality are needed before implementation of HBOT in routine clinical practice in patients with diabetic foot ulcers can be justified.’
Note: in Stoekenbroek study F is grouped with ischaemic ulcers, while in the current evidence table, study F is grouped with ‘Mixed or unknown’ (foot ischaemia defined as toe blood pressure <60 mmHg was present in 57% of study population)
[Note: in a post hoc analysis of study F (Löndahl 2011 Diabetologica 54, 65-68), a correlation is found between low TcPO2 and non-healing of ulcers by HBOT (at <25mmHg TcPO2 healing rate was 0%) which is not in support of the theory that HBOT is more effective for ischaemic ulcers]
Study quality (risk of bias) of included studies determined with modified version of the Cochrane checklist: Adequate randomization Allocation concealment Patient blinding Clinician blinding Assessor blinding Baseline similarity Complete follow-up available All patients accounted for Intention-to-treat analysis Similar co-interventions A: ??-??+???+ B: +?-?++++++ C: ++++++++++ D: +?-?++++?+ E: +?-??-?-?+ F: ++++++++++ G: +?-?++++?+ overall study quality mediocre; most studies lack proper reporting of treatment allocation; only two trials of high quality (C,F)
Heterogeneity: very large clinical heterogeneity (patient population; treatment; definition of outcome measures), methodological heterogeneity, and statistical heterogeneity; meta-analysis is inappropriate.
Note: definition of wound healing deviates in E (: excludes healing after a procedure in the operating room);definition of amputation also deviates in E (: transmetatarsal amputations were classified as major); in B, there is a reduction in major amputations but an increase in minor amputations (possibly due to improper blinding and earlier surgery in the intervention group; earlier minor amputations may result in fewer major amputatiions);
Note: low sample sizes, short followup (except A,C,F), and small number of events; most studies are underpowered.
Note: sham therapy allows blinding of patients and caretakers (C,F), but involves hyperbaric air. Hyperbaric air (20% oxygen) may have a therapeutic effect, possibly minimizing the difference between intervention (HBOT) and control. |
Verantwoording
Autorisatiedatum en geldigheid
Laatst beoordeeld : 13-04-2017
Laatst geautoriseerd : 01-07-2017
Geplande herbeoordeling : 01-01-2022
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep wel/niet [nog nader te bepalen door NIV] in stand gehouden. Uiterlijk in 2021 bepaalt het bestuur van de Nederlandse Internisten Vereniging (NIV) of deze richtlijn (module) nog actueel is. Op modulair niveau is een onderhoudsplan beschreven. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De NIV is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
Andere autoriserende partijen:
- Nederlands Huisartsen Genootschap
- WCS Kenniscentrum Wondzorg
- Eerste Associatie van Diabetes Verpleegkundigen
- Nederlandse Vereniging van Podotherapeuten
- ProVoet (Brancheorganisatie voor de Pedicure)
- Nederlandse Vereniging van Diabetes Podotherapeuten
- Wondplatform Nederland
- Diabetesvereniging Nederland
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van Medisch Specialisten (www.kennisinstituut.nl) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Patiëntenparticipatie bij deze richtlijn werd mede gefinancierd uit de Kwaliteitsgelden Patiënten Consumenten (SKPC) binnen het programma KIDZ.
Doel en doelgroep
Doel
De richtlijn heeft als doelstelling zorgprofessionals handvatten te bieden voor de diagnostiek, preventie en behandeling van deze aandoeningen om ulcera, amputaties en levenslang verlies van mobiliteit en kwaliteit van leven te voorkomen. Een tweede doel is dat zorgprofessionals beter inzicht krijgen in de mogelijkheden en beperkingen van de andere disciplines betrokken bij de zorg voor deze complexe groep patiënten. Tenslotte beschrijft de richtlijn hoe de zorg voor een patiënt met een voetulcus het beste georganiseerd kan worden in Nederland.
Doelgroep
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen die betrokken zijn bij de (preventieve) zorg voor patiënten met diabetes mellitus en voetulcera of ACN. Deze beroepsgroepen bestaan onder andere uit huisartsen, praktijkondersteuners, (vaat)chirurgen, orthopedisch chirurgen, internisten, revalidatieartsen, apothekers, podotherapeuten, diabetespodotherapeuten, medisch pedicures, orthopedisch schoentechnici, gipsverbandmeesters, wondverpleegkundigen, wondconsulenten, verpleegkundig specialisten, physician assistants, en diabetes verpleegkundigen.
Samenstelling werkgroep
De richtlijn Diabetische voet is onderdeel van de Netwerkrichtlijn diabetes mellitus ontwikkeld onder overkoepelend voorzitterschap van dr. P.H.L.M. (Nel) Geelhoed, internist-endocrinoloog, Haaglanden Medisch Centrum, Den Haag (Nederlandse Internisten Vereniging).
Voor het ontwikkelen van de richtlijn Diabetische voet is in 2014 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van relevante specialismen die betrokken zijn bij de zorg voor personen met diabetes mellitus en (een risico op) een diabetische voet (zie hieronder).
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep werkte gedurende twee jaar aan de totstandkoming van de richtlijn.
De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
- Prof. Dr. N.C. (Nicolaas) Schaper, internist-endocrinoloog, Maastricht UMC+ (voorzitter); Nederlandse Internisten Vereniging
- Dr E.J.G. (Edgar) Peters, Internist- Infectieziekten en Acute Geneeskunde, afd. Interne Geneeskunde, VU medisch centrum, Amsterdam; Nederlandse Internisten Vereniging
- M.C.J. (Marion) Knippels, Internist in opleiding (AIOS), Maastricht UMC+; Nederlandse Internisten Vereniging
- J. (Jaap) Kroon, huisarts en kaderarts diabetes, Huisartsenpraktijk Anderegglaan, Nuenen; Nederlands Huisartsen Genootschap
- B.A. (Bela) Pagrach, Diabetes/wondverpleegkundige, Ziekenhuis Amstelland, Amstelveen; WCS Kenniscentrum Wondzorg en Eerste Associatie Van Diabetesverpleegkundigen
- Drs M.A. (Margreet) van Putten, arts, Fontys Hoge Scholen, Eindhoven; Nederlandse Vereniging van Podotherapeuten
- Dr J.G. (Sjef) van Baal, vaatchirurg, ZGT, Almelo; Nederlandse Vereniging voor Heelkunde
- Dr S.A. (Sicco) Bus, bewegingswetenschapper, afd. Revalidatie, AMC, Universiteit van Amsterdam; studiegroep Neurovasculaire Complicaties van Diabetes
- Dr A.P. (Antal) Sanders, revalidatiearts, Leids Universitair Medisch Centrum, Leiden; Nederlandse Vereniging van Revalidatieartsen
- Drs A.E.B. (Arthur) Kleipool, orthopedisch chirurg, OLVG Amsterdam; Nederlandse Orthopaedische Vereniging
- Drs L.A. (Loes) Lemmens, senior beleidsmedewerker, ProVoet; ProVoet (Brancheorganisatie voor de Pedicure)
- P.W.C. (Paul) Buchrnhornen, schoentechnicus, Buchrnhornen Orthopedie BV; op persoonlijke titel
- I. (Ingrid) Ruys, diabetespodotherapeut, Maxima Medisch Centrum, Veldhoven; Nederlandse Vereniging van Diabetes Podotherapeuten en Wondplatform Nederland
- L. (Lian) Stoeldraaijers, diabetespodotherapeut, Podotherapie Valkenswaard, Valkenswaard; Nederlandse Vereniging van Podotherapeuten en Nederlandse Vereniging van Diabetes Podotherapeuten
- Drs D.S.V. (Dayline) Coffie, beleidsadviseur, Diabetesvereniging Nederland
Met ondersteuning van:
- Dr. K.N.J. (Koert) Burger, epidemioloog, senior adviseur Kennisinstituut van Medisch Specialisten
- J. (Joppe) Tra (MSc), adviseur Kennisinstituut van Medisch Specialisten
- C. (Carla) Sloof (MSc), medisch informatiespecialist, St. Antonius Ziekenhuis, Nieuwegein
- L. (Linda) Niesink (MSc), medisch informatiespecialist, Kennisinstituut van Medisch Specialisten
- S.K. (Sanne) Josso, secretaresse, Kennisinstituut van Medisch Specialisten
- N.F. (Natalia) Bullock, secretaresse, Kennisinstituut van Medisch Specialisten
Met dank aan:
- S.A.V. (Suzanne) van Asten, arts, afd. Interne Geneeskunde, VU medisch centrum, Amsterdam
Belangenverklaringen
De “KNMG-Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling” is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of ze in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Reputatie management |
Extern gefinancierd onderzoek |
Kennisvalorisatie |
Overige belangen |
Ondernomen actie |
|
Schaper |
hoofd onderafdeling Endocrinologie, interne geneeskunde, Maastricht UMC |
Voorzitter 7e int. Symp on the diabetic foot; Voorzitter international guidance on management of the diabetic foot (International Working Group on the Diabetic Foot) Lid Wetenschappelijke Advies Raad Diabetes Fonds |
geen |
geen |
geen |
geen |
Zie nevenfuncties |
geen |
Geen |
|
Kroon |
Huisarts, Kaderhuisarts Diabetes |
Stafarts Diabetes bij zorggroep PoZoB (betaald. |
geen |
geen |
Lid geweest van Commissie/ Werkgroep: Multidisciplinaire samenwerking rond preventie van Diabetische voetulcera |
geen |
Kaderhuisarts Diabetes, bijzondere belangstelling voor diabetische voet |
nee |
Geen |
|
Van Baal |
Vaatchirurg |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
Geen |
|
Van Putten |
docent opleiding Podotherapie, Fontys Paramedische Hogeschool Eindhoven |
bestuurslid ProVoet (onkostenvergoeding), bestuurslid NVvP (onkostenvergoeding); bestuursfuncties beëindigd in 2015 |
niet van toepassing |
niet van toepassing |
Zie bestuursfuncties. Het geven van lezingen/cursussen op het gebied van preventie van diabetische voetulcera. |
niet van toepassing |
niet van toepassing |
geen |
Geen |
|
Pagrach |
Diabetesverpleegkundige |
betaald als docent |
Aviescommissie: Lilly |
niet van toepassing |
EADV |
niet van toepassing |
geen |
geen |
Geen |
|
Bus |
Senior onderzoeker |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
Geen |
|
Lemmens |
senior beleidsmedewerker Provoet |
geen |
geen |
geen |
ruim acht jaar werkzaam in pedicurebranche en wordt duidelijk gezien als vertegenwoordiger van die branche |
geen |
geen |
geen |
Geen |
|
Peters |
internist, aandachtsgebieden infectieziekten en acute geneeskunde VUMC |
Werkgroep: -richtlijn infections desease Soc America: diabetische Voet |
geen |
geen |
geen |
Fond Nuts Ohra: subsidie onderzoek naar chirurgische behandeling neuropathie |
Expertise op gebied diabetische voet en diabetische voet infecties. Geen patent. |
geen |
Geen |
|
Sanders |
Revalidatiearts (65%) |
Lid van Raad van Advies ' Orthopedisch Instrument Makerijken /Orthopedische Schoentechnische Bedrijven van de Stichting Erkenningsregeling voor leveranciers voor Medische Hulpmiddelen (SEMH) (alleen een onkostenvergoeding wordt betaald) |
geen |
geen |
geen |
geen |
geen |
geen |
Geen |
|
Kleipool |
meelezer orthopedisch chirurg |
bestuurslid werkgroep Voet en Enkel NOV |
geen |
geen |
bestuurslid werkgroep voet en enkel NOV |
geen |
geen |
geen |
Geen |
|
Buchrnhornen |
orthopedisch schoenmaker |
lid raad van Advies Fontys Hogescholen opleiding podotherapie |
geen |
geen |
geen |
geen |
geen |
geen |
Geen |
|
Ruijs |
diabetespodotherapeut Maxima Medisch Centrum te Veldhoven |
vz NVvDP, penningmeester WPN, Bestuurslid ISPO, deelnemer Raad van Advies Fontys Hogescholen, Lid maatschappelijke advies Raad (MAR) Diabetesfonds. Alle genoemde functies zijn onbetaald. |
geen |
geen |
NVvDP en WPN |
geen |
geen |
geen |
Geen |
|
Knippels |
medeauteur als AIOS |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
Geen |
|
Coffie |
Beleidsadviseur DVN |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
Geen |
|
Stoeldraaijers |
diabetespodotherapeut, Podotherapie Valkenswaard |
bestuurslid Ned Ver Diabetes Podotherapeuten (onbetaald), lid werkgroep Kwaliteitsstandaard Complexe Wondzorg (onbetaald), lid commissie Wetenschap & Innovatie Ver Podotherapeuten (onkostenvergoeding) |
geen |
geen |
NVvP en NVvDP |
geen |
geen |
geen |
geen |
Inbreng patiëntenperspectief
Het patiëntenperspectief werd ingebracht door een afvaardiging van de patiëntenvereniging in de werkgroep en een in een eerder stadium door de patiëntenvereniging uitgevoerde enquête onder haar leden (zie richtlijn Diabetes Mellitus; NIV, 2014). De conceptrichtlijn is tevens voor commentaar voorgelegd aan de patiëntenvereniging (Diabetesvereniging Nederland).
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens zijn er knelpunten aangedragen via een invitational conference (gezamenlijk voor zeven richtlijnen die deel uitmaken van de netwerkrichtlijn diabetes, diabetische voet, diabetische retinopathie, diabetische neuropathie, kinderen, ouderen met comorbiditeit, diabetes en zwangerschap, diabetes en psychiatrie) door: de NIV, Diabetesvereniging Nederland (DVN), Eerste Associatie Van Diabetesverpleegkundigen (EADV), Inspectie voor de Gezondheidszorg, Koninklijke Nederlandse Organisatie van Verloskundigen (KNOV), Menzis, Nefarma, Nederlandse Federatie van Universitair Medische Centra (NFU), Nederlands Huisartsen Genootschap (NHG), Nederlands Oogheelkundig Gezelschap (NOG), Nederlandse Vereniging voor Anesthesiologie (NVA), Nederlandse Vereniging van Diëtisten (NVD), Nederlandse Vereniging voor Kindergeneeskunde (NVK), Nederlandse Vereniging voor Klinische Geriatrie (NVKG), Nederlandse Vereniging voor Neurologie (NVN), Nederlandse Vereniging voor Obstetrie & Gynaecologie (NVOG), Nederlandse Vereniging van Diabetes Podotherapeuten (NVvDP), Optometristen Vereniging Nederland (OVN), Provoet (Brancheorganisatie voor de Pedicure), Verpleegkundigen & Verzorgenden Nederland (V&VN), Verenso, WCS Kenniscentrum Wondzorg, Zorgverzekeraars Nederland (ZN), en Zorginstituut Nederland (ZIN). Een verslag van de invitational conference is opgenomen onder aanverwante producten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk (maar niet kritiek) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de kritieke uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Voor deze richtlijn is geen overkoepelende oriënterende zoekactie uitgevoerd. Voor de afzonderlijke uitgangsvragen is aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module van desbetreffende uitgangsvraag.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of bias (ROB) tabellen.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, matig, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Matig |
|
|
Laag |
|
|
Zeer laag |
|
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008), en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje Overwegingen.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Randvoorwaarden.
Indicatorontwikkeling
Bij de richtlijn zijn geen nieuwe kwaliteitsindicatoren ontwikkeld omdat er voor diabetes al voldoende indicatoren bestaan, onder andere behorend bij de NDF Zorgstandaard Diabetes.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk onderzoek van belang wordt geacht, is als aanbeveling in de bijlage Kennislacunes beschreven (onder aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisatie voorgelegd ter commentaar. Daarnaast werden de volgende verenigingen en organisaties benaderd voor commentaar: Nederlandse Vereniging voor Neurologie, Nefarma (Vereniging innovatieve geneesmiddelen Nederland), Nederlandse Federatie van Universitair Medische Centra, Nederlandse Vereniging voor Klinische Geriatrie, Nierpatiënten Vereniging Nederland, Verpleegkundigen & Verzorgenden Nederland, Verenso, Zorgverzekeraars Nederland, Zorginstituut Nederland, Inspectie voor de Gezondheidszorg, Nederlandse Diabetes Federatie, Stichting LOOP, Stichting Stipezo, Nederlandse Vereniging voor Radiologie, Nederlandse Vereniging voor Hyperbare Geneeskunde, Nefemed, NVOS-Orthobanda, Stichting Ineen. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
- Brouwers MC, Kho ME, Browman GP, et al. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010. Review. PubMed PMID: 20603348.
- Medisch Specialistische Richtlijnen 2.0. Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html. 2012.
- Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van Medisch Specialisten.
- Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group. 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
- Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008 May 24;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Zoekverantwoording
Zoekacties zijn opvraagbaar. Neem hiervoor contact op met de Richtlijnendatabase.

